Review of Food Surfactants on Improving Protein Powder Solubility
-
摘要: 蛋白质粉作为一种重要的食品营养与功能基料,在食品加工产业中应用场景广泛。然而在溶解过程中,由于界面效应所导致蛋白质粉结块、聚沉现象,使其溶解性降低,严重制约了食品蛋白质的应用及经济价值。食品表面活性剂可有效结合蛋白质粉,降低其溶解过程中发生的界面效应。因此,食品表面活性剂可更为广泛地应用于蛋白质粉溶解性能的提升。本文综述了食品表面活性剂的主要类型、与蛋白质结合的作用机制及对蛋白质粉溶解过程各阶段的影响,以期为食品表面活性剂在高溶解性蛋白质粉中的应用提供理论参考。Abstract: As an important nutritional and functional base for food, protein powders are widely used in the food processing industry. However, the solubility of protein powders is reduced during the dissolution process due to lumping and agglomeration caused by interfacial effects, which severely limits the application and economic value of food proteins. Food surfactants can effectively bind protein powders and reduce the interfacial effects that occur during the dissolution process. Therefore, food surfactants can be more widely used to improve the solubility of protein powders. This paper reviews the main types of food surfactants, their mechanism of action on protein binding, and their effects on the various stages of protein powder solubilization, intending to provide a theoretical reference for the application of food surfactants in highly soluble protein powders.
-
Keywords:
- protein powder /
- solubility /
- food surfactant /
- interface /
- food processing
-
蛋白质粉作为一种重要的食品基料,以其高加工适用性(如乳化性、凝胶性、起泡性),可有效改善食品的感官性状,在食品加工中应用场景广泛[1]。此外,蛋白质粉以其高营养价值常作为营养强化剂被加入到奶粉、饮料、面包中[2]。然而,蛋白质粉在溶解的过程中极易发生结块和聚沉现象,使溶解性降低,进而影响蛋白质粉的高加工适用性。因此,寻找一种提升蛋白质粉溶解性以及冲调性的有效策略是食源性蛋白质功能配料创制和开发中亟待研究和解决的问题之一。
蛋白质粉的溶解性可用润湿性、下沉性、分散性和溶解度四个指标进行评价[3]。溶解性受到多种因素影响:首先,蛋白质粉溶解性与其内部各成分相互作用有关,如蛋白质和糖类的非共价相互作用[4]、蛋白质间的疏水相互作用及蛋白质与其表面盐离子形成盐桥等都会影响蛋白质溶解性[1,5]。此外,蛋白质粉的粉体粒度和表面成分等也会影响蛋白质粉的溶解性[6],越小的粉体粒度其比表面积就越大,蛋白质粉越易结块[7],而表面成分的疏水性则会影响蛋白质的水化作用,故两者都不利于粉末的润湿。最后,蛋白质粉溶解性也与溶液的环境因素有关,例如溶液的pH、温度和离子强度等都会影响蛋白质的结构从而影响其溶解性[8-9]。目前研究者们已采用多种物理、化学方法提升蛋白质粉的溶解性,例如超声[10]、流化床造粒[11]、超声辅助pH调节法[12]、微波辅助磷酸化法[13]等来改善蛋白质粉的溶解性。然而,采用物理方法存在耗能大、机械设备昂贵等缺点,而化学方法所引入的有机物难以控制和被完全去除。因此,针对以上技术方法的局限性,寻求一种绿色环保、安全有效的方法更符合我国食品加工业中可持续发展的需求。
食品表面活性剂分子具有不对称的亲水和亲油结构,这使得它能够吸附在不同相的界面上(水/油或气/液或气/固)[14-15],食品表面活性剂的疏水端为疏水性烷基,对水不表现出亲和力[16]。在界面上,绝大多数表面活性剂即使在较低浓度下,也可以发生定向吸附,大幅度降低溶液的表面张力。而在溶液中,食品表面活性剂可以根据浓度差异,以单体或胶束的形式存在[17]。表面活性剂分子在界面上吸附以及在溶液中的自组装能力,使其在制药工业、农业和日化行业[18-20]等领域被广泛应用。尤其是在食品加工领域,表面活性剂已经作为分散剂和润湿剂被用于改善冲调饮料、可可粉等粉状食品的亲水性和分散性。因此,基于食品表面活性剂对粉体的润湿性、分散性、溶解度等显著的提升效果,食品表面活性剂或可成为一种改善食源性蛋白质粉溶解性的有效策略。因此,本文对食品表面活性剂的主要类型、性质及与蛋白质的作用机制、食品表面活性剂对蛋白质粉溶解过程各阶段的影响及作用条件等角度进行综述,以期为蛋白质粉溶解性的提升提供理论指导。
1. 食品表面活性剂分类、性质及作用机制
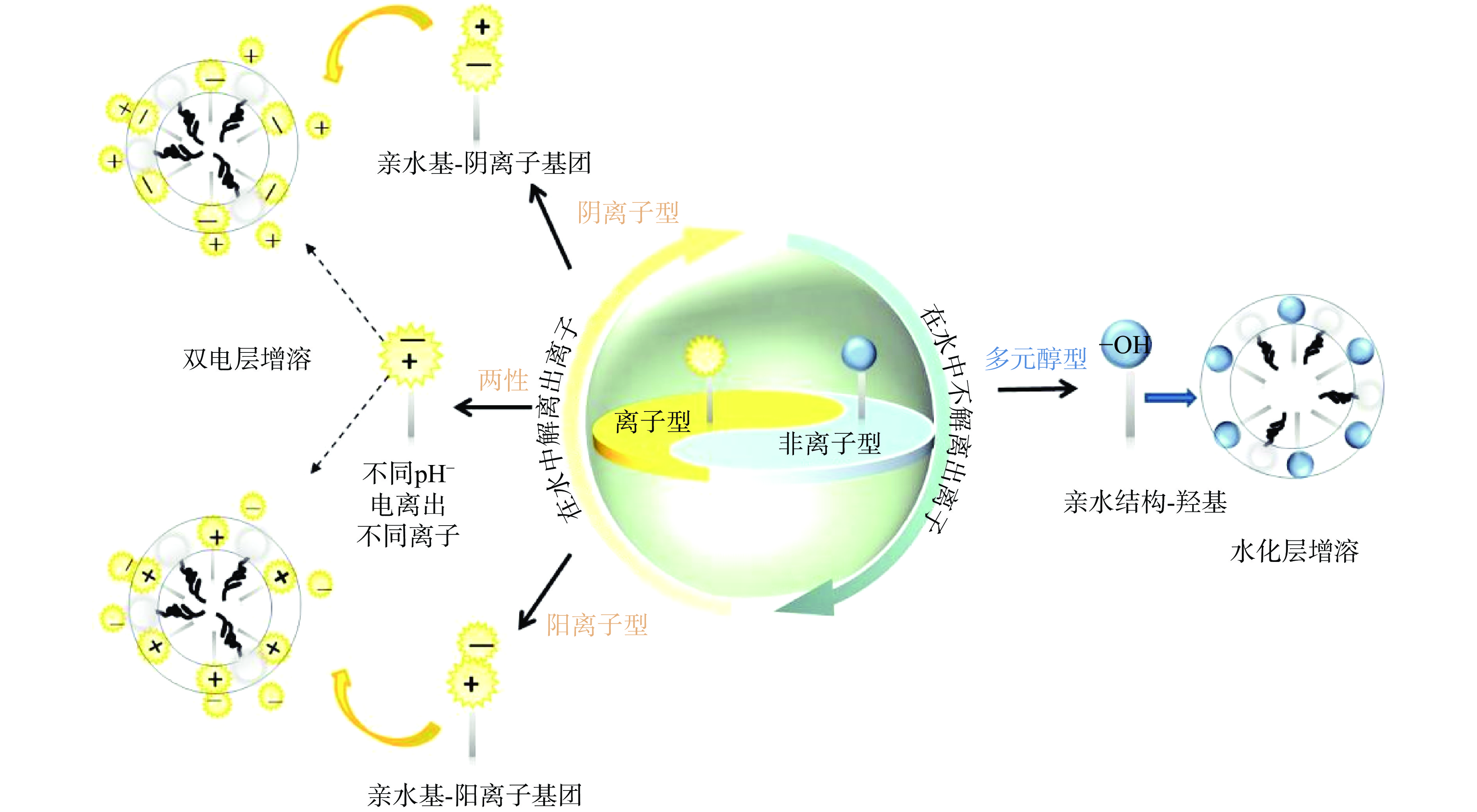
根据食品表面活性剂亲水端在水中的解离性质可以将其分为离子型和非离子型[16]。离子型食品表面活性剂根据解离电荷性质差异,又可分为阴离子型、阳离子型和两性离子型。非离子型食品表面活性剂以多元醇型食品表面活性剂为代表。蛋白质大分子与食品表面活性剂的相互作用方式与食品表面活性剂的类型有关。其中,离子型食品表面活性剂改善蛋白质粉溶解性的机理为双电层增溶,而非离子型食品表面活性剂是通过形成水化层来发挥作用。图1展示了不同类型食品表面活性剂增溶蛋白质粉可能的机理。本节将对食品表面活性剂类型、性质及与蛋白质的作用机制进行综述。
1.1 离子型食品表面活性剂
1.1.1 阴离子型食品表面活性剂
阴离子型食品表面活性剂是一种亲水端带有负电荷的表面活性剂,应用最广,可作为分散剂、润湿剂、发泡剂和乳化剂等[21]。当这种食品表面活性剂与水混合时,会产生带负电荷的阴离子,与蛋白质发生的静电作用较强,在溶液中电离出的阳离子通常为碱性金属离子(Na+,K+)[22]。根据亲水基团的不同,阴离子食品表面活性剂分为磷酸酯、脂肪酸盐型、硫酸盐型、磺酸盐、羧酸盐型[23]。经联合国粮农组织和世界卫生组织批准的阴离子食品表面活性剂包括硬脂酰乳酸钙(钠)、硬脂酰富马酸钠、十二烷基磺酸钠、海藻酸钠、果胶钠等。
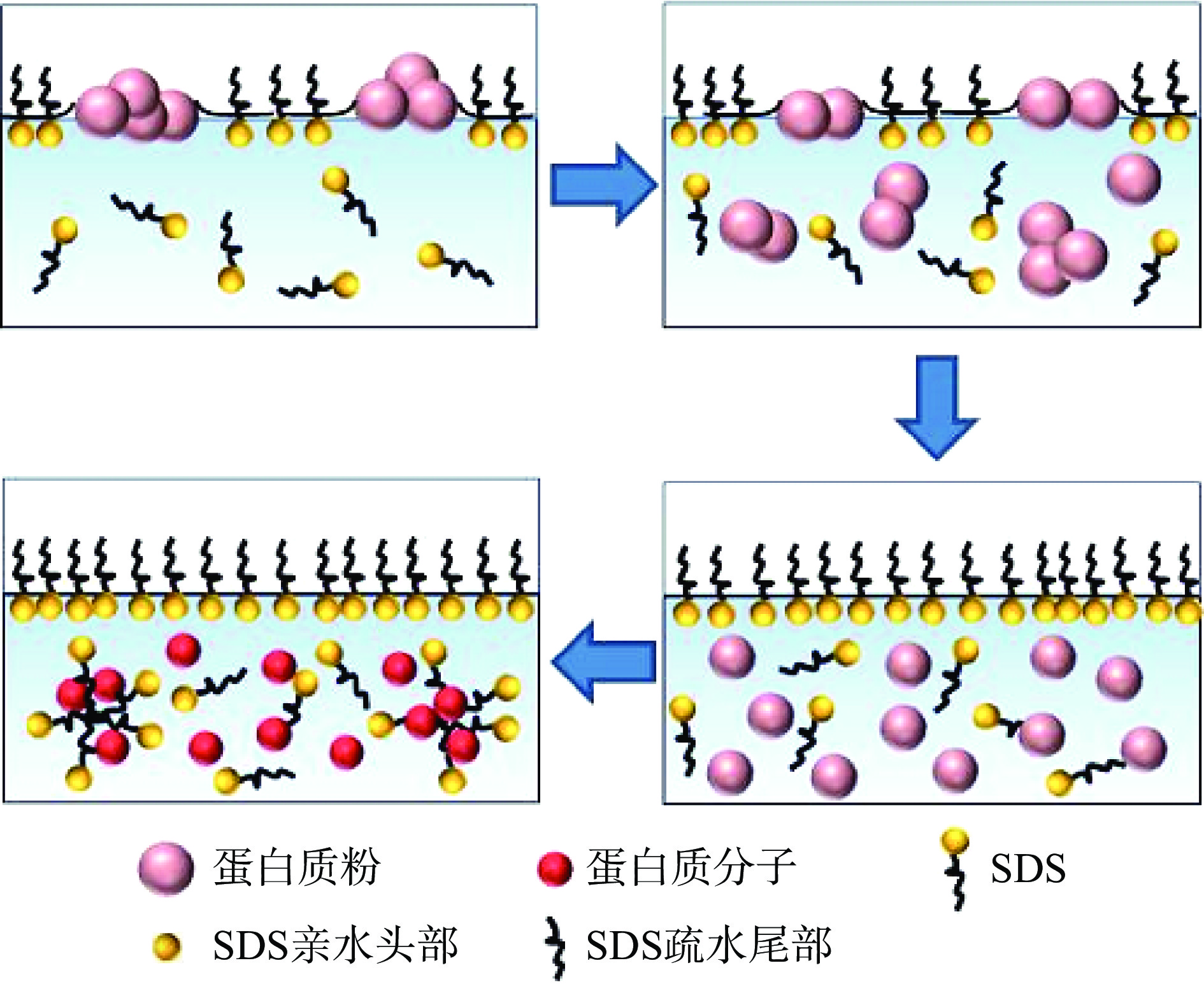
蛋白质较差的溶解性影响其在食品工业中的应用。阴离子型食品表面活性剂改善蛋白质溶解性的研究广泛,但其作用效果受到多种因素的影响。首先,阴离子型食品表面活性剂与蛋白质的相互作用或结合程度取决于溶液的pH,当pH<pI时,蛋白质带净正电荷,此时由于电荷的中和作用,会导致形成蛋白质-阴离子食品表面活性剂配合物沉淀;相反,当溶液pH>pI时,带净负电荷的蛋白质与阴离子型食品表面活性剂通过疏水相互作用形成可溶性复合物,蛋白质间的静电斥力增加了其分散性和溶解度[24]。其次,蛋白质和食品表面活性剂的比率会影响蛋白质-食品表面活性剂复合物的形成及蛋白质性质,正如S Nakai等[24]发现10% (w/w)的亚油酸钠使油菜籽蛋白几乎完全溶解,但是并未阐明蛋白质和表面活性剂的比率影响蛋白质溶解性的内在原因。Xia等[25]利用荧光光谱法探究了不同卵磷脂浓度与肌原纤维蛋白在高盐浓度下的相互作用,发现随着卵磷脂浓度的增加,蛋白质发生了进一步的荧光猝灭现象并且溶解度提高,作者认为两者之间存在氢键和疏水相互作用。与Xia的猜想相似,Giroux等[26]提出了离子型表面活性剂导致蛋白质变性理论,他认为离子型表面活性剂导致蛋白质变性与表面活性剂浓度有关。随着表面活性剂/蛋白质比例增加,附着在蛋白质表面的表面活性剂使其溶解度和热稳定性逐渐增加,然而比例进一步增加会使蛋白质三级结构展开并暴露出大量的疏水基团,使溶解度降低。因此,阴离子型食品表面活性剂增加蛋白质溶解度存在最适复配比。单媛媛[27]发现利用十二烷基硫酸钠(Sodium dodecyl sulfate,SDS)可破坏蛋白质之间的氢键、疏水键等次级键进而破坏蛋白质的天然构象,蛋白质暴露更多的疏水基团并与SDS发生静电相互作用形成双电层进而增加蛋白质的静电斥力,从而增加卵黏蛋白的溶解性(图2)。
1.1.2 阳离子型食品表面活性剂
食品的表面污染和腐败主要与真菌有关,为延长食品货架期和保证食品安全性,抗菌剂和防腐剂的使用受到食品从业者的关注。阳离子型表面活性剂主要是季铵盐(-R4N+)类化合物,由于其表面的阳离子基团能够很好地吸附细菌表面的负电荷所以多用作抗菌剂和消毒剂,它可以与非离子型表面活性剂共用,但它与阴离子型表面活性剂共用时会导致阴阳离子相互结合,使其降低或失去活性[28]。传统阳离子型表面活性剂通常具有皮肤刺激性或毒性,因此在食品工业中,设计和生产食品级阳离子表面活性剂具有挑战性和广泛应用前景。在最近的研究中,精氨酸型阳离子食品表面活性剂已被设计并应用于果蔬及肉制品的防腐[29-30],另外,月桂酸精氨酸酯增强食品级包装材料(结晶纳米纤维素)在非极性聚合物基质中的分散性已经得到证实[31]。阳离子型表面活性剂的两亲性赋予其助溶和助分散能力,其中研究最充分的一类分散剂是烷基链表面活性剂(ACSs),它已被证明可以促进纳米碳材料在水中的分散和溶解,但ACSs在高剂量下是有毒的,这对于食品分散具有局限性[32]。因此,食品级阳离子型表面活性剂多应用于防腐,作为分散剂或润湿剂的报道鲜少。
1.1.3 两性离子型食品表面活性剂
两性离子型食品表面活性剂属于离子型表面活性剂的范畴,但与阴离子型食品表面活性剂和阳离子型食品表面活性剂不同的是,它可以根据溶液的pH呈现不同的带电性[33-34]。一般来说,两性离子型食品表面活性剂整体表现为电中性,在等电点以下它表现为阳离子型食品表面活性剂行为,相反在较高pH下表现为阴离子型食品表面活性剂行为[35]。两性离子型食品表面活性剂的pH依赖性使得其与蛋白质相互作用的情况更加复杂,因此在研究蛋白质-两性离子型食品表面活性剂复合改善蛋白质性质的过程中,综合考虑特定蛋白质的等电点、带电性和食品表面活性剂带电性等至关重要。
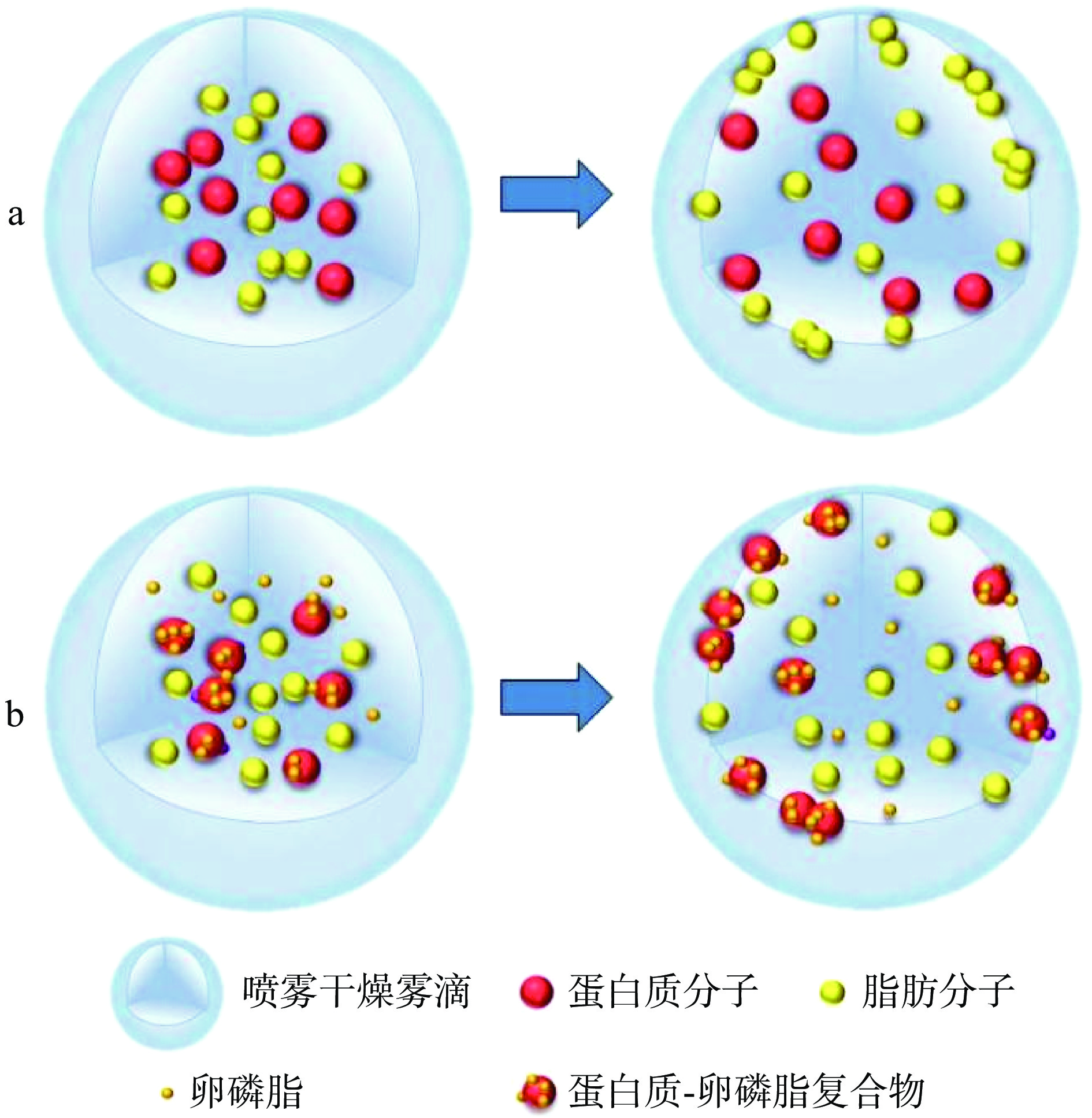
两性离子型表面活性剂按所含阴离子类型可分为卵磷脂型、甜菜碱型、咪唑啉型和氨基酸型,其中甜菜碱型、咪唑啉型和氨基酸型表面活性剂更多的应用于日化领域,而大豆卵磷脂作为分散剂和润湿剂应用于速溶奶粉、速溶豆粉等食品加工产业中的研究最广泛,且复水后的饮品不会产生不良的风味,GB 2760-2015中规定其在固体饮料中的使用量按稀释倍数增加[36-37]。溶液中的大豆卵磷脂同时含有亲水的带电基团和疏水基团,具备离子型食品表面活性剂的所有特征,可以与蛋白质通过静电相互作用、疏水相互作用和氢键作用等结合,形成的蛋白质-卵磷脂复合物影响蛋白质的溶解特性[38]。Hammes等[39]解释了大豆卵磷脂改善奶粉润湿性的内在机理。研究表明,向浓缩牛奶中添加1% (w/w)的卵磷脂后进行喷雾干燥,奶粉润湿时间由5 min缩短至63.9 s,且这种改性方式对奶粉颗粒的含水量、形态、颜色和粒径分布影响不大。其作用机理如图3所示:对于未加入卵磷脂的牛奶在喷雾干燥时(图3a),脂肪优先迁移到雾滴表面;加入卵磷脂后(图3b),疏水相互作用促进了卵磷脂与蛋白的结合,而喷雾干燥时形成的蛋白质-卵磷脂复合物优先于脂肪迁移到蛋白质粉的最外层,颗粒表面脂肪覆盖率减少,因此改善了干燥蛋白质颗粒的润湿性。与阴离子型表面活性剂和阳离子型表面活性剂相比,两性离子型表面活性剂的毒性更低,更适合在食品中的应用[33]。
1.2 非离子型食品表面活性剂
非离子型食品表面活性剂是在水溶液中不离解成离子的表面活性剂,它们是根据其亲水基团的类型进行详细划分的[40]。以多元醇类为代表的非离子食品表面活性剂在溶液中呈电中性,且不受溶液pH和其他离子影响,可通过疏水相互作用和氢键与蛋白质结合形成水化层结构,进而改善蛋白质粉溶解性。非离子型食品表面活性剂相对于离子型食品表面活性剂而言,其与蛋白质的作用较弱,一方面,这可能是由于非离子型食品表面活性剂不存在带电基团,与蛋白质结合时,疏水相互作用力相较静电相互作用力更弱;另一方面,非离子食品表面活性剂的临界胶束浓度(critical micelle concentration,CMC)值较小,在溶液中的单体浓度很难达到与蛋白质协同结合的浓度。联合国粮农组织和世界卫生组织批准使用的食品非离子型食品表面活性剂包括甘油脂肪酸酯、丙二醇脂肪酸酯、山梨糖醇酐脂肪酸酯、蔗糖脂肪酸酯、Tween等。其中,山梨糖醇酐脂肪酸酯、Tween、甘油脂肪酸酯等常被应用于乳清蛋白粉和咖啡中以增加其速溶性。
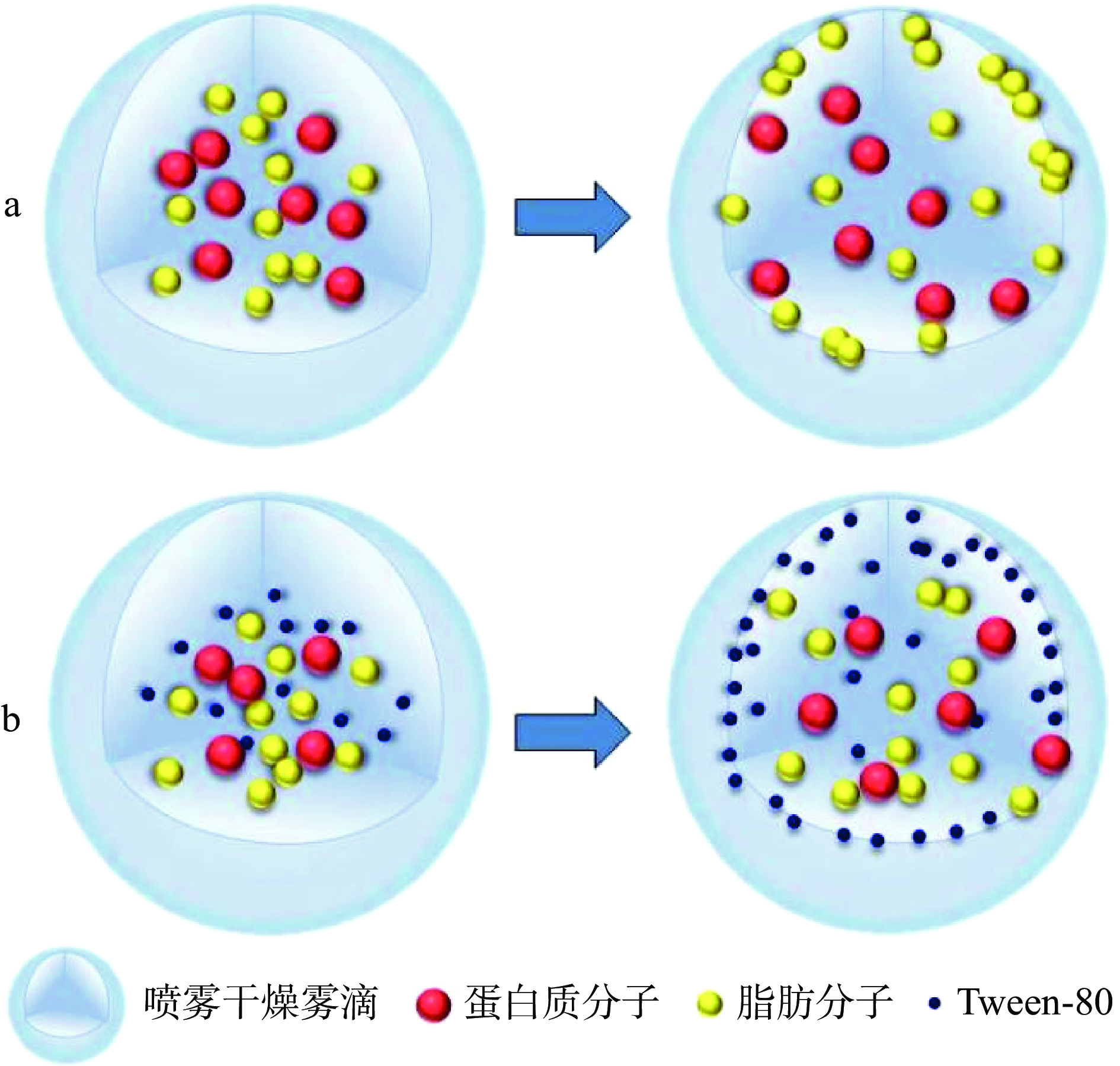
非离子型食品表面活性剂可有效地增加蛋白质溶解性:首先,非离子型食品表面活性剂通过疏水相互作用使蛋白质亲水性增加[41];其次,非离子型食品表面活性剂与界面上的蛋白质发生竞争吸附有利于增加蛋白质粉的溶解性[42]。由此可见,非离子型食品表面活性剂不仅可以通过与蛋白质的相互作用增加蛋白质粉的溶解性,还可以通过其特有的吸附特性改善蛋白质粉的表面特性。Tween-80和蔗糖脂肪酸酯是常见的多元醇型食品非离子型食品表面活性剂,在提升食品蛋白质粉溶解性方面应用广泛,GB 2760-2015中规定Tween-80在固体蛋白饮料中作为分散剂的最大使用量分别为2.0 g/kg,而蔗糖脂肪酸酯可按稀释倍数增大使用量。Lallbeeharry等[43]在喷雾干燥前向全脂牛奶中加Tween-80,可有效提高乳粉的润湿性,这是由于Tween-80在喷雾干燥过程中传质速度较快,与半干雾滴中的脂肪和蛋白质发生竞争吸附,优先于脂肪和蛋白质吸附在油-水界面上并对脂肪球表面进行改性(亲水头部向外,疏水尾插向脂肪),干燥后的粉末表面形成了由食品表面活性剂组成的可湿性外壳,其作用机理如图4所示。同样,蔗糖脂肪酸酯可以与蛋白质发生疏水相互作用而改善蛋白质粉溶解性。研究者们通过控制蔗糖脂肪酸酯中脂肪酸残基的碳数和酯化度,或对不同酯化度的蔗糖酯进行混配,使得亲水亲油平衡值(hydrophilic lipophilic balance,HBL)在1~18内分布[44]。当HLB范围为7~9时,可作为良好的润湿剂;HLB的范围在15~18内,可作为良好的增溶剂[45]。因此,蔗糖酯提升蛋白质粉溶解性的作用显著。然而,非离子型表面活性剂中,聚氧乙烯型表面活性剂在低剂量口服时的致癌性和致变异性限制了其在食品中的应用,其主要用于化妆品及纺织领域。
2. 食品表面活性剂对蛋白质粉溶解过程的影响
蛋白质粉的溶解过程被分为4个步骤[46]:润湿、下沉、分散和溶解。任何一个过程都会影响蛋白质粉的溶解,但这些步骤并不是接续发生的,它们同时发生且相互影响,因此不能够清晰的分开。食品表面活性剂对蛋白质粉溶解有积极影响。一方面,食品表面活性剂的特殊结构使得其具有降低界面张力的作用;另一方面,食品表面活性剂可以通过疏水相互作用(所有以上食品表面活性剂类型)、静电相互作用(离子型、两性离子型食品表面活性剂)、氢键(所有以上食品表面活性剂类型)等与蛋白质结合。食品表面活性剂-蛋白质混合体系界面吸附有两种机理:增溶和置换,即界面上的蛋白质与食品表面活性剂形成复合物而进入水相,或界面上的蛋白质被食品表面活性剂置换[47]。当食品表面活性剂达到其临界胶束浓度时,食品表面活性剂在溶液中形成的胶团对蛋白质起到增溶作用。食品表面活性剂对蛋白质粉溶解度的提升主要是通过调节蛋白质粉的润湿性、分散性和溶解度来实现的。
2.1 润湿性
研究表明润湿是蛋白质粉溶解的限速步骤[48],它会影响粉末接下来的下沉及分散过程。导致蛋白质粉不易润湿的原因可以分为以下几种:a.蛋白质粉表面的难湿成分(如脂肪);b.粉体性质(粉末细微,比表面积大导致粉末团聚);c.难湿水化膜的形成(蛋白质薄膜)。食品工业为解决粉末难被润湿的问题,已采用流化床喷涂粘结剂的造粒的方法来减小粉体比表面积,有效的防止了粉末聚集[49]。然而,最适合粉末被润湿的粒径尺寸难以控制,因此还需要过筛进行粉末的分级处理。另外,流化床造粒方法是两段制粒法,操作复杂。喷雾干燥方法仍是现在食品工业中制备蛋白质粉的常用方法,但是喷雾干燥粉末比表面积大,并且高温导致的传热传质现象使水分快速蒸发,颗粒表面迅速成壳,脂肪等不溶物质迁移到颗粒表面等导致粉末不易被润湿。为解决以上问题,研究者们在采用喷雾干燥制备基础粉末的同时,向颗粒表面喷涂卵磷脂、吐温等食品表面活性剂,通过接触角和润湿时间对润湿性进行评价,发现蛋白质粉的润湿性显著提升。例如,Wu等[11]通过向乳清分离蛋白粉表面喷涂2% (w/v)的卵磷脂,粉末的润湿时间从(36±1)min下降到(42±2) s。作者同时利用接触角对润湿性进行了评价,发现原乳清分离蛋白粉的接触角在200 s时为45°,而喷涂2% (w/v)卵磷脂后,粉末的接触角在1.52 s时就达到了0°。Ji等[50]也有相似的发现,喷涂5% (w/w)卵磷脂的乳清分离蛋白粉的润湿性从>20 min下降到(3±1) s。润湿性的改善是由于食品表面活性剂和蛋白质粉的团聚形成了大尺寸颗粒,增加了粉体表面不规则度和颗粒间的孔隙度,这有利于增加水的可接触面积。此外,卵磷脂与蛋白质形成的卵磷脂-蛋白质复合物吸附到粉末表面显著降低了界面张力使粉末更容易浸没在水中。粉末与水面接触时形成的难湿水化膜是阻碍蛋白质粉润湿的主要因素。当蛋白质粉被加入到溶液中时,即使粉末中不含有脂肪,界面上也会出现一层薄膜阻碍蛋白质粉的进一步润湿,这层薄膜被认为是蛋白质覆盖层,Gaiani等[51]的研究发现,蛋白质粉的组成成分及含量影响粉体的润湿性,且粉体润湿性与蛋白质表面覆盖率呈负相关。这是因为,大量的蛋白质堆积在粉体表面时会形成致密的蛋白质网膜,水分难以渗入粉体,导致粉末的润湿性差[52]。食品表面活性剂与蛋白质通过疏水相互作用或静电相互作用与蛋白质形成的复合物破坏了致密的蛋白质网络结构。因此,食品表面活性剂对改善蛋白质粉溶解性至关重要。
2.2 分散性
分散性是指粉末状颗粒之间解离并分散在溶液中的能力[53]。蛋白质粉在溶液中的分散涉及到小的固体颗粒从大颗粒表面释放,此时水分进入到颗粒的间隙中使蛋白质粉团聚体崩裂瓦解,然后使蛋白质粉颗粒分布在水中[13]。结块是影响蛋白质粉分散速度的因素之一,粉末结块可以被看作是粉末颗粒通过各种不同的分子间作用力,如范德华力、静电力和磁性而发生聚集[54],但是粉体之间的聚集并不是严密的。通常,堆积的蛋白质粉颗粒之间会存在微小的间隙,蛋白质粉块内部固-固界面的分离是改善蛋白质粉分散性的切入点。当食品表面活性剂存在于蛋白质溶液中时,食品表面活性剂通过作用于这些蛋白质间隙中暴露的基团,使固-固界面产生排斥作用,因此在搅拌溶解的过程中可以有效减小粉体颗粒分散所需的机械功,改善蛋白质粉的分散性[55]。离子型食品表面活性剂吸附在间隙时,静电斥力使颗粒易于分散在溶液中,正如冯进[56]发现十二醇葡萄糖双子表面活性剂(Gemini-C12)与热变性卵白蛋白(OVA)相互作用时,Gemini-C12可以填充颗粒表面OVA吸附层留下的空隙,从而提高了纳米颗粒的贮藏稳定性和再分散性。
2.3 溶解度
蛋白质溶解度的热力学定义是在一定的离子浓度、温度、pH和其他添加剂存在的情况下,与固体相结晶相平衡的蛋白质浓度[57]。蛋白质溶解度受内外多种因素的影响,能够导致蛋白质变性的外在因素如高温、强酸强碱、强离子浓度等都会使蛋白质凝结或絮沉,从而降低蛋白质的溶解度。而影响蛋白质溶解度的内在因素主要取决于蛋白质表面氨基酸的亲疏水性,因此从蛋白质自身性质出发,探究能够影响蛋白质表面亲疏水性的因素,是改善其溶解性的根本途径。Zhang等[58]研究发现,向花生蛋白溶液中加入15 wt%的Tween-20能显著提高蛋白质的溶解度。这是因为,Tween-20与花生蛋白的疏水表面发生了疏水相互作用,并覆盖了蛋白质表面的这些疏水区域,导致花生蛋白亲水性和溶解度增加。马爽[59]通过添加不同剂量的食品表面活性剂,使蛋黄粉复配后溶解度提高了6.45%。这些食品表面活性剂改变了蛋白质的自身性质,降低了蛋白质表面的疏水性,从而有效增溶蛋白质。增溶的机理与食品表面活性剂的临界胶束浓度有关。增溶剂在临界胶束浓度以下时,被增溶物的溶解度几乎不变,当增溶剂的浓度达到临界胶束浓度以后,食品表面活性剂形成胶束,使被增溶物的溶解度显著增高。但是,被增溶物所进入胶束的位点与其化学结构、食品表面活性剂的种类及溶剂的性质有关。食品表面活性剂的增溶位点可分为以下四种情况[60]:a增溶于胶团的内核;b增溶于胶团的定向食品表面活性剂分子之间,形成栅栏结构;c增溶于胶团表面;d增溶于食品表面活性剂的极性基团之间。对于蛋白质这种两亲性分子来说,极易被吸附在胶束的亲水基表面或定向排列于胶束的栅状层,形成混合胶束。此时,蛋白质表面的疏水基团与食品表面活性剂胶团中的疏水位点发生疏水性相互作用,掩埋了蛋白质表面的部分疏水氨基酸,从而蛋白质溶解度得到改善。
3. 影响食品表面活性剂改善蛋白质粉溶解性的因素
3.1 蛋白质粉中固形物含量
蛋白质溶液的固形物含量会影响干燥过程中半干液滴内部水分迁移速度。因为,在对含有固体的液滴进行干燥时,半干液滴表面的水分会被优先除去,而后液滴内部逐渐受热,促进水分迁移并蒸发。然而对于高固形物含量的液滴来说,半干燥颗粒内的水分扩散将构成传质的主要阻力。当颗粒内部水分扩散的速度远低于其表面水分蒸发速度时,液滴表面会形成一层硬的表面壳,从而阻碍食品表面活性剂在液滴表面的富集,影响食品表面活性剂改善蛋白质粉润湿性效果。Tian等[61]通过喷雾干燥前加入卵磷脂或Tween-80生产速溶全脂奶粉时,对比固形物含量分别是32 wt%和43 wt%的乳滴润湿性,发现高固体奶含水量更低,除去表面水分所需时间短,干燥过程中快速成壳,在很大程度上抑制了干燥引起的食品表面活性剂迁移和表面富集。此外,高固体奶的粘度高于低固体奶,降低了各物料在干燥诱导迁移过程中的扩散率。因此,在干燥制粉时,适当的固形物含量能够确保雾滴内部传热传质速度与表面水分蒸发速度相适宜,使食品表面活性剂发挥更大的作用。
3.2 食品表面活性剂浓度
食品表面活性剂降低表面张力程度及其与蛋白质的相互作用与食品表面活性剂的浓度有关。适当的浓度可以增加食品表面活性剂在蛋白质粉表面的覆盖率,降低蛋白质表面疏水性,对溶解性的改善效果更加明显。马爽[59]将不同添加量的卵磷脂(0.5%、1.0%、1.5%、2.0%、2.5% (w/w))对全蛋粉和蛋黄粉溶解性的影响进行了研究,发现卵磷脂添加量分别为1.5% (w/w)和2% (w/w)时,全蛋粉和蛋黄粉的分散性和水合能力最好,这是由于食品表面活性剂可以最大程度的吸附在蛋白质粉的表面形成一层单分子覆盖层,颗粒之间不再因复水作用而相互粘聚,进而提高了蛋粉的分散性。然而,当食品表面活性剂在界面上形成的单层吸附达到饱和时,表面张力不会随食品表面活性剂含量的增加而降低。
3.3 食品表面活性剂类型
食品表面活性剂通过促进蛋白质结构展开和与蛋白质形成复合物提高粉末的溶解性。对于结构已知且在中性溶液中整体呈电负性的蛋白质,阴离子型食品表面活性剂往往能够中和蛋白质表面多余的正电荷而使其净负电荷增加,静电斥力的增大有助于粉末在分散过程中的分离[62]。相反,当蛋白质表面整体电荷为正时,阳离子型食品表面活性剂通过疏水性互作用与蛋白质结合,增加蛋白质间静电斥力,对改善粉末的润湿和分散更显著。然而,对于某些表面性质未知的蛋白质,非离子型食品表面活性剂往往是首选,这是因为其良好的生物相容性且对电解质的敏感性较低。另外,蛋白质与食品表面活性剂间的疏水相互作用部分决定了复合物的形成及结构,非离子型食品表面活性剂形成胶束的临界浓度较低,这使表面疏水性强的蛋白质能够迅速加溶于胶束中促进溶解。因此,根据蛋白质带电性及疏水性等特征选择适当食品表面活性剂类型,对改善蛋白质粉溶解性至关重要。单媛媛[27]通过向含有β-巯基乙醇的卵黏蛋白中添加1% (w/w)的Tween-80和3% (w/w)的PEG4000等非离子型食品表面活性剂,发现添加3% (w/w)的PEG4000有效的提高了卵黏蛋白的溶解性,并且与1% (w/w)的Tween-80配合使用时,卵黏蛋白完全溶解呈澄清透明溶液。古扎努尔·艾斯卡尔[63]通过非离子型食品表面活性剂组合(即单硬脂酸甘油酯、蔗糖酯和糖脂肪酸酯单硬脂酸甘油酯按1:1:1)有效降低表面张力,提高了大豆分离蛋白的溶解性和粘度。
3.4 食品表面活性剂与蛋白质粉的混合方式
向蛋白质粉中添加食品表面活性剂的方式会影响作用效果,进而造成蛋白质溶解性的差异。食品表面活性剂与蛋白质的混合方式包括干混和湿混,干混即通过滚筒或机械搅拌机将蛋白质粉末和食品表面活性剂粉末直接混合均匀制粉;湿混可以分为两类,其一,向蛋白质溶液中加入食品表面活性剂后进行干燥,得到含有食品表面活性剂的蛋白质粉;其二,通过流化床向蛋白质粉表面喷涂食品表面活性剂溶液制粉。王娟等[64]分别用直接机械搅拌法、喷雾干燥法和冷冻干燥法生产速溶卵磷脂复合大豆蛋白粉时发现,三种生产方式均能提高大豆蛋白粉的溶解性,但是喷雾干燥法制得的蛋白质粉的溶解性显著高于直接机械搅拌法,这可能是由于喷雾干燥法可使卵磷脂与蛋白质结合,改善蛋白质自身表面性质,更加均匀的分散并吸附在蛋白质粉的表面。而采用机械搅拌法不能够使蛋白质和食品表面活性剂产生疏水性互作用或静电相互作用等内部作用力,且存在混合不均匀等现象。故湿混较干混更能有效的改善蛋白质粉的溶解性。
4. 结论与展望
食品表面活性剂以其两亲性的结构特点,可以通过降低溶液表面张力,与蛋白质发生疏水或静电相互作用,从而达到改善蛋白质粉溶解性的效果。有相关研究表面,卵磷脂、蔗糖酯、Tween等常用的食品表面活性剂在提高蛋白质粉润湿性、分散性及溶解度方面作用效果显著。然而,复配了食品表面活性剂的蛋白质粉会导致产品颜色加深或产生不良气味,出于对产品品质的要求,在今后的工作中可以将原本气味较重的食品表面活性剂与其他类型食品表面活性剂配合使用,以期在达到在同等改善蛋白质粉溶解性的效果下,更好地保持产品感官性质。除此之外,双食品表面活性剂或三食品表面活性剂与蛋白质相互作用的内在机制值得进一步的研究。目前,可应用于改善蛋白质粉溶解性的食源性表面活性剂种类仍然有限,尝试开发安全性高且增溶效果强的人工合成食品表面活性剂是未来研究的热点,将为速溶型蛋白质基料的开发和创制提供新思路。
-
-
[1] WU S, FITZPATRICK J, CRONIN K, et al. The effect of pH on the wetting and dissolution of milk protein isolate powder[J]. Journal of Food Engineering,2019,240:114−119. doi: 10.1016/j.jfoodeng.2018.07.022
[2] MONIKA W, RENATA R, REGINE S, et al. Physico-chemical properties of an innovative gluten-free, low-carbohydrate and high protein-bread enriched with pea protein powder[J]. Scientific Reports,2021,11(1):14498−14498. doi: 10.1038/s41598-021-93834-0
[3] NNAEDOZIE C C, SANDERS C, MONTES E C, et al. Investigation of rehydration of food powder mixtures[J]. Powder Technology,2019,353:311−319. doi: 10.1016/j.powtec.2019.05.043
[4] 叶晶. 婴儿配方粉品质分析及冲调性研究[D]. 哈尔滨: 东北农业大学, 2018 YE J. Powdered infant formula quality analysis and brewability study[D]. Harbin: Northeast Agricultural University, 2018.
[5] PEISHAN L, LONG S, YONGGUO J. Using microwave-assisted phosphorylation to improve foaming and solubility of egg white by response surface methodology[J]. Poultry Science,2019,98(12):7110−7117. doi: 10.3382/ps/pez424
[6] TRISTAN F, JENNIFER B, CAROLE P-T, et al. Impact of the whey protein/casein ratio on the reconstitution and flow properties of spray-dried dairy protein powders[J]. Powder Technology,2021,391:275−281. doi: 10.1016/j.powtec.2021.06.026
[7] 张爱琴, 孙乾, 李芳, 等. 超微粉碎对红花籽粕蛋白质形态和理化功能性的影响[J]. 食品与发酵工业,2019,45(1):115−120. [ZHANG A Q, SUN Q, LI F, et al. Effects of ultramicro pulverization on protein morphology and physicochemical properties of safflower seed meal[J]. Food and Fermentation Industries,2019,45(1):115−120. doi: 10.13995/j.cnki.11-1802/ts.016496 [8] YAN T, AHMED T, PEIPEI Z, et al. Effects of protein concentration, pH, and NaCl concentration on the physicochemical, interfacial, and emulsifying properties of β-conglycinin[J]. Food Hydrocolloids,2021,118:106784. doi: 10.1016/j.foodhyd.2021.106784
[9] JACOB R G, RAM R P, FRANCESCA B, et al. Pilot-scale production and physicochemical characterisation of spray-dried nanoparticulated whey protein powders[J]. International Journal of Dairy Technology,2021,74(3):581−591. doi: 10.1111/1471-0307.12797
[10] 李笑笑, 孙东晓, 张祎, 等. 高场强超声波对大豆分离蛋白溶解性的改善作用[J]. 现代食品科技,2021,37(6):124−128,174. [LI X X, SUN D X, ZHANG Y, et al. Improving the solubility of soybean protein isolate by high-intensity ultrasound[J]. Modern Food Science and Technology,2021,37(6):124−128,174. [11] WU S, FITZPATRICK J, CRONIN K, et al. Effects of spraying surfactants in a fluidised bed on the rehydration behaviour of milk protein isolate powder[J]. Journal of Food Engineering,2020,266(C):109694.
[12] ZHANG L, PAN Z, SHEN K, et al. Influence of ultrasound-assisted alkali treatment on the structural properties and functionalities of rice protein[J]. Journal of Cereal Science,2018,79:204−209. doi: 10.1016/j.jcs.2017.10.013
[13] LI P, JIN Y, SHENG L. Impact of microwave assisted phosphorylation on the physicochemistry and rehydration behaviour of egg white powder[J]. Food Hydrocolloids,2020,100(C):105380.
[14] 沈立. 阳离子表面活性剂在固-液界面上的吸附机制[J]. 宝鸡文理学院学报 ( 自然科学版 ) ,2019,39(4):47−54. [SHEN L. Adsorption mechanism of cationic surfactants at the silica solid-aqueous interface[J]. J Baoji Univ Arts & Sc (Nat. Sci. Ed),2019,39(4):47−54. doi: 10.13467/j.cnki.jbuns.2019.04.011 [15] 董睿. 离子型表面活性剂的固液界面性质研究[D]. 贵阳: 贵州大学, 2019 DONG R. The porperties of the ionic surfactant at the solid/liquid interface[D]. Guiyang: Guizhou University, 2019.
[16] 陈青明. 表面活性剂的化学结构和应用研究[J]. 低碳世界,2021,11(8):227−228. [CHEN Q M. Research on the chemical structure and application of surfactants[J]. Low Carbon World,2021,11(8):227−228. doi: 10.3969/j.issn.2095-2066.2021.08.109 [17] 张晓光. 表面张力法和电导法对比测定表面活性剂临界胶束浓度[J]. 化学教育(中英文),2021,42(18):134−136. [ZHANG X G. Comparison of determination of surfactant critical micelle concentration by surface tension and conductivity methods[J]. Chinese Journal of Chemical Education,2021,42(18):134−136. [18] 郝姗姗, 赵莉, 徐宝财. 表面活性剂的性能与应用(ⅩⅩⅦ)[J]. 日用化学工业,2016,46(3):129−135. [HSO S S, ZHAO L, XU B C. Performance and applications of surfactants(ⅩⅩⅦ)[J]. China Surfactant Detergent & Cosmetics,2016,46(3):129−135. doi: 10.13218/j.cnki.csdc.2016.03.002 [19] 杨泽宇, 台秀梅, 刘惠民, 等. 表面活性剂在化妆品中的应用[J]. 日用化学品科学,2019,42(10):50−55. [YANG Z Y, TAI X M, LIU H M, et al. Applications of surfactants in cosmetics[J]. Detergent & Cosmetics,2019,42(10):50−55. doi: 10.3969/j.issn.1006-7264.2019.10.010 [20] 张冬喜, 李新钰, 石磊, 等. 高耐碱表面活性剂的开发及在工业清洗中的应用[J]. 沈阳化工大学学报,2020,34(2):97−106. [ZHANG D X, LI X Y, SHI L, et al. Development of high alkali-resistant surfactant and its application in Industrial Cleaning[J]. Journal of Shenyang University of Chemical Technology,2020,34(2):97−106. doi: 10.3969/j.issn.2095-2198.2020.02.001 [21] 马凤仙. 表面活性剂在润滑油中的应用[J]. 化工设计通讯,2019,45(7):148,197. [MA F X. Analysis of the application of surfactant in lubricating oil[J]. Chemical Engineering Design Communications,2019,45(7):148,197. doi: 10.3969/j.issn.1003-6490.2019.07.097 [22] SHITAL S, SUNITA P, T S, et al. Application of surfactant in various fields[J]. International Journal of Scientific & Engineering Research,2015,6(12):30−32.
[23] SUHAIL M, JANAKIRAMAN A K, A K, et al. Surfactants and their role in pharmaceutical product development: An overview[J]. Journal of Pharmacy and Pharmaceutics,2019,6(2):72−82.
[24] NAKAI S, HO L, TUNG M A, et al. Solubilization of rapeseed, soy and sunflower protein isolates by surfactant and proteinase treatments[J]. Canadian Institute of Food Science and Technology Journal,1980,13(1):14−22. doi: 10.1016/S0315-5463(80)73296-0
[25] XIA W, MA L, CHEN X, et al. Physicochemical and structural properties of composite gels prepared with myofibrillar protein and lecithin at various ionic strengths[J]. Food Hydrocolloids,2018,82:135−143. doi: 10.1016/j.foodhyd.2018.03.044
[26] GIROUX H J, BRITTEN M. Heat treatment of whey proteins in the presence of anionic surfactants[J]. Food Hydrocolloids,2003,18(4):685−692.
[27] 单媛媛. 鸡蛋清卵粘蛋白的纯化、增溶及抗感染活性研究[D]. 武汉: 华中农业大学, 2013 SHAN Y Y. Research on the preparation, solubility enhancement and anti-infection of ovomucin from hen egg[D]. Wuhan: Huazhong Agricultural University, 2013.
[28] GELARDI G, MANTELLATO S, D M. Science and technology of concrete admixtures[M]. England: Woodhead Publishing, 2016: 149-218.
[29] GAIKWAD K K, LEE S M, LEE J S, et al. Development of antimicrobial polyolefin films containing lauroyl arginate and their use in the packaging of strawberries[J]. Journal of Food Measurement and Characterization,2017,11(4):1706−1716. doi: 10.1007/s11694-017-9551-0
[30] MANRIQUE Y, GIBIS M, SCHMIDT H, et al. Influence of application sequence and timing of eugenol and lauric arginate (LAE) on survival of spoilage organisms[J]. Food Microbiology,2017,64:210−218. doi: 10.1016/j.fm.2017.01.002
[31] CHI K, CATCHMARK J M. Enhanced dispersion and interface compatibilization of crystalline nanocellulose in polylactide by surfactant adsorption[J]. Cellulose,2017,24(11):4845−4860. doi: 10.1007/s10570-017-1479-3
[32] HUGH M, MICHAŁ B, SILVIA G. Biocompatible dispersants for carbon nanomaterials[J]. Applied Sciences,2021,11(22):10565. doi: 10.3390/app112210565
[33] 王学川, 郝东艳, 魏超, 等. 两性表面活性剂在皮革加脂中的应用研究进展[J]. 中国皮革,2020,49(6):20−26. [WANG X C, HAO D Y, WEI C, et al. Research progress on the application of amphoteric surfactants in lether fatliquoring[J]. China Leather,2020,49(6):20−26. doi: 10.13536/j.cnki.issn1001-6813.2020-007-004 [34] SEUNGYEOP B, DONGWOOK S, GYUCHANG K, et al. Influence of amphoteric and anionic surfactants on stability, surface tension, and thermal conductivity of Al2O3/water nanofluids[J]. Case Studies in Thermal Engineering,2021,25:100995. doi: 10.1016/j.csite.2021.100995
[35] RATAN S, ANIRUDDHA P, ATANU R, et al. Properties and applications of amphoteric surfactant: A concise review[J]. Journal of Surfactants and Detergents,2021,24(5):709−730. doi: 10.1002/jsde.12542
[36] 韩敏. 表面活性剂在食品工业中的应用与发展[J]. 河南化工,2010,27(4):1−2, 4. [HAN M. Application and development of surfactant in food industry[J]. Henan Chemical Industry,2010,27(4):1−2, 4. doi: 10.3969/j.issn.1003-3467.2010.04.001 [37] 王浩, 刘素稳, 郭宝芹, 等. 速溶蛋白粉的研制[J]. 食品工业科技,2007(11):126−128. [WANG H, LIUU S W, GUO B Q, et al. Development of instant protein powder[J]. Science and Technology of Food Industry,2007(11):126−128. doi: 10.3969/j.issn.1002-0306.2007.11.038 [38] 刘宝华, 张菀坤, 伍丹, 等. 大豆蛋白—磷脂交互作用与乳液特性构效关系研究进展[J]. 中国食物与营养, 2017, 23(9): 31−35 LIU B H, ZHANG W K, WU D, et al. The relationship between interaction of soybean protein-phospholipid and emulsion properties[J] Food and Nutrition in China, 2017, 23(9): 31−35.
[39] HAMMES M V, ENGLERT A H, NOREñA C P Z, et al. Study of the influence of soy lecithin addition on the wettability of buffalo milk powder obtained by spray drying[J]. Powder Technology,2015,277:237−243. doi: 10.1016/j.powtec.2015.02.047
[40] 缑卫军, 吴朝阳. 浅谈表面活性剂的特性与应用[J]. 山西科技,2020,35(6):15−20. [HOU W J, WU C Y. An introduction to the properties and applications of surfactants[J]. Shanxi Science and Technology,2020,35(6):15−20. doi: 10.3969/j.issn.1004-6429.2020.06.005 [41] 程欢, 唐传核. 不同HLB值非离子型表面活性剂与粘蛋白的相互作用[J]. 现代食品科技,2018,34(9):64−69. [CHENG H, TANG C H. Interaction between nonionic surfactants with different HLB values an mucin[J]. Modern Food Science and Technology,2018,34(9):64−69. doi: 10.13982/j.mfst.1673-9078.2018.9.011 [42] 娄丽丽, 章绍兵, 王小花. 吐温与蛋白质相互作用的研究进展[J]. 粮食与油脂,2018,31(3):6−8. [LOU L L, ZHANG S B, WANG X H. Research progress on interaction of Tween and protein[J]. Cereals & Oils,2018,31(3):6−8. doi: 10.3969/j.issn.1008-9578.2018.03.002 [43] LALLBEEHARRY P, TIAN Y, FU N, et al. Effects of ionic and nonionic surfactants on milk shell wettability during co-spray-drying of whole milk particles[J]. Journal of Dairy Science,2014,97(9):5303−5314. doi: 10.3168/jds.2013-7772
[44] 石爽, 曾锦毓, 张鹏, 等. 糖基表面活性剂的研究进展[J]. 天津造纸,2020,42(1):6−11. [SHI S, ZENG J L, ZHANG P, et al. Research progress of sugar based surfactants[J]. Tianjin Paper Making,2020,42(1):6−11. doi: 10.3969/j.issn.1674-5469.2020.01.002 [45] 张锐, 王玉, 高正松, 等. 聚山梨酯80的化学组分与其增溶作用的关系研究[J]. 中国药学杂志,2015,50(10):876−880. [ZHANG R, WANG Y, GAO Z S, et al. Relationship between the chemical composition of polysorbate 80 and its solubilization effect[J]. Chinese Pharmaceutical Journal,2015,50(10):876−880. [46] ONG X Y, TAYLOR S E, RAMAIOLI M. Rehydration of food powders: Interplay between physical properties and process conditions[J]. Powder Technology,2020,371:142−153. doi: 10.1016/j.powtec.2020.05.066
[47] SHEN Y, CHANG C, SHI M, et al. Interactions between lecithin and yolk granule and their influence on the emulsifying properties[J]. Food Hydrocolloids,2020,101(C):105510.
[48] 余韵. 浓缩乳蛋白粉复水性对高蛋白中间水分食品体系质地的影响[D]. 无锡: 江南大学, 2019 YU Y. Effect of rehydration properties of milk protein concentrate on texture of high-protein intermediate moistuer food system[D]. Wuxi: Jiangnan University, 2019.
[49] DONGHYUN L, ANDRES L, MINJEONG L, et al. Fluidized-bed granulation of probiotics-encapsulated spray-dried skim milk powder: Effects of a fluidizing aid, moisture-activation and dehydration[J]. Foods,2021,10(7):1600. doi: 10.3390/foods10071600
[50] JI J, CRONIN K, FITZPATRICK J, et al. Enhanced wetting behaviours of whey protein isolate powder: The different effects of lecithin addition by fluidised bed agglomeration and coating processes[J]. Food Hydrocolloids,2017,71:94−101. doi: 10.1016/j.foodhyd.2017.05.005
[51] GAIANI C, MORAND M, SANCHEZ C, et al. How surface composition of high milk proteins powders is influenced by spray-drying temperature[J]. Colloids and Surfaces B: Biointerfaces,2009,75(1):377−384.
[52] ANDERSSON I M, MILLQVIST-FUREBY A, SOMMERTUNE J, et al. Impact of protein surface coverage and layer thickness on rehydration characteristics of milk serum protein/lactose powder particles[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects,2019,561:395−404. doi: 10.1016/j.colsurfa.2018.10.073
[53] 迟玉杰, 沈青, 赵英, 等. 提高全蛋粉速溶性的研究[J]. 中国家禽,2016,38(12):1−3. [CHI Y J, SHEN Q, ZHAO Y, et al. An investigation into improving the quick solubility of whole egg powder[J]. China Poultry,2016,38(12):1−3. doi: 10.16372/j.issn.1004-6364.2016.12.001 [54] 李延华, 王伟军, 郭亮, 等. 食品粉末颗粒间的相互作用及结块行为的研究进展[J]. 中国粮油学报,2019,34(3):126−132. [LI Y H, WANG W J, GUO L, et al. Research progress on the interactions among particles and caking behavior of food powder[J]. Journal of the Chinese Cereals and Oils Association,2019,34(3):126−132. doi: 10.3969/j.issn.1003-0174.2019.03.022 [55] 陶贤平, 陆小东, 许春江. 表面活性剂对食品级甘氨酸的防结块效果研究[J]. 应用化工,2009,38(2):248−251,259. [TAO X P, LU X D, XU C J. Study of anticaking effects of surfactant on food grade glycine[J]. Applied Chemical Industry,2009,38(2):248−251,259. doi: 10.3969/j.issn.1671-3206.2009.02.027 [56] 冯进. 基于葡萄糖双子表面活性剂和卵白蛋白的生物活性物质载体制备和特性研究[D]. 杭州: 浙江大学, 2017 FENG J. Preparation and characterization of bioactive delivery systems based on gemini alkyl O-glucoside surfactants and ovalbumin[D]. Hangzhou: Zhejiang University, 2017.
[57] KRAMER R M, SHENDE V R, MOTL N, et al. Toward a molecular understanding of protein solubility: increased negative surface charge correlates with increased solubility[J]. Biophysical Journal,2012,102(8):1907−1915. doi: 10.1016/j.bpj.2012.01.060
[58] ZHANG S B, WANG X H, LI X, et al. Effects of Tween 20 and transglutaminase modifications on the functional properties of peanut proteins[J]. Journal of the American Oil Chemists' Society,2020,97(1):93−103. doi: 10.1002/aocs.12309
[59] 马爽. 蛋粉冲调特性及复合型功能蛋粉的研究与开发[D]. 长春: 吉林大学, 2012 MA S. Research and development of fast dissolvability and compound functional egg powder[D]. Changchun: Jilin University, 2012.
[60] 葛毅强, 孙爱东, 蔡同一, 等. 食用乳化剂与增溶剂及其在食品工业中的应用[J]. 食品工业科技,1998(3):78−80. [GE Y Q, SUN A D, CAI T Y, et al. Food emulsifiers and solubilisers and their applications in the food industry[J]. Science and Technology of Food Industry,1998(3):78−80. doi: 10.13386/j.issn1002-0306.1998.03.040 [61] TIAN Y, FU N, WU W D, et al. Effects of co-spray drying of surfactants with high solids milk on milk powder wettability[J]. Food and Bioprocess Technology,2014,7(11):3121−3135. doi: 10.1007/s11947-014-1323-9
[62] ZOU H, ZHAO N, LI S, et al. Physicochemical and emulsifying properties of mussel water-soluble proteins as affected by lecithin concentration[J]. International Journal of Biological Macromolecules,2020,163:180−189. doi: 10.1016/j.ijbiomac.2020.06.225
[63] 古扎努尔·艾斯卡尔. 表面活性剂对大豆分离蛋白及其水解物物化特性影响的研究[D]. 杭州: 浙江大学, 2014 AISIKAER G. Effect of surfantant on phvsicochemical properties of soy protein isolates and its hydrolvsates[D]. Hangzhou: Zhejiang University, 2014.
[64] 王娟, 柴莎莎, 张世宏, 等. 复合大豆蛋白粉研制工艺研究[J]. 粮油加工 ( 电子版 ) ,2015(7):27−31. [WANG J, CHAI S S, ZHANG S H, et al. Development of compound soy protein powder[J]. Cereals and Oils Processing (Electronic),2015(7):27−31. -
期刊类型引用(0)
其他类型引用(1)





 下载:
下载:
 下载:
下载:
