Effect of Konjac Gum on the Gel Structure and Rheological Properties of Myofibrillar Protein-Soy Protein Isolate Composite
-
摘要: 为开发低盐肉制品并降低肉制品生产成本,本研究考察了不同盐浓度下魔芋胶对大豆分离蛋白(Soy protein isolate,SPI)-肌原纤维蛋白(Myofibrillar protein,MP)复合体系凝胶特性的影响。采用流变仪和扫描电镜对SPI-MP复合凝胶的流变学特性和微观结构进行分析,评价SPI、魔芋胶、盐浓度等因素对MP凝胶形成的影响。结果表明:在低盐浓度(0.3 mol/L NaCl)下,相比于4% MP体系,3% MP-1% SPI体系的凝胶强度和持水性都显著升高(P<0.05),凝胶强度从43 g增至97 g,持水性从36%增至50%。但添加高剂量SPI(2% MP-2% SPI体系)却减弱了其对凝胶强度和持水性的增强作用。在0.6 mol/L盐浓度下,相比于4% MP体系,2% MP-2% SPI体系的凝胶强度从177 g降低至89 g。高添加量魔芋胶对MP-SPI复合体系的凝胶强度和持水性具有增强作用,在0.3 mol/L 盐浓度下,添加1%魔芋胶后2% MP-2% SPI体系的凝胶强度从66 g增至93 g,其持水性也从44%增至65%。这表明高剂量魔芋胶可减弱高剂量大豆分离蛋白对MP-SPI复合体系凝胶的破坏作用。扫描电镜结果表明,这主要是魔芋胶的强持水能力及大豆分离蛋白的填充起到了凝胶促进作用。因此,在0.3 mol/L盐浓度下,0.5%~1%添加量的魔芋胶能够很好地改善低SPI替代量(1%)的MP蛋白凝胶特性。Abstract: To develop low-salt meat products and achieve the reduction in costs of meat production, the effect of konjac gum on the gel properties of soy protein isolate (SPI)-myofibrillar protein (MP) composite at various salt concentrations was investigated in this study. For the purpose of evaluating the effects of SPI, konjac gum, salt concentration, and other factors on MP gel formation, rheological properties and microstructures of the SPI-MP composite gels were analyzed using a rheometer and scanning electron microscopy. The obtained results indicated that at low salt concentration (0.3 mol/L NaCl), the gel strength of 3% MP-1% SPI composite gel significantly increased (P<0.05) to 97 g relative to 43 g of the 4% MP gel, and the water-holding capacity also increased from 36% to 50%. However, the gel strength and water-holding capacity were decreased when the replacement amount of SPI increased (2% MP-2% SPI composite) compared with 3% MP-1% SPI composite. The gel strength decreased from 177 g of 4% MP to 89 g of 2% MP-2% SPI composite with at 0.6 mol/L NaCl concentration. The gel strength and water holding capacity of the MP-SPI composite gel were increased after adding high amount of konjac gum. At 0.3 mol/L NaCl concentration, the gel strength of 2% MP-2% SPI composite increased from 66 g to 93 g after adding 1% konjac gum, and the water holding capacity also increased from 44% to 65%. Therefore, konjac gum can eliminate the disruption of SPI on the gel formation of MP. The results of scanning electron microscopy revealed that the strong water-holding capacity of konjac gum and the filling effect of SPI led to the increase in gel strength. Consequently, at the concentration of 0.3 mol/L salt, 0.5%~1% konjac gum could improve the characteristics of MP protein gel with low SPI substitution (1%).
-
Keywords:
- konjac gum /
- soy protein isolate /
- myofibrillar protein /
- gel properties /
- salt concentration
-
肌肉蛋白质由肌原纤维蛋白(Myofibrillar protein,MP)、肌浆蛋白及基质蛋白共同构成,总肌肉蛋白中约55%~60%为肌原纤维蛋白[1]。MP包含肌球蛋白、肌动蛋白、原肌球蛋白等多种蛋白质,通常在离子强度较高的缓冲液中提取,因此被称为盐溶性蛋白[2−3]。这些蛋白质在肉制品功能特性中扮演着重要角色,特别是MP,其凝胶特性对凝胶肉制品品质起着决定性作用[4]。在热诱导凝胶过程中,MP内部棒状的亲水尾部会起到关键的凝胶连接作用,导致三维网络结构形成,将水分子固定在凝胶内部[5−7]。这种良好的凝胶性不仅可以提高产品的持水性,还能更好的分散油滴,提高产品乳化性,赋予凝胶肉制品良好的质地和口感[8]。因此,如何改善MP凝胶特性对于肉制品加工至关重要。然而,MP热诱导凝胶过程受到诸多因素影响,包括蛋白组成和肌肉种类等内在特性,以及盐浓度、压力、pH、加热速率、外源添加物(转谷氨酰胺酶、多糖、多酚)等加工条件[9−11]。盐浓度对肌原纤维蛋白溶出组分的构成和肌原纤维蛋白间的相互作用具有显著影响,MP在低盐浓度下表现出聚集状态,导致蛋白质构象改变,降低肉制品品质[12−13]。但是,盐摄入过多与中风和高血压的发生率增加密切相关[14]。因此,消费者对低盐肉制品的需求不断增加,提高低盐肉制品的产品性能是肉制品市场发展的新方向[15−16]。通过引入功能物质来进一步改善低盐MP特性对探索凝胶化过程中与基质特性密切相关的样品组分之间的相互作用至关重要。
大豆分离蛋白(soy protein isolates,SPI)作为优质的植物蛋白,有着许多优良的功能特性,如持水性、凝胶性,因此被广泛用于肉制品工业中。在肉制品生产过程中加入SPI不仅改善了肉制品的质地,使其更加嫩滑,还降低了成本,丰富了蛋白种类,已成为乳化香肠加工的新方向。Jiang等[17]发现,不同pH处理后的SPI加入到MP中可增强复合凝胶的凝胶强度和流变特性。Herrero等[18]研究也发现,向生肉糜中加入SPI后进行加热,其硬度和咀嚼性都有所增加。然而,也有研究报道,SPI的质地改善作用与其添加量密切相关。Chin等[19]使用2.2%的商业SPI作为肉蛋白的替代物之后,观察到bologna香肠的凝胶强度未出现显著改变,但当替代率达到4.4%时,其口感却开始变得柔软。这说明添加高剂量大豆分离蛋白反而会使凝胶强度、弹性和持水性下降,从而影响肉制品品质。因此,迫切需要探索保持SPI-MP复合蛋白体系的弹性和持水性的方法。魔芋胶是由魔芋产生的中性多糖,其主要成分是葡甘露聚糖,可以作为低热能、低蛋白质、高膳食纤维成分添加到食品中[20]。魔芋胶可与淀粉、卡拉胶、结冷胶等一起添加于肉制品生产过程中,可协同促进MP形成凝胶。低添加量下的魔芋胶有利于体系形成较好的凝胶结构,可显著提高体系粘度[21]。杨振等[22]发现MP的储能模量G´和损失模量G″随魔芋粉添加量增加而逐渐增大,并且添加魔芋粉可以改善凝胶的网状空间结构。
目前,关于非肉蛋白和多糖共同调控MP凝胶特性的研究较少,Hasanpour等[23]分别研究了黄原胶和大豆浓缩蛋白对鲢鱼鱼糜储藏过程中物理化学特性的影响,Lin等[24]研究了卡拉胶和海藻酸钠对含SPI的低脂肉圆制品乳化性的影响,均未对多糖-MP-SPI复合体系的凝胶性能和流变性能进行系统研究。本实验以SPI在肉制品中应用的实际需求为导向,研究魔芋胶对MP-SPI复合凝胶体系的影响,为低盐肉制品开发和改善含SPI的肉制品品质提供理论支持,为多糖和SPI在肉制品中的进一步应用提供理论基础。
1. 材料与方法
1.1 材料与仪器
魔芋胶 山东惠发食品有限公司;大豆分离蛋白 平顶山天晶植物蛋白有限公司;猪外脊肉 购于无锡欧尚超市;氯化钠、牛血清蛋白、氢氧化钠、硫酸铜、浓盐酸、酒石酸钾钠、氯化镁、EGTA、磷酸氢二钠、无水乙醇、磷酸二氢钠、戊二醛、二甲基硅油 均为分析纯,购于国药集团化学试剂有限公司。
BJRJ-12T台式绞肉机 中国嘉兴艾博不锈钢机械工程有限公司;SK2200H型超声波清洗器 上海科导超声仪器有限公司;TA-XT Plus质构仪 英国Stable Micro Systems公司;超级恒温水浴锅 金坛市新航仪器厂;AR G2流变仪 美国TA Instrument公司;TM3030扫描电镜 日立高新技术公司;TDL-5-A台式离心机 上海飞鸽公司;XL-30 ESEM环境扫描电镜 FEI公司;T18 basic高速均质机 英国IKA公司。
1.2 实验方法
1.2.1 肌原纤维蛋白的提取
参考Park等[25]的方法从猪外脊瘦肉中提取肌原纤维蛋白。称取适量猪外脊瘦肉,加入4倍体积(V/m)的分离缓冲液(0.1 mol/L NaCl,2 mmol/L MgCl2,50 mmol/L Na2HPO4,1 mmol/L EGTA,pH7.0),斩拌混匀,将混合液离心(2000×g,15 min,4 ℃),取沉淀。重复两次以确保提取完全。加入4倍体积(V/m)0.1 mol/L NaCl溶液,离心两次(2000×g,15 min,4 ℃),在最后一次离心前用双层纱布过滤掉可见的网状物结缔组织,将混合液的pH调到6.25,最后将肌原纤维蛋白分离物在碎冰中保存。采用双缩脲法测定MP中的蛋白含量,用牛血清蛋白作为标准蛋白制作标准曲线。
1.2.2 魔芋胶-SPI-MP三元体系的建立
本文设置了三个盐浓度梯度(0.1、0.3、0.6 mol/L NaCl浓液),以探究不同盐浓度对凝胶形成的影响。将大豆分离蛋白分别溶解于相应盐浓度的磷酸盐缓冲液(pH6.2)中,搅拌4 h以确保大豆分离蛋白充分溶解,从而得到质量分数为5%的大豆分离蛋白溶液。称取一定质量的魔芋胶粉末,配制成5%浓度的溶液,加热至80 ℃,保持10 min,冷却,即得到魔芋胶溶液。将肌原纤维蛋白和大豆分离蛋白以1:0、3:1、1:1(w/w)三种比例混合,每个样品的蛋白浓度均保持在40 mg/mL,魔芋胶添加量分别为0%、0.1%、0.5%和1%。
1.2.3 流变性质的测定
复合蛋白凝胶粘弹性参照Liu等[26]的方法对凝胶粘弹性进行测定,利用AR G2流变仪在样品形变的线性区域,先测定样品的线性粘弹区,采用Strain Sweep模式,由0.1%扫描到10%,确定平台区域,选择合适的应变值,采用小幅正弦振荡模式对0.3、0.6 mol/L NaCl两个盐浓度混合样品形成凝胶过程中弹性模量(G′)的变化进行测定。使用直径为2 cm的平板夹具,从30 ℃以2 ℃/min的升温速率升到80 ℃,频率为0.1 Hz,最大应变为0.02,板间距为1 mm,在夹具与样品的边缘滴加硅油,以防止水分蒸发,将保护盖扣在夹具外部,记录混合蛋白体系热诱导凝胶过程中整个体系的弹性模量变化。
1.2.4 复合蛋白体系凝胶强度测定
凝胶强度采用质构仪进行测定。称取5 g样品于16.8 mm的平底玻璃管中,用保鲜膜封口,水浴加热至80 ℃(1.0~1.2 ℃/min)。达到80 ℃后,将样品置于冰水中快速冷却,并在4 ℃冰箱中放置过夜。将放置过夜的凝胶样品先在25 ℃的恒温水浴中平衡1 h再进行测定。质构仪设定参数:P/0.5圆柱形探头,测定前速度1.0 mm/s,测定速度为0.5 mm/s,测后速度为10 mm/s,测定距离为样品高度的50%,触发类型为自发,触发力为5 g,数据获得速度为200 pps。在探头下压过程中最大感应力定义为凝胶强度。
1.2.5 混合样品的凝胶持水性测定
参照Xiong等[27]的方法测定混合样品的凝胶持水性。将制备得到的蛋白凝胶放置过夜,然后在室温下平衡1 h进行测试。均匀取样以减少实验误差,取出2 g(m0)样品于5 mL离心管中,样品和离心管总质量为m1,在4 ℃下10000×g离心10 min后,弃去上清液,并用滤纸吸去凝胶表面残留的水分,最后将离心管置于分析天平中称量,此时的样品和离心管质量为m2。凝胶持水性(WHC)按式(1)计算:
WHC(%)=m2−m1m0×100 (1) 式中:WHC—凝胶持水性,%;m0—样品质量,g;m1—离心前样品和离心管总质量,g;m2—离心后将上清液倒掉并用滤纸吸附表面残留水分后称重获得的样品和离心管总质量,g。
1.2.6 复合蛋白体系微观结构的测定
利用环境扫描电镜(ESEM)观察凝胶的微观结构,将制备的蛋白凝胶切成约5 mm×3 mm×7 mm的凝胶块,并粘于ESEM专用的圆形模具上,并置于ESEM样品室中观察。测试条件:加速电压20 kV,恒压119.97 Pa,放大倍数为2000倍。
1.2.7 复合蛋白体系应力松弛测定
线性粘弹区测定,利用流变仪,采用Strain Sweep模式,由0.1%扫描到10%,确定线性粘弹区,选择合适的应变值。在间隙为1 mm样品台上添加适量样品,将多余样品刮掉,周围涂上硅油防止水分蒸发。先升温至80 ℃(2 ℃/min),然后迅速降到20 ℃。采用Stress relaxation模式,最大应变为0.02,松弛时间定为25 min,得到样品的应力松弛曲线。测定时对照组MP浓度为40 mg/mL,多糖组添加量为0.5%。
1.3 数据处理
所有处理重复3次,数据用平均值±标准偏差表示。采用Excel 2016进行数据分析,并用Origin 8.0作图。使用Statistics软件对数据进行显著性分析,P<0.05为具有显著性差异。
2. 结果与分析
2.1 魔芋胶对SPI-MP复合蛋白体系弹性模量的影响
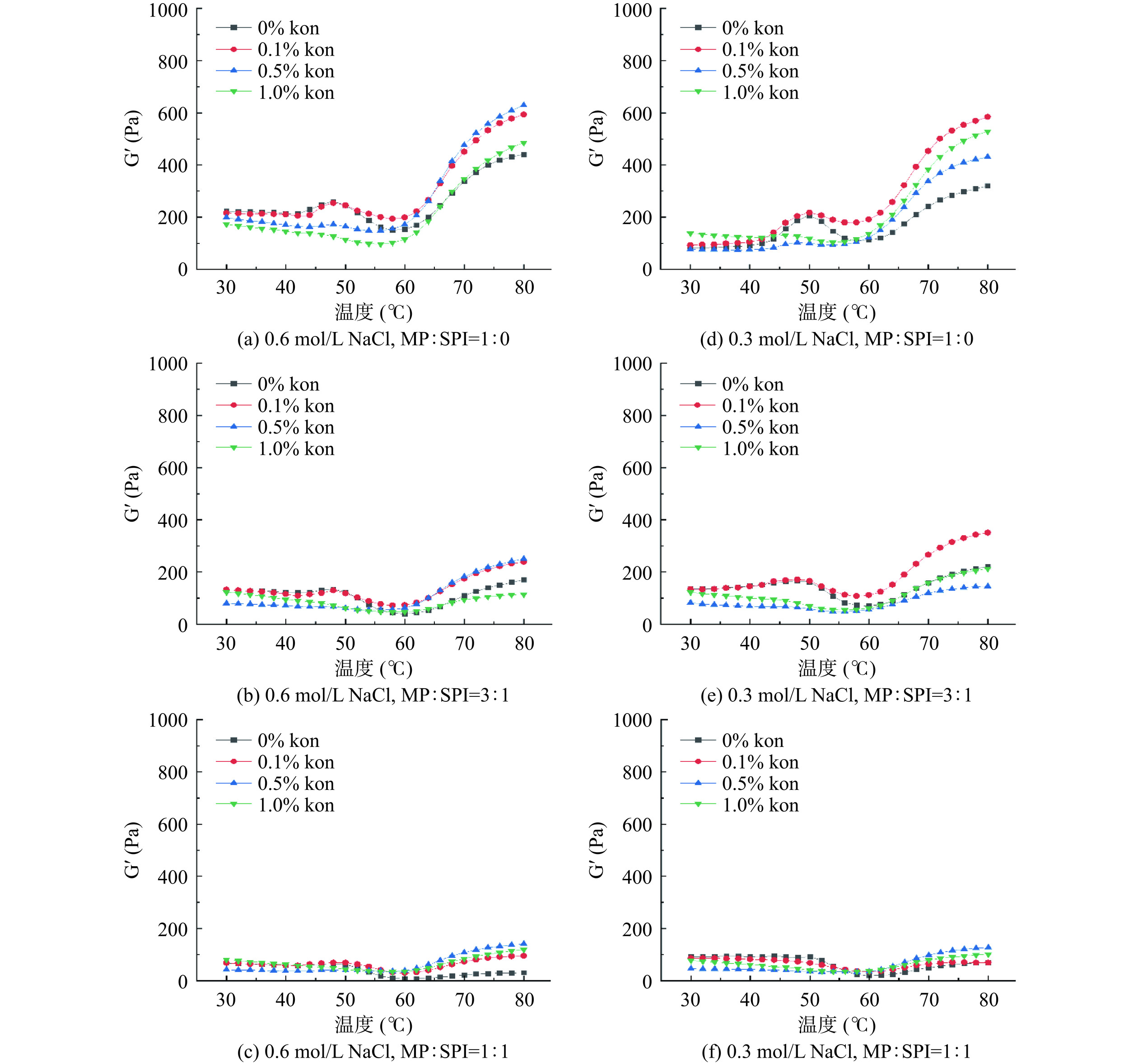
不同的盐浓度下魔芋胶对SPI-MP复合蛋白弹性模量的影响如图1所示。实验发现,在0.1 mol/L NaCl盐浓度下,体系几乎无法形成凝胶,所以只研究复合蛋白体系在0.3和0.6 mol/L NaCl盐浓度下的流变特性变化。在0.6 mol/L盐浓度下,对比不同魔芋胶添加量下MP凝胶的G′发现,当魔芋胶添加量为0.5%时,其G′达到最高值;当添加量增至1%时,G′明显降低。加入SPI后,复合蛋白凝胶体系的G′显著(P<0.05)降低,并且SPI比例越高,G′越低,这可能是SPI加入后减少了加热期间肌球蛋白重链的聚集,导致交联峰往高温方向推移[28]。因此在高盐浓度下,SPI对MP凝胶存在一定干扰作用。对比两种盐浓度下MP和SPI-MP体系的G′,可以发现在0.3 mol/L低盐浓度下,随着魔芋胶添加量的增大,复合蛋白体系G′先升高后下降,最大值出现在0.1%添加量处。在1% SPI-3% MP体系中,当添加高剂量魔芋胶时,体系G′比对照组G′还小,说明添加高剂量魔芋胶对MP-SPI复合蛋白体系形成凝胶具有破坏作用。
2.2 魔芋胶对SPI-MP复合蛋白体系凝胶强度的影响
魔芋胶对SPI-MP复合蛋白体系凝胶强度的影响如表1所示,在0.1 mol/L盐浓度下,当魔芋胶添加量低于0.5%时,所有样品组凝胶强度均很弱。添加0.1%魔芋胶后,4% MP和1% SPI-3% MP体系中的凝胶强度明显降低,从23.2 g和25.4 g分别降至12.9 g和14.8 g;当魔芋胶添加量继续增加时,两种体系的凝胶强度相比于对照组显著(P<0.05)提升,并在1%时达到最大值。综上所述,在0.1 mol/L盐浓度下,添加SPI能够促进凝胶形成,这可能是SPI填充进凝胶网络中,增强了凝胶强度。然而低添加量(0.1%)魔芋胶无法有效地与MP形成足够的相互作用,反而导致凝胶结构不稳定,降低了凝胶强度。当添加量进一步升高时,才显示出凝胶促进作用。在0.3 mol/L盐浓度下,低添加量(1%)SPI同样能增强MP蛋白的凝胶强度,但高剂量SPI却能破坏凝胶,这可能是因为过量SPI与MP之间相互作用,导致凝胶结构紊乱[28−29]。
表 1 魔芋胶添加量对不同盐浓度下复合蛋白体系凝胶强度的影响(g)Table 1. Effect of konjac adding levels on the gel strength of MP-SPI composite under different salt levels (g)盐浓度
(mol/L)蛋白比例 魔芋胶添加量(%) 0 0.1 0.5 1 0.1 4% MP 23.2±3.1f 12.9±1.3g 31.8±2.0e 74.6±5.7c 3% MP+1% SPI 25.4±5.2ef 14.8±2.5g 124.5±10.1a 147.5±5.3a 2% MP+2% SPI 26.9±3.2ef 51.1±2.5d 81.8±4.2c 90.3±4.8b 0.3 4% MP 43.7±4.2e 102.7±5.5c 129.5±7.4b 143.8±8.7a 3% MP+1% SPI 97.7±5.2c 124.5±3.5b 123.8±8.0b 131.2±8.0b 2% MP+2% SPI 66.2±2.2d 23.6±4.0f 65.2±1.9d 93.0±8.9c 0.6 4% MP 177.7±12.3b 188.0±9.8b 225.3±11.3a 175.5±11.1b 3% MP+1% SPI 89.3±1.8ef 102.5±5.0d 140.0±6.3c 99.1±2.8de 2% MP+2% SPI 22.9±3.6h 48.1±4.4g 77.1±2.5f 95.3±6.7de 注:同一盐浓度不同字母(a~g)表示结果具有显著性差异(P<0.05)。 在0.6 mol/L盐浓度下,随着SPI添加量增大,复合蛋白凝胶强度逐渐降低,这说明SPI对复合蛋白凝胶的破坏作用具有剂量效应。添加0.1%魔芋胶后,纯MP和1% SPI-3% MP体系中凝胶强度从177.7 g和89.3 g分别增至188.0 g和102.5 g;当魔芋胶添加量从0.5%增至1%时,纯MP和1% SPI-3%MP体系中的凝胶强度却显著降低(P<0.05),这说明添加过量魔芋胶会破坏蛋白凝胶结构。但魔芋胶对2% SPI-2% MP体系蛋白凝胶强度的增强作用具有剂量效应。高盐浓度下,MP分子充分溶解,与魔芋胶分子之间的氢键作用得以增强,使凝胶强度增加,但添加过量的魔芋胶反而妨碍了MP凝胶网络的形成[30]。在0.1和0.3 mol/L盐浓度下,MP分子与SPI及魔芋胶的之间包埋和氢键作用力,使得添加低剂量SPI和高剂量魔芋胶的复合蛋白体系取得了较好的凝胶强度[31]。
2.3 魔芋胶对SPI-MP复合蛋白体系持水性的影响
持水性可直接影响肉制品的风味、嫩度、颜色等食用品质。魔芋胶对SPI-MP复合蛋白体系持水性的影响如表2所示。在0.1和0.3 mol/L盐浓度下,对比4% MP、1% SPI-3% MP和2% SPI-2% MP体系的持水性发现,3% MP-1% SPI体系的持水性显著提高(P<0.05),并且随着魔芋胶添加量增大,蛋白凝胶的持水性不断增强。这说明低盐浓度下,SPI和魔芋胶均能显著提高样品持水性。当魔芋胶添加量达到0.5%以上时,低盐浓度下复合蛋白凝胶的持水性普遍均低于70%,原因可能是在低盐浓度下MP的溶解较差,不能够使蛋白分子与魔芋胶充分相互作用,无法提高其持水性[19]。
表 2 魔芋胶添加量对不同盐浓度下复合蛋白体系持水性的影响(%)Table 2. Effect of konjac adding levels on the WHC of MP-SPI composite with various salt levels (%)盐浓度
(mol/L)蛋白比例 魔芋胶添加量(%) 0 0.1 0.5 1 0.1 4% MP 44.15±0.95de 46.90±1.58de 41.72±3.33e 60.36±7.07b 3% MP+1% SPI 57.09±2.02b 57.33±4.31b 56.79±4.96bc 68.95±6.80a 2% MP+2% SPI 46.78±1.76de 49.80±1.81cd 55.56±5.88bc 61.28±2.81b 0.3 4% MP 36.80±0.82f 40.68±2.59ef 51.45±8.62bc 67.35±5.03a 3%MP+1%SPI 50.63±0.89bcd 52.16±1.61bc 47.02±2.14cd 53.68±6.41b 2% MP+2% SPI 44.91±1.23de 48.79±2.18bcd 50.86±0.67bcd 65.84±2.44a 0.6 4% MP 87.35±2.89a 82.26±6.65ab 72.20±3.70cd 75.78±9.29bc 3% MP+1% SPI 60.77±3.36efg 59.02±3.32fg 71.43±6.48cd 65.76±6.03def 2% MP+2% SPI 43.55±2.36i 46.34±1.84hi 52.96±3.59gh 67.80±3.13cde 注:同一盐浓度不同字母(a~i)表示结果具有显著性差异(P<0.05)。 在0.6 mol/L盐浓度下,纵向分析数据,随着SPI的加入,复合蛋白体系的持水性显著下降(P<0.05),而魔芋胶可以减弱SPI对复合凝胶持水性的破坏作用。研究不同添加量魔芋胶对MP和MP-SPI体系凝胶强度的影响发现,添加0.5%魔芋胶后,3% MP-1% SPI体系的持水性达到最大值为71.43%;而当魔芋胶添加量增至1%时,持水性反而减小,说明过量魔芋胶对复合蛋白凝胶持水性具有破坏作用。在低盐和高盐条件下,魔芋胶均能剂量依赖性地提高2% MP-2% SPI复合蛋白凝胶体系的持水性。
2.4 魔芋胶对SPI-MP复合蛋白体系微观结构的影响
不同盐浓度下0.5%魔芋胶对复合蛋白凝胶微观结构的影响如图2所示。在0.6 mol/L 盐浓度下,MP充分溶解,添加0.5%魔芋胶后,两者相互作用形成较为致密的网状结构。添加1% SPI样品的微观结构如图2b所示,发现由于SPI的加入,形成了一些棒状纤维结构,SPI被包埋在MP凝胶体系中,与图2a相比,形成了更为紧密和均一的结构。
2.5 利用应力松弛方法分析魔芋胶对复合蛋白凝胶的影响
Nussinovitch等[32]研究发现,琼脂凝胶的平衡模量与凝胶强度之间具有很好的正相关关系,即凝胶的强度越大,获得的平衡模量也就越大。Tang等[33]也发现低酰基结冷胶断裂应力和平衡模量之间也有较好相关性,通常凝胶的强度用凝胶的断裂应力表示,平衡模量与凝胶的网络交联程度有很大的相关性。在食品中往往采用质构仪对食品体系进行应力松弛分析来表征样品化学成分的变化。目前,应力松弛方法大多是定性分析,并且由于本研究中样品成分比较复杂,所以只能定性分析。如表3所示,在0.3和0.6 mol/L盐浓度下,SPI取代1% MP后,每组样品的平衡模量值G(t)都有所下降,可能原因是SPI在MP中多以颗粒填充形式存在,虽然在低盐浓度下,可以提高样品的凝胶强度,但是SPI的加入使得体系的有效网格数减少,所以获得平衡模量都减小。添加魔芋胶降低了体系的G(t),原因可能与其在MP凝胶中的存在形式有关,蛋白凝胶内的物理交联点移动较多,最终获得平衡模量偏小。这说明高盐浓度下,纯MP自身能形成较好的网络结构,加入魔芋胶会破坏这种网络结构。这很好地解释了高盐浓度下添加1%魔芋胶导致肌原纤维蛋白凝胶强度减弱的现象。而向复合蛋白凝胶体系加入魔芋胶后,其平衡模量却降低,这可能是因为复合蛋白凝胶性质是多种作用力综合作用的结果,由蛋白之间、蛋白与多糖之间相互作用以及它们自身的性质共同决定。
表 3 各组样品的平衡模量值G(t)Table 3. Balance modulus value G(t) of the samples盐浓度
(mol/L)蛋白比例 对照组(Pa) 魔芋胶(Pa) 0.3 MP:SPI=1:0 296 122 MP:SPI=3:1 150 111 0.6 MP:SPI=1:0 544 246 MP:SPI=3:1 189 162 3. 结论
本研究探讨了魔芋胶对SPI-MP复合体系的凝胶特性和持水性的影响,明确了魔芋胶-SPI-MP三相体系中复合凝胶强度的影响因素。结果表明:在低盐浓度(0.3 mol/L NaCl)下,添加1%SPI可促进MP凝胶,并且其凝胶持水力也进一步提高,过量SPI却对凝胶形成具有破坏作用。扫描电镜结果显示,低添加量下SPI可填充进MP凝胶网络中,并且伴有一些棒状纤维结构产生,增强了凝胶强度。魔芋胶的加入可形成更为致密的网络结构,从而改善SPI-MP复合体系的凝胶强度和持水性。高盐浓度下,添加SPI后复合蛋白凝胶强度和持水性均被破坏,魔芋胶的加入可减弱这种破坏作用。综上所述,添加较低含量SPI代替肉蛋白可增强乳化肉制品凝胶强度,并且魔芋胶也可以进一步改善复合蛋白体系的凝胶强度和持水力。上述结果进一步阐明了不同盐浓度下SPI对MP的干扰效应,为低盐肉制品开发以及大豆分离蛋白在肉制品中的应用提供了理论依据。
-
表 1 魔芋胶添加量对不同盐浓度下复合蛋白体系凝胶强度的影响(g)
Table 1 Effect of konjac adding levels on the gel strength of MP-SPI composite under different salt levels (g)
盐浓度
(mol/L)蛋白比例 魔芋胶添加量(%) 0 0.1 0.5 1 0.1 4% MP 23.2±3.1f 12.9±1.3g 31.8±2.0e 74.6±5.7c 3% MP+1% SPI 25.4±5.2ef 14.8±2.5g 124.5±10.1a 147.5±5.3a 2% MP+2% SPI 26.9±3.2ef 51.1±2.5d 81.8±4.2c 90.3±4.8b 0.3 4% MP 43.7±4.2e 102.7±5.5c 129.5±7.4b 143.8±8.7a 3% MP+1% SPI 97.7±5.2c 124.5±3.5b 123.8±8.0b 131.2±8.0b 2% MP+2% SPI 66.2±2.2d 23.6±4.0f 65.2±1.9d 93.0±8.9c 0.6 4% MP 177.7±12.3b 188.0±9.8b 225.3±11.3a 175.5±11.1b 3% MP+1% SPI 89.3±1.8ef 102.5±5.0d 140.0±6.3c 99.1±2.8de 2% MP+2% SPI 22.9±3.6h 48.1±4.4g 77.1±2.5f 95.3±6.7de 注:同一盐浓度不同字母(a~g)表示结果具有显著性差异(P<0.05)。 表 2 魔芋胶添加量对不同盐浓度下复合蛋白体系持水性的影响(%)
Table 2 Effect of konjac adding levels on the WHC of MP-SPI composite with various salt levels (%)
盐浓度
(mol/L)蛋白比例 魔芋胶添加量(%) 0 0.1 0.5 1 0.1 4% MP 44.15±0.95de 46.90±1.58de 41.72±3.33e 60.36±7.07b 3% MP+1% SPI 57.09±2.02b 57.33±4.31b 56.79±4.96bc 68.95±6.80a 2% MP+2% SPI 46.78±1.76de 49.80±1.81cd 55.56±5.88bc 61.28±2.81b 0.3 4% MP 36.80±0.82f 40.68±2.59ef 51.45±8.62bc 67.35±5.03a 3%MP+1%SPI 50.63±0.89bcd 52.16±1.61bc 47.02±2.14cd 53.68±6.41b 2% MP+2% SPI 44.91±1.23de 48.79±2.18bcd 50.86±0.67bcd 65.84±2.44a 0.6 4% MP 87.35±2.89a 82.26±6.65ab 72.20±3.70cd 75.78±9.29bc 3% MP+1% SPI 60.77±3.36efg 59.02±3.32fg 71.43±6.48cd 65.76±6.03def 2% MP+2% SPI 43.55±2.36i 46.34±1.84hi 52.96±3.59gh 67.80±3.13cde 注:同一盐浓度不同字母(a~i)表示结果具有显著性差异(P<0.05)。 表 3 各组样品的平衡模量值G(t)
Table 3 Balance modulus value G(t) of the samples
盐浓度
(mol/L)蛋白比例 对照组(Pa) 魔芋胶(Pa) 0.3 MP:SPI=1:0 296 122 MP:SPI=3:1 150 111 0.6 MP:SPI=1:0 544 246 MP:SPI=3:1 189 162 -
[1] NOH S W, SONG D H, HAM Y K, et al. Interaction of porcine myofibrillar proteins and various gelatins:Impacts on gel properties[J]. Food Science of Animal Resources,2019,39(2):229−239. doi: 10.5851/kosfa.2019.e18
[2] WANG X, WANG L, YANG K, et al. Radio frequency heating improves water retention of pork myofibrillar protein gel:An analysis from water distribution and structure[J]. Food Chemistry,2021,350:129265. doi: 10.1016/j.foodchem.2021.129265
[3] XIE Y S, YU X L, WANG Z M, et al. The synergistic effects of myofibrillar protein enrichment and homogenization on the quality of cod protein gel[J]. Food Hydrocolloids,2022,137:107468.
[4] WU Q, ZANG M, ZHAO B, et al. Effect of citrus fiber on the phosphate-mediated gel properties of myofibrillar protein and partial replacement of phosphate[J]. LWT,2023,173:114274. doi: 10.1016/j.lwt.2022.114274
[5] JIANG S, ZHAO S C, JIA X W, et al. Thermal gelling properties and structural properties of myofibrillar protein including thermo-reversible and thermo-irreversible curdlan gels[J]. Food Chemistry,2020,311:126018. doi: 10.1016/j.foodchem.2019.126018
[6] 王立健, 罗程, 潘雪峰, 等. 纤维素替代淀粉对肌原纤维蛋白凝胶特性的影响[J]. 中国农业科学,2022,55(11):2227−2238. [WANG L J, LUO C, PAN X F, et al. Effects of cellulose replacing starch on the gel properties of myofibrillar protein[J]. Scientia Agricultura Sinica,2022,55(11):2227−2238.] doi: 10.3864/j.issn.0578-1752.2022.11.012 WANG L J, LUO C, PAN X F, et al. Effects of cellulose replacing starch on the gel properties of myofibrillar protein[J]. Scientia Agricultura Sinica, 2022, 55(11): 2227−2238. doi: 10.3864/j.issn.0578-1752.2022.11.012
[7] 陈立德. 肌原纤维蛋白凝胶作用力影响因素的研究[D]. 重庆:西南大学, 2010. [CHEN L D. Study effect on chemical interactions of myofibrillar protein gels[D]. Chongqing:Southwest University, 2010.] CHEN L D. Study effect on chemical interactions of myofibrillar protein gels[D]. Chongqing: Southwest University, 2010.
[8] 王静宇, 胡新, 刘晓艳, 等. 肌原纤维蛋白热诱导凝胶特性及化学作用力研究进展[J]. 食品与发酵工业,2020,46(8):300−306. [WANG J Y, HU X, LIU X Y, et al. Advances in heat-induced gel properties and chemical forces of myofibrillar protein gel[J]. Food and Fermentation Industries,2020,46(8):300−306.] WANG J Y, HU X, LIU X Y, et al. Advances in heat-induced gel properties and chemical forces of myofibrillar protein gel[J]. Food and Fermentation Industries, 2020, 46(8): 300−306.
[9] CHEN Y T, XU A Q, YANG R, et al. Myofibrillar protein structure and gel properties of Trichiurus haumela surimi subjected to high pressure or high pressure synergistic heat[J]. Food and Bioprocess Technology,2020,13(4):589−598. doi: 10.1007/s11947-020-02416-x
[10] WANG S Q, LIN R, CHENG S S, et al. Assessment of water mobility in surf clam and soy protein system during gelation using LF-NMR technique[J]. Foods,2020,9(2):213. doi: 10.3390/foods9020213
[11] 杨子怡, 吴晗, 饶伟丽, 等. 复合磷酸盐对3类肉制品品质的影响研究[J]. 现代食品,2020(14):15−17. [YANG Z Y, WU H, RAO W L, et al. Effect of compound phosphate on the quality of three kinds of meat products[J]. Modern Food Science & Technology,2020(14):15−17.] YANG Z Y, WU H, RAO W L, et al. Effect of compound phosphate on the quality of three kinds of meat products[J]. Modern Food Science & Technology, 2020(14): 15−17.
[12] BI C H, WANG P L, SUN D Y, et al. Effect of high-pressure homogenization on gelling and rheological properties of soybean protein isolate emulsion gel[J]. Journal of Food Engineering,2020,277:109923. doi: 10.1016/j.jfoodeng.2020.109923
[13] SUN X D, HOLLEY R A. Factors influencing gel formation by myofibrillar proteins in muscle foods[J]. Comprehensive Reviews in Food Science & Food Safety,2011,10(1):33−51.
[14] ARGEL N S, RANALLI A N, CALIFANO A N, et al. Influence of partial pork meat replacement by pulse flour on physicochemical and sensory characteristics of low-fat burgers[J]. Journal of the Science of Food and Agriculture,2020,100(10):3932−3941. doi: 10.1002/jsfa.10436
[15] ZHANG H, LI X, SUN S, et al. Effects of carboxymethyl chitosan on the oxidation stability and gel properties of myofibrillar protein from frozen pork patties[J]. International Journal of Biological Macromolecules,2023,234:123710. doi: 10.1016/j.ijbiomac.2023.123710
[16] GAO Y, WANG S, LIU H, et al. Design and characterization of low salt myofibrillar protein-sugar beet pectin double-crosslinked gels pretreated by ultrasound and Konjac glucomannan:Conformational and gelling properties[J]. Food Hydrocolloids,2023,141:108717. doi: 10.1016/j.foodhyd.2023.108717
[17] JIANG J, XIONG Y L. Extreme pH treatments enhance the structure-reinforcement role of soy protein isolate and its emulsions in pork myofibrillar protein gels in the presence of microbial transglutaminase[J]. Meat Science,2013,93(3):469−476. doi: 10.1016/j.meatsci.2012.11.002
[18] HERRERO A M, CARMON P, COFRADES S, et al. Raman spectroscopic determination of structural changes in meat batters upon soy protein addition and heat treatment[J]. Food Research International,2008,41(7):765−772. doi: 10.1016/j.foodres.2008.06.001
[19] CHIN K B, GO M Y, XIONG Y L. Konjac flour improved textural and water retention properties of transglutaminase-mediated, heat-induced porcine myofibrillar protein gel:Effect of salt level and transglutaminase incubation[J]. Meat Science,2009,81(3):565−572. doi: 10.1016/j.meatsci.2008.10.012
[20] FENG Y Y, LIANG X, ZHANG J M, et al. Effects of transglutaminase coupled with κ-carrageenan on the rheological behaviors, gel properties and microstructures of meat batters[J]. Food Hydrocolloids,2023,146:109265.
[21] CHATTERJEE D G, BRAMBILIA S, BOWKER B C, et al. Effect of tapioca flour on physicochemical properties and sensory descriptive profiles of chicken breast meat patties[J]. Journal of Applied Poultry Research,2019,28(3):598−605. doi: 10.3382/japr/pfy076
[22] 杨振, 孔保华, 夏秀芳, 等. 魔芋粉对鲤鱼肌原纤维蛋白凝胶特性的影响[J]. 食品科学,2012,33(11):116−120. [YANG Z, KONG B H, XIA X F, et al. Influence of konjac flour on gel properties of myofibrillar proteins from common carp[J]. Food Science,2012,33(11):116−120.] YANG Z, KONG B H, XIA X F, et al. Influence of konjac flour on gel properties of myofibrillar proteins from common carp[J]. Food Science, 2012, 33(11): 116−120.
[23] HASANPOUR F, HOSEINI E, MOTALEBI A A, et al. Effects of soy protein concentrate and xanthan gum on physical properties of silver carp (Hypophthalmichthys molitrix) surimi[J]. Iranian Journal of Fisheries Sciences,2012,11(3):518−530.
[24] LIN K W, MEI M Y. Influences of gums, soy protein isolate, and heating temperatures on reduced-fat meat batters in a model system[J]. Food Chemistry and Toxicology,2000,65(1):45−52.
[25] PARK D, XIONG Y L. Oxidative modification of amino acids in porcine myofibrillar protein isolates exposed to three oxidizing systems[J]. Food Chemistry,2007,103(2):607−616.
[26] LIU G, XIONG Y L. Thermal transitions and dynamic gelling properties of oxidatively modified myosin, β-lactoglobulin, soy 7S globulin and their mixtures[J]. Journal of the Science of Food and Agriculture,2000,80(12):1728−1734. doi: 10.1002/1097-0010(20000915)80:12<1728::AID-JSFA711>3.0.CO;2-A
[27] XIONG Y L, BLANCHARD S P, MEANS W J. Properties of boiler myofibril gels containing emulsified lipids[J]. Poultry Science,1992,71(9):1548−1555. doi: 10.3382/ps.0711548
[28] 杜洪振, 陈倩, 杨振, 等. 预热处理大豆蛋白对鲤鱼肌原纤维蛋白凝胶和流变学特性的影响[J]. 食品科学,2019,40(12):55−61. [DU H Z, CHEN Q, YANG Z, et al. Effect of preheated soy proteins on gelling and rheological properties of common carp myofibrillar protein[J]. Food Science,2019,40(12):55−61.] doi: 10.7506/spkx1002-6630-20180510-161 DU H Z, CHEN Q, YANG Z, et al. Effect of preheated soy proteins on gelling and rheological properties of common carp myofibrillar protein[J]. Food Science, 2019, 40(12): 55−61. doi: 10.7506/spkx1002-6630-20180510-161
[29] 姜帅, 曹传爱, 康辉, 等. 燕麦β-葡聚糖对肌原纤维蛋白乳化和凝胶特性的影响[J]. 食品科学技术学报,2019,37(5):32−41. [JIANG S, CAO C A, KANG H, et al. Effects of oat β-glucan on emulsifying and gel properties of myofibrillar protein[J]. Journal of Food Science and Technology,2019,37(5):32−41.] doi: 10.3969/j.issn.2095-6002.2019.05.005 JIANG S, CAO C A, KANG H, et al. Effects of oat β-glucan on emulsifying and gel properties of myofibrillar protein[J]. Journal of Food Science and Technology, 2019, 37(5): 32−41. doi: 10.3969/j.issn.2095-6002.2019.05.005
[30] 潘玉雪, 徐欣东, 张润峰, 等. 凝胶多糖自组装作用及其应用研究进展[J]. 食品科学,2022,43(15):265−274. [PAN Y X, XU X D, ZHANG R F, et al. Progress in research on self-assembly of curdlan and its application[J]. Food Science,2022,43(15):265−274.] doi: 10.7506/spkx1002-6630-20210530-354 PAN Y X, XU X D, ZHANG R F, et al. Progress in research on self-assembly of curdlan and its application[J]. Food Science, 2022, 43(15): 265−274. doi: 10.7506/spkx1002-6630-20210530-354
[31] CHIN K B, KEETON J T, LONGNECKER M T, et al. Utilization of soy protein isolate and konjac blends in a low-fat bologna (model system)[J]. Meat Science,1999,53(1):45−57. doi: 10.1016/S0309-1740(99)00035-2
[32] NUSSINOVITCH A, AK M M, NORMAND M D, et al. Characterization of gellan gels by uniaxial compression, stress relaxation and creep[J]. Journal of Texture Studies,1990,21(1):37−50. doi: 10.1111/j.1745-4603.1990.tb00463.x
[33] TANG J, TUNG M A, ZENG Y. Characterization of gellan gels using stress relaxation[J]. Journal of Food Engineering,1998,38(3):279−295.
-
期刊类型引用(0)
其他类型引用(3)





 下载:
下载:

 下载:
下载:



