Optimization of Ultrasonic-assisted Extraction of Polyphenols from Taraxacum kok-saghyz Rodin Roots and Its Antioxidant, Hypoglycemic Activity in Vitro
-
摘要: 以青胶蒲公英根为原料,选取液料比、超声功率、提取温度和提取时间作为试验因子,在单因素实验基础上,采用响应面法对青胶蒲公英根多酚超声辅助提取工艺进行优化,并对提取的青胶蒲公英根多酚的体外抗氧化及降糖活性进行了测定。结果表明:青胶蒲公英根多酚提取的最优条件为液料比33:1 mL/g,超声功率270 W,提取温度61 ℃,提取时间31 min,在此条件下青胶蒲公英根多酚得率为1.46%±0.03%。体外活性研究表明,青胶蒲公英根多酚提取物清除DPPH自由基和ABTS+自由基的半抑制浓度(IC50)分别为54.06和39.27 µg/mL,对α-淀粉酶和α-葡萄糖苷酶的IC50值分别为133.26和50.22 µg/mL,这表明青胶蒲公英根多酚具有较强的体外抗氧化和降糖能力。本研究可为青胶蒲公英的综合开发利用提供理论依据。Abstract: Using Taraxacum kok-saghyz Rodin (TKS) roots as the raw material, the liquid-solid ratio, ultrasonic power, extraction temperature, and extraction time were selected as experimental factors. On the basis of single factor experiments, the response surface methodology was used to optimize the ultrasonic-assisted extraction process of polyphenols from the TKS roots. The in vitro antioxidant and hypoglycemic activity of the polyphenols extracted from TKS roots were measured. The results showed that the optimal extraction conditions were liquid-solid ratio of 33:1 mL/g, ultrasonic power of 270 W, extraction temperature of 61 ℃, and extraction time of 31 min. Under these conditions, the yield of polyphenols from TKS roots was 1.46%±0.03%. The in vitro activity test showed that the half inhibitory concentrations (IC50) of polyphenol extracts on DPPH and ABTS+ radicals were 54.06 and 39.27 µg/mL, respectively, the IC50 values for α-amylase and α-glucosidase were 133.26 and 50.22 µg/mL, respectively. This indicated that the polyphenols from TKS roots had strong antioxidant and hypoglycemic activities in vitro. This study can provide theoretical basis for the comprehensive development and utilization of TKS.
-
青胶蒲公英(Taraxacum kok-saghyz Rodin,TKS),又被称为橡胶草,为菊科蒲公英属植物,近年来,因其根部含有丰富而优质的天然橡胶而备受关注[1]。青胶蒲公英根部除了富含橡胶,还含有菊糖、多酚等大量活性成分。Ramirez-Cadavid等[2]对橡胶草根的成分进行了分析,结果表明:干根中灰分含量为11.8%,主要无机元素为K、Ca、P和Cl,脂肪酸占5.2%,其中亚油酸、棕榈酸和亚麻酸含量最丰富,菊糖占17%,酚类化合物占2%。本课题组的前期研究结果也表明,青胶蒲公英富含不饱和脂肪酸,特别是亚麻酸和亚油酸,并含有大量具有药用价值的挥发性成分[3]。陈江艳等[4]采用超声波法提取橡胶草根菊糖,菊糖提取率为20.14%±0.19%。Putter等[5]从青胶蒲公英根的丙酮提取物中鉴定出13种三萜类化合物。Kong等[6]从青胶蒲公英叶和根的甲醇提取物中鉴定了164种化合物,包括萜类、黄酮类、香豆素类和有机酸类等。因此,对于青胶蒲公英资源的开发不能仅局限于其天然橡胶,要提高经济价值,降低其橡胶生产成本,还需对其非胶成分进行全面开发利用,将它们提取分离并转化为对不同商业部门有价值的产品或原材料。
蒲公英含有丰富的酚类化合物,主要有木犀草素、槲皮素、橙皮素、芫花素、咖啡酸、绿原酸、菊苣酸、阿魏酸、对羟基苯甲酸、对香豆酸等[7−8],地上部分的类黄酮含量高于根系[9],叶提取物中总酚含量和抗氧化活性最高[10]。菊苣酸、绿原酸和咖啡酸等羟基肉桂酸衍生物是蒲公英叶、茎、花瓣中的主要酚酸[11],它们具有抗氧化、抗炎、抗诱变、抗癌等活性[10,12−13]。蒲公英叶和花提取物中还富含木犀草素-7-O-葡萄糖苷、木犀草素-7-二糖苷和木犀草素,这些类黄酮和酚酸等其他类抗氧化剂一起可用于保护人体免受自由基侵害[10,14]。研究表明,从叶片和花瓣中提取的蒲公英多酚能够降低氧化应激,提高免疫力,促进肝脏排毒[15]。蒲公英多酚的提取主要采用纯水或一定体积分数的乙醇作为溶剂[16−18]。这些研究基本都是以蒙古蒲公英(Taraxacum mongolicum)、药用蒲公英(Taraxacum officinale)为研究对象,目前对于青胶蒲公英的研究主要集中在根部橡胶上,有关其多酚的研究还鲜有报道。Molinu等[19]对生长在撒丁岛地中海条件下的青胶蒲公英叶片中的酚类化合物进行了研究,结果表明叶片总酚含量为106.4 g GAE/kg、单宁酚为58.5 g GAE/kg和总黄酮含量为22.9 g CE/kg,但未对根中的多酚进行分析,也未探讨提取工艺。以青胶蒲公英根为研究对象,在提取橡胶前,先采用乙醇提取其中的多酚,可充分利用资源,提高青胶蒲公英经济价值。
从植物中提取多酚的方法主要有传统溶剂提取、超声波提取、微波提取、酶辅助提取等[20]。超声波提取是利用超声波产生的空化效应、机械效应和热效应破坏植物细胞壁,从而加速溶剂的渗入和有效成分的溶出[21],具有快速高效,成本低,不受目标物质极性和分子量大小等的限制,不破坏有效成分等优点,在某些情况下比微波提取速度更快也更安全,可广泛用于多酚、皂苷、生物碱、黄酮及多糖等成分的提取[22]。本文采用超声辅助提取青胶蒲公英根多酚,考察了液料比、超声功率、提取温度和时间对多酚得率的影响,采用响应面法对工艺参数进行了优化。并通过测定多酚提取物对DPPH和ABTS+自由基的清除能力、对α-淀粉酶和α-葡萄糖苷酶的抑制能力评价了其体外抗氧化及降糖活性,以为青胶蒲公英多酚在食品、化妆品、医药等领域的进一步深入研究与利用提供理论依据。
1. 材料与方法
1.1 材料与仪器
青胶蒲公英根 新疆农业科学院作物品种资源研究所提供,青胶蒲公英根洗净后在45 ℃干燥箱中烘干,然后粉碎过40目筛,收集筛选后的样品(99%),保存在密封袋中,4 ℃冷藏备用;没食子酸标准品(HPLC≥98%) 上海源叶生物科技有限公司;α-葡萄糖苷酶(G5003-100U)、α-淀粉酶(A3176-500kU)、2,2′-联氮双(3-乙基苯并噻唑啉-6-磺酸)二铵盐(ABTS)、1,1-二苯基-2-苦基肼(DPPH) Sigma-Aldrich公司;对硝基苯基-α-D-吡喃葡萄糖苷(pNPG)、阿卡波糖、维生素C、福林酚、过硫酸钾、无水乙醇、无水碳酸钠、磷酸氢二钠、磷酸二氢钠、3,5-二硝基水杨酸(DNS)、酒石酸钾钠 均为国产分析纯。
HR-150AZ电子分析天平 日本A&D公司;KQ-300DB超声波清洗机 昆山市超声仪器有限公司;TGL-20B高速台式离心机 上海安亭科学仪器厂;EMS-20数显恒温磁力搅拌水浴锅 金坛市科顺仪器厂;RE-3000旋转蒸发仪 上海亚荣生化仪器厂;SHB-III循环水式真空泵 郑州长城科工贸有限公司;Synergy H1多功能酶标仪 美国伯腾仪器有限公司。
1.2 实验方法
1.2.1 青胶蒲公英根多酚的提取
称取1.0 g的青胶蒲公英根粉末于提取容器中,加入一定量的80%乙醇溶液,在一定的超声功率和提取温度下提取一定时间后,离心(8000 r/min,10 min),沉淀再重复提取2次,合并上清液,备用。
1.2.2 单因素实验
采用控制变量法,固定因素水平为液料比30:1 mL/g、超声功率270 W、提取温度50 ℃、提取时间30 min,分别考察了不同液料比(10:1、20:1、30:1、40:1、50:1 mL/g)、提取时间(10、20、30、40、50 min)、超声功率(180、210、240、270、300 W)、提取温度(30、40、50、60、70 ℃)对超声辅助提取青胶蒲公英根多酚得率的影响。
1.2.3 响应面试验设计
根据单因素实验结果,以提取时间(X1)、液料比(X2)、提取温度(X3)、超声功率(X4)为自变量,青胶蒲公英根多酚得率(Y)为目标值,设计了四因素三水平的响应面优化试验,试验因素水平见表1。
表 1 响应面试验设计因素水平Table 1. Factors and levels of response surface design因素 水平 −1 0 1 提取时间(min) X1 20 30 40 液料比(mL/g) X2 20:1 30:1 40:1 提取温度(℃) X3 50 60 70 超声功率(W) X4 240 270 300 1.2.4 多酚得率的测定
1.2.4.1 标曲的制作
精确称取没食子酸25 mg,用水溶解并定容到250 mL,配制成0.1 mg/mL的没食子酸对照品溶液。取25 mL比色管,分别加入对照品溶液0、0.1、0.2、0.4、0.6、0.8、1.0 mL,加蒸馏水补足至10 mL,加入0.3 mL福林酚试剂,摇匀后室温下静置5 min,再加入1 mL 15%碳酸钠溶液,摇匀,室温避光反应2 h后在746 nm测定吸光值,以没食子酸浓度(μg/mL)为横坐标,吸光度为纵坐标,绘制标准曲线,得线性回归方程y=0.0104x+0.015,R2=0.9978。
1.2.4.2 多酚的测定及得率的计算
按1.2.1中青胶蒲公英根多酚提取方法,提取液定容至100 mL后得待测样液。取待测液0.2 mL按1.2.4.1方法操作测定吸光度,并按下式计算多酚得率:
Y(%)=c×D×V×10−6m×100 式中:Y表示多酚得率,%;c为待测液质量浓度,μg/mL;D为稀释倍数;V为样液体积,mL;m为原料质量,g。
1.2.5 青胶蒲公英根多酚提取物体外抗氧化和降糖活性测定
将青胶蒲公英根多酚粗提液过AB-8大孔树脂纯化,70%乙醇洗脱,洗脱液旋蒸除乙醇后冻干,得到多酚提取物,测定其对DPPH和ABTS+自由基清除能力评价体外抗氧化活性,测定α-淀粉酶和α-葡萄糖苷酶抑制能力评价降糖活性。
1.2.5.1 DPPH自由基清除能力的测定
参考Lu等[23]报道的方法对青胶蒲公英根多酚提取物的清除DPPH自由基活性进行分析。在96孔板中加入100 μL DPPH溶液(0.2 mmol/L,乙醇配制)和100 μL不同浓度的样液,混匀后在室温下黑暗处反应30 min,在517 nm处测定吸光度。自以维生素C为阳性对照。
自由基清除率(%)=(1−A1−A2A0)×100 式中:A0为只有DPPH溶液的吸光度,A1为DPPH和样品混合液的吸光度,A2为只有样品溶液的吸光度。
1.2.5.2 ABTS+自由基清除能力的测定
ABTS+自由基清除能力试验参考Lu等[23]报道的方法稍作修改。ABTS溶液是通过将ABTS原液(7 mmol/L)与过硫酸钾(2.45 mmol/L)在室温下于暗处反应12~16 h而制得。用无水乙醇稀释ABTS溶液,使其在734 nm处的吸光度为0.7,得到ABTS使用液。将50 μL不同浓度的样品溶液与150 μL ABTS使用液混合,于室温下暗处反应20 min后,在734 nm波长处测定吸光度。以维生素C为阳性对照。
ABTS+自由基清除率(%)=(1−A1−A2A0)×100 式中:A0为只有ABTS溶液的吸光度,A1为ABTS和样品混合液的吸光度,A2为只有样品溶液的吸光度。
1.2.5.3 α-淀粉酶抑制能力
将多酚提取物先溶解于二甲基亚砜(DMSO)中,临用前以磷酸盐缓冲液(PBS,20 mmol/L,pH6.9)稀释到所需浓度,DMSO的最终体积分数均为0.1%。在对照中也加入等量的DMSO。α-淀粉酶活性抑制试验参考de-Bellis等[24]的方法并稍作修改。取100 μL样液(10~1000 μg/mL)和100 μL α-淀粉酶溶液(0.5 mg/mL,0.1 mol/L pH6.9的PBS配制),在37 ℃下孵育10 min。然后加入100 μL淀粉溶液(1%,0.1 mol/L pH6.9的PBS配制)混合,在37 ℃下孵育10 min,最后加入200 μL 3,5-二硝基水杨酸试剂,沸水浴5 min。当反应液冷却到室温后,从各管中取出100 μL到96孔板上,每孔中加入100 µL蒸馏水,用酶标仪在540 nm波长处测定吸光度。以阿卡波糖为阳性对照。
α-淀粉酶抑制率(%)=(1−A1−A2A3−A4)×100 式中:A1为样品吸光度,A2为背景吸光度(PBS替代酶液),A3为阴性对照吸光度(PBS替代样液),A4为阴性对照背景吸光度(PBS替代样液及酶液)。
1.2.5.4 α-葡萄糖苷酶抑制能力
通过测定底物4-硝基苯基-α-D-吡喃葡萄糖苷(pNPG)中对硝基苯酚(pNP)的释放量来测定α-葡萄糖苷酶的活性。参考de-Bellis等[24]的方法,50 μL样品溶液(10~1000 μg/mL)和100 μL α-葡萄糖苷酶(0.2 U/mL,0.1 mol/L pH6.9的PBS配制)混合,在37 ℃下孵育10 min。然后加入50 μL pNPG溶液(5 mmol/L,0.1 mol/L pH 6.9的PBS配制),在37 ℃下再孵育30 min。最后加入100 μL的碳酸钠(1 mol/L)终止反应,用酶标仪在波长为405 nm处测定吸光度。以阿卡波糖为阳性对照。
α-葡萄糖苷酶抑制率(%)=(1−A1−A2A3−A4)×100 式中:A1为样品吸光度,A2为背景吸光度(PBS替代酶液),A3为阴性对照吸光度(PBS替代样液),A4为阴性对照背景吸光度(PBS替代样液及酶液)。
1.3 数据处理
所有实验均重复3次,实验结果以平均值±标准差(SD)表示,使用SPSS 23和OriginPro 2021软件对实验结果进行统计分析和可视化处理;采用Expert-Design 10软件进行响应面试验设计与分析。
2. 结果与分析
2.1 单因素实验
2.1.1 液料比对多酚得率的影响
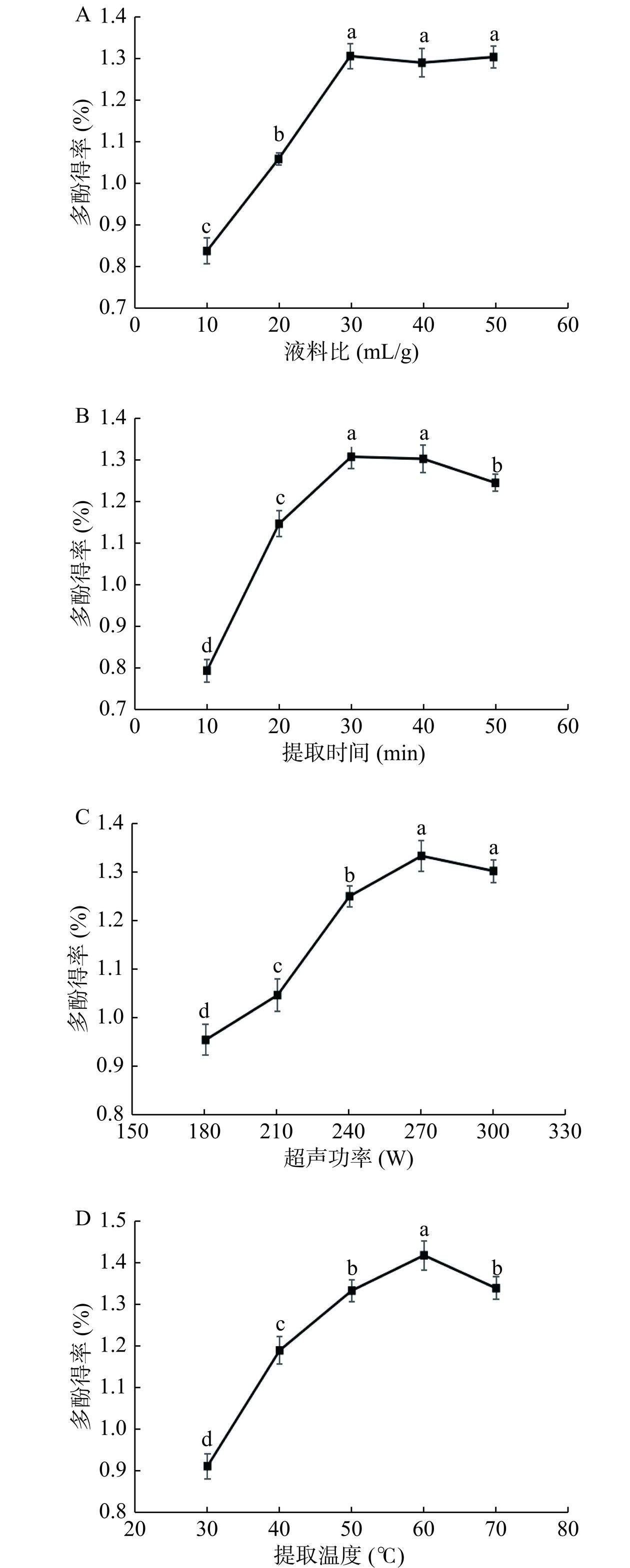
液料比对青胶蒲公英根多酚提取得率的影响如图1A所示。液料比从10:1 mL/g增加到30:1 mL/g,多酚得率不断增加,当液料比为30:1 mL/g时达到最大值。继续增加液料比,多酚得率不再有明显增加,基本维持不变,这说明此时青胶蒲公英根中多酚的溶出量已经趋于饱和,继续增加液料比不仅增加溶剂消耗,还可能会使更多的色素等醇溶性杂质溶解出来[25],这会增加后续工序的工作量及成本,因此适宜的液料比为30:1 mL/g。
2.1.2 提取时间对多酚得率的影响
提取时间对青胶蒲公英根多酚提取得率的影响如图1B所示,在10~30 min多酚得率随着时间的增加而不断提高,在30 min时达到最大值,继续延长时间,多酚得率呈下降趋势。这可能是由于这些化合物在超声波的机械作用下从植物细胞膜溶解和扩散到溶剂介质中需要一定的时间,延长提取时间可提高多酚的提取量。但随着时间的延长,已溶出的一些多酚类物质易发生氧化而损失,且一些不稳定组分的结构在长时间超声下易被破坏[26],因此提取时间过长得率会显著下降(P<0.05)。提取时间过长还会增加能耗,因此确定适宜提取时间为30 min。
2.1.3 超声功率对多酚得率的影响
超声功率对青胶蒲公英根多酚提取得率的影响如图1C所示。由图可见,在一定范围内随着超声功率的增加,多酚得率不断增加,在超声功率为270 W时达到最大值,继续增加功率,多酚得率无显著变化,且呈下降趋势。超声波在提取体系中所产生的空化效应和机械作用会随着超声功率的增加而增强,从而加速植物细胞的破碎和多酚物质的溶出,因而在一定范围内增加超声功率可提高多酚得率,但功率过高,会使得溶解的杂质更多,影响多酚提取[27],且高功率的超声波会造成一些多酚物质的降解[28],因此确定超声功率为270 W。
2.1.4 提取温度对多酚得率的影响
提取温度对青胶蒲公英根多酚提取得率的影响如图1D所示,提取温度在30~60 ℃的范围内,多酚的得率随温度的升高而增加,在达到60 ℃之后开始下降。温度升高可增加空化气泡数量和蒲公英根表面接触面积,降低溶剂介质黏度和密度,这些都有利于酚类物质从植物体中释放,提高溶解度和扩散系数[29]。且温度升高可能会破坏植物细胞成分,导致细胞膜通透性增加,从而加速酚类化合物的溶出。但是,高温会破坏部分热不稳定性多酚成分,因此,确定青胶蒲公英根多酚提取的最佳温度为60 ℃。
2.2 响应面法优化青胶蒲公英根多酚提取工艺
2.2.1 响应面试验设计与结果
综合单因素实验结果,选择提取时间(X1)、液料比(X2)、提取温度(X3)和超声功率(X4)4个因素作为变量,以多酚得率为响应值(Y),根据Box-Benhnken试验设计原理设计响应面试验优化青胶蒲公英根多酚的提取工艺参数,试验设计及结果见表2。对实验结果进行分析与拟合,建立了多酚得率(Y)与各因素变量之间关系的二次回归方程模型:Y(%)=1.454+0.051X1+0.123X2+0.017X3+8.33E−03X4−0.02X1X2−5.00E−03X1X3−7.50E−03X1X4−2.50E−03X2X3+2.50E−03X3X4−0.113X12−0.14X22−0.119X32−0.127X42。
表 2 响应面试验设计及结果Table 2. Response surface test design and results试验号 X1提取时间 X2液料比 X3提取温度 X4超声功率 Y多酚得率(%) 1 0 1 0 1 1.31 2 0 0 0 0 1.48 3 0 1 0 −1 1.30 4 1 0 0 −1 1.26 5 −1 −1 0 0 1.03 6 0 0 0 0 1.44 7 1 −1 0 0 1.14 8 0 0 −1 −1 1.20 9 0 0 0 0 1.46 10 1 0 1 0 1.30 11 1 0 0 1 1.28 12 0 0 0 0 1.46 13 0 −1 −1 0 1.05 14 −1 1 0 0 1.31 15 0 0 1 1 1.23 16 0 0 1 −1 1.22 17 −1 0 0 1 1.18 18 0 0 −1 1 1.20 19 −1 0 −1 0 1.13 20 0 −1 1 0 1.08 21 1 0 −1 0 1.26 22 0 1 −1 0 1.30 23 −1 0 0 −1 1.13 24 −1 0 1 0 1.19 25 0 −1 0 −1 1.06 26 0 0 0 0 1.43 27 0 −1 0 1 1.07 28 0 1 1 0 1.33 29 1 1 0 0 1.34 通过方差分析(ANOVA)对回归模型进行综合评价,结果见表3。该回归模型的F=110.44,P<0.0001,这说明回归模型达到了极显著的水平,失拟项P=0.6831>0.05,失拟不显著,决定系数R2=0.991,因此,所拟合的回归模型拟合度很好,可用于分析和预测超声波法提取青胶蒲公英根多酚的工艺。回归模型中一次项X1、X2和X3的回归系数都达到了极显著的水平(P<0.01),交互项X1X2的回归系数达到显著水平(P<0.05),二次项X12、X22、X32和X42的回归系数均达到极显著的水平(P<0.01),剩余的其它项对青胶蒲公英根多酚得率的影响均不显著(P>0.05)。4个因素对青胶蒲公英根多酚得率的影响顺序为液料比(X2)>提取时间(X1)>提取温度(X3)>超声功率(X4)。
表 3 回归模型方差分析结果Table 3. Analysis of variance for regression model来源 平方和 自由度 均方 F值 P值 显著性 模型 0.48 14 0.034 110.44 <0.0001 ** X1 0.031 1 0.031 100.3 <0.0001 ** X2 0.18 1 0.18 582.45 <0.0001 ** X3 3.33E−03 1 3.33E−03 10.78 0.0054 ** X4 8.33E−04 1 8.33E−04 2.7 0.1229 X1X2 1.60E−03 1 1.60E−03 5.18 0.0392 * X1X3 1.00E−04 1 1.00E−04 0.32 0.5786 X1X4 2.25E−04 1 2.25E−04 0.73 0.408 X2X3 2.50E−05 1 2.50E−05 0.081 0.7803 X2X4 0 1 0 0 1 X3X4 2.50E−05 1 2.50E−05 0.081 0.7803 X12 0.083 1 0.083 267.11 <0.0001 ** X22 0.13 1 0.13 413.18 <0.0001 ** X32 0.092 1 0.092 297.52 <0.0001 ** X42 0.1 1 0.1 336.18 <0.0001 ** 残差 4.33E−03 14 3.09E−04 失拟项 2.81E−03 10 2.81E−04 0.74 0.6831 纯误差 1.52E−03 4 3.80E−04 总和 0.48 28 注:*表示显著(P<0.05),**表示极显著(P<0.01)。 2.2.2 响应面分析
各交互作用的响应曲面和等高线如图2所示。响应曲面和等高线图直观地反映了两两因素交互作用对青胶蒲公英根多酚提取得率的影响情况,响应曲面的坡度越陡峭、等高线越密集,说明研究因素对青胶蒲公英根多酚提取得率的影响越大,等高线图为椭圆则表明两因素之间存在交互作用,越接近于圆,交互作用越小。从图2可以看出,液料比与提取时间的响应曲面倾斜度较高,等高线呈椭圆形,说明液料比与提取时间的交互作用对青胶蒲公英根多酚提取得率的影响显著。其它两两因素间的等高线图都接近于圆,说明它们之间交互作用弱。
2.2.3 最优提取工艺参数的确定
根据响应面分析建立的二次回归模型预测青胶蒲公英根多酚最佳提取工艺条件为:提取时间31.40 min、液料比33.15:1 mL/g、提取温度61.28 ℃、超声功率269.55 W,预测在此条件下的多酚得率为1.48%。根据实际操作调整参数为:提取时间31 min,液料比33:1 mL/g、提取温度61 ℃、超声功率270 W。按此工艺条件进行了5次平行实验,测得青胶蒲公英根多酚的得率为1.46%±0.03%,与模型给出的预测值基本一致,故模型具有可行性,优化的工艺参数准确可靠。
2.3 青胶蒲公英根多酚提取物的体外抗氧化活性
2.3.1 DPPH自由基清除能力
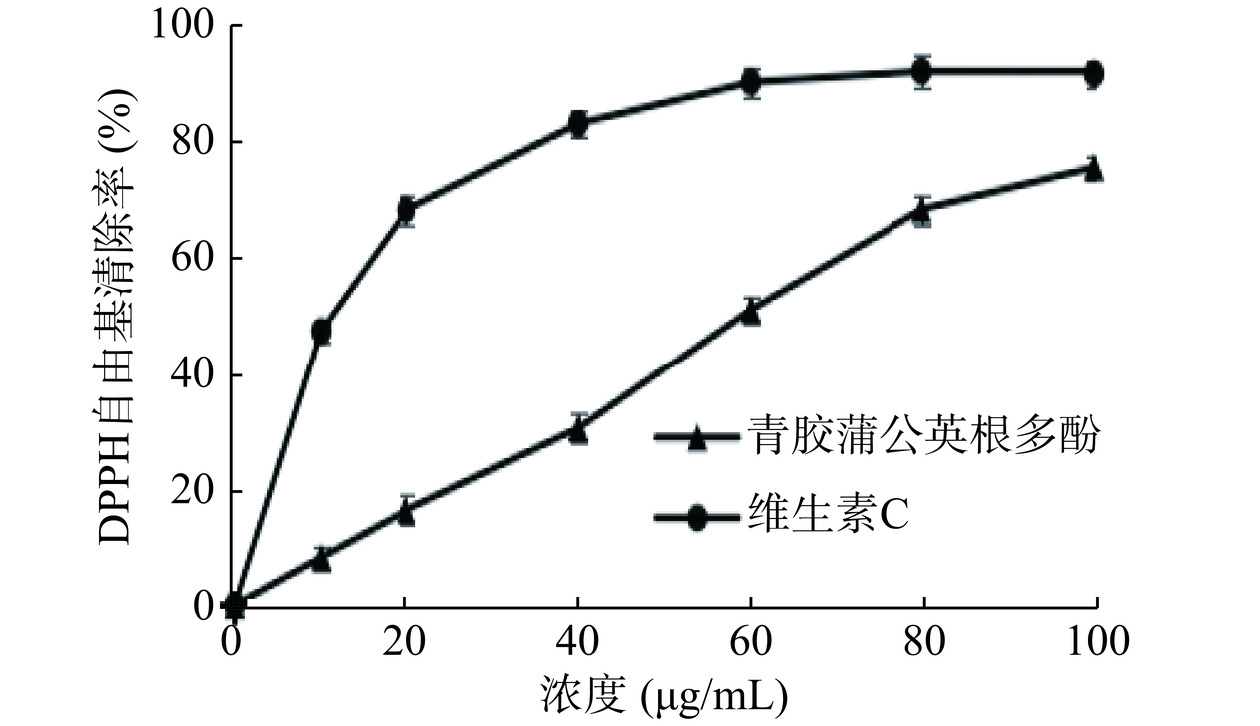
DPPH自由基是一种稳定的自由基,但遇到质子供体时会被清除,已被广泛用于各种天然产物的清除自由基能力的研究中[30]。青胶蒲公英根多酚对DPPH自由基清除能力测试的结果如图3所示,在试验浓度范围内,清除率随着样品浓度的增加而增加,当浓度为100 µg/mL时,清除率达75.79%,青胶蒲公英根多酚对DPPH自由基的半抑制浓度(IC50)为54.06 µg/mL,对照品维生素C的IC50值为10.34 µg/mL。这表明青胶蒲公英根多酚具有一定的清除DPPH自由基能力,但低于维生素C。
2.3.2 ABTS+自由基清除能力
ABTS法是一种使用非常广泛的间接检测天然产物的抗氧化活性的方法,青胶蒲公英根多酚对ABTS+自由基清除率测定结果如图4所示,在试验浓度范围内,清除率随着样品浓度的增加而不断增加,在100 µg/mL时,青胶蒲公英根多酚对ABTS+自由基的清除率达82.90%,略低于对照品维生素C的清除率(95.85%)。青胶蒲公英根多酚和维生素C的IC50值分别为39.27和13.90 µg/mL。由此可知,青胶蒲公英根多酚具有较强的清除ABTS+自由基能力,但低于维生素C。青胶蒲公英根多酚提取物对DPPH和ABTS+自由基的清楚能力均弱于蒲公英多酚[18],这可能是由于根中的多酚含量低于叶,且多酚种类存在差异。
2.4 青胶蒲公英根多酚对α-淀粉酶和α-葡萄糖苷酶活性的抑制作用
糖尿病是威胁人类健康的重要慢性病之一,α-淀粉酶和α-葡萄糖苷酶能促进胃肠道内食物中的碳水化合物(如淀粉)水解成单糖,单糖在体内被吸收后引起血糖水平升高。根据大量研究表明,抑制α-淀粉酶和α-葡萄糖苷酶被认为是糖尿病治疗最有效的方法之一[31−32]。目前,糖尿病的首选方式就是服用抑制剂类药物。植物提取物可以通过抑制肠道α-葡萄糖苷酶复合物来抑制餐后血糖水平[33],其中的多酚类、萜类、多糖类和苯丙素类化合物等都具有良好的抑制效果[34−35]。本文研究了青胶蒲公英根多酚对α-淀粉酶和α-葡萄糖苷酶的抑制活性。如图5和图6所示,青胶蒲公英根多酚对α-淀粉酶和α-葡萄糖苷酶的抑制率均随样品浓度的增加而增大,在试验浓度范围内(10~1000 µg/mL)呈浓度依赖性,在1000 µg/mL时对α-淀粉酶和α-葡萄糖苷酶活性的抑制率分别达75.19%和86.34%,其IC50值分别为133.26和50.22 µg/mL,阳性对照阿卡波糖对α-淀粉酶和α-葡萄糖苷酶的IC50值分别为24.70和30.14 µg/mL。这说明青胶蒲公英根多酚对α-淀粉酶和α-葡萄糖苷酶都表现出较强的抑制作用,具有开发成降糖药物的潜力。
3. 结论
采用超声波辅助提取青胶蒲公英根多酚,研究了液料比、超声功率、提取温度和提取时间对多酚得率的影响,在单因素实验的基础上利用Design Expert软件设计响应面试验对提取工艺进行了优化。根据所建立的二次回归模型预测多酚最佳提取工艺条件为:液料比33:1 mL/g、超声功率270 W、提取时间31 min、提取温度61 ℃。在此条件下进行5次平行实验进行验证,多酚得率为1.46%±0.03%,与模型给出的预测值(1.48%)基本一致,优化的工艺参数准确可靠。体外活性研究表明,青胶蒲公英根多酚提取物清除DPPH自由基和ABTS+自由基的半抑制浓度(IC50)分别为54.06和39.27 µg/mL,对α-淀粉酶和α-葡萄糖苷酶的IC50值分别为133.26和50.22 µg/mL,这表明青胶蒲公英根多酚具有较好的体外抗氧化活性,且具有一定的降糖能力。本研究为青胶蒲公英资源的综合开发利用提供了理论基础,为青胶蒲公英多酚在食品、化妆品、医药等领域的进一步深入研究与利用提供理论依据。
-
表 1 响应面试验设计因素水平
Table 1 Factors and levels of response surface design
因素 水平 −1 0 1 提取时间(min) X1 20 30 40 液料比(mL/g) X2 20:1 30:1 40:1 提取温度(℃) X3 50 60 70 超声功率(W) X4 240 270 300 表 2 响应面试验设计及结果
Table 2 Response surface test design and results
试验号 X1提取时间 X2液料比 X3提取温度 X4超声功率 Y多酚得率(%) 1 0 1 0 1 1.31 2 0 0 0 0 1.48 3 0 1 0 −1 1.30 4 1 0 0 −1 1.26 5 −1 −1 0 0 1.03 6 0 0 0 0 1.44 7 1 −1 0 0 1.14 8 0 0 −1 −1 1.20 9 0 0 0 0 1.46 10 1 0 1 0 1.30 11 1 0 0 1 1.28 12 0 0 0 0 1.46 13 0 −1 −1 0 1.05 14 −1 1 0 0 1.31 15 0 0 1 1 1.23 16 0 0 1 −1 1.22 17 −1 0 0 1 1.18 18 0 0 −1 1 1.20 19 −1 0 −1 0 1.13 20 0 −1 1 0 1.08 21 1 0 −1 0 1.26 22 0 1 −1 0 1.30 23 −1 0 0 −1 1.13 24 −1 0 1 0 1.19 25 0 −1 0 −1 1.06 26 0 0 0 0 1.43 27 0 −1 0 1 1.07 28 0 1 1 0 1.33 29 1 1 0 0 1.34 表 3 回归模型方差分析结果
Table 3 Analysis of variance for regression model
来源 平方和 自由度 均方 F值 P值 显著性 模型 0.48 14 0.034 110.44 <0.0001 ** X1 0.031 1 0.031 100.3 <0.0001 ** X2 0.18 1 0.18 582.45 <0.0001 ** X3 3.33E−03 1 3.33E−03 10.78 0.0054 ** X4 8.33E−04 1 8.33E−04 2.7 0.1229 X1X2 1.60E−03 1 1.60E−03 5.18 0.0392 * X1X3 1.00E−04 1 1.00E−04 0.32 0.5786 X1X4 2.25E−04 1 2.25E−04 0.73 0.408 X2X3 2.50E−05 1 2.50E−05 0.081 0.7803 X2X4 0 1 0 0 1 X3X4 2.50E−05 1 2.50E−05 0.081 0.7803 X12 0.083 1 0.083 267.11 <0.0001 ** X22 0.13 1 0.13 413.18 <0.0001 ** X32 0.092 1 0.092 297.52 <0.0001 ** X42 0.1 1 0.1 336.18 <0.0001 ** 残差 4.33E−03 14 3.09E−04 失拟项 2.81E−03 10 2.81E−04 0.74 0.6831 纯误差 1.52E−03 4 3.80E−04 总和 0.48 28 注:*表示显著(P<0.05),**表示极显著(P<0.01)。 -
[1] 陈云汉. 蒲公英橡胶草胶乳提取工艺的研究[D]. 北京:北京化工大学, 2019. [CHEN Y H. Study on extraction process of Taraxacum kok-saghyz latex[D]. Beijing:Beijing University of Chemical Technology, 2019.] CHEN Y H. Study on extraction process of Taraxacum kok-saghyz latex[D]. Beijing: Beijing University of Chemical Technology, 2019.
[2] RAMIREZ-CADAVID D A, COMISH K, MICHEL F C. Taraxacum kok-saghyz (TK):Compositional analysis of a feedstock for natural rubber and other bioproducts[J]. Industrial Crops and Products,2017,107:624−640. doi: 10.1016/j.indcrop.2017.05.043
[3] ZHANG N, CHEN T, YE S, et al. Comparative analysis with GC-MS of fatty acids and volatile compounds of Taraxacum kok-saghyz Rodin and Taraxacum officinale as edible resource plants[J]. Separations,2022,9(10):314. doi: 10.3390/separations9100314
[4] 陈江艳, 王维滔, 董益阳, 等. 响应面优化蒲公英橡胶草菊糖提取工艺及其MALDI-TOF MS分析[J]. 食品工业科技,2022,43(1):205−212. [CHEN J Y, WANG W T, DONG Y Y, et al. Optimization of extraction of inulin from Taraxacum kok-saghyz Rodin by response surface methodology and its MALDI-TOF MS analysis[J]. Science and Technology of Food Industry,2022,43(1):205−212.] CHEN J Y, WANG W T, DONG Y Y, et al. Optimization of extraction of inulin from Taraxacum kok-saghyz Rodin by response surface methodology and its MALDI-TOF MS analysis[J]. Science and Technology of Food Industry, 2022, 43(1): 205−212.
[5] PUTTER K M, VAN DEENEN N, MULLER B, et al. The enzymes OSC1 and CYP716A263 produce a high variety of triterpenoids in the latex of Taraxacum koksaghyz[J]. Scientific Reports,2019,9(1):5942. doi: 10.1038/s41598-019-42381-w
[6] KONG J, CHEN J, YUE Y, et al. Ultrasonic/microwave-assisted extraction and rapid quantitative determination of active ingredients in Taraxacum kok-saghyz Rodin by ultra-high-performance liquid chromatography tandem mass spectrometry[J]. International Journal of Mass Spectrometry,2021,470:116700. doi: 10.1016/j.ijms.2021.116700
[7] HU C. Taraxacum:Phytochemistry and health benefits[J]. Chinese Herbal Medicines,2018,10(4):353−361. doi: 10.1016/j.chmed.2018.08.003
[8] SHI S Y, ZHANG Y P, HUANG K L, et al. Flavonoids from Taraxacum mongolicum[J]. Biochemical Systematics Ecology,2008,36(5-6):437−440. doi: 10.1016/j.bse.2007.09.013
[9] WILLIAMS C A, GOLDSTONE F, GREENHAM J. Flavonoids, cinnamic acids and coumarins from the different tissues and medicinal preparations of Taraxacum officinale[J]. Phytochemistry,1996,42(1):121−127. doi: 10.1016/0031-9422(95)00865-9
[10] XUE Y, ZHANG S, DU M, et al. Dandelion extract suppresses reactive oxidative species and inflammasome in intestinal epithelial cells[J]. Journal of Functional Foods,2017,29:10−18. doi: 10.1016/j.jff.2016.11.032
[11] XIE P J, HUANG L X, ZHANG C H, et al. Skin-care effects of dandelion leaf extract and stem extract:Antioxidant properties, tyrosinase inhibitory and molecular docking simulations[J]. Industrial Crops Products,2018,111:238−246. doi: 10.1016/j.indcrop.2017.10.017
[12] SATO Y, ITAGAKI S, KUROKAWA T, et al. In vitro and in vivo antioxidant properties of chlorogenic acid and caffeic acid[J]. International Journal of Pharmaceutics,2011,403(1-2):136−138. doi: 10.1016/j.ijpharm.2010.09.035
[13] JEDREJEK D, KONTEK B, LIS B, et al. Evaluation of antioxidant activity of phenolic fractions from the leaves and petals of dandelion in human plasma treated with H2O2 and H2O2/Fe[J]. Chemico-Biological Interactions,2017,262:29−37. doi: 10.1016/j.cbi.2016.12.003
[14] GONZALEZ-CASTEJON M, VISIOLI F, RODRIGUEZ-CASADO A. Diverse biological activities of dandelion[J]. Nutrition Reviews,2012,70(9):534−547. doi: 10.1111/j.1753-4887.2012.00509.x
[15] LIS B, JEDREJEK D, STOCHMAL A, et al. Assessment of effects of phenolic fractions from leaves and petals of dandelion in selected components of hemostasis[J]. Food Research International,2018,107:605−612. doi: 10.1016/j.foodres.2018.03.012
[16] 刘杨, 赵婧, 梁莉, 等. 响应面优化蒲公英多酚超声波辅助乙醇提取工艺及其抗氧化性[J]. 食品工业科技,2017,38(2):287−292. [LIU Y, ZHAO J, LIANG L, et al. Optimization of ultrasonic-assisted alcohol extraction of polyphenols from dandelion and their antioxidant activity[J]. Science and Technology of Food Industry,2017,38(2):287−292.] LIU Y, ZHAO J, LIANG L, et al. Optimization of ultrasonic-assisted alcohol extraction of polyphenols from dandelion and their antioxidant activity[J]. Science and Technology of Food Industry, 2017, 38(2): 287−292.
[17] 梁引库, 张萍, 徐仲阳, 等. 蒲公英提取物对煎炸菜籽油品质的影响[J]. 食品科技,2019,44(10):206−211. [LIANG Y K, ZHANG P, XU Z Y, et al. Effect of dandelion extract on the quality of fried rapeseed oil[J]. Food Science and Technology,2019,44(10):206−211.] LIANG Y K, ZHANG P, XU Z Y, et al. Effect of dandelion extract on the quality of fried rapeseed oil[J]. Food Science and Technology, 2019, 44(10): 206−211.
[18] 崔艳平, 聂玮, 迟晓君, 等. 蒲公英多酚提取工艺优化及抗氧化活性研究[J]. 安徽农业科学,2021,49(8):175−180. [CUI Y P, NIE W, CHI X J, et al. Study on optimization of extraction technology and antioxidant activity of dandelion polyphenols[J]. Journal of Anhui Agricultural Sciences,2021,49(8):175−180.] doi: 10.3969/j.issn.0517-6611.2021.08.046 CUI Y P, NIE W, CHI X J, et al. Study on optimization of extraction technology and antioxidant activity of dandelion polyphenols[J]. Journal of Anhui Agricultural Sciences, 2021, 49(8): 175−180. doi: 10.3969/j.issn.0517-6611.2021.08.046
[19] MOLINU M G, PILUZZA G, CAMPESI G, et al. Antioxidant sources from leaves of russian dandelion[J]. Chemistry & Biodiversity,2019,16(8):e1900250.
[20] 贺银菊, 张旋俊, 杨再波, 等. 响应面优化紫果西番莲叶多酚超声辅助提取工艺及其抗氧化活性[J]. 食品工业科技,2021,42(1):212−216,226. [HE Y J, ZHANG X J, YANG Z B, et al. Optimization of ultrasonic-assisted extraction of polyphenols in the purple passionfruit leaves by response surface methodology and its antioxidant activity[J]. Science and Technology of Food Industry,2021,42(1):212−216,226.] HE Y J, ZHANG X J, YANG Z B, et al. Optimization of ultrasonic-assisted extraction of polyphenols in the purple passionfruit leaves by response surface methodology and its antioxidant activity[J]. Science and Technology of Food Industry, 2021, 42(1): 212−216,226.
[21] WEN C, ZHANG J, ZHANG H, et al. Advances in ultrasound assisted extraction of bioactive compounds from cash crops-A review[J]. Ultrasonics Sonochemistry,2018,48:538−549. doi: 10.1016/j.ultsonch.2018.07.018
[22] LI L, YANG X, PAN L, et al. Comparing three methods of extraction of Auricularia auricula polysaccharides[J]. Current Topics in Nutraceutical Research,2019,17(1):7−10.
[23] LU S H, ZUO H J, SHI J X, et al. Two new glycosides from the leaves of Ligustrum robustum and their antioxidant activities and inhibitory effects on alpha-glucosidase and alpha-amylase[J]. South African Journal of Botany,2019,125:521−526. doi: 10.1016/j.sajb.2019.07.028
[24] de-BELLIS R, CHIARANTINI L, POTENZA L, et al. High production of secondary metabolites and biological activities of Cydonia oblonga Mill. pulp fruit callus[J]. Journal of Functional Foods,2022,94:105133. doi: 10.1016/j.jff.2022.105133
[25] 裴斐, 陶虹伶, 蔡丽娟, 等. 响应面试验优化辣木叶多酚超声辅助提取工艺及其抗氧化活性[J]. 食品科学,2016,37(20):24−30. [PEI F, TAO H L, CAI L J, et al. Optimization of polyphenols from Moringa oleifera Lam. leaves by ultrasound-assisted extraction using response surface methodology and their antioxidant activities[J]. Food Science,2016,37(20):24−30.] doi: 10.7506/spkx1002-6630-201620005 PEI F, TAO H L, CAI L J, et al. Optimization of polyphenols from Moringa oleifera Lam. leaves by ultrasound-assisted extraction using response surface methodology and their antioxidant activities[J]. Food Science, 2016, 37(20): 24−30. doi: 10.7506/spkx1002-6630-201620005
[26] 穆谈航, 叶嘉, 杨明建, 等. 石榴皮多酚提取工艺优化及其贮藏稳定性研究[J]. 食品工业科技,2021,42(11):142−146. [MU T H, YE J, YANG J M, et al. Optimization of extraction technology and storage stability of polyphenols from pomegranate peel[J]. Science and Technology of Food Industry,2021,42(11):142−146.] MU T H, YE J, YANG J M, et al. Optimization of extraction technology and storage stability of polyphenols from pomegranate peel[J]. Science and Technology of Food Industry, 2021, 42(11): 142−146.
[27] 李映新, 梁婧, 何阳, 等. 黑老虎果皮多酚超声辅助提取工艺及其抗氧化活性研究[J]. 中国食品添加剂,2022,33(4):48−54. [LI Y X, LIANG J, HE Y, et al. Study on the ultrasonic-assisted extraction technology and antioxidant activity of polyphenols from Kadsura coccinea peel[J]. China Food Additives,2022,33(4):48− 54.
[28] 张国强, 郭晓东, 薛文华, 等. 西藏野生卷叶黄精多酚的提取及其抗氧化活性分析[J]. 食品科学,2017,38(6):236−241. [ZHANG G Q, GUO X D, XUE W H, et al. Extraction and antioxidant activities of polyphenols from Tibetan wild Polygonatum cirrhifolium[J]. Food Science,2017,38(6):236−241.] doi: 10.7506/spkx1002-6630-201706037 ZHANG G Q, GUO X D, XUE W H, et al. Extraction and antioxidant activities of polyphenols from Tibetan wild Polygonatum cirrhifolium[J]. Food Science, 2017, 38(6): 236−241. doi: 10.7506/spkx1002-6630-201706037
[29] HEMWIMOL S, PAVASANT P, SHOTIPRUK A. Ultrasound-assisted extraction of anthraquinones from roots of Morinda citrifolia[J]. Ultrasonics Sonochemistry,2006,13(6):543−548. doi: 10.1016/j.ultsonch.2005.09.009
[30] LIU Z, JIAO Y, LU H, et al. Chemical characterization, antioxidant properties and anticancer activity of exopolysaccharides from Floccularia luteovirens[J]. Carbohydrate Polymers,2020,229:115432. doi: 10.1016/j.carbpol.2019.115432
[31] ETXEBERRIA U, GARZA LAURA A L DE LA, CAMPION J, et al. Antidiabetic effects of natural plant extracts via inhibition of carbohydrate hydrolysis enzymes with emphasis on pancreatic alpha amylase[J]. Expert Opinion on Therapeutic Targets,2012,16(3):269−297. doi: 10.1517/14728222.2012.664134
[32] LORDAN S, SMYTH T J, SOLER-VILA A, et al. The α-amylase and α-glucosidase inhibitory effects of Irish seaweed extracts[J]. Food Chemistry,2013,141(3):2170−2176. doi: 10.1016/j.foodchem.2013.04.123
[33] ORTIZ-ANDRADE R, ESTRADA-SOTO S, VILLALOBOS-MOLINA R, et al. Alpha-glucosidase inhibitory activity of the methanolic extract from Tournefortia hartwegiana:Anantihyperglycemic agent[J]. Acta Pharmacologica Sinica,2006,27:338−339.
[34] LS A, YW A, MING M B. Inhibition of α-amylase by polyphenolic compounds:Substrate digestion, binding interactions and nutritional intervention[J]. Trends in Food Science & Technology,2020,104:190−207.
[35] MF A, WL A, TL B, et al. Characterization of promising natural blue pigment from Vaccinium bracteatum thunb. leaves:Insights of the stability and the inhibition of α-amylase[J]. Food Chemistry,2020,326(2):126962.
-
期刊类型引用(6)
1. 闫昱辛,何美军,李宇,袁晓曼,谭旭辉,程名,罗凯,廖璐婧. 铁皮石斛叶多糖美白和抗氧化活性. 植物研究. 2025(01): 111-118 .  百度学术
百度学术
2. 代丽丽,王景,魏许瑞,马庆亚,王娜,都治香. 基于PI3K/Akt信号通路研究灯盏花乙素对子宫内膜癌Ishikawa细胞的影响. 中国临床药理学杂志. 2024(01): 27-31 .  百度学术
百度学术
3. 张琦,包小波,田冲冲. 灯盏花乙素增强4T1乳腺癌细胞对顺铂敏感性的体内外研究. 食品工业科技. 2024(05): 331-340 .  本站查看
本站查看
4. 王佳恩,殷子喻,马莉,李双良,符德欢. 灯盏乙素抗肿瘤作用机制研究进展. 中草药. 2024(13): 4608-4621 .  百度学术
百度学术
5. 张琦,田冲冲,张洋,方晨曦,卜薇,李凤. 灯盏花乙素通过PPARγ-PGC1α-UCP1通路改善小鼠肥胖作用及机制. 药物评价研究. 2024(08): 1787-1796 .  百度学术
百度学术
6. 田冲冲,张琦,陈延绅. 基于肠道微生态探讨灯盏花乙素对乳腺癌小鼠的化疗增敏作用及其机制. 中国微生态学杂志. 2024(12): 1374-1381+1387 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:




 下载:
下载:



