Effect of Ultrasonic Treatment on Physicochemical and Functional Properties of Goat Milk Casein
-
摘要: 以山羊奶酪蛋白为原料,利用不同强度超声处理山羊奶酪蛋白,探究超声处理对山羊奶酪蛋白的pH和电导率、Zeta电位、浊度等理化指标以及乳化性和起泡性等功能特性的影响。结果表明,与未处理相比,超声处理后山羊奶酪蛋白pH下降,电导率变化不显著(P>0.05);Zeta电位绝对值在400 W处理2 min时达到最大值27.85±1.55 mV;浊度值与未处理相比显著性降低(P<0.05);与未处理相比,超声处理可以减小蛋白平均粒径,并在700 W处理6 min时达到最低值,由383.20±13.07 nm减少至176.17±4.28 nm;扫描电镜结果表明超声改变了酪蛋白原有表观形态,导致不规则碎片的产生;超声处理后的酪蛋白乳化性在100 W处理10 min时提高了41.44%。在400 W处理10 min时起泡性和泡沫稳定性显著增加(P<0.05),分别达到最大值32.88%±0.07%和91.93%±0.19%。综上,超声处理产生的空化效应以及机械作用可以为山羊奶酪蛋白提供更好的理化特性和功能特性。Abstract: In this experiment, goat milk casein was used as raw material. Goat milk casein was treated with different ultrasonic intensities to explore the effects of ultrasonic treatment on the pH, conductivity, Zeta potential, turbidity and other physical and chemical indexes, as well as the functional characteristics of emulsification and foaming. The results showed that compared with untreated group, after ultrasonic treatment, the pH decreased and the conductivity had no significant change (P>0.05). The absolute value of Zeta potential reached the maximum value of 27.85±1.55 mV when treated at 400 W for 2 min. Turbidity was significantly decreased compared with untreated group (P<0.05). Ultrasonic treatment reduced the particle size of casein which reached its lowest value at 700 W treatment for 6 min, from 383.20±13.07 nm to 176.17±4.28 nm. Scanning electron microscopy results showed that ultrasound changed the original apparent morphology of casein, resulting in the formation of irregular fragments. After ultrasonic treatment, the emulsification at 100 W for 10 min was increased by 41.44%, and the foaming capacity and foaming stability of goat milk casein at 400 W for 10 min were significantly increased (P<0.05), reaching the maximum value of 32.88%±0.07% and 91.93%±0.19%, respectively. In conclusion, the cavitation effect and mechanical action produced by ultrasonic treatment can provide better physicochemical and functional properties for goat milk casein.
-
山羊奶酪蛋白(Goat milk casein,GMC)是存在于山羊奶中一类全价蛋白质[1]。有研究表明[2]山羊奶低水平的αs1-酪蛋白解决了30%~40%的牛奶过敏问题。山羊奶酪蛋白水解后可产生多种生物活性肽,可以参与免疫调节和神经调节等[3]。因此可用于营养强化剂或功能性食品辅料投入到食品加工中。在乳蛋白加工过程中,蛋白结构可能会改变,如疏水基的外露、基团的絮凝等,这些变化会影响蛋白的功能表达,进而影响食品品质。不同改性方式作用于酪蛋白可促进其理化和功能特性的改变,进而提高食品加工中对蛋白的高效利用。
超声作为一种非热物理技术在食品工业中应用广泛,在植物蛋白中,如辣木籽蛋白的超声改性促进其消化性能,并经超声处理后的消化产物具有更高的抗氧化活性[4];在动物蛋白中,如乳清蛋白浓缩物通过高强度超声诱导处理促进了蛋白与果胶复合物的乳液稳定性,这表明超声的使用可能会改变生物聚合物的结构,改变了蛋白质-多糖之间的分子结构及其相互作用力[5]。薛海燕等[6]对牛乳酪蛋白超声处理表明超声可以改变蛋白结构进而影响抗原性,并且抗原性与无规则卷曲含量呈正相关。Yang等[7]的研究表明超声处理改善了酪蛋白溶解性以及消化特性。Madadlou等[8]的研究表明超声处理破坏了酪蛋白胶束进而影响蛋白溶液的凝胶形成,增强了凝胶强度,这对于酸奶以及酸凝胶等产品有促进作用。
目前关于不同加工处理方式作用于酪蛋白的研究原料大多来源于牛奶[9−10],与牛奶相比山羊奶矿物质含量高;具有小尺寸的脂肪球,易于消化吸收;此外可以维护肠道健康,促进肠道中有益微生物生长等[11]。本实验以不同超声处理强度作用于山羊奶酪蛋白溶液,分析超声处理对酪蛋白的理化和功能特性的影响,探究超声处理技术在该领域的潜在应用,为山羊奶酪蛋白在食品工业进一步开发利用提供理论基础。
1. 材料与方法
1.1 材料与仪器
新鲜山羊奶 湖南羴牧营养品科技有限公司提供,来自羴牧牧业五桂牧场且从正常饲养、无传染性疾病的健康山羊乳房挤出未经处理的山羊乳;乙酸、磷酸二氢钠、磷酸氢二钠、十二烷基硫酸钠 均为分析纯,国药集团化学试剂有限公司;大豆油 试剂级,上海麦克林生化科技有限公司。
Bante-920 pH计 上海班特仪器制造有限公司;TGL-16M冷冻离心机 湘仪离心机仪器;BioTek酶标仪 美国伯腾仪器有限公司;ZETASIZER NANO ZS纳米粒度仪 马尔文帕纳科仪器有限公司;LKAT18数显型分散机 德国艾卡集团;LGJ-25真空冷冻干燥机 四环福瑞科仪科技发展(北京)有限公司;SCIENTZ-IID超声波细胞粉碎机 宁波新芝生物科技股份有限公司;DDS-11A电导率仪 上海雷磁台式电导率仪。
1.2 实验方法
1.2.1 山羊奶酪蛋白的制备
山羊奶酪蛋白的提取采用Magalhaes等[12]的方法并略加修改。首先将鲜奶用双层纱布过滤除杂,在4 ℃下以6500 r/min离心15 min,去除上层脂肪得脱脂奶。加热至45 ℃,使用10%乙酸持续搅拌下,将pH调节至4.1(等电点)。以6500 r/min,离心15 min分离酪蛋白和乳清,得到的沉淀即为粗品酪蛋白,最后水洗去除一些水溶性杂质,直至上清无色。将得到的沉淀物放入−80 ℃预冻2 h,后经冷冻干燥并收集粉末于4 ℃密封保存以备实验。经凯氏定氮法测得的蛋白质含量为85.52%。
1.2.2 酪蛋白溶液的制备
参考Han等[13]的方法,将酪蛋白粉末溶于pH7.4、0.02 mol/L的Na2HPO4–NaH2PO4缓冲液中,制备1%(w/v)的酪蛋白溶液,并在磁力搅拌器上搅拌30 min,最后需放4 ℃冰箱过夜水合,使蛋白溶液充分溶解。
1.2.3 超声处理酪蛋白溶液
使用直径为12 mm探头的超声波细胞破碎仪对溶液进行处理。取150 mL的酪蛋白溶液于烧杯中,并将探头置于液面下2~3 cm处,为防止超声中产生过热现象,采用冰水浴降温处理。实验过程中采用间断式超声处理模式,即每次超声工作3 s,间歇3 s。参考Han等[13]的方法以及预实验结果,超声功率设置为100、400、700 W,超声处理时间为2、6、10 min,未处理组为未经超声处理。
1.2.4 pH和电导率的测定
所有经过超声处理后样品需提前恢复至室温,用pH计直接浸泡测定样品pH。采用电导率仪测定电导率。
1.2.5 Zeta电位的测定
样品平衡时间120 s,实验温度25 ℃条件下采用纳米粒度仪进行测定。蛋白浓度为1%(w/v),每个样品测定3次取平均值。
1.2.6 浊度的测定
酪蛋白溶液经过超声处理后立即进行浊度的测定,测定所采取的方法参考汪娟[14]的方法并略加修改。蛋白浓度为1%(w/v),用酶标仪在600 nm波长下测定样品的吸光度A600来表征样品的浊度。
1.2.7 平均粒径和多分散指数(PDI)的测定
选取蛋白浓度1%(w/v)并参考李子超[15]的方法,纳米粒度仪相关参数设定:温度为25 ℃,颗粒折射率为1.450,颗粒吸收率为0.8872,分散剂为水,分散剂折射率为1.330。实验重复3次,取平均值。
1.2.8 扫描电镜
加速电压为10 kV,在开始扫描成像之前,用胶将少量经过冻干的蛋白样品粉末粘到小块铁板上,喷金后上样扫描观察,放大倍数为200倍。
1.2.9 乳化性和乳化稳定性的测定
参考Du等[16]的方法,并略加修改。取大豆油与酪蛋白溶液(1%,w/v)按1:3比例混匀,10000 r/min离心2 min。立即从烧杯底部取乳液50 µL到5 mL 0.1%(w/v)SDS溶液中混匀,并在500 nm下对其进行吸光度测定。混合液在室温下静置10 min后,重复操作,记录在500 nm处吸光度值。
采用方程式计算乳化活性指数(EAI,m2/g)和乳化稳定性指数(ESI,min)。每个EAI和ESI评价共三个重复。
EAI(m2/g)=2×2.303×A0C×φ×10000×100 ESI(min)=A0A0−A10×10 式中:A0表示第0 min时样品在500 nm处的吸光度;A10表示第10 min时样品在500 nm处的吸光度;C是蛋白质样品的浓度,g/mL;φ为实验中油的体积分数0.25。
1.2.10 起泡性和泡沫稳定性的测定
根据Jiang等[17]的方法,并略加修改。样品浓度设置为10 mg/mL,取1 mL样品置于离心管中,在室温条件下利用高速剪切分散机均质,设置转速为11400 r/min,时间2 min,分别记录第0 min和第10 min泡沫和溶液的总体积。其中FC表示起泡性,FS表示泡沫稳定性。
FC(%)=V0−VCVC×100 FS(%)=V10−VCV0−VC×100 式中:VC为均质前样品体积,mL;V0为均质后样品在第0 min的体积,mL;V10为均质后样品静置10 min的体积,mL。
1.3 数据处理
采用Excel 2021软件进行数据整理,每次实验需重复测定3次,取平均值,以SPSS Statistics 21进行单因素方差分析(ANOVA)和LSD多重比较,以P<0.05表示差异显著;采用Origin Pro 2021软件进行绘图。
2. 结果与分析
2.1 超声处理对山羊奶酪蛋白pH和电导率的影响
超声处理对山羊奶酪蛋白pH测定结果如表1所示,结果表明,与未处理组相比,经过超声处理后样品的pH发生了显著性变化(P<0.05),超声处理后的pH减小,在400 W,2 min时达到最低6.77。pH降低可能是隐藏在蛋白质胶束内的酸性氨基酸残基等经超声处理后暴露出来,也有可能是磷酸酯键的酶解作用导致[18]。蛋白溶液电导率是溶解蛋白粉的固有特性,取决于带电物质的性质和数量[19],由表1可知本实验研究的不同的超声功率以及时间对蛋白溶液电导率没有显著性影响(P>0.05),这与Arzeni等[20]对蛋清蛋白以及大豆分离蛋白的电导率测定结果类似,但Jambark等[21]对乳清蛋白产物进行超声处理的研究结果表明电导率显著增加,可能是因为超声产生的“空穴效应”会促使一些自由基和其他化合物的产生,还有研究表明超声处理大豆分离蛋白导致溶液的电导率下降,可能由于超声处理会产生一些不导电的聚集体,所以会导致溶液电导率降低,同时当物质粘度增加时,阻碍了离子的运动也会导致电导率降低[22]。造成这样的差异可能是由于样本不同,山羊奶酪蛋白溶液本身电导率较低,超声处理对其影响较小,以及仪器设备不同等综合作用引起。
表 1 超声处理对酪蛋白溶液pH和电导率的影响Table 1. Effect of ultrasonic treatment on pH and conductivity of casein solution超声处理强度(W-min) pH 电导率(mS/cm) 未处理 6.83±0.00a 2.80±0.24a 100-2 6.79±0.00bcd 2.80±0.23a 100-6 6.78±0.00cd 2.89±0.23a 100-10 6.78±0.00cd 2.89±0.23a 400-2 6.77±0.00d 2.79±0.22a 400-6 6.79±0.00bcd 2.87±0.21a 400-10 6.78±0.00cd 2.84±0.22a 700-2 6.80±0.00b 2.80±0.24a 700-6 6.79±0.00bc 2.90±0.24a 700-10 6.78±0.01bcd 2.91±0.23a 注:同列不同上标小写字母表示差异显著(P<0.05)。 2.2 超声处理对山羊奶酪蛋白Zeta电位的影响
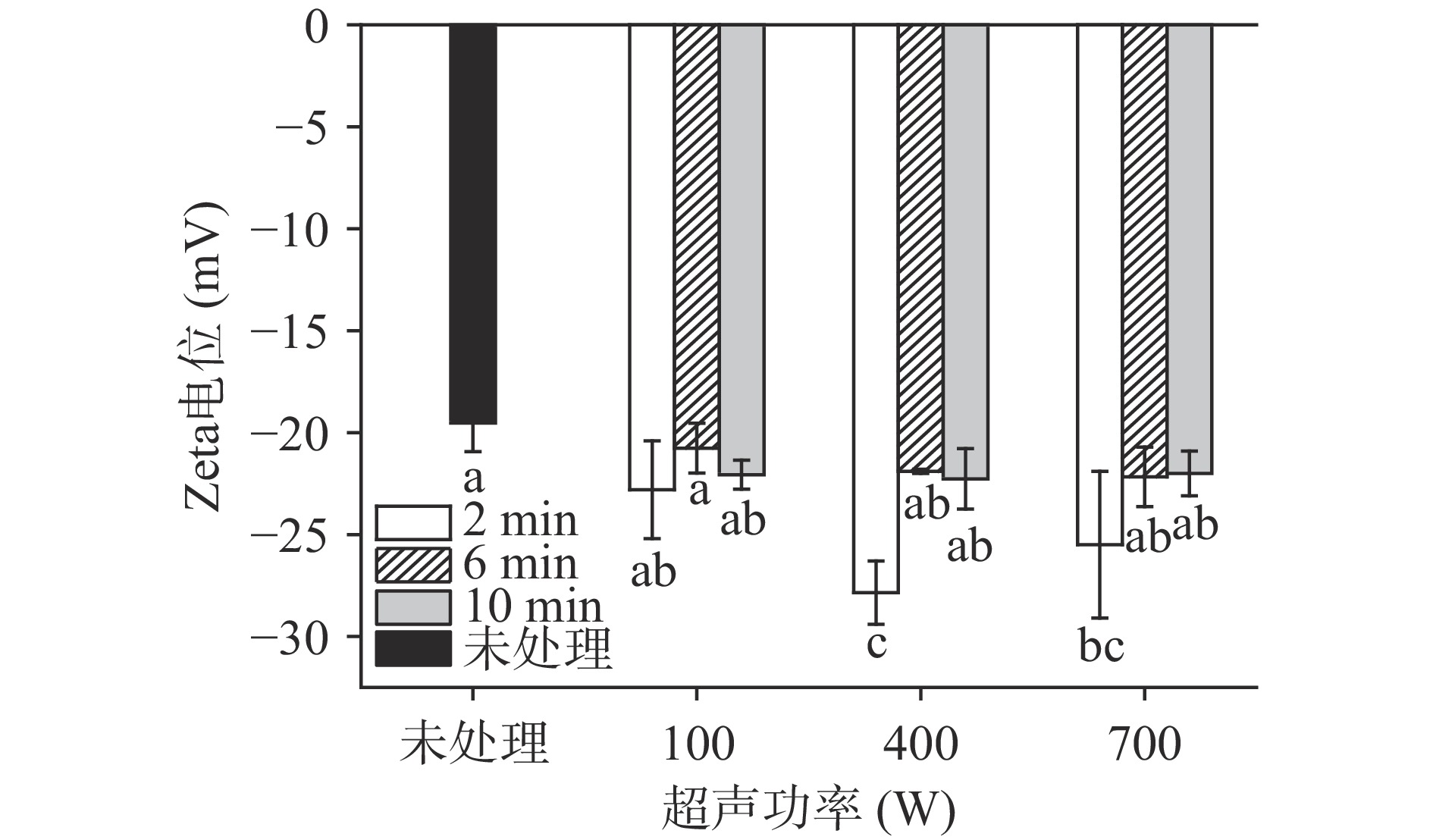
不同强度超声处理酪蛋白Zeta电位结果如图1所示。Zeta电位与蛋白质表面电荷绝对值相近,其绝对值越大表明分子之间静电相互作用力越强,可阻止蛋白分子聚集,从而维持溶液体系稳定以及蛋白泡沫稳定性[23]。由图1可知,检测到的蛋白溶液电位值均为负值,说明溶液中带负电荷的氨基酸高于带正电荷的氨基酸。未经处理的酪蛋白的电位绝对值为19.53±1.39 mV,在2 min超声条件下,随着超声功率的增加,Zeta电位绝对值增大,且在400 W时电位绝对值最高为27.85±1.55 mV,与未处理相比显著增加(P<0.05),可能是因为超声导致酪蛋白结构展开,酪蛋白基团电离程度增加,使其暴露出更多负电荷氨基酸,静电斥力增强,抑制蛋白质分子的聚集[24],增大功率至700 W时电位绝对值变化不显著(P>0.05),在400 W功率下处理2 min后继续延长超声作用时间导致电位绝对值显著下降(P<0.05),可能是由于存在酪蛋白表面的有效电荷减少,静电斥力作用低,溶液稳定性降低导致蛋白重新聚集[25]。
2.3 超声处理对山羊奶酪蛋白浊度的影响
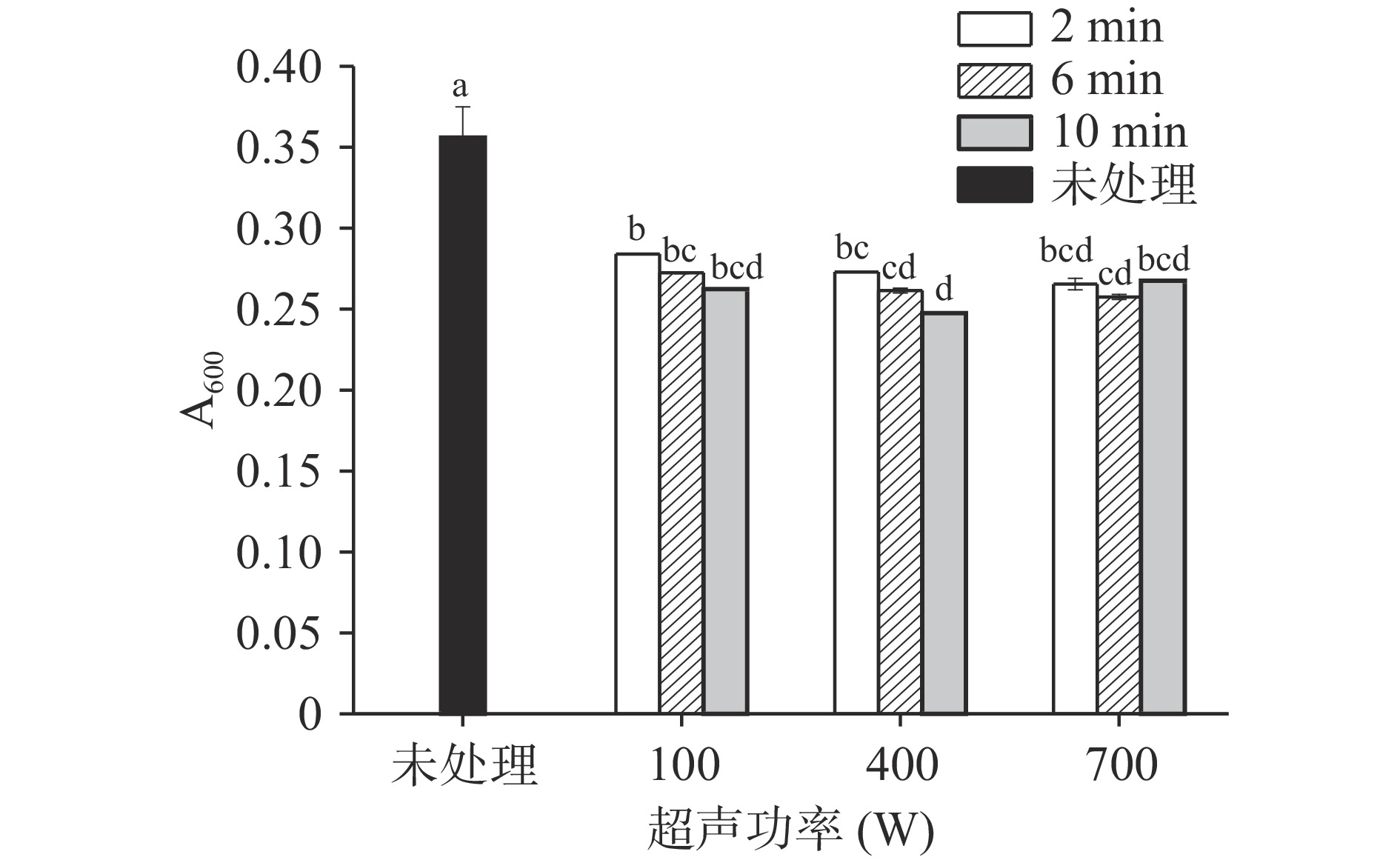
浊度的测定结果如图2所示。酪蛋白溶液经超声处理后浊度值下降,显著低于未处理组(P<0.05)。未处理组的浊度值较高说明未溶解的聚合物较多,因此浊度值也就大。100 W和400 W超声处理的羊乳酪蛋白浊度随着超声处理时间的增加而逐渐降低,在400 W超声10 min时浊度达到最低,由最初的0.356降至0.248。Chandrapala等[26]的研究结果也表明超声处理会使乳清蛋白或乳清蛋白-酪蛋白结合体系的分解,破坏脂肪球膜,从而浊度值相应降低。700 W超声6 min浊度值由0.356降至0.258,10 min后又略微增加到0.268。有研究表明超声处理可以降低酪蛋白溶液的粒径和浊度,粒径降低则蛋白颗粒光散射的表面积增加,使得蛋白质溶液浊度降低,但是在超声波的高频振动以及剪切力作用下,蛋白质分子发生了部分解离、变形以及聚集等现象,导致蛋白质聚集体的形成,从而使浊度值增加[27−28]。
2.4 超声处理对山羊奶酪蛋白粒径和多分散指数(PDI)的影响
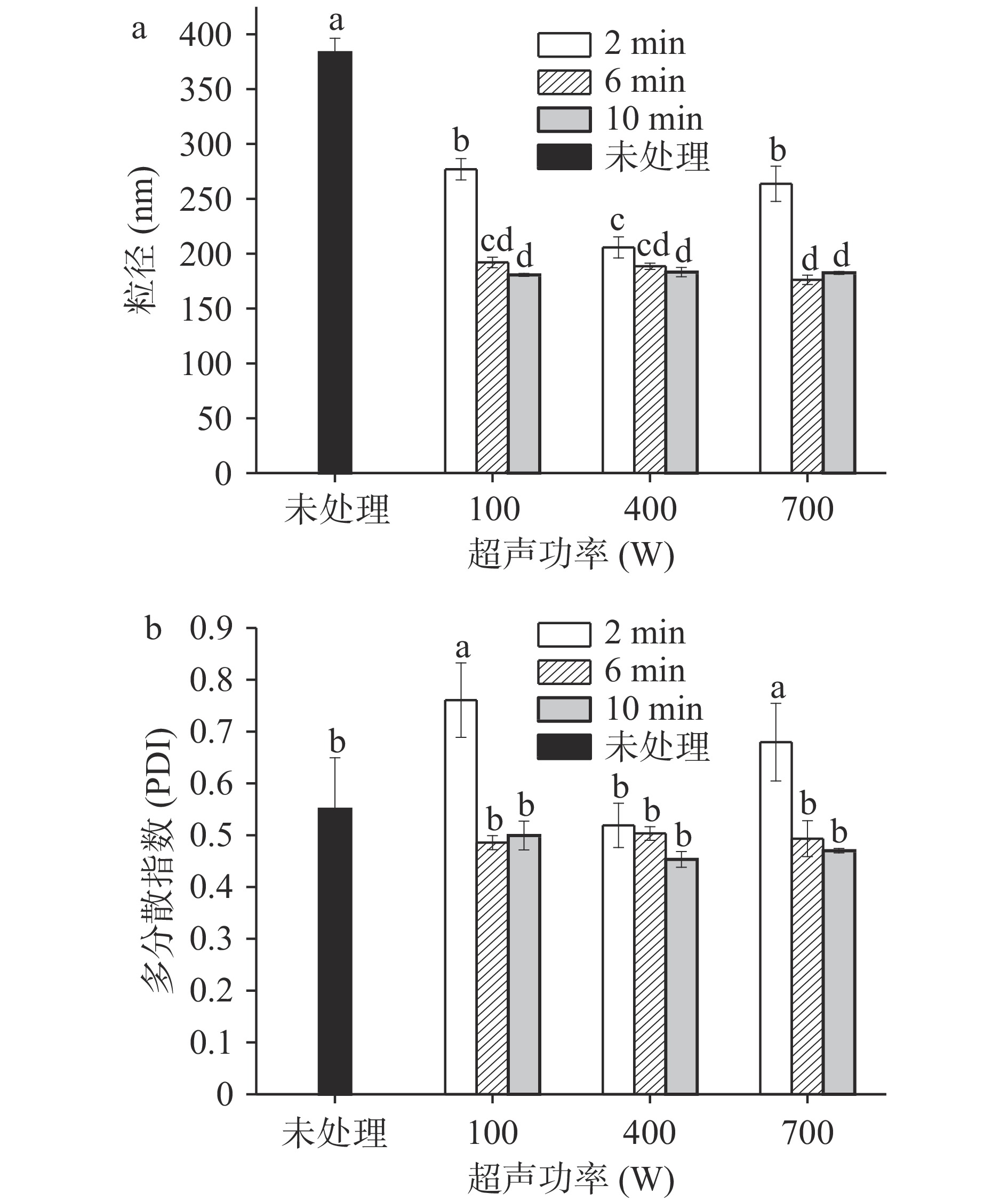
图3为不同超声处理下的酪蛋白的粒径和多分散指数(PDI),由图3(a)可知,与未处理组相比,100 W和400 W超声处理下,随着时间的增加酪蛋白的平均粒径显著降低(P<0.05);在700 W超声处理强度下,随着时间的增加,酪蛋白的平均粒径有先下降后略有上升的趋势。未处理组的酪蛋白平均粒径为383.20±13.07 nm,当700 W处理6 min时蛋白粒径达到最低176.17±4.28 nm。在2 min处理时间下,随着功率的增加粒径先减小后在700 W增大;在6 min和10 min处理条件下,粒径逐渐降低趋于平稳无显著性差异(P>0.05)。结果说明超声波产生的湍流以及高剪切力能够促使蛋白颗粒粒径的减小,但是超声强度的增加会促使蛋白颗粒碰撞过于频繁,受损的蛋白颗粒通过非共价和共价相互作用重新聚合[29]。
多分散性指数(PDI)是评价粒径分布的一个指标,数值越小代表粒度越均匀,分布越集中[30]。由图3(b)可知,超声处理前后酪蛋白的PDI值大多集中在0.40~0.60,表明体系属于适中分散体系。未处理的酪蛋白PDI为0.55±0.10,当400 W处理10 min时PDI最低,为0.45±0.02,表明超声处理可以促进蛋白分布趋于均匀。在100 W功率下,随着时间延长蛋白溶液中粒子PDI减小,但在2 min时粒度分布比未处理效果差,可能是由于低功率条件下,超声产生的机械效应低,粒径分布不够完全;在400 W时,随着时间增加,PDI与未处理无明显差异(P>0.05),颗粒分布均匀[31];700 W功率下随着时间延长PDI逐渐下降,最终趋于平稳,但在2 min时PDI比未处理较大,可能是由于超声波产生的能量密度过大,小部分用于空化以及机械效应,还会产生热能,这些协同效应,可能会产生聚集导致分布变大进而PDI变大[31],持续超声作用下大颗粒不断被破碎形成小颗粒,分布更均匀的小粒子数量逐渐增加,最终趋于平稳。在2 min超声时间下,随着功率增加,PDI表现为先减小随后增加的现象,说明短时高功率超声可能会加速粒子的碰撞;在6 min与10 min超声时间下功率的增加对酪蛋白溶液的分散无显著性影响(P>0.05)。
2.5 超声处理对山羊奶酪蛋白扫描电镜的测定结果
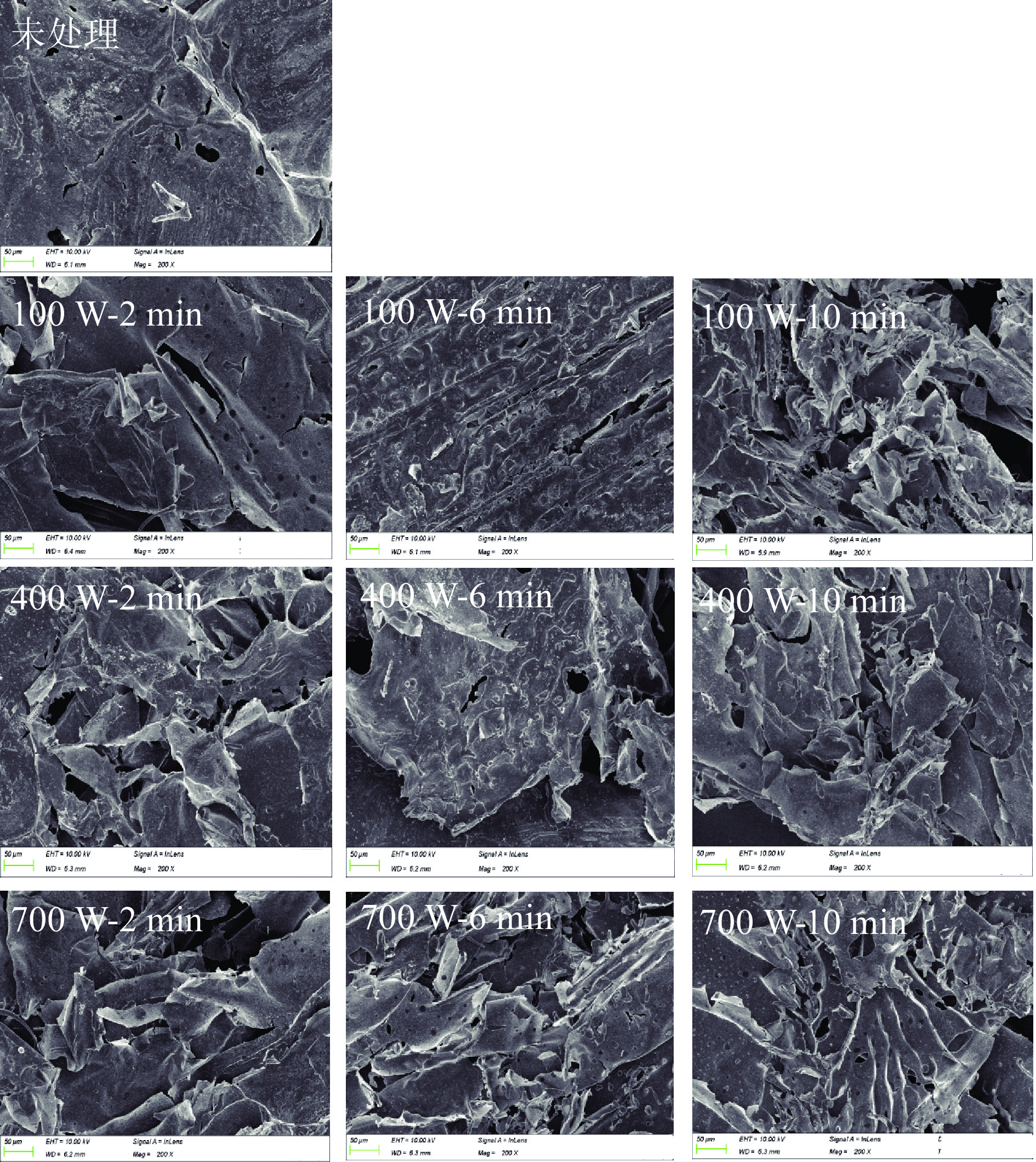
图4所示是冻干未经超声处理的酪蛋白以及超声处理后的酪蛋白在200倍放大的扫描电镜图。由图4可知,与未处理组比较,经过超声处理之后的蛋白表面有明显撕裂,多呈不规则状与文献报道一致[10]。蛋白这些微观形态的变化可能是由于超声过程中空化泡崩溃时产生的冲击波、剪切力等使蛋白分子之间的交联破坏[10]。在100 W和400 W处理下,可以看出随着时间延长酪蛋白表面撕裂程度越大,而当功率提升至700 W时,虽会有碎片产生但微观形貌与400 W无明显差别,表明超声强度达到一定大小后再继续提高对酪蛋白微观结构没有显著性影响。
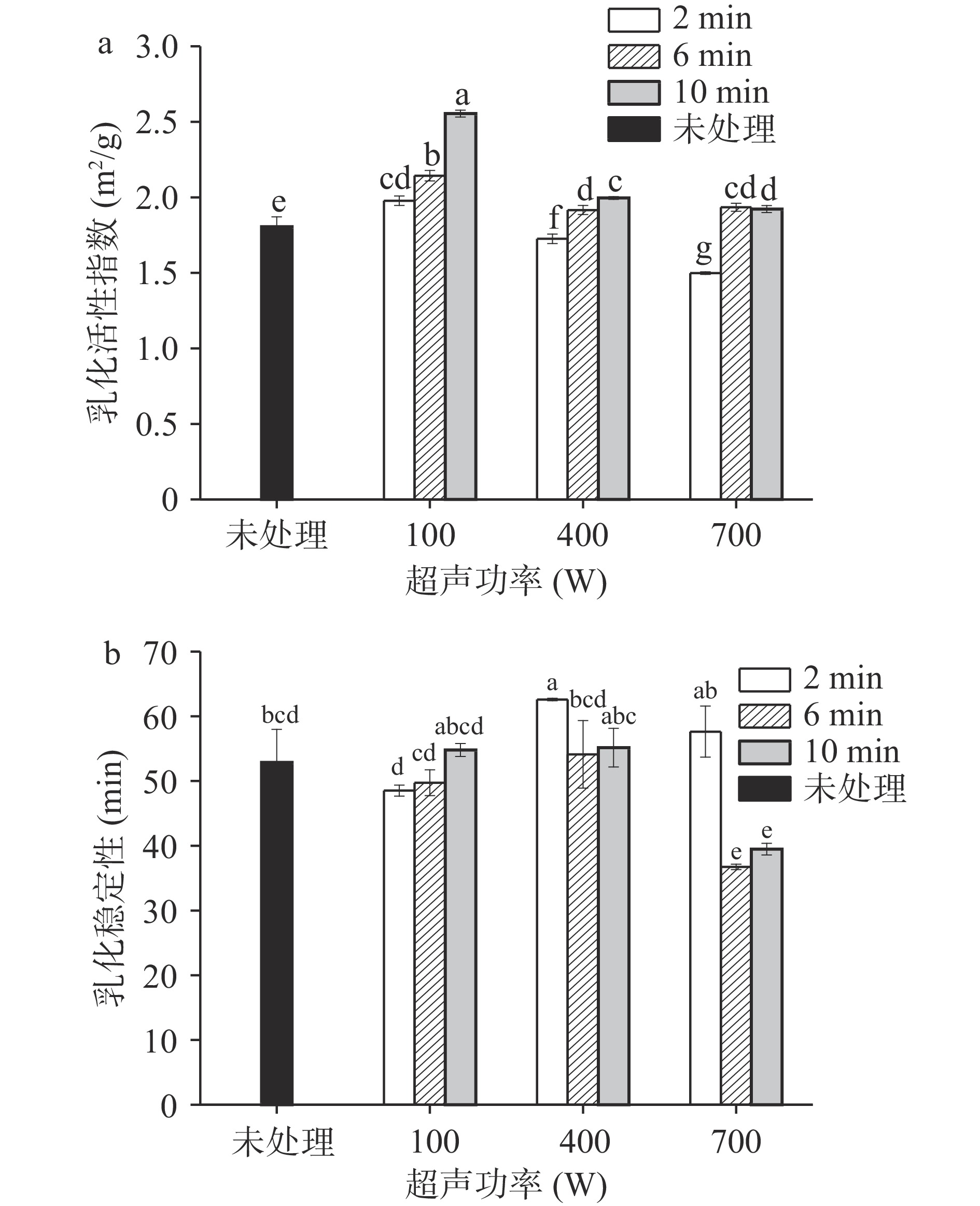
2.6 超声处理对山羊奶酪蛋白乳化性和乳化稳定性的影响
图5为不同超声功率以及时间的处理下酪蛋白的乳化性和乳化稳定性的变化。由图5(a)可知,经过超声处理后的酪蛋白的乳化性与未处理相比有显著性变化(P<0.05),总体来看,当超声时间一定时,随着功率的增加,酪蛋白乳化性整体呈逐渐减少的趋势,说明高功率超声处理时,蛋白变性程度高,分子结构重新排列,蛋白分子可能聚集,降低了乳化性[32]。在超声功率100 W时,随着超声时间的延长乳化性逐渐提升,10 min处理条件下,乳化性有最大值2.56±0.02 m2/g,与未处理相比提高了41.44%,乳化性的增加可能是因为超声波作用于蛋白质减小了颗粒尺寸,使蛋白质更易吸附于油水界面,从而提高乳化性[33],但在700 W处理条件下,6 min时乳化性最佳,说明长时间超声也会导致蛋白的变性,颗粒聚集[32]。由图5(b)可知,100 W超声条件下随着时间延长,乳化稳定性与未处理组没有显著差异(P>0.05)。在400 W处理2 min时与未处理相比显著性提高(P<0.05),达到最高62.60±0.20 min,在此功率下随着超声时间的增加,酪蛋白溶液的乳化稳定性变差。700 W超声功率下,延长超声时间对乳液稳定性没有促进作用,一方面有研究表明超声处理破坏了静电平衡从而导致乳液稳定性下降[34];另一方面在超声作用下,蛋白分子完整性遭到破坏,同时超声波产生的瞬时极端温度和压力可能会改变分子的灵活性使部分颗粒聚集或解离导致乳化稳定性的降低[35]。
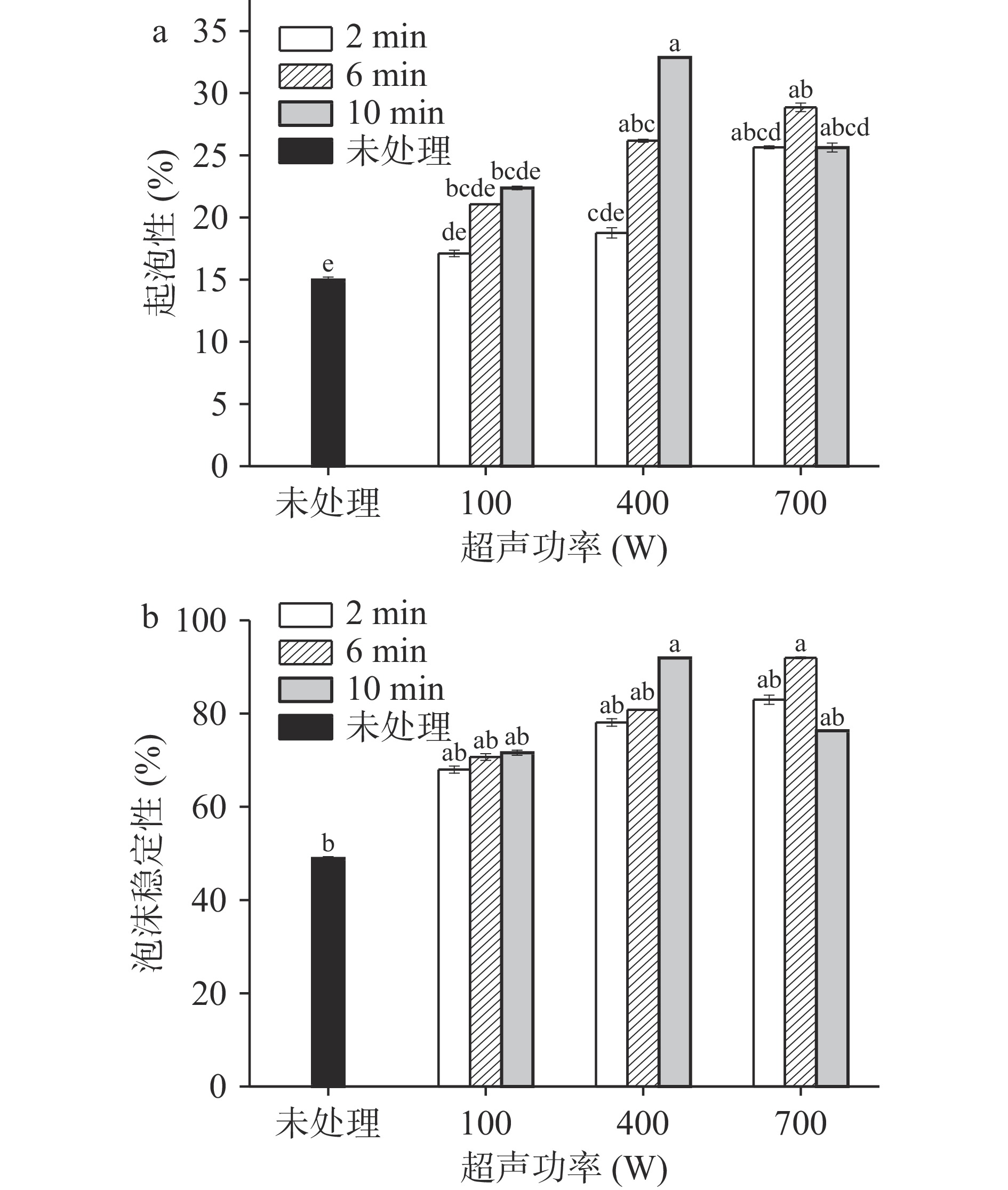
2.7 超声处理对山羊奶酪蛋白起泡性和泡沫稳定性的影响
不同超声强度对酪蛋白起泡性和泡沫稳定性的影响结果如图6所示,经过超声处理后酪蛋白的起泡性和泡沫稳定性均有不同程度改善。总体来说,2 min和6 min处理下随着功率的增加起泡性和泡沫稳定性都在增加,但是超声10 min各项性能会出现先增加后降低的趋势。Lin等[36]研究表明600 W超声时间大于5 min时会使酪蛋白颗粒聚集,疏水基隐藏,降低蛋白质多肽链之间的相互作用,从而导致功能特性不佳。
由图6可知超声功率100 W和400 W时,起泡性和泡沫稳定性随着时间增加而增加,在400 W超声10 min时最佳,分别为32.88%±0.07%、91.93%±0.19%,说明超声处理使得酪蛋白结构展开,促进蛋白质分子在气液交界面扩展与吸附[37],进而增加了蛋白质的起泡能力,但700 W处理10 min下起泡性和泡沫稳定性下降,表明高功率长时间超声处理作用下破坏了气液界面的平衡,泡沫不易形成[38],有研究表明蛋白质的流变学特性会影响蛋白质的泡沫稳定性,超声处理可使蛋白的黏度降低,破坏了蛋白质分子间网状结构,使得泡沫无法维持原有稳定的形态,从而导致泡沫稳定性下降[39]。
3. 结论
采用不同强度超声对山羊奶酪蛋白溶液进行处理,结果表示,与未处理相比,酪蛋白溶液pH发生显著性变化(P<0.05)且随着超声强度的增大部分蛋白溶液的pH减小,释放出更多酸性氨基酸并在400 W,2 min时达到最低6.77;电导率值总体有上升趋势,但无显著性差异(P>0.05);Zeta电位绝对值有不同程度的增加促进蛋白溶液趋于稳定,但是长时间超声作用会破坏平衡;超声的机械作用可以显著降低酪蛋白溶液的浊度值(P<0.05);通过粒径以及扫描电镜可以看出超声处理改变了酪蛋白颗粒的尺寸大小,酪蛋白由光滑状变为不规则撕裂状。在超声功率100 W处理10 min时酪蛋白乳化性能最佳为2.56±0.02 m2/g;超声处理也可以促进气液界面的吸附进而提高了起泡性能;说明超声处理能够促进酪蛋白空间结构以及理化指标的变化,导致内部疏水基暴露,进而提高功能特性,但是高功率(700 W)超声条件会导致蛋白颗粒重新聚集,影响各项指标。
-
表 1 超声处理对酪蛋白溶液pH和电导率的影响
Table 1 Effect of ultrasonic treatment on pH and conductivity of casein solution
超声处理强度(W-min) pH 电导率(mS/cm) 未处理 6.83±0.00a 2.80±0.24a 100-2 6.79±0.00bcd 2.80±0.23a 100-6 6.78±0.00cd 2.89±0.23a 100-10 6.78±0.00cd 2.89±0.23a 400-2 6.77±0.00d 2.79±0.22a 400-6 6.79±0.00bcd 2.87±0.21a 400-10 6.78±0.00cd 2.84±0.22a 700-2 6.80±0.00b 2.80±0.24a 700-6 6.79±0.00bc 2.90±0.24a 700-10 6.78±0.01bcd 2.91±0.23a 注:同列不同上标小写字母表示差异显著(P<0.05)。 -
[1] DHASMANA S, DAS S, SHRIVASTAVA S. Potential nutraceuticals from the casein fraction of goat's milk[J]. Journal of Food Biochemistry,2022,46(6):e13982.
[2] RIBEIRO A C, RIBERIO S D A. Specialty products made from goat milk[J]. Small Ruminant Research,2010,89(2-3):225−233. doi: 10.1016/j.smallrumres.2009.12.048
[3] QIAN J, ZHENG L, ZHAO Y, et al. Stability, bioavailability, and structure-activity relationship of casein-derived peptide YPVEPF with a sleep-enhancing effect[J]. Journal of Agricultural and Food Chemistry,2022,70(47):14947−14958. doi: 10.1021/acs.jafc.2c05024
[4] 巫艳慧, 唐诗琦, 杜秋函, 等. 超声改性对辣木籽蛋白体外消化特性的影响[J]. 中国食品学报,2023,23(2):111−120. [WU Y H, TANG S Q, DU Q H, et al. Effect of ultrasound modification on in vitro digestion characteristics of Moringa oleifera seeds water-solution protein[J]. Journal of Chinese Institute of Food Science and Technology,2023,23(2):111−120.] WU Y H, TANG S Q, DU Q H, et al. Effect of ultrasound modification on in vitro digestion characteristics of Moringa oleifera seeds water-solution protein[J]. Journal of Chinese Institute of Food Science and Technology, 2023, 23(2): 111−120.
[5] ALBANO K M, NICOLETTI V R. Ultrasound impact on whey protein concentrate-pectin complexes and in the O/W emulsions with low oil soybean content stabilization[J]. Ultrasonics Sonochemistry,2018,41:562−571. doi: 10.1016/j.ultsonch.2017.10.018
[6] 薛海燕, 操歌, 贺宝元, 等. 超声处理对牛乳酪蛋白结构及抗原性的影响[J]. 食品科学,2019,40(23):123−129. [XUE H Y, CAO G, HE B Y, et al. Effect of ultrasonic treatment on the structure and antigenicity of bovine caseins[J]. Food Science,2019,40(23):123−129.] doi: 10.7506/spkx1002-6630-20181101-013 XUE H Y, CAO G, HE B Y, et al. Effect of ultrasonic treatment on the structure and antigenicity of bovine caseins[J]. Food Science, 2019, 40(23): 123−129. doi: 10.7506/spkx1002-6630-20181101-013
[7] YANG M, ZENG Q, WANG Y, et al. Effect of ultrasound pretreatment on the physicochemical properties and simulated gastrointestinal digestibility of micellar casein concentrates[J]. LWT,2021,136:110319. doi: 10.1016/j.lwt.2020.110319
[8] MADADILOU A, EMAM-DIOMEN Z, MOUSAVI M E, et al. Acid-induced gelation behavior of sonicated casein solutions[J]. Ultrasonics Sonochemistry,2010,17(1):153−158. doi: 10.1016/j.ultsonch.2009.06.009
[9] WANG C, XIE Q, WANG Y, et al. Effect of ultrasound treatment on allergenicity reduction of milk casein via colloid formation[J]. Journal of Agricultural and Food Chemistry,2020,68(16):4678−4686. doi: 10.1021/acs.jafc.9b08245
[10] XU B, YUAN J, WANG L, et al. Effect of multi-frequency power ultrasound (MFPU) treatment on enzyme hydrolysis of casein[J]. Ultrasonics Sonochemistry,2020,63:104930. doi: 10.1016/j.ultsonch.2019.104930
[11] CHAN S, POWAR P, MEHRA R. A review on nutritional advantages and nutraceutical properties of cow and goat milk[J]. International Journal of Applied Research,2021,7:101−105.
[12] MAGALHAES I S, GUIMARAES A D B, TRIBST A A L, et al. Ultrasound-assisted enzymatic hydrolysis of goat milk casein:Effects on hydrolysis kinetics and on the solubility and antioxidant activity of hydrolysates[J]. Food Research International,2022,157:111310. doi: 10.1016/j.foodres.2022.111310
[13] HAN T, WANG M, WANG Y, et al. Effects of high-pressure homogenization and ultrasonic treatment on the structure and characteristics of casein[J]. LWT,2020,130:109560. doi: 10.1016/j.lwt.2020.109560
[14] 汪娟. 大豆分离蛋白与特定风味化合物相互作用机制的研究[D]. 广州:华南理工大学, 2018. [WANG J. Interaction of selected volatile flavor compounds and soy protein isolate[D]. Guangzhou:South China University of Technology, 2018.] WANG J. Interaction of selected volatile flavor compounds and soy protein isolate[D]. Guangzhou: South China University of Technology, 2018.
[15] 李子超. 乳源酪蛋白结构差异性的研究及其抗菌肽制备[D]. 广州:暨南大学, 2012. [LI Z C. Research on the protein structure differences and antibacterial peptides preparation of milk casein from different species[D]. Guangzhou:Jinan University, 2012.] LI Z C. Research on the protein structure differences and antibacterial peptides preparation of milk casein from different species[D]. Guangzhou: Jinan University, 2012.
[16] DU X, JING H, WANG L, et al. Characterization of structure, physicochemical properties, and hypoglycemic activity of goat milk whey protein hydrolysate processed with different proteases[J]. LWT,2022,159:113257. doi: 10.1016/j.lwt.2022.113257
[17] JIANG S J, ZHAO X H. Transglutaminase-induced cross-linking and glucosamine conjugation of casein and some functional properties of the modified product[J]. International Dairy Journal,2011,21(4):198−205. doi: 10.1016/j.idairyj.2010.12.004
[18] SAKURAI K, KONUMA T, YAGI M, et al. Structural dynamics and folding of β-lactoglobulin probed by heteronuclear NMR[J]. Biochimica et Biophysica Acta (BBA)-General Subjects,2009,1790(6):527−537. doi: 10.1016/j.bbagen.2009.04.003
[19] SU Y L, LIU L, LU J, et al. Effect of power ultrasound pre-treatment on the physical and functional properties of reconstituted milk protein concentrate[J]. Journal of Food Engineering,2014,124:11−18. doi: 10.1016/j.jfoodeng.2013.09.013
[20] ARZENI C, MARTINEZ K, ZEMA P, et al. Comparative study of high intensity ultrasound effects on food proteins functionality[J]. Journal of Food Engineering,2012,108(3):463−472. doi: 10.1016/j.jfoodeng.2011.08.018
[21] JAMBRAK A R, MASON T J, LELAS V, et al. Effect of ultrasound treatment on solubility and foaming properties of whey protein suspensions[J]. Journal of Food Engineering,2008,86(2):281−287. doi: 10.1016/j.jfoodeng.2007.10.004
[22] RAHMAN M M, LAMSAL B P. Ultrasound-assisted extraction and modification of plant-based proteins:Impact on physicochemical, functional, and nutritional properties[J]. Comprehensive Reviews in Food Science and Food Safety,2021,20(2):1457−1480. doi: 10.1111/1541-4337.12709
[23] 李慧娜. 大豆分离蛋白和浓缩蛋白乳液稳定性的比较及改性研究[D]. 郑州:河南工业大学, 2018. [LI H N. The comparative and modification study on the emulsion stabilities between soybean protein isolate and concentrates[D]. Zhengzhou:Henan University of Technology, 2018.] LI H N. The comparative and modification study on the emulsion stabilities between soybean protein isolate and concentrates[D]. Zhengzhou: Henan University of Technology, 2018.
[24] 康石花. 超声波处理对鹰嘴豆蛋白化学结构及功能特性的影响[D]. 石河子:石河子大学, 2023. [KANG S H. Effects of ultrasonic treatment on chemical structure and functional properties of chickpea protein isolate[D]. Shihezi:Shihezi University, 2023.] KANG S H. Effects of ultrasonic treatment on chemical structure and functional properties of chickpea protein isolate[D]. Shihezi: Shihezi University, 2023.
[25] 周若楠. 预热超声对菠萝蜜种子分离蛋白起泡性及其机制的研究[D]. 南昌:南昌大学, 2021. [ZHOU R N. Study on the foaming properties and its mechanism of jackfruit seed protein isolate induced by preheating and ultrasound treatments[D]. Nanchang:Nanchang University, 2021.] ZHOU R N. Study on the foaming properties and its mechanism of jackfruit seed protein isolate induced by preheating and ultrasound treatments[D]. Nanchang: Nanchang University, 2021.
[26] CHANDRAPALA J, MARTIN G J O, ZISU B, et al. The effect of ultrasound on casein micelle integrity[J]. Journal of Dairy Science,2012,95(12):6882−6890. doi: 10.3168/jds.2012-5318
[27] MADADLOU A, MOUSAVI M E, EMAM-DJOMEH Z, et al. Sonodisruption of re-assembled casein micelles at different pH values[J]. Ultrasonics Sonochemistry,2009,16(5):644−648. doi: 10.1016/j.ultsonch.2008.12.018
[28] 毕爽, 江连洲, 毛惠婷, 等. 超声波处理对大豆分离蛋白—磷脂相互作用及其复合物功能性质的影响[J]. 食品科学,2016(17):1−6. [BI S, JIANG L Z, MAO H T, et al. Effect of ultrasound on soybean protein isolate-phospholipid interaction and functional properties of their composite system[J]. Food Science,2016(17):1−6.] doi: 10.7506/spkx1002-6630-201617001 BI S, JIANG L Z, MAO H T, et al. Effect of ultrasound on soybean protein isolate-phospholipid interaction and functional properties of their composite system[J]. Food Science, 2016(17): 1−6. doi: 10.7506/spkx1002-6630-201617001
[29] TANG C H, WANG X Y, YANG X Q, et al. Formation of soluble aggregates from insoluble commercial soy protein isolate by means of ultrasonic treatment and their gelling properties[J]. Journal of Food Engineering,2009,92(4):432−437. doi: 10.1016/j.jfoodeng.2008.12.017
[30] MCCLEMENTS D J, RAO J. Food-grade nanoemulsions:Formulation, fabrication, properties, performance, biological fate, and potential toxicity[J]. Critical Reviews in Food Science and Nutrition,2011,51(4):285−330. doi: 10.1080/10408398.2011.559558
[31] 茅芝娟, 张昆明, 黄永春, 等. 壳聚糖W/O型乳状液的超声辅助制备及其稳定性[J]. 食品科学,2021,42(2):8−16. [MAO Z J, ZHANG K M, HUANG Y C, et al. Ultrasonic-assisted preparation and stability evaluation of W/O emulsion containing chitosan[J]. Food Science,2021,42(2):8−16.] doi: 10.7506/spkx1002-6630-20191026-296 MAO Z J, ZHANG K M, HUANG Y C, et al. Ultrasonic-assisted preparation and stability evaluation of W/O emulsion containing chitosan[J]. Food Science, 2021, 42(2): 8−16. doi: 10.7506/spkx1002-6630-20191026-296
[32] 仲志峰. 热超声处理对绿豆分离蛋白结构和界面活性及乳化功能的影响[D]. 无锡:江南大学, 2020. [ZHONG Z F. The effect of thermosonication on structural, interfacial, and emulsifying properties of mung bean protein isolate[D]. Wuxi:Jiangnan University, 2020.] ZHONG Z F. The effect of thermosonication on structural, interfacial, and emulsifying properties of mung bean protein isolate[D]. Wuxi: Jiangnan University, 2020.
[33] 齐冬, 王骁, 刘斌, 等. 大豆分离蛋白超声乳化作用机理[J]. 食品科学,2023,44(9):32−38. [QI D, WANG X, LIU B, et al. Mechanistic analysis and application of ultrasonic emulsification of soy protein isolate[J]. Food Science,2023,44(9):32−38.] doi: 10.7506/spkx1002-6630-20220412-139 QI D, WANG X, LIU B, et al. Mechanistic analysis and application of ultrasonic emulsification of soy protein isolate[J]. Food Science, 2023, 44(9): 32−38. doi: 10.7506/spkx1002-6630-20220412-139
[34] 孙颜君, 李志刚, 莫蓓红, 等. 超高压处理对浓缩乳清蛋白80加工性质和蛋白结构的影响[J]. 食品工业科技,2015,36(12):78−82. [SUN Y J, LI Z G, MO B H, et al. Effect of high hydrostatic pressure treatment on the functionality and protein structure of whey protein concentrate80[J]. Science and Technology of Food Industry,2015,36(12):78−82.] SUN Y J, LI Z G, MO B H, et al. Effect of high hydrostatic pressure treatment on the functionality and protein structure of whey protein concentrate80[J]. Science and Technology of Food Industry, 2015, 36(12): 78−82.
[35] LI R, CUI Q, WANG G, et al. Relationship between surface functional properties and flexibility of soy protein isolate-glucose conjugates[J]. Food Hydrocolloids,2019,95:349−357. doi: 10.1016/j.foodhyd.2019.04.030
[36] LIN L, CUI H, HE R, et al. Effect of ultrasonic treatment on the morphology of casein particles[J]. Ultrasonics Sonochemistry,2014,21(2):513−519. doi: 10.1016/j.ultsonch.2013.08.017
[37] BOLONTRADE A J, SCILINGO A A, ANON M C. Amaranth proteins foaming properties:Film rheology and foam stability–Part 2[J]. Colloids and Surfaces B:Biointerfaces,2016,141:643−650. doi: 10.1016/j.colsurfb.2014.10.061
[38] SHARMA P, OEY I, EVERETT D W. Thermal properties of milk fat, xanthine oxidase, caseins and whey proteins in pulsed electric field-treated bovine whole milk[J]. Food Chemistry,2016,207:34−42. doi: 10.1016/j.foodchem.2016.03.076
[39] 邹婕, 王琪, 马美湖, 等. 高场强超声对蛋清液起泡特性的影响[J]. 中国食品学报,2022,22(1):163−171. [ZOU J, WANG Q, MA M H, et al. Effects of high intensity ultrasound on foaming characteristics of egg white liquid[J]. Journal of Chinese Institute of Food Science and Technology,2022,22(1):163−171.] ZOU J, WANG Q, MA M H, et al. Effects of high intensity ultrasound on foaming characteristics of egg white liquid[J]. Journal of Chinese Institute of Food Science and Technology, 2022, 22(1): 163−171.
-
期刊类型引用(3)
1. 张敏杰,杨武德,代叶,李玮,魏晴,梁珊珊. 黔产不同商品规格金钗石斛质量评价研究. 亚太传统医药. 2024(04): 39-43 .  百度学术
百度学术
2. 林鑫静,张明,李鑫,周春阳,蒲跃,袁斌,范艺缤,范润勇,夏天琴,尤俊,杨晓曦,胥正敏. 调脏舒秘合剂小鼠急性毒性实验研究. 现代中医药. 2023(02): 91-95 .  百度学术
百度学术
3. 杨吉容,石京山. 金钗石斛破壁粉对自发性高血压大鼠血压及心功能的影响. 遵义医科大学学报. 2022(06): 699-705 .  百度学术
百度学术
其他类型引用(2)





 下载:
下载:
 下载:
下载:
