Effect of Heat Treatment on the Stability of the Tuna Protein Emulsion
-
摘要: 热处理是影响蛋白乳液稳定性的重要因素,本文研究了不同热处理温度(30、50、70、80、90 ℃,30 min)对金枪鱼蛋白乳液理化性能的影响。结果表明,与未进行热处理的样品相比,经过热处理的蛋白乳液乳化性能发生显著变化(P<0.05)。随着热处理温度的上升,金枪鱼蛋白乳液的表面疏水性、黏度、Zeta电位、乳化活性和乳化稳定性均呈现先增大再减小的趋势。加热温度在30~70 ℃范围内,蛋白二级结构展开,疏水性基团暴露,乳液黏度增大,液滴粒径减小,乳液稳定性增加;加热温度超过70 ℃后,蛋白分子重新聚集,与油滴结合的氨基酸残基重新进入蛋白质内部,液滴出现絮凝现象,乳液也变得不稳定。SDS-PAGE图谱显示70 ℃热处理30 min能够提升油-水界面蛋白质吸附量,液滴分布均匀,粒径达到最小值102.6 nm,黏度达到最大为43.87 Pa·s,贮藏28 d后没有出现乳析现象,乳液状态最稳定。综上,适当的热处理能提升金枪鱼蛋白乳液的稳定性。Abstract: Heat treatment is an important factor affecting the stability of the protein emulsion. This paper investigated the effects of different heat treatment temperature (30, 50, 70, 80 and 90 ℃, 30 min) on the physicochemical properties of tuna protein emulsion. The results showed that the emulsifying property of the heat-treated protein emulsion changed significantly compared with those without heat treatment (P<0.05). Surface hydrophobicity, viscosity, Zeta-potential, emulsifying activity and emulsion stability of tuna protein emulsion increased first and then decreased with the rise of heat treatment temperature. Within 30~70 ℃ of heating, protein secondary structure unfolded, hydrophobic groups exposed, the viscosity of emulsion increased, the particle size of the droplet decreased and the stability of the emulsion increased. After the heating temperature exceeded 70 ℃, the protein molecules reassembled, the amino acid residues bound to the oil droplets reentered the protein interior, the droplets appeared flocculation and the emulsion became unstable. The results of SDS-PAGE illustrated that the amount of protein adsorption at the oil-water interface increased, the droplet distribution was uniform, the particle size reached the minimum value of 102.6 nm, the viscosity reached the maximum of 43.87 Pa·s at 70 ℃ for 30 min. There was no stratification in the emulsion after 28-days of storage and the emulsion had the best stability at this temperature. To sum up, appropriate heat treatment could improve the stability of the tuna protein emulsion.
-
Keywords:
- tuna protein /
- heat treatment /
- emulsion /
- temperature /
- stability
-
金枪鱼富含二十二碳六烯酸(docose hexaenoie acid,DHA)、二十碳五烯酸(eicosapentaenoic acid,EPA)以及人体所需的全部必需氨基酸,营养价值远超普通肉类蛋白和植物蛋白,然而受捕捞和运输条件的限制,金枪鱼产品的应用范围还较为狭窄。有研究证实鱼类蛋白具有阻碍油滴聚集和脂质氧化的功效,在乳液中能够作为乳化剂使用[1]。目前对金枪鱼的研究主要集中于生鱼片的运输贮藏[2]、副产物的分离制备[3]及工艺优化[4]、肌原纤维蛋白凝胶特性[5]等方面,而对金枪鱼蛋白作为乳化剂的研究几乎没有,开展金枪鱼蛋白的研究有助于提高金枪鱼的商业利用率,也可以为海产类食品的应用提供新的资源。
影响蛋白乳液稳定性的因素很多,包括蛋白浓度、油体积分数、pH、离子强度、加工方式[6]等。热处理作为一种乳液加工过程中不可或缺的方法,在提高产品质量、杀菌等各个方面都发挥着不可替代的作用。热处理也是蛋白改性常用的方法之一,加热至变性温度以上通常会导致蛋白质结构的展开和嵌入其中的氨基酸基团暴露[7]。PAN等[8]发现,随着温度升高,鲢鱼肌原纤维蛋白的浑浊度增加,而明度逐渐降低。TRAORE等[9]报告,在100 ℃持续10或30 min可诱导猪肉肌原纤维的氧化、构象变化以及形成蛋白质聚集体。JANTAKOSON等[10]发现在100 ℃预热处理后,斑节对虾的肌肉蛋白具有比未进行预热处理更高的白度值和剪切力。YE[11]通过观察热处理温度对乳清蛋白分离物稳定水包油型(O/W)乳液中界面吸附蛋白组成的影响,发现预热温度的升高会造成吸附的β-乳球蛋白含量增加,但α-乳清蛋白含量降低。
目前,热处理对金枪鱼蛋白乳化性质的影响研究还未见报道,因此本文以金枪鱼蛋白为研究对象,通过测定不同温度热处理时金枪鱼蛋白乳液的乳化活性、乳化稳定性、乳析指数和蛋白组成等理化指标,以及28 d贮藏期内乳液稳定性的变化,探讨热处理对蛋白乳液体系乳化性质的影响,为金枪鱼蛋白在食品乳化体系中的应用提供参考。
1. 材料与方法
1.1 材料与仪器
冷冻金枪鱼柳 浙江融创食品工业有限公司提供;无水乙醇、盐酸、氢氧化钠、无水硫酸铜、氯化钠、氯化钾、磷酸二氢钠、磷酸氢二钠、酒石酸钾钠、乙酸、考马斯亮蓝R-250、十二烷基磺酸钠(SDS) 国药集团化学试剂有限公司;丙烯酰胺 美国BIO-RAD公司;三羟甲基氨基甲烷(Tris) 美国Amresco公司;以上试剂均为分析纯级;牛血清蛋白(BSA) 深圳辉诺生物科技有限公司;蛋白定量(Folin法)测试盒(100T) 北京鼎国生物技术有限责任公司;曲拉通X-100(Triton X-100) 德国Merck公司;其他常规化学试剂或药品均为化学纯或分析纯。
SQP电子天平 赛多利斯科技仪器有限公司;S312-90电动恒速搅拌器 上海梅颖浦仪器仪表制造有限公司;雷磁PHS-3C精密pH计 上海仪电科学仪器股份有限公司;Avanti JXN-30高速冷冻离心机 美国贝克曼库尔特公司;T6-1650E紫外分光光度计 北京普析通用仪器有限责任公司;XHF-DY高速分散器 宁波新芝生物科技股份有限公司;AH210高压均质机 加拿大ATS仪器公司;NDJ-5S旋转黏度计 上海方瑞仪器有限公司;Zetasizer NanoZS90流变仪 江苏岱洛医疗科技有限公司;DF-101S恒温水浴锅 河南省予华仪器有限公司;NanoBrook Omni激光粒度及Zeta电位仪 美国布鲁克海文仪器公司;MICROPHOT-FXA尼康显微镜 日本尼康株式会社;DYY-6C电泳仪 北京六一生物科技有限公司。
1.2 实验方法
1.2.1 金枪鱼蛋白的提取及乳液的制备
参照LI等[12]的方法提取金枪鱼肌原纤维蛋白。将冷冻金枪鱼柳解冻后搅碎,取大约10 g碎肉与40 mL磷酸钠缓冲液(0.02 mol/L,pH7.5)混合均质3次,每次持续90 s。所得匀浆以5000 r/min离心15 min,取沉淀与磷酸钠缓冲液混合,重复离心2次使蛋白充分溶解。向最终沉淀物中加入4倍体积的磷酸钠缓冲液(0.02 mol/L,pH7.0),在相同条件下离心3次,所得上清液中含有金枪鱼肌原纤维蛋白。用双缩脲法测定金枪鱼蛋白溶液质量浓度,以BSA作标准。所有操作均在4 ℃条件下进行。
将制得的蛋白分散在磷酸盐缓冲液(0.05 mmol/L,pH7.0)中配制成质量浓度为5 g/L的蛋白溶液,分散在10 mmol/L柠檬酸-咪唑缓冲液中,加入浓度为0.04%的NaN3避免微生物的繁殖,经水化过夜,向其中加入5%质量比的大豆油,经12000 r/min高速剪切3 min后再以60 MPa均质3次获得状态均一的乳液。分别在30、50、70、80、90 ℃加热乳液30 min,迅速冷却至室温后储存在4 ℃条件下待测,对照组不加热。
1.2.2 表面疏水性测定
根据SINDY等[13]的方法测定并稍加修改。向2 mL蛋白乳液中添加0.4 mL 1 g/L的溴酚蓝,混匀后离心(7000 r/min,15 min),得到的上清液用蒸馏水稀释10倍后测定其吸光度(波长595 nm),用磷酸盐缓冲液做空白对照。根据以下公式计算表面疏水性。
表面疏水性(μg)=200×A1−A2A1 (1) 式中:A1表示空白样的吸光度;A2表示样品的吸光度。
1.2.3 粒径和电位的测定
采用陈艾霖等[14]的方法测定并稍加修改。将10 g蛋白乳液稀释300倍以避免多重散射,利用Zetasizer NanoZS90粒径仪测定乳液粒径和电位,设定温度为25 ℃。样品在4 ℃下贮藏28 d,每隔7 d测定其粒径和电位。
1.2.4 黏度的测定
选用1号转子,将乳液样品放在间距为2.0 mm的30 mm平行板上,在20 ℃下以30 r/min进行测量,时间为60 s。
1.2.5 乳化活性和乳化稳定性的测定
参照LI等[15]的方法测定乳化活性和乳化稳定性。取50 μL蛋白乳液与5 mL 1 g/L的SDS溶液混匀,立即测定波长为500 nm处的吸光度,记作A0,并以SDS溶液做空白对照。样品静置10 min后再次测定吸光度,记作A10。乳化活性(EAI)、乳化稳定性(ESI)的计算公式如下:
EAI(m2/g)=2×2.303×A0×NC×φ×10000 (2) ESI(%)=A0×tA0−A10 (3) 式中:A0表示0 min时的吸光度值;N表示稀释倍数,100;C表示蛋白质量浓度,g/mL;φ表示乳液中大豆油的体积分数,%;t表示时间间隔,10 min;A10表示10 min时的吸光度值。
1.2.6 乳析指数的测定
根据SURH等[16]的方法并稍改动测定乳析指数。用25 mL的玻璃瓶将蛋白乳液密封贮藏28 d(4 ℃),每隔7 d测定瓶中乳液析出清液层的高度(H0)和乳液总高度(H1),并用下式计算乳析指数(CI):
乳析指数(%)=H0H1×100 (4) 式中:H0表示乳液析出层的高度;H1表示乳液总高度。
1.2.7 微观结构的测定
取10 μL乳液均匀滴在载玻片上,确保无气泡后盖上盖玻片,使用光学显微镜在10倍目镜、40倍物镜下观察并拍照。
1.2.8 SDS-PAGE凝胶电泳
参照郝梦等[17]的方法并稍加改动。向100 μL蛋白溶液中加入50 μL上样缓冲液,取10 μL混合液放到由12%分离胶和5%浓缩胶组成的聚丙烯酰胺凝胶上。初始电压设定80 V,进入分离胶后调为120 V,电泳结束后用考马斯亮蓝染色2 h,脱色后观察蛋白质条带变化。
1.3 数据处理
实验结果每组重复3次,结果以平均值±标准差表示。采用Excel 2017、Origin 2018进行数据处理及图像绘制,用SPSS19.0进行单因素方差分析(显著性P<0.05)。
2. 结果与分析
2.1 热处理对金枪鱼蛋白乳液表面疏水性的影响
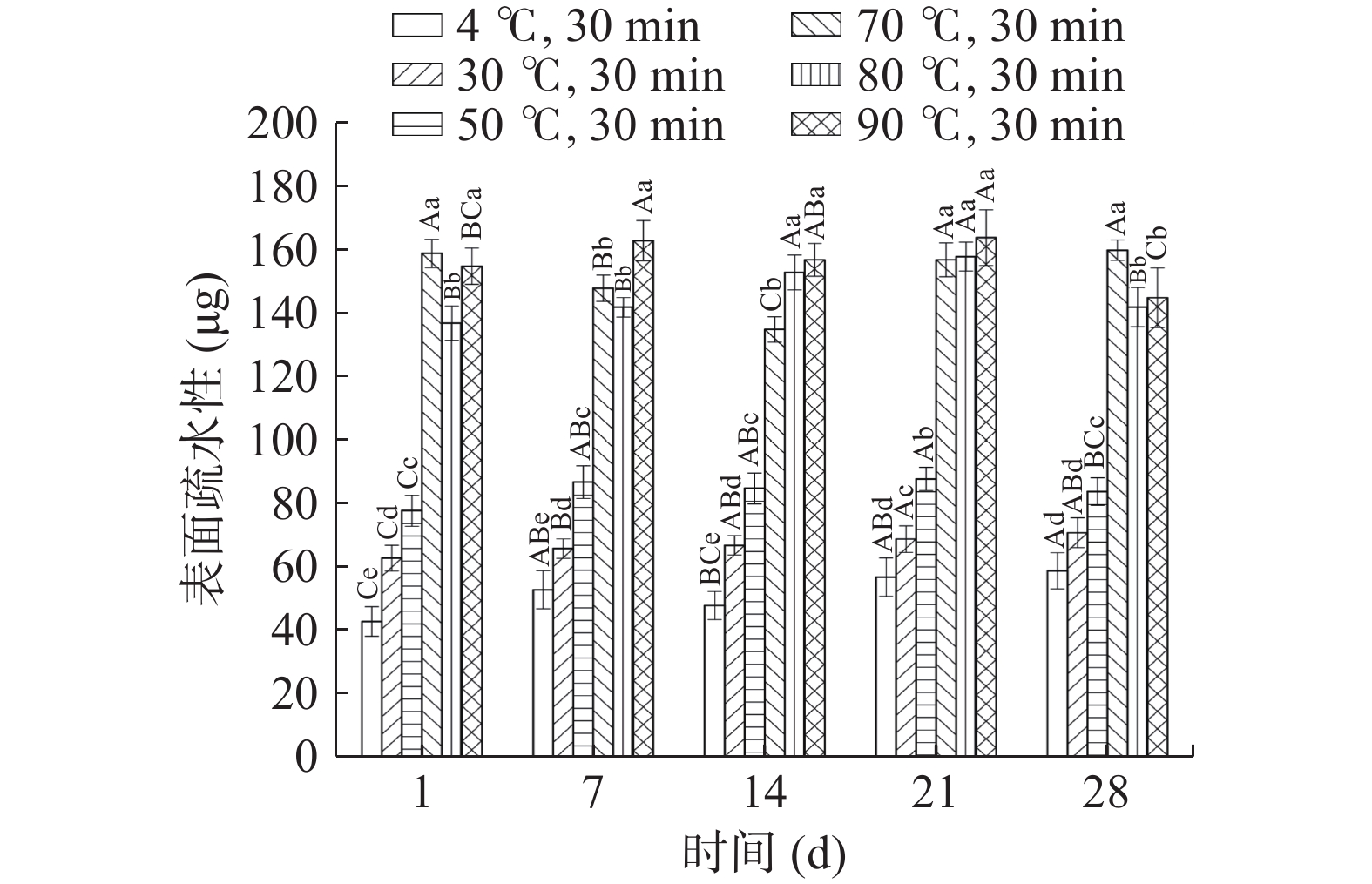
表面疏水性是评估蛋白质变性情况的重要指标,它能够反映出极性环境中蛋白质分子内部氨基酸残基的暴露程度[18]。蛋白质被破坏后,包埋在内部的疏水基团暴露增多,促进蛋白质吸附到油滴表面[19],从而提高乳液体系的表面疏水性。
图1展示了不同热处理条件下金枪鱼蛋白乳液贮藏28 d的表面疏水性变化。热处理温度从30 ℃升至70 ℃的过程中,金枪鱼蛋白表面疏水性有显著上升趋势(P<0.05),这可能是由于在适当的热处理温度下,蛋白分子发生去折叠现象,其内部的疏水氨基酸残基外露。温度继续升高,蛋白质的表面疏水性下降,可能是高温促使肌原纤维蛋白分子聚集成簇,暴露的氨基酸残基重新进入蛋白质内部造成的。郭子璇等[20]在20、60、100 ℃下加热牡蛎蛋白,发现随着温度升高,其表面疏水性系数从初始的17.5升至最大值为21.16,说明蛋白二级结构在加热过程中展开,逐步过渡到三级、四级结构,疏水性基团增多。MA等[21]在研究热处理温度对鳕鱼蛋白理化性质的影响时也发现,随着预热温度从70 ℃升高到80 ℃,鳕鱼蛋白表面疏水性显著增加,在80 ℃时观察到最大值,当温度进一步升高到100 ℃时,表面疏水性降低,与本研究得出的规律相似。每7 d测定样品表面疏水性发现,未经热处理以及30和50 ℃热处理的金枪鱼蛋白乳液表面疏水性数值均显著低于其他热处理组(P<0.05)。贮藏14 d时80和90 ℃热处理的蛋白乳液表面疏水性高于70 ℃热处理的乳液样品,分析其原因可能是在冷藏过程中,蛋白质分子发生改性,其内部的疏水性氨基酸基团暴露。贮藏第28 d时,80和90 ℃热处理的金枪鱼蛋白乳液表面疏水性下降,低于70 ℃热处理组,这是因为在持续低温条件下,被降解的蛋白质小分子借助疏水相互作用重新缔合,暴露的疏水性氨基酸基团又被包埋于更大的蛋白质聚集体内部[22]。
2.2 热处理对金枪鱼蛋白乳液粒径的影响
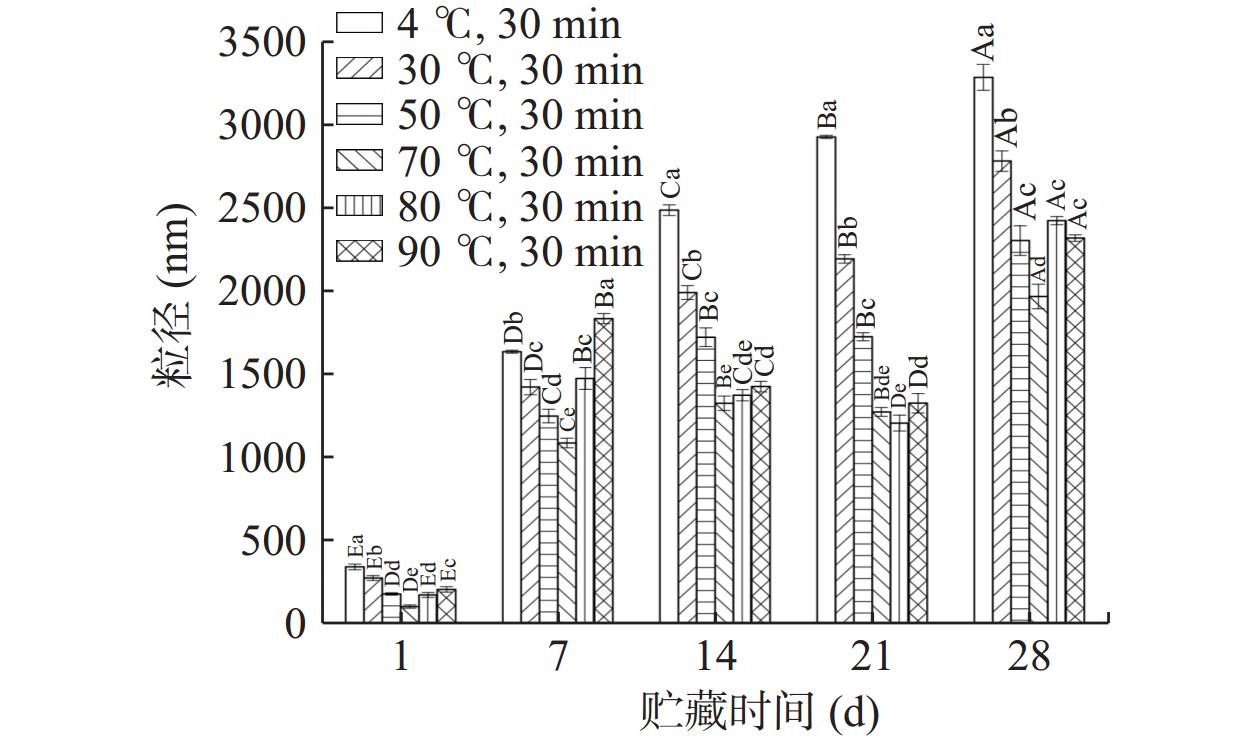
液滴颗粒粒径是评价乳液乳化能力的重要指标之一,乳液体系越稳定,液滴之间越不易聚集,液滴粒径的增幅越缓慢[23]。图2是热处理后贮藏28 d金枪鱼蛋白乳液的粒径变化情况,在相同贮藏天数下的液滴粒径随热处理温度的升高呈现先减小后增大的趋势(P<0.05)。70 ℃加热时蛋白乳液液滴的初始粒径最小为102.6 nm,较未加热组降低了239.4 nm,这说明一定范围内的热处理会提高蛋白分子的疏水相互作用,使液滴保持更长时间的分散[24]。同时加热过程会造成原本被掩藏的一些非极性基团暴露于油-水界面上,使更多的蛋白分子包裹着油滴颗粒,造成颗粒不易结聚或絮凝,乳液稳定性增强[14]。温度高于70 ℃时,乳液粒径增大,这可能是由于在达到一定的温度之后,氨基酸残基与其他分子之间会以氢键和二硫键的方式形成聚集体[25],蛋白质与油滴之间的结合作用被破坏。经4 ℃贮藏28 d后,未加热的金枪鱼蛋白乳液粒径高达3292 nm,较贮藏初始时增加2950 nm;而经过30、50、70、80和90 ℃加热的蛋白乳液粒径分别增加了2512.33、2130、1869.4、2255.62、2117.64 nm,增幅较未加热组更为缓慢,其中70 ℃加热的蛋白乳液粒径变化最小,可能是加热后的乳液黏度增加,液滴颗粒的聚集受阻。SHAO等[26]测试14 d贮藏期内不同浓度及热处理条件下大豆分离蛋白的稳定性,发现经加热处理后,各浓度下的蛋白乳液都表现出了比未加热样品更优良的抗聚集性和稳定性。这说明加热处理蛋白乳液能够增大液滴的空间位阻,降低液滴间碰撞次数,从而达到减少液滴聚集的目的[27]。热处理温度为70 ℃的金枪鱼蛋白乳液粒径最小,贮藏过程中的增幅最慢,证明稳定性最好。
2.3 热处理对金枪鱼蛋白乳液电位和黏度的影响
Zeta电位与乳液液滴间的相互排斥或吸引有关,能够表征蛋白质表面的电荷量,可用来指示乳化体系的稳定性[28]。Zeta电位的绝对值代表其稳定性大小,绝对值越大,表示体系越趋于稳定[29];正负代表粒子带何种电荷,若蛋白质表面带正电的氨基酸基团数目多于带负电基团数时,该值为正,反之为负。
表1为不同热处理条件下金枪鱼蛋白乳液的电位和黏度变化情况。Zeta电位绝对值在升温过程中变化显著(P<0.05),从30 ℃的23.39 mV增至70 ℃的29.87 mV,这种现象可能是因为加热改变了蛋白质分子构象,无规则卷曲增加,带电基团和氨基酸残基暴露到蛋白质分子表面,增强了液滴互斥作用,使其不易聚集[30−31],使乳液体系更加稳定。ZHAO等[32]通过对谷蛋白进行热处理,发现经100 ℃加热60 min后谷蛋白表面电位绝对值显著增大,这与本研究结果一致,说明带负电氨基酸基团的暴露能够增强蛋白分子柔性,使乳液趋于稳定。温度继续上升,乳液表面电位绝对值却降低,分析其原因可能是高温使更多带正电荷的基团暴露,减轻了液滴间的静电排斥作用[33],加剧乳液絮凝现象的产生。
表 1 热处理对金枪鱼蛋白乳液电位和黏度的影响Table 1. Effect of heat treatment on the potential and viscosity of the tuna protein emulsion组别 电位(mV) 黏度(Pa·s) 4 ℃ −19.23±0.65d 13.29±0.44f 30 ℃,30 min −23.39±0.49c 15.74±0.74e 50 ℃,30 min −25.38±1.22c 29.28±1.02c 70 ℃,30 min −29.87±1.24a 43.87±1.56a 80 ℃,30 min −26.98±1.06b 37.38±1.33b 90 ℃,30 min −24.65±0.32c 26.29±0.24d 注:同列不同上标小写字母表示差异显著(P<0.05)。 由表1中可以看出,经过热处理后的金枪鱼蛋白乳液黏度值显著提高(P<0.05),其中70 ℃热处理的乳液黏度最大为43.87 Pa·s,这表明Zeta电位和黏度之间存在一定关联性,温度升高造成液滴间静电排斥力增大,推迟了液滴絮凝或聚集的时间,乳液的黏度和稳定性得以提升[34]。同时,加热能够使某些疏水基团暴露,在液滴表面形成一层致密的膜状结构[14],令油滴与蛋白质的结合能力增强,黏度增大。随着温度继续上升至80、90 ℃,乳液表面黏度降低,这表明蛋白质结构变得无序,蛋白质分子与油滴间的疏水相互作用被破坏,油滴聚集或絮凝现象增多,这与YAN等[19]的研究结果一致。
2.4 热处理对金枪鱼蛋白乳液乳化活性和乳化稳定性的影响
蛋白质的乳化性是一种重要功能特性,指的是油和水结合形成乳化液的能力,能够表征蛋白质分子间以及蛋白质与脂肪的结合能力。乳化活性是指在油水混合过程中,蛋白质作为乳化剂能够保持油-水界面稳定的程度;乳化稳定性是指蛋白质抵抗外界因素加速乳化体系分层的能力[35],这两个指标最常用于评价蛋白质的乳化性。
在不同的加热温度下,金枪鱼蛋白的乳化活性和乳化稳定性的变化趋势如图3所示。随着温度上升,金枪鱼蛋白乳液的EAI值和ESI值的变化趋势均为先升后降,50 ℃和70 ℃时EAI值没有显著区别(P>0.05),均大于其他处理组,70 ℃时ESI值最大,此时液滴颗粒较小,没有明显絮凝现象。这个发现与刘慧清[36]的研究结果一致,分析其原因可能是随着加热温度升高,蛋白质二级结构展开,更多的疏水基团暴露出来覆盖在油滴表面,界面处的蛋白吸附量增多,导致液滴不易聚集或絮凝,乳液也不易分层。但是当温度超过一定范围时,蛋白分子热运动加剧,蛋白空间结构遭到破坏,溶解度和疏水性受到影响,絮凝和聚集现象加剧[35],乳化活性和乳化稳定性随之降低。LIU等[37]在研究热处理对紫苏蛋白乳化性质时也发现,经70~90 ℃热处理的蛋白乳液稳定性较好,但当温度超过90 ℃时乳液显示出较差的稳定性。
2.5 热处理对金枪鱼蛋白乳液乳析指数的影响
蛋白乳液的乳析现象又被称为分层现象,是由水油两相的密度不同造成的,两相密度差越大,液滴颗粒粒径越大,外相黏度越小,越易发生分层现象。因此乳析指数可以用来表征乳液稳定性,乳析指数越小,乳液稳定性越好。
金枪鱼蛋白乳液经过不同温度热处理后贮藏28 d的乳析指数变化情况如图4所示。各温度条件处理下的蛋白乳液乳析指数均随着贮藏时间的增加而升高,没有进行热处理的乳液乳析指数在储存1 d后已经超过38%,说明乳化体系不稳定;相较之下,50~80 ℃加热时的乳液乳析指数显著降低(P<0.05),在贮藏28 d后仍保持稳定未分层,这可能是由于经过加热的蛋白乳液黏度增大,颗粒粒径减小,界面处吸附的蛋白质增多,表面张力下降,液滴聚集程度下降。70 ℃处的乳液乳析指数在7~28 d任一贮藏节点内均显著低于其它组(P<0.05),此时金枪鱼蛋白乳液黏度最大,粒径最小,粒度分布均匀,电位绝对值最高,液滴所带电荷数目达到最多,液滴间的互斥作用明显增强。彭伟伟[6]研究豌豆蛋白经过50~100 ℃热处理后的乳液分层情况,发现热处理后的乳液乳析指数均低于未经过热处理的样品,在14 d贮藏期内不易发生分层现象。陈艾霖等[14]对罗非鱼分离蛋白乳液热处理后的稳定性变化研究也证实了这个推论。以上结果再次证实合适的热处理可以提高乳液的稳定性,有助于延长贮藏时间。
2.6 热处理对金枪鱼蛋白乳液微观结构的影响
对金枪鱼蛋白乳液进行不同温度热处理后观察其液滴的微观结构,结果如图5所示。未加热和加热处理的乳液中均能观察到较大尺寸的油滴,证明乳液中始终存在未被吸附的蛋白质分子。热处理前的乳液液滴粒径较大,且呈无规则排布。经过50和70 ℃加热的乳液液滴粒径变小,液滴的聚集情况减少;在80和90 ℃加热30 min后,乳液中的一些液滴再次出现了聚结、絮凝现象。这与2.2中乳液颗粒粒径会随着加热温度的上升呈现出先减小再增大的变化规律相吻合,这说明在一定的温度范围内加热金枪鱼蛋白乳液能够降低其油-水界面的张力,增大黏度,增强液滴间的静电排斥作用,使得液滴不易凝结;而如果受热温度过高,则会使乳液液滴丧失抗聚集的能力[38],重新聚集成为较大的颗粒。
2.7 热处理对金枪鱼乳液蛋白组成的影响
为了研究不同温度热处理对金枪鱼肌原纤维蛋白吸附能力的影响,利用SDS-PAGE分别检测未加热以及在30、50、70、80、90 ℃加热的金枪鱼蛋白分子量,结果如图6所示。与标准蛋白分子质量SDS-PAGE图对比后发现,在各组样品中,界面蛋白膜的主要成分为肌球蛋白重链(200 kDa)、C-蛋白(135~150 kDa)、肌动蛋白(41~61 kDa)、原肌球蛋白(34~36 kDa)[39]。当加热温度从30 ℃上升到70 ℃时,肌球蛋白重链和肌动蛋白条带颜色逐渐加深,这可能是由于经过适当热处理后的金枪鱼蛋白表面疏水性升高,其内部的氨基酸残基暴露并与油滴结合,使油-水界面处的蛋白吸附量大大增高。温度继续上升至80、90 ℃时,电泳条带颜色明显变浅,这与2.1中得出的金枪鱼蛋白乳液表面疏水性结论一致,进一步证明70 ℃热处理可以获得更大的界面蛋白吸附量。潘成磊等[35]比较不同加热温度对猪肝水溶性蛋白-大豆油乳化体系吸附蛋白含量的差异,发现随着温度的上升,电泳条带的颜色先变深再变浅,条带数目先增多再减少,界面蛋白吸附量同样呈现先上升再下降的趋势。
3. 结论
金枪鱼蛋白具备丰富的营养价值和优良的功能特性,属于优质蛋白源。本实验研究结果显示,与未进行热处理相比,经过热处理后的金枪鱼蛋白乳液的蛋白质二级结构显著改变,无规则卷曲增加,疏水基团和氨基酸残基暴露于液滴表面,液滴之间的互斥作用增强,不易发生絮凝现象。随着热处理温度上升,金枪鱼蛋白乳液的表面疏水性、黏度、Zeta电位、乳化活性和乳化稳定性等指标均呈现先上升后下降的趋势,液滴粒径则是先减小再增大。70 ℃热处理时,金枪鱼蛋白乳液的各项指标整体优于其他组,且贮藏28 d未出现分层情况,从SDS-PAGE图也可以看出此温度下的条带颜色明显加深,乳化体系界面蛋白吸附量高于其他温度热处理的样品。80、90 ℃热处理后液滴重新聚集,不利于乳液稳定。因此得出结论,选择70 ℃作为金枪鱼蛋白乳液的热处理温度最为适宜。此结论为金枪鱼蛋白的合理利用和相关产品的研发加工提供了理论依据,对丰富金枪鱼副产品市场具有积极作用。
-
表 1 热处理对金枪鱼蛋白乳液电位和黏度的影响
Table 1 Effect of heat treatment on the potential and viscosity of the tuna protein emulsion
组别 电位(mV) 黏度(Pa·s) 4 ℃ −19.23±0.65d 13.29±0.44f 30 ℃,30 min −23.39±0.49c 15.74±0.74e 50 ℃,30 min −25.38±1.22c 29.28±1.02c 70 ℃,30 min −29.87±1.24a 43.87±1.56a 80 ℃,30 min −26.98±1.06b 37.38±1.33b 90 ℃,30 min −24.65±0.32c 26.29±0.24d 注:同列不同上标小写字母表示差异显著(P<0.05)。 -
[1] CHALAMAIAH M, DINESH KUMAR B, HEMALATHA R, et al. Fish protein hydrolysates:Proximate composition, amino acid composition, antioxidant activities and applications:A review[J]. Food Chemistry,2012,135(4):3020−3038. doi: 10.1016/j.foodchem.2012.06.100
[2] 姜晓娜. 模拟物流过程中黄鳍金枪鱼品质变化的研究[D]. 杭州:浙江工商大学, 2018. [JIANG X N. Study on the quality change of yellowfin tuna in simulated logistics process[D]. Hangzhou:Zhejiang Gongshang University, 2018.] JIANG X N. Study on the quality change of yellowfin tuna in simulated logistics process[D]. Hangzhou: Zhejiang Gongshang University, 2018.
[3] 戴铭锐. 金枪鱼多肽的理化特性及其与海藻酸钠的自组装研究[D]. 广州:广州大学, 2019. [DAI M R. Physicochemical properties of tuna peptides and their self-assembly with sodium alginate[D]. Guangzhou:Guangzhou University, 2019.] DAI M R. Physicochemical properties of tuna peptides and their self-assembly with sodium alginate[D]. Guangzhou: Guangzhou University, 2019.
[4] 杨会成, 胡世伟, 周小敏, 等. 金枪鱼骨胶原蛋白肽螯合钙制备工艺及对MG-63细胞碱性磷酸酶分泌的影响[J]. 中国海洋药物,2020,39(1):9−18. [YANG H C, HU S W, ZHOU X M, et al. Preparation of collagen peptide from tuna bone chelated calcium and its effect on alkaline phosphatase secretion in MG-63 cells[J]. Chinese Journal of Marine Drugs,2020,39(1):9−18.] YANG H C, HU S W, ZHOU X M, et al. Preparation of collagen peptide from tuna bone chelated calcium and its effect on alkaline phosphatase secretion in MG-63 cells[J]. Chinese Journal of Marine Drugs, 2020, 39(1): 9−18.
[5] 孙攀. 超声波处理对金枪鱼肌原纤维蛋白理化特性、结构和凝胶特性的影响[D]. 锦州:渤海大学, 2019. [SUN P. Effects of ultrasonic treatment on physico-chemical properties, structure and gel properties of tuna (Thunnus tonggol) myofibrilla protrins[D]. Jinzhou:Bohai University, 2019.] SUN P. Effects of ultrasonic treatment on physico-chemical properties, structure and gel properties of tuna (Thunnus tonggol) myofibrilla protrins[D]. Jinzhou: Bohai University, 2019.
[6] 彭伟伟. 热处理对豌豆蛋白乳化性质及界面吸附行为的影响[D]. 无锡:江南大学, 2016. [PENG W W. Effect of heat treatment on the emulsifying property and interfacial adsorption behavior of pea proteins[D]. Wuxi:Jiangnan University, 2016.] PENG W W. Effect of heat treatment on the emulsifying property and interfacial adsorption behavior of pea proteins[D]. Wuxi: Jiangnan University, 2016.
[7] WANG J M, XIA N, YANG X Q, et al. Adsorption and dilatational rheology of heat-treated soy protein at the oil-water interface:Relationship to structural properties[J]. Journal of Agricultural and Food Chemistry,2012,60(12):3302−3310. doi: 10.1021/jf205128v
[8] PAN J, SHEN H X, YOU J, et al. Changes in physiochemical properties of myofibrillar protein from silver carp (Hypophthalmichthys mollitrix) during heat treatment[J]. Journal of Food Biochemistry,2011,35(3):939−952. doi: 10.1111/j.1745-4514.2010.00431.x
[9] TRAORE S, AUBRY L, GATELLIER P, et al. Effect of heat treatment on protein oxidation in pig meat[J]. Meat Science,2012,91(1):14−21. doi: 10.1016/j.meatsci.2011.11.037
[10] JANTAKOSON T, KIJROONGROJANA K, BENJAKUL S, et al. Effect of high pressure and heat treatments on black tiger shrimp (Penaeus monodon Fabricius) muscle protein[J]. International Aquatic Research,2012,4(1):1−2. doi: 10.1186/2008-6970-4-1
[11] YE A Q. Surface protein composition and concentration of whey protein isolate-stabilized oil-in-water emulsions:Effect of heat treatment[J]. Colloids and Surfaces B:Biointerfaces,2010,78(1):24−29. doi: 10.1016/j.colsurfb.2010.02.001
[12] LI X X, SUN P, MA Y Y. Effect of ultrasonic thawing on the water-holding capacity, physicochemical properties and structure of frozen tuna (Thunnus tonggol) myofibrillar proteins[J]. Journal of the Science of Food and Agriculture,2019,99(11):5083−5091. doi: 10.1002/jsfa.9752
[13] SINDY P S, KU K M, DONG M Y, et al. Adhesion and removal of E. coli K12 as affected by leafy green produce epicuticular wax composition, surface roughness, produce and bacterial surface hydrophobicity, and sanitizers[J]. International Journal of Food Microbiology,2020,334:108834. doi: 10.1016/j.ijfoodmicro.2020.108834
[14] 陈艾霖, 刘璐, 宋春勇, 等. 热处理对罗非鱼分离蛋白乳液稳定性的影响[J]. 广东海洋大学学报,2021,41(5):94−100. [CHEN A L, LIU L, SONG C Y, et al. Improving the stability of tilapia protein isolate emulsion by heat treatment[J]. Journal of Guangdong Ocean University,2021,41(5):94−100.] doi: 10.3969/j.issn.1673-9159.2021.05.012 CHEN A L, LIU L, SONG C Y, et al. Improving the stability of tilapia protein isolate emulsion by heat treatment[J]. Journal of Guangdong Ocean University, 2021, 41(5): 94−100. doi: 10.3969/j.issn.1673-9159.2021.05.012
[15] LI Y Y, KONG B H, LIU Q, et al. Improvement of the emulsifying and oxidative stability of myofibrillar protein prepared oil-in-water emulsions by addition of zein hydrolysates[J]. Process Biochemistry,2016,53:116−124.
[16] SURH J, DECKER E A, MCLEMENTS D J. Influence of pH and pectin type on properties and stability of sodium-caseinate stabilized oil-in-water emulsions[J]. Food Hydrocolloids,2005,20(5):607−618.
[17] 郝梦, 毛书灿, 周志, 等. 热处理和蛋白浓度对肌原纤维蛋白乳液的稳定性和流变特性的影响[J]. 食品工业科技,2022,43(23):56−63. [HAO M, MAO S C, ZHOU Z, et al. Effect of heat treatment and protein concentration on the stability and rheological properties of myofibrillillin emulsion[J]. Science and Technology of Food Industry,2022,43(23):56−63.] HAO M, MAO S C, ZHOU Z, et al. Effect of heat treatment and protein concentration on the stability and rheological properties of myofibrillillin emulsion[J]. Science and Technology of Food Industry, 2022, 43(23): 56−63.
[18] 贾娜, 林世文, 王乐田, 等. 没食子酸诱导肌原纤维蛋白巯基含量和表面疏水性变化对蛋白凝胶特性的影响[J]. 食品科学,2020,41(22):1−7. [JIA N, LIN S W, WANG L T, et al. Effect of changes in sulfhydryl content and surface hydrophobicity of myofibrillar protein induced by gallic acid on its gel properties[J]. Food Science,2020,41(22):1−7.] doi: 10.7506/spkx1002-6630-20190829-323 JIA N, LIN S W, WANG L T, et al. Effect of changes in sulfhydryl content and surface hydrophobicity of myofibrillar protein induced by gallic acid on its gel properties[J]. Food Science, 2020, 41(22): 1−7. doi: 10.7506/spkx1002-6630-20190829-323
[19] YAN X H, ZHAO J X, ZENG Z L, et al. Effects of preheat treatment and polyphenol grafting on the structural, emulsifying and rheological properties of protein isolate from Cinnamomum camphora seed kernel[J]. Food Chemistry,2022,377:132044. doi: 10.1016/j.foodchem.2022.132044
[20] 郭子璇, 陈慧, 王震宇, 等. 热处理对牡蛎蛋白结构及功能特性的影响[J]. 大连工业大学学报,2020,39(4):235−240. [GUO Z X, CHEN H, WANG Z Y, et al. Effect of heat treatment on the structure and functional properties of oyster protein[J]. Journal of Dalian Polytechnic University,2020,39(4):235−240.] GUO Z X, CHEN H, WANG Z Y, et al. Effect of heat treatment on the structure and functional properties of oyster protein[J]. Journal of Dalian Polytechnic University, 2020, 39(4): 235−240.
[21] MA W C, WANG J M, WU D. Effects of preheat treatment on the physicochemical and interfacial properties of cod proteins and its relation to the stability of subsequent emulsions[J]. Food Hydrocolloids,2021,112:106338. doi: 10.1016/j.foodhyd.2020.106338
[22] 王发祥, 张付兰, 刘永乐, 等. 草鱼冷藏过程中肌原纤维蛋白的变化[J]. 食品工业科技,2015,36(18):82−86. [WANG F X, ZHANG F L, LIU Y L, et al. Changes in myofibrillar proteins of grass carp during chilling storage[J]. Science and Technology of Food Industry,2015,36(18):82−86.] WANG F X, ZHANG F L, LIU Y L, et al. Changes in myofibrillar proteins of grass carp during chilling storage[J]. Science and Technology of Food Industry, 2015, 36(18): 82−86.
[23] 李欢欢, 陈伊凡, 张晋, 等. 热处理对酶解蛋黄液功能特性和热稳定性的影响[J]. 中国食品学报,2020,20(10):105−114. [LI H H, CHEN Y F, ZHANG J, et al. Effect of heat treatment on the functional properties and thermal stability of liquid egg yolk hydrolyzed with trypsin[J]. Journal of Chinese Institute of Food Science and Technology,2020,20(10):105−114.] LI H H, CHEN Y F, ZHANG J, et al. Effect of heat treatment on the functional properties and thermal stability of liquid egg yolk hydrolyzed with trypsin[J]. Journal of Chinese Institute of Food Science and Technology, 2020, 20(10): 105−114.
[24] SLIWINSKI E L, ROUBOS P J, ZOET F D, et al. Effects of heat on physicochemical properties of whey protein-stabilised emulsions[J]. Colloids and Surfaces B:Biointerfaces,2003,31(1):231−242.
[25] SOURDET S, RELKIN P, CESAR B. Effects of milk protein type and pre-heating on physical stability of whipped and frozen emulsions[J]. Colloids and Surfaces B:Biointerfaces,2003,31(1):55−64.
[26] SHAO Y, TANG C H. Characteristics and oxidative stability of soy protein-stabilized oil-in-water emulsions:Influence of ionic strength and heat pretreatment[J]. Food Hydrocolloids,2013,37:149−158.
[27] LI Q Y, ZHAO Z T. Interfacial characteristics, colloidal properties and storage stability of dairy protein-stabilized emulsion as a function of heating and homogenization[J]. RSC Advances,2020,10(20):11883−11891.
[28] SUI X N, BI S, QI B K, et al. Impact of ultrasonic treatment on an emulsion system stabilized with soybean protein isolate and lecithin:Its emulsifying property and emulsion stability[J]. Food Hydrocolloids,2017,63:727−734.
[29] BOUZID H, BAUDRY M R, PAUGAM L, et al. Impact of zeta potential and size of caseins as precursors of fouling deposit on limiting and critical fluxes in spiral ultrafiltration of modified skim milks[J]. Journal of Membrane Science,2008,314(1):67−75.
[30] 黄雯婷, 茅宇虹, 蔡珍玲, 等. 不同条件下乳清蛋白水解物乳化性的变化及机理分析[J]. 中国食品学报,2023,23(3):99−110. [HUANG W T, MAO Y T, CAI Z L, et al. The changes and mechanism of the emulsifying properties of whey protein hydrolysates at various conditions[J]. Journal of Chinese Institute of Food Science and Technology,2023,23(3):99−110.] HUANG W T, MAO Y T, CAI Z L, et al. The changes and mechanism of the emulsifying properties of whey protein hydrolysates at various conditions[J]. Journal of Chinese Institute of Food Science and Technology, 2023, 23(3): 99−110.
[31] LIU C H, WANG R C, HE S H, et al. The stability and gastro-intestinal digestion of curcumin emulsion stabilized with soybean oil bodies[J]. LWT,2020,131:109663. doi: 10.1016/j.lwt.2020.109663
[32] ZHAO M, XIONG W F, CHEN B X, et al. Enhancing the solubility and foam ability of rice glutelin by heat treatment at pH12:Insight into protein structure[J]. Food Hydrocolloids,2020,103(C):105626.
[33] 齐宝坤, 赵城彬, 江连洲, 等. 不同热处理温度下大豆11S球蛋白Zeta电位、粒径和红外光谱分析[J]. 食品科学,2018,39(24):54−58. [QI B K, ZHAO C B, JIANG L Z, et al. Analysis of Zeta potential, particle size and infrared spectroscopy of 11S glycinin at different heat treatment temperatures[J]. Food Science,2018,39(24):54−58.] doi: 10.7506/spkx1002-6630-201824009 QI B K, ZHAO C B, JIANG L Z, et al. Analysis of Zeta potential, particle size and infrared spectroscopy of 11S glycinin at different heat treatment temperatures[J]. Food Science, 2018, 39(24): 54−58. doi: 10.7506/spkx1002-6630-201824009
[34] KUMAR K, NIKOLIA A D, WASAN D T. Mechanisms of stabilization of water-in-crude oil emulsions[J]. Industrial & Engineering Chemistry Research,2001,40(14):3009−3014.
[35] 潘成磊, 丁景, 董唯, 等. 热处理温度对猪肝水溶性蛋白乳化性质的影响[J]. 食品与发酵工业,2019,45(16):82−89. [PAN C L, DING J, DONG W, et al. Effect of heat treatment temperature on emulsifying properties of water-soluble proteins in pig liver[J]. Food and Fermentation Industries,2019,45(16):82−89.] PAN C L, DING J, DONG W, et al. Effect of heat treatment temperature on emulsifying properties of water-soluble proteins in pig liver[J]. Food and Fermentation Industries, 2019, 45(16): 82−89.
[36] 刘慧清. 罗非鱼蛋白乳化特性的研究[D]. 湛江:广东海洋大学, 2013. [LIU H Q. Study on emulsifying properties of protein from tilapia[D]. Zhanjiang:Guangdong Ocean University, 2013.] LIU H Q. Study on emulsifying properties of protein from tilapia[D]. Zhanjiang: Guangdong Ocean University, 2013.
[37] LIU N, CHEN Q N, LI G H, et al. Properties and stability of perilla seed protein-stabilized oil-in-water emulsions:Influence of protein concentration, pH, NaCl concentration and thermal treatment[J]. Molecules,2018,23(7):1533−1533. doi: 10.3390/molecules23071533
[38] 肖丁浩. pH值调节和热处理改善罗非鱼-大豆共沉淀蛋白乳液的稳定性及茶皂素的影响研究[D]. 湛江:广东海洋大学, 2022. [XIAO D H. Study on improvement of the stability of tilapia-soybean co-precipitated protein emulsion by pH and heat treatment and effect of tea saponin[D]. Zhanjiang:Guangdong Ocean University, 2022.] XIAO D H. Study on improvement of the stability of tilapia-soybean co-precipitated protein emulsion by pH and heat treatment and effect of tea saponin[D]. Zhanjiang: Guangdong Ocean University, 2022.
[39] 康鹏, 雷晓民, 葛武鹏, 等. 不同巴氏杀菌处理对绵羊乳总蛋白及乳清蛋白二级结构的影响[J]. 食品安全质量检测学报,2021,12(23):9219−9225. [KANG P, LEI X M, GE W P, et al. Effects of different pasteurization treatments on the secondary structure of total proteins and whey protein in sheep milk[J]. Journal of Food Safety & Quality,2021,12(23):9219−9225.] doi: 10.3969/j.issn.2095-0381.2021.23.spaqzljcjs202123034 KANG P, LEI X M, GE W P, et al. Effects of different pasteurization treatments on the secondary structure of total proteins and whey protein in sheep milk[J]. Journal of Food Safety & Quality, 2021, 12(23): 9219−9225. doi: 10.3969/j.issn.2095-0381.2021.23.spaqzljcjs202123034
-
期刊类型引用(2)
1. 张黎梅,汪云飞,陈艳,董天秋,马文思,陈娴. HPLC-DAD法测定养生茶中的双氯芬酸钠. 食品与发酵科技. 2025(01): 169-172 .  百度学术
百度学术
2. 李肖斐. 超高效液相色谱-串联质谱法测定酵素梅中12种酚汀(酚丁)、酚酞及其酯类衍生物或类似物. 食品安全导刊. 2025(07): 105-109 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:




 下载:
下载:



