Optimization of Purification Process of Konjac Glucomannan by Response Surface Methodology
-
摘要: 魔芋粉中脂肪、蛋白质等限制魔芋葡甘聚糖的应用,因此对魔芋粉进行纯化处理得到纯度更高的魔芋葡甘聚糖应用于食品、药品等产业。本研究采用乙醇作为溶剂,对利用超声波辅助纯化魔芋粉的工艺进行优化。经过单因素实验分析料液比、乙醇浓度、超声时间、超声功率、超声温度5个相关因素的显著性,选择料液比、乙醇浓度和超声时间为较显著的因子进行分析。而后通过响应面拟合模型对各相关因素进行优化,最终确定在料液比1:102(g/mL)、乙醇浓度73%、超声时间55 min、超声功率175 W、超声温度50 ℃条件下,魔芋葡甘聚糖含量为88.1%,与预测值相近,纯化工艺切实可行。利用红外光谱仪和X射线衍射仪测定优化前后样品结构,未发现明显差异。经该工艺纯化后的魔芋粉中魔芋葡甘聚糖含量明显高于未纯化魔芋粉,且结构受影响较小,本文旨在为魔芋葡甘聚糖的高效开发和利用提供理论依据。Abstract: The fat, protein and other compounds in konjac powder limit the application of konjac glucomannan. Konjac glucomannan with relatively high purity could be applied in food, medicine and other sectors. This research aimed to optimize the ultrasonic assisted purification process of glucomannan from konjac powder with ethanol. The significance effects of five relevant factors including the ratio of konjac powder to ethanol, ethanol concentration, ultrasonic time, power and temperature were analyzed based on single factor analysis of variance. The first three aforementioned factors were selected for further analysis their significant effects on the purity of glucomannan. Moreover, the relevant factors were optimized via response surface model fitting. The final optimized parameters were as follows: 1:102 (g/mL) for the ratio of konjac powder to ethanol, 73% ethanol, 55 min ultrasonic time, 175 W ultrasonic power, 50 ℃ ultrasonic temperature. The content of konjac glucomannan under the process condition was 88.1%, which was close to the predicted value, and the purification process of glucomannan from konjac powder was feasible. The structure of the samples before and after optimization were measured by infrared spectroscopy and X-ray diffraction with no significant difference. The content of konjac glucomannan in the purified konjac powder by this process was significantly higher than that in the unpurified one, and the structure was less affected. Results from this study could provide theoretical support for efficient utilization of konjac glucomannan and development of relevant functional products.
-
Keywords:
- response surface /
- ultrasonic /
- konjac glucomannan /
- purity
-
魔芋是一种多年生草本植物,主要生长在位于亚洲东南部亚热带的山区或丘陵地带[1],在我国广泛种植于陕西、甘肃以及云、贵、川等地,是我国重要的经济作物[2−3]。魔芋中含有不溶性淀粉、纤维素、蛋白质以及脂类[4],其主要食用部位是球状块茎。魔芋葡甘聚糖(Konjac Glucommannan,KGM)作为球状块茎中占比最多的成分,含量可达到50%以上[5−6],KGM含量也常用作评价魔芋粉质量优劣的关键指标[7]。
KGM由葡萄糖和甘露糖结合构成[8−9],可作为天然的食品防腐剂用于防止食品变质以及虫害[10],也能够预防多种慢性疾病,包括降低血糖、胆固醇、甘油三酯和血压水平[11]等,还能通过调节新陈代谢、改善胃肠道环境、增加有益菌、增强饱腹感以达到减肥的目的[12−13],现已被应用于临床医药等领域[14−15]。此外KGM还具有水溶性好、胶凝性极佳、生物可降解性强等诸多优良特性[16−17],许多文献也报道过其在食品包装膜方面的进展[18−20],已被引入许多国家用作食品添加剂和膳食补充剂,在食品、医药、化工[21−24]等领域均具有很好的应用价值,因此提高KGM含量的研究对研发和应用具有重要意义。
目前KGM的纯化方法大致包括乙醇沉淀法、生物酶法、Pb(AC)2法等,但存在引入重金属离子、KGM得率较低、操作复杂且效率低下等问题,限制其应用于食品产业加工[25−26]。由于KGM具有易溶于水而不溶于有机溶剂的特点[27],本研究采用超声波辅助乙醇沉淀法进行纯化[28],运用响应面试验设计出魔芋粉中KGM的最优纯化条件,测定得率,并通过傅立叶红外光谱仪(FT-IR)和X射线衍射仪(XRD)对其优化前后的结构进行表征,以期为KGM的进一步开发和利用提供理论基础和思路借鉴。
1. 材料与方法
1.1 材料与仪器
魔芋粉 湖南省好味屋食品有限公司;硫酸、氢氧化钠、无水乙醇、溴化钾 均为分析纯,国药集团化学试剂有限公司;葡萄糖标准溶液 中国氪道试剂公司;DNS显色液 中国飞净生物科技有限公司。
1510-02624全波长高速酶标仪 赛默飞世尔科技中国有限公司;101-2AB型电热鼓风干燥箱 天津市泰斯特仪器有限公司;S-LC电热恒温水浴锅 北京市永光明医疗仪器有限公司;BS224S电子天平 赛多利斯科学仪器北京有限公司;KH-250DE型数控超声波清洗器 昆山禾创超声仪器有限公司;LD5-2A离心机 北京雷勃尔离心机有限公司;IRAffinity-1傅立叶红外光谱仪、XRD-6000型X射线衍射仪 日本岛津公司。
1.2 实验方法
1.2.1 葡萄糖标准曲线的制作
分别移取0、0.4、0.8、1.2、1.6、2.0 mL的1 mg/mL葡萄糖标准溶液于6个25 mL具塞试管中并用蒸馏水补至2 mL,加入1.5 mL DNS,100 ℃水解5 min,冷却后定容。移取样液于酶标板,在540 nm处测其吸光值,绘制标准曲线。标准曲线方程为Y=0.3589X+0.0006(R2=0.9945),可见葡萄糖含量在0~1.0 mg/mL范围内有良好的线性关系。
1.2.2 魔芋粉中KGM含量的测定
魔芋粉的纯化[26]:称取1 g魔芋粉加入乙醇溶液,搅拌均匀后在一定的超声温度、功率和时间下进行纯化,过滤后称取0.1900~0.2000 g滤渣加入蒸馏水,溶胀3 h后于离心机转速4000 r/min下离心20 min,上清液即为提取液。
KGM含量的测定参照NY/T 494-2010魔芋粉标准附录A[29]。根据公式(1)计算其含量。
(1) 式中:ε为KGM水解前后葡萄糖和甘露糖残基的分子量之比,ε=0.9;T为KGM水解液的葡萄糖含量,单位为毫克(mg);T0为KGM提取液的葡萄糖含量,单位为毫克(mg);m为魔芋粉样品质量,单位为克(g);w为样品含水量,%。
1.2.3 魔芋粉中KGM得率的测定
根据公式(2)计算KGM得率[30]。
(2) 式中:KGM质量与魔芋粉质量,单位均为毫克(mg)。
1.2.4 单因素实验
1.2.4.1 料液比对KGM含量的影响
准确称量魔芋粉每份1.0 g,将乙醇浓度、超声温度、超声时间以及超声功率分别设定为80%、50 ℃、45 min、200 W,料液比分别调为1:40、1:60、1:80、1:100、1:120(g/mL),在该条件下进行实验,考察料液比对其含量的影响。
1.2.4.2 乙醇浓度对KGM含量的影响
准确称量魔芋粉每份1.0 g,将料液比、超声温度、超声时间以及超声功率分别设定为1:100(g/mL)、50 ℃、45 min、200 W,乙醇浓度分别为50%、60%、70%、80%、90%,在该条件下进行实验,考察乙醇浓度对其含量的影响。
1.2.4.3 超声温度对KGM含量的影响
准确称量魔芋粉每份1.0 g,将乙醇浓度、料液比、超声时间以及超声功率分别设定为70%、1:100(g/mL)、45 min、200 W,超声温度在30、40、50、60、70 ℃下进行实验,考察超声温度对其含量的影响。
1.2.4.4 超声功率对KGM含量的影响
准确称量魔芋粉每份1.0 g,将乙醇浓度、料液比、超声温度以及超声时间分别设定为70%、1:100(g/mL)、50 ℃、45 min,超声功率分别为125、150、175、200、225 W,在该条件下进行实验,考察超声功率对其含量的影响。
1.2.4.5 超声时间对KGM含量的影响
准确称量魔芋粉每份1.0 g,将乙醇浓度、料液比、超声温度以及超声功率分别设定为70%、1:100(g/mL)、50 ℃、175 W,超声时间分别为15、30、45、60、75 min,在该条件下进行实验,考察超声功率对其含量的影响。
1.2.5 响应面试验设计
基于单因素实验结果,排除对含量影响不显著(P>0.05)的因素,选择料液比、乙醇浓度和超声时间的相关水平进行Box-Behnken试验设计以确定最优条件,具体试验水平参照表1。
表 1 响应面试验因素水平设计Table 1. Factor level design of response surface test因素 水平 −1 0 1 A料液比(g/mL) 1:80 1:100 1:120 B乙醇浓度(%) 60 70 80 C超声时间(min) 45 60 75 1.3 结构表征
1.3.1 FT-IR测定
将样品与溴化钾烘干,按质量比1:50混合研磨,压片后放入红外光谱仪,在波数范围4000~500 cm−1,分辨率4 cm−1下测定[31]。
1.3.2 XRD测定
将样品置于载玻片压片,放入X射线衍射仪测试。测试条件:室温,管压40 kV,电流40 mA,2θ扫描范围4°~40°,速率2°/min条件下进行[32]。
1.4 数据处理
每组实验进行三次平行,结果用平均值表示。运用IBS SPSS Statistics 26进行单因素显著性分析,Origin2022软件进行图形绘制,Design-Expert 13.0进行响应面试验结果分析。
2. 结果与分析
2.1 单因素实验结果分析
2.1.1 料液比对KGM含量的影响
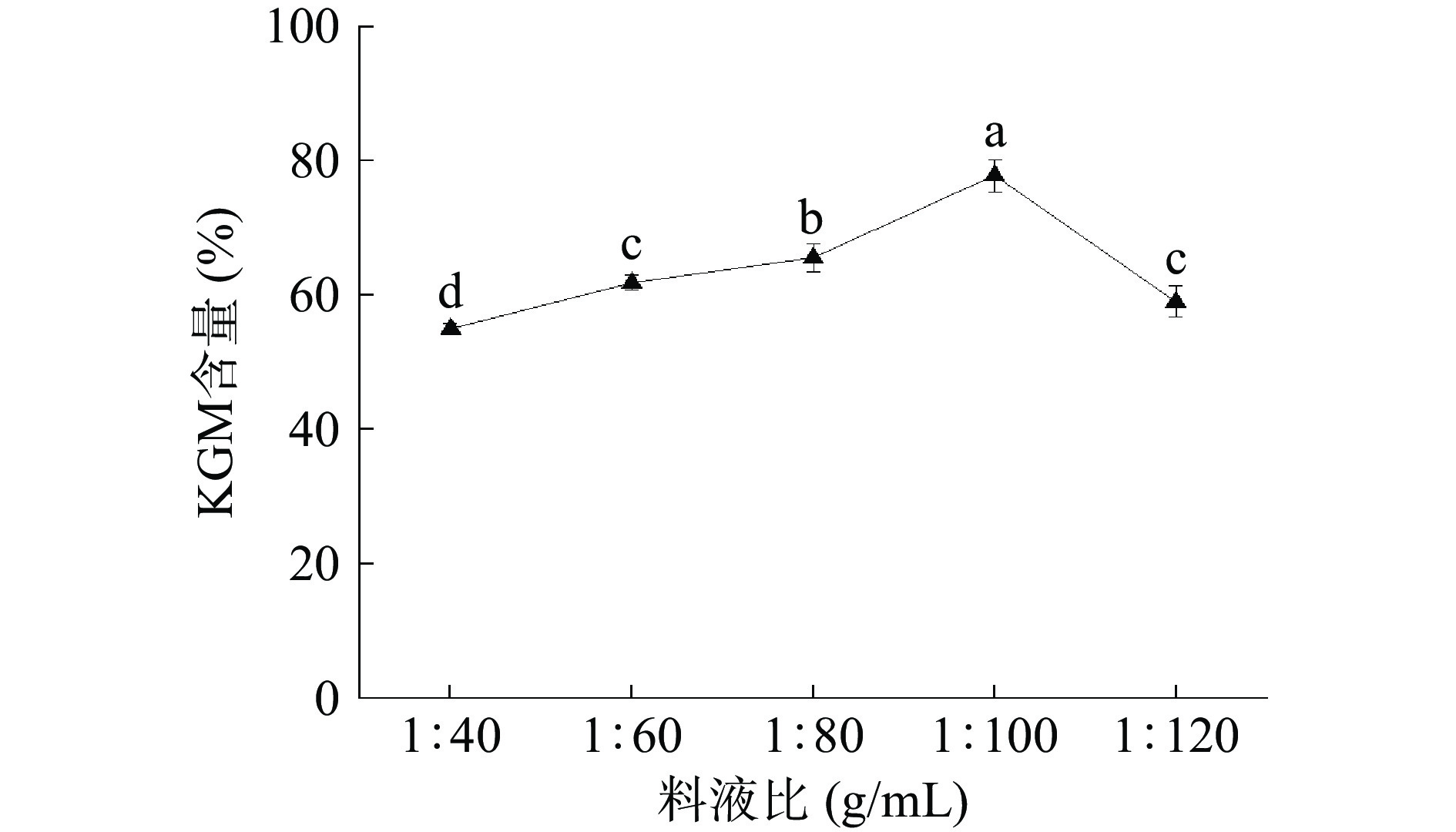
如图1所示,料液比较少时,魔芋粉中大分子物质难以解聚溶出,KGM的含量因此较低[33]。随着料液比的增大,乙醇量相对增多,KGM含量逐渐升高。当料液比为1:100(g/mL)时,KGM含量达到最大值77.88%后逐渐下降。因为其在乙醇量相对较多的情况下发生过度溶胀,包埋大量水分[34],过多水溶剂的存在导致部分KGM溶解于水中,含量在此情况下开始下降。通过统计学分析,料液比对KGM含量的影响有显著差异(P<0.05),其中料液比为1:100(g/mL)时极显著,选取料液比1:80、1:100、1:120(g/mL)进行响应面试验。
2.1.2 乙醇浓度对KGM含量的影响
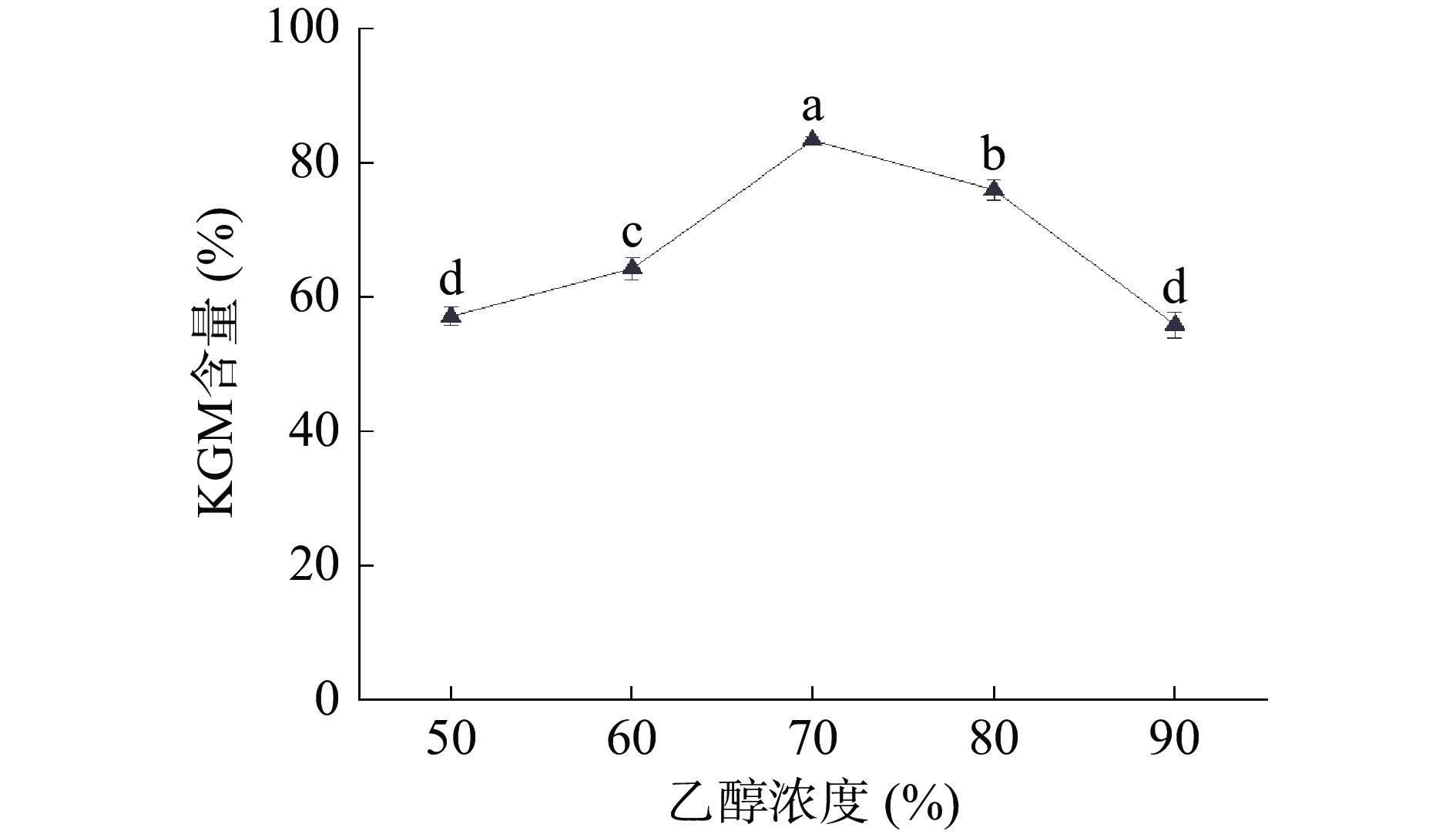
如图2所示,魔芋粉加入乙醇溶液后,其中的KGM、蛋白质、淀粉等物质溶于水,在乙醇浓度较低的条件下,KGM所受到的沉淀作用较小,而且其中一部分可能会溶解到水溶剂中流失,导致含量较低[30]。而随着乙醇浓度增长至70%时,KGM含量达到了最大值为83.41%。乙醇浓度继续增大,抑制KGM分子的伸展,不能有效地将其包裹、结合的杂质释放,导致含量降低[35]。通过统计学分析,乙醇浓度对KGM含量的影响有显著差异(P<0.05),其中乙醇浓度70%时极显著,选取乙醇浓度60%、70%、80%进行响应面试验。
2.1.3 超声温度对KGM含量的影响
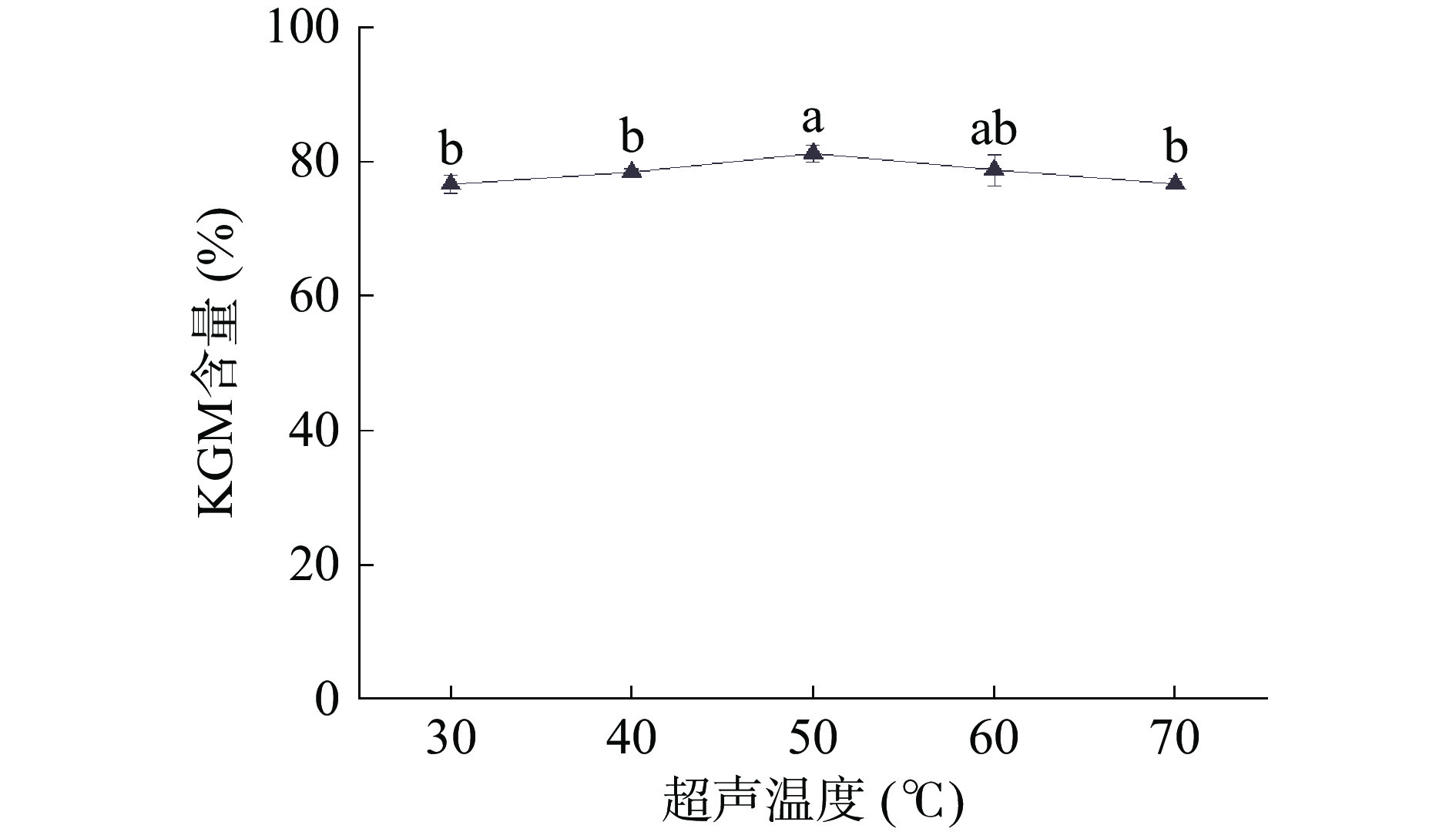
图3所示,当超声温度为50 ℃时,含量达到最大值81.24%。这是由于温度较低时,魔芋粉中大分子物质结合较为紧密,升温使得分子从魔芋粉中扩散的速率提高[33],超声温度继续升高,可能会导致KGM分子结构遭到破坏,含量有所下降。通过统计学分析,超声温度对KGM含量的影响没有显著差异(P>0.05)。因此,后续实验中超声温度固定为50 ℃。
2.1.4 超声功率对KGM含量的影响
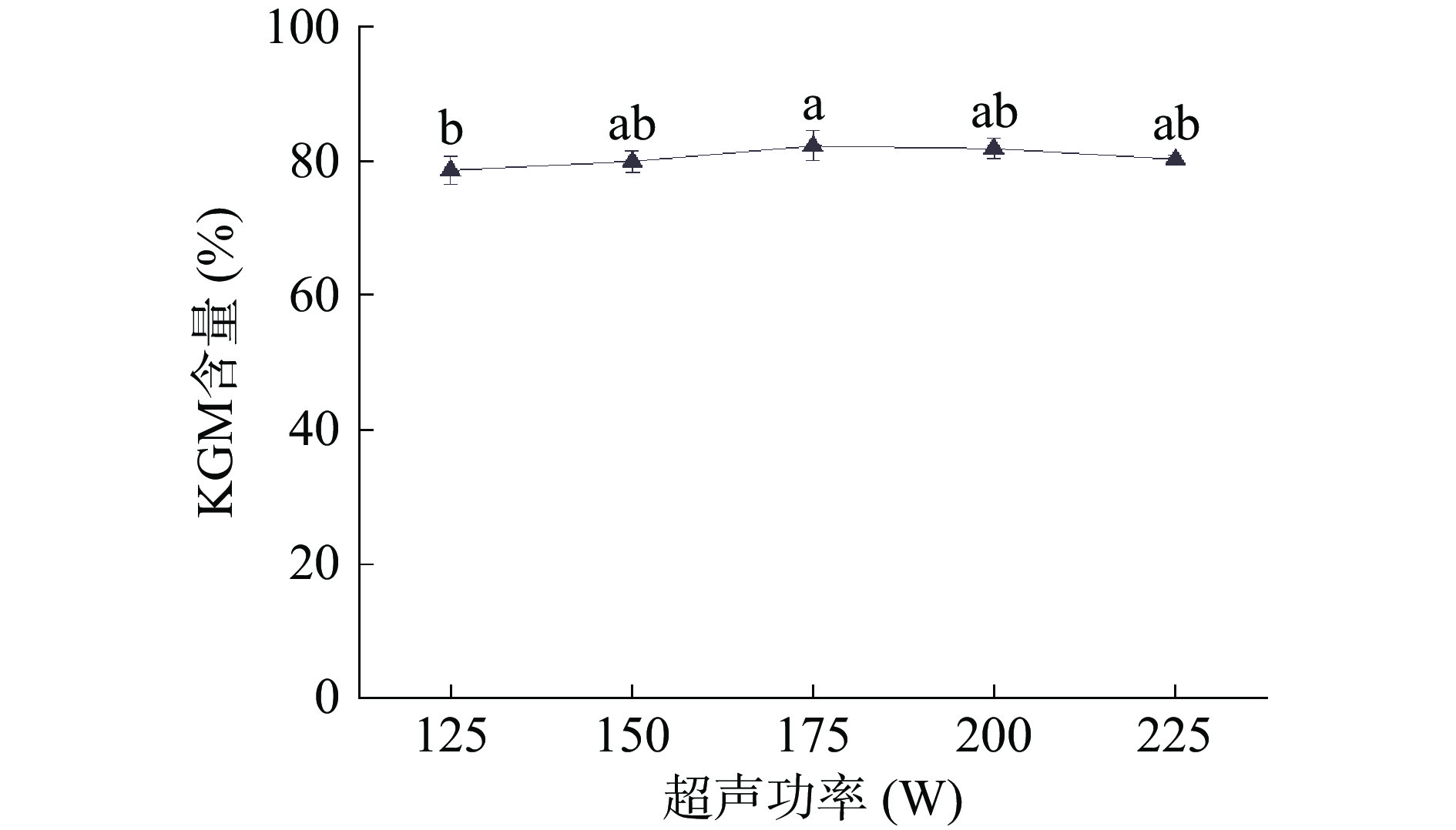
如图4所示,功率过小影响了超声波对魔芋粉的破坏作用,未能完全打开分子链,使杂质不能有效溶出,因此KGM含量较低。随着超声功率达175 W,含量达到了最大值82.26%。随着功率继续增大,在空化作用下多糖分子结构遭到破坏,细胞壁破碎加剧,导致KGM含量逐渐减少[5,31]。通过统计学分析,超声功率对KGM含量的影响没有显著差异(P>0.05)。因此,后续实验中超声功率固定为175 W。
2.1.5 超声时间对KGM含量的影响
由图5可知,随超声时间达到60 min,KGM含量逐渐升高至88.75%,随后下降。因为在超声时间较短的条件下,KGM与其他分子物质结合紧密,分子链未能完全打开,杂质也未能完全释放。而长时间的超声作用又使KGM的结构不稳定,空化作用导致分子链遭到破坏[5,31],KGM含量因此下降。通过统计学分析,超声时间对KGM含量的影响有显著差异(P<0.05),其中超声时间为60 min时极显著,选取超声时间45、60、75 min进行响应面试验。
2.2 响应面试验结果分析
参考Box-Behnken原理,优化试验设计结果如表2所示。
表 2 响应面试验设计及结果Table 2. Response surface experimental design and results试验号 A 料液比 B 乙醇浓度 C 超声时间 Y KGM含量(%) 1 −1 −1 0 58.57 2 1 −1 0 52.62 3 −1 1 0 70.68 4 1 1 0 63.85 5 −1 0 −1 72.45 6 1 0 −1 67.67 7 −1 0 1 64.88 8 1 0 1 68.02 9 0 −1 −1 63.01 10 0 1 −1 77.92 11 0 −1 1 58.75 12 0 1 1 71.74 13 0 0 0 88.64 14 0 0 0 86.25 15 0 0 0 90.66 16 0 0 0 87.81 17 0 0 0 87.72 根据表2中的数据对试验结果回归拟合,得到模型对应的回归方程为:Y=88.22−1.8A+6.41B−2.21C−0.22AB+1.98AC−0.48BC−13.19A2−13.59B2−6.77C2,对二次回归方程进行方差分析,结果见表3。
表 3 回归模型的方差分析Table 3. Analysis of variance in regression model方差来源 平方和 自由度 均方 F值 P值 显著性 模型 2293.4 9 254.82 59.78 <0.0001 ** A-料液比 25.99 1 25.99 6.1 0.0429 * B-乙醇浓度 328.19 1 328.19 77.00 <0.0001 ** C-超声时间 38.98 1 38.98 9.15 0.0193 * AB 0.1936 1 0.1936 0.0454 0.8373 AC 15.68 1 15.68 3.68 0.0966 BC 0.9216 1 0.9216 0.2162 0.6561 A² 732.86 1 732.86 171.94 <0.0001 ** B² 777.98 1 777.98 182.52 <0.0001 ** C² 192.87 1 192.87 45.25 0.0003 ** 残差 29.84 7 4.26 失拟项 19.41 3 6.47 2.48 0.2003 不显著 净误差 10.43 4 2.61 总离差 2323.24 16 注:**为差异极显著(P<0.01),*为差异显著(P<0.05)。 由表3结果分析可知,失拟项不显著(P=0.2003),且本试验所采用的回归模型是极显著水平(P<0.01),因此该模型可取。R2adj=0.9872,意味着该模型可信度较高。一次项B差异极显著(P<0.01),A、C差异显著(P<0.05),二次项A2,B2,C2对含量的影响极显著(P<0.01);各试验条件下三个因素影响KGM含量的程度大小为:乙醇浓度>超声时间>料液比。
图6响应面图可以看出,乙醇浓度比料液比的坡度稍陡峭,结合等高线图,乙醇浓度轴向的等高线较密集,表明与料液比相比,乙醇浓度的影响稍显著。较椭圆形的等高线图和陡峭的响应面图,说明了料液比和乙醇浓度具有交互效应。在不改变超声时间、超声温度和超声功率的条件下,随料液比的增加和乙醇浓度的升高,KGM含量会先升高达到峰值后再减小。
图7响应面图可以看出,超声时间比料液比的坡度更为陡峭,结合等高线图,超声时间轴向的等高线更加密集,表明超声时间对KGM含量的影响更为显著。椭圆形的等高线图和陡峭的响应面图,说明了料液比和超声时间的交互作用较强。在不改变乙醇浓度、超声温度和超声功率的条件下,随料液比的增加和超声时间的延长,KGM含量会先升高达到峰值后再减小。
图8所示响应面图可以看出,乙醇浓度比超声时间更陡峭,结合等高线图,乙醇浓度轴向的等高线更密集,表明与超声时间相比,乙醇浓度对KGM含量的影响更显著。椭圆形的等高线图和陡峭的响应面图,说明了乙醇浓度和超声时间交互效应较强。在不改变其他条件的基础上,超声时间的延长和乙醇浓度的升高会使KGM含量先升高达到峰值后再减小。
利用Design-Expert软件得出,魔芋粉最佳纯化条件是料液比1:101.538(g/mL),乙醇浓度72.777%,超声时间为54.808 min,KGM含量可达88.672%。根据实际操作进行修整,料液比、乙醇浓度、超声时间分别为1:102(g/mL)、73%和55 min,通过三次验证实验得到KGM含量为88.1%±1.05%,与预测值较为接近,说明优化模型是合理可行的。
经公式(1)计算纯化前KGM含量为59.70%±0.97%,纯化后含量为88.1%±1.05%;经公式(2)计算纯化前KGM得率为52.24%±1.29%,纯化后得率为62.93%±1.73%。因此,工艺优化后KGM含量与得率均显著提高。
2.3 结构表征
2.3.1 FT-IR图谱分析
为了解纯化前后官能团的变化情况,采用傅里叶红外光谱仪对其结构进行探测[36],如图9红外图谱所示,吸收峰的形状以及出现位置大致相同,未出现新的吸收峰,这与所报道的结果一致[37]。KGM中-OH的伸缩振动峰出现在3000~3700 cm−1之间,这是多糖的特征峰[38]。在2800~3000 cm−1范围内的峰由-CH3和-CH2基团中的-CH键拉伸所产生。在1647 cm−1处的吸收带代表分子内氢键的特征峰。
2.3.2 XRD图谱分析
如图10所示,纯化前后KGM的XRD图谱在2θ处于4°~40°间均未表现出明显的结晶峰,在2θ处于20°左右时均出现一个较宽的弥散峰,与报道所述一致[39]。此外,没有观察到新的特征峰的出现,说明纯化工艺对KGM结构、结晶度以及氢键作用力的影响微弱[39]。
3. 结论
本研究通过单因素和响应面试验确定魔芋粉最佳纯化工艺条件:超声时间、乙醇浓度、料液比、超声温度和超声功率分别为55 min、73%、1:102(g/mL)、50 ℃、175 W,该条件下KGM含量与模型预测值相差较小,达到88.1%±1.05%。经计算该工艺条件下KGM得率为62.93%。随后对其优化前后的结构进行表征,对比两者的FT-IR图谱和XRD图谱,未发现明显差异,证明该优化工艺对KGM结构影响较弱。因此在不改变KGM结构的前提下,应用该工艺可以更加低廉、高效、无损地对魔芋粉进行纯化,得到纯度更高的KGM,为其应用于食品药品等行业加工生产提供基础理论和研究方向。
-
表 1 响应面试验因素水平设计
Table 1 Factor level design of response surface test
因素 水平 −1 0 1 A料液比(g/mL) 1:80 1:100 1:120 B乙醇浓度(%) 60 70 80 C超声时间(min) 45 60 75 表 2 响应面试验设计及结果
Table 2 Response surface experimental design and results
试验号 A 料液比 B 乙醇浓度 C 超声时间 Y KGM含量(%) 1 −1 −1 0 58.57 2 1 −1 0 52.62 3 −1 1 0 70.68 4 1 1 0 63.85 5 −1 0 −1 72.45 6 1 0 −1 67.67 7 −1 0 1 64.88 8 1 0 1 68.02 9 0 −1 −1 63.01 10 0 1 −1 77.92 11 0 −1 1 58.75 12 0 1 1 71.74 13 0 0 0 88.64 14 0 0 0 86.25 15 0 0 0 90.66 16 0 0 0 87.81 17 0 0 0 87.72 表 3 回归模型的方差分析
Table 3 Analysis of variance in regression model
方差来源 平方和 自由度 均方 F值 P值 显著性 模型 2293.4 9 254.82 59.78 <0.0001 ** A-料液比 25.99 1 25.99 6.1 0.0429 * B-乙醇浓度 328.19 1 328.19 77.00 <0.0001 ** C-超声时间 38.98 1 38.98 9.15 0.0193 * AB 0.1936 1 0.1936 0.0454 0.8373 AC 15.68 1 15.68 3.68 0.0966 BC 0.9216 1 0.9216 0.2162 0.6561 A² 732.86 1 732.86 171.94 <0.0001 ** B² 777.98 1 777.98 182.52 <0.0001 ** C² 192.87 1 192.87 45.25 0.0003 ** 残差 29.84 7 4.26 失拟项 19.41 3 6.47 2.48 0.2003 不显著 净误差 10.43 4 2.61 总离差 2323.24 16 注:**为差异极显著(P<0.01),*为差异显著(P<0.05)。 -
[1] GAO S, ZHANG L, CAO J. Synthesis and characterization of poly (ester urethane)/nitrokonjac glucomannan semi-interpenetrating polymer networks[J]. Journal of Applied Polymer Science,2003,90(8):2224−2228. doi: 10.1002/app.12882
[2] 孙思力, 杨伟东, 胡肖肖, 等. 魔芋葡甘露低聚糖制备研究进展[J]. 科技视界,2022(29):89−91. [SUN S L, YANG W D, HU X X, et al. Research progress in preparation of konjac glucomannan oligosaccharides[J]. Science and Technology Vision,2022(29):89−91.] SUN S L, YANG W D, HU X X, et al . Research progress in preparation of konjac glucomannan oligosaccharides[J]. Science and Technology Vision,2022 (29 ):89 −91 .[3] 颜吉强, 莫新元, 林婷, 等. 不同温度处理下魔芋葡甘聚糖膜的制备及其表征[J]. 食品科技,2022,47(12):38−43. [YAN J Q, MO X Y, LIN T, et al. Preparation and characterization of konjac glucomannan films treated at different temperatures[J]. Food Research International,2022,47(12):38−43.] YAN J Q, MO X Y, LIN T, et al . Preparation and characterization of konjac glucomannan films treated at different temperatures[J]. Food Research International,2022 ,47 (12 ):38 −43 .[4] TATIRAT O, CHAROENREIN S. Physicochemical properties of konjac glucomannan extracted from konjac flour by a simple centrifugation process[J]. LWT-Food Science and Technology,2011,44(10):2059−2063. doi: 10.1016/j.lwt.2011.07.019
[5] 郭晟. 三种魔芋葡甘聚糖不同特性比较研究[D]. 长沙:湖南农业大学, 2012. [GUO S. Comparative study on different characteristics of three kinds of konjac glucomannan[D]. Changsha:Hunan Agricultural University, 2012.] GUO S. Comparative study on different characteristics of three kinds of konjac glucomannan[D]. Changsha: Hunan Agricultural University, 2012.
[6] 张凌, 聂娅娜, 朱诗萌. 响应面法优化魔芋葡甘聚糖的纯化条件[J]. 中国食品添加剂,2015(3):152−157. [ZHANG L, NIE Y N, ZHU S M. Optimization of purification conditions of konjac glucomannan by response surface methodology[J]. China Food Additives,2015(3):152−157.] ZHANG L, NIE Y N, ZHU S M . Optimization of purification conditions of konjac glucomannan by response surface methodology[J]. China Food Additives,2015 (3 ):152 −157 .[7] 唐晓东, 孙莹莹, 李瑜, 等. 酶法降解魔芋葡甘聚糖工艺研究[J]. 农产品加工,2022(22):35−37,40. [TANG X D, SUN Y Y, LI Y, et al. Study on enzymatic degradation of konjac glucomannan[J]. Academic Periodical of Farm Products Processing,2022(22):35−37,40.] TANG X D, SUN Y Y, LI Y, et al . Study on enzymatic degradation of konjac glucomannan[J]. Academic Periodical of Farm Products Processing,2022 (22 ):35 −37,40 .[8] 张升晖, 吴绍艳, 颜益智, 等. 魔芋葡甘露聚糖纯化及性能研究[J]. 食品科学,2005(9):275−277. [ZHANG S H, WU S Y, YAN Y Z, et al. Purification and properties of konjac glucomannan[J]. Food Science,2005(9):275−277.] doi: 10.3321/j.issn:1002-6630.2005.09.065 ZHANG S H, WU S Y, YAN Y Z, et al . Purification and properties of konjac glucomannan[J]. Food Science,2005 (9 ):275 −277 . doi: 10.3321/j.issn:1002-6630.2005.09.065[9] 陈曦, 赵丹. 魔芋葡甘聚糖制备低聚糖及抗氧化研究进展[J]. 生物技术,2023,33(1):129−134. [CHEN X, ZHAO D. Preparation of oligosaccharides from konjac glucomannan and antioxidation research progress[J]. Biotechnology,2023,33(1):129−134.] CHEN X, ZHAO D . Preparation of oligosaccharides from konjac glucomannan and antioxidation research progress[J]. Biotechnology,2023 ,33 (1 ):129 −134 .[10] 张露瀛. 魔芋葡甘聚糖的生物学功效及其在食品中的应用[J]. 食品界,2017(6):93. [ZHANG L Y. Biological efficacy of konjac glucomannan and its application in food[J]. Food and More,2017(6):93.] ZHANG L Y . Biological efficacy of konjac glucomannan and its application in food[J]. Food and More,2017 (6 ):93 .[11] CHEN H, NIE Q, HU J, et al. Hypoglycemic and hypolipidemic effects of glucomannan extracted from konjac on type 2 diabetic rats[J]. Journal of Agricultural and Food Chemistry,2019,67(18):5278−5288. doi: 10.1021/acs.jafc.9b01192
[12] DU Q, LIU J, DING Y. Recent progress in biological activities and health benefits of konjac glucomannan and its derivatives[J]. Bioactive Carbohydrates and Dietary Fibre,2021,26:100270. doi: 10.1016/j.bcdf.2021.100270
[13] 张颖. 魔芋葡甘聚糖理化性质及应用前景[J]. 食品安全导刊,2023(18):148−150. [ZHANG Y. Physicochemical properties and application prospects of konjac glucomannan[J]. China Food Safety Magazine,2023(18):148−150.] ZHANG Y . Physicochemical properties and application prospects of konjac glucomannan[J]. China Food Safety Magazine,2023 (18 ):148 −150 .[14] 郭丽萍. 不同水化与流变学性质魔芋葡甘露聚糖调控血糖和抑制肥胖的功能研究[D]. 无锡:江南大学, 2021. [GUO L P. Study on the function of konjac glucomannan with different hydration and rheological properties in regulating glycemic response and preventing obesity[D]. Wuxi:Jiangnan University, 2021.] GUO L P. Study on the function of konjac glucomannan with different hydration and rheological properties in regulating glycemic response and preventing obesity[D]. Wuxi: Jiangnan University, 2021.
[15] CHEN H, NIE Q, HU J, et al. Glucomannans alleviated the progression of diabetic kidney disease by improving kidney metabolic disturbance[J]. Molecular Nutrition & Food Research,2019,63(12):1801008.
[16] ZHANG W, RHIM J W. Recent progress in konjac glucomannan-based active food packaging films and property enhancement strategies[J]. Food Hydrocolloids, 2022:107572.
[17] DU Y, WANG L, MU R, et al. Fabrication of novel konjac glucomannan/shellac film with advanced functions for food packaging[J]. International Journal of Biological Macromolecules,2019,131:36−42. doi: 10.1016/j.ijbiomac.2019.02.142
[18] NETO R J G, GENEVRO G M, DE ALMEIDA PAULO L, et al. Characterization and in vitro evaluation of chitosan/konjac glucomannan bilayer film as a wound dressing[J]. Carbohydrate Polymers,2019,212:59−66. doi: 10.1016/j.carbpol.2019.02.017
[19] SUN J, JIANG H, WU H, et al. Multifunctional bionanocomposite films based on konjac glucomannan/chitosan with nano-ZnO and mulberry anthocyanin extract for active food packaging[J]. Food Hydrocolloids,2020,107:105942. doi: 10.1016/j.foodhyd.2020.105942
[20] 石停凤, 潘廷跳, 鄢光欢. 魔芋葡甘聚糖复合膜及其研究进展[J]. 热带生物学报,2016,7(4):510−516. [SHI T F, PAN T T, YAN G H. Konjac glucomannan composite membrane and its research progress[J]. Journal of Tropical Biology,2016,7(4):510−516.] SHI T F, PAN T T, YAN G H . Konjac glucomannan composite membrane and its research progress[J]. Journal of Tropical Biology,2016 ,7 (4 ):510 −516 .[21] 刘锋, 陈雪怡, 邹海良, 等. 大豆蛋白负载魔芋葡甘聚糖对Cd(Ⅱ)的吸附性能[J]. 化工进展,2016,35(8):2592−2597. [LIU F, CHEN X Y, ZOU H L, et al. Adsorption properties of konjac glucomannan loaded with soybean protein for Cd(Ⅱ)[J]. Chemical Industry and Engineering Progress,2016,35(8):2592−2597.] LIU F, CHEN X Y, ZOU H L, et al . Adsorption properties of konjac glucomannan loaded with soybean protein for Cd(Ⅱ)[J]. Chemical Industry and Engineering Progress,2016 ,35 (8 ):2592 −2597 .[22] DEVARAJ R D, REDDY C K, XU B. Health-promoting effects of konjac glucomannan and its practical applications:A critical review[J]. International Journal of Biological Macromolecules,2019,126:273−281. doi: 10.1016/j.ijbiomac.2018.12.203
[23] 张佳璇, 韦翠萍, 童彩玲, 等. 甘蓝提取物对魔芋葡甘聚糖凝胶流变特性的影响[J]. 食品研究与开发,2023,44(9):8−14. [ZHANG J X, WEI C P, TONG C L, et al. Effect of cabbage extract on rheological properties of konjac glucomannan gel[J]. Food Research and Development,2023,44(9):8−14.] doi: 10.12161/j.issn.1005-6521.2023.09.002 ZHANG J X, WEI C P, TONG C L, et al . Effect of cabbage extract on rheological properties of konjac glucomannan gel[J]. Food Research and Development,2023 ,44 (9 ):8 −14 . doi: 10.12161/j.issn.1005-6521.2023.09.002[24] BEHERA S S, RAY R C. Nutritional and potential health benefits of konjac glucomannan, a promising polysaccharide of elephant foot yam, Amorphophallus konjac K. Koch:A review[J]. Food Reviews International,2017,33(1):22−43. doi: 10.1080/87559129.2015.1137310
[25] 吴远艳. 魔芋葡甘露聚糖的提纯以及化学改性研究进展[J]. 陕西农业科学,2017,63(4):63−67. [WU Y Y. Research progress in purification and chemical modification of konjac glucomannan[J]. Shaanxi Journal of Agricultural Sciences,2017,63(4):63−67.] WU Y Y . Research progress in purification and chemical modification of konjac glucomannan[J]. Shaanxi Journal of Agricultural Sciences,2017 ,63 (4 ):63 −67 .[26] 聂娅娜. 魔芋葡甘聚糖的纯化及在米饭中的应用研究[D]. 长春:吉林大学, 2016. [NIE Y N. Purification of konjac glucomannan and its application in rice[D]. Changchun:Jilin University, 2016.] NIE Y N. Purification of konjac glucomannan and its application in rice[D]. Changchun: Jilin University, 2016.
[27] 王元. 魔芋葡甘聚糖的结构及保健功能研究[J]. 现代食品,2021(7):113−115. [WANG Y. Study on the structure and health function of konjac glucomannan[J]. Modern Food,2021(7):113−115.] WANG Y . Study on the structure and health function of konjac glucomannan[J]. Modern Food,2021 (7 ):113 −115 .[28] 魏晓梅, 来国丹, 何芳, 等. 云南省花魔芋葡甘露聚糖提取方法的优化及测定[J]. 中国野生植物资源,2022,41(1):20−25. [WEI X M, LAI G D, HE F, et al. Optimization and determination of extraction method for konjac glucomannan from Yunnan Province[J]. Chinese Wild Plant Resources,2022,41(1):20−25.] WEI X M, LAI G D, HE F, et al . Optimization and determination of extraction method for konjac glucomannan from Yunnan Province[J]. Chinese Wild Plant Resources,2022 ,41 (1 ):20 −25 .[29] 张盛林. 中华人民共和国农业行业标准魔芋粉:NY/T 494-2010[S]. 中华人民共和国农业部:西南大学、四川省产品质量监督检验检测院等, 2010:6-7. [ZHANG S L. Agricultural industry standard of the People's Republic of China Konjac flour:NY/T 494-2010[S]. Ministry of Agriculture of the People's Republic of China:Southwest University, Sichuan Provincial Institute of Product Quality Supervision, Inspection and Testing, et al. 2010:6-7.] ZHANG S L. Agricultural industry standard of the People's Republic of China Konjac flour: NY/T 494-2010[S]. Ministry of Agriculture of the People's Republic of China: Southwest University, Sichuan Provincial Institute of Product Quality Supervision, Inspection and Testing, et al. 2010: 6-7.
[30] 王瑶, 宁杰, 宋庆贺, 等. 响应面法优化魔芋葡甘露聚糖制备工艺及其理化性质分析[J]. 食品研究与开发,2020,41(18):154−161. [WANG Y, NING J, SONG Q H, et al. Optimization of preparation and physicochemical properties of konjac glucomannan by response surface methodology[J]. Food Research and Development,2020,41(18):154−161.] WANG Y, NING J, SONG Q H, et al . Optimization of preparation and physicochemical properties of konjac glucomannan by response surface methodology[J]. Food Research and Development,2020 ,41 (18 ):154 −161 .[31] 范盛玉, 严竟, 朱坤, 等. 辣椒红色素对魔芋葡甘聚糖-大豆分离蛋白复合凝胶性质的影响[J]. 食品与发酵工业,2023,49(8):216−222. [FAN S Y, YAN J, ZHU K, et al. Effects of capsanthin on properties of konjac glucomannan-soybean protein isolate composite gel[J]. Food and Fermentation Industries,2023,49(8):216−222.] FAN S Y, YAN J, ZHU K, et al . Effects of capsanthin on properties of konjac glucomannan-soybean protein isolate composite gel[J]. Food and Fermentation Industries,2023 ,49 (8 ):216 −222 .[32] WANG M, LI Y C, MENG F B, et al. Effect of honeysuckle leaf extract on the physicochemical properties of carbox ymethyl konjac glucomannan/konjac glucomannan/gelatin composite edible film[J]. Food Chemistry:X,2023,18:100675. doi: 10.1016/j.fochx.2023.100675
[33] 计艳艳. 魔芋甘露低聚糖的制备与抗氧化性研究及应用[D]. 长春:吉林大学, 2018. [JI Y Y. Preparation and antioxidant activity of konjac mannan oligosaccharide and its application[D]. Changchun:Jilin University, 2018.] JI Y Y. Preparation and antioxidant activity of konjac mannan oligosaccharide and its application[D]. Changchun: Jilin University, 2018.
[34] 覃海强, 林伟泉, 麦馨允. 响应面法优化超声波辅助提取魔芋葡甘聚糖的工艺[J]. 轻工科技,2016,32(12):16−19. [QIN H Q, LIN W Q, MAI X Y. Optimization of ultrasonic assisted extraction of konjac glucomannan by response surface methodology[J]. Light Industry Science and Technology,2016,32(12):16−19.] QIN H Q, LIN W Q, MAI X Y . Optimization of ultrasonic assisted extraction of konjac glucomannan by response surface methodology[J]. Light Industry Science and Technology,2016 ,32 (12 ):16 −19 .[35] 路鹏. 响应面法优化魔芋膳食纤维提取及结合有氧运动对大鼠高脂血症的影响[J]. 粮食与油脂,2020,33(4):97−100. [LU P. Optimization of konjac dietary fiber extraction using response surface methodology and the effect of aerobic exercise on hyperlipidemia in rats[J]. Cereals and Oils,2020,33(4):97−100.] LU P . Optimization of konjac dietary fiber extraction using response surface methodology and the effect of aerobic exercise on hyperlipidemia in rats[J]. Cereals and Oils,2020 ,33 (4 ):97 −100 .[36] LI J, ZHU M, GU L, et al. Freeze-thaw stability of konjac glucomannan hydrogels supplemented with natural tapioca/corn dtarch[J]. LWT,2023,182:114841. doi: 10.1016/j.lwt.2023.114841
[37] 唐贵丹. 魔芋葡甘露聚糖的纯化及应用研究[D]. 重庆:西南大学, 2008. [TANG G D. Studies on purification and application of konjac glucomannan[D]. Chongqing:Southwest University, 2008.] TANG G D. Studies on purification and application of konjac glucomannan[D]. Chongqing: Southwest University, 2008.
[38] NGUYEN T A, DO T T, NGUYEN T D, et al. Isolation and characteristics of polysaccharide from Amorphophallus corrugatus in Vietnam[J]. Carbohydrate Polymers,2011,84(1):64−68. doi: 10.1016/j.carbpol.2010.10.074
[39] 胡艳, 李悦, 吴玉萍, 等. 低浓度乙醇对魔芋葡甘聚糖理化特性及其结构影响的研究[J/OL]. 食品与发酵工业, 1−11 [2024-02-25]. https://doi.org/10.13995/j.cnki.11-1802/ts.036368. [HU Y, LI Y, WU Y P, et al. Effects of low-concentration ethanol on physicochemical properties and structure of konjac glucomannan[J/OL]. Food and Fermentation Industries, 1−11 [2024-02-25]. https://doi.org/10.13995/j.cnki.11-1802/ts.036368.] HU Y, LI Y, WU Y P, et al. Effects of low-concentration ethanol on physicochemical properties and structure of konjac glucomannan[J/OL]. Food and Fermentation Industries, 1−11 [2024-02-25]. https://doi.org/10.13995/j.cnki.11-1802/ts.036368.
-
期刊类型引用(6)
1. 王寿峰,兰茜,雍登金,杨惠妮,胡敏. 利用核磁氢谱定量白酒中的酸酯总量. 食品与发酵工业. 2025(06): 306-310 .  百度学术
百度学术
2. 陶兰德,车富红,郭建慧,林有兰,王生库,孙海浪,冯声宝. 天佑德青稞酒中酸酯总量的测定及比对分析. 酿酒. 2023(04): 88-91 .  百度学术
百度学术
3. 陈茂飞,焦富,袁进,李巧玉,聂叶,李代鑫. 酱香型白酒酒醅中近红外快速检测乳酸的模型构建. 酿酒科技. 2023(09): 75-80 .  百度学术
百度学术
4. 宗绪岩,彭厚博,吴键航,盛旭峰,李丽. 化学计量学结合NIR对浓香型白酒年份、等级的研究. 包装与食品机械. 2022(02): 87-94 .  百度学术
百度学术
5. 翟双,张贵宇,庹先国,朱雪梅,罗林. 近红外光谱结合二维卷积在白酒基酒判别中的应用. 食品科技. 2022(09): 250-256 .  百度学术
百度学术
6. 宋艳,杨洋,张学平,许驰,王毓,蔡亮,李子文. 中红外光谱技术结合竞争性自适应重加权算法快速分析白酒风味组分. 中国酿造. 2022(12): 230-234 .  百度学术
百度学术
其他类型引用(4)





 下载:
下载:






 下载:
下载:



