Analysis of Nutritional Components, Active Components and Polysaccharide Properties of Phellinus igniarius
-
摘要: 为探寻不同桑黄子实体中营养、活性成分及抗氧化活性差异,本研究比较分析了5种桑黄的营养、活性成分含量及其多糖的抗氧化活性,以此为评价指标筛选优质桑黄子实体,采用rDNA ITS序列分析对目标桑黄进行鉴定,并对其多糖的抗氧化活性进行测定,通过紫外光谱、傅里叶变换红外光谱和高效液相色谱分析多糖性质。结果表明,供试桑黄在营养、活性成分含量及多糖抗氧化活性方面均存在较大差异;其中,桑黄S-4中粗纤维、粗蛋白、多糖、总酚、总黄酮、总三萜含量相对较高,粗脂肪和灰分含量相对较低,且S-4多糖对DPPH自由基、ABTS+自由基和O−2自由基的清除能力均较好,半抑制浓度(IC50)分别为35.07、12.87、91.34 μg/mL,对ABTS+自由基的清除能力与抗坏血酸相当;将S-4作为目标桑黄,经鉴定,为杨树桑黄;紫外、红外光谱和单糖组成分析表明S-4多糖具有典型的多糖类特征吸收峰,是含有β-糖苷键和呋喃环的多糖,主要由葡萄糖、半乳糖、岩藻糖、葡萄糖醛酸、核糖和甘露糖组成。S-4的营养、活性成分含量相对丰富,其多糖具有良好的抗氧化能力,为优良桑黄子实体的筛选及多糖开发利用提供参考。Abstract: In order to explore the differences of nutrition, active components and antioxidant activity in the fruiting bodies of different Phellinus igniarius, this study compared the nutritional and active ingredient contents of five species of Phellinus igniarius as well as their antioxidant activity of polysaccharides for the sake of obtaining high quality Phellinus igniarius fruiting bodies. The target Phellinus igniarius was identified by rDNA ITS sequence analysis and the antioxidant activity of its polysaccharide was determined. The properties of polysaccharides were analyzed by ultraviolet spectrum, Fourier transform infrared spectrum and high performance liquid chromatography. The results showed that significant differences in the nutrition, active ingredient content and polysaccharide antioxidant activity of different species were observed. The contents of crude fiber, crude protein, polysaccharide, total phenol, total flavone and total triterpene in S-4 were relatively high, while the contents of crude fat and ash were relatively low. S-4 polysaccharides demonstrated excellent DPPH radical, ABTS+ radical and O−2 radical scavenging ability, and the half-inhibitory concentration (IC50) were 35.07, 12.87 and 91.34 μg/mL, respectively. The scavenging ability of S-4 polysaccharides against ABTS+ radical was equivalent to that of ascorbic acid. S-4 was used as the target Phellinus igniarius, and was identified as Sanghuangporus vaninii. Ultraviolet, infrared spectrum and monosaccharide composition analysis showed that S-4 polysaccharides had typical polysaccharide characteristic absorption peak, which was composed of glucose, galactose, fucose, glucuronic acid, ribose and mannose, containing β-glycoside bond and furan ring. The S-4 was relatively rich in nutrients and active ingredients, and its polysaccharides had good antioxidant capacity, which would provide a reference for the screening of excellent Phellinus igniarius fruiting bodies and the development and utilization of polysaccharides.
-
桑黄又称桑耳、桑臣或胡孙眼,在我国已有两千多年的药用历史,是一类药用真菌的统称,其药用价值在《神农本草经》、《药性论》、《本草纲目》等中医学专著中都有记载[1−2],具有“利五脏、排毒气”等功效,可治疗痢疾、血崩、崩漏带下、闭经、脐腹涩痛等疾病[3]。近数十年来学者们对于桑黄这类真菌的分类属性达成共识,认为它们是担子菌门(asidiomycota)蘑菇纲(Agaricomycetes)锈革菌目(Hymenochaetales)锈革菌科(Hymenochaetaceae)的大型多孔菌[4]。桑黄营养丰富、具有保健功效,其营养和药效成分主要有粗纤维、粗蛋白、粗脂肪、多糖、酚类、黄酮类和萜类等[5]。多糖作为其主要活性成分,具有抗氧化[6−7]、抗肿瘤[8]、降血糖[9]、免疫调节[10]和抗炎[11−12]等功能。
随着人们的健康意识不断增强,营养丰富且具有良好保健功效的药用真菌不断受到消费者的欢迎,桑黄以较高的药用价值受到了广泛关注,成为产品开发关注的焦点[13]。目前,桑黄在国外已被用于制造抗癌药品、养颜保健品及抑制艾滋病的新药[14]。国内已有学者研制出桑黄酒[15]、桑黄曲奇饼干[16]、桑黄茶[17]等一系列以桑黄或桑黄多糖为主要成分的产品,但市场上桑黄精深加工产品仍较少。不同桑黄子实体之间营养成分、活性成分含量差异较大,其多糖活性也有所不同[18−19],桑黄质量难以控制,制约桑黄产业的进一步发展。
为探寻不同桑黄子实体中营养和活性成分含量差异,发掘具有更好生物活性的多糖,本研究选取5种桑黄子实体,对其营养、活性成分进行比较分析,并对优良桑黄子实体的多糖进行抗氧化能力及单糖组成分析,为桑黄优良品种的筛选及多糖开发利用提供参考依据,为开发天然有效的抗氧化产品提供依据,为桑黄更好地应用于食品、药品、保健品和化妆品等领域提供理论支持。
1. 材料与方法
1.1 材料与仪器
桑黄子实体(编号S-1、S-2、S-3、S-4、S-5) 山东省农业科学院提供;香草醛、没食子酸标准品 上海源叶生物有限公司;重蒸酚、2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(ABTS) 北京索莱宝生物科技有限公司;1,1-二苯基-2-三硝基苯肼(DPPH) 北京酷来搏科技有限公司;单糖标准品 上海安谱实验科技股份有限公司;其余试剂均为国产。
JFM38马弗炉 JISHICO公司;K9840凯氏定氮仪 济南海能仪器股份有限公司;SZF-06A粗脂肪测定仪 上海新嘉电子有限公司;UV-6100紫外可见分光光度计 METASH公司;L550离心机 cence公司;SynergyH1M酶标仪 美国BioTek公司;Nicolet IS5傅里叶变换红外光谱仪 美国Thermo公司;1200液相色谱仪 美国Agilent公司。
1.2 实验方法
1.2.1 样品制备
将5种供试桑黄子实体于60 ℃烘箱中烘干,粉碎机粉碎,过80目筛,收集粉末密封保存备用。
1.2.2 营养成分含量测定
分别采用GB/T 5009.10-2003、GB 5009.5-2016(凯氏定氮法)、GB 5009.6-2016(索氏抽提法)和GB 5009.4-2016(食品中总灰分的测定)测定样品粗纤维、粗蛋白、粗脂肪和灰分含量。
1.2.3 多糖提取及含量测定
称取各样品适量,采用热水浸提法,料液比1:20,提取温度95 ℃,提取时间120 min,抽滤,重复上述操作1次,合并滤液,旋转蒸发浓缩后加入三倍体积95%乙醇,4 ℃醇沉20 h后冻干沉淀,得到粗多糖。沉淀用蒸馏水溶解,定容至250 mL,采用苯酚-硫酸法测定多糖含量。以葡萄糖质量浓度(mg/mL)为横坐标,吸光度为纵坐标做葡萄糖标准曲线方程为Y1=11.72X1−0.0256(R2=0.9979),得率按下式计算:
得率(%)=W2W1×100 式中:W1表示桑黄子实体的质量(g);W2表示多糖的质量(g)。
1.2.4 总黄酮、总酚、总三萜含量测定
按照胡文继[20]的方法进行提取,采用AlCl3比色法[21]测定总黄酮含量,以芦丁质量浓度(mg/mL)为横坐标,吸光度为纵坐标做芦丁标准曲线方程为Y2=3.1474X2−0.0.0061(R2=0.9996);采用Folin-Ciocalteu比色法[22]测定总酚含量,以没食子酸质量浓度(mg/mL)为横坐标,吸光度为纵坐标做没食子酸标准曲线方程为Y3=30.775X3+0.0245(R2=0.9985);采用NY/T 3676-2020测定总三萜含量,以齐墩果酸质量浓度(mg/mL)为横坐标,吸光度为纵坐标做齐墩果酸标准曲线方程为Y4=2.2493X4−0.0054(R2=0.9986)。
1.2.5 多糖抗氧化能力测定
1.2.5.1 清除DPPH自由基能力
取多糖溶液500 μL于2 mL离心管中,按照Pan等[23]报道的方法进行测定,多糖样品的最终反应浓度为125 μg/mL。空白组用500 μL蒸馏水代替样品,对照组用500 μL无水乙醇代替DPPH-乙醇溶液。按照公式(1)计算DPPH自由基清除率。
清除率(%)=(1−A1−A2A0)×100 (1) 式中:A1表示样品组吸光度平均值;A2表示对照组吸光度平均值;A0表示空白组吸光度平均值。
1.2.5.2 清除ABTS+自由基能力
取100 μL多糖溶液于2 mL离心管中,加入300 μL ABTS工作液,参照连俊辉[24]的方法进行测定,多糖样品的最终反应浓度为50 μg/mL。按照公式(1)计算ABTS+自由基清除率。
1.2.5.3 清除超氧阴离子(O−2)自由基能力
取200 μL多糖溶液于2 mL离心管中,按照徐高飞[25]的方法进行测定,多糖样品的最终反应浓度为500 μg/mL。按照公式(1)计算超氧阴离子自由基清除率。
1.2.5.4 还原力
取200 μL多糖溶液于2 mL离心管中,多糖样品的最终反应浓度为500 μg/mL,参考张晨[26]的方法进行测定,吸光度值数值越大还原力越强,对照组用蒸馏水代替三氯化铁溶液,按照公式(2)计算还原力。
还原力=A1−A2 (2) 式中:A1表示样品组吸光度平均值;A2表示对照组吸光度平均值。
1.2.6 分子生物学鉴定
对S-4子实体提取基因组DNA,送至青岛睿博兴科公司进行内转录间隔区(ITS)测序,将所得的ITS序列与GenBank(https://www.ncbi.nlm.nih.gov/)网站中已知的序列进行BLAST(https://blast.ncbi.nlm.nih.gov/Blast.cgi)分析,从中获得与所得的ITS序列具有相似同源性的序列,使用MEGA 7.0软件,采用NJ(Neighbor Joining)法构建系统发育树。
1.2.7 目标桑黄多糖抗氧化能力测定
根据反应体系,将多糖以及VC分别配制成反应浓度为3.125、6.25、12.5、50、100、200、400 μg/mL的溶液体系,按照1.2.2的方法进行测定。
1.2.8 多糖除蛋白
多糖样品采用Sevag法除蛋白[27−28],弃掉有机相和蛋白层,保留水相层,重复脱蛋白操作至无蛋白层析出,经活性炭脱色和透析后用于紫外光谱分析、FT-IR分析和单糖组成分析。
1.2.9 紫外光谱分析
配制0.5 mg/mL的多糖溶液,利用紫外可见分光光度计在波长200~400 nm范围内扫描[29]。
1.2.10 FT-IR分析
取适量干燥多糖粉末混到一定量干燥KBr粉末中磨样,利用压片机压成片,用傅立叶变换红外光谱仪在4000~400 cm−1范围进行扫描分析[30]。
1.2.11 单糖组成分析
参照文献[31]的方法测定单糖组成。色谱条件:采用Agilent 1200型高效液相色谱系统分析,C18 Agilent(4.6 mm×150 mm×5 μm)色谱柱,流动相为0.01 mol/L的磷酸盐缓冲液-乙腈(82:18),流速1.0 mL/min,柱温25 ℃,进样量10 μL,检测波长245 nm。
1.3 数据处理
实验结果以3次平行实验的平均值±标准差表示,实验数据使用SPSS 27.0软件进行统计学分析,图表均采用Origin 2018软件进行绘制,使用MEGA 7.0软件构建系统发育树。
2. 结果与分析
2.1 桑黄子实体营养成分、活性成分含量测定
2.1.1 营养成分含量测定
对5种桑黄子实体的粗纤维、粗蛋白、粗脂肪和灰分含量分析结果见表1。供试桑黄粗纤维含量差异较大,粗纤维含量最高的是S-4,为33.40%,显著高于(P<0.05)其他四种桑黄子实体,粗纤维含量由高到低依次为S-4、S-5、S-2、S-1、S-3。在粗蛋白含量上,S-1粗蛋白含量最高,为23.10%,其次是S-3和S-4,两者粗蛋白含量分别为19.41%和18.77%,差异不显著(P>0.05)。粗脂肪含量较高的是S-1、S-3,两者粗脂肪含量均为1.67%,粗脂肪含量较低的是S-2、S-4和S-5,三者粗脂肪含量分别为1.37%、1.13%和0.83%。供试桑黄子实体灰分含量有显著差异(P<0.05),S-1灰分含量最高,为10.87%,S-5灰分含量最低,为4.07%,相差2.7倍。
表 1 桑黄子实体营养成分含量Table 1. Nutrient content of fruiting bodies of Phellinus igniarius桑黄编号 粗纤维(%) 粗蛋白(%) 粗脂肪(%) 灰分(%) S-1 22.77±0.61c 23.10±0.78a 1.67±0.09a 10.87±0.19a S-2 31.63±0.42b 10.53±0.17c 1.37±0.05b 5.54±0.09c S-3 17.47±0.48d 19.41±0.21b 1.67±0.12a 8.64±0.10b S-4 33.40±0.86a 18.77±0.02b 1.13±0.09c 4.47±0.02d S-5 32.07±0.31b 5.55±0.28d 0.83±0.05d 4.07±0.03e 注:表中同列不同小写字母表示差异显著(P<0.05),表2同。 2.1.2 活性成分含量测定
对供试桑黄子实体活性成分含量进行分析,结果见表2。供试桑黄子实体多糖、总酚、总黄酮和三萜含量差异较大。多糖含量由高到低为S-1、S-3、S-4、S-5、S-2,其中S-1、S-3和S-4的多糖含量差异不显著(P>0.05),分别为1.27%、1.20%和1.19%。总酚含量最高的是S-4,为0.34%,其总酚含量显著高于(P<0.05)其余4种桑黄子实体。总黄酮含量最高的是S-3,为1.67%,其次是S-4,为1.37%,含量最低的是S-5,为0.11%。总三萜含量最高的是S-1,为2.85%,其次是S-4,为2.71%,最低的是S-5,为1.59%。
表 2 桑黄子实体活性成分含量Table 2. Content of active component in fruiting bodies of Phellinus igniarius桑黄编号 多糖(%) 总酚(%) 总黄酮(%) 总三萜(%) S-1 1.27±0.09a 0.21±0.02b 0.48±0.05c 2.85±0.06a S-2 0.26±0.02c 0.23±0.01b 0.23±0.02d 2.79±0.11ab S-3 1.20±0.21a 0.26±0.03b 1.67±0.03a 2.70±0.02b S-4 1.19±0.02a 0.34±0.02a 1.37±0.01b 2.71±0.04b S-5 0.59±0.08b 0.21±0.01b 0.11±0.01e 1.59±0.07c 2.2 桑黄子实体多糖抗氧化能力比较分析
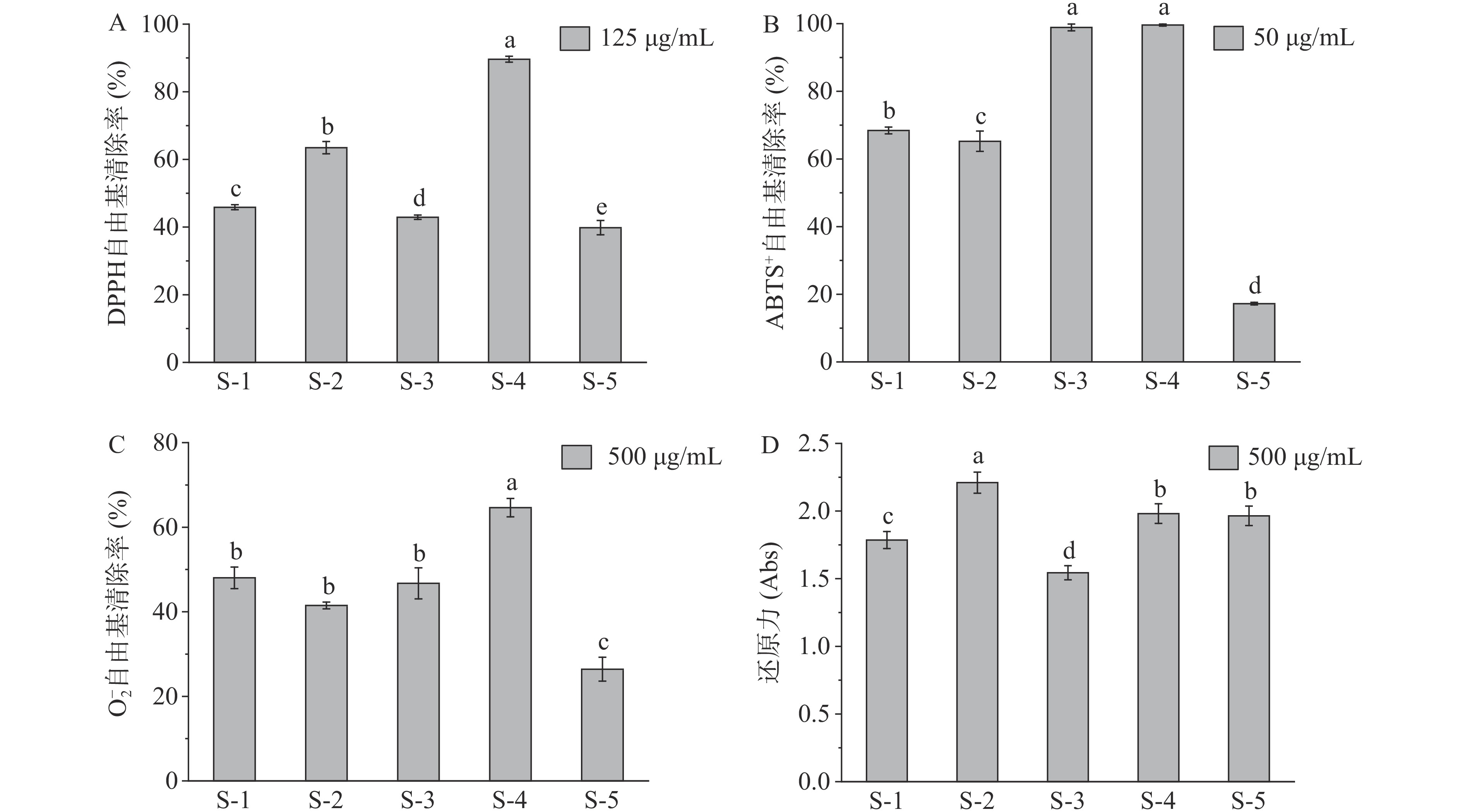
为筛选产高抗氧化能力多糖的桑黄,对供试桑黄子实体多糖进行抗氧化能力的比较分析,结果见图1。不同桑黄子实体多糖的抗氧化能力存在显著差异(P<0.05)。从S-4中提取的多糖,其对DPPH自由基、ABTS+自由基和O−2自由基均具有较强的清除能力,体现出较强的抗氧化能力。还原力最强的是S-2,S-4次之,但S-2的多糖对这三种自由基的清除率均显著低于S-4(P<0.05)。综合考虑,选择S-4作为目标桑黄,并对其多糖进行抗氧化能力验证和性质分析。
2.3 目标桑黄分子生物学鉴定
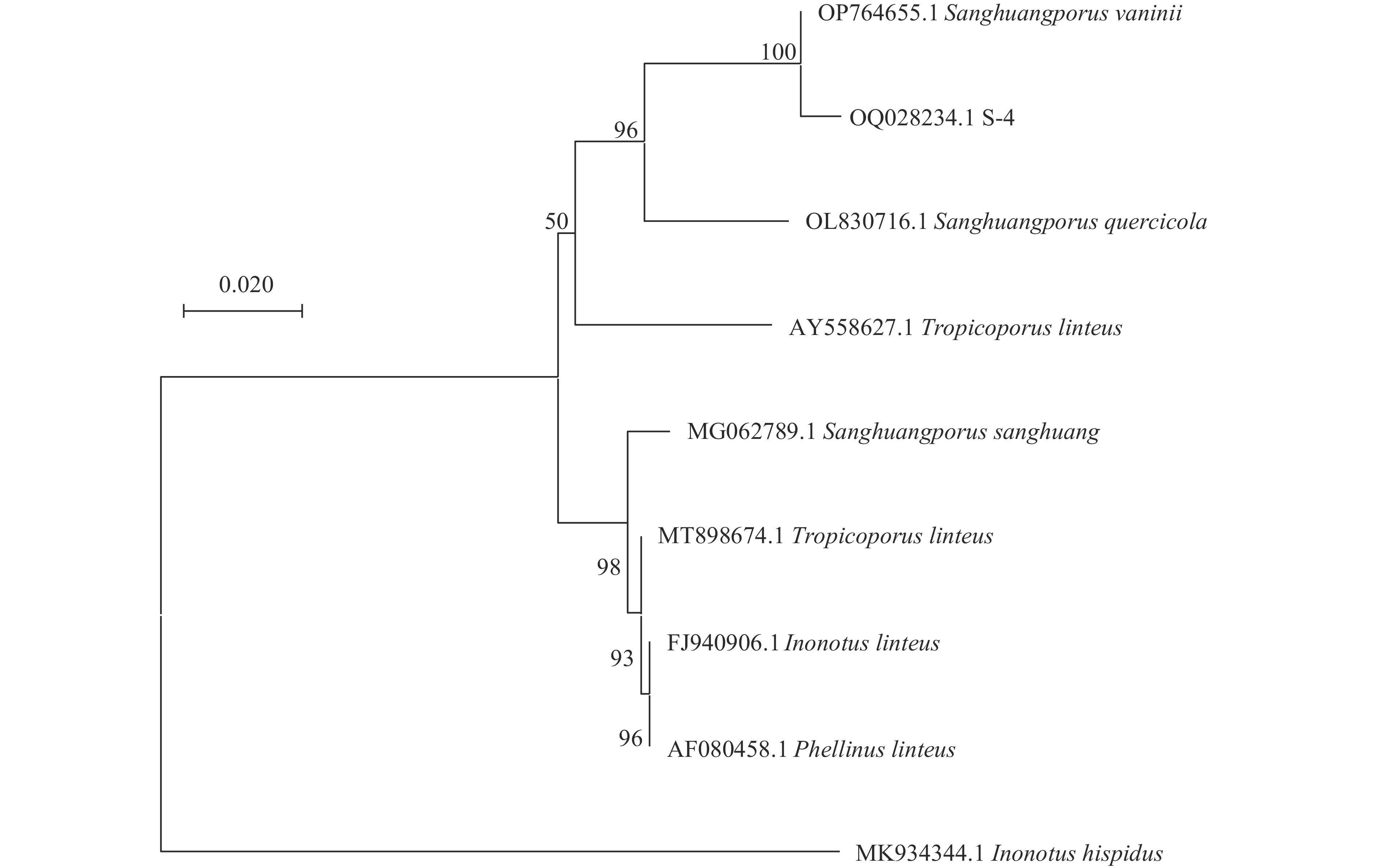
经ITS测序获得S-4的ITS序列(GeneBank No. OQ028234.1),用MEGA 7.0软件构建系统发育树,结果显示其与杨树桑黄(Sanghuangporus vaninii)聚为一族,如图2所示,因此将该桑黄命名为Sanghuangporus vaninii S-4。
2.4 目标桑黄多糖抗氧化能力测定
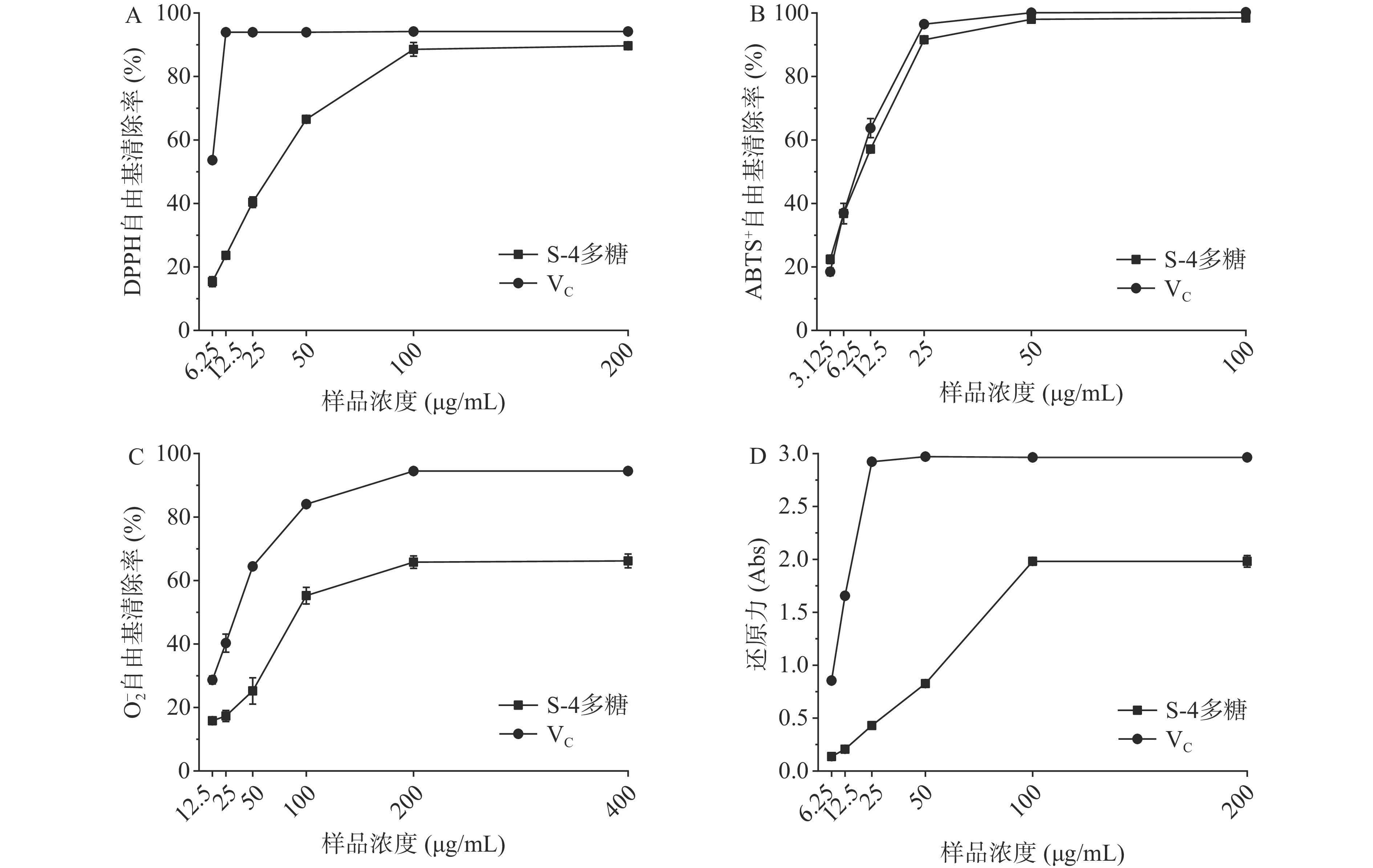
由图3可知,在一定浓度范围内,S-4多糖的抗氧化能力随多糖浓度的升高而升高,呈现出剂量依赖性,在达到最高抑制率或最大还原力后,不再增加。在多糖浓度为100 μg/mL时,S-4多糖对DPPH自由基的清除率达到最大值,最大清除率为89.81%(图3A)。在多糖浓度为50 μg/mL时,对ABTS+自由基的清除率达到最大值,最大清除率为99.81%(图3B)。S-4多糖对O−2自由基清除能力在多糖浓度200 μg/mL时达到最强,最大清除率64.63%(图3C)。S-4多糖的还原力在多糖浓度100 μg/mL时达到最大值,此时吸光值为1.981(图3D)。S-4多糖对DPPH和ABTS+自由基有极强的的清除能力,并且最大清除率与VC相当,体现出较好的抗氧化能力。
S-4多糖对DPPH自由基、ABTS+自由基和O−2自由基的IC50值分别为35.07、12.87、91.34 μg/mL,并且对于ABTS+自由基的清除能力要强于DPPH自由基和O−2自由基。因此,该多糖具有较强的抗氧化活性。
2.5 紫外光谱分析
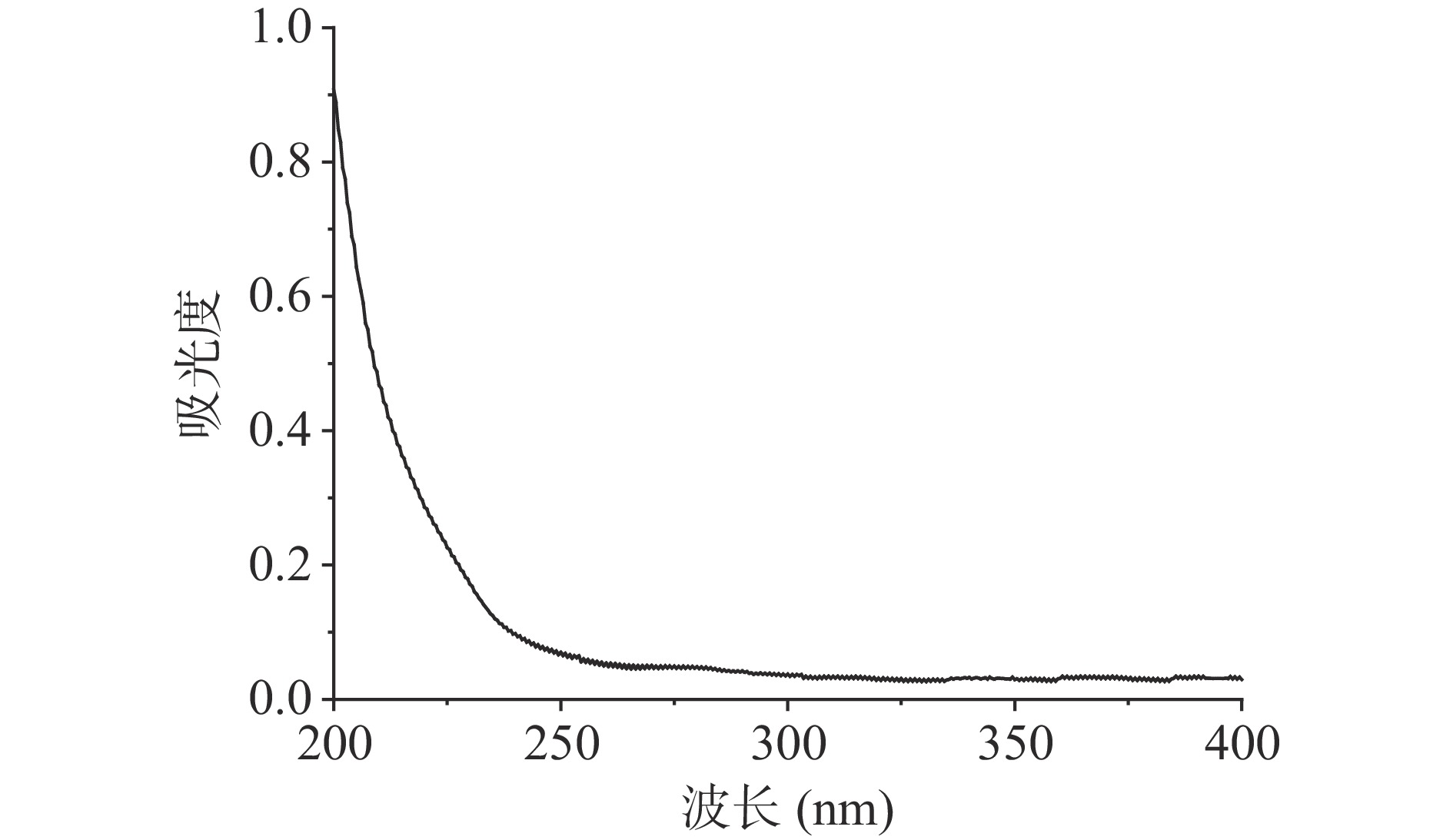
S-4多糖紫外扫描结果如图4所示,在波长200 nm附近有明显糖类特征吸收峰,在波长260、280 nm附近无明显核酸和蛋白质吸收峰,表明多糖经过Sevag除蛋白、活性炭脱色和透析后不含大量的核酸和蛋白质。
2.6 FT-IR分析
S-4多糖红外光谱分析结果如图5所示,3404 cm−1附近是多糖中O-H键之间的伸缩振动[32];2928 cm−1附近是甲基或亚甲基的C-H键伸缩振动[33];1420~1200 cm−1范围内为C-H的变角振动峰,以上三个区域的吸收峰可判定S-4多糖具有糖类结构[34]。1629 cm−1附近的吸收峰是羧基中C=O非对称伸缩振动引起,也是糖醛酸的特征吸收峰[35];1200~1000 cm−1范围内出现2个吸收峰位置,表明含有呋喃糖[36];890 cm−1出现吸收峰表明其糖苷键以β-构型为主[37]。因此,该多糖为含有β-型糖苷键和呋喃环的多糖,并且含有糖醛酸。
2.7 单糖组成分析
对S-4多糖和单糖标准品进行PMP柱前衍生化高效液相色谱分析,结果如图6所示,单糖种类及含量见表3。S-4多糖的单糖组成为甘露糖、核糖、葡萄糖醛酸、葡萄糖、半乳糖和岩藻糖。其中,葡萄糖含量最高,为238159.38 mg/kg,半乳糖含量次之,为194119.69 mg/kg。岩藻糖、葡萄糖醛酸和核糖的含量分别为114574.88、43532.40、33480.93 mg/kg。甘露糖含量最低,仅有8122.79 mg/kg。
表 3 S-4多糖单糖组成Table 3. Monosaccharide composition of polysaccharides of S-4单糖种类 含量(mg/kg) 甘露糖 8122.79 核糖 33480.93 葡萄糖醛酸 43532.40 葡萄糖 238159.38 半乳糖 194119.69 岩藻糖 114574.88 Wan等[38]从杨树桑黄子实体中提取出的对人非小细胞肺癌有明显的抑制作用的水溶性多糖SVP-1,由葡萄糖、半乳糖、岩藻糖、甘露糖、阿拉伯糖、果糖、葡萄糖醛酸、半乳糖醛酸和甘露糖组成,与本研究中构成S-4多糖的6种单糖中有5种同样的单糖,并且同样以β-构型为主。由于实验条件限制,本研究并未测定多糖结构,后续会继续对S-4多糖的结构进行深入研究。
3. 讨论与结论
本研究采用热水浸提法提取桑黄多糖,在本实验设置的参数下,S-4多糖的得率为4.92%。李有贵等[39]同样采用热水浸提法提取野生和人工栽培桑黄子实体的多糖,但二者得率仅1%左右。形成这种差异的原因一方面是提取条件参数的设置,另一方面也与桑黄品种的不同有关。后续将尝试采用其他安全无毒的提取方式提取S-4多糖,旨在提升多糖得率。
在分析多糖抗氧化能力时,发现S-2多糖的还原能力强于S-4多糖,但其对三种自由基的清除作用却弱于S-4多糖,原因可能是S-2多糖中含有某种带有Fe2+的物质,该物质可能为杂质。另外,由于实验方法不同,也可能是受到试剂或实验体系的影响。蔡铭等[40]在比较猴头菇粗多糖的抗氧化能力时,也出现了类似现象,其中E-HeP对于羟自由基的清除能力最强,但其对DPPH自由基和ABTS+自由基的清除能力和还原力却弱于D-HeP。故在比较不同多糖的体外抗氧化能力时要全面考察,本文分析了三种自由基的清除率及还原力,实验结果较为可靠。
随着桑黄制品的不断丰富,桑黄多糖也逐渐被应用于各类产品的研发,目前也已经可以将桑黄中的有效药用成分提取出来,再进行产品研发,充分发挥其广泛的药理作用。近年来,桑黄在食品工业中的应用范围逐渐扩大,日本、韩国等地已经将桑黄列为食品、健康食品,甚至是药品,而我国目前对于桑黄精深加工产品的开发仍然较为匮乏。本研究通过对比五种桑黄的主要营养、活性成分含量及多糖的四种抗氧化能力,发现S-4具有相对丰富的营养及活性成分,其多糖具有相对较强的抗氧化活性,有一定的开发潜力,作为优良桑黄子实体应用于桑黄精深加工产品开发具有一定可行性,后续将尝试利用S-4多糖以咀嚼片或口服液的形式开发功能性食品。
-
表 1 桑黄子实体营养成分含量
Table 1 Nutrient content of fruiting bodies of Phellinus igniarius
桑黄编号 粗纤维(%) 粗蛋白(%) 粗脂肪(%) 灰分(%) S-1 22.77±0.61c 23.10±0.78a 1.67±0.09a 10.87±0.19a S-2 31.63±0.42b 10.53±0.17c 1.37±0.05b 5.54±0.09c S-3 17.47±0.48d 19.41±0.21b 1.67±0.12a 8.64±0.10b S-4 33.40±0.86a 18.77±0.02b 1.13±0.09c 4.47±0.02d S-5 32.07±0.31b 5.55±0.28d 0.83±0.05d 4.07±0.03e 注:表中同列不同小写字母表示差异显著(P<0.05),表2同。 表 2 桑黄子实体活性成分含量
Table 2 Content of active component in fruiting bodies of Phellinus igniarius
桑黄编号 多糖(%) 总酚(%) 总黄酮(%) 总三萜(%) S-1 1.27±0.09a 0.21±0.02b 0.48±0.05c 2.85±0.06a S-2 0.26±0.02c 0.23±0.01b 0.23±0.02d 2.79±0.11ab S-3 1.20±0.21a 0.26±0.03b 1.67±0.03a 2.70±0.02b S-4 1.19±0.02a 0.34±0.02a 1.37±0.01b 2.71±0.04b S-5 0.59±0.08b 0.21±0.01b 0.11±0.01e 1.59±0.07c 表 3 S-4多糖单糖组成
Table 3 Monosaccharide composition of polysaccharides of S-4
单糖种类 含量(mg/kg) 甘露糖 8122.79 核糖 33480.93 葡萄糖醛酸 43532.40 葡萄糖 238159.38 半乳糖 194119.69 岩藻糖 114574.88 -
[1] 包海鹰, 杨烁, 李庆杰, 等. “桑黄”的本草补充考证[J]. 菌物研究,2017,15(4):264−270 BAO H Y, YANG S, LI Q J, et al. Supplementary textual research on “ Sanghuang”[J]. Journal of Fungal Research,2017,15(4):264−270.
[2] 雷萍, 张文隽, 吴亚召, 等. 鲍姆桑黄五个品种栽培特性及功能成分的比较分析[J]. 菌物学报,2022,41(2):274−280 LEI P, ZHANG W J, WU Y Z, et al. Comparative analysis of cultivation characteristics and functional constituents of five varieties of Sang huangporus baumii[J]. Mycosystema,2022,41(2):274−280.
[3] 朱琳, 崔宝凯. 药用真菌桑黄的研究进展[J]. 菌物研究,2016,14(4):201−209 ZHU L, CUI B K. Progress on the studies of medicinal mushrooms “ Sanghuang” group[J]. Journal of Fungal Research,2016,14(4):201−209.
[4] 吴声华, 戴玉成. 药用真菌桑黄的种类解析[J]. 菌物学报,2020,39(5):781−794 WU S H, DAI Y C. Species clarification of the medicinal fungus Sanghuang[J]. Mycosystema,2020,39(5):781−794.
[5] 付立忠, 陆娜, 闫静, 等. 三种桑黄属真菌人工栽培子实体营养、药效成分及抗氧化活性分析评价[J]. 菌物学报,2021,40(8):2148−2158 FU L Z, LU N, YAN J, et al. Analyses and evaluation of nutrition, active component and antioxidant activities of fruiting bodies of three species of Sanghuangporus[J]. Mycosystema,2021,40(8):2148−2158.
[6] ZHANG J J, CHEN B S, DAI H Q, et al. Sesquiterpenes and polyphenols with glucose-uptake stimulatory and antioxidant activities from the medicinal mushroom Sanghuangporus sanghuang[J]. Chinese Journal of Natural Medicines,2021,19(9):693−699. doi: 10.1016/S1875-5364(21)60101-2
[7] 李瑞雪, 王钰婷, 夏家凤, 等. 桑黄菌丝体中多糖提取工艺优化及其体外抗氧化活性分析[J]. 中国农学通报,2019,35(29):143−150 LI R X, WANG Y T, XIA J F, et al. Optimization of extraction process of polysaccharide of Phellinus igniarius mycelium and analysis of its antioxidant activity in vitro[J]. Chinese Agricultural Science Bulletin,2019,35(29):143−150.
[8] CHENG J W, SONG J L, WANG Y B, et al. Conformation and anticancer activity of a novel mannogalactan from the fruiting bodies of Sanghuangporus sanghuang on HepG2 cells[J]. Food Research International,2022,156:111336. doi: 10.1016/j.foodres.2022.111336
[9] HOU R R, ZHOU L J, FU Y, et al. Chemical characterization of two fractions from Sanghuangporus sanghuang and evaluation of antidiabetic activity[J]. Journal of Functional Foods,2021,87:104825. doi: 10.1016/j.jff.2021.104825
[10] 刘帅, 莫俊恺, 潘丹阳, 等. 桑黄多糖的药理作用及提取方法研究进展[J]. 生物技术通报,2018,34(12):63−67 LIU S, MO J K, PAN D Y, et al. Research progress on pharmacological actions and extraction methods of polysaccharide from Phellinus igniarius[J]. Biotechnology Bulletin,2018,34(12):63−67.
[11] 胡涛. 桑黄多糖抗炎与降脂功能的评估及其分子机理研究[D]. 长沙:中南林业科技大学, 2019 HU T. The anti-inflammation and lipid-lowering effects and the potential molecular mechanism of Phellinus linteus[D]. Changsha:Central South University of Forestry and Technology, 2019.
[12] 郎明紫, 曾鹏, 刘明明, 等. 桑黄多糖的研究进展[J]. 蚕桑通报,2017,48(2):14−18 LANG M Z, ZENG P, LIU M M, et al. Research progress on polysaccharide from Phellinus baumii[J]. Bulletin of Sericulture,2017,48(2):14−18.
[13] 李彦颖, 张祺, 陈晓华, 等. 桑黄多糖的分离纯化、生物活性及其产品开发研究进展[J]. 食药用菌, 2022, 30(1):26-31,61 LI Y Y, ZHANG Q, CHEN X H, et al. Research progress in purification, bio-activity and product development of polysaccharides from Sanghuangporus polysaccharides from Sanghuangporus[J]. Edible and Medicinal Mushrooms, 2022, 30(1):26-31,61.
[14] 李小群, 梁贵秋, 刘开莉, 等. 桑黄活性成分的提取方法及应用研究进展[J]. 广西蚕业,2022,59(1):41−50 LI X Q, LIANG G Q, LIU K L, et al. Research progress on extraction methods and application of active components of Phellinus igniarius[J]. Guangxi Sericulture,2022,59(1):41−50.
[15] 王青春. 桑黄酒的研制及其质量评价[D]. 长春:吉林农业大学, 2022 WANG Q C. Development and quality evaluation of Sanghuang wine[D]. Changchun:Jilin Agricultural University, 2022.
[16] 王婷. 粗毛纤孔菌的驯化栽培及其固体发酵菌粉抗肿瘤作用和产品开发[D]. 长春:吉林农业大学, 2016 WANG T. Research on domestication and cultivation of Inonotus hispidus and antitumor activity of its solid fermentation power and developing new product with it[D]. Changchun:Jilin Agricultural University, 2016.
[17] 邵伟, 陈良辉, 熊泽, 等. 桑黄液体发酵茶饮料工艺研究[J]. 中国酿造,2016,35(12):184−187 SHAO W, CHEN L H, XIONG Z, et al. Study on the process of Phellinus igniarius tea beverage with submerged fermentatio[J]. China Brewing,2016,35(12):184−187.
[18] 李小欢, 谢远娇, 王欢, 等. 不同栽培基质桑黄化学成分及抗氧化活性比较[J]. 食品安全质量检测学报, 2021, 12(23):9183−9188 LI X H, XIE Y J, WANG H, et al. Comparison of chemical constituents and antioxidant activities of SangHuangprous vaninii in different substrates[J]. Journal of Food Safety and Quality, 2016, 35(12):184−187.
[19] 王伟科, 宋吉玲, 闫静, 等. 采收期对代料栽培桑黄子实体活性成分含量和抗氧化活性的影响[J]. 菌物学报, 2020, 39(12):2369−2379 WANG W K, SONG J L, YAN J, et al. Effects of harvest time on content of active components and antioxidant activities of fruiting bodies of Sanghuangporus cultivated with substitute materials[J]. Mycosystema, 2020, 39(12):2369−2379.
[20] 胡文继. 猴头菌发酵菌丝体纯化多糖的抗阿尔茨海默症活性研究[D]. 长春:吉林大学, 2021 HU W J. Study on the anti-Alzheimer′s disease activity of purified polysaccharides from Hericium erinaceus fermentation mycelium[D]. Changchun, Jilin University, 2021.
[21] 吴亚召, 雷萍, 张文隽, 等. 桑黄黄酮液体发酵培养基的优化[J]. 中国食用菌,2016,35(5):21−23,27 doi: 10.13629/j.cnki.53-1054.2016.05.006 WU Y Z, LEI P, ZHANG W J, et al. Optimization of liquid medium for fermenting flavones from Phellinus linteus[J]. Edible Fungi of China,2016,35(5):21−23,27. doi: 10.13629/j.cnki.53-1054.2016.05.006
[22] 张梅梅, 魏志文, 刘玉冰, 等. Folin-Ciocalteu比色法测定桦褐孔菌多酚的条件优化[J]. 菌物学报,2011,30(2):295−304 ZHANG M M, WEI Z W, LIU Y B, et al. Optimization on determination of polyphenols from Inonotus obliquus by Folin-Ciocalteu colorimetry[J]. Mycosystema,2011,30(2):295−304.
[23] PAN L C, ZHU Y M, ZHU Z Y, et al. Chemical structure and effects of antioxidation and against α-glucosidase of natural polysaccharide from Glycyrrhiza inflata Batalin[J]. International Journal of Biological Macromolecules,2020,155:560−571. doi: 10.1016/j.ijbiomac.2020.03.192
[24] 连俊辉. 花脸香蘑菌丝体多糖的提取、抗氧化性及其益生活性研究[D]. 长春:吉林大学, 2021 LIAN J H. Study on extraction, antioxidant activity and probiotics activity of polysaccharide from mycelia of Lepista Sordida[D]. Changchun:Jilin University, 2021.
[25] 徐高飞. 七种食药用菌子实体的营养和功能成分及抗氧化分析[D]. 南宁:广西大学, 2020 XU G F. Analysis of nutritional and functional components and antioxidation of fruiting bodies among seven edible and medicinal musheroom[D]. Nanning:Guangxi University, 2020.
[26] 张晨. 杏鲍菇菌丝体多糖的分离纯化及抗衰老、抗糖尿病活性分析[D]. 泰安:山东农业大学, 2018 ZHANG C. Purification, anti-aging and anti-diabetic effects of mycelia polysaccharides feom Pleurotus eryngii[D]. Taian:Shandong Agricultural University, 2018.
[27] ZHANG H, NIE S P, CUI S W, et al. Characterization of a bioactive polysaccharide from Ganoderma atrum:Re-elucidation of the fine structure[J]. Carbohydrate Polymers,2017,158:58−67. doi: 10.1016/j.carbpol.2016.11.088
[28] WANG J, CHEN H X, WANG Y W, et al. Synthesis and characterization of a new Inonotus obliquus polysaccharide-iron (III) complex[J]. International Journal of Biological Macromolecules,2015,75:210−217. doi: 10.1016/j.ijbiomac.2015.01.041
[29] 岳雨曦, 王小燕, 柏丁丁, 等. 野阳合多糖及其纯化组分对胆汁酸的结合能力[J]. 食品科学,2018,39(12):154−160 YUE Y X, WANG X Y, BAI D D, et al. Characterization and bile acid-binding ability of polysaccharides purified from tubers of Habenaria ciliolaris Kranzl its fractions[J]. Food Science,2018,39(12):154−160.
[30] GAO Z, YUAN F F, LI H P, et al. The ameliorations of Ganoderma applanatum residue polysaccharides against CCl4 induced liver injury[J]. International Journal of Biological Macromolecules,2019,137:1130−1140. doi: 10.1016/j.ijbiomac.2019.07.044
[31] CHEN Z, ZHANG W, TANG X Y, et al. Extraction and characterization of polysaccharides from Semen Cassiae by microwave-assisted aqueous two-phase extraction coupled with spectroscopy and HPLC[J]. Carbohydrate Polymers,2016,144:263−270. doi: 10.1016/j.carbpol.2016.02.063
[32] LI S H, GAO A, DONG S, et al. Purification, antitumor and immunomodulatory activity of polysaccharides from soybean residue fermented with Morchella esculenta[J]. International Journal of Biological Macromolecules,2017,96:26−34. doi: 10.1016/j.ijbiomac.2016.12.007
[33] 赵彪希, 张海德, 张媚健, 等. 冬虫夏草多糖单糖组成及免疫活性研究[J]. 食品工业科技,2020,41(13):27−31 doi: 10.13386/j.issn1002-0306.2020.13.005 ZHAO B X, ZHANG H D, ZHANG M J, et al. The Monosaccharides composition and immune activity of polysaccharides from Cordyceps sinensis[J]. Science and Technology of Food Industry,2020,41(13):27−31. doi: 10.13386/j.issn1002-0306.2020.13.005
[34] XU S Y, LIU J P, HUANG X S, et al. Ultrasonic-microwave assisted extraction, characterization and biological activity of pectin from jackfruit peel[J]. LWT-Food Science and Technology,2018,90:577−582. doi: 10.1016/j.lwt.2018.01.007
[35] DU Y Q, LIU Y, WANG J H. Polysaccharides from Umbilicaria esculenta cultivated in Huangshan Mountain and immunomodulatory activity[J]. International Journal of Biological Macromolecules,2015,72:1272−1276. doi: 10.1016/j.ijbiomac.2014.09.057
[36] 张建军. 红平菇菌丝体多糖的提取、结构分析和抗糖尿病作用研究[D]. 泰安:山东农业大学, 2016 ZHANG J J. Studies on the extraction, characterization, and anti-diabetic effects of mycelia polysaccarides from Pleurotus djamor[D]. Taian:Shandong Agricultural University, 2016.
[37] LUO X P, DUAN Y Q, YANG W Y, et al. Structural elucidation and immunostimulatory activity of polysaccharide isolated by subcritical water extraction from Cordyceps militaris[J]. Carbohydrate Polymers,2017,157:794−802. doi: 10.1016/j.carbpol.2016.10.066
[38] WAN X L, JIN X, WU X M, et al. Structural characterisation and antitumor activity against non-small cell lung cancer of polysaccharides from Sanghuangporus vaninii[J]. Carbohydrate Polymers,2022,276:118798. doi: 10.1016/j.carbpol.2021.118798
[39] 李有贵, 钟石, 计东风 . 野生与人工栽培桑黄子实体中的粗多糖和粗酚含量及药用活性比较[J]. 蚕业科学,2016 ,42 (5 ):882 −891 .LI Y G, ZHONG S, JI D F . A comparison on contents and medicinal activities of crude polysaccharides and crude polyphenols between wild and cultivated fruit bodies of Phellinus spp.[J]. Science of Sericulture,2016 ,42 (5 ):882 −891 .[40] 蔡铭, 陈思, 骆少磊, 等. 膜分离与醇沉技术纯化猴头菇粗多糖的比较[J]. 食品科学,2019,40(9):83−90 CAI M, CHEN S, LUO S L, et al. Comparison of membrane separation and alcohol precipitation for the separation of crude polysaccharides from Hericium erinaceus[J]. Food Science,2019,40(9):83−90.
-
期刊类型引用(7)
1. 张夏寅,朱婧婧,徐恩波,朱艳云,陈健初. 马铃薯复合蛋白挤压制备植物基肉干的质构及成型性研究. 食品与发酵工业. 2025(06): 208-217 .  百度学术
百度学术
2. 曲美霖,胡俊君,程哲,李云龙. 绿豆预熟化工艺及品质研究进展. 食品与机械. 2024(02): 227-232 .  百度学术
百度学术
3. 刘远琨,高婷婷,张丽,高泽岳,陈晨,乌玉洁,付宸睿. 挤压型植物基人造肉的来源及加工工艺研究进展. 粮食加工. 2024(04): 80-82+99 .  百度学术
百度学术
4. 朱志远,许石骏,黄子渝,耿树香,宁德鲁,叶永丽,孙秀兰. 挤压工艺对核桃蛋白高水分挤压组织化特性影响. 中国粮油学报. 2024(08): 105-113 .  百度学术
百度学术
5. 蔡硕,靳高阳,顾瑞娟,王玉堂. 萌发处理对藜麦分离蛋白结构和功能特性的影响. 中国食品学报. 2023(05): 11-20 .  百度学术
百度学术
6. 毕崇慧,马雨心,王莉,李凡,段玉敏,肖志刚,王鹏. 挤压温度对火麻蛋白理化、加工功能特性的影响. 食品安全质量检测学报. 2023(19): 280-287 .  百度学术
百度学术
7. 李玉蝶,李玟君,汪海燕,宋青云,庞子皓,肖一郎,汪超,李玮. 戊糖乳杆菌发酵对花生不同蛋白组分结构的影响. 食品科学. 2023(22): 74-79 .  百度学术
百度学术
其他类型引用(3)





 下载:
下载:


 下载:
下载:



