Simultaneous Determination of 76 Veterinary Drugs and Their Metabolites in Pork by QuEChERS-Ultra High Performance Liquid Chromatography-Tandem Mass Spectrometry
-
摘要: 为提高猪肉中多兽药残留检测的效率,建立了QuEChERS结合超高效液相色谱-串联质谱(UPLC-MS/MS)同时测定猪肉中5类76种兽药及其代谢物残留量的方法,包括喹诺酮类、磺胺类、硝基咪唑类、大环内酯类、苯并咪唑类。样品经酸化乙腈提取,无水硫酸钠盐析,提取液经C18和无水硫酸镁净化后分为两部分,一部分用于22种弱极性化合物的直接测定,另一部分氮吹浓缩后复溶,用于54种强极性化合物的测定。76种化合物均采用电喷雾电离正离子模式多反应监测(MRM),基质匹配外标法定量分析。结果表明,76种兽药及其代谢物线性关系良好,相关系数均大于0.995,方法定量限均低于10 μg/kg,加标回收率为61.3%~96.2%,相对标准偏差(RSD)为2.0%~14.6%。方法应用于170批市售猪肉,其中23批次样品检出2类5种兽药残留。该方法简便快速、准确可靠,适用于猪肉中多类兽药残留的快速筛查和精准检测。
-
关键词:
- 高效液相色谱-串联质谱 /
- QuEChERS /
- 猪肉 /
- 兽药残留
Abstract: In order to improve the efficiency of the detection of multiple veterinary drug residues in pork, a method for the simultaneous determination of 5 types of 76 veterinary drugs and their metabolites residues in pork, including quinolones, sulfonamides, nitroimidazoles, macrolides and benzimidazoles, was established by QuEChERS combined with ultra-high performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS). The samples were extracted with acidified acetonitrile and salted out by anhydrous sodium sulfate. The extract was divided into two parts after purified by C18 and anhydrous magnesium sulfate. One part was used for direct determination of the 22 weakly polar compounds, and the other part was concentrated by nitrogen blowing for the determination of the 54 strongly polar compounds. The 76 compounds were analyzed in multiple reaction monitoring (MRM) mode via electrospray ionization, and quantified by matrix matching external standard method. The results showed that the correlation coefficients were greater than 0.995, and the limits of quantification (LOQs) were lower than 10 μg/kg. The recoveries ranged from 61.3% to 96.2%, with the relative standard deviation (RSD) between 2.0% and 14.6%. The method was applied to 170 pork samples sold in the market, 23 samples of which were detected with 2 types of 5 veterinary drugs residues. The method was simple, rapid, accurate, reliable, and suitable for rapid screening and accurate detection of multiple veterinary drug residues in pork. -
我国是猪肉生产和消费大国,其质量安全问题主要来源于兽药残留[1-3]。长期食用兽药残留超标的猪肉,会造成人体内兽药蓄积,抑制人体的免疫功能,危害人体健康[4-6]。兽药种类繁多,结构多样,化学性质也存在较大差异[7-9]。目前的国标检测方法大多是测定某一种或某一类药物,在实际检测中往往需要反复取样,并采用不同的方法进行样品前处理,耗时耗力,无法实现对多种类兽药残留的同时检测,因而在发生食品安全突发事件时和应急保障工作中就显得力不从心[10-12]。因此,简便、快速、高通量、高灵敏度已成为未来兽药残留检测领域发展的趋势[13-15]。
近年来,快速、简便、便宜、高效、可靠、安全的QuEChERS样品前处理方法结合高灵敏度、高选择性的超高效液相色谱-串联质谱(UPLC-MS/MS)技术已经开始应用于动物源性食品的兽药残留检测[16-20],研究者通过不断改进净化方式和净化材料,对动物源性食品中的多种类兽药残留的测定进行了探索[21-22]。值得一提的是,兽药理化性质差异较大,色谱保留能力和溶解性也各不相同,采用QuEChERS技术净化后得到的溶液通常为高比例有机相,若直接进样容易出现不同程度的溶剂效应。许多研究者采用氮吹后高比例水相复溶的方式来减少溶剂效应,但往往一些弱极性的兽药又难以复溶。针对这一问题,本研究建立了一种基于化合物色谱行为和溶解性的集成化分类方式,以理化性质各异的18种喹诺酮类、23种磺胺类、10种硝基咪唑类、9种大环内酯类、16种苯并咪唑类兽药及其代谢物作为研究对象,将这76种化合物分为弱极性的Q1组和强极性的Q2组,选择猪肉为代表基质,采用QuEChERS技术一步净化后分组进行UPLC-MS/MS测定,既能解决弱极性化合物的溶解性问题又能减少强极性化合物的溶剂效应。该方法操作简便、快速、灵敏度和准确度高,有拓展更多类别兽药及其代谢物的潜力,为猪肉中多类别兽药残留检测提供了有力的技术支撑。
1. 材料与方法
1.1 材料与仪器
甲醇中18种喹诺酮类混标溶液、甲醇中23种磺胺类混标溶液、乙腈中10种硝基咪唑类混标溶液、甲醇中9种大环内酯类抗生素混标溶液、甲醇中16种苯丙咪唑类混标溶液 100 μg/mL,天津阿尔塔科技有限公司;乙腈、甲醇 色谱纯,德国Merck公司;甲酸 色谱纯,德国CNW公司;N-丙基乙二胺(PSA)、十八烷基键合硅胶(C18)(40~50 μm)、石墨化炭黑(GCB) 天津Agela Technologies公司;无水硫酸钠、无水硫酸镁 分析纯,重庆川东化工公司;聚四氟乙烯(PTFE)滤膜 0.22 μm,美国Agilent公司;实验用水 超纯水;猪肉样品 购自重庆市内超市及农贸市场。
QTRAP 5500型三重四级杆/复合线性离子阱质谱仪 美国AB SCIEX公司; Acquity UPLC H-Class超高效液相色谱仪 美国WATERS公司;VORTEX GENIUS3型涡旋振荡仪 德国IKA公司;Milli-Q型超纯水机 美国Millipore公司;MSE225P-ICE-DU型电子天平 德国Sartorius公司;超声波清洗器 德国Elma公司;MD200-2型氮吹仪 杭州奥盛仪器有限公司。
1.2 实验方法
1.2.1 标准溶液的配制
标准中间溶液:分别准确移取1 mL标准品,用乙腈定容至10 mL,得到10 μg/mL的标准中间溶液,−20 ℃避光保存。
混合标准工作溶液:分别移取1 mL标准中间溶液,用乙腈定容至10 mL,得到1 μg/mL混合标准工作溶液,4 ℃避光保存。
1.2.2 样品前处理
1.2.2.1 样品提取
称取均质试样5 g(精确至0.01 g)于50 mL离心管中,加入2 mL乙腈饱和的正己烷,涡旋混合30 s,再加入0.2%甲酸乙腈10 mL,涡旋混合30 s;加入6 g无水硫酸钠后迅速振摇,涡旋1 min,37 kHz超声提取15 min后,以8000 r/min离心5 min,待净化。
1.2.2.2 提取液净化
移取5 mL提取液到含有500 mg无水硫酸镁和500 mg C18吸附剂的离心管中,涡旋1 min后以8000 r/min离心5 min。离心后取1 mL上清液经0.22 μm PTFE滤膜过滤后供Q1组目标化合物的测定;同时取2 mL上清液在40 ℃下用氮气吹干,残渣中加入0.5 mL 0.1%甲酸乙腈-0.1%甲酸水(v/v,2:8),涡旋混匀后经0.22 μm PTFE滤膜过滤,供Q2组目标化合物的测定。
1.2.3 基质标准曲线的配制
称取7份阴性猪肉样品各5 g,按“1.2.2”操作步骤进行后,得到空白基质溶液,分别加入混合标准工作溶液,配制成基质标准系列工作溶液。
1.2.4 仪器条件
1.2.4.1 色谱条件
色谱柱:WATERS ACQUITY UPLC HSS T3(50 mm×2.1 mm,1.8 μm);柱温:40 ℃;流动相:A为0.1%甲酸乙腈,B为0.1%甲酸水;流速:0.4 mL/min;进样量:5 μL;Q1组梯度洗脱程序:0~1.0 min,90%~5% B;1.0~2.5 min,5% B;2.5~2.6 min,5%~90% B;2.6~4.0 min,90% B;Q2组梯度洗脱程序:0~4.5 min,95%~85% B;4.5~6.0 min,85%~5% B;6.0~6.5 min,5% B;6.5~6.6 min,5%~95% B;6.6~8 min,95% B。
1.2.4.2 质谱条件
离子源:电喷雾离子源(ESI);扫描方式:正离子扫描;监测模式:多反应监测(MRM);喷雾电压:5500 V;气帘气(CUR)压力:35 psi;雾化气(GS1)压力:50 psi;辅助气(GS2)压力:50 psi;离子源温度(TEM):550 ℃;76种兽药及其代谢物的质谱参数见表1。
表 1 76种兽药及其代谢物的保留时间、母离子、子离子、去簇电压和碰撞能量Table 1. Retention times, parent ions, product ions, declustering potentials (DPs), and collision energies (CEs) of the 76 veterinary drugs and their metabolites序号 分组 分类 化合物 保留时间(min) 母离子
(m/z)子离子( m/z ) DP(V) CE(eV) 1 Q1 喹诺酮类 氟甲喹 1.76 262.1 202.0*/244.1 80 43/23 2 Q1 喹诺酮类 恶喹酸 1.61 262.1 216.1*/244.1 80 28/23 3 Q1 喹诺酮类 萘啶酸 1.76 233.1 187.0*/215.1 90 31/19 4 Q1 磺胺类 磺胺喹恶啉 1.64 301.0 156.0*/108.0 50 23/33 5 Q1 磺胺类 苯甲酰磺胺 1.64 277.0 156.0*/108.0 100 15/31 6 Q1 磺胺类 磺胺苯吡唑 1.66 315.1 155.9*/222.1 100 28/23 7 Q1 磺胺类 磺胺硝苯 1.72 336.0 198.0*/294.0 100 28/20 8 Q1 大环内酯类 竹桃霉素 1.51 688.1 544.3*/158.2 40 24/32 9 Q1 大环内酯类 红霉素 1.54 734.1 576.3*/158.2 70 27/38 10 Q1 大环内酯类 克拉霉素 1.62 748.3 158.1*/590.2 50 38/23 11 Q1 大环内酯类 阿奇霉素 1.63 749.1 158.2*/591.3 60 38/30 12 Q1 大环内酯类 吉他霉素 1.60 772.1 108.9*/215.0 50 40/34 13 Q1 大环内酯类 交沙霉素 1.66 828.1 174.1*/109.4 50 39/40 14 Q1 大环内酯类 泰乐菌素 1.54 916.1 173.8*/772.6 50 44/39 15 Q1 大环内酯类 替米考星 1.43 869.5 174.1*/132.2 78 55/55 16 Q1 苯并咪唑类 丙氧苯咪唑 1.51 250.1 218.1*/176.1 100 23/38 17 Q1 苯并咪唑类 阿苯达唑 1.64 266.1 234.1*/191.1 100 27/42 18 Q1 苯并咪唑类 甲苯咪唑 1.66 296.2 264.1*/105.1 100 27/44 19 Q1 苯并咪唑类 芬苯达唑 1.77 300.0 268.1*/159.3 100 30/43 20 Q1 苯并咪唑类 氟苯达唑 1.69 314.2 123.4*/282.7 100 47/32 21 Q1 苯并咪唑类 芬苯达唑砜 1.65 332.1 300.0*/159.2 100 29/50 22 Q1 苯并咪唑类 奥芬达唑 1.51 316.0 159.0*/191.0 80 43/30 23 Q2 喹诺酮类 恩诺沙星 5.76 360.1 316.1*/245.3 80 28/36 24 Q2 喹诺酮类 环丙沙星 5.21 332.1 288.1*/245.1 80 25/33 25 Q2 喹诺酮类 培氟沙星 5.10 334.2 290.0*/233.0 100 23/35 26 Q2 喹诺酮类 沙拉沙星 5.88 386.1 342.1*/299.0 100 23/35 27 Q2 喹诺酮类 氧氟沙星 4.99 362.1 318.1*/261.1 100 24/34 28 Q2 喹诺酮类 洛美沙星 5.53 352.2 308.2*/265.1 103 21/45 29 Q2 喹诺酮类 诺氟沙星 4.94 320.2 276.2*/233.1 110 24/30 30 Q2 喹诺酮类 西诺沙星 6.02 263.1 188.8*/244.1 80 37/22 31 Q2 喹诺酮类 达氟沙星 5.69 358.1 340.1*/82.2 80 30/47 32 Q2 喹诺酮类 双氟沙星 5.90 400.0 299.2*/382.0 80 38/28 33 Q2 喹诺酮类 司帕沙星 5.90 393.0 292.1*/375.1 70 32/23 34 Q2 喹诺酮类 氟罗沙星 4.81 370.1 326.2*/269.0 70 22/30 35 Q2 喹诺酮类 马波沙星 4.46 363.2 72.2*/345.1 60 22/22 36 Q2 喹诺酮类 依诺沙星 4.68 321.2 232.0*/303.0 60 45/32 37 Q2 喹诺酮类 奥比沙星 5.78 396.1 352.0*/295.0 70 21/32 38 Q2 磺胺类 磺胺嘧啶 2.20 251.1 156.0*/108.1 63 22/34 39 Q2 磺胺类 磺胺二甲基嘧啶 4.20 279.1 156.1*/186.1 75 35/25 40 Q2 磺胺类 磺胺甲基嘧啶 3.19 265.1 156.1*/172.0 73 24/24 41 Q2 磺胺类 磺胺间甲氧嘧啶 5.50 281.1 156.1*/108.1 85 24/31 42 Q2 磺胺类 磺胺甲基异噁唑 5.91 254.1 156.1*/108.1 100 21/32 43 Q2 磺胺类 磺胺间二甲氧嘧啶 6.21 311.1 156.1*/108.1 60 25/33 44 Q2 磺胺类 磺胺邻二甲氧嘧啶 5.93 311.1 156.1*/108.1 60 25/33 45 Q2 磺胺类 磺胺氯哒嗪 5.60 285.1 156.1*/108.1 80 18/33 46 Q2 磺胺类 甲氧苄啶 4.05 291.1 230.0*/261.1 70 30/30 47 Q2 磺胺类 磺胺醋酰 1.74 215.1 156.1*/108.2 120 15/27 48 Q2 磺胺类 磺胺吡啶 2.89 250.1 156.1*/184.2 100 20/20 49 Q2 磺胺类 磺胺脒 0.60 215.1 156.1*/108.2 120 15/27 50 Q2 磺胺类 磺胺恶唑 4.11 268.0 156.1*/113.2 100 19/21 51 Q2 磺胺类 磺胺噻唑 2.81 256.1 156.1*/108.2 100 19/27 52 Q2 磺胺类 磺胺二甲异噁唑 6.04 268.0 156.1*/113.2 100 19/21 53 Q2 磺胺类 磺胺甲噻二唑 4.45 271.0 156.1*/108.2 100 19/27 54 Q2 磺胺类 磺胺二甲异嘧啶 2.19 279.1 124.1*/186.1 75 27/25 55 Q2 磺胺类 磺胺甲氧哒嗪 4.40 281.1 156.1*/108.1 85 24/31 56 Q2 磺胺类 磺胺对甲氧嘧啶 4.65 281.1 156.1*/108.1 85 24/31 57 Q2 硝基咪唑类 甲硝唑 1.54 172.1 82.0*/128.1 70 29/23 58 Q2 硝基咪唑类 地美硝唑 1.85 142.1 96.2*/81.0 60 20/31 59 Q2 硝基咪唑类 洛硝哒唑 2.05 201.4 140.1*/55.3 60 14/25 60 Q2 硝基咪唑类 4-硝基咪唑 0.77 114.1 83.9*/68.0 50 18/25 61 Q2 硝基咪唑类 羟基甲硝唑 1.12 187.7 123.0*/126.1 60 22/22 62 Q2 硝基咪唑类 2-甲基-5-硝基咪唑 1.06 128.2 41.8*/82.0 70 44/20 63 Q2 硝基咪唑类 羟甲基甲硝咪唑 1.49 158.3 55.0*/140.2 50 20/17 64 Q2 硝基咪唑类 氯甲硝咪唑 3.00 162.1 115.8*/144.8 80 21/20 65 Q2 硝基咪唑类 苯硝咪唑 2.64 164.1 118.1*/91.0 80 25/50 66 Q2 硝基咪唑类 异丙硝唑 5.74 169.8 124.1*/109.2 100 24/42 67 Q2 大环内酯类 螺旋霉素 5.93 843.4 174.0*/141.8 50 45/45 68 Q2 苯并咪唑类 噻苯咪唑 3.35 202.0 175.0*/131.3 120 34/43 69 Q2 苯并咪唑类 5-羟基噻苯咪唑 2.87 218.2 191.0*/147.2 100 34/43 70 Q2 苯并咪唑类 2-氨基-5-苯甲酰苯并咪唑 5.93 238.1 105.0*/133.1 120 32/32 71 Q2 苯并咪唑类 阿苯达唑-2-氨基砜 3.09 240.0 133.1*/198.1 120 37/25 72 Q2 苯并咪唑类 2-氨基氟苯达唑 5.97 256.1 95.0*/123.2 100 44/35 73 Q2 苯并咪唑类 阿苯达唑亚砜 5.44 282.2 208.0*/191.3 100 26/26 74 Q2 苯并咪唑类 阿苯达唑砜 6.02 298.2 159.0*/224.0 100 48/34 75 Q2 苯并咪唑类 5-羟基甲苯咪唑 5.92 298.2 160.0*/266.1 100 46/28 76 Q2 苯并咪唑类 坎苯达唑 6.00 303.2 217.0*/261.1 100 37/34 注:*表示定量离子。 2. 结果与分析
2.1 色谱条件的优化
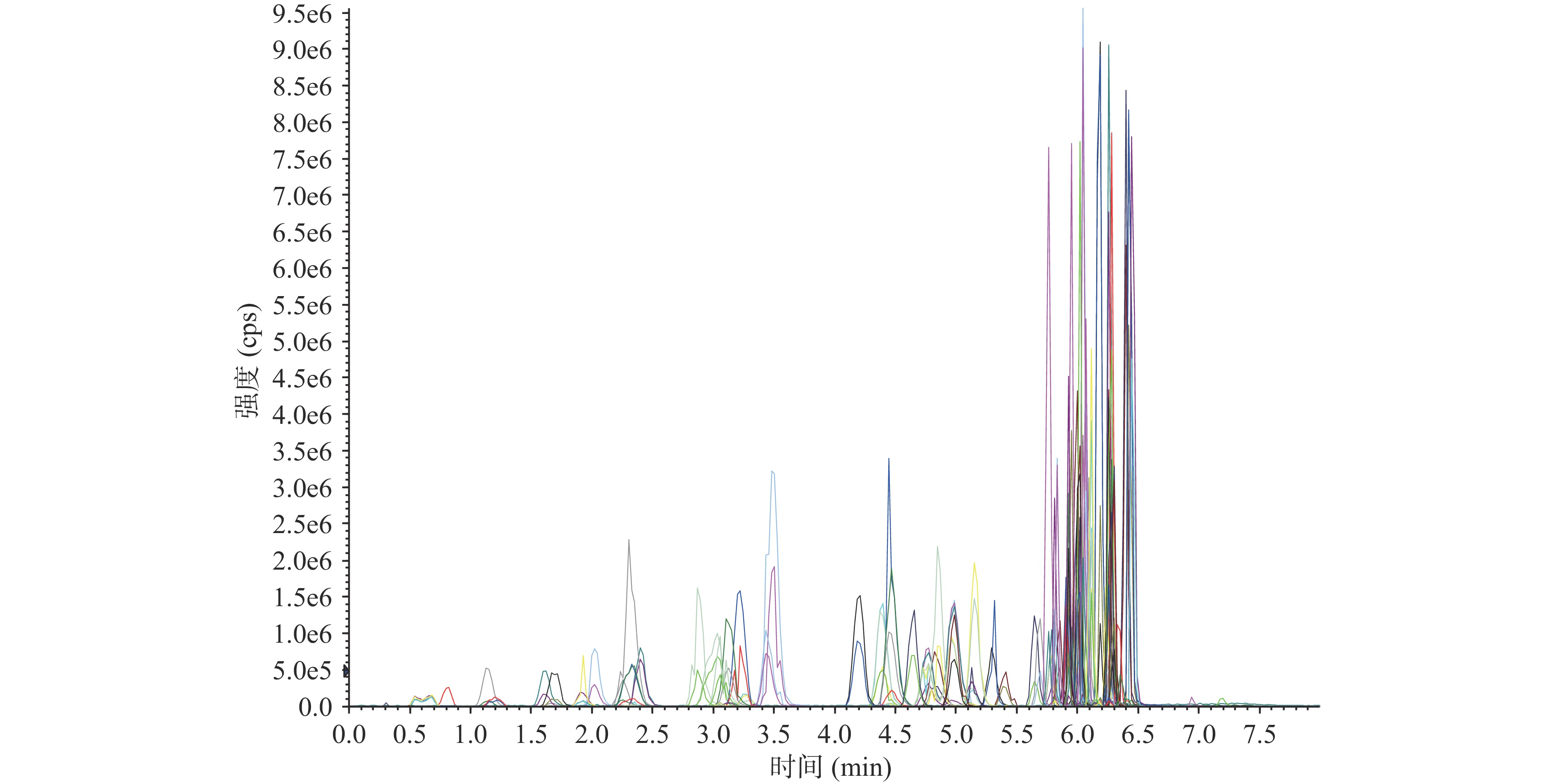
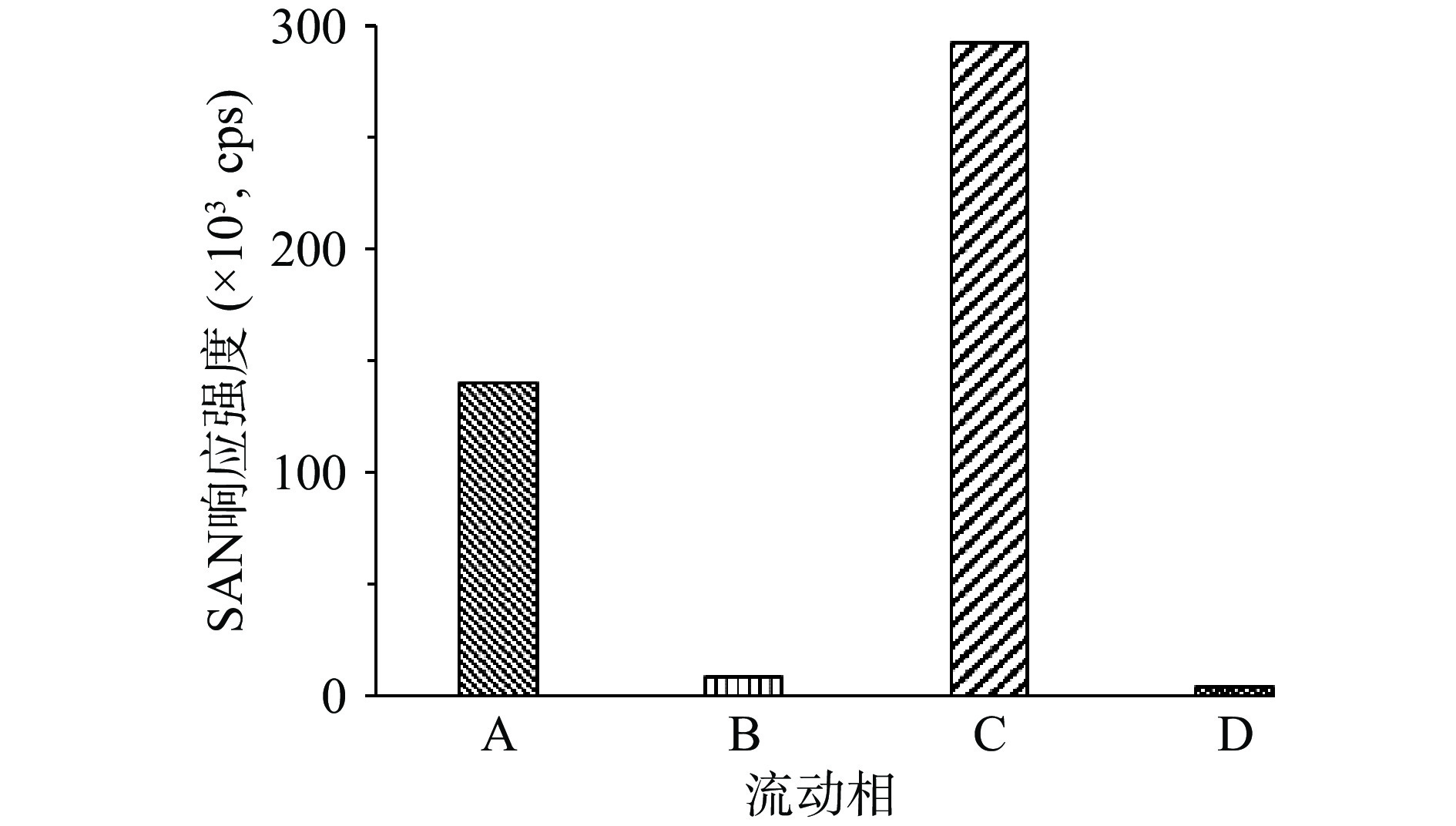
由于部分磺胺类及硝基咪唑类化合物的极性 较强,本研究选用对极性小分子保留性能优良的 WATERS ACQUITY HSS T3色谱柱进行色谱分离。考虑到样品前处理采用乙腈体系作为提取溶剂,本实验选择乙腈和水的混合体系作为流动相,并考察了流动相中引入pH调节剂甲酸或离子对试剂乙酸铵对76种兽药及其代谢物的色谱峰形及质谱响应的影响。结果表明,乙腈-水作流动相时,喹诺酮类和苯丙咪唑类化合物的色谱峰拖尾明显;乙腈-10 mmol/L乙酸铵水溶液作流动相时,喹诺酮类化合物峰形仍然不理想;0.1%甲酸乙腈-0.1%甲酸水溶液和0.1%甲酸乙腈-含0.1%甲酸10 mmol/L乙酸铵水溶液作流动相时,喹诺酮类和苯并咪唑类化合物的峰形均得到明显改善,说明流动相中引入甲酸可有效改善这两类化合物的峰形(图1)。但流动相中乙酸铵的引入会使得磺胺硝苯(SAN)的质谱响应降低1个数量级以上(图2),因此本研究选择0.1%甲酸乙腈-0.1%甲酸水溶液作为流动相进行梯度洗脱。考虑到磺胺类化合物有5组同分异构体(磺胺醋酰/磺胺脒、磺胺恶唑/磺胺二甲异噁唑、磺胺二甲基嘧啶/磺胺二甲异嘧啶、磺胺间甲氧嘧啶/磺胺对甲氧嘧啶/磺胺甲氧哒嗪、磺胺间二甲氧嘧啶/磺胺邻二甲氧嘧啶),实验采用先缓后陡的梯度洗脱程序,可以兼顾76种化合物的峰形和质谱响应。
2.2 复溶液的选择
由于76种兽药及其代谢物极性差异较大,因此样品前处理过程中复溶液的选择非常关键。本实验考察了76种化合物的混合标准溶液(30 ng/mL)氮吹干后,分别用0.1%甲酸乙腈-0.1%甲酸水体积比为5:95、20:80、50:50、80:20的溶液和0.1%甲酸乙腈复溶时各化合物的色谱行为,发现3种喹诺酮类、4种磺胺类、8种大环内酯类、7种苯并咪唑类共22种化合物(Q1组)无显著溶剂效应,而其它54种化合物(Q2组)在有机相占比越高时色谱保留能力越差。当有机相占比≤20%时,76种化合物色谱保留效果较好,无显著溶剂效应。由图3可见,复溶液中有机相占比越低,Q1组化合物尤其是苯并咪唑类的峰面积越小,这可能是由于这些化合物极性较弱,复溶液中乙腈含量变低后对这些化合物的溶解能力变差。结果表明,即使含有相同官能团的同类别的兽药,其色谱保留效果和溶解性也存在较大差异,因此现行标准中同类别兽药同时检测的方法并不合理。
本实验根据色谱行为和溶解性将76种兽药及其代谢物分为两组进行测定(Q1组和Q2组):Q1组为弱极性的22种化合物,在色谱柱上保留较好,无显著溶剂效应,因而经提取净化后的样液即可直接测定;Q2组为强极性的54种化合物,溶剂效应较强,样液需经氮吹后用0.1%甲酸乙腈-0.1%甲酸水溶液(v/v,2:8)复溶后测定。此外,由于Q1组化合物在色谱柱上普遍保留较强,按照2.1优化出的梯度条件洗脱后保留时间均集中在6.0~6.5 min。为节省分析时间,本研究采用更陡的梯度程序洗脱Q1组的22种化合物,见图4。
2.3 提取溶剂的优化
乙腈和甲醇是兽药残留检测中常用的提取剂,乙腈与甲醇相比渗透性更强且沉淀蛋白的效果更好,因此本实验选择乙腈作为主要提取溶剂。考虑到多数化合物含碱性基团,适量添加甲酸可以提供酸性环境,与目标化合物结合成盐从而提高提取效率,本实验考察了乙腈和0.1%、0.2%、0.5%、1%、2%、5%甲酸乙腈作为提取剂时,猪肉基质中Q1组和Q2组化合物的平均回收率(图5a和图5b)。实验发现,当采用小于0.2%的甲酸乙腈提取时,可提高各类化合物的平均回收率,这可能是由于甲酸的加入提高了各化合物在乙腈中的溶解度[23];当采用大于0.2%的甲酸乙腈提取时,除喹诺酮类以外,其它4类化合物的平均回收率逐渐下降,这可能是由于甲酸含量的增加提高了提取剂对基质的渗透作用,使得更多的共提物进入到提取液中造成基质干扰,降低了化合物的离子化效率[24];其中Q2组的磺胺类平均回收率下降最明显,当采用5%甲酸乙腈提取时,平均回收率低至13.7%,较0.2%甲酸乙腈提取时降低了80.4%,这可能是由于氮吹导致磺胺在过高的酸性环境下发生了一定程度的损失[15,23]。从图6可以看出,当采用0.2%甲酸乙腈作为提取剂时,回收率在60%~120%范围内的化合物最多。因此本研究最终选择0.2%甲酸乙腈作为提取剂。
2.4 净化条件的优化
QuEChERS方法常用的吸附剂主要有PSA、C18和GCB,PSA可用来去除有机酸、糖类等极性干扰物,C18能够吸附脂肪、磷脂等非极性杂质,GCB对平面结构分子有很强的亲和性,能有效去除色素和甾醇。由于PSA对喹诺酮类和磺胺类存在吸附作用[25-28],本实验选择C18和GCB考察猪肉基质中76种兽药及其代谢物的回收率,发现样品提取液经GCB净化后,磺胺硝苯、苯硝咪唑、螺旋霉素、替米考星以及18种喹诺酮类和16种苯并咪唑类化合物回收率均低于20%。因此,本研究选择C18作为吸附剂。
实验考察了使用50、100和200 mg/mL C18吸附剂时76种兽药及其代谢物的回收率,发现各化合物的回收率均无显著变化。然而,猪肉样品基质复杂,采用0.2%甲酸乙腈提取时容易共提出大量的磷脂,造成污染仪器,降低色谱柱寿命。因此,本实验进一步比较了不同用量C18吸附剂对猪肉样品提取液中磷脂的净化效果。将液相色谱柱替换为双通接头后,以猪肉中最为常见的磷脂酰胆碱(PC)作为代表磷脂,选择PC的特征碎片离子m/z 184进行母离子扫描得到总离子流图[29]。由图7可见,采用C18吸附剂净化后,无论是直接测定还是氮吹后复溶再测定,PC峰均明显降低,且出峰时间越靠后的PC峰降低越明显。图7c和图7f表明,0.9 min左右的色谱峰高均随着C18吸附剂用量的增加逐渐下降;采用Q1组的直接测定法,当C18吸附剂的用量≥50 mg/mL时峰高变化不明显;采用Q2组的氮吹后测定法,当C18吸附剂的用量≥100 mg/mL时峰高变化不明显。因此,本研究确定每1 mL样品提取液中C18吸附剂的用量为100 mg。
![]() 图 7 按照Q1组和Q2组样品前处理操作时猪肉基质提取液净化效果注:a为按照Q1组样品前处理操作净化前的色谱图;b为按照Q1组样品前处理操作净化后的色谱图;c为按照Q1组样品前处理操作不同用量C18吸附剂时PC质谱响应;d为按照Q2组样品前处理操作净化前的色谱图;e为按照Q2组样品前处理操作净化后的色谱图;f为按照Q2组样品前处理操作不同用量C18吸附剂时PC质谱响应。Figure 7. Purification effect of the extract solution from pork when using sample pretreatment of group Q1 and Q2
图 7 按照Q1组和Q2组样品前处理操作时猪肉基质提取液净化效果注:a为按照Q1组样品前处理操作净化前的色谱图;b为按照Q1组样品前处理操作净化后的色谱图;c为按照Q1组样品前处理操作不同用量C18吸附剂时PC质谱响应;d为按照Q2组样品前处理操作净化前的色谱图;e为按照Q2组样品前处理操作净化后的色谱图;f为按照Q2组样品前处理操作不同用量C18吸附剂时PC质谱响应。Figure 7. Purification effect of the extract solution from pork when using sample pretreatment of group Q1 and Q22.5 基质效应
基质效应是样品离子化时样品基质与目标化合物相互竞争电离而导致目标化合物的响应强度发生不同程度增强或减弱的现象。按照公式:基质效应(ME,%)=(样品基质中添加相同含量化合物的响应值/纯溶剂中化合物的响应值−1)×100,计算76种兽药及其代谢物的基质效应,ME为正值表示增强的基质效应,负值表示抑制的基质效应,绝对值越大表示基质效应越强[30],见表2。76种兽药及其代谢物中有3种喹诺酮类、1种磺胺类、6种大环内酯类、3种苯并咪唑类化合物基质效应的绝对值高于20%,说明猪肉基质复杂,即使采用QuEChERS技术净化后仍然对部分化合物存在较强的基质效应。因此,本研究采用空白基质标准曲线定量来校正基质效应。
表 2 76种化合物的回归方程、相关系数、定量限、加标回收率、相对标准偏差和基质效应(n=6)Table 2. Regression equations, correlation coefficients (r), limits of quantitations (LOQs), spiked recoveries, RSD andMe of the 76 compounds (n=6)序号 化合物 线性方程 相关系数r LOQ
(μg/kg)低水平加标(μg/kg) 中水平加标(μg/kg) 高水平加标(μg/kg) 基质效应
(%)回收率(%) RSD(%) 回收率(%) RSD(%) 回收率(%) RSD(%) A 喹诺酮类 1 恩诺沙星 y=8.77919e4 x+4.84266e4 0.99887 0.4 64.1 7.5 71.4 7.9 71.7 9.4 10.5 2 环丙沙星 y=4.18761e4 x+17851.16215 0.99995 1.6 61.8 5.7 67.5 5.9 66.7 4.6 −7.9 3 培氟沙星 y=6.63777e4 x−3354.75582 0.99983 1.0 71.1 7.8 77.3 6.3 77.0 3.5 12.3 4 沙拉沙星 y=5.99307e4 x+6.50456e4 0.99921 0.5 61.3 5.2 66.6 5.4 66.8 6.1 −5.5 5 氧氟沙星 y=1.45192e5 x+3.99343e4 0.99961 0.7 66.5 2.9 75.5 2.4 74.2 7.5 17.3 6 洛美沙星 y=8.77989e4 x−7611.92400 0.99968 1.2 63.8 7.7 69.8 5.0 69.6 4.4 4.2 7 氟甲喹 y=1.35255e5 x+6475.09899 0.99966 1.0 73.5 8.2 80.4 7.3 78.8 7.8 35.9 8 诺氟沙星 y=4.15611e4 x+2827.31987 0.99999 0.6 63.1 8.9 71.3 7.6 72.1 4.4 8.0 9 西诺沙星 y=5.93231e4 x+9574.84394 0.99993 0.5 70.4 2.4 74.1 6.7 76.1 8.5 18.9 10 达氟沙星 y=2.29035e5 x+3.79034e5 0.99587 0.4 69.2 5.3 77.9 4.2 77.8 8.8 19.1 11 恶喹酸 y=4772.72729 x+3.07264e4 0.99532 6.6 91.9 9.5 86.4 7.5 93.6 8.3 2.9 12 萘啶酸 y=1.51124e5 x+1.46960e5 0.99589 0.4 76.4 5.4 79.9 9.8 82.3 4.7 31.0 13 双氟沙星 y=24869.42943 x−11043.08797 0.99989 0.7 67.2 8.1 74.2 7.8 74.4 7.0 31.5 14 司帕沙星 y=7.50198e4 x+7117.77919 0.99968 0.5 61.9 6.4 67.1 4.0 68.2 7.0 0.9 15 氟罗沙星 y=9.32207e4 x−13190.26022 0.99994 0.6 64.5 7.2 69.0 3.9 70.2 7.0 18.5 16 马波沙星 y=5.80599e4 x−7484.00978 0.99992 0.6 61.6 6.3 69.2 14.2 66.3 7.2 4.1 17 依诺沙星 y=7.31679e4 x+26628.95143 0.99825 0.8 63.1 6.5 69.6 7.1 71.6 10.3 2.8 18 奥比沙星 y=9.19517e4 x+1.33648e5 0.99985 0.5 64.5 6.8 63.1 4.0 66.9 9.1 13.5 B 磺胺类 1 磺胺嘧啶 y =5.84613e4 x+6053.52902 0.99928 1.0 72.1 5.7 70.4 5.7 76.1 11.3 −15.5 2 磺胺二甲基嘧啶 y =15303.64269 x+4893.06738 0.99961 0.9 71.6 3.5 75.1 4.2 76.7 10.9 −13.0 3 磺胺甲基嘧啶 y=6.46915e4 x−2498.83651 0.99938 0.5 78.5 6.4 75.6 3.8 78.3 4.3 −17.8 4 磺胺间甲氧嘧啶 y =5.25886e4 x+3980.10513 0.9998 0.7 72.3 7.4 69.2 3.1 73.7 8.3 19.2 5 磺胺甲基异噁唑 y =3.69051e4 x+8854.49948 0.99985 0.8 73.8 4.3 75.4 5.8 77.8 8.4 0.1 6 磺胺间二甲氧嘧啶 y=1.14726e5 x+7.88381e4 0.99808 1.4 68.9 6.5 70.1 7.2 72.9 5.3 19.6 7 磺胺邻二甲氧嘧啶 y=1.08816e5 x+8.06670e4 0.99632 1.5 72.2 4.8 73.6 5.8 76.3 12.2 3.9 8 磺胺喹恶啉 y=4.19304e4 x+3.83946e4 0.99816 0.5 83.1 6.1 87.3 3.3 89.6 4.0 5.3 9 磺胺氯哒嗪 y=5.04529e4 x−5999.96334 0.99995 0.7 65.5 5.2 65.7 4.6 69.1 13.3 15.5 10 甲氧苄啶 y=1.38957e5 x+4.38855e4 0.99778 0.6 62.4 13.0 64.4 12.4 66.9 4.5 14.2 11 磺胺醋酰 y=15113.48769 x−5063.34401 0.99699 1.2 67.1 6.8 68.7 13.0 71.2 10.0 19.5 12 磺胺吡啶 y=6.47060e4 x+8942.74485 0.99878 0.5 82.8 8.1 84.1 8.9 88.8 14.4 −22.7 13 磺胺脒 y=13912.19605 x+2735.05120 0.99997 1.0 70.4 9.0 67.7 8.6 72.5 7.9 7.3 14 磺胺恶唑 y=7.95421e4 x+24453.19716 0.99927 1.1 74.1 7.1 69.8 5.8 74.7 7.0 2.1 15 磺胺噻唑 y=6.42743e4 x+9122.26320 0.99988 0.9 73.3 6.8 69.2 3.8 75.2 7.0 −8.7 16 磺胺二甲异噁唑 y=4.25223e4 x+14870.05950 0.99883 1.2 69.4 3.4 65.9 6.5 71.8 5.4 9.9 17 磺胺甲噻二唑 y=5.73779e4 x+131.02092 0.99921 1.0 63.7 4.8 63.4 8.8 66.7 6.5 1.9 18 苯甲酰磺胺 y=4.63782e4 x+10966.83686 0.99950 1.8 82.2 5.7 85.5 5.6 89.1 3.4 −8.5 19 磺胺二甲异嘧啶 y=1.13749e5 x−5720.81666 0.99982 1.2 67.0 8.5 68.0 9.7 71.3 10.2 −19.2 20 磺胺甲氧哒嗪 y =6.38340e4 x+8075.34550 0.99994 0.8 64.8 9.2 68.9 5.3 70.3 8.8 19.3 21 磺胺苯吡唑 y=19023.10054 x+9056.69007 0.99822 0.8 82.8 3.6 90.2 3.5 91.1 2.9 4.3 22 磺胺硝苯 y=3620.11395 x+3.40577e4 0.99718 2.0 78.0 6.6 84.0 8.2 84.9 5.5 −18.6 23 磺胺对甲氧嘧啶 y=9.95313e4 x+23154.12760 0.99954 1.2 84.3 12.9 82.2 5.1 86.7 8.5 −10.2 C 硝基咪唑类 1 甲硝唑 y=4.47588e4 x−10207.54416 0.99989 1.2 78.6 5.0 86.3 6.7 84.6 4.4 −2.1 2 地美硝唑 y=6.63294e4 x+10630.09481 0.99992 1.0 72.0 6.0 73.4 5.0 76.2 14.6 9.3 3 洛硝哒唑 y=20704.64833 x−3229.22793 0.99994 0.8 80.1 12.4 80.9 6.8 85.0 4.4 −12.4 4 4-硝基咪唑 y=16555.59582 x+12972.60635 0.99678 1.4 65.0 6.3 68.6 10.4 69.3 6.6 2.3 5 羟基甲硝唑 y=6701.54251 x−3165.48560 0.99711 2.0 70.2 10.6 72.1 7.1 74.8 8.8 2.2 6 2-甲基-5-硝基咪唑 y=5940.05641 x+12547.97091 0.99976 0.6 70.9 8.9 75.7 5.2 75.5 13.1 −7.1 7 羟甲基甲硝咪唑 y=11551.04400 x+4.15116e4 0.99672 1.8 72.6 6.9 69.7 9.2 74.3 5.3 11.3 8 氯甲硝咪唑 y=13661.14335 x+3950.87767 0.99740 2.1 68.3 8.5 74.5 4.8 76.5 10.6 4.1 9 苯硝咪唑 y=1.20497e5 x+6.34526e4 0.99981 0.6 65.6 4.0 68.8 3.8 69.9 7.3 15.9 10 异丙硝唑 y=8.46358e4 x+2767.15574 0.99977 0.5 65.6 9.3 63.6 9.5 68.0 8.8 0.3 D 大环内酯类 1 竹桃霉素 y=1.50001e5 x+13805.95765 0.99944 0.9 88.5 6.8 96.2 9.5 95.0 7.9 −19.0 2 红霉素 y=11771.66737 x−4635.79587 0.99802 1.0 94.7 8.0 93.0 11.1 96.2 6.4 −31.1 3 克拉霉素 y=8.72120e4 x−3.66243e4 0.99906 1.2 83.4 6.9 87.5 6.4 89.7 7.7 −26.2 4 阿奇霉素 y=27376.31810 x−3754.40816 0.99968 0.7 85.3 12.6 82.7 14.3 87.8 6.6 −20.2 5 吉他霉素 y=1343.82820 x+914.46496 0.99662 1.0 74.0 5.6 78.1 6.9 80.0 4.8 −5.1 6 交沙霉素 y=1772.62792 x+4951.40019 0.99996 1.0 78.4 13.6 84.9 7.8 83.9 8.4 −31.8 7 螺旋霉素 y=2553.39535 x+1897.72306 0.99665 2.6 72.0 7.1 68.6 6.9 72.6 8.0 45.1 8 泰乐菌素 y=7142.20118 x−3284.89451 0.99792 8.8 85.8 9.8 90.8 8.8 92.5 6.4 3.4 9 替米考星 y=3103.37890 x+5314.52058 0.99649 8.9 68.7 12.8 75.1 10.9 75.0 6.8 20.2 E 苯并咪唑类 1 噻苯咪唑 y=2.66215e5 x+5.78693e4 0.9996 0.4 65.4 6.4 67.3 5.3 69.7 5.5 3.3 2 5-羟基噻苯咪唑 y=1.17664e5 x−543.07894 0.99970 0.5 70.1 7.3 67.9 5.4 72.9 13.5 2.4 3 2-氨基-5-苯甲
酰苯并咪唑y=1.02057e5 x+1846.69510 0.99977 0.9 61.6 4.5 63.8 7.1 69.2 4.5 −7.9 4 阿苯达唑-2-氨基砜 y=1.28590e5 x−19174.60489 0.99867 0.5 64.6 5.1 63.5 4.1 66.5 8.8 12.6 5 丙氧苯咪唑 y=2.37419e5 x+2.37457e5 0.99590 0.4 73.7 6.7 80.5 12.4 81.0 7.5 −2.1 6 2-氨基氟苯达唑 y=8.12271e4 x+23593.63964 0.99983 0.7 61.4 4.2 65.5 6.0 71.2 10.1 −9.7 7 阿苯达唑 y=2.35718e5 x+1.50045e5 0.99799 1.0 70.9 7.0 76.2 5.5 77.6 4.4 2.6 8 阿苯达唑亚砜 y=7.95412e4 x+861.48543 0.99994 0.4 64.9 5.7 63.0 4.9 67.4 4.5 23.5 9 甲苯咪唑 y=2.13796e5 x+1.80789e5 0.99739 0.6 79.8 2.0 84.5 10.8 86.6 6.5 7.3 10 阿苯达唑砜 y=1.44073e5 x+7.05995e4 0.99787 0.5 68.1 6.1 67.6 4.4 69.5 6.3 27.2 11 5-羟基甲苯咪唑 y=3.04862e4 x+5623.43029 0.99955 0.6 63.1 6.5 62.8 7.7 64.3 9.4 12.1 12 芬苯达唑 y=1.76930e5 x+9.22278e4 0.99662 1.0 71.0 3.2 75.6 2.4 77.1 5.0 15.7 13 坎苯达唑 y=1.67852e5 x+1.54293e5 0.99573 0.5 63.7 7.3 65.6 10.2 67.6 5.5 6.6 14 氟苯达唑 y=4.66398e4 x+12853.82427 0.99614 0.5 78.5 3.1 85.4 13.8 84.9 5.5 5.6 15 芬苯达唑砜 y=2.00387e5 x+8.12650e4 0.99848 0.6 79.9 3.4 86.8 12.1 85.1 3.7 8.3 16 奥芬达唑 y=1.33556e5 x+6.25765e4 0.99718 0.7 79.3 5.6 82.6 9.2 84.6 5.3 21.6 2.6 方法学验证
2.6.1 线性范围与检出限
采用阴性猪肉样品制备空白基质标准曲线,按优化的实验条件进行测试,以目标化合物定量离子的峰面积(y)为纵坐标、质量浓度(x,ng/mL)为横坐标绘制标准曲线,得到76种兽药及其代谢物的线性回归方程和相关系数,如表2所示。结果表明,76种化合物在相应的浓度范围内线性关系良好,相关系数r均大于0.995,按照定量离子信噪比(S/N)≥10时计算定量限(LOQ),76种化合物的定量限(LOQ)均低于10 μg/kg。
2.6.2 回收率及精密度
在阴性猪肉样品中添加三个浓度水平的标准溶液,分别进行6次平行实验,考察76种化合物的加标回收率和精密度。结果表明,76种化合物回收率范围在61.3%~96.2%之间,相对标准偏差(RSD)在2.0%~14.6%之间,符合GB/T 27404-2008《实验室质量控制规范 食品理化检测》 附录F中对回收率及精密度的要求,可满足日常检测需要。
2.7 实际样品测定
采用本研究建立的方法,对170批次猪肉样品进行全面筛查,其中23批次样品检出5种兽药残留量超出GB 31650-2019《食品安全国家标准 食品中兽药最大残留限量》规定限量。与现行国家标准方法进行比较,实验结果采用配对T检验方法进行分析,结果显示5个项目P>0.05,差异无统计学意义,因此认为两种方法检测结果无显著性差异,详见表3。
表 3 本方法与国家标准方法比较Table 3. Comparison between established method and the state standard methods
方法恩诺沙星 磺胺间甲氧嘧啶 磺胺嘧啶 磺胺甲基嘧啶 甲氧苄啶 本文所建
方法本文所建
方法本文所建
方法GB 31658.17-2021 本文所建
方法GB 31658.17-2021 本文所建
方法GB 31658.17-2021 本文所建
方法GB/T 21316-2007 检测值
(μg/kg)3853 3812 1900 2004 517 518 277 281 79.4 79.7 514 498 14562 14598 520 527 770 779 87.3 87.3 382 378 3915 3951 204 202 3552 3497 100.5 99.7 393 407 416 422 354 361 402 409 66.1 67.9 233 235 / / 417 423 / / / / 169 173 / / / / / / / / P 0.428 0.116 0.106 0.611 0.592 注:“/”表示未检出。 3. 结论
本研究结合QuEChERS样品前处理技术和UPLC-MS/MS技术,建立了可同时检测猪肉中性质各异的5类76种兽药及其代谢物的方法。根据化合物色谱行为和溶解性,将76种兽药及其代谢物进行集成化归类,分为弱极性的Q1组22种化合物和强极性的Q2组54种化合物,以猪肉为代表基质,采用一步净化后分组测定的方式,既能解决弱极性化合物的溶解性问题又能减少强极性化合物的溶剂效应。在优化的色谱质谱条件以及样品前处理提取、净化和复溶条件下,该方法测定76种化合物回收率范围在61.3%~96.2%之间,相对标准偏差(RSD)小于15%,LOQ小于10 μg/kg,可满足猪肉中多类别兽药残留同时检测的需要。
-
图 7 按照Q1组和Q2组样品前处理操作时猪肉基质提取液净化效果
注:a为按照Q1组样品前处理操作净化前的色谱图;b为按照Q1组样品前处理操作净化后的色谱图;c为按照Q1组样品前处理操作不同用量C18吸附剂时PC质谱响应;d为按照Q2组样品前处理操作净化前的色谱图;e为按照Q2组样品前处理操作净化后的色谱图;f为按照Q2组样品前处理操作不同用量C18吸附剂时PC质谱响应。
Figure 7. Purification effect of the extract solution from pork when using sample pretreatment of group Q1 and Q2
表 1 76种兽药及其代谢物的保留时间、母离子、子离子、去簇电压和碰撞能量
Table 1 Retention times, parent ions, product ions, declustering potentials (DPs), and collision energies (CEs) of the 76 veterinary drugs and their metabolites
序号 分组 分类 化合物 保留时间(min) 母离子
(m/z)子离子( m/z ) DP(V) CE(eV) 1 Q1 喹诺酮类 氟甲喹 1.76 262.1 202.0*/244.1 80 43/23 2 Q1 喹诺酮类 恶喹酸 1.61 262.1 216.1*/244.1 80 28/23 3 Q1 喹诺酮类 萘啶酸 1.76 233.1 187.0*/215.1 90 31/19 4 Q1 磺胺类 磺胺喹恶啉 1.64 301.0 156.0*/108.0 50 23/33 5 Q1 磺胺类 苯甲酰磺胺 1.64 277.0 156.0*/108.0 100 15/31 6 Q1 磺胺类 磺胺苯吡唑 1.66 315.1 155.9*/222.1 100 28/23 7 Q1 磺胺类 磺胺硝苯 1.72 336.0 198.0*/294.0 100 28/20 8 Q1 大环内酯类 竹桃霉素 1.51 688.1 544.3*/158.2 40 24/32 9 Q1 大环内酯类 红霉素 1.54 734.1 576.3*/158.2 70 27/38 10 Q1 大环内酯类 克拉霉素 1.62 748.3 158.1*/590.2 50 38/23 11 Q1 大环内酯类 阿奇霉素 1.63 749.1 158.2*/591.3 60 38/30 12 Q1 大环内酯类 吉他霉素 1.60 772.1 108.9*/215.0 50 40/34 13 Q1 大环内酯类 交沙霉素 1.66 828.1 174.1*/109.4 50 39/40 14 Q1 大环内酯类 泰乐菌素 1.54 916.1 173.8*/772.6 50 44/39 15 Q1 大环内酯类 替米考星 1.43 869.5 174.1*/132.2 78 55/55 16 Q1 苯并咪唑类 丙氧苯咪唑 1.51 250.1 218.1*/176.1 100 23/38 17 Q1 苯并咪唑类 阿苯达唑 1.64 266.1 234.1*/191.1 100 27/42 18 Q1 苯并咪唑类 甲苯咪唑 1.66 296.2 264.1*/105.1 100 27/44 19 Q1 苯并咪唑类 芬苯达唑 1.77 300.0 268.1*/159.3 100 30/43 20 Q1 苯并咪唑类 氟苯达唑 1.69 314.2 123.4*/282.7 100 47/32 21 Q1 苯并咪唑类 芬苯达唑砜 1.65 332.1 300.0*/159.2 100 29/50 22 Q1 苯并咪唑类 奥芬达唑 1.51 316.0 159.0*/191.0 80 43/30 23 Q2 喹诺酮类 恩诺沙星 5.76 360.1 316.1*/245.3 80 28/36 24 Q2 喹诺酮类 环丙沙星 5.21 332.1 288.1*/245.1 80 25/33 25 Q2 喹诺酮类 培氟沙星 5.10 334.2 290.0*/233.0 100 23/35 26 Q2 喹诺酮类 沙拉沙星 5.88 386.1 342.1*/299.0 100 23/35 27 Q2 喹诺酮类 氧氟沙星 4.99 362.1 318.1*/261.1 100 24/34 28 Q2 喹诺酮类 洛美沙星 5.53 352.2 308.2*/265.1 103 21/45 29 Q2 喹诺酮类 诺氟沙星 4.94 320.2 276.2*/233.1 110 24/30 30 Q2 喹诺酮类 西诺沙星 6.02 263.1 188.8*/244.1 80 37/22 31 Q2 喹诺酮类 达氟沙星 5.69 358.1 340.1*/82.2 80 30/47 32 Q2 喹诺酮类 双氟沙星 5.90 400.0 299.2*/382.0 80 38/28 33 Q2 喹诺酮类 司帕沙星 5.90 393.0 292.1*/375.1 70 32/23 34 Q2 喹诺酮类 氟罗沙星 4.81 370.1 326.2*/269.0 70 22/30 35 Q2 喹诺酮类 马波沙星 4.46 363.2 72.2*/345.1 60 22/22 36 Q2 喹诺酮类 依诺沙星 4.68 321.2 232.0*/303.0 60 45/32 37 Q2 喹诺酮类 奥比沙星 5.78 396.1 352.0*/295.0 70 21/32 38 Q2 磺胺类 磺胺嘧啶 2.20 251.1 156.0*/108.1 63 22/34 39 Q2 磺胺类 磺胺二甲基嘧啶 4.20 279.1 156.1*/186.1 75 35/25 40 Q2 磺胺类 磺胺甲基嘧啶 3.19 265.1 156.1*/172.0 73 24/24 41 Q2 磺胺类 磺胺间甲氧嘧啶 5.50 281.1 156.1*/108.1 85 24/31 42 Q2 磺胺类 磺胺甲基异噁唑 5.91 254.1 156.1*/108.1 100 21/32 43 Q2 磺胺类 磺胺间二甲氧嘧啶 6.21 311.1 156.1*/108.1 60 25/33 44 Q2 磺胺类 磺胺邻二甲氧嘧啶 5.93 311.1 156.1*/108.1 60 25/33 45 Q2 磺胺类 磺胺氯哒嗪 5.60 285.1 156.1*/108.1 80 18/33 46 Q2 磺胺类 甲氧苄啶 4.05 291.1 230.0*/261.1 70 30/30 47 Q2 磺胺类 磺胺醋酰 1.74 215.1 156.1*/108.2 120 15/27 48 Q2 磺胺类 磺胺吡啶 2.89 250.1 156.1*/184.2 100 20/20 49 Q2 磺胺类 磺胺脒 0.60 215.1 156.1*/108.2 120 15/27 50 Q2 磺胺类 磺胺恶唑 4.11 268.0 156.1*/113.2 100 19/21 51 Q2 磺胺类 磺胺噻唑 2.81 256.1 156.1*/108.2 100 19/27 52 Q2 磺胺类 磺胺二甲异噁唑 6.04 268.0 156.1*/113.2 100 19/21 53 Q2 磺胺类 磺胺甲噻二唑 4.45 271.0 156.1*/108.2 100 19/27 54 Q2 磺胺类 磺胺二甲异嘧啶 2.19 279.1 124.1*/186.1 75 27/25 55 Q2 磺胺类 磺胺甲氧哒嗪 4.40 281.1 156.1*/108.1 85 24/31 56 Q2 磺胺类 磺胺对甲氧嘧啶 4.65 281.1 156.1*/108.1 85 24/31 57 Q2 硝基咪唑类 甲硝唑 1.54 172.1 82.0*/128.1 70 29/23 58 Q2 硝基咪唑类 地美硝唑 1.85 142.1 96.2*/81.0 60 20/31 59 Q2 硝基咪唑类 洛硝哒唑 2.05 201.4 140.1*/55.3 60 14/25 60 Q2 硝基咪唑类 4-硝基咪唑 0.77 114.1 83.9*/68.0 50 18/25 61 Q2 硝基咪唑类 羟基甲硝唑 1.12 187.7 123.0*/126.1 60 22/22 62 Q2 硝基咪唑类 2-甲基-5-硝基咪唑 1.06 128.2 41.8*/82.0 70 44/20 63 Q2 硝基咪唑类 羟甲基甲硝咪唑 1.49 158.3 55.0*/140.2 50 20/17 64 Q2 硝基咪唑类 氯甲硝咪唑 3.00 162.1 115.8*/144.8 80 21/20 65 Q2 硝基咪唑类 苯硝咪唑 2.64 164.1 118.1*/91.0 80 25/50 66 Q2 硝基咪唑类 异丙硝唑 5.74 169.8 124.1*/109.2 100 24/42 67 Q2 大环内酯类 螺旋霉素 5.93 843.4 174.0*/141.8 50 45/45 68 Q2 苯并咪唑类 噻苯咪唑 3.35 202.0 175.0*/131.3 120 34/43 69 Q2 苯并咪唑类 5-羟基噻苯咪唑 2.87 218.2 191.0*/147.2 100 34/43 70 Q2 苯并咪唑类 2-氨基-5-苯甲酰苯并咪唑 5.93 238.1 105.0*/133.1 120 32/32 71 Q2 苯并咪唑类 阿苯达唑-2-氨基砜 3.09 240.0 133.1*/198.1 120 37/25 72 Q2 苯并咪唑类 2-氨基氟苯达唑 5.97 256.1 95.0*/123.2 100 44/35 73 Q2 苯并咪唑类 阿苯达唑亚砜 5.44 282.2 208.0*/191.3 100 26/26 74 Q2 苯并咪唑类 阿苯达唑砜 6.02 298.2 159.0*/224.0 100 48/34 75 Q2 苯并咪唑类 5-羟基甲苯咪唑 5.92 298.2 160.0*/266.1 100 46/28 76 Q2 苯并咪唑类 坎苯达唑 6.00 303.2 217.0*/261.1 100 37/34 注:*表示定量离子。 表 2 76种化合物的回归方程、相关系数、定量限、加标回收率、相对标准偏差和基质效应(n=6)
Table 2 Regression equations, correlation coefficients (r), limits of quantitations (LOQs), spiked recoveries, RSD andMe of the 76 compounds (n=6)
序号 化合物 线性方程 相关系数r LOQ
(μg/kg)低水平加标(μg/kg) 中水平加标(μg/kg) 高水平加标(μg/kg) 基质效应
(%)回收率(%) RSD(%) 回收率(%) RSD(%) 回收率(%) RSD(%) A 喹诺酮类 1 恩诺沙星 y=8.77919e4 x+4.84266e4 0.99887 0.4 64.1 7.5 71.4 7.9 71.7 9.4 10.5 2 环丙沙星 y=4.18761e4 x+17851.16215 0.99995 1.6 61.8 5.7 67.5 5.9 66.7 4.6 −7.9 3 培氟沙星 y=6.63777e4 x−3354.75582 0.99983 1.0 71.1 7.8 77.3 6.3 77.0 3.5 12.3 4 沙拉沙星 y=5.99307e4 x+6.50456e4 0.99921 0.5 61.3 5.2 66.6 5.4 66.8 6.1 −5.5 5 氧氟沙星 y=1.45192e5 x+3.99343e4 0.99961 0.7 66.5 2.9 75.5 2.4 74.2 7.5 17.3 6 洛美沙星 y=8.77989e4 x−7611.92400 0.99968 1.2 63.8 7.7 69.8 5.0 69.6 4.4 4.2 7 氟甲喹 y=1.35255e5 x+6475.09899 0.99966 1.0 73.5 8.2 80.4 7.3 78.8 7.8 35.9 8 诺氟沙星 y=4.15611e4 x+2827.31987 0.99999 0.6 63.1 8.9 71.3 7.6 72.1 4.4 8.0 9 西诺沙星 y=5.93231e4 x+9574.84394 0.99993 0.5 70.4 2.4 74.1 6.7 76.1 8.5 18.9 10 达氟沙星 y=2.29035e5 x+3.79034e5 0.99587 0.4 69.2 5.3 77.9 4.2 77.8 8.8 19.1 11 恶喹酸 y=4772.72729 x+3.07264e4 0.99532 6.6 91.9 9.5 86.4 7.5 93.6 8.3 2.9 12 萘啶酸 y=1.51124e5 x+1.46960e5 0.99589 0.4 76.4 5.4 79.9 9.8 82.3 4.7 31.0 13 双氟沙星 y=24869.42943 x−11043.08797 0.99989 0.7 67.2 8.1 74.2 7.8 74.4 7.0 31.5 14 司帕沙星 y=7.50198e4 x+7117.77919 0.99968 0.5 61.9 6.4 67.1 4.0 68.2 7.0 0.9 15 氟罗沙星 y=9.32207e4 x−13190.26022 0.99994 0.6 64.5 7.2 69.0 3.9 70.2 7.0 18.5 16 马波沙星 y=5.80599e4 x−7484.00978 0.99992 0.6 61.6 6.3 69.2 14.2 66.3 7.2 4.1 17 依诺沙星 y=7.31679e4 x+26628.95143 0.99825 0.8 63.1 6.5 69.6 7.1 71.6 10.3 2.8 18 奥比沙星 y=9.19517e4 x+1.33648e5 0.99985 0.5 64.5 6.8 63.1 4.0 66.9 9.1 13.5 B 磺胺类 1 磺胺嘧啶 y =5.84613e4 x+6053.52902 0.99928 1.0 72.1 5.7 70.4 5.7 76.1 11.3 −15.5 2 磺胺二甲基嘧啶 y =15303.64269 x+4893.06738 0.99961 0.9 71.6 3.5 75.1 4.2 76.7 10.9 −13.0 3 磺胺甲基嘧啶 y=6.46915e4 x−2498.83651 0.99938 0.5 78.5 6.4 75.6 3.8 78.3 4.3 −17.8 4 磺胺间甲氧嘧啶 y =5.25886e4 x+3980.10513 0.9998 0.7 72.3 7.4 69.2 3.1 73.7 8.3 19.2 5 磺胺甲基异噁唑 y =3.69051e4 x+8854.49948 0.99985 0.8 73.8 4.3 75.4 5.8 77.8 8.4 0.1 6 磺胺间二甲氧嘧啶 y=1.14726e5 x+7.88381e4 0.99808 1.4 68.9 6.5 70.1 7.2 72.9 5.3 19.6 7 磺胺邻二甲氧嘧啶 y=1.08816e5 x+8.06670e4 0.99632 1.5 72.2 4.8 73.6 5.8 76.3 12.2 3.9 8 磺胺喹恶啉 y=4.19304e4 x+3.83946e4 0.99816 0.5 83.1 6.1 87.3 3.3 89.6 4.0 5.3 9 磺胺氯哒嗪 y=5.04529e4 x−5999.96334 0.99995 0.7 65.5 5.2 65.7 4.6 69.1 13.3 15.5 10 甲氧苄啶 y=1.38957e5 x+4.38855e4 0.99778 0.6 62.4 13.0 64.4 12.4 66.9 4.5 14.2 11 磺胺醋酰 y=15113.48769 x−5063.34401 0.99699 1.2 67.1 6.8 68.7 13.0 71.2 10.0 19.5 12 磺胺吡啶 y=6.47060e4 x+8942.74485 0.99878 0.5 82.8 8.1 84.1 8.9 88.8 14.4 −22.7 13 磺胺脒 y=13912.19605 x+2735.05120 0.99997 1.0 70.4 9.0 67.7 8.6 72.5 7.9 7.3 14 磺胺恶唑 y=7.95421e4 x+24453.19716 0.99927 1.1 74.1 7.1 69.8 5.8 74.7 7.0 2.1 15 磺胺噻唑 y=6.42743e4 x+9122.26320 0.99988 0.9 73.3 6.8 69.2 3.8 75.2 7.0 −8.7 16 磺胺二甲异噁唑 y=4.25223e4 x+14870.05950 0.99883 1.2 69.4 3.4 65.9 6.5 71.8 5.4 9.9 17 磺胺甲噻二唑 y=5.73779e4 x+131.02092 0.99921 1.0 63.7 4.8 63.4 8.8 66.7 6.5 1.9 18 苯甲酰磺胺 y=4.63782e4 x+10966.83686 0.99950 1.8 82.2 5.7 85.5 5.6 89.1 3.4 −8.5 19 磺胺二甲异嘧啶 y=1.13749e5 x−5720.81666 0.99982 1.2 67.0 8.5 68.0 9.7 71.3 10.2 −19.2 20 磺胺甲氧哒嗪 y =6.38340e4 x+8075.34550 0.99994 0.8 64.8 9.2 68.9 5.3 70.3 8.8 19.3 21 磺胺苯吡唑 y=19023.10054 x+9056.69007 0.99822 0.8 82.8 3.6 90.2 3.5 91.1 2.9 4.3 22 磺胺硝苯 y=3620.11395 x+3.40577e4 0.99718 2.0 78.0 6.6 84.0 8.2 84.9 5.5 −18.6 23 磺胺对甲氧嘧啶 y=9.95313e4 x+23154.12760 0.99954 1.2 84.3 12.9 82.2 5.1 86.7 8.5 −10.2 C 硝基咪唑类 1 甲硝唑 y=4.47588e4 x−10207.54416 0.99989 1.2 78.6 5.0 86.3 6.7 84.6 4.4 −2.1 2 地美硝唑 y=6.63294e4 x+10630.09481 0.99992 1.0 72.0 6.0 73.4 5.0 76.2 14.6 9.3 3 洛硝哒唑 y=20704.64833 x−3229.22793 0.99994 0.8 80.1 12.4 80.9 6.8 85.0 4.4 −12.4 4 4-硝基咪唑 y=16555.59582 x+12972.60635 0.99678 1.4 65.0 6.3 68.6 10.4 69.3 6.6 2.3 5 羟基甲硝唑 y=6701.54251 x−3165.48560 0.99711 2.0 70.2 10.6 72.1 7.1 74.8 8.8 2.2 6 2-甲基-5-硝基咪唑 y=5940.05641 x+12547.97091 0.99976 0.6 70.9 8.9 75.7 5.2 75.5 13.1 −7.1 7 羟甲基甲硝咪唑 y=11551.04400 x+4.15116e4 0.99672 1.8 72.6 6.9 69.7 9.2 74.3 5.3 11.3 8 氯甲硝咪唑 y=13661.14335 x+3950.87767 0.99740 2.1 68.3 8.5 74.5 4.8 76.5 10.6 4.1 9 苯硝咪唑 y=1.20497e5 x+6.34526e4 0.99981 0.6 65.6 4.0 68.8 3.8 69.9 7.3 15.9 10 异丙硝唑 y=8.46358e4 x+2767.15574 0.99977 0.5 65.6 9.3 63.6 9.5 68.0 8.8 0.3 D 大环内酯类 1 竹桃霉素 y=1.50001e5 x+13805.95765 0.99944 0.9 88.5 6.8 96.2 9.5 95.0 7.9 −19.0 2 红霉素 y=11771.66737 x−4635.79587 0.99802 1.0 94.7 8.0 93.0 11.1 96.2 6.4 −31.1 3 克拉霉素 y=8.72120e4 x−3.66243e4 0.99906 1.2 83.4 6.9 87.5 6.4 89.7 7.7 −26.2 4 阿奇霉素 y=27376.31810 x−3754.40816 0.99968 0.7 85.3 12.6 82.7 14.3 87.8 6.6 −20.2 5 吉他霉素 y=1343.82820 x+914.46496 0.99662 1.0 74.0 5.6 78.1 6.9 80.0 4.8 −5.1 6 交沙霉素 y=1772.62792 x+4951.40019 0.99996 1.0 78.4 13.6 84.9 7.8 83.9 8.4 −31.8 7 螺旋霉素 y=2553.39535 x+1897.72306 0.99665 2.6 72.0 7.1 68.6 6.9 72.6 8.0 45.1 8 泰乐菌素 y=7142.20118 x−3284.89451 0.99792 8.8 85.8 9.8 90.8 8.8 92.5 6.4 3.4 9 替米考星 y=3103.37890 x+5314.52058 0.99649 8.9 68.7 12.8 75.1 10.9 75.0 6.8 20.2 E 苯并咪唑类 1 噻苯咪唑 y=2.66215e5 x+5.78693e4 0.9996 0.4 65.4 6.4 67.3 5.3 69.7 5.5 3.3 2 5-羟基噻苯咪唑 y=1.17664e5 x−543.07894 0.99970 0.5 70.1 7.3 67.9 5.4 72.9 13.5 2.4 3 2-氨基-5-苯甲
酰苯并咪唑y=1.02057e5 x+1846.69510 0.99977 0.9 61.6 4.5 63.8 7.1 69.2 4.5 −7.9 4 阿苯达唑-2-氨基砜 y=1.28590e5 x−19174.60489 0.99867 0.5 64.6 5.1 63.5 4.1 66.5 8.8 12.6 5 丙氧苯咪唑 y=2.37419e5 x+2.37457e5 0.99590 0.4 73.7 6.7 80.5 12.4 81.0 7.5 −2.1 6 2-氨基氟苯达唑 y=8.12271e4 x+23593.63964 0.99983 0.7 61.4 4.2 65.5 6.0 71.2 10.1 −9.7 7 阿苯达唑 y=2.35718e5 x+1.50045e5 0.99799 1.0 70.9 7.0 76.2 5.5 77.6 4.4 2.6 8 阿苯达唑亚砜 y=7.95412e4 x+861.48543 0.99994 0.4 64.9 5.7 63.0 4.9 67.4 4.5 23.5 9 甲苯咪唑 y=2.13796e5 x+1.80789e5 0.99739 0.6 79.8 2.0 84.5 10.8 86.6 6.5 7.3 10 阿苯达唑砜 y=1.44073e5 x+7.05995e4 0.99787 0.5 68.1 6.1 67.6 4.4 69.5 6.3 27.2 11 5-羟基甲苯咪唑 y=3.04862e4 x+5623.43029 0.99955 0.6 63.1 6.5 62.8 7.7 64.3 9.4 12.1 12 芬苯达唑 y=1.76930e5 x+9.22278e4 0.99662 1.0 71.0 3.2 75.6 2.4 77.1 5.0 15.7 13 坎苯达唑 y=1.67852e5 x+1.54293e5 0.99573 0.5 63.7 7.3 65.6 10.2 67.6 5.5 6.6 14 氟苯达唑 y=4.66398e4 x+12853.82427 0.99614 0.5 78.5 3.1 85.4 13.8 84.9 5.5 5.6 15 芬苯达唑砜 y=2.00387e5 x+8.12650e4 0.99848 0.6 79.9 3.4 86.8 12.1 85.1 3.7 8.3 16 奥芬达唑 y=1.33556e5 x+6.25765e4 0.99718 0.7 79.3 5.6 82.6 9.2 84.6 5.3 21.6 表 3 本方法与国家标准方法比较
Table 3 Comparison between established method and the state standard methods
方法恩诺沙星 磺胺间甲氧嘧啶 磺胺嘧啶 磺胺甲基嘧啶 甲氧苄啶 本文所建
方法本文所建
方法本文所建
方法GB 31658.17-2021 本文所建
方法GB 31658.17-2021 本文所建
方法GB 31658.17-2021 本文所建
方法GB/T 21316-2007 检测值
(μg/kg)3853 3812 1900 2004 517 518 277 281 79.4 79.7 514 498 14562 14598 520 527 770 779 87.3 87.3 382 378 3915 3951 204 202 3552 3497 100.5 99.7 393 407 416 422 354 361 402 409 66.1 67.9 233 235 / / 417 423 / / / / 169 173 / / / / / / / / P 0.428 0.116 0.106 0.611 0.592 注:“/”表示未检出。 -
[1] 吴永宁, 邵兵, 沈建忠. 兽药残留检测与监控技术[M]. 北京:化学工业出版社, 2007 WU Y N, SHAO B, SHEN J Z. Detection and monitoring technology of veterinary drug residues[M]. Beijing:Chemical Industry Press, 2007.
[2] 张蕾, 张玉娇, 王玉宁, 等. 肉中的兽药和瘦肉精残留及其检测技术研究进展[J]. 食品工业科技,2023,44(3):481−488 ZHANG L, ZHANG Y J, WANG Y N, et al. The residue of veterinary medicine and leanness-enhancing agents in meat and advance in detection technology[J]. Science and Technology of Food Industry,2023,44(3):481−488.
[3] 裴斐, 韩萍, 王杰, 等. 基于UHPLC-Q-TOF/MS法同时检测猪肉中主要抗生素类兽药残留[J]. 食品工业科技,2022,43(10):298−304 PEI P, HAN P, WANG J, et al. Simultaneous determination of major antibiotics veterinary drug residues in pork by UHPLC-Q-TOF/MS[J]. Science and Technology of Food Industry,2022,43(10):298−304.
[4] 谢瑜杰, 仝凯旋, 彭涛, 等. 液相色谱-四极杆/静电场轨道阱质谱快速筛查和确证畜禽肉及水产品中160种兽药残留[J/OL]. 分析试验室:1−28. https://doi. org/10.13595/j. cnki. issn1000-0720.2022. 040901 XIE Y J, TONG K X, PENG T, et al. Rapid screening and confirmation of 160 veterinary drugs in livestock and poultry meat and aquatic products by liquid chromatography-quadrupole/orbitrap mass spectrometry[J/OL]. Chinese Journal of Analysis Laboratory: 1−28. https://doi.org/10.13595/j.cnki.issn1000-0720.2022.040901.
[5] 马宁, 王杰, 裴斐, 等. 屠宰、预冷和市售阶段猪肉及内脏中兽药残留分析与风险评估[J]. 食品科学,2020,41(16):314−319 MA N, WANG J, PEI F, et al. Determination and risk assessment of veterinary drugs in pork meat and viscera during slaughter, pre-cooling and sale[J]. Food Science,2020,41(16):314−319.
[6] 杨兆甜, 吴亚婕, 王莹, 等. 超高效液相色谱-串联质谱法检测猪肉中多兽药残留[J]. 食品与生物技术学报,2020,39(7):44−50 YANG Z T, WU Y J, WANG Y, et al. Determination of veterinary drugs in porcine muscle by UPLC-MS/MS method[J]. Journal of Food Science and Biotechnology,2020,39(7):44−50.
[7] RAHMAN M, LEE D J, JO A, et al. Onsite/on-field analysis of pesticide and veterinary drug residues by a state-of-art technology:A review[J]. Separation Science, 2021, 1−19.
[8] 刘柏林, 谢继安, 赵紫微, 等. 固相萃取-超高效液相色谱-串联质谱法同时测定动物源性食品中11种禁限兽药及代谢物[J]. 色谱,2021,39(4):406−414 doi: 10.3724/SP.J.1123.2020.05012 LIU B L, XIE J, ZHAO Z W, et al. Simultaneous determination of 11 prohibited and restricted veterinary drugs and their metabolites in animal-derived foods by ultra performance liquid chromatography-tandem mass spectrometry coupled with solid phase extraction[J]. Chinese Journal of Chromatography,2021,39(4):406−414. doi: 10.3724/SP.J.1123.2020.05012
[9] 汪建妹, 徐彦, 周敏, 等. UiO-67分散固相萃取/超高效液相色谱-串联质谱法测定猪肉中6种大环内酯类兽药残留[J/OL]. 分析试验室. http://kns.cnki.net/kcms/detail/11.2017.TF.20220622.0852.001.html[WANG J M, XU Y, ZHOU M, et al. Dispersive solid phase extraction based on UiO-67 coupled with ultra-high performance liquid chromatography-tandem mass spectrometry for the determination of six macrolides residues in pork[J]. Chinese Journal of Analysis Laboratory. http://kns.cnki.net/kcms/detail/11.2017.TF.20220622.0852.001.html WANG J M, XU Y, ZHOU M, et al. Dispersive solid phase extraction based on UiO-67 coupled with ultra-high performance liquid chromatography-tandem mass spectrometry for the determination of six macrolides residues in pork[J]. Chinese Journal of Analysis Laboratory. http://kns.cnki.net/kcms/detail/11.2017.TF.20220622.0852.001.html
[10] WANG C, LI X, YU F, et al. Multi-class analysis of veterinary drugs in eggs using dispersive-solid phase extraction and ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Food Chemistry,2020,334:127598.
[11] YE S B, HUANG Y, LIN D Y. QuEChERS sample pre-processing with UPLC-MS/MS:A method for detecting 19 quinolone-based veterinary drugs in goat's milk[J]. Food Chemistry, 2022373(Part B):131466.
[12] 申佳璐, 王梁, 赵青, 等. 畜禽肉及鸡蛋中多种兽药残留前处理技术研究进展[J]. 食品安全质量检测学报,2022,13(15):4840−4849 SHEN J L. WANG L, ZHAO Q, et al. Research progress on pretreatment technology of multiple veterinary drug residues in meat and eggs[J]. Journal of Food Safety and Quality,2022,13(15):4840−4849.
[13] KALOGEROPOULOU A G, KOSMA C I, ALBANIS T A. Simultaneous determination of pharmaceuticals and metabolites in fish tissue by QuEChERS extraction and UHPLC Q/Orbitrap MS analysis[J]. Analytical and Bioanalytical Chemistry,2021(28):413−420.
[14] 周瑞铮, 陈锦杭, 张树权, 等. 分散固相萃取结合液相色谱-串联质谱法测定淡水鱼中9种磺胺类和3种喹诺酮类药物残留量[J]. 食品安全质量检测学报,2021,12(17):406−414 ZHOU R Z, CHEN J H, ZHANG S Q, et al. Determination of 9 kinds of sulfonamides and 3 kinds of quinolones residues in freshwater fish by dispersive solid phase extraction coupled with liquid chromatography-tandem mass spectrometry[J]. Journal of Food Safety and Quality,2021,12(17):406−414.
[15] 李文杰, 倪建秀, 丁春晖, 等. QuEChERS-UPLC-MS/MS法同时测定青虾中27种兽药残留[J]. 安徽农业科学,2021,49(24):197−212 LI W J, NI J X, DING C H, et al. Simultaneous determination of 27 veterinary drug residues in freshwater shrimp by QuEChERS-UPLC-MS/MS[J]. Journal of Agriculture Science,2021,49(24):197−212.
[16] ANASTASSIADES M, LEHOTAY S J, STAJNBAHER D, et al. Fast and easy multiresidue method employing acetonitrile extraction/partitioning and dispersive solid-phase extraction for the determination of pesticide residues in produce[J]. Journal of AOAC International,2003,86(2):412−431. doi: 10.1093/jaoac/86.2.412
[17] DESMARCHELIER A, BESSAIRE T, SAVOY M C, et al. Screening of 154 veterinary drug residues in foods of animal origin using LC-MS/MS[J]. Journal of AOAC International,2020,104 (3):650−681.
[18] BESSAIRE T, MUJAHID C, BECK A, et al. Screening of 23 β-lactams in foodstuffs by LC-MS/MS using an alkaline QuEChERS-like extraction[J]. Food Additives & Contaminants Part A Chemistry Analysis Control Exposure & Risk Assessment,2018,35(4):661−673.
[19] GOESSENS T, HUYSMAN S, TROYER N, et al. Multiclass analysis of 46 antimicrobial drug residues in pond water using UHPLC-Orbitrap-HRMS and application to freshwater ponds in Flanders, Belgium[J]. Talanta,2020(220):121326.
[20] 方从容, 高洁, 王雨昕, 等. QuEChERS-超高效液相色谱-串联质谱法测定鸡蛋中125种兽药残留[J]. 色谱,2018,36(11):1119−1131 doi: 10.3724/SP.J.1123.2018.06007 FANG C R, GAO J, WANG Y X, et al. Determination of 125 veterinary drugs residues in eggs by QuEChERS-ultra-high performance liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Chromatography,2018,36(11):1119−1131. doi: 10.3724/SP.J.1123.2018.06007
[21] 黄永桥, 宋光林, 毛敏霞, 等. QuEChERS结合UPLC-MS/MS法测定畜肉中8种抗真菌药物残留[J]. 食品科学,2022,43(12):334−340 HUANG Y Q, SONG G L, MAO M X, et al. Determination of eight antifungal drug residues in meat by QuEChERS extraction coupled with UPLC-MS/MS[J]. Food Science,2022,43(12):334−340.
[22] 欧阳少伦, 蓝草, 陈文锐, 等. 在线净化/液相色谱-四极杆/静电场轨道阱高分辨质谱法快速筛查水产品中123种兽药残留[J]. 分析测试学报,2022,41(3):309−318 OUYANG S L, LAN C, CHEN W R, et al. Rapid screening and confirmation of 123 veterinary drugs in aquatic products by on-line cleanup/liquid chromatography-quadrupole/electrostatic field orbitrap high-resolution mass spectrometry[J]. Journal of Instrumental Analysis,2022,41(3):309−318.
[23] 洪妍妍, 陈海玲, 王翠玲, 等. 样品前处理QuEChERS法及新型吸附材料在水产品中抗生素残留分析中的应用进展[J]. 食品安全质量检测学报,2022,13(21):6898−6906 HONG Y Y, CHEN H L, WANG C L, et al. Application progress of sample pretreatment QuEChERS method and new adsorbents materials in the analysis of antibiotic residues in aquatic products[J]. Journal of Food Safety and Quality,2022,13(21):6898−6906.
[24] 郭添荣, 万渝平, 孙利, 等. 通过式固相萃取结合超高效液相色谱-四极杆/静电场轨道阱高分辨质谱快速筛查畜禽肉中108种兽药残留[J]. 分析化学,2022,50(2):271−277 GUO T R, WAN Y P, SUN L, et al. Rapid screening and confirmation of 108 kinds of veterinary drug residues in livestock and poultry meat by solid phase extraction purification and liquid chromatography coupled with quadrupole/orbitrap mass spectrometry[J]. Chinese Journal of Analytical Chemistry,2022,50(2):271−277.
[25] 郭海霞, 肖桂英, 张禧庆, 等. QuEChERS-超高效液相色谱-串联质谱法同时检测猪肉中121种兽药[J]. 色谱,2015,33(12):1242−1250 doi: 10.3724/SP.J.1123.2015.09016 GUO H X, XIAO G Y, ZHANG X Q, et al. Simultaneous determination of 121 veterinary drugs in pork by QuEChERS and ultra performance liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Chromatography,2015,33(12):1242−1250. doi: 10.3724/SP.J.1123.2015.09016
[26] 曲斌, 朱志谦, 陆桂萍, 等. QuEChERS-UPLC-MS/MS快速测定猪肝中20种磺胺类药物残留[J]. 药物分析杂志,2012,32(8):1457−1464 QU B, ZHU Z Q, LU G P, et al. UPLC-MS/MS via QuEChERS rapid determination of twenty sulphonamide residues in pig liver[J]. Chinese Journal of Pharmaceutical Analysis,2012,32(8):1457−1464.
[27] 刘进玺, 王铁良, 胡京枝, 等. QuEChERS结合HPLC-MS/MS同时测定鱼肉中多种兽药残留[J]. 食品与发酵工业,2021,47(19):252−257 LIU J X, WANG T L, HU J Z, et al. Determination of veterinary drug residues in fish by QuEChERS method with HPLC-MS/MS[J]. Food and fermentation industries,2021,47(19):252−257.
[28] 易江华, 段振娟, 方国臻, 等. QuEChERS方法在食品农兽药残留检测中的应用[J]. 中国食品学报,2013,13(2):153−158 YI J H, DUAN Z J, FANG G Z, et al. Study of QuEChERS method for the detection of pesticide and veterinary drug residues in foods[J]. Journal of Chinese Institute of Food Science and Technology,2013,13(2):153−158.
[29] 王友谊, 张虹, 戴志远. 直接进样电喷雾串联质谱法测定草鱼肌肉组织中磷脂[J]. 分析化学,2012,40(6):6898−6906 WANG Y Y, ZHANG H, DAI Z Y. Determination of phospholipids from Ctenopharyngodon idellus muscle by direct-injection electrospray ionization tandem mass spectrometry[J]. Chinese Journal of Analytical Chemistry,2012,40(6):6898−6906.
[30] 卞华, 秦宇, 虞成华, 等. 复合式提取净化体系结合超高效液相色谱-串联质谱法检测畜禽肉中120种抗生素药物残留[J]. 色谱,2019,37(2):162−176 doi: 10.3724/SP.J.1123.2018.10003 BIAN H, QIN Y, YU C H, et al. Simultaneous determination of 120 veterinary antibiotics in meat by combined pretreatment system coupled with ultra-performance liquid chromatography-tandem mass spectrometry[J]. Chinese Journal of Chromatography,2019,37(2):162−176. doi: 10.3724/SP.J.1123.2018.10003





 下载:
下载:





 下载:
下载:



