Stability and Mechanism of Oyster Peptide Hydrolysate Zinc Nanoparticles during in Vitro Gastrointestinal Digestion
-
摘要: 本研究旨在探究体外模拟消化对牡蛎源肽锌纳米粒(OPH-Zn)稳定性及其结构的影响,揭示OPH-Zn在胃肠道消化过程中的动态变化规律。采用各种光谱仪(紫外、红外和荧光)、电镜(扫描和透射)以及粒度仪测定模拟消化液中OPH-Zn的锌含量、表面形貌、二级结构以及粒径分布变化。研究发现,OPH-Zn总锌含量高达228.89±2.53 mg/g;在模拟胃液消化过程中,OPH-Zn和ZnSO4对照中可溶性锌含量变化不大,且两个样品无显著差异(P>0.05);转为模拟肠液消化时,OPH-Zn和ZnSO4的锌溶解性分别降低了28.07%和55.31%(P<0.05),与ZnSO4相比,OPH-Zn可溶性锌含量显著高于ZnSO4(P<0.05);光谱分析发现,OPH-Zn在模拟胃液和肠液中保持相对稳定,但在由胃液过渡到肠液时,Zn2+与肽键中氧原子和氮原子的配位作用发生变化,电镜结果显示不同消化程度的OPH-Zn表面微观结构和颗粒大小也存在一定差异。结果表明,OPH-Zn在模拟胃肠道消化中具有一定的稳定性,是一种有商业潜力的补锌剂,同时其结构变化的规律也为肽锌纳米粒的开发和后续研究提供了一定的研究基础。Abstract: The aim of this study was to investigate the effects of in vitro simulated digestion on the stability and structure of oyster protein hydrolysate zinc nanoparticles (OPH-Zn), and to reveal the dynamic variation rule of OPH-Zn under different degrees of gastrointestinal digestion. Atomic absorption spectrophotometer, UV scanner, infrared spectrometer, fluorescence spectrometer, scanning electron microscope, transmission electron microscope and particle size analyzer were used to determine the zinc content, surface morphology, secondary structure and molecular weight distribution of OPH-Zn in digestive fluid in simulated gastrointestinal digestion process. The results showed that the total zinc content of OPH-Zn was 228.89±2.53 mg/g. During simulated gastric digestion, soluble zinc content in OPH-Zn and ZnSO4 controls remained stable basically, and there was no significant difference between the two samples (P>0.05). When the digestion was transferred from the stomach to the intestine, the zinc solubility of OPH-Zn and ZnSO4 decreased by 28.07% and 55.31% (P<0.05), respectively. The soluble zinc content of OPH-Zn was significantly higher than that of ZnSO4 during the whole intestinal digestion (P<0.05). The spectral analysis showed that OPH-Zn remained relatively stable in simulated gastric juice and intestinal juice, but the coordination between the oxygen and nitrogen atoms of peptide bond and Zn2+ was changed during the transition from gastric juice to intestinal juice. The results of electron microscopy showed that the surface microstructure and particle size of OPH-Zn were different with different levels of digestion. The results revealed that the OPH-Zn had a certain stability in simulating gastrointestinal digestion and was a potential zinc supplement with commercial potential. At the same time, the structural changes of OPH-Zn would also provide a certain research basis for the development and follow-up study of peptide-zinc nanoparticles.
-
锌作为人体必需的微量元素之一,在维持人体正常生命活动和生理状态方面具有不可替代的作用,被称为“生命元素”,参与人体内数百种功能蛋白质和酶的组成[1]。锌与身体健康和疾病密切相关,人体的生长发育、免疫功能、脂质代谢等生命活动都离不开锌的作用。缺锌可以延缓机体的生长和发育、损害性腺功能、导致神经和免疫功能障碍[2-3]。机体内锌的平衡取决于锌的吸收和代谢。自然界中锌的来源极其丰富,造成机体缺锌的主要原因在于膳食来源的锌易与食物中的植酸结合为不溶物,从而无法被肠道吸收。因此,开发有效的补锌制剂改善机体健康具有重要的意义。
目前补锌制剂主要分为三大类:无机态锌、简单有机酸锌和锌的氨基酸、蛋白质螯合物[4]。传统上的补锌剂如硫酸锌、葡萄糖酸锌等往往存在微碱性环境下易沉淀、生物利用度低,以及刺激胃肠道等缺点,不宜长期使用[5-6]。作为第三代补锌剂,肽锌螯合物较无机锌具有更好的促锌吸收能力,因而受到国内外学者的关注[7],但其促锌吸收机制尚不清晰。肽锌螯合物的胃肠稳定性决定了其被机体吸收的形式、路径及剂量。因此,明确肽锌纳米粒的胃肠道消化规律,对揭示其吸收机制至关重要。
牡蛎别名海蛎、蛎蛤、牡蛤、蛎子、蚝等,是世界上第一大养殖贝类,也是人类可利用的重要海洋生物资源之一[8]。牡蛎富含蛋白质和锌等成分,营养价值极高,素有“海洋牛奶”的美誉。牡蛎中的蛋白质在消化酶的作用下可水解为生物活性多肽[9]。研究发现,牡蛎肽具有一定的锌螯合能力,可以促近锌的吸收[9-10]。目前,对牡蛎肽锌螯合物的研究多集中在纳米粒的制备、结构表征以及形成机理等方面,而关于纳米粒的胃肠道消化动力学行为的研究较少。为进一步明晰牡蛎源肽锌纳米粒的消化吸收机制,本研究利用扫描电镜、透射电镜、紫外光谱、红外光谱、荧光光谱和动态光散射等手段分析牡蛎源肽锌纳米粒在胃肠道消化过程中的表面状态和二级结构的变化,进而评价其胃肠道消化的稳定性,为后续肽锌螯合物的工业化生产和纳米型复合物补锌剂的开发提供理论依据。
1. 材料与方法
1.1 材料与仪器
新鲜牡蛎肉 采购于广西钦州海鲜市场;碱性蛋白酶(2×105 U/g)、胃蛋白酶(1000 NF)、胰蛋白酶(4000 U/g) 均为南宁庞博生物工程有限公司;猪胆盐 成都市科隆化学品有限公司;无水乙醇 成都市科隆化学品有限公司;盐酸、七水硫酸锌 国药集团化学试剂有限公司;碳酸氢钠、磷酸氢二钠 成都金山化学试剂有限公司;氯化钡 成都市科隆化学品有限公司;其他试剂均为分析纯。
ZWY-110X50恒温培养振荡器 上海智城分析仪器制造有限公司;TGL-16M台式高速冷冻离心机 常州金坛良友仪器有限公司;LGJ-12真空冷冻干燥机 北京松源华兴科技发展有限公司;ME204E电子天平 梅特勒-托利多仪器有限公司;ST3100实验室pH计 奥豪斯仪器有限公司;RE52AA旋转蒸发仪 上海亚荣生化仪器厂;iCE 3500原子吸收光谱仪 美国赛默飞世尔科技公司;UV-2100紫外可见分光光度计 上海优尼柯有限公司;赛默飞世尔Lumina荧光光度计、Thermo Scientific Nicolet iS20傅里叶变换红外光谱 赛默飞世尔科技公司;捷克TESCAN MIRA LMS扫描电子显微镜 北京亚科晨旭科技有限公司;日立HT7700透射电子显微镜 Advanced Microscope Techniques Corp;NanoBrook Omni多角度粒度及高灵敏Zeta电位分析仪 美国布鲁克海文仪器公司。
1.2 实验方法
1.2.1 牡蛎源肽锌纳米粒的制备
参照Zhang等[10]的方法进行肽锌纳米粒的制备。首先,采用碱性蛋白酶酶解牡蛎匀浆(去壳打浆)制备酶解液,酶解条件为:加酶量5‰,温度50 ℃,pH8.0,酶解时间10.0 h,100 ℃水浴灭酶10 min,离心(8000 r/min,10 min),过滤,取滤液,超滤,取分子量<10 kD的多肽,冻干即为牡蛎多肽(OPH)。取OPH用蒸馏水配制成10 mg/mL的溶液,取一定体积的OPH溶液与硫酸锌(100 mg/mL)混合,使OPH与ZnSO4·7H2O质量比为1:2,pH6.5,置于45 ℃恒温水浴摇床(140 r/min)中反应10 min。取出后冷却,加入3倍体积的75%乙醇,4 ℃静置过夜,离心,去除上清液,加入乙醇清洗沉淀3次以上,直至用氯化钡检测无硫酸根检出为止,冻干,备用,即为牡蛎源肽锌纳米粒(OPH-Zn)。
1.2.2 牡蛎肽锌螯合能力的测定
总锌含量反映了牡蛎肽与Zn2+的络合能力,是评价肽锌纳米粒螯合能力的基础。根据Li等[11]测锌含量的方法稍作修改,称取定量牡蛎源肽锌纳米粒3份并设置空白对照,经酸性溶液消解后用iCE 3500原子吸收光谱仪测定总锌含量。总锌含量计算公式如下:
X=(ρ−ρ0)×Vm 式中:X表示牡蛎源肽锌纳米粒的锌含量(mg/g);ρ表示试样溶液中锌的质量浓度(mg/L); ρ0 表示空白溶液锌的质量浓度(mg/L);V表示消化液的定容体积(L);m表示称样量(g)。
1.2.3 OPH-Zn的体外模拟消化
模拟胃肠道消化过程依据Sun等[12]的方法进行调整修改。用0.01 mol/L盐酸溶液溶解胃蛋白酶模拟胃液,用0.1 mol/L NaHCO3溶液溶解胰酶和猪胆盐模拟肠液。将已制备的牡蛎源肽锌纳米粒溶解于去离子水中,同时配制等锌含量的硫酸锌溶液作对照。37 ℃孵育30 min,按1:100 (w/w)的酶与底物的比例加入,维持pH为2。分别于胃消化过程0、30、60、90 min 取出消化液。胃消化后,将pH调整至7.5,然后加入肠液。在肠道消化过程0、30、60、90和150 min取出消化液。将所有消化液分别于100 ℃加热20 min灭酶,然后于20 ℃、2500 r/min离心20 min,取上清液,4 ℃贮藏,备用。
1.2.4 Zn2+溶解度分析
为测定牡蛎源肽锌纳米粒在胃肠道中的溶解性,取1.2.3消化液离心所得上清液,参照1.2.2总锌测定方法用原子吸收光谱仪测定其可溶性锌含量。Zn2+溶解度计算公式如下:
锌离子溶解度(%)= 可溶性锌含量 总锌含量 ×100 1.2.5 紫外光谱分析
将样品溶液倒入石英皿中,以去离子水完成空白校准,紫外分光光度计的检测扫描波长范围为 190~400 nm[13]。
1.2.6 荧光光谱分析
取适量消化液样品,蒸馏水作对照,设激发波长280 nm,室温条件下测定样品在300~500 nm处的发射光谱,狭缝宽度5 nm,激发和发射石英管的路径长度为1.0 cm [14]。
1.2.7 扫描电镜观察
取适量牡蛎源肽锌纳米粒在胃部消化90 min和肠部消化150 min的消化液冻干品,用导电胶分别将其粘贴在铝样台上,然后在上面喷洒一层薄薄的金膜,置于扫描电镜能谱仪中用扫描电子显微镜进行观察拍片,选取区域进行能谱扫描分析[15]。
1.2.8 透射电镜观察
将胃部消化90 min的消化液和肠部消化不同阶段消化液(0、30、60、90、150 min)滴在涂有碳膜的铜网上,室温风干,用透射电子显微镜观察样品形貌[16]。
1.2.9 粒径分布测定
根据Walczak等[17]的研究方法,使用NanoBrook Omni多角度粒度及高灵敏Zeta电位分析仪,通过动态光散射(DLS)测定牡蛎源肽锌纳米粒在胃肠道消化过程中的粒径大小分布情况。
1.2.10 傅里叶变换红外光谱分析
采用液体池法,将胃部消化0、90 min的消化液样品和肠部消化0、150 min的消化液样品用注射器注入液体池进行测试,ZnSO4溶液为对照。将液体池平放于桌面,在窗片上滴加试样(约1 mL),选择合适厚度的垫片置于窗片上对齐,用另一窗片压于其上,盖上压圈后装入仪器测试架中进行测定[18]。
1.3 数据处理
所有数据均从重复三次的实验中获得,结果以平均值±标准差表示。数据通过 Excel 软件整理,用SPSS软件进行数据显著性分析,用Origin软件进行绘图。
2. 结果与分析
2.1 牡蛎源肽锌纳米粒的锌含量信息与评价
2.1.1 锌螯合能力的测定
参照1.2.2的方法及公式计算测定本研究制得的牡蛎源肽锌纳米粒的总锌含量高达228.89±2.35 mg/g。相较于其他食源性蛋白肽,本研究所制备得到的牡蛎肽具备更强的锌螯合能力[12, 19]。Li等[20]从牡蛎中制备了锌结合多肽,锌含量达到101.08±3.10 mg/g。肽锌螯合物是一种具有环状结构的有机化合物,它是由Zn2+按一定摩尔比以共价键同肽结合而成的。肽螯合金属的能力与很多因素有关,其中包括肽中氨基酸组成、氨基酸序列、疏水性及空间结构密切相关[21]。
2.1.2 Zn2+溶解度分析
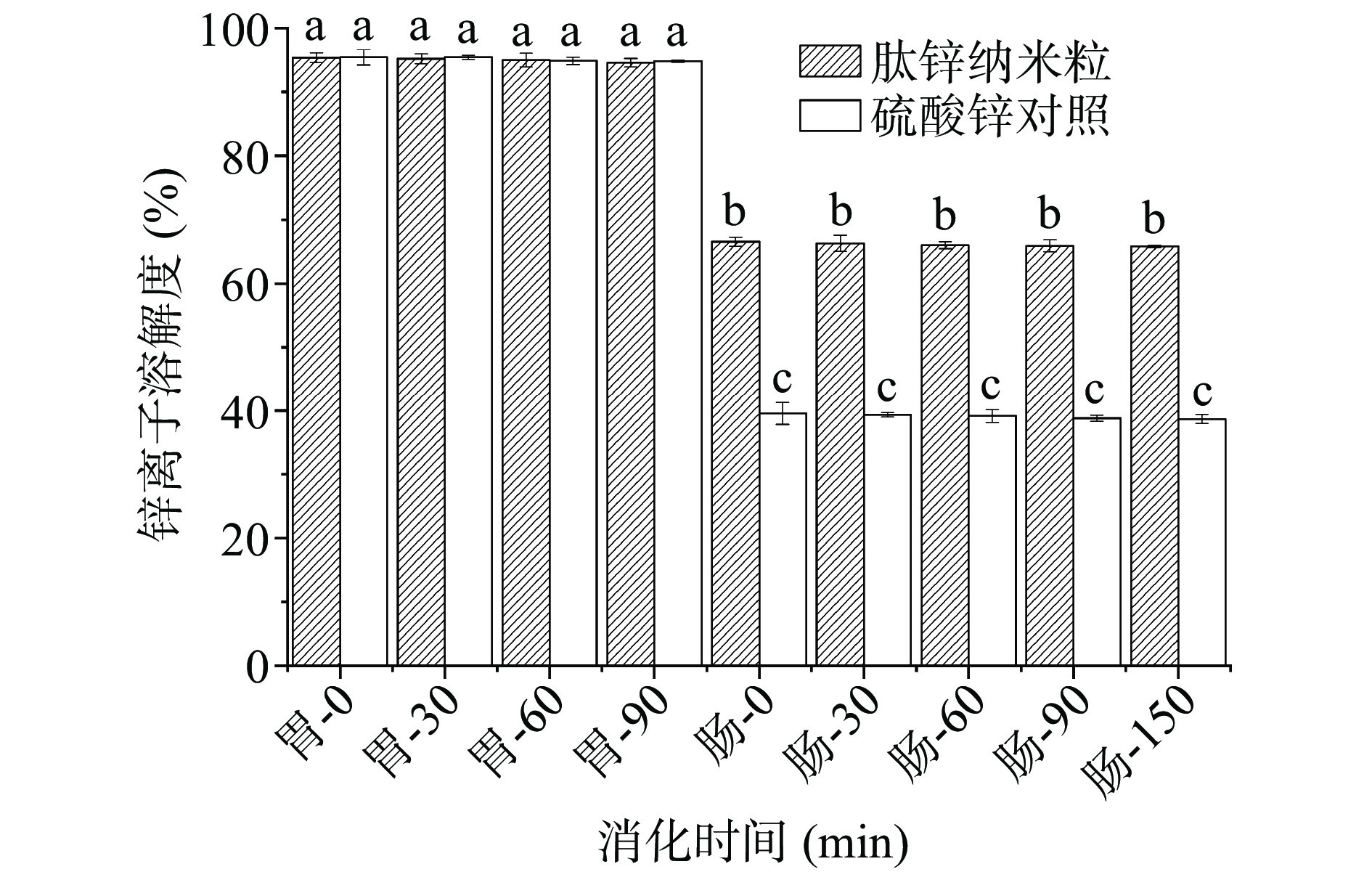
金属离子的溶解性高低是决定其体内生物利用率以及吸收效果好坏的重要参数。螯合物一经人体摄入后,会暴露在胃肠部蛋白酶以及各种盐离子下,这些因素都可能会影响锌的溶解性。因此,本研究针对OPH-Zn和ZnSO4在模拟胃肠道中锌的溶解性进行了分析。从图1可以看出,OPH-Zn和ZnSO4在胃肠道环境下可保持高的溶解性,随着胃液消化的进行,可溶性锌含量呈现略微下降的趋势,但Zn2+溶解度基本保持在95.00%左右,无显著性差异(P>0.05);而由胃部转为肠部消化时,OPH-Zn和ZnSO4中Zn2+的溶解性会迅速降低,分别从94.59%、94.85%骤降至66.52%、39.54%,随着肠液消化过程的进行,可溶性锌含量呈现逐渐下降的趋势,OPH-Zn和 ZnSO4的溶解性分别稳定在66.00%和39.00%左右,该趋势与报道相一致[10]。金属离子在偏酸性的胃部环境下保持高的溶解性有助于提高其在十二指肠和近端空肠中的吸收[22]。在微碱性的肠道条件下,Zn2+可与-OH形成Zn(OH)2沉淀,从而导致可溶性锌含量的降低。
对于绝大多数金属元素而言,当膳食中某种元素缺乏时,该元素的溶解性会严重影响其在肠部的吸收效率,而肽金属螯合物的形成可有效提高金属的溶解性,从而促进其吸收[23]。模拟胃肠道消化实验结果表明,与ZnSO4相比,OPH-Zn可有效提高锌在肠道中的溶解性,这意味着OPH-Zn可以提高锌的生物利用度,具有作为食品添加剂用于食品领域的潜能。
2.2 牡蛎源肽锌纳米粒消化过程中的紫外光谱分析
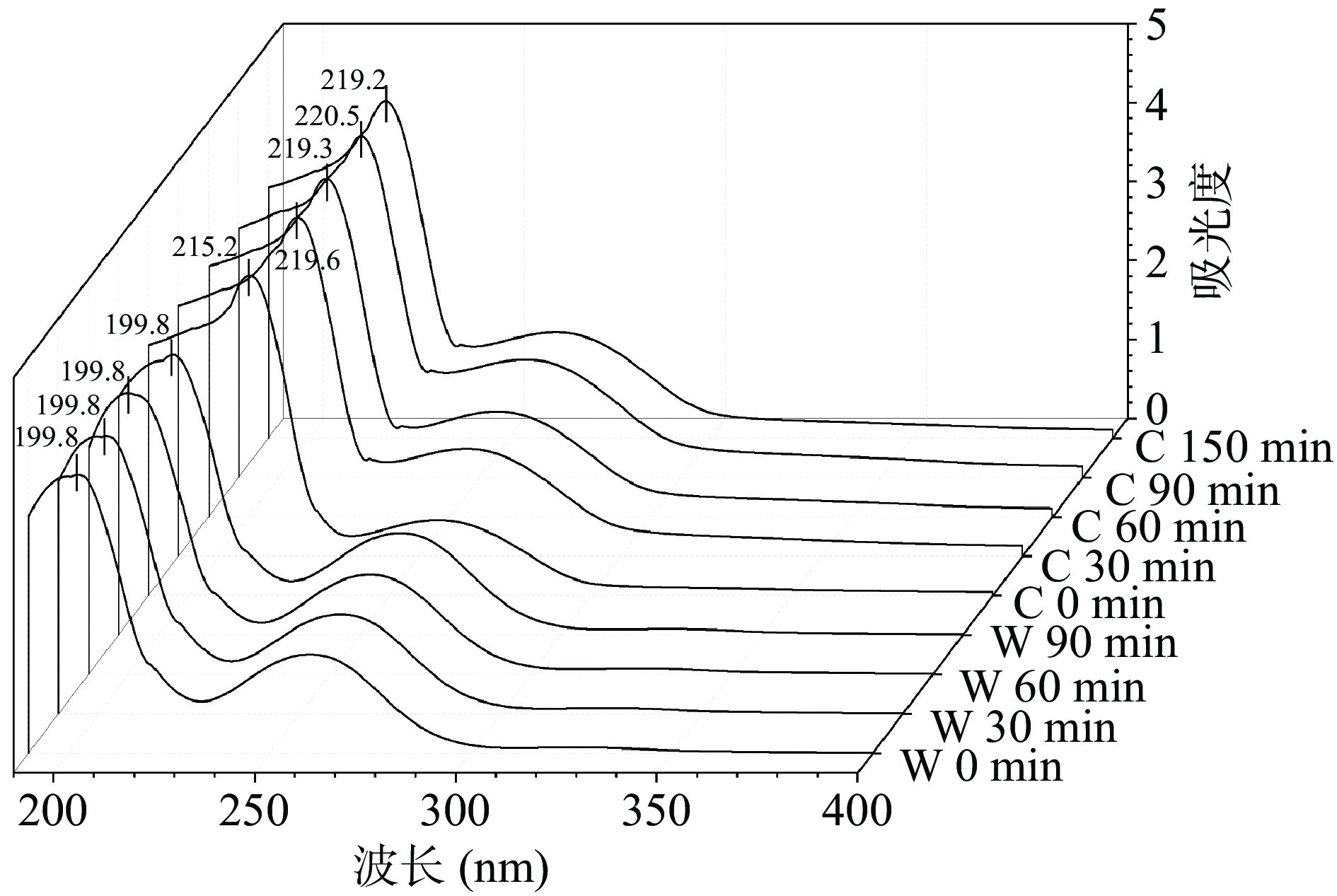
紫外-可见吸收光谱分析被认为是研究纳米粒子结构转变的一种简单而有效的方法[24],用紫外分光光度法分析物质的结构特征,从位错的变化可以分析样品经过不同程度胃肠道消化后的差异和不同的紫外吸收光谱的强度。图2显示了牡蛎源肽锌纳米粒在不同消化程度下紫外光谱差异,牡蛎源肽锌纳米粒在胃消化0、30、60、90 min过程中,紫外吸收峰显示在199.8 nm处。肠道消化初始阶段(C 0 min),吸收峰移动到215.2 nm处,肠道消化30、60、90、150 min时,吸收峰继续红移到219.6、219.3、220.5、219.2 nm处。这是由于在消化过程中,环境pH的变化影响了Zn2+与多肽的螯合,由此引起了肽键(C=O)的电子跃迁,发生了n→π*电子转移[11, 15, 19]。此外,在262 nm波长处有较弱的吸收峰,从胃液消化转移到肠液消化后,该吸收峰小幅右移,且强度略微升高,这可能是消化过程中配体N—C—O电子发生跃迁的结果[11, 19]。
2.3 牡蛎源肽锌纳米粒消化过程中的荧光光谱分析
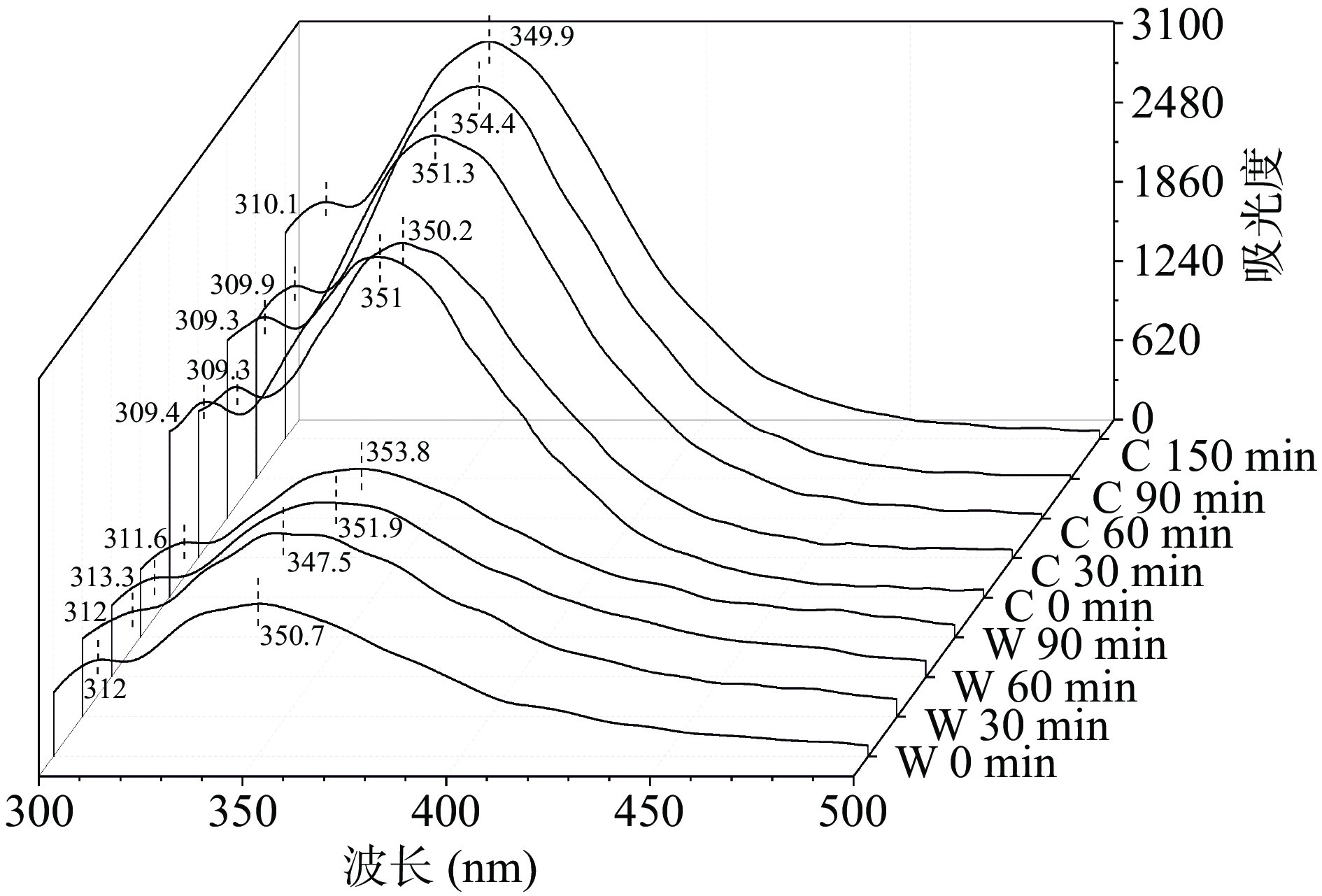
待测物质因吸收光能而被激发,然后由激发态跃迁为基态从而发出荧光,荧光光谱分析法是基于荧光强度的变化来进行定性和定量分析。由于蛋白质中含有苯丙氨酸(Phe)、酪氨酸(Tyr)和色氨酸(Trp)等可在一定波长下激发产生内源荧光的氨基酸,当蛋白质或多肽结构发生改变,如折叠或与小分子物质结合后,荧光强度即会发生改变,因此可利用蛋白质或肽内源荧光强度的变化间接反映蛋白质或肽与Zn2+的结合程度[25]。图3为OPH-Zn在胃肠道消化过程中荧光图谱的变化。从图中可以看出,在300~500 nm范围内随波长的增加,胃部和肠部荧光强度整体均呈现先升高后降低的趋势;与胃部相比而言,肠道处的荧光强度显著增强。早期研究发现,蛋白质或肽中金属离子的引入会引起蛋白质或肽的折叠,而氨基酸或肽与锌螯合时容易发生聚集现象,从而导致内源荧光淬灭[26]。在模拟消化过程中尤其是肠道消化时,OH-与肽段中的氨基酸竞争Zn2+形成Zn(OH)2,使得肽中产生内源荧光的氨基酸重新得到释放,由此引起荧光强度的变化。
2.4 牡蛎源肽锌纳米粒消化过程中的扫描电镜观察
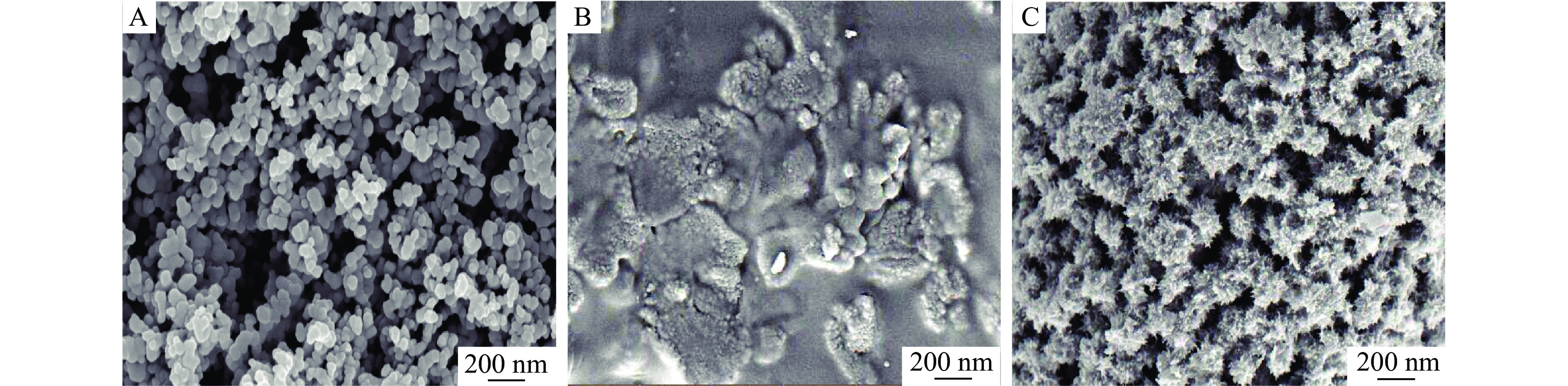
形态特征是对物体最直观的描述,而扫描电镜(SEM)具有几纳米的分辨率,可以将微小的甚至检测不到的物质放大几千倍,是一种评价食品材料形态特性的常用方法[11]。图4A、B、C分别显示了牡蛎源肽锌纳米粒消化前、胃部消化90 min与肠部消化150 min的表面形态,其中图A为前期研究成果[10]。由此看出牡蛎源肽锌纳米粒呈颗粒状结构,表面光滑,大小分布均匀,经过胃部消化后,表面略粗糙,原有颗粒聚集无规则块状且尺寸变大,到肠部消化时,其呈现表面更为粗糙的球状颗粒,且大小分布相对均匀。
在金属离子螯合之后,肽锌螯合物显示出具有相对均匀分布的纳米级颗粒,螯合物的形成不仅涉及肽和金属离子之间的共价相互作用,而且还涉及肽分子之间的非共价相互作用[27],这些力的作用使肽发生自组装行为[28],使肽与Zn2+之间的强相互作用导致形成更致密的颗粒。胃消化阶段,肽链上的电荷在酸性pH下被中和,电荷与Zn2+的相互作用丧失,使牡蛎源肽锌纳米粒发生解体。肠消化时pH提高到7.5,牡蛎源肽锌纳米粒重新形成更小尺寸的网格[29]。Perego等[30]表明,经过胃肠道消化后,酪蛋白磷酸肽钙聚集体变小,更有利于钙的吸收。
2.5 牡蛎源肽锌纳米粒消化过程中的透射电镜观察
肽锌螯合物主要通过Zn2+通道和小肽转运途径促进锌的肠道吸收[20],因此针对肠消化的不同时间段做了透射电子显微镜的观察,跟踪牡蛎源肽锌纳米粒的肠道消化动态、颗粒大小及团聚信息,监测肠道消化过程中Zn2+的存在形式。图5透射电子显微镜显示牡蛎源肽锌纳米粒在胃消化时同时存在圆球形和不规则块状形,原因是胃里部分螯合物发生分解,多肽与部分Zn2+解离,多肽之间的自组装导致颗粒变大[27-28],与扫描电子显微镜观察结果一致。进入肠道消化后,随消化时间的延长,大块颗粒慢慢解聚,开始纳米粒的重塑过程,部分游离Zn2+与多肽重新结合形成牡蛎源肽锌纳米粒[29],到肠消化60和90 min,小球状颗粒增多,至肠消化150 min均呈现均匀小球体,该结果与扫描电镜及粒径分布结果吻合。
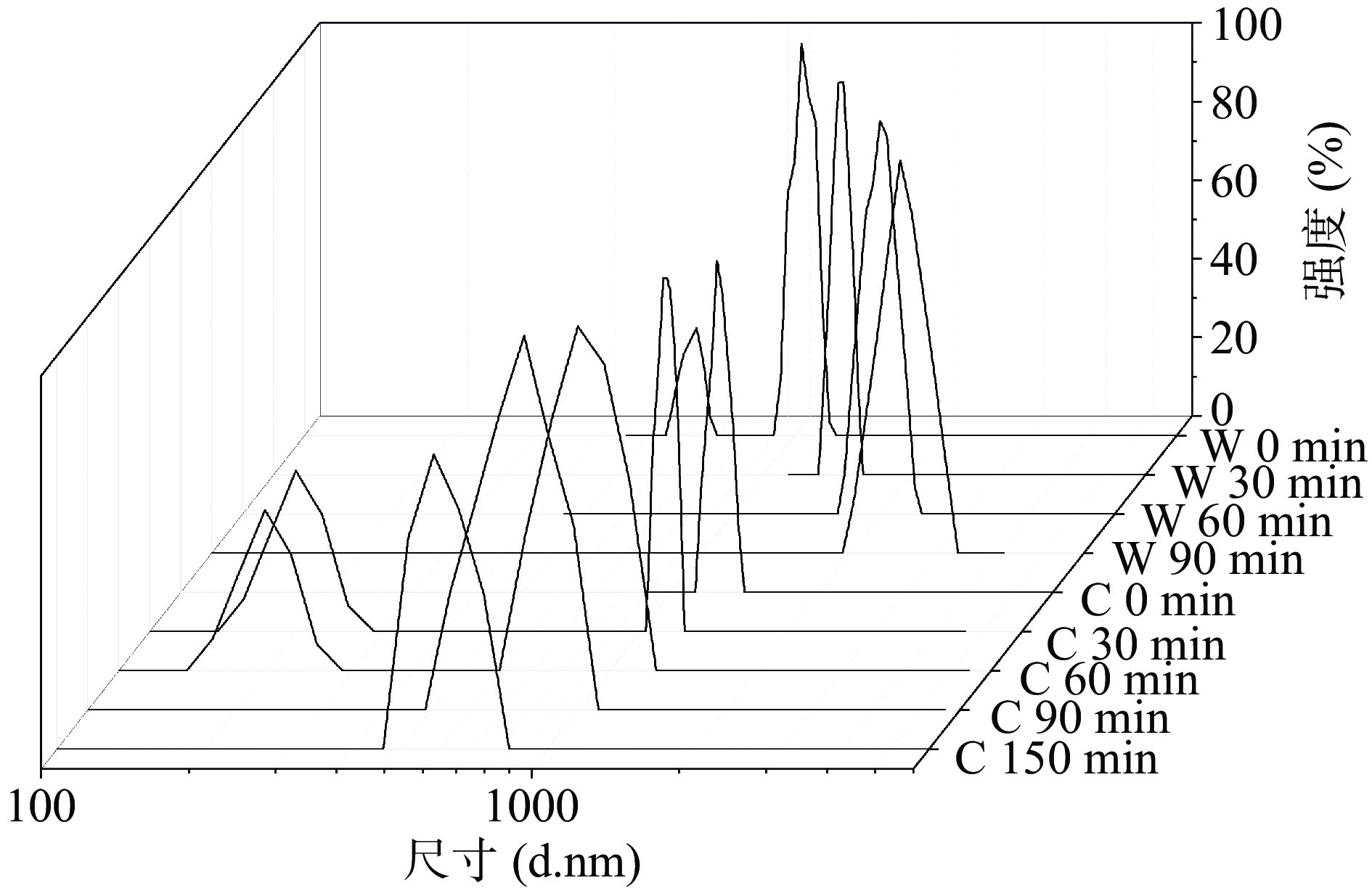
2.6 牡蛎源肽锌纳米粒消化过程中的粒径分布
粒径大小及其分布是评价纳米粒的重要参数,通过动态光散射(DLS)跟踪测定纳米粒在消化时的大小分布及解体情况[10]。牡蛎源肽锌纳米粒在胃肠道消化过程中的粒径分布如图6所示,整体来看,纳米粒在消化过程中大小分布均匀,并且集中在一个颗粒相对较大的峰中,但胃消化的粒径大于肠消化,胃消化0、30、60、90 min的过程中颗粒尺寸分布分别为1031.20±128、1417.86±107、1992.19±52、2536.28±87 nm,肠消化0、30、60、90、150 min过程中颗粒尺寸分布分别为1240.43±68、1132.88±27、863.32±44、775.41±57、586.63±29 nm。这种现象可能与复合物的解体有关,纳米粒在胃的过酸性环境中H+浓度的增加引起复合物的解聚,肽分子发生重组装,颗粒变大;当消化到肠液环境pH升高至7.5时,纳米粒的尺寸分布略有减小,表明在小肠pH条件下,牡蛎源肽锌纳米粒发生了自聚集,同时在胰蛋白酶的水解作用下使肽分子酶解成更小的肽或氨基酸并与锌重新螯合,在Cui等[29, 31]的海参卵肽钙复合体中也发现了一致结果。
粒径分布结果趋势与扫描电镜结果吻合,但干燥状态下测得的扫描电镜大小比用水溶液动态光散射(DLS)测量的小,这是因为纳米粒的单体形式(约900 Da)不能被DLS技术检测到,因为DLS只能测量分子量范围为103~2×107 Da的大小[32],因此,这种现象可能是由于Zn2+诱导溶液中的牡蛎肽的自组装,导致用DLS技术测量的大小偏大[27],在对玉米醇溶蛋白纳米颗粒的形态观察中也发现了类似的结果[16]。
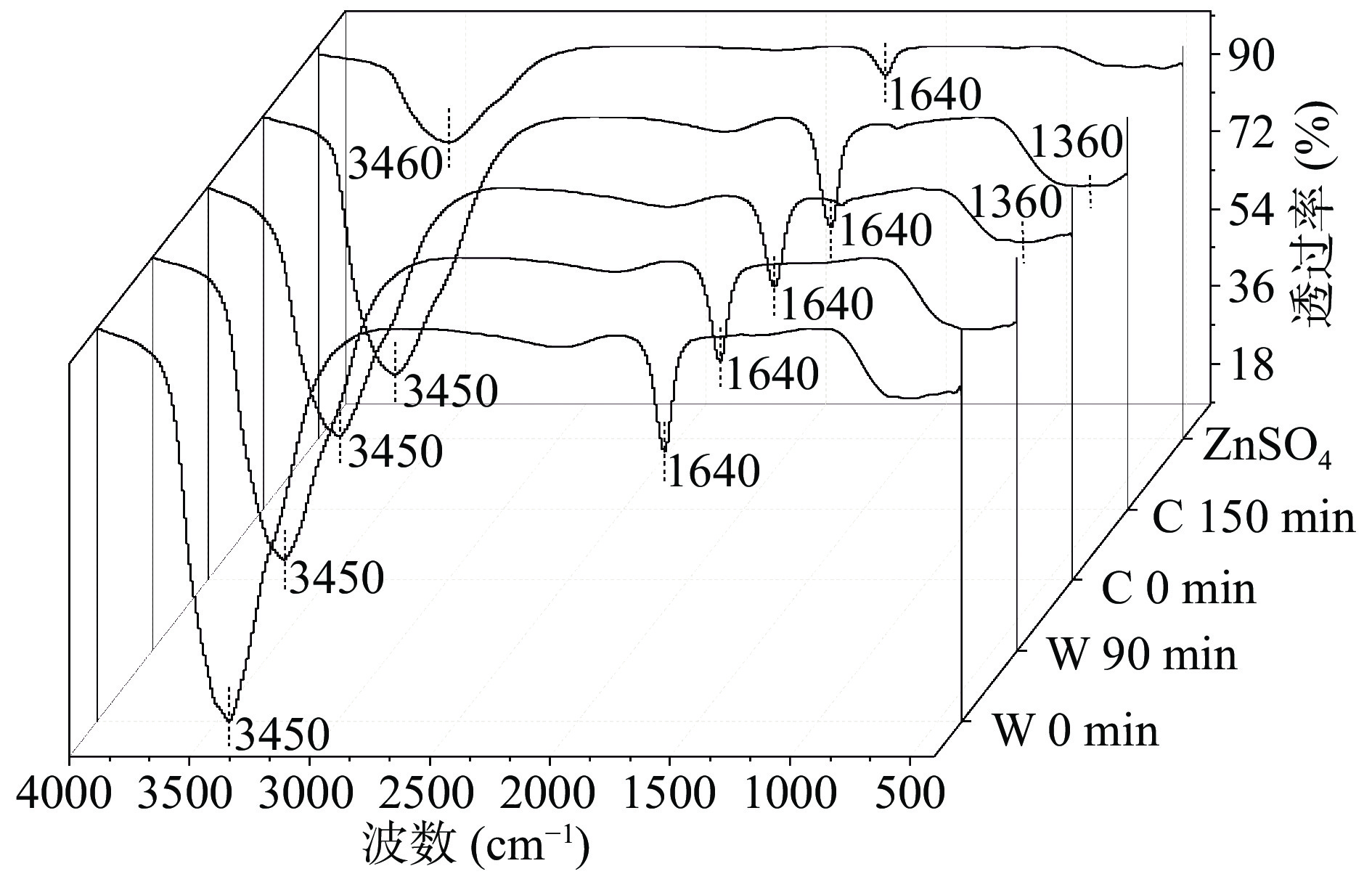
2.7 牡蛎源肽锌纳米粒消化过程中的傅里叶变换红外光谱分析
FTIR光谱可用于分析物质的组成并检测其官能团,是研究锌-肽复合物结合机理的有效方法,峰的变化可以反映锌与肽活性基团之间的相互作用[33]。不同消化程度的牡蛎源肽锌纳米粒在400~4000 cm–1波长范围内的红外光谱如图7所示,3450 cm−1处的吸收峰归因于-C-N基团的伸缩振动,胃液消化过程中,牡蛎源肽锌纳米粒在该位置吸收峰的透过率升高,吸收强度下降,说明牡蛎源肽锌纳米粒在胃液中发生部分解离,Zn2+与-NH键处的原子连接被断开[34],但肠液消化过程中峰强度变化不大,表明牡蛎源肽锌纳米粒在肠液中能够一定程度的保持稳定。在酰胺I带波长1640 cm−1处有吸收峰,是由于-C=O键的拉伸造成的[12, 29]。在消化过程中,该位置吸收峰几乎保持不变说明了该官能团在模拟胃肠道消化中保持稳定状态,与紫外结果一致。另外,在肠道消化中发现了在1360 cm−1处属于-COOH的吸收峰,该吸收带由-COO-Zn键产生,说明在消化过程中该官能团与Zn2+的结合情况发生了变化,这一现象与Zhu等[33]的研究结果一致。
3. 结论
本研究通过模拟体外胃肠道消化,研究不同消化程度下牡蛎源肽锌纳米粒的锌含量、状态及其结构变化,进而探究牡蛎源肽锌纳米粒的胃肠道动力学稳定性。结果表明,牡蛎源肽锌纳米粒的总锌含量高达228.89±2.35 mg/g,与硫酸锌相比,牡蛎源肽锌纳米粒可提高胃肠道中可溶性锌含量,具有更好的胃肠稳定性,这与Zn2+与肽键中羰基、羧基氧和氨基氮原子的配位作用不无关系。本研究表明牡蛎源肽锌纳米粒可以提高锌在人胃肠道的生物利用度,可作为新的锌营养补充剂开发利用,同时也为牡蛎深加工利用提供了新的方向。然而,具有锌螯合能力的肽序列需要进行进一步表征,以分析其分子结构与螯合能力之间的关系,肽锌纳米粒胃肠道消化过程中的肽组学信息和体内吸收机制还有待进一步研究。
-
-
[1] DEPCIUCH J, SOWA-KUCMA M, NOWAK G, et al. The role of zinc deficiency-induced changes in the phospholipid-protein balance of blood serum in animal depression model by Raman, FTIR and UV-vis spectroscopy[J]. Biomed Pharmacother,2017,89:549−558. doi: 10.1016/j.biopha.2017.01.180
[2] WANG C, LI B, AO J. Separation and identification of zinc-chelating peptides from sesame protein hydrolysate using IMAC-Zn2+ and LC-MS/MS[J]. Food Chem,2012,134(2):1231−1238. doi: 10.1016/j.foodchem.2012.02.204
[3] 曹玉惠, 张娟娟, 王再扬, 等. 牡蛎源类蛋白反应修饰肽的分离纯化及肽锌螯合物的结构表征[J]. 高等学校化学学报,2018,39(3):470−475. [CAO Y H, ZHANG J J, WANG Z Y, et al. Separation and identification of oyster peptide modified by plastein reaction and characterization of peptide-zinc complexes[J]. Chemical Journal of Chinese Universities,2018,39(3):470−475. doi: 10.7503/cjcu20170570 [4] LIU X, WANG Z, YIN F, et al. Zinc-chelating mechanism of sea cucumber (Stichopus japonicus)-derived synthetic peptides[J]. Mar Drugs,2019,17(8):438. doi: 10.3390/md17080438
[5] 王玉婷, 王志耕, 梅林, 等. 酪蛋白锌螯合工艺优化及其结合位点解[J]. 食品与发酵工业,2016,42(11):142−147. [WANG Y T, WANG Z G, MEI L, et al. Optimization of chelating process parameters of casein zinc and its binding sites analysis[J]. Food and Fermentation Industries,2016,42(11):142−147. doi: 10.13995/j.cnki.11-1802/ts.201611025 [6] PRASAD A S. Zinc: An antioxidant and anti-inflammatory agent: Role of zinc in degenerative disorders of aging[J]. J Trace Elem Med Biol,2014,28(4):364−371. doi: 10.1016/j.jtemb.2014.07.019
[7] MIQUEL E, FARRÉ R. Effects and future trends of casein phosphopeptides on zinc bioavailability[J]. Trends in Food Science & Technology,2007,18(3):139−143.
[8] 王允茹, 蔡秋杏, 张晨晓, 等. 北部湾海区三种常见牡蛎的蛋白质及氨基酸营养分析与评价[J]. 食品工业科技,2022,43(7):310−316. [[WANG Y R, CAI Q X, ZHANG C X, et al. Analysis and evaluation of protein and amino acid nutrition of three common oysters in Beibu Gulf[J]. Science and Technology of Food Industry,2022,43(7):310−316. doi: 10.13386/j.issn1002-0306.2021070302 [9] CHEN D, LIU Z, HUANG W, et al. Purification and characterisation of a zinc-binding peptide from oyster protein hydrolysate[J]. Journal of Functional Foods,2013,5(2):689−697. doi: 10.1016/j.jff.2013.01.012
[10] ZHANG Z, ZHOU F, LIU X, et al. Particulate nanocomposite from oyster (Crassostrea rivularis) hydrolysates via zinc chelation improves zinc solubility and peptide activity[J]. Food Chem,2018,258:269−277. doi: 10.1016/j.foodchem.2018.03.030
[11] LI C, BU G, CHEN F, et al. Preparation and structural characterization of peanut peptide-zinc chelate[J]. CyTA-Journal of Food,2020,18(1):409−416. doi: 10.1080/19476337.2020.1767695
[12] SUN R, LIU X, YU Y, et al. Preparation process optimization, structural characterization and in vitro digestion stability analysis of Antarctic krill (Euphausia superba) peptides-zinc chelate[J]. Food Chem,2021,340:128056. doi: 10.1016/j.foodchem.2020.128056
[13] 刘晶晶, 徐蕴桃, 朱晨慧, 等. 河蚬抗氧化肽—锌螯合物的制备及结构表征[J]. 食品与机械,2020,36(10):28−31, 48. [LIU J J, XUN Y T, ZHU C H, et al. Preparation and structural characterization of zinc-binding antioxidant peptides from Corbicula fluminea hydrolysate[J]. Food & Machinery,2020,36(10):28−31, 48. doi: 10.13652/j.issn.1003-5788.2020.10.006 [14] SUN N, CUI P, LIN S, et al. Characterization of sea cucumber (Stichopus japonicus) ovum hydrolysates: Calcium chelation, solubility and absorption into intestinal epithelial cells[J]. J Sci Food Agric,2017,97(13):4604−4611. doi: 10.1002/jsfa.8330
[15] 柯枭, 胡晓, 杨贤庆, 等. 罗非鱼皮胶原蛋白肽-锌螯合物的制备及结构表征与体外消化分析[J]. 食品与发酵工业,2021,47(14):38−44. [KE X, HU X, YANG X Q, et al. Preparation, structure characterization and in vitro gastrointestinal digestion of tilapia skin collagen peptide-zinc chelate[J]. Food and Fermentation Industries,2021,47(14):38−44. doi: 10.13995/j.cnki.11-1802/ts.026625 [16] ZHANG Y, NIU Y, LUO Y, et al. Fabrication, characterization and antimicrobial activities of thymol-loaded zein nanoparticles stabilized by sodium caseinate-chitosan hydrochloride double layers[J]. Food Chem,2014,142:269−275. doi: 10.1016/j.foodchem.2013.07.058
[17] WALCZAK A P, KRAMER E, HENDRIKSEN P J, et al. In vitro gastrointestinal digestion increases the translocation of polystyrene nanoparticles in an in vitro intestinal co-culture model[J]. Nanotoxicology,2015,9(7):886−894. doi: 10.3109/17435390.2014.988664
[18] 刘艳, 谷瑞增, 贾福怀, 等. 牡蛎肽螯合锌成分分析、结构表征及促细胞增殖作用[J]. 食品工业,2019,40(9):221−224. [LIU Y, GU R Z, JIA F H, et al. Composition analysis, structural characterization and promoting cell proliferation of oyster peptide-zinc chelates[J]. The Food Industry,2019,40(9):221−224. [19] 富天昕, 张舒, 盛亚男, 等. 绿豆多肽锌螯合物的制备及其结构与体外消化的分析[J]. 食品科学,2020,41(4):59−66. [FU T X, ZHANG S, SHENG Y N, et al. Preparation, structure and in vitro digestibility of zinc-chelating mung bean peptide[J]. Food Science,2020,41(4):59−66. doi: 10.7506/spkx1002-6630-20190710-137 [20] LI J, GONG C, WANG Z, et al. Oyster-derived zinc-binding peptide modified by plastein reaction via zinc chelation promotes the intestinal absorption of zinc[J]. Mar Drugs,2019,17(6):341. doi: 10.3390/md17060341
[21] WANG B, XIE N, LI B. Influence of peptide characteristics on their stability, intestinal transport, and in vitro bioavailability: A review[J]. J Food Biochem,2019,43(1):e12571. doi: 10.1111/jfbc.12571
[22] CAETANO-SILVA M E, NETTO F M, BERTOLDO-PACHECO M T, et al. Peptide-metal complexes: Obtention and role in increasing bioavailability and decreasing the pro-oxidant effect of minerals[J]. Critical Reviews in Food Science and Nutrition,2021,61(9):1470−1489. doi: 10.1080/10408398.2020.1761770
[23] ZHAO L, HUANG Q, HUANG S, et al. Novel peptide with a specific calcium-binding capacity from whey protein hydrolysate and the possible chelating mode[J]. J Agric Food Chem,2014,62(42):10274−10282. doi: 10.1021/jf502412f
[24] WANG Y, LI M, XU X, et al. Formation of protein corona on nanoparticles with digestive enzymes in simulated gastrointestinal fluids[J]. J Agric Food Chem,2019,67(8):2296−2306. doi: 10.1021/acs.jafc.8b05702
[25] ZHAO L, HUANG S, CAI X, et al. A specific peptide with calcium chelating capacity isolated from whey protein hydrolysate[J]. Journal of Functional Foods,2014,10:46−53. doi: 10.1016/j.jff.2014.05.013
[26] BEYER R L, HOANG H N, APPLETON T G, et al. Metal clips induce folding of a short unstructured peptide into an alpha-helix via turn conformations in water. Kinetic versus thermodynamic products[J]. Journal of The American Chemical Society,2004,126(46):15096−150105. doi: 10.1021/ja0453782
[27] CUI P, LIN S, HAN W, et al. The formation mechanism of a sea cucumber ovum derived heptapeptide-calcium nanocomposite and its digestion/absorption behavior[J]. Food Funct,2019,10(12):8240−8249. doi: 10.1039/C9FO01335K
[28] SONTZ P A, SONG W J, TEZCAN F A. Interfacial metal coordination in engineered protein and peptide assemblies[J]. Curr Opin Chem Biol,2014,19:42−49. doi: 10.1016/j.cbpa.2013.12.013
[29] CUI P, LIN S, JIN Z, et al. In vitro digestion profile and calcium absorption studies of a sea cucumber ovum derived heptapeptide-calcium complex[J]. Food Funct,2018,9(9):4582−4592. doi: 10.1039/C8FO00910D
[30] PEREGO S, DEL FAVERO E, DE LUCA P, et al. Calcium bioaccessibility and uptake by human intestinal like cells following in vitro digestion of casein phosphopeptide-calcium aggregates[J]. Food Funct,2015,6(6):1796−1807. doi: 10.1039/C4FO00672K
[31] CUI P, SUN N, JIANG P, et al. Optimised condition for preparing sea cucumber ovum hydrolysate-calcium complex and its structural analysis[J]. International Journal of Food Science & Technology,2017,52(8):1914−1922.
[32] GUERIN J, KRIZNIK A, RAMALANJAONA N, et al. Interaction between dietary bioactive peptides of short length and bile salts in submicellar or micellar state[J]. Food Chem,2016,209:114−122. doi: 10.1016/j.foodchem.2016.04.047
[33] ZHU S, ZHENG Y, HE S, et al. Novel Zn-binding peptide isolated from soy protein hydrolysates: Purification, structure, and digestion[J]. J Agric Food Chem,2021,69(1):483−490. doi: 10.1021/acs.jafc.0c05792
[34] LIAO W, LAI T, CHEN L, et al. Synthesis and characterization of a walnut peptides-zinc complex and its antiproliferative activity against human breast carcinoma cells through the induction of apoptosis[J]. J Agric Food Chem,2016,64(7):1509−1519. doi: 10.1021/acs.jafc.5b04924
-
期刊类型引用(1)
1. 梅洁,李芳,王晓雯,马慧,邱晓柔,刘思悦,孔令明. 核桃谷蛋白多肽及其肽锌螯合物的分离纯化、鉴定与结合位点分析. 食品科学. 2024(22): 2208-2216 .  百度学术
百度学术
其他类型引用(2)







 下载:
下载:

 下载:
下载:



