Anti-photoaging Effect and Mechanism of Tomato and Aronia melanocarpa Extract
-
摘要: 为了研究了番茄、野樱莓提取物抗皮肤光老化功效和机制,在UVB辐照HaCaT细胞模型上,研究了番茄、野樱莓提取物对细胞凋亡、活性氧(Reactive oxygen species,ROS)、前列腺素E2(Prostaglandin E2,PGE2)的影响。在UVB辐照ICR小鼠模型上,通过苏木精-伊红(hematoxylin-eosin,HE)染色评价番茄野樱莓组合物(LA)抵御皮肤光老化作用。研究皮肤组织中超氧化物歧化酶(superoxide dismutase,SOD)活性、丙二醛(Malondialdehyde,MDA)水平以及促炎因子白细胞介素-1β(Interleukin-1β,IL-1β)、白细胞介素-6(Interleukin-6,IL-6)、环氧化酶-2(Cyclooxygenase-2,COX-2)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)的表达变化。结果表明,番茄提取物和野樱莓提取物对HaCaT不存在细胞毒性。在HaCaT细胞光老化模型中,与模型组相比,100 μg/mL番茄提取物组和30 μg/mL野樱莓提取物组凋亡细胞数量显著减少(P<0.05)。100 μg/mL野樱莓提取物能够显著降低ROS水平(P<0.01)。100 μg/mL浓度下,野樱莓提取物和番茄提取物组都能够显著降低PGE2(P<0.05)。与模型组相比,口服LA能够使真皮厚度显著降低(P<0.01),皮肤组织中SOD活性显著增加(P<0.01),MDA水平显著降低(P<0.01),促炎因子IL-6、COX-2、TNF-α显著降低(P<0.05)。番茄、野樱莓提取物组合可以改善UVB诱导的氧化应激和炎症反应,具有抗光老化功效。Abstract: In order to investigate the anti-photoaging effect and mechanism of tomato and aronia extracts, the effects of tomato extract and aronia extract on apoptosis, reactive oxygen species (ROS) and prostaglandin E2 (PGE2) were studied in UVB-irradiated HaCaT cells. Hematoxylin-eosin (HE) staining was used to evaluate the anti-photoaging effect of tomato and aronia complex (LA) on skin photoaging in UVB-irradiated ICR mice. The activity of superoxide dismutase (SOD), the level of malondialdehyde (MDA) and the expression of pro-inflammatory factors interleukin-1β (IL-1β), interleukin-6 (IL-6), cyclooxygenase-2 (COX-2) and tumor necrosis factor-α (TNF-α) were detected. The results showed that tomato extract and aronia extract were not cytotoxic to HaCaT cells. In the photoaging model of HaCaT cells, compared with the model group, the number of apoptotic cells in 100 μg/mL tomato extract group and 30μg/mL aronia extract group were significantly decreased (P<0.05). Aronia extract (100 μg/mL) significantly decreased ROS level (P<0.01). At 100 μg/mL, PEG2 was significantly decreased in both tomato and aronia extract groups (P<0.05). Compared with the model group, LA treatment group resulted in a significant reduction in dermal thickness (P<0.01) and MDA levels (P<0.01), and a significant increase in SOD activity (P<0.01) in skin tissue, while the proinflammatory factors IL-6, COX-2 and TNF-α were all significantly decreased (P<0.05). Tomato and aronia complex can improve oxidative stress and inflammation induced by UVB, and has the effect of anti-photoaging.
-
Keywords:
- tomato /
- Aronia melanocarpa /
- skin /
- UVB /
- photoaging
-
皮肤衰老是一种复杂的生物学现象,包括内源性衰老和外源性衰老。内源性衰老是随着时间流逝生理和基因变化的必然结果,这些变化不仅发生在皮肤上,还发生在其他人体组织中。外源性老化是由于暴露于外部刺激(如紫外线辐射、环境毒素和传染性物质)导致DNA改变,以及皮肤皱纹、弹性降低、松弛和粗糙的外观变化[1]。阳光是对皮肤威胁最大的外部因素,因此,外源性老化也被称为光老化[2]。紫外线是阳光的重要组成部分,它通过与细胞内的发色体和光敏剂相互作用,产生过量的自由基,进而在皮肤细胞中产生严重的氧化应激。氧化应激可导致细胞损伤(如脂质过氧化和DNA碎片化)、细胞凋亡、炎症反应。长期紫外辐照会造成皮肤衰老,主要表现为皮肤红斑、粗糙、褶皱、表皮增厚和色素沉着[3]。
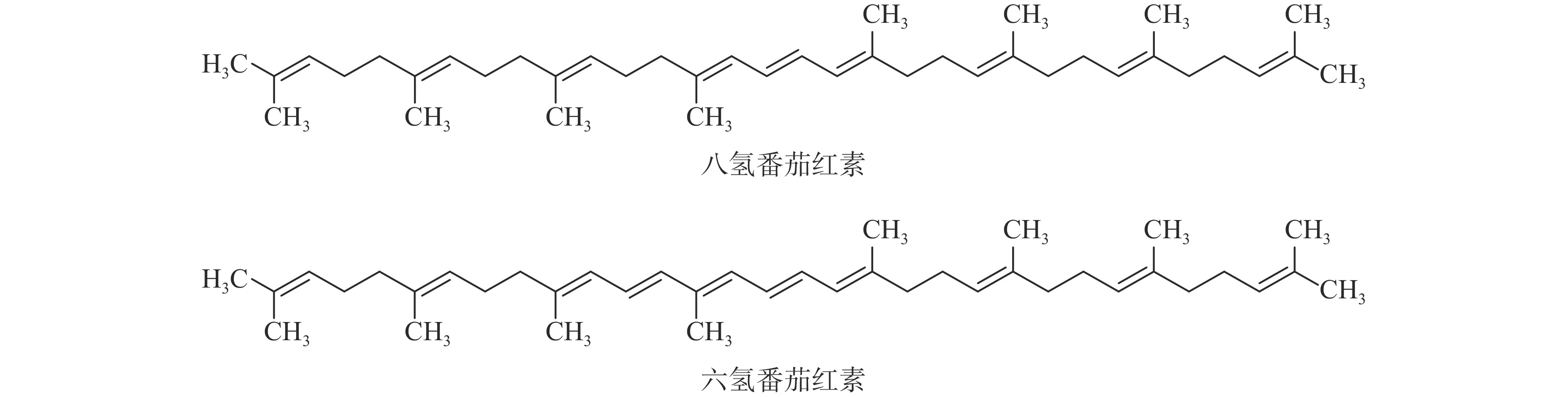
番茄Lycopersicon esculintum Mill.(LE)是人们生活中最常食用的蔬菜之一,含有丰富的类胡萝卜素。有颜色的类胡萝卜素,如番茄红素和β-胡萝卜素等已广泛应用于膳食补充剂中,通过摄入含有类胡萝卜素的食物或补充剂能够实现类胡萝卜素在皮肤中的沉积,显著抑制MMPs表达和MDA形成,以保护皮肤免受光照伤害[4]。有报道指出口服或局部使用这些颜色强烈的类胡萝卜素,会一定程度上造成皮肤黄色、橙色或红色的现象[5]。而无色番茄红素未见相关报道。无色的多氢番茄红素在皮肤中的积累比番茄红素更高效[6]。多氢番茄红素中的八氢番茄红素(phytoene)和六氢番茄红素(phytofluene)(见图1),由于烯烃链更短,所以能够最大限度地吸收紫外线[7]。这些研究提示无色番茄红素也具有光保护潜力。临床研究发现[8-9],口服番茄提取物Phytofl ORAL(相当于5 mg/d多氢番茄红素),能够提升皮肤抵御紫外辐照的能力,改善皮肤亮度,减少皮肤干燥和粗糙程度,均匀肤色和改善皮肤纹理。当皮肤受到紫外辐照发生损伤时,这类含有多氢番茄红素的番茄提取物通过何种生理机制发挥抗光老化作用还有待进一步的研究。
本文中关注的另一植物是野樱莓Aronia melanocarpa(AM),别名黑果腺肋花楸,富含花青素和原花青素。体外研究发现野樱莓提取物对N,N-二苯基三硝基苯肼自由基(DPPH·)具有较好的清除能力,可见其具有抗氧化活性[10]。局部使用野樱莓提取物能够抑制对苯二甲酸造成的耳肿胀,减少促炎细胞因子TNF-α、IL-1β和IL-6的表达,进一步研究发现野樱莓提取物可能通过抑制ROS-丝裂原活化蛋白激酶(MAPK)-核因子-κB(NF-κB)信号通路,抑制促炎介质的表达,从而发挥抗炎活性[11]。以累积剂量150 mJ/cm2 UVB辐照的ICR小鼠,连续1周背部涂抹1%野樱莓提取物,与模型对照组相比,皮肤厚度减少,MMP-1和MMP-3免疫化学反应减少,I型和III型胶原荧光反应增加,由此可见外用野樱莓提取物能够通过减弱UVB诱导的胶原蛋白破坏来减轻紫外光造成的光损伤[12]。但目前仅有外用延衰的研究,缺少口服野樱莓美容功效报道。Zhao等[13]发现口服野樱莓提取物通过调节AMPK/SIRT1/NF-κB通路抑制炎症,显著延缓小鼠脑衰老。此研究中口服延衰功效并未聚焦于皮肤,同时欠缺抗光老化的相关机制研究。
为了减少对皮肤颜色的影响,本研究将使用含有多氢番茄红素的番茄提取物和富含花青素的野樱莓提取物,在UVB辐照HaCaT角质形成细胞光损伤模型上,分别考察二者对紫外造成的细胞凋亡以及ROS、PGE2的影响。之后会进一步在UVB辐照ICR小鼠光老化模型上进行研究,探究口服番茄提取物和野樱莓提取物的混合物(以下简称为LA)能否通过抗炎抗氧化途径,减少皮肤的紫外损伤。以此填补番茄提取物和野樱莓提取物合用抗光老化功效机制研究的空白。为利用番茄提取物和野樱莓提取物研发功能性食品提供参考。
1. 材料与方法
1.1 材料与仪器
番茄提取物(含有11.00%类胡萝卜素,其中包括9.00%多氢番茄红素、30.07%饱和脂肪酸、50.02%不饱和脂肪酸) 以色列Lycored有限公司;野樱莓提取物(又名黑果腺肋花楸果果汁粉,花青素含量为1.8%,原花青素含量为8.55%,总糖11.6%,纤维3.20%,糊精为40%) 广州康莱食品添加剂有限公司;DL-α生育酚乙酸酯、羧甲基纤维素钠(CMC-Na)、H2DCF-DA、吖啶橙 Sigma公司;CCK-8、β-半乳糖苷酶染色试剂盒 Servicebio公司;RPMI1640培养基 Hyclone公司;青-链霉素 武汉Boster生物技术有限公司;0.25%胰蛋白酶 Gibco公司;胎牛血清 上海普飞生物技术有限公司;PGE2 ELISA试剂盒、SOD检测试剂盒、MDA检测试剂盒、COX-2 ELISA检测试剂盒 南京建成生物工程研究所;脱毛膏 广州依露化妆品有限公司;无水乙醇 杭州宏达化工仪器有限公司;二甲苯、盐酸分化液、中性树胶 国药集团化学试剂有限公司;苏木素染液 杭州浩克生物科技有限公司;氨水 MACKLIN上海麦克林生化科技有限公司;TNF-α ELISA检测试剂盒、IL-1β ELISA检测试剂盒、IL-6 ELISA检测试剂盒 博士德生物工程有限公司;人角质形成细胞系HaCaT 上海复祥生物科技有限公司;SPF级ICR雄性小鼠 32只,4周龄,体重18±2 g,购自浙江省医学科学院(实验动物生产许可证号:SCXK(浙)2019-0002)。
SH-4B紫外灯 上海希格玛高技术有限公司;D3024R台式高速冷冻型微量离心机 DragonLab;FBZ2001-up-p标准试剂型纯水仪 青岛富勒姆科技有限公司;SpectraMax M4多功能酶标仪 Molecular Devices公司;EG1150C包埋机、RM2235切片机、TP1020脱水机 LEICA公司;51A011 KD-P组织摊片机 浙江金华科迪仪器设备有限公司;HGPF-50烤箱 上海跃进医疗器械有限公司;DP260s达科为染色机 深圳市达科为医疗科技有限公司。
1.2 实验方法
1.2.1 样品制备
细胞实验中维生素E、番茄提取物用DMSO预溶,野樱莓提取物粉末用生理盐水新鲜配制,而后三者以新鲜RPMI1640培养基(10%胎牛血清,100 U/mL链霉素和100 U/mL青霉素)调至终浓度。维生素E终浓度为40 μg/mL,番茄提取物和野樱莓提取物终浓度为30和100 μg/mL。
动物实验中维生素E终浓度为80 mg/kg。根据文献所述多氢番茄红素抗光老化人体起效剂量为5 mg/d[8],原花青素美容功效人体起效剂量为24 mg/kg[14],因此本研究中使用50 mg/d番茄提取物和300 mg/d番茄提取物进行实验。最终番茄提取物和野樱莓提取物以1:6的质量比混合为混合物LA(相当于人体剂量为350 mg/d)。用0.1 mL/10 g体重的0.5% CMC-Na溶液配制样品,LA的最终给药剂量为53.08 mg/kg。
1.2.2 番茄提取物和野樱莓提取物抗UVB辐照HaCaT细胞光老化试验
1.2.2.1 CCK8法检测番茄提取物和野樱莓提取物对HaCaT细胞存活率的影响
将人角质形成细胞系HaCaT培养于RPMI1640培养基中(10%胎牛血清,100 U/mL链霉素和100 U/mL青霉素),移去培养基后,在室温下,经0.25%胰酶消化2 min,用含有10% FBS的培养基终止消化,1200 r/min离心10 min,用RPMI1640培养基重悬,并接种铺盘。利用2~4代的HaCaT细胞进行衰老实验。
将HaCaT细胞以2×104细胞/孔接种在96孔板中,在完全培养基中孵育24 h后,用生理盐水或10、30、100、300、1000 μg/L提取物进行处理。生理盐水组为对照组。48 h后,每孔加入10 μL CCK8溶液,反应1 h,使用酶标仪在450 nm处测定吸光值(OD)。细胞存活率(%)=(OD实验组−OD空白对照)/(OD对照组−OD空白对照)×100[15]。
1.2.2.2 HaCaT细胞培养
待HaCaT细胞生长至90%融合时,用0.25%胰蛋白酶消化,后以1×105个/mL接种于6孔培养板,贴壁后给予40 μg/mL维生素E,30、100 μg/mL番茄提取物和30、100 μg/mL野樱莓提取物分别处理24 h,待其70%融合时,移去培养基,进行UVB辐照。空白组和模型组细胞使用等量生理盐水处理24 h。模型组和各受试物处理组进行UVB辐照,紫外线与细胞之间的距离为15 cm,UVB能谱为312 nm,UVB强度为20 mJ/cm2。照射后,继续用受试物孵育,进行后续检测。
1.2.2.3 番茄提取物和野樱莓提取物对UVB导致HaCaT凋亡细胞数的影响
用Hoechst和吖啶橙(AO)染色法检测HaCaT的细胞凋亡指数[16]。在440 nm的荧光显微镜下,Hoechst染色和AO染色可见活细胞和死细胞的核。将细胞置于6孔培养板中培养,UVB辐照后,继续用受试物孵育6 h,PBS洗涤后,用不同的染料(10 μg/mL)染色30 min,在40倍的330/380 nm激发滤光片和440 nm阻挡滤光片荧光显微镜下观察细胞。选择物镜整体观察区域,计数细胞核碎裂或凝结的细胞数量。
1.2.2.4 H2DCF-DA测定ROS
UVB辐照后,继续用受试物孵育24 h后,用探针2’,7’-二氯荧光素-二乙酸测定ROS的形成[17-18]。荧光法测定细胞内ROS,37 ℃下,用10 mmol/L H2DCF-DA 孵育细胞15分钟。然后用0.01 mol/L PBS(pH7.3~7.4,包含0.9% NaCl)冲洗细胞两次,将细胞板放入酶标仪中。激发波长485 nm,发射波长538 nm。测定吸光值(OD)。荧光值DCF(a.u.)=OD实验组/OD对照[19]。
1.2.2.5 ELISA检测PGE2
UVB辐照后,受试物孵育24 h后,使用ELISA试剂盒测量培养上清中的PGE2浓度。
1.2.3 LA对UVB辐照小鼠皮肤光老化的影响
1.2.3.1 动物准备
选用4周龄雄性ICR小鼠,体重18±2 g,适应性喂养(温度为22~25 ℃,相对湿度为40%~70%,光照-黑暗循环为12 h:12 h,自由摄食饮水)1周后,开始试验。动物实验通过浙江省医学科学院实验动物伦理委员会批准,批准号:20201021-006。动物饲养于浙江省医学科学院实验动物中心SPF级动物房,实验动物使用许可证号:SYXK(浙)2019-0011。
1.2.3.2 动物分组及给药
实验开始前,称量实验动物体重并将32只ICR小鼠随机分为4组,每组8只。设置空白组、模型组、维生素E组(80 mg/kg)和LA组(53.08 mg/kg),空白组和模型组均给予0.5% CMC-Na溶液,各组动物每天灌胃1次,每只灌胃体积为0.1 mL/10 g体重,连续灌胃4周。
1.2.3.3 光老化小鼠模型的建立
除空白组外,其他各组实验动物用脱毛膏去除背部毛发,每天置于50 mL离心管中并固定尾部,离心管壁具有2×2 cm的空洞以便于紫外线直接照射动物皮肤,灯管距离背部1 cm。紫外线UVB照射剂量为:每周一、三、五照射,第一周每次54 mJ/cm2,第二周每次108 mJ/cm2,第三周和第四周每次均为200 mJ/cm2,总计量为1686 mJ/cm2[20]。
1.2.3.4 皮肤样本处理
分别于照射前和用药后1、2、3、4周时使用游标卡尺测量实验动物背部皮肤厚度。实验4周后,取小鼠背部正中面积为1 cm×1 cm大小,重量约0.5 g的完整皮肤组织,迅速放入10%中性甲醛固定,作组织切片进行组织形态学观察及计算机分析。
1.2.3.5 皮肤组织HE染色
将标本固定于10%甲醛溶液,按常规石蜡包埋、切片(约5 μm);切片脱蜡至水;入苏木素液中染色5 min,流水冲洗1次;1%盐酸酒精分化液分色15 s,流水冲洗2次;70%和90%酒精中各脱水10 min,1%伊红染色30 s,自来水冲洗,凉干;二甲苯透明,中性树胶封片。细胞核呈蓝色,细胞浆及间质呈红色。在光学显微镜下观察表皮和真皮情况,统计表皮和真皮厚度。
1.2.3.6 皮肤组织中的SOD活性和MDA含量的测定
取背部脱毛后皮肤组织约0.5 g,经预冷生理盐水漂洗,除去皮下脂肪和结缔组织,滤纸拭干,称重。量筒量取该组织块9倍重量预冷生理盐水,用眼科小剪剪碎皮肤组织块后倒入匀浆管中,与生理盐水混合后,用内切式组织匀浆机制成10%组织匀浆液,10000 r/min低温离心10 min,取上清备用。按照试剂盒说明书进行SOD活性和MDA含量测定。
1.2.3.7 皮肤组织中的TNF-α、IL-1β、IL-6、COX-2的测定
取组织匀浆上清液,采用酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)法测定皮肤组织匀浆液中TNF-α、IL-1β、IL-6、COX-2水平,具体操作严格参照试剂盒说明。
1.3 数据处理
采用Origin 9.0绘图软件作图,SigmaStat软件进行数据分析。所有数据均以均值±标准差表示,组间比较采用成组t检验,P<0.05表明结果具有统计学显著性。
2. 结果与分析
2.1 番茄提取物和野樱莓提取物对HaCaT细胞抗光老化作用的影响
2.1.1 番茄提取物和野樱莓提取物对HaCaT细胞存活率的影响
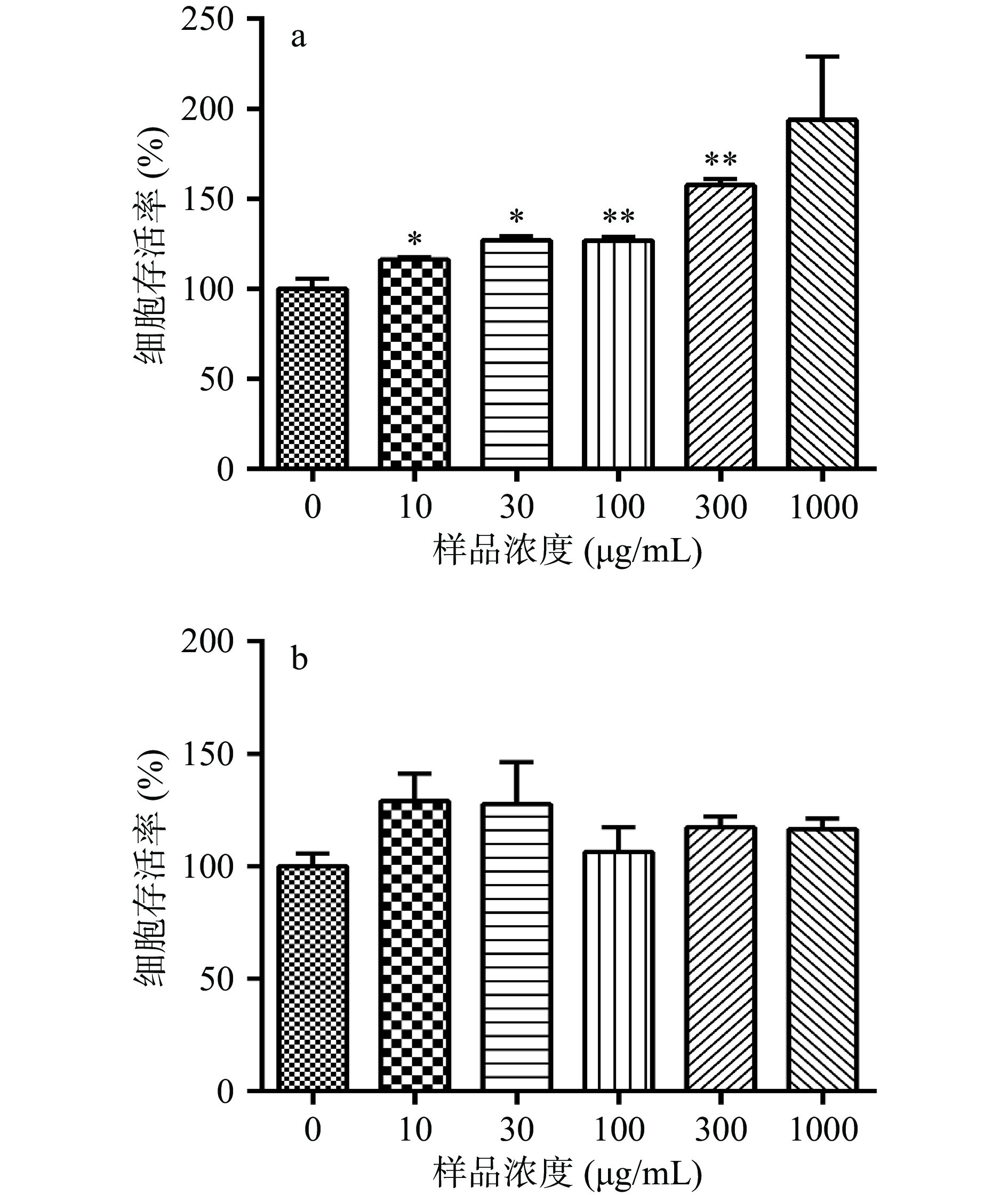
采用CCK8法检测番茄提取物和野樱莓提取物对HaCaT细胞是否具有毒性。图2结果表明,与对照组相比,番茄提取物在10、30、100、300 μg/mL显著(P<0.05)促进HaCaT细胞增殖。由于300 μg/mL番茄提取物使HaCaT存活率显著提升了57.5%,可知此浓度下对细胞增殖影响较大。同时为了便于后续机制研究能够有较为明显的变化呈现,因此选择对细胞存活率影响较小的30和100 μg/mL进行后续研究。野樱莓提取物在10~1000 μg/mL浓度范围内对HaCaT细胞的增殖没有显著影响。为了便于对番茄提取物和野樱梅提取物进行比较研究,在后续实验中将采用30、100 μg/mL浓度的番茄提取物和野樱莓提取物来进行各项细胞学研究。
2.1.2 番茄提取物和野樱莓提取物对UVB致HaCaT凋亡的影响
由表1所示,UVB辐照后含有凝聚的凋亡小体的角质形成细胞数量显著增加(P<0.05)。研究显示UVB辐射具有极强地基因毒性,将导致细胞凋亡,表现为胞膜有小泡状形成和细胞核碎裂[21]。本文中所述细胞模型呈现出细胞凋亡的显著增加,展现出UVB对角质形成细胞造成的光损伤特点。这也与Umar Muzaffer等[16]研究中,紫外辐照使HaCaT细胞凋亡体数量提高84.29%的报道一致。
表 1 受试物对UVB诱导HaCaT细胞凋亡的影响Table 1. Effect of test samples on cell apoptosis of HaCaT cell induced by UVB经过番茄提取物、野樱莓提取物和维生素E处理能够显著降低UVB导致的凋亡,提示上述受试物具有抗UVB诱导HaCaT细胞凋亡的作用,其中40 μg/mL维生素E显著减少凋亡细胞个数(P<0.05)。还能看到100 μg/mL番茄提取物和30 μg/mL野樱莓提取物显著减少凋亡细胞个数(P<0.05),但相较于维生素E未见显著差异。Fazekas等 [22]发现外用番茄红素能够有效减少紫外造成的细胞凋亡,通过抑制半胱天冬酶(caspase)-3的裂解,恢复增殖细胞核抗原(PCNA),阻断UVB损伤后的凋亡通路来防止DNA损伤。Calò等[23]研究发现富含花青素的欧洲越橘提取物能够显著减少紫外辐照后HaCaT凋亡细胞比例。本研究结果与上述文献报道相一致。
2.1.3 番茄提取物和野樱莓提取物对细胞中ROS和PGE2的影响
由表2所示,与空白组相比,UVB会导致角质形成细胞中ROS生成显著增加(P<0.05),100 μg/mL番茄提取物组ROS的荧光值极显著降低(P<0.01)。与维生素E相比,100 μg/mL野樱莓提取物有显著增加(P<0.05),其余提取物受试组均未有显著差异。与模型组相比,经过100 μg/mL番茄提取物和维生素E处理后荧光值能够显著降低(P<0.05),提示上述受试物均具有清除自由基的作用。结果显示,番茄提取物能够缓解UVB造成的ROS过度生成,减少氧化应激导致的细胞凋亡。这与Sara等[24]研究结果一致,富含类胡萝卜素的柿子提取物能够显著抑制紫外诱导角质形成细胞中ROS的产生。此外,ROS的降低可能是通过激活核因子E2相关因子2(Nrf2),刺激血红素氧合酶-1(HO-1)的表达,提高细胞抗氧化能力,使ROS生成维持正常水平,发挥细胞保护作用[25]。
表 2 受试物对UVB诱导HaCaT细胞中ROS和PGE2的影响Table 2. Effect of test samples on ROS and PGE2 in HaCaT cell induced by UVB组别 ROS(a.u.) PGE2(ng/g) 空白组 1.00±0.09 129.99±7.04 模型组 1.24±0.07* 188.11±18.04* 番茄提取物30 μg/mL 1.13±0.05$ 224.96±88.38 番茄提取物100 μg/mL 0.91±0.04**## 113.80±9.71**# 野樱莓提取物30 μg/mL 1.21±0.09 142.44±13.10 野樱莓提取物100 μg/mL 1.26±0.01*$ 152.74±12.85*# 维生素E 1.04±0.04# 108.62±41.62 表 3 受试物对ICR小鼠皮肤厚度的影响Table 3. Effect of test samples on skin thickness of ICR mice组别 皮肤厚度(mm) 空白组 1.60±0.36 模型组 3.45±0.45** 维生素E组 2.83±0.81** LA组 2.49±0.41**## 表 4 受试物对ICR小鼠真皮表皮厚度的影响Table 4. Effect of test samples on dermis and epidermis thickness of ICR mice组别 真皮厚度(μm) 表皮厚度(μm) 空白组 335.67±79.55 8.34±1.93 模型组 554.81±104.46** 40.35±22.25* 维生素E组 365.48±41.32## 25.85±11.73* LA组 354.18±93.20## 19.90±14.15 表 5 受试物对受试物对UVB诱导ICR小鼠光老化皮肤中SOD活性和MDA水平的影响Table 5. Effect of test samples on SOD activity and MDA level in skin of UVB induced skin photoaging model ICR mice组别 SOD(U/mg) MDA(nmol/mg) 空白组 22.20±24.44 11.08±1.42 模型组 13.95±13.27 22.72±1.64** 维生素E组 16.48±29.91 17.31±2.58**## LA 112.54±13.29**##$$ 13.02±2.24##$ 表 6 受试物对UVB诱导ICR小鼠光老化皮肤中炎症因子的影响Table 6. Effect of cytokine in skin of UVB induced skin photoaging model ICR mice组别 IL-1β(pg/mL) IL-6(pg/mL) COX-2(ng/mL) TNF-α(pg/mL) 空白组 77.79±59.57 84.89±50.88 3.94±1.23 8.12±7.29 模型组 118.30±113.21 162.63±63.79** 5.05±3.61 30.02±0.28** 维生素E组 101.20±107.47 102.55±71.42 3.63±2.52# 17.48±6.45**# LA 32.24±26.23* 63.34±44.14# 2.53±1.22# 4.95±3.39## 由表2所示,UVB会导致角质形成细胞中PGE2生成显著增加(P<0.05),与空白组相比,100 μg/mL番茄提取物也能够使PGE2生成极显著减低(P<0.01)。与维生素E相比,番茄提取物和野樱莓提取物均未有显著差异。值得注意的是,与模型组相比,100 μg/mL番茄提取物能够使PGE2生成显著减低到(113.80±9.71)ng/g(P<0.05)。这与Yoshihisa等[26]的研究结果一致,类胡萝卜素显著降低HaCaT角质形成细胞中COX-2的mRNA水平,减少PGE2的释放。Joseph Schwager等[27]的研究显示,番茄提取物还能够通过降低巨噬细胞中NO、PGE2、TNF-α、IL-1β和IL-6的产生,发挥抗炎作用。相较于模型组,经过100 μg/mL野樱莓提取物处理后显著降为(152.74±12.85)ng/g(P<0.05)。研究发现[28-29]花青素可能通过下调UVB诱导的COX-2,降低PGE2。在光老化细胞模型中,研究发现番茄提取物和野樱莓提取物具有清除ROS和PGE2的作用。在Azahara等[30]研究中发现外用类胡萝卜素通过Nrf-2途径下调COX-2和iNOS,上调HO-1蛋白,从而减轻UVB诱导的红斑。预测番茄提取物和野樱莓提取物可能通过提升皮肤细胞抗氧化能力缓解紫外造成的氧化应激,同时可能通过下调COX-2,减少PGE2、TNF-α、IL-1β和IL-6等促炎因子,来缓解紫外造成的皮肤损伤。接下来将在动物光老化模型中进一步研究番茄提取物和野樱莓提取物组合物的抗光老化机制。
2.2 LA对UVB辐照小鼠皮肤光老化的影响
2.2.1 皮肤厚度的变化
如表3实验结果所示,模型组皮肤厚度为(3.45±0.45)mm,与空白组相比,模型组小鼠皮肤厚度显著增加(P<0.01),维生素E组和LA组也显著增加(P<0.01)。这是由于UVB照射造成皮肤的急性损伤,由于炎症反应和水肿,常表现为皮肤厚度增加[31]。此外还观察到,LA组小鼠皮肤厚度为(2.49±0.41)mm,与模型组相比,LA能够显著降低皮肤厚度(P<0.01)。Fazekas等[23]发现番茄红素剂量依赖性地抑制UVB导致的皮肤厚度增加,与本研究结果一致。与维生素E组相比,LA组皮肤厚度有下降趋势,但无统计学差异。
2.2.2 LA对光老化小鼠皮肤组织病理学形态影响
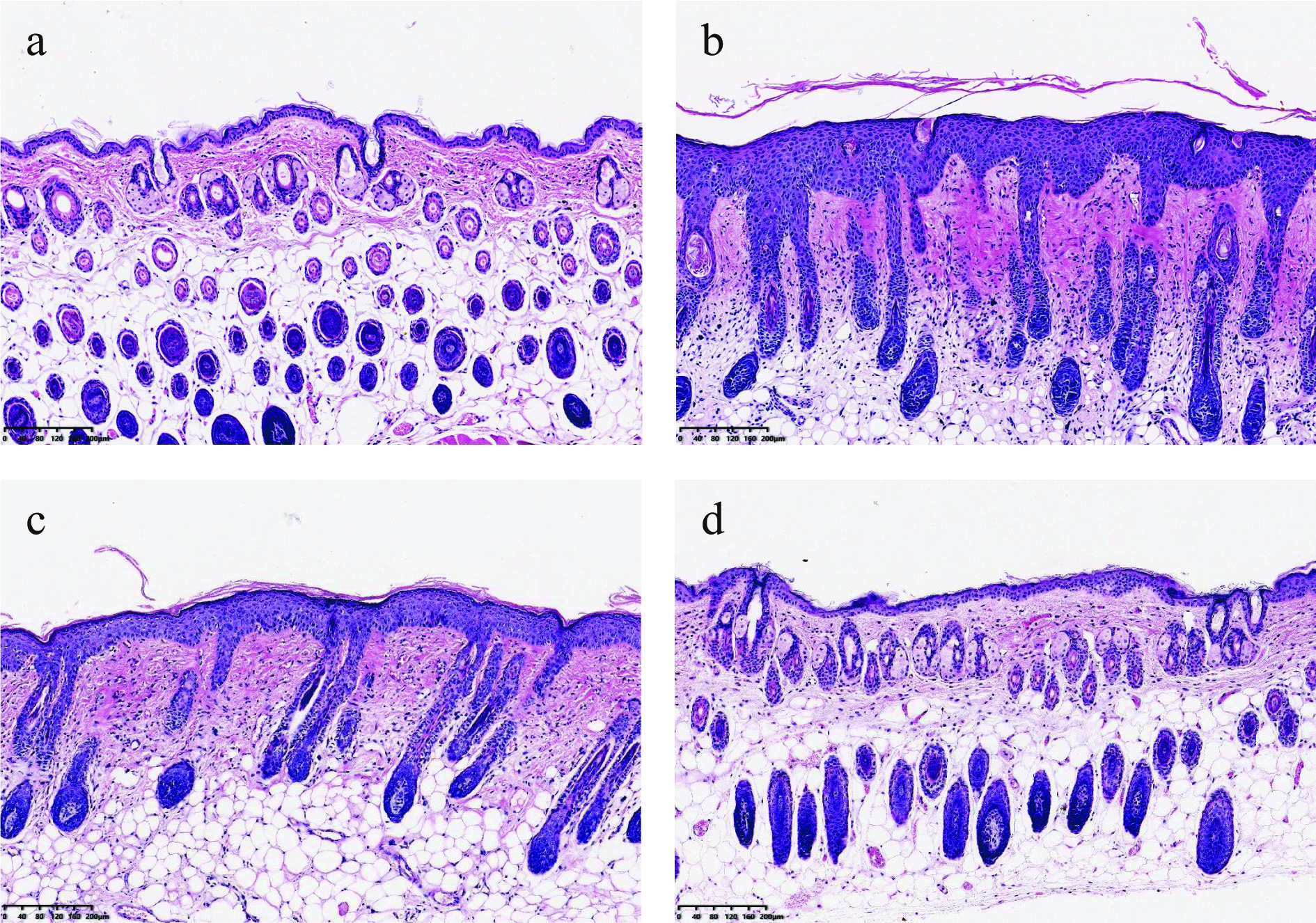
空白组小鼠皮肤组织结构完整,细胞分层清晰,表皮层较薄,真皮层中可以看到波浪状胶原纤维束,排列有序分布均匀,间质中均匀分布着成纤维细胞。模型组小鼠的皮肤结构紊乱,与对照组相比表皮层不规则地增厚,真皮层组织排列紊乱,胶原纤维断裂成团严重,有较多的炎性细胞浸润,这与文献[32-33]研究的紫外线引起的光老化小鼠皮肤变化特征是一致的。与模型组相比,维生素E组小鼠皮肤表皮厚度稍有减少,真皮层仍有成团现象,但排列较整齐,炎性细胞浸润有所减少。LA组小鼠的皮肤组织受损程度得到缓解,表皮结构完整厚度较薄,真皮层纤维排列趋向整齐,层次较清晰,极少有成团现象,比维生素E组更接近正常小鼠皮肤。
通过组织切片HE染色图片分析可知,与空白组比较,经过紫外辐照后的小鼠真皮和表皮厚度显著增加(P<0.05)。与模型组相比,LA组和维生素E组真皮厚度显著降低(P<0.01)(图3)。LA和维生素E都有降低表皮厚度的趋势,但与模型组相比没有显著性差异。与维生素E组相比,LA组真皮厚度和表皮厚度均有降低趋势,但无统计学差异。综合来看,LA能够显著降低紫外造成的真皮变厚,具有改善表皮变厚的趋势。
2.2.3 LA对光老化小鼠皮肤中SOD活性和MDA水平的影响
如表5所示,紫外照射导致皮肤中SOD活性降低,但与空白组相比没有显著性差异。与空白组相比,LA组能够极显著增加SOD活性(P<0.01)。与模型组相比,服用了LA能够使SOD活性极显著增加(P<0.01)。紫外照射导致皮肤中MDA显著增加到(22.72±1.64)U/mg(P<0.01),LA和维生素E能够分别使MDA显著降低到(13.02±2.24)nmol/mg和(17.31±2.58)nmol/mg(P<0.01)。与维生素E组相比,LA组SOD活性极显著增加(P<0.01),MDA水平显著降低(P<0.05)。暴露于紫外光下能通过各种机制间接导致ROS的产生。当ROS产生过多,超过了自身的抗氧化防御能力,就会发展为氧化应激。氧化应激能够导致细胞损伤、细胞凋亡和细胞死亡。MDA是脂质过氧化的重要产物之一,MDA水平能够客观反映自由基的水平[34]。本研究结果表明口服番茄提取物和野樱莓提取物的混合物能够提高光老化小鼠皮肤中SOD活性,降低MDA水平。杨斌等[4]研究显示番茄红素灌胃对UVA照射引起的MDA含量升高有显著抑制作用,本研究结果与其一致。Hatta等[35]已经证明,当八氢番茄红素和六氢番茄红素被添加到饮食中时,这些活性成分会优先在皮肤中积累。口服吸收的植物活性成分,通过血液循环运输到皮肤,提升SOD活力,清除多余自由基,减少紫外造成的氧化应激,减少细胞凋亡。
2.2.4 LA对光老化小鼠皮肤中IL-1β、IL-6、COX-2、TNF-α的影响
在UVB诱导下,与空白组相比,模型组皮肤中炎症因子IL-6和TNF-α极显著增加(P<0.01),而IL-1β、COX-2具有上升趋势。值得注意的是,与空白组相比,LA使皮肤中IL-1β显著降低(P<0.05)。给与受试物后,与模型组相比,维生素E能够显著降低COX-2和TNF-α水平(P<0.05)。LA使皮肤中IL-6显著下降为(63.34±44.14)pg/mL(P<0.05),COX-2显著下降为(2.53±1.22)ng/mL(P<0.05)、TNF-α极显著降低到(4.95±3.39)pg/mL(P<0.01)。与维生素E组相比,LA组IL-1β、IL-6、TNF-α、COX-2均有下降趋势,但无统计学差异。光老化皮肤中抗氧化防御机制水平降低,ROS会刺激皮肤中的炎症反应,使皮肤的中性粒细胞浸润增加,炎症反应增加[36]。急性UVB照射导致真皮肥大细胞脱颗粒增加[37]。通过释放组胺和PGE2等促炎介质,导致血管扩张、外溢和细胞浸润,产生辐射红斑[38]。本研究弥补了Tsoyi等[28]研究中只有外用抗光老化机制研究的不足,证明了口服LA能够通过降低皮肤中促炎因子TNF-α、IL-6、COX-2来缓解紫外造成的炎症反应,说明了细胞模型研究中PGE2的减少,可能是由于下调COX-2产生的结果。
研究发现UVB诱导皮肤炎症反应信号通路,如UVB激活细胞外信号调节激酶(ERK)1/2、c-Jun N-末端激酶(JNK)和p38通路[39]。随后,由c-Jun和c-Fos组成的AP-1复合物被磷酸化的JNK反式激活,诱导COX-2、TNF-α和IL-8等基因的表达[40]。这些研究表明天然植物成分或可通过抑制p38和ERK1/2 MAPK或NF-κB信号通路[41],减少COX-2表达和PGE2的生成。口服LA是否通过抑制MAPK/NF-κB信号通路来缓解紫外造成的皮肤光老化现象,这还需要进一步的研究验证。
3. 结论
本文发现番茄提取物和野樱莓提取物均能够清除ROS,抑制PGE2过度生成,减少UVB辐照造成的角质形成细胞凋亡,但其抑制光老化造成细胞凋亡的信号通路的机理还需要深入研究。口服二者组合物LA通过提高皮肤中SOD活力,降低MDA水平,显著下调IL-6、COX-2、TNF-α表达,减少炎症反应,改善UVB造成的皮肤异常增厚。但LA中番茄提取物和野樱莓提取物是否存在着协同增效作用还需要进一步的研究验证。综合来看,番茄提取物和野樱莓提取物具有保护皮肤减少紫外光老化损伤的作用,这为进一步探索番茄提取物和野樱莓提取物抗光老化的机制研究奠定了基础,为它们在美容保健品领域的应用提供了科学依据。
-
表 1 受试物对UVB诱导HaCaT细胞凋亡的影响
Table 1 Effect of test samples on cell apoptosis of HaCaT cell induced by UVB
表 2 受试物对UVB诱导HaCaT细胞中ROS和PGE2的影响
Table 2 Effect of test samples on ROS and PGE2 in HaCaT cell induced by UVB
组别 ROS(a.u.) PGE2(ng/g) 空白组 1.00±0.09 129.99±7.04 模型组 1.24±0.07* 188.11±18.04* 番茄提取物30 μg/mL 1.13±0.05$ 224.96±88.38 番茄提取物100 μg/mL 0.91±0.04**## 113.80±9.71**# 野樱莓提取物30 μg/mL 1.21±0.09 142.44±13.10 野樱莓提取物100 μg/mL 1.26±0.01*$ 152.74±12.85*# 维生素E 1.04±0.04# 108.62±41.62 表 3 受试物对ICR小鼠皮肤厚度的影响
Table 3 Effect of test samples on skin thickness of ICR mice
组别 皮肤厚度(mm) 空白组 1.60±0.36 模型组 3.45±0.45** 维生素E组 2.83±0.81** LA组 2.49±0.41**## 表 4 受试物对ICR小鼠真皮表皮厚度的影响
Table 4 Effect of test samples on dermis and epidermis thickness of ICR mice
组别 真皮厚度(μm) 表皮厚度(μm) 空白组 335.67±79.55 8.34±1.93 模型组 554.81±104.46** 40.35±22.25* 维生素E组 365.48±41.32## 25.85±11.73* LA组 354.18±93.20## 19.90±14.15 表 5 受试物对受试物对UVB诱导ICR小鼠光老化皮肤中SOD活性和MDA水平的影响
Table 5 Effect of test samples on SOD activity and MDA level in skin of UVB induced skin photoaging model ICR mice
组别 SOD(U/mg) MDA(nmol/mg) 空白组 22.20±24.44 11.08±1.42 模型组 13.95±13.27 22.72±1.64** 维生素E组 16.48±29.91 17.31±2.58**## LA 112.54±13.29**##$$ 13.02±2.24##$ 表 6 受试物对UVB诱导ICR小鼠光老化皮肤中炎症因子的影响
Table 6 Effect of cytokine in skin of UVB induced skin photoaging model ICR mice
组别 IL-1β(pg/mL) IL-6(pg/mL) COX-2(ng/mL) TNF-α(pg/mL) 空白组 77.79±59.57 84.89±50.88 3.94±1.23 8.12±7.29 模型组 118.30±113.21 162.63±63.79** 5.05±3.61 30.02±0.28** 维生素E组 101.20±107.47 102.55±71.42 3.63±2.52# 17.48±6.45**# LA 32.24±26.23* 63.34±44.14# 2.53±1.22# 4.95±3.39## -
[1] ZHANG S, DUAN E. Fighting against skin aging: the way from bench to bedside[J]. Cell Transplantation, 2018, 27(2): 096368971772575.
[2] CAVINATO M, JANSEN D P. Molecular mechanisms of UVB-induced senescence of dermal fibroblasts and its relevance for photoaging of the human skin[J]. Experimental Gerontology,2017,94:78−82. doi: 10.1016/j.exger.2017.01.009
[3] GU Y, HAN J, JIANG C, et al. Biomarkers, oxidative stress and autophagy in skin aging[J]. Ageing Research Reviews,2020,59:101036. doi: 10.1016/j.arr.2020.101036
[4] 杨斌, 刁庆春, 钟白玉, 等. 番茄红素对长波紫外线照射大鼠皮肤中丙二醛形成和基质金属蛋白酶表达的抑制作用[J]. 中华医学美学美容杂志,2006,12(6):358−361. [YANG B, DIAO Q C, ZHONG B Y, et al. Lycopene prevents UVA-induced MDA formation and matrix metalloproteinases mRNA expression in rat skin[J]. Chinese Journal of Medical Aesthetics and Cosmetology,2006,12(6):358−361. doi: 10.3760/cma.j.issn.1671-0290.2006.06.011 YANG B, DIAO Q C, ZHONG B Y, et al. Lycopene prevents UVA-induced MDA formation and matrix metalloproteinases mRNA expression in rat skin[J]. Chin J Med Aesth, 2006, 12(6): 358-361. doi: 10.3760/cma.j.issn.1671-0290.2006.06.011
[5] SANTOS V M, CAMILO A G, SOUZA L A, et al. A woman with treated breast cancer, recent neurological symptoms and xanthoderma[J]. Acta Medica Iranica, 2013: 195−198.
[6] MELÉNDEZ M A J, MAPELLI B P, STINCO C M. The colourless carotenoids phytoene and phytofluene: From dietary sources to their usefulness for the functional foods and nutricosmetics industries[J]. Journal of Food Composition and Analysis,2018,67:91−103. doi: 10.1016/j.jfca.2018.01.002
[7] MELÉNDEZ M A J, STINCO C M, MAPELLI B P. Skin carotenoids in public health and nutricosmetics: The emerging roles and applications of the UV radiation-absorbing colourless carotenoids phytoene and phytofluene[J]. Nutrients,2019,11(5):1093. doi: 10.3390/nu11051093
[8] VON O B L, HAVAS F, RAMOT O, et al. Phytoene and phytofluene for (photo) protection, anti-aging, lightening and evening of skin tone[J]. Sofw Journal Internationales Journal Fur Angewandte Wissenschaft,2014,140:8−12.
[9] VON O B L, FISHBEIN D, HAVAS F, et al. The photoprotective effects of a food supplement tomato powder rich in phytoene and phytofluene, the colorless carotenoids, a preliminary study[J]. Glob Dermatol,2015,2:178−182.
[10] 史俊燕, 邓天, 侯相林. 野樱莓果实提取物抗氧化性研究[J]. 农产品加工,2015,8(15):14−16. [SHI J Y, DENG T, HOU X L. Antioxidative activity from extracts of aronia[J]. Farm Products Processing,2015,8(15):14−16. SHI J Y, DENG T S, HOU X L. Antioxidative activity from extracts of aronia[J]. Farm Products Processing, 2015, 8: 14-16.
[11] GOH A R, YOUN G S, YOO K Y, et al. Aronia melanocarpa concentrate ameliorates pro-inflammatory responses in HaCaT keratinocytes and 12-O-tetradecanoylphorbol-13-acetate-induced ear edema in mice[J]. Journal of Medicinal Food,2016,19(7):654−662. doi: 10.1089/jmf.2015.3624
[12] HER Y, LEE T K, KIM J D, et al. Topical application of aronia melanocarpa extract rich in chlorogenic acid and rutin reduces UVB-induced skin damage via attenuating collagen disruption in mice[J]. Molecules,2020,25(19):4577. doi: 10.3390/molecules25194577
[13] ZHAO Y, LIU X, ZHENG Y, et al. Aronia melanocarpa polysaccharide ameliorates inflammation and aging in mice by modulating the AMPK/SIRT1/NF-κB signaling pathway and gut microbiota[J]. Scientific Reports,2021,11(1):1−15. doi: 10.1038/s41598-020-79139-8
[14] FURUMURA M, SATO N, KUSABA N, et al. Oral administration of french maritime pine bark extract (Flavangenol(®)) improves clinical symptoms in photoaged facial skin. Clinical Interventions in Aging. 2012, 7: 275-86.
[15] 戴妍, 林捷, 郑华, 等. 鸡肉酶解物对HepG2细胞抗氧化活性及小鼠血清抗氧化酶活性的影响[J]. 食品工业科技,2020,41(15):310−314,331. [DAI Y, LIN J, ZHENG H, et al. Effect of chicken hydrolysate on antioxidative activity of HepG2 cells and antioxidative enzyme activity of mouse serum[J]. Science and Technology of Food Industry,2020,41(15):310−314,331. DAI Y, LIN J, ZHENG H, et al. Effect of chicken hydrolysate on antioxidative activity of HepG2 cells and antioxidative enzyme activity of mouse serum[J]. Science and Technology of Food Industry, 2020, 41(15): 310- 314, 331.
[16] MUZAFFER U, PAUL V I, PRASAD N R, et al. Juglans regia L. protects against UVB induced apoptosis in human epidermal keratinocytes[J]. Biochemistry and Biophysics Reports,2018,13:109−115. doi: 10.1016/j.bbrep.2018.01.004
[17] MOU K, LIU W, HAN D, et al. HMGB1/RAGE axis promotes autophagy and protects keratinocytes from ultraviolet radiation-induced cell death[J]. Journal of Dermatological Science,2017,85(3):162−169. doi: 10.1016/j.jdermsci.2016.12.011
[18] BARALLA E, DEMONTIS M P, VARONI M V, et al. Bisphenol A and bisphenol S oxidative effects in sheep red blood cells: An in vitro study[J]. BioMed Research International, 2021, 2021.
[19] VITALE N, KISSLINGER A, PALADINO S, et al. Resveratrol couples apoptosis with autophagy in UVB-irradiated HaCaT cells[J]. PloS One,2013,8(11):e80728. doi: 10.1371/journal.pone.0080728
[20] CHOI S H, CHOI S I, JUNG T D, et al. Anti-photoaging effect of jeju putgyul (unripe citrus) extracts on human dermal fibroblasts and ultraviolet B-induced hairless mouse skin[J]. International Journal of Molecular Sciences,2017,18(10):2052. doi: 10.3390/ijms18102052
[21] SU Z Y, YANG Z Z, XU Y Q, et al. Apoptosis, autophagy, necroptosis, and cancer metastasis[J]. Molecular Cancer,2015,14(1):48. doi: 10.1186/1476-4598-14-1
[22] FAZEKAS Z, GAO D, SALADI R N, et al. Protective effects of lycopene against ultraviolet B-induced photodamage[J]. Nutrition and Cancer,2003,47(2):181−187. doi: 10.1207/s15327914nc4702_11
[23] CALÒ R, MARABINI L. Protective effect of vaccinium myrtillus extract against UVA-and UVB-induced damage in a human keratinocyte cell line (HaCaT cells)[J]. Journal of Photochemistry and Photobiology B:Biology,2014,132:27−35. doi: 10.1016/j.jphotobiol.2014.01.013
[24] GEA B S, MORENO C B, DE LA CASA L, et al. Carotenoids from persimmon (Diospyros kaki Thunb.) byproducts exert photoprotective, antioxidative and microbial anti-adhesive effects on HaCaT[J]. Pharmaceutics,2021,13(11):1898. doi: 10.3390/pharmaceutics13111898
[25] IMRAN M, GHORAT F, UL H I, et al. Lycopene as a natural antioxidant used to prevent human health disorders[J]. Antioxidants,2020,9(8):706. doi: 10.3390/antiox9080706
[26] YOSHIHISA Y, REHMAN M U, SHIMIZU T. Astaxanthin, a xanthophyll carotenoid, inhibits ultraviolet-induced apoptosis in keratinocytes[J]. Experimental dermatology,2014,23(3):178−183. doi: 10.1111/exd.12347
[27] SCHWAGER J, RICHARD N, MUSSLER B, et al. Tomato aqueous extract modulates the inflammatory profile of immune cells and endothelial cells[J]. Molecules,2016,21(2):168. doi: 10.3390/molecules21020168
[28] TSOYI K, PARK H B, KIM Y M, et al. Anthocyanins from black soybean seed coats inhibit UVB-induced inflammatory cylooxygenase-2 gene expression and PGE2 production through regulation of the nuclear factor-κB and phosphatidylinositol 3-kinase/Akt pathway[J]. Journal of Agricultural and Food Chemistry,2008,56(19):8969−8974. doi: 10.1021/jf801345c
[29] HE Y, HU Y, JIANG X, et al. Cyanidin-3-O-glucoside inhibits the UVB-induced ROS/COX-2 pathway in HaCaT cells[J]. Journal of Photochemistry and Photobiology B: Biology,2017,177:24−31. doi: 10.1016/j.jphotobiol.2017.10.006
[30] RODRÍGUEZ L A, ÁVILA R J, GONZÁLEZ-RODRÍGUEZ M L, et al. Fucoxanthin-containing cream prevents epidermal hyperplasia and UVB-induced skin erythema in mice[J]. Marine Drugs,2018,16(10):378. doi: 10.3390/md16100378
[31] ALAM S, PAL A, SINGH D, et al. Topical application of nexrutine inhibits ultraviolet B-induced cutaneous inflammatory responses in SKH-1 hairless mouse[J]. Photodermatology, Photoimmunology & Photomedicine,2018,34(1):82−90.
[32] VIYOCH J, MAHINGSA K, INGKANINAN K. Effects of thai musa species on prevention of UVB-induced skin damage in mice[J]. Food and Chemical Toxicology,2012,50(12):4292−4301. doi: 10.1016/j.fct.2012.08.060
[33] MOON J M, PARK S H, JHEE K H, et al. Protection against UVB-induced wrinkle formation in SKH-1 hairless mice: Efficacy of tricin isolated from enzyme-treated zizania latifolia extract[J]. Molecules,2018,23(9):2254. doi: 10.3390/molecules23092254
[34] AMER R I, EZZAT S M, ABOREHAB N M, et al. Downregulation of MMP1 expression mediates the anti-aging activity of Citrus sinensis peel extract nanoformulation in UV induced photoaging in mice[J]. Biomedicine & Pharmacotherapy,2021,138:111537.
[35] HATA T R, SCHOLZ T A, PERSHING L K, et al. Non-invasive raman spectroscopic detection of carotenoids in human skin[J]. Journal of Investigative Dermatology,2000,115(3):441−448. doi: 10.1046/j.1523-1747.2000.00060.x
[36] DE JAGER T L, COCKRELL A E, DU PLESSIS S S. Ultraviolet light induced generation of reactive oxygen species[J]. Ultraviolet Light in Human Health, Diseases and Environment, 2017: 15−23.
[37] SIISKONEN H, SMORODCHENKO A, KRAUSE K, et al. Ultraviolet radiation and skin mast cells: Effects, mechanisms and relevance for skin diseases[J]. Experimental Dermatology,2018,27(1):3−8. doi: 10.1111/exd.13402
[38] PENTLAND A P, MAHONEY M, JACOBS S C, et al. Enhanced prostaglandin synthesis after ultraviolet injury is mediated by endogenous histamine stimulation. A mechanism for irradiation erythema[J]. The Journal of Clinical Investigation,1990,86(2):566−574. doi: 10.1172/JCI114746
[39] PRASANTH M I, GAYATHRI S, BHASKAR J P, et al. Understanding the role of p38 and JNK mediated MAPK pathway in response to UV-A induced photoaging in caenorhabditis elegans[J]. Journal of Photochemistry and Photobiology B: Biology,2020,205:111844. doi: 10.1016/j.jphotobiol.2020.111844
[40] HUR S, LEE Y S, YOO H, et al. Homoisoflavanone inhibits UVB-induced skin inflammation through reduced cyclooxygenase-2 expression and NF-κB nuclear localization[J]. Journal of Dermatological Science,2010,59(3):163−169. doi: 10.1016/j.jdermsci.2010.07.001
[41] MUTHUSAMY V, PIVA T J. The UV response of the skin: A review of the MAPK, NF kappaB and TNF alpha signal transduction pathways[J]. Archives of Dermatological Research,2010,302(1):5−17.
-
期刊类型引用(2)
1. 王海萍,李爽,李慧,王伟光,秦鹏. 同位素稀释HPLC-MS法测定爆米花中7种真菌毒素. 食品安全导刊. 2025(07): 89-91 .  百度学术
百度学术
2. 祝伟霞,于卓然,郁露,刘亚风,魏蔚. 液相色谱-四极杆/静电场轨道阱高分辨质谱测定植物油中8种真菌毒素. 中国口岸科学技术. 2024(11): 48-53 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:
 下载:
下载:



