Process Optimization of Ultrasonic Co-germination for Enriching Black Highland Barley Polyphenols and Analysis of Phenolic Acid Composition
-
摘要: 研究以黑青稞为原料,采用单因素实验及Box-Behnken响应曲面法优化超声波协同萌发处理富集黑青稞多酚的最佳工艺参数,并在此基础上比较超声波协同萌发处理前后黑青稞的酚酸组成差异。结果表明,超声协同萌发富集黑青稞多酚的最佳工艺为:超声预处理功率350 W、超声处理温度30 ℃、超声处理时间25 min、萌发时间64 h,在此条件下黑青稞的总酚含量(688.84±5.30 mg/100 g DW)最高。酚酸物质结果表明,萌发处理显著提高了主要酚酸物质中原儿茶酸(游离和结合)、对羟基苯甲酸(游离)、香草酸(游离)、咖啡酸(游离)、丁香酸(游离)、对香豆酸(游离)的含量,分别提高为未处理组的14.49、1.54、4.73、1.67、1.46、3.73、11.49倍;而超声波协同萌发处理显著增加了尿黑酸(结合)、咖啡酸(结合)、对香豆酸(结合)、阿魏酸(结合)的含量,分别提高为未处理组的39.24、1.09、1.60、1.13倍。抗氧活性结果表明,经萌发处理及超声波协同萌发处理的黑青稞其DPPH·清除能力均显著增加,分别提高为未处理组的11.66%、21.55%。综上分析,萌发处理及超声协同萌发处理均为富集黑青稞中酚类物质及提高抗氧化活性的有效手段,可根据不同酚酸物质单体及形态选择合适的富集方法,该研究可为进一步提高黑青稞的利用价值提供参考。Abstract: In this study, the single factor experiment and the Box-Behnken response surface method were employed to find the optimum process parameters of ultrasonic co-germination on enriching black highland barley polyphenols, and the differences in phenolic acid composition were compared before and after ultrasonic co-germination treatment on the basis. The results showed that the optimal process parameters were obtained with ultrasonic pretreatment power 350 W at 30 ℃ for 25 min, and germination time 64 h. The total phenolic content of black highland barley (688.84±5.30 mg/100 g DW) was the highest under the conditions. The results for phenolic acids showed that the contents of protocatechuic acid (free and bound), p-hydroxybenzoic acid (free), vanillic acid (free), caffeic acid (free), syringic acid (free) and p-coumaric acid (free) were increased significantly in the main phenolic acids, which was 14.49, 1.54, 4.73, 1.67, 1.46, 3.73 and 11.49 times of the untreated group respectively after germination treatment. The contents of homogentisic acid (bound), caffeic acid (bound), p-coumaric acid (bound) and ferulic acid (bound) were increased significantly after ultrasonic co-germination treatment, which was 39.24, 1.09, 1.60 and 1.13 times of the untreated group respectively. The DPPH-scavenging capacity treated with germination and ultrasonic co-germination increased significantly by 11.66% and 21.55%, respectively. In summary, both treatments were effective means for enriching phenolic substances and improving antioxidant activity in black highland barley, and suitable enrichment methods could be selected according to different phenolic acid monomers and forms. This study could provide the reference for further improving the utilization value of black highland barley.
-
青稞又称裸大麦,是青藏高原的一种特色农作物,主要分布在海拔4200~4500 m的高寒地区,具有高蛋白、高纤维、高直链淀粉、高β-葡聚糖及低糖低脂的营养特色[1]。目前关于青稞活性物质的研究大多集中在β-葡聚糖、膳食纤维及多酚类化合物方面,其中多酚类化合物因其良好的抗氧化、抗癌、抗炎、抑菌活性而受到广泛关注。本团队前期研究发现,有色青稞含有更丰富的酚类物质及更高的生物活性[2],具有更高的应用前景。但大量研究表明,青稞中的酚类物质多以结合态形式存在,且主要(约95%)与细胞壁多糖连接而成[3],生物可利用度较低,在实际应用中难以发挥其价值。研究表明通过外界手段刺激植物的生长代谢能够有效实现多酚等活性物质的富集并提高其生物利用率[4]。因此,通过干预谷物代谢途径的手段诱导青稞中酚类物质的富集,对黑青稞及其酚类物质的开发利用具有指导意义。
萌发是一种有效改善和增强植物组织结构及营养品质的方式[5-6]。多项临床和流行病学研究表明,发芽全谷物有利于降低胆固醇、抗糖尿病、抗癌以及改善肠道微生物群[7-10]。超声波是一种安全高效的物理刺激手段,研究表明适当的超声波刺激能够提高谷物种子的萌发率[11]。近年来也有学者采用超声波胁迫萌发的方式对谷物进行处理并得到了理想的效果。据报道,经超声波处理后的发芽黑糙米总酚含量明显提高[12]。此外,Ding等[13]研究发现超声处理5 min能够显著增加发芽燕麦的蒽酰胺含量,且萌发24 h其DPPH自由基清除率提高了28.50%。但不同强度的超声处理以及不同时间的萌发处理会对谷物中的活性物质积累产生不同的影响,过度的超声波处理可能会引发酚类物质的降解[14-15]。目前关于青稞中活性物质富集的相关研究还未见报道,且超声波协同萌发处理后酚酸类化合物及抗氧化活性的变化尚不明确。为高效利用萌发技术的优势,进一步提高全谷物生物活性,本研究旨在通过响应面优化试验确定超声波协同萌发处理富集黑青稞多酚的最佳工艺,并探究超声波协同萌发处理前后黑青稞酚酸组成及其抗氧化活性的变化,以期为黑青稞的精深加工及其产品研发提供理论依据。
1. 材料与方法
1.1 材料与仪器
青稞(昆仑20号) 青海省农林科学院提供;福林酚(优级纯) 北京索莱宝科技有限公司;丙酮、乙酸乙酯、甲醇(分析纯) 国药集团化学试剂有限公司;没食子酸、尿黑酸、原儿茶酸、对羟基苯甲酸、绿原酸、香草酸、邻羟基苯乙酸、咖啡酸、丁香酸、对香豆酸、阿魏酸、藜芦酸、苯甲酸、水杨酸、邻香豆酸(纯度≥98.0%) 上海源叶生物科技有限公司;1,1-二苯基-2-三硝基苯肼(1,1-Diphenyl-2-Picrylhydrazyl,DPPH) 美国Sigma公司。
KQ-500GDV恒温数控超声波清洗器 昆山市超声仪器有限公司;HWS-250F恒温恒湿培养箱 宁波普朗特仪器有限公司;HK-04A手提式万能粉碎机 上海科恒实业发展有限公司;TGL-20M高速台式冷冻离心机 湖南长沙湘仪离心机仪器有限公司;Retavapor R-215旋转蒸发仪 瑞士布奇有限公司;N4S紫外可见分光光度计 上海仪电分析仪器有限公司;DIONEX UltiMate 3000超高效液相色谱-Orbitrap质谱联用仪(UHPLC-Q/Exactive)(配有可加热的电喷雾离子源(HESI)及Xcalibur3.0数据处理系统) 美国Thermo Fisher Scientific公司。
1.2 实验方法
1.2.1 未处理黑青稞样品的制备
选择颗粒饱满、无破损的青稞种子,粉碎、过80目筛备用。
1.2.2 萌发黑青稞样品的制备
1.2.2.1 预处理
选择颗粒饱满、无破损的青稞种子,用自来水冲洗除去杂质与灰尘,并用1%次氯酸钠溶液浸泡20 min进行消毒,随后用蒸馏水冲洗干净,用3倍体积的蒸馏水将青稞种子置于20 ℃下浸泡12 h。
1.2.2.2 正常萌发黑青稞样品的制备
浸泡后的黑青稞种子沥干水分后置于铺有双层滤纸的培养皿中,于28 ℃条件下进行萌发,期间每隔4 h喷洒蒸馏水使种子保持湿润,萌发结束后将黑青稞样品冷冻干燥24 h,粉碎、过80目筛备用。
1.2.2.3 超声波协同萌发黑青稞样品的制备
浸泡后的黑青稞种子沥干水分装入透明自封袋中,置于超声波清洗器的水槽中,设置一定的超声波条件对青稞种子进行胁迫处理。随后将其置于铺有双层滤纸的培养皿中,于28 ℃条件下进行萌发,期间每隔4 h喷洒蒸馏水使种子保持湿润,萌发结束后将黑青稞样品冷冻干燥24 h,粉碎、过80目筛备用。
1.2.3 多酚富集工艺单因素实验
取昆仑20号青稞,在萌发时间为48 h、超声功率300 W、超声时间30 min、超声温度30 ℃的恒定条件下,分别考察萌发时间(24、36、48、60、72、84 h)、超声功率(200、300、400、500 W)、超声时间(10、20、30、40、50 min)、超声温度(20、25、30、35、40 ℃)对萌发青稞中酚类物质的影响。
1.2.4 多酚富集工艺响应面试验
根据单因素实验结果,采用Box-Behnken响应面试验设计方法以萌发时间、超声功率和超声时间为显著影响因素,以总酚含量为响应值设计三因素三水平响应面分析试验,试验设计如表1所示。
表 1 响应面试验因素与水平Table 1. Response surface test factors and levels水平 A 萌发时间(d) B 超声功率(W) C 超声时间(min) −1 48 300 20 0 60 350 25 1 72 400 30 1.2.5 酚类物质的提取
1.2.5.1 游离酚提取
准确称取1.0 g青稞全粉,加入25 mL体积分数为80%的丙酮溶液,振荡后室温条件下超声处理20 min,3000 r/min离心15 min,收集上清液,残渣用同样方法提取一次。合并两次上清液,于45 ℃下旋转蒸干,残余物用无水甲醇定容至10 mL,并用0.45 μm有机膜过滤,即得到青稞游离酚提取物,−20 ℃避光保存。
1.2.5.2 结合酚提取
向提取完游离酚的残渣中加入20 mL正己烷,振荡后3000 r/min离心5 min,离心结束后弃去上清液,向沉淀物中加入17 mL体积分数为11%的盐酸-甲醇溶液,摇匀后于70 ℃下水浴1 h,用20 mL乙酸乙酯萃取两次,合并萃取液并在45 ℃下旋转蒸干,用无水甲醇定容至10 mL,并用0.45 μm有机膜过滤,得到青稞结合酚提取物,−20 ℃避光保存。
1.2.6 多酚含量的测定
游离酚、结合酚含量的测定采用Folin-Ciocalteu法,总酚含量即为二者之和,具体参照杨希娟等[16]的方法。多酚含量以100 g样品中(干重)没食子酸当量计,没食子酸标准曲线:y=0.0038x+0.0785(50~400 μg/mL,R2=0.9987)。
1.2.7 酚酸类物质组成分析
对不同萌发方式下黑青稞样品的酚酸组分进行定性定量分析,具体方法参照文献[17]进行测定。色谱条件:色谱柱为Hypersil GOLD aQ(100 mm×2.1 mm);柱温30 ℃;样品盘温度(4±0.5)℃;流动相:0.9%乙酸-水溶液(A相),甲醇(B相);梯度洗脱;洗脱程序:−0.5~0 min、20% B,0~9 min、20%~100% B,9~10 min、100% B,10~11 min、100%~20% B,11~14 min、20% B;流速0.3 mL/min;进样量1 μL。质谱条件:采用电喷雾离子源(ESI);扫描模式为Full MS(扫描范围100~850 m/z);正/负离子扫描模式;载气采用高纯氮气(纯度>99.5%),鞘气流速40个单位,辅气流速10个单位,吹扫气流速0个单位;喷雾电压2.80 kV;离子透镜电压频率55,毛细管温度300 ℃,辅气热源温度300 ℃。
1.3 数理处理
采用Excel和SPSS26进行数据整理及分析,数据以三次重复试验结果的平均值±标准差(Means±SD)表示。采用Duncan法进行多组样本间差异显著性分析;采用Design Expert 10.0.1软件进行中心组合试验设计;采用OriginPro软件作图。
2. 结果与分析
2.1 单因素实验结果
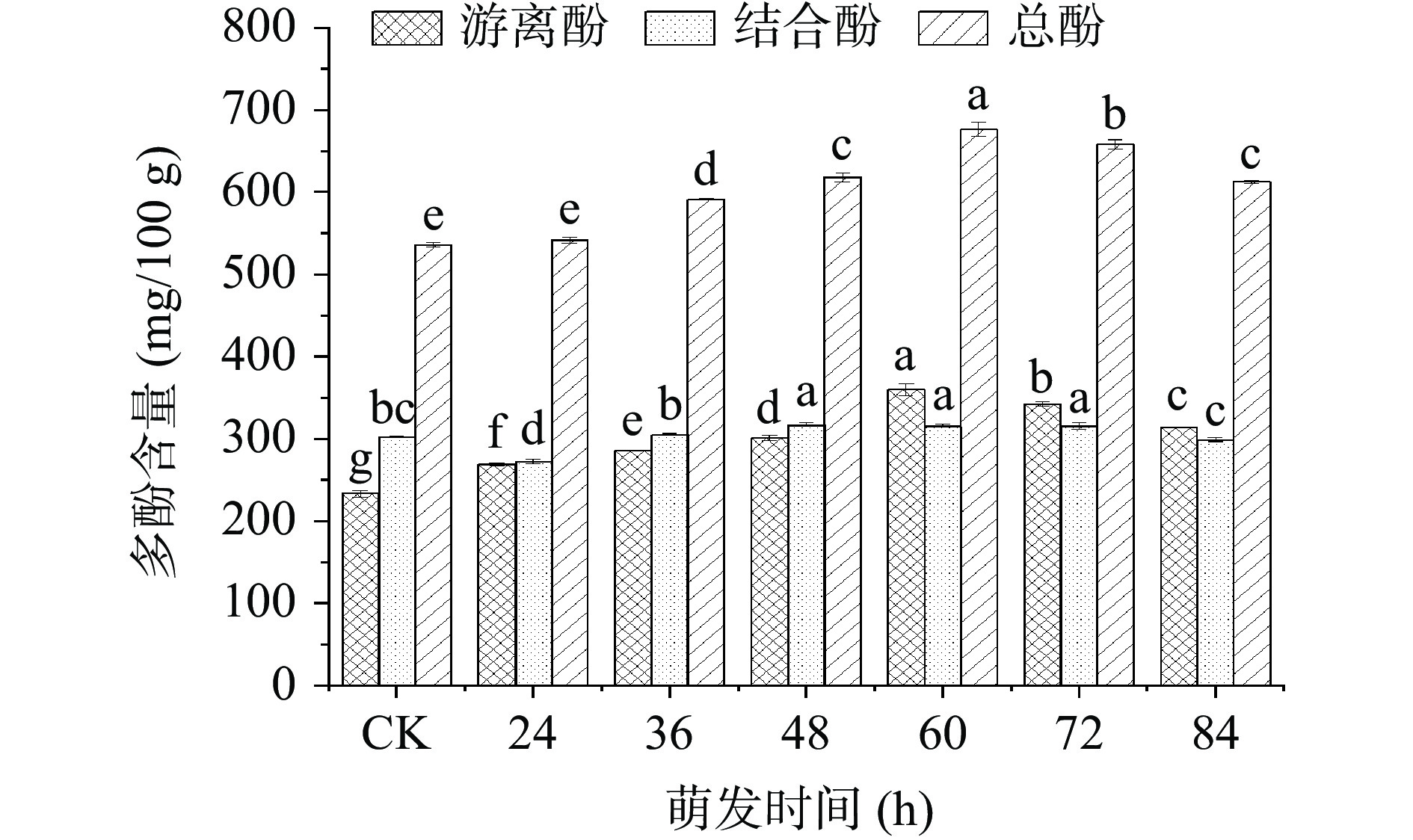
2.1.1 不同萌发时间对青稞中多酚含量的影响
不同萌发时间对青稞中多酚含量的影响见图1,CK为未处理黑青稞。由图1可知,黑青稞萌发24 h时结合酚及总酚略低于对照组,这与付晓燕等[18]的研究结果一致。可能是因为萌发初期多酚氧化酶的活力较高[19],因此部分多酚被氧化分解。萌发24 h后,随着萌发时间的延长,青稞中游离酚、结合酚、总酚含量均呈先升高后降低的趋势且存在显著性差异(P<0.05)。当萌发60 h时游离酚、结合酚及总酚含量均最高,分别为359.99±7.35、316.11±1.13和676.11±8.48 mg/100 g,与对照组相比分别提高了54.37%、4.45%和26.18%。其中游离态酚类物质含量上升的原因可能是因为青稞中的酚类物质主要以游离态和结合态形式存在,其中结合态酚类物质多与蛋白质、多糖、淀粉及纤维等大分子结合,多被细胞壁束缚,不能直接提取出来,而在萌发过程中一系列复杂的反应使共价键发生断裂,使结合酚转化为游离酚[20]。而结合酚含量的增加可能与萌发过程中新的酚类物质的合成有关[21]。当萌发时间超过60 h后多酚含量呈现下降趋势,可能是因为萌发后期种子的呼吸作用[22]消耗了部分酚类物质。因此,在富集多酚的响应面试验中选择48~72 h的萌发时间范围。
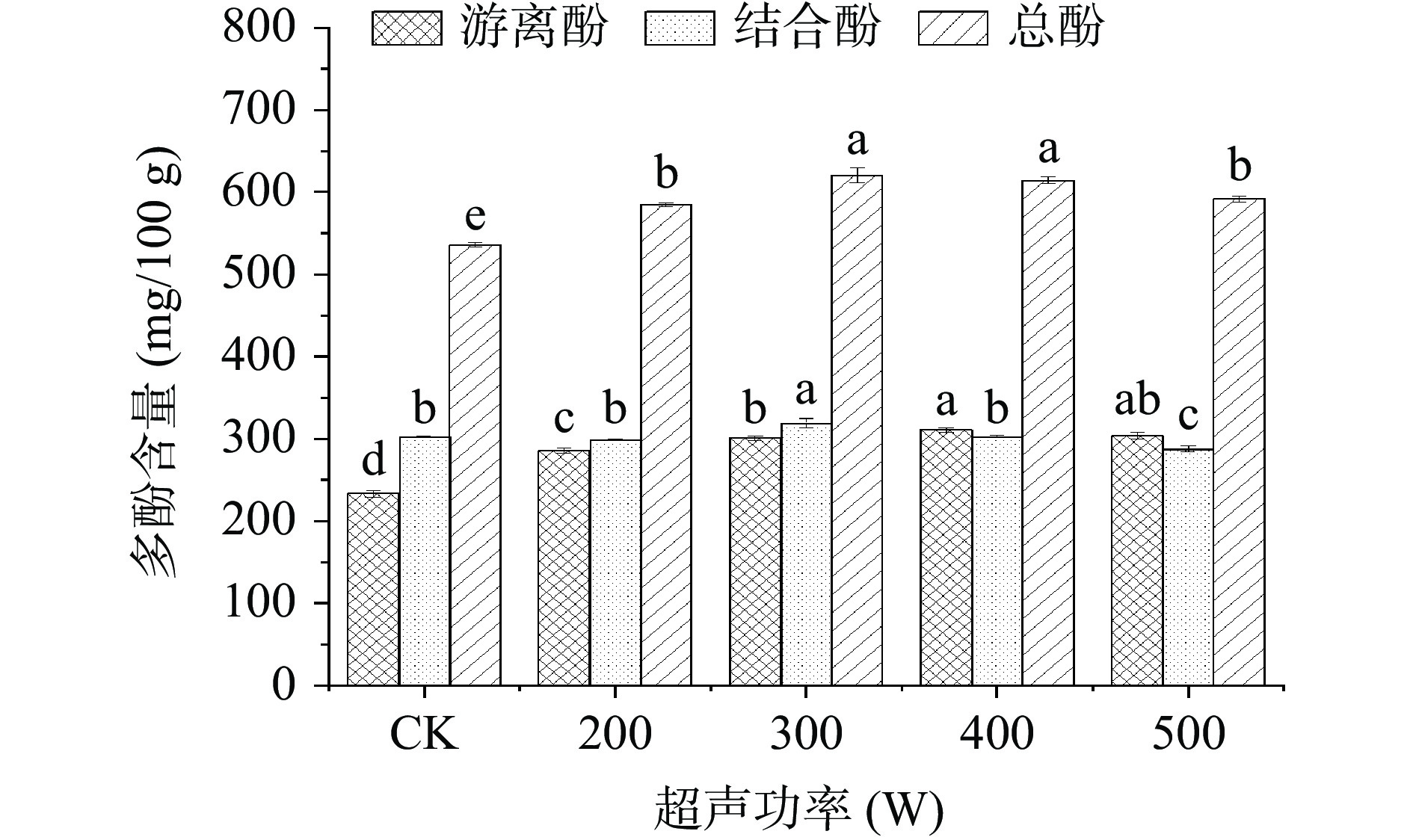
2.1.2 不同超声功率对青稞中多酚含量的影响
不同超声功率对青稞中多酚含量的影响见图2,CK为未处理黑青稞。由图2可知,不同功率超声处理后的黑青稞中多酚含量存在差异,且游离酚、结合酚及总酚含量随着超声波功率的增加均呈现先增加后略有下降的趋势。当超声波功率为300 W时结合酚含量、总酚含量最高,分别达到319.48±5.73和620.34±8.82 mg/100 g,与对照组相比提高了5.56%、15.77%。而超声波功率为400 W时游离酚含量最高(310.87±2.97 mg/100 g),与对照组相比提高了33.31%。这可能是由于超声波引发的空化及化学效应破坏了黑青稞的细胞结构,使得其细胞内容物释放[23],促进了游离酚、结合酚及总酚含量的提高。由图2可知,随着超声波功率的增加,当超声波功率为500 W时,结合酚及总酚含量显著降低(P<0.05),可能是过高的超声波功率引发了酚类物质的降解[24],且实验过程中发现500 W的超声波处理对黑青稞的萌发具有不利影响,其芽长及发芽率均低于300、400 W处理组。结果表明高功率的超声波处理不利于黑青稞总酚的富集。因此,选择300、350、400 W作为后续响应面试验的超声波功率优化水平。
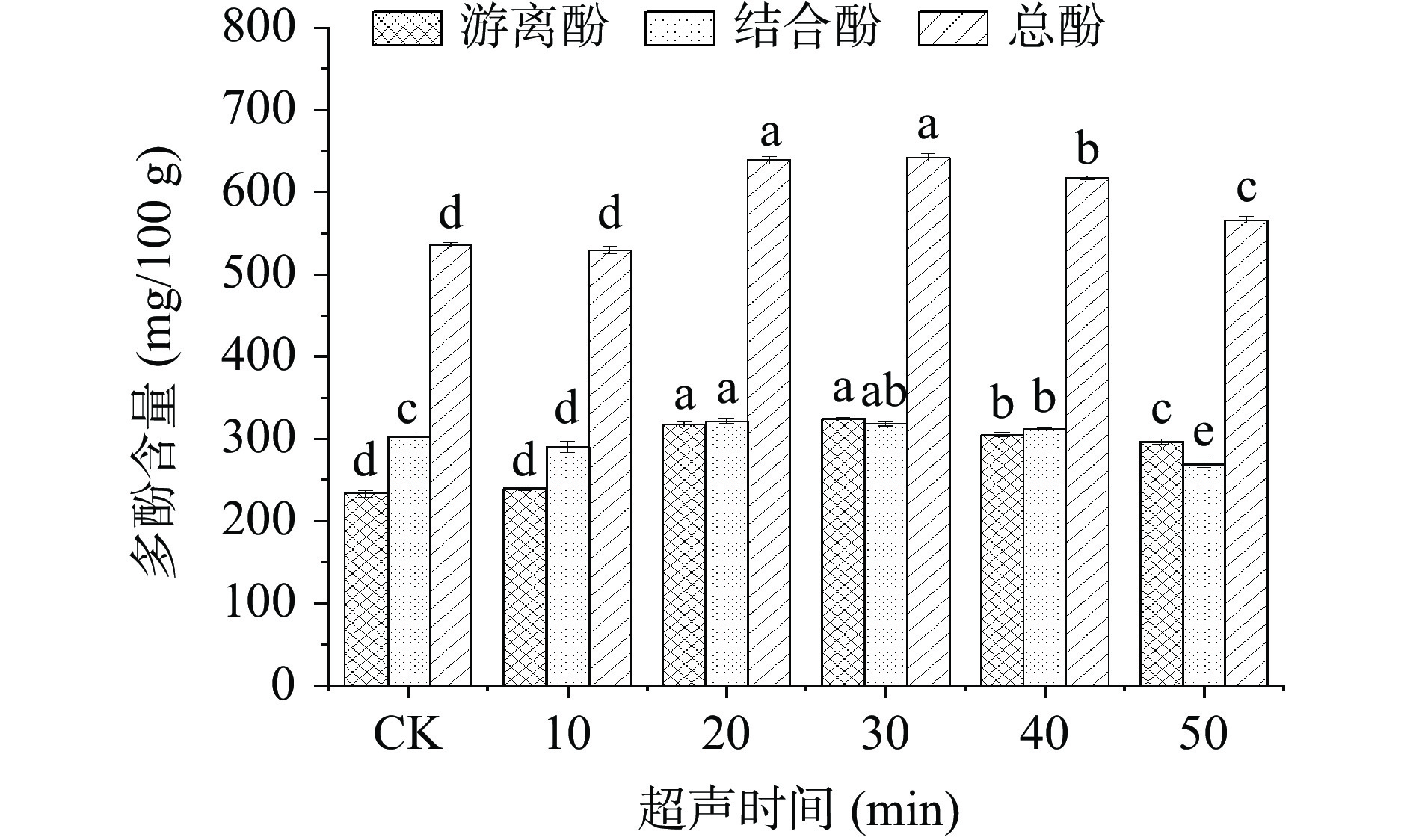
2.1.3 不同超声时间对青稞中多酚含量的影响
不同超声时间对青稞中多酚含量的影响见图3,CK为未处理黑青稞。由图3可知,与对照组相比,当超声波预处理时间为10 min时,萌发青稞中游离酚与总酚含量无显著性变化而结合酚含量明显降低,这与Fonteles等[25]的研究结果类似,可能是因为预处理时间过短暂未对种子内部多酚代谢途径产生明显的影响,其引发的空穴效应反而使水分子产生羟基自由基与多酚反应从而消耗掉部分酚类物质[26]。此后随着超声波处理时间的延长,游离酚、结合酚及总酚含量均呈现先增加后降低的趋势。其中当超声时间为20 min时结合酚含量最高(321.87±2.78 mg/100 g),与对照组相比提高了6.35%,而超声时间为30 min时游离酚、总酚含量达到最高,分别为323.65±2.38、641.74±4.38 mg/100 g,与对照组相比分别提高了38.79%、19.76%,且与超声20 min无显著差异(P>0.05)。可以看出超声处理对游离酚的提高率显著高于结合酚,这可能是由于随着超声时间的延长,结合酚与多糖等大分子连接的化学键逐渐断裂,使结合态酚类化合物发生变化产生了大量的游离态酚类化合物[27]。当超声时间高于30 min,游离酚、结合酚及总酚含量均显著降低(P<0.05),可能是过长时间的超声波处理会破坏酚类化合物的结构[28],部分酚类物质发生分解使其含量降低。因此,在富集多酚的响应面试验中选择了20~30 min的超声波时间范围。
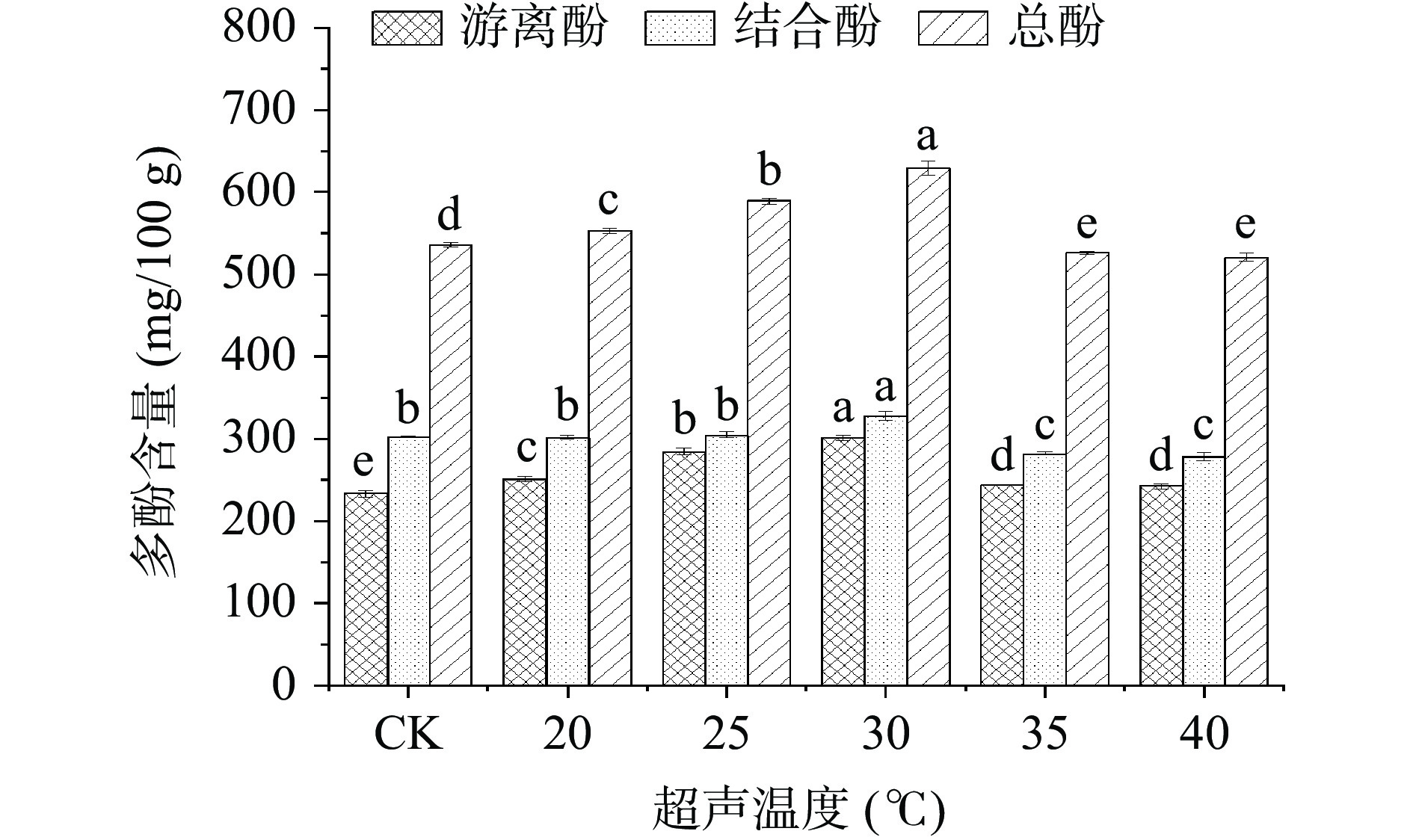
2.1.4 不同超声温度对青稞中多酚含量的影响
超声温度是富集青稞多酚含量的主要影响因素之一。一般情况下,超声温度的增加与酚类化合物的基质键断裂、溶解度增加密切相关[29]。不同超声温度对青稞中多酚含量的影响见图4,CK为未处理黑青稞。由图4可知,不同超声温度处理对游离酚、总酚的含量具有显著性影响,且在20~35 ℃范围内随温度的升高呈先升高后降低的变化趋势。其中,当超声温度为30 ℃时,游离酚及总酚含量达到最高,分别为300.86±3.27和629.26±8.82 mg/100 g,与对照组相比分别提高了29.02%、17.43%。这可能是因为适当的温度下,酚类化合物的溶解度有所提高[30],且形成空化核的数量也增加[31],有利于酚类物质的提取,使得酚类物质含量显著增加。当超声温度为35 ℃时,酚类物质含量显著降低,这主要是由于温度升高时空化强度降低[32-33],另外高温也会导致一些热敏性酚类物质发生降解[34],使得酚类物质含量显著降低。因此最终确定30 ℃为超声波协同萌发处理富集黑青稞多酚的最佳超声温度。
2.2 响应面试验结果
在单因素实验结果的基础上,采用Box-Behnken响应面试验设计,以总酚含量为考察响应值,选择萌发时间(A)、超声功率(B)和超声时间(C)为自变量,对超声协同萌发青稞中多酚的富集工艺进行优化,结果分析见表2、表3。
表 2 Box-Behnken试验设计及结果Table 2. Box-Behnken experimental design and results实验号 A B C 总酚含量
(mg/100 g DW)1 −1 −1 0 581.66±3.69 2 1 −1 0 600.74±3.30 3 −1 1 0 581.23±1.17 4 1 1 0 629.25±3.36 5 −1 0 −1 598.94±0.97 6 1 0 −1 649.46±4.20 7 −1 0 1 574.25±4.87 8 1 0 1 645.70±4.02 9 0 −1 −1 593.19±2.33 10 0 1 −1 630.20±3.52 11 0 −1 1 591.37±7.78 12 0 1 1 601.80±4.56 13 0 0 0 684.17±6.11 14 0 0 0 687.60±2.09 15 0 0 0 668.43±8.78 16 0 0 0 679.51±3.37 17 0 0 0 686.39±9.54 表 3 回归模型方差分析Table 3. Variance analysis of regression model变异来源 平方和 自由度 均方 F值 P值 显著性 模型 26566.24 9 2951.80 31.01 <0.0001 ** A 4468.43 1 4468.43 46.95 0.0002 ** B 712.91 1 712.91 7.49 0.0290 ** C 430.27 1 430.27 4.52 0.0711 AB 209.38 1 209.38 2.20 0.1816 AC 109.52 1 109.52 1.15 0.3190 BC 176.62 1 176.62 1.86 0.2153 A2 5165.63 1 5165.63 54.28 0.0002 ** B2 9690.45 1 9690.45 101.82 <0.0001 ** C2 3567.05 1 3567.05 37.48 0.0005 ** 残差 666.23 7 95.18 失拟项 423.58 3 141.19 2.33 0.2161 误差 242.64 4 60.66 总变异 27232.46 16 R2=0.9755 R2Adj=0.9441 CV=1.55% 注:*P<0.05,表示差异显著;**P<0.01,表示差异极显著。 利用Design Expert 10.0.1软件进行二次多元回归拟合,得到总酚含量对自变量A、B和C的二次多项回归拟合方程为:多酚含量(mg/100 g DW)=681.22+23.63A+9.44B−7.33C+7.23AB+5.23AC−6.65BC−35.03A2−47.97B2−29.11C2
由表3回归模型的方差分析可知,本次试验的拟合模型是极显著的(P<0.0001),失拟项不显著(P=0.2161>0.05),说明模型拟合较好,可以用该回归方程代替试验真实点对试验结果进行分析。决定系数R2=0.9755,调整决定系数R2Adj=0.9441,表示预测值与实际值有较好的拟合度,该模型能够良好的反映出变量与响应值之间的变化关系;变异系数值较低(CV=1.55%),表示测量值具有很高的精确度和可靠性。因此,该模型可用于分析和预测超声协同萌发富集青稞多酚的最优工艺参数。由表3回归模型系数显著性检验结果可知,一次项A、B影响极显著(P<0.01),C影响不显著(P>0.05),且各因素对总酚含量的影响程度依次为:A>B>C,即萌发时间>超声功率>超声时间。二次项A2、B2、C2对总酚含量影响极显著(P<0.01),而交互项AB、AC、BC对总酚含量影响不显著。
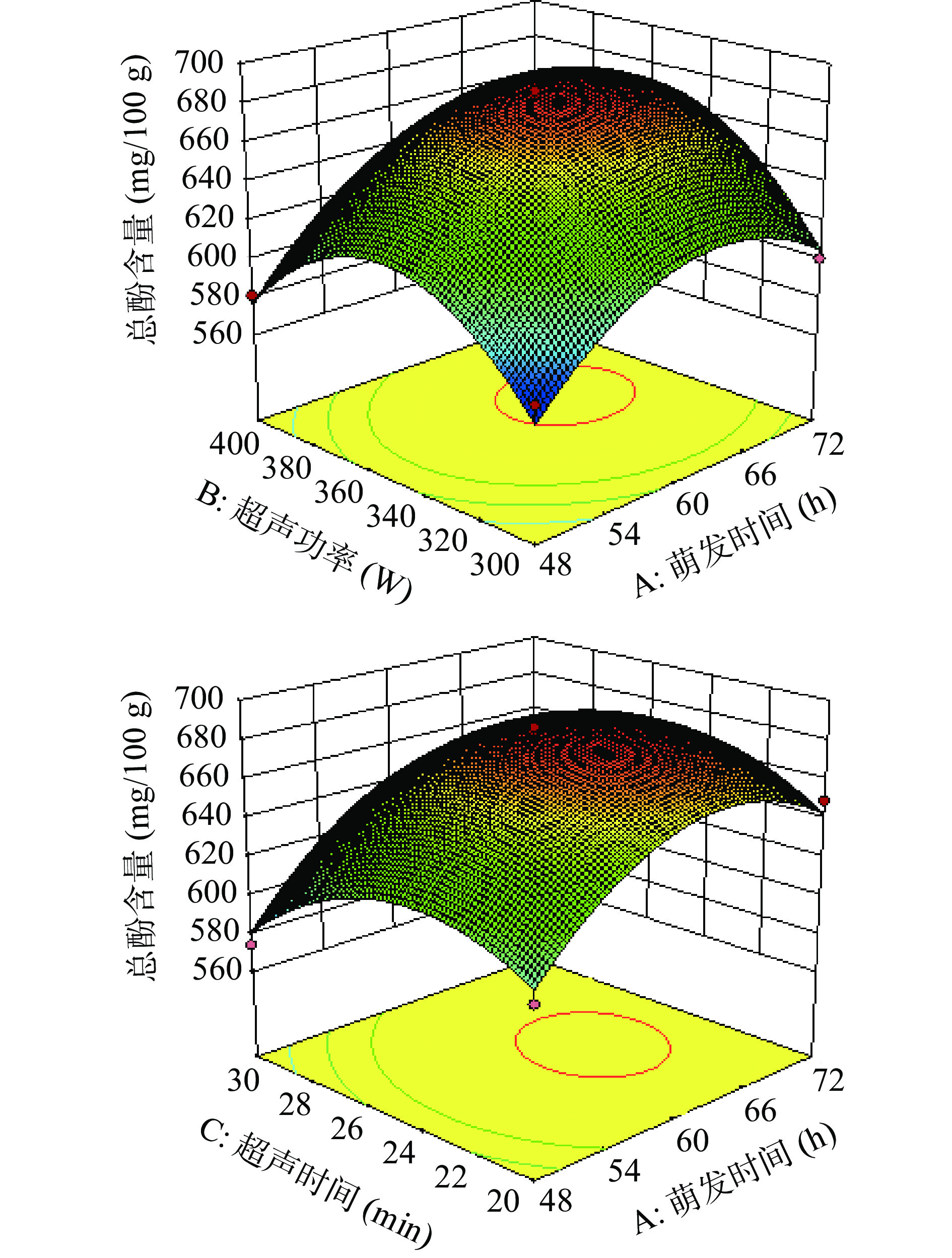
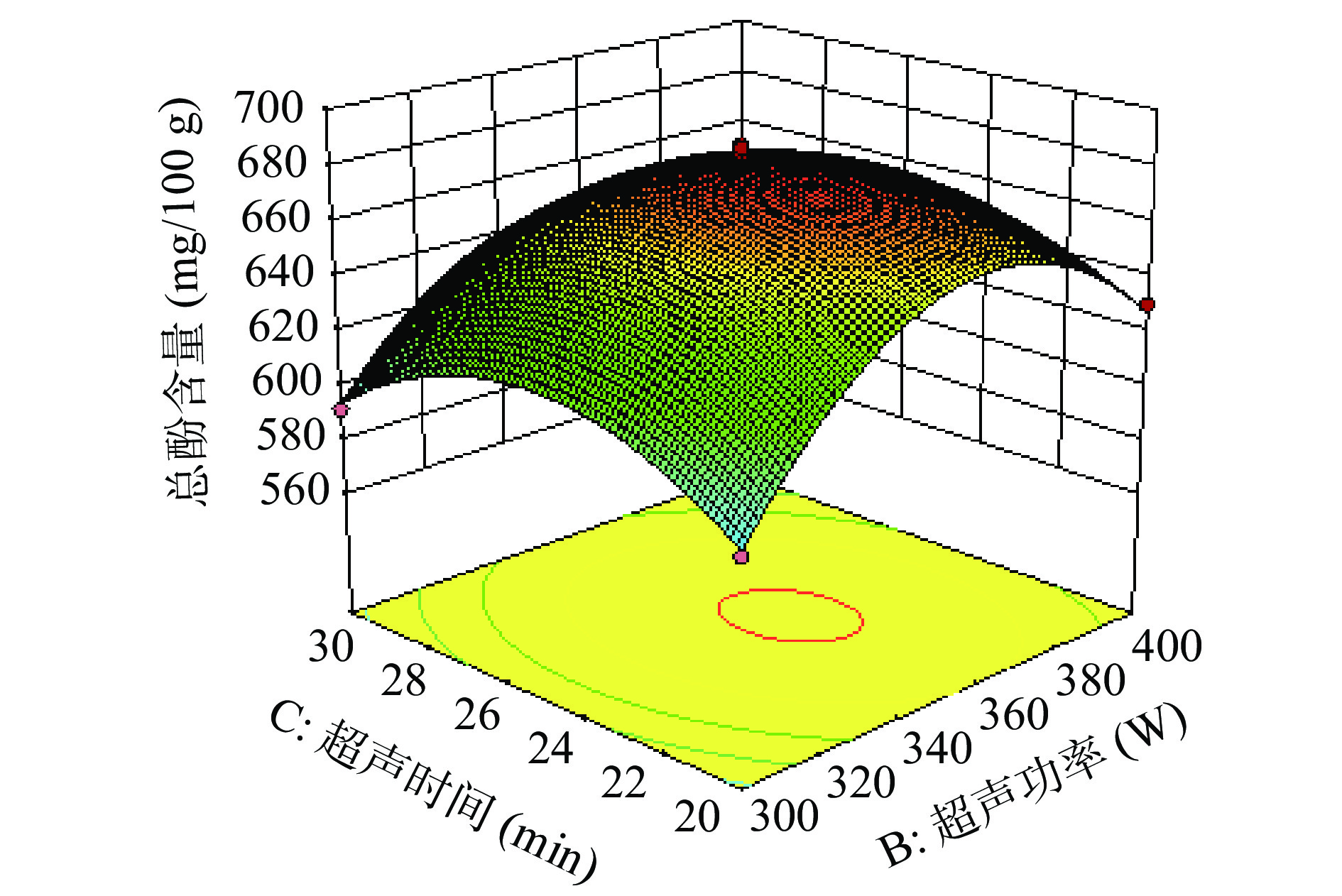
根据回归方程得出不同因素的响应面分析图及等高线图结果见图5。由图5可以看出,交互作用的等高线均呈圆形,可知两者交互作用不显著,与方差分析结果相符。根据二次多项回归拟合方程由响应面软件预测的最优工艺为:超声功率356.57 W、超声时间25.45 min、萌发时间64.11 h,在该条件下萌发青稞中的总酚含量应为686.30 mg/100 g。为了考察预测结果的可靠性,应在最优工艺条件下进行验证实验,但考虑到仪器功能的限制及操作简便,故调整黑青稞富集多酚的最优工艺参数为:超声功率350 W、超声时间25 min、萌发时间64 h。在此条件下进行3次平行试验,得到黑青稞中总酚平均含量为688.84±5.30 mg/100 g,与模型的预测值接近,表明所得的模型具有一定的实验指导意义。
2.3 不同萌发处理方式对黑青稞中酚酸类物质组成的影响
采用UHPLC-MS/MS分别测定了未处理黑青稞、超声协同萌发最优工艺处理后黑青稞以及28 ℃下正常萌发64 h后黑青稞中酚酸类物质的组成及含量的变化(见表4)。由表4可知,与未处理相比,经萌发处理后黑青稞的游离酚酸含量(173.65±2.80 mg/100 g)、总酚酸总量(377.28±2.36 mg/100 g)均显著增加,分别提高了173.27%、26.25%,而结合酚酸含量降低了13.45%。而经超声波协同萌发处理后的黑青稞游离酚酸含量(98.99±0.99 mg/100 g)、结合酚酸总量(281.72±3.33 mg/100 g)、总酚酸总量(380.71±4.21 mg/100 g)均显著高于未处理组,分别增加了55.78%、20.14%和27.40%(P<0.05)。结果显示萌发处理及超声波协同萌发处理均能有效提高游离型酚酸含量,其中萌发处理对其提高更为显著,而针对结合酚酸的研究结果显示仅有超声波协同萌发处理其含量显著提高,这可能因为超声波处理对青稞种子细胞壁的破坏较为剧烈,由于种子自身的抗逆性,细胞不断增殖而产生新的细胞壁,而游离态酚类物质从细胞内部运输到细胞壁与纤维素等大分子结合产生新的结合酚[35]。
表 4 萌发前后黑青稞中酚酸类物质组成及含量(mg/100 g DW)Table 4. Composition and content of phenolic acids in black highland barley before and after germination (mg/100 g DW)酚酸类物质名称 未处理 超声波-萌发 正常萌发
没食子酸游离型 1.13±0.08a 0.96±0.19a 1.27±0.19a 结合型 2.01±0.16b 1.39±0.19c 2.86±0.24a 总酚类物质 3.14±0.19b 2.35±0.30c 4.13±0.38a
尿黑酸游离型 3.16±0.10c 4.42±0.15a 4.11±0.18b 结合型 0.39±0.20b 15.26±0.49a 0.58±0.49b 总酚类物质 3.55±0.29c 19.68±0.60a 4.68±0.65b
原儿茶酸游离型 2.40±0.06b 1.46±0.21b 34.83±1.49a 结合型 5.52±0.09b 5.86±0.07b 8.49±0.48a 总酚类物质 7.92±0.10b 7.32±0.18b 43.31±1.01a
对羟基苯甲酸游离型 2.87±0.14c 8.35±0.19b 13.61±0.15a 结合型 1.29±0.55a 1.04±0.10a 1.28±0.21a 总酚类物质 4.17±0.64c 9.39±0.19b 14.88±0.30a
绿原酸游离型 0.28±0.03a nd nd 结合型 nd nd nd 总酚类物质 0.28±0.03a nd nd
香草酸游离型 12.51±0.41c 15.30±0.39b 20.87±1.78a 结合型 4.65±0.45a 3.60±0.45b 3.53±0.37b 总酚类物质 17.15±0.26b 18.90±0.31b 24.39±1.83a
邻羟基苯乙酸游离型 0.32±0.11a 0.56±0.13a 0.32±0.13a 结合型 0.28±0.03a 0.11±0.01a 0.23±0.11a 总酚类物质 0.60±0.25a 0.67±0.12a 0.54±0.17a
咖啡酸游离型 3.96±0.06b 5.56±0.33a 5.79±0.10a 结合型 26.62±0.85b 29.10±0.12a 24.38±0.20c 总酚类物质 30.58±0.91b 34.67±0.39a 30.17±0.23b
丁香酸游离型 1.68±0.12c 4.38±0.48b 6.25±0.23a 结合型 1.95±0.48a 1.41±0.37a 1.23±0.06a 总酚类物质 3.63±0.50c 5.79±0.20b 7.48±0.25a
对香豆酸游离型 5.76±0.39c 40.56±0.70b 66.16±0.36a 结合型 8.55±0.22c 13.71±0.37a 12.64±0.41b 总酚类物质 14.31±0.25c 54.28±0.71b 78.80±0.58a
阿魏酸游离型 20.46±0.34a 10.17±0.78c 12.56±0.06b 结合型 179.21±5.56b 202.69±1.85a 141.58±1.97c 总酚类物质 199.67±5.25b 212.86±2.05a 154.13±1.97c
藜芦酸游离型 0.49±0.21b 0.99±0.05a 0.70±0.24ab 结合型 0.21±0.08b 0.56±0.31b 1.28±0.49a 总酚类物质 0.70±0.25b 1.54±0.35ab 1.98±0.72a
苯甲酸游离型 7.84±1.68a 6.00±0.24ab 5.67±0.04b 结合型 2.14±0.15b 4.94±0.89a 2.84±0.30b 总酚类物质 9.98±1.79a 10.94±1.06a 8.51±0.25a
水杨酸游离型 0.69±0.08b 0.29±0.08c 1.42±0.08a 结合型 0.74±0.19a 0.41±0.03b 0.45±0.05b 总酚类物质 1.43±0.15b 0.71±0.09c 1.88±0.03a
邻香豆酸游离型 nd nd 0.11±0.01a 结合型 1.72±0.09b 1.64±0.14b 2.28±0.23a 总酚类物质 1.72±0.09b 1.64±0.14b 2.40±0.23a
总酚酸游离型 63.54±2.44c 98.99±0.99b 173.65±2.80a 结合型 235.29±6.47b 281.72±3.33a 203.63±0.44c 总酚类物质 298.83±5.75b 380.71±4.21a 377.28±2.36a 注:nd表示未检出,小写字母表示同行不同列差异显著(P<0.05)。 萌发处理及超声波协同萌发处理前后黑青稞的酚酸类物质均主要以结合态形式存在,其中阿魏酸含量均最高,是黑青稞最主要的酚酸类物质,这与Yang等[36]的研究结果一致。原儿茶酸(结合)、香草酸(游离)、咖啡酸(结合)、对香豆酸(游离和结合)、阿魏酸(游离和结合)及苯甲酸(游离)为处理前后黑青稞中主要的酚酸类物质,而对羟基苯甲酸(游离)、咖啡酸(游离)为萌发处理及超声波协同萌发处理共有的主要酚酸物质。此外,原儿茶酸(游离)与丁香酸(游离)为萌发处理后的主要酚酸物质,尿黑酸(结合)为超声波协同萌发处理的主要酚酸类物质。
与未处理组相比,经萌发处理后其主要酚酸类物质单体中以游离态形式存在的原儿茶酸、对羟基苯甲酸、香草酸、咖啡酸、丁香酸、对香豆酸增加显著,分别提高为未处理组的14.49、4.73、1.67、1.46、3.73、11.49倍;以结合态形式存在的主要酚酸类物质单体中原儿茶酸、对香豆酸增加显著,为未处理组的1.54、1.48倍。而经超声波协同萌发处理后的黑青稞中主要酚酸类物质单体中以游离态形式存在的对羟基苯甲酸、香草酸、咖啡酸、对香豆酸含量增加明显,分别提高为未处理组的2.91、1.22、1.41、7.05倍;而以结合态形式存在的主要酚酸类物质单体中尿黑酸、咖啡酸、对香豆酸、阿魏酸分别提高为未处理组的39.24、1.09、1.60和1.13倍。结果显示,萌发处理显著提高了主要酚酸物质中原儿茶酸(游离和结合)、对羟基苯甲酸(游离)、香草酸(游离)、咖啡酸(游离)、丁香酸(游离)、对香豆酸(游离)的含量。而超声波协同萌发处理显著提高了主要酚酸物质中尿黑酸(结合)、咖啡酸(结合)、对香豆酸(结合)、阿魏酸(结合)的含量。
此外超声协同萌发后阿魏酸(游离)、苯甲酸(游离)含量均低于未处理黑青稞;经萌发处理后咖啡酸(结合)、阿魏酸(游离和结合)、苯甲酸(游离)含量也降低;且绿原酸在萌发及超声协同萌发处理后均未检出,可能是因为一些酚类物质单体在萌发期间发生了氧化降解,另外,还与酚类化合物之间存在相互作用或发生络合反应有关[37]。
综合而言,萌发及超声波协同萌发处理均能够显著提高黑青稞的总酚酸含量,这与糙米萌发后酚酸含量的增加趋势一致[38]。超声协同萌发能够明显提高黑青稞中结合酚酸的含量,而萌发处理能够明显提高黑青稞中游离酚酸的含量,该结果可为富含多酚的产品研发提供理论依据。
2.4 萌发前后黑青稞中总酚含量及体外抗氧化能力的变化
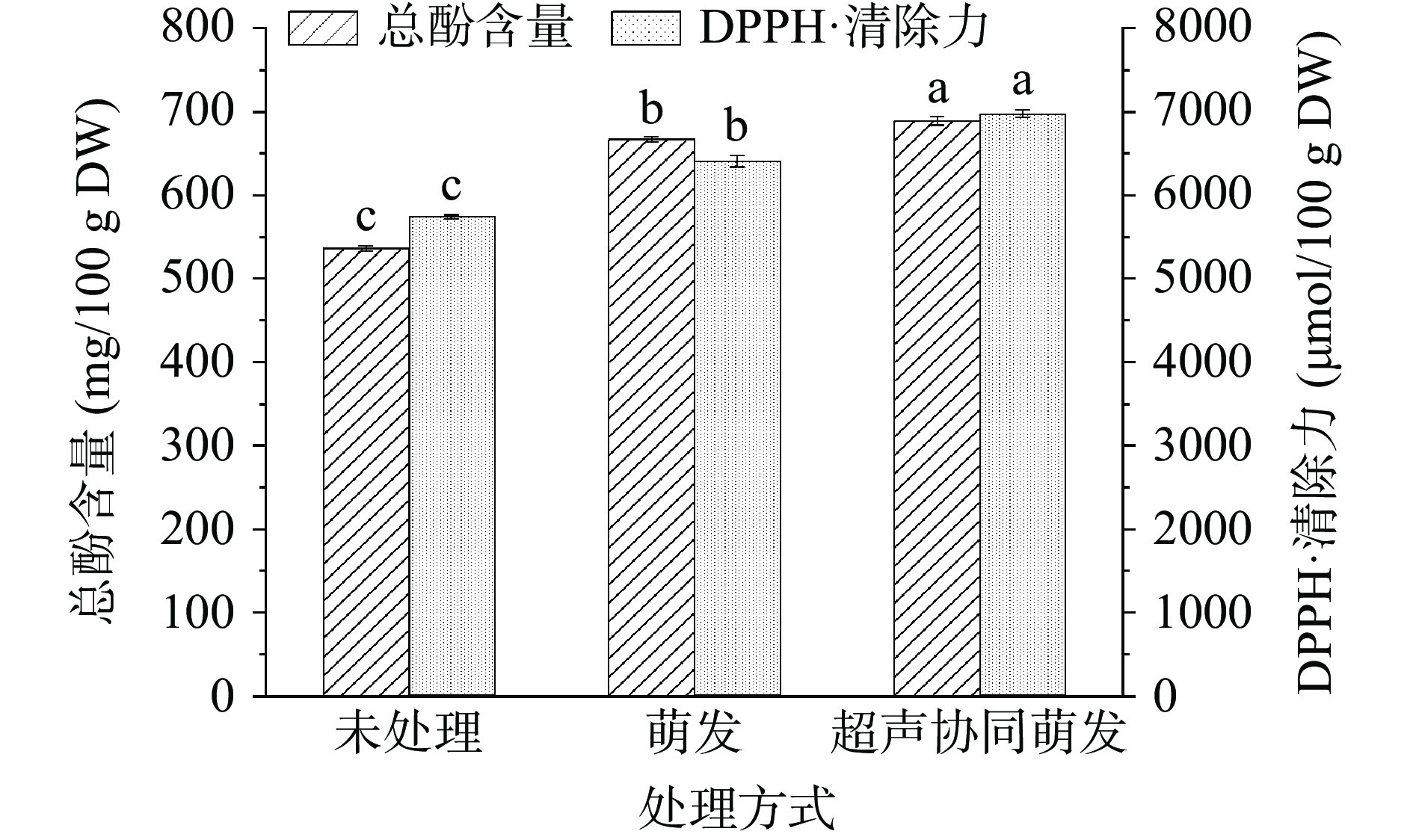
根据最优工艺的结果制备黑青稞萌发样品,比较未处理黑青稞、超声波协同萌发处理后黑青稞以及相同萌发时间、温度条件下正常萌发黑青稞中的总酚含量以及体外抗氧化活性的差异,结果见图6。由图6可知,经萌发处理及超声波协同萌发处理后黑青稞的总酚含量显著增加(分别为669.32±8.11、688.84±5.30 mg/100 g),与未处理组相比其含量分别提高了24.91%和28.55%,这与Wang等[39]的研究结果一致,说明超声波协同萌发处理能够显著提高谷物中酚类物质的含量。此外,经萌发及超声波协同萌发处理后黑青稞的DPPH·清除能力均显著提高(P<0.05),且超声波协同萌发处理组的DPPH·清除能力显著高于萌发处理组(P<0.05)。与对照组相比,萌发后DPPH·清除能力提高了11.66%,而超声协同萌发处理组提高了21.55%。这与Tang等[40]的研究结果类似,说明超声波协同萌发能够显著提高黑青稞的体外抗氧化能力。综合而言,超声波协同萌发在提高谷物酚类物质含量及抗氧化活性方面具有一定的优越性。
3. 结论
本研究采用单因素和Box-Behnken响应曲面法优化超声协同萌发富集黑青稞多酚的工艺参数,得到了最优工艺为:超声温度30 ℃、超声功率350 W、超声时间25 min、萌发时间64 h时,在此条件下黑青稞中总酚含量达到688.84±5.30 mg/100 g,与对照组相比,提高了28.55%。经UHPLC-MS/MS检测分析,萌发处理能够显著提高黑青稞中游离酚酸的含量,而超声协同萌发能够显著提高黑青稞中结合酚酸的含量,其中萌发处理显著提高了主要酚酸物质中原儿茶酸(游离和结合)、对羟基苯甲酸(游离)、香草酸(游离)、咖啡酸(游离)、丁香酸(游离)、对香豆酸(游离)的含量(P<0.05)。而超声波协同萌发处理显著提高了主要酚酸物质中尿黑酸(结合)、咖啡酸(结合)、对香豆酸(结合)、阿魏酸(结合)的含量(P<0.05)。此外,与对照组相比,萌发处理及超声波协同萌发处理的黑青稞其DPPH·清除能力均显著增加,分别提高了11.66%、21.55%(P<0.05)。综合而言,超声协同萌发处理能够提高黑青稞的酚类物质及抗氧化活性,该研究可为进一步提高黑青稞的利用价值提供参考。
-
表 1 响应面试验因素与水平
Table 1 Response surface test factors and levels
水平 A 萌发时间(d) B 超声功率(W) C 超声时间(min) −1 48 300 20 0 60 350 25 1 72 400 30 表 2 Box-Behnken试验设计及结果
Table 2 Box-Behnken experimental design and results
实验号 A B C 总酚含量
(mg/100 g DW)1 −1 −1 0 581.66±3.69 2 1 −1 0 600.74±3.30 3 −1 1 0 581.23±1.17 4 1 1 0 629.25±3.36 5 −1 0 −1 598.94±0.97 6 1 0 −1 649.46±4.20 7 −1 0 1 574.25±4.87 8 1 0 1 645.70±4.02 9 0 −1 −1 593.19±2.33 10 0 1 −1 630.20±3.52 11 0 −1 1 591.37±7.78 12 0 1 1 601.80±4.56 13 0 0 0 684.17±6.11 14 0 0 0 687.60±2.09 15 0 0 0 668.43±8.78 16 0 0 0 679.51±3.37 17 0 0 0 686.39±9.54 表 3 回归模型方差分析
Table 3 Variance analysis of regression model
变异来源 平方和 自由度 均方 F值 P值 显著性 模型 26566.24 9 2951.80 31.01 <0.0001 ** A 4468.43 1 4468.43 46.95 0.0002 ** B 712.91 1 712.91 7.49 0.0290 ** C 430.27 1 430.27 4.52 0.0711 AB 209.38 1 209.38 2.20 0.1816 AC 109.52 1 109.52 1.15 0.3190 BC 176.62 1 176.62 1.86 0.2153 A2 5165.63 1 5165.63 54.28 0.0002 ** B2 9690.45 1 9690.45 101.82 <0.0001 ** C2 3567.05 1 3567.05 37.48 0.0005 ** 残差 666.23 7 95.18 失拟项 423.58 3 141.19 2.33 0.2161 误差 242.64 4 60.66 总变异 27232.46 16 R2=0.9755 R2Adj=0.9441 CV=1.55% 注:*P<0.05,表示差异显著;**P<0.01,表示差异极显著。 表 4 萌发前后黑青稞中酚酸类物质组成及含量(mg/100 g DW)
Table 4 Composition and content of phenolic acids in black highland barley before and after germination (mg/100 g DW)
酚酸类物质名称 未处理 超声波-萌发 正常萌发
没食子酸游离型 1.13±0.08a 0.96±0.19a 1.27±0.19a 结合型 2.01±0.16b 1.39±0.19c 2.86±0.24a 总酚类物质 3.14±0.19b 2.35±0.30c 4.13±0.38a
尿黑酸游离型 3.16±0.10c 4.42±0.15a 4.11±0.18b 结合型 0.39±0.20b 15.26±0.49a 0.58±0.49b 总酚类物质 3.55±0.29c 19.68±0.60a 4.68±0.65b
原儿茶酸游离型 2.40±0.06b 1.46±0.21b 34.83±1.49a 结合型 5.52±0.09b 5.86±0.07b 8.49±0.48a 总酚类物质 7.92±0.10b 7.32±0.18b 43.31±1.01a
对羟基苯甲酸游离型 2.87±0.14c 8.35±0.19b 13.61±0.15a 结合型 1.29±0.55a 1.04±0.10a 1.28±0.21a 总酚类物质 4.17±0.64c 9.39±0.19b 14.88±0.30a
绿原酸游离型 0.28±0.03a nd nd 结合型 nd nd nd 总酚类物质 0.28±0.03a nd nd
香草酸游离型 12.51±0.41c 15.30±0.39b 20.87±1.78a 结合型 4.65±0.45a 3.60±0.45b 3.53±0.37b 总酚类物质 17.15±0.26b 18.90±0.31b 24.39±1.83a
邻羟基苯乙酸游离型 0.32±0.11a 0.56±0.13a 0.32±0.13a 结合型 0.28±0.03a 0.11±0.01a 0.23±0.11a 总酚类物质 0.60±0.25a 0.67±0.12a 0.54±0.17a
咖啡酸游离型 3.96±0.06b 5.56±0.33a 5.79±0.10a 结合型 26.62±0.85b 29.10±0.12a 24.38±0.20c 总酚类物质 30.58±0.91b 34.67±0.39a 30.17±0.23b
丁香酸游离型 1.68±0.12c 4.38±0.48b 6.25±0.23a 结合型 1.95±0.48a 1.41±0.37a 1.23±0.06a 总酚类物质 3.63±0.50c 5.79±0.20b 7.48±0.25a
对香豆酸游离型 5.76±0.39c 40.56±0.70b 66.16±0.36a 结合型 8.55±0.22c 13.71±0.37a 12.64±0.41b 总酚类物质 14.31±0.25c 54.28±0.71b 78.80±0.58a
阿魏酸游离型 20.46±0.34a 10.17±0.78c 12.56±0.06b 结合型 179.21±5.56b 202.69±1.85a 141.58±1.97c 总酚类物质 199.67±5.25b 212.86±2.05a 154.13±1.97c
藜芦酸游离型 0.49±0.21b 0.99±0.05a 0.70±0.24ab 结合型 0.21±0.08b 0.56±0.31b 1.28±0.49a 总酚类物质 0.70±0.25b 1.54±0.35ab 1.98±0.72a
苯甲酸游离型 7.84±1.68a 6.00±0.24ab 5.67±0.04b 结合型 2.14±0.15b 4.94±0.89a 2.84±0.30b 总酚类物质 9.98±1.79a 10.94±1.06a 8.51±0.25a
水杨酸游离型 0.69±0.08b 0.29±0.08c 1.42±0.08a 结合型 0.74±0.19a 0.41±0.03b 0.45±0.05b 总酚类物质 1.43±0.15b 0.71±0.09c 1.88±0.03a
邻香豆酸游离型 nd nd 0.11±0.01a 结合型 1.72±0.09b 1.64±0.14b 2.28±0.23a 总酚类物质 1.72±0.09b 1.64±0.14b 2.40±0.23a
总酚酸游离型 63.54±2.44c 98.99±0.99b 173.65±2.80a 结合型 235.29±6.47b 281.72±3.33a 203.63±0.44c 总酚类物质 298.83±5.75b 380.71±4.21a 377.28±2.36a 注:nd表示未检出,小写字母表示同行不同列差异显著(P<0.05)。 -
[1] 周红, 张杰, 张文刚, 等. 青海黑青稞营养及活性成分分析与评价[J]. 核农学报,2021,35(7):1609−1618. [ZHOU H, ZHANG J, ZHANG W G, et al. Analysis and evaluation of nutrition and active components of Qinghai black highland barley[J]. Journal of Nuclear Agriculture,2021,35(7):1609−1618. ZHOU H, ZHANG J, ZHANG W G, et al. Analysis and evaluation of nutrition and active components of Qinghai black highland barley[J]. Journal of Nuclear Agriculture, 2021, 35(7): 1609-1618.
[2] 杨希娟, 党斌, 徐菲, 等. 不同粒色青稞酚类化合物含量与抗氧化活性的差异及评价[J]. 中国粮油学报,2017,32(9):34−42. [YANG X J, DANG B, XU F, et al. Difference and evaluation of phenolic compounds content and antioxidant activity of different grain-colored highland barley[J]. Journal of China Cereals and Oils,2017,32(9):34−42. doi: 10.3969/j.issn.1003-0174.2017.09.006 YANG X J, DANG B, XU F, et al. Difference and evaluation of phenolic compounds content and antioxidant activity of different grain-colored highland barley[J]. Journal of China Cereals and Oils, 2017, 32(9): 34-42. doi: 10.3969/j.issn.1003-0174.2017.09.006
[3] LI J X, ZHANG H, YANG X J, et al. Trapping of reactive carbonyl species by fiber-bound polyphenols from whole grains under simulated physiological conditions[J]. Food Research International,2022,156:111142. doi: 10.1016/j.foodres.2022.111142
[4] DING J Z, HOU G, NEMZER B V, et al. Effects of controlled germination on selected physicochemical and functional properties of whole-wheat flour and enhanced γ-aminobutyric acid accumulation by ultrasonication[J]. Food Chemistry,2018,243:214−221. doi: 10.1016/j.foodchem.2017.09.128
[5] WU F, YANG N, TOURE, et al. Germinated brown rice and its role in human health[J]. Critical Reviews in Food Science and Nutrition,2013,53(5):451−463. doi: 10.1080/10408398.2010.542259
[6] KHANG D T, DUNG T N, ELAZAAWELY A A, et al. Phenolic profiles and antioxidant activity of germinated legumes[J]. Foods,2016,5(2):27.
[7] GONG L, WEN T, WANG J. Role of the microbiome in mediating health effects of dietary components[J]. Journal of Agricultural and Food Chemistry,2020,68(46):12820−12835. doi: 10.1021/acs.jafc.9b08231
[8] HO J N, SON M E, LIM W C, et al. Anti-obesity effects of germinated brown rice extract through down-regulation of lipogenic genes in high fat diet-induced obese mice[J]. Journal of the Agricultural Chemical Society of Japan,2012,76(6):1068−1074.
[9] HSU T F, KISE M, WANG M F, et al. Effects of pre- germinated brown rice on blood glucose and lipid levels in free- living patients with impaired fasting glucose or type 2 diabetes[J]. Journal of Nutritional Science and Vitaminology,2018,54(2):163−168.
[10] YAO F, ZHANG J Y, XIAO X, et al. Antitumor activities and apoptosis- regulated mechanisms of fermented barley extract in the transplantation tumor model of human HT-29 cells in nude mice[J]. Biomedical and Environmental Sciences,2017,30(1):10−21.
[11] 卞紫秀, 汪建飞, 王顺民. 超声波处理下苦荞麦萌发及富集黄酮工艺优化研究[J]. 安徽工程大学学报,2018,33(5):7−13. [BIAN Z X, WANG J F, WANG S M. Study on optimization of germination and flavonoids enrichment process of tartary buckwheat under ultrasonic treatment[J]. Journal of Anhui Engineering University,2018,33(5):7−13. doi: 10.3969/j.issn.2095-0977.2018.05.002 BIAN Z X, WANG J F, WANG S M. Study on optimization of germination and flavonoids enrichment process of tartary buckwheat under ultrasonic treatment[J]. Journal of Anhui Engineering University, 2018, 33(5): 7-13. doi: 10.3969/j.issn.2095-0977.2018.05.002
[12] 雷月, 宫彦龙, 邓茹月, 等. 超声波辅助喷雾加湿法富集发芽黑糙米生物活性物质工艺的响应面优化[J]. 食品工业科技,2020,41(4):105−113. [LEI Y, GONG Y L, DENG R Y, et al. Optimization of ultrasonic-assisted spray and wet enrichment of bioactive substances from germinated black brown rice by response surface methodology[J]. Science and Technology of Food Industry,2020,41(4):105−113. LEI Y, GONG Y L, DENG R Y, et al. Optimization of ultrasonic-assisted spray and wet enrichment of bioactive substances from germinated black brown rice by response surface methodology[J]. Science and Technology of Food Industry, 2020, 41(4): 105-113.
[13] DING J Z, JOHNSON J, CHU Y F, et al. Enhancement of γ-aminobutyric acid, avenanthramides, and other health-promoting metabolites in germinating oats (Avena sativa L.) treated with and without power ultrasound[J]. Food Chemistry,2019,283:239−247. doi: 10.1016/j.foodchem.2018.12.136
[14] IGNACIO L R, CARLOS M V. Use of ultrasonication to increase germination rates of arabidopsis seeds[J]. Plant Methods,2017,13(1):1−6. doi: 10.1186/s13007-016-0152-4
[15] DONG J, LIU Y, LIANG Z, et al. Investigation on ultrasound-assisted extraction of salvianolic acid B from Salvia miltiorrhiza root[J]. Ultrasonics Sonochemistry,2010,17(1):61−65. doi: 10.1016/j.ultsonch.2009.05.006
[16] 杨希娟, 党斌, 樊明涛. 溶剂提取对青稞中不同形态多酚组成及抗氧化活性的影响[J]. 食品科学,2018,39(24):239−248. [YANG X J, DANG B, FAN M T. Effect of solvent extraction on polyphenol composition and antioxidant activity of different forms in highland barley[J]. Food Science,2018,39(24):239−248. doi: 10.7506/spkx1002-6630-201824036 YANG X J, DANG B, FAN M T. Effect of solvent extraction on polyphenol composition and antioxidant activity of different forms in highland barley[J]. Food Science, 2018, 39(24): 239-248. doi: 10.7506/spkx1002-6630-201824036
[17] 陈朴, 于燕波, 沈起兵, 等. 超高效液相色谱-串联Orbitrap质谱(Q-Exactive)对湿热质人群代谢表型的分析[J]. 质谱学报,2017,38(5):541−550. [CHEN P, YU Y B, SHEN Q B, et al. Analysis of metabolic phenotype of damp-heat people by ultra-high performance liquid chromatography-tandem Orbitrap mass spectrometry (Q-Exactive)[J]. Acta Mass Spectrometry,2017,38(5):541−550. doi: 10.7538/zpxb.youxian.2016.0062 CHEN P, YU Y B, SHEN Q B, et al. Analysis of metabolic phenotype of damp-heat people by ultra-high performance liquid chromatography-tandem Orbitrap mass spectrometry (Q-Exactive)[J]. Acta Mass Spectrometry, 2017, 38(5): 541-550. doi: 10.7538/zpxb.youxian.2016.0062
[18] 付晓燕, 胡崇琳, 田斌强, 等. 燕麦发芽过程中酚类物质的变化[J]. 食品科学,2011,32(5):137−142. [FU X Y, HU C L, TIAN B Q, et al. Changes of phenolic compounds during oat germination[J]. Food Science,2011,32(5):137−142. FU X Y, HU C L, TIAN B Q, et al. Changes of phenolic compounds during oat germination[J]. Food Science, 2011, 32(5): 137-142.
[19] SKOGLUND M, PETERSON D M, ANDERSSON R, et al. Avenanthramide content and related enzyme activities in oats as affected by steeping and germination[J]. Journal of Cereal Science,2008,48(2):294−303. doi: 10.1016/j.jcs.2007.09.010
[20] HUMBERSTONE F J, BRIGGS D E. Extraction and assay of ferulic acid esterase from malted barley[J]. Journal of the Institute of Brewing,2000,106:21−29. doi: 10.1002/j.2050-0416.2000.tb00036.x
[21] GAN R Y, LUI W Y, WU K, et al. Bioactive compounds and bioactivities of germinated edible seeds and sprouts: An updated review[J]. Trends Food Science and Technology,2017,59:1−14. doi: 10.1016/j.jpgs.2016.11.010
[22] DINI I, TRNORE G C, DINI A, et al. Antioxidant compound contents and antioxidant activity before and after cooking in sweet and bitter Chenopodium quinoa seeds[J]. LWT-Food Science and Technology,2010,43(3):447−451. doi: 10.1016/j.lwt.2009.09.010
[23] KENTISH S, FENG H. Applications of power ultrasound in food processing[J]. Annual Review of Food Science and Technology,2014,5(1):263−284. doi: 10.1146/annurev-food-030212-182537
[24] LOU Z, WANG H, ZHANG M, et al. Improved extraction of oil from chickpea under ultrasound in a dynamic system[J]. Journal of Food Engineering,2010,98(1):13−18. doi: 10.1016/j.jfoodeng.2009.11.015
[25] FONTELES, THATYANE V, MAIA C, et al. Power ultrasound processing of cantaloupe melon juice: Effects on quality parameters[J]. Food Research International,2012,48(1):41−48. doi: 10.1016/j.foodres.2012.02.013
[26] 王涓, 潘忠礼, 马海乐, 等. 超声波的空化作用及其对多酚稳定性的影响[J]. 食品工业科技,2014,35(19):388−391. [WANG J, PAN Z L, MA H L, et al. Cavitation of ultrasonic wave and its influence on polyphenol stability[J]. Science and Technology of Food Industry,2014,35(19):388−391. WANG J, PAN Z L, MA H L, et al. Cavitation of ultrasonic wave and its influence on polyphenol stability[J]. Science and Technology of Food Industry, 2014, 35(19): 388-391.
[27] 王彩霞, 刘富明, 郭静雨, 等. 蓝色小麦游离酚和结合酚的综合提取及红外光谱分析[J]. 中国粮油学报,2020,35(10):189−195. [WANG C X, LIU F M, GUO J Y, et al. Comprehensive extraction and infrared spectrum analysis of free phenol and bound phenol in blue wheat[J]. Chinese Journal of Cereals and Oils,2020,35(10):189−195. WANG C X, LIU F M, GUO J Y, et al. Comprehensive extraction and infrared spectrum analysis of free phenol and bound phenol in blue wheat[J]. Chinese Journal of Cereals and Oils, 2020, 35(10): 189-195.
[28] OREOPOULOU A, TSIMOGIANNIS D, OREOPOULOU V. Extraction of polyphenols from aromatic and medicinal plants: An overview of the methods and the effect of extraction parameters[J]. Polyphenols in Plants, 2019: 243-259.
[29] KATSAMPA P, VALSAMEDOU E, GRIGORAKIS S, et al. A green ultrasound-assisted extraction process for the recovery of antioxidant polyphenols and pigments from onion solid wastes using Box-Behnken experimental design and kinetics[J]. Industrial Crops and Products,2015,77:535−543. doi: 10.1016/j.indcrop.2015.09.039
[30] MOURAD B, NESRIN C, FAIK A, et al. The optimization of ultrasonic-assisted extraction of Centaurea sp. antioxidative phenolic compounds using response surface methodology[J]. Journal of Applied Research on Medicinal and Aromatic Plants,2021,25:100330. doi: 10.1016/j.jarmap.2021.100330
[31] FILGUEIRAS A V, CAPELO J L, LAVILLA I, et al. Comparison of ultrasound-assisted extraction and microwave-assisted digestion for determination of magnesium, manganese and zinc in plant samples by flame atomic absorption spectrometry[J]. Talanta,2000,53(2):433−441. doi: 10.1016/S0039-9140(00)00510-5
[32] EETEZARI M H, KRUUS P. Effect of frequency on sonochemical reactions II. Temperature and intensity effects[J]. Ultrasonics Sonochemistry,1996,3(1):19−24. doi: 10.1016/1350-4177(95)00037-2
[33] RASO J, MANAS P, PAGAN R, et al. Influence of different factors on the output power transferred into medium by ultrasound[J]. Ultrasonics Sonochemistry,1999,5(4):157−162. doi: 10.1016/S1350-4177(98)00042-X
[34] CHEW K, KHOO M, THOO Y, et al. Effect of ethanol concentration, extraction time and extraction temperature on the recovery of phenolic compounds and antioxidant capacity of Orthosiphon stamineus extracts[J]. International Food Research Journal,2011,18(4):1427−1435.
[35] XU L, WANG P, ALI B, et al. Changes of the phenolic compounds and antioxidant activities in germinated adlay seeds[J]. Journal of the Science of Food and Agriculture,2017,97(12):4227−4234. doi: 10.1002/jsfa.8298
[36] YANG X J, DANG B, FAN M T. Free and bound phenolic compound content and antioxidant activity of different cultivated blue highland barley varieties from the Qinghai-Tibet Plateau[J]. Molecules,2018,23(4):879. doi: 10.3390/molecules23040879
[37] GE X, SALEH A S M, JING L, et al. Germination and drying induced changes in the composition and content of phenolic compounds in naked barley[J]. Journal of Food Composition and Analysis,2021,95:103594. doi: 10.1016/j.jfca.2020.103594
[38] DONG H C, SEUNNG T L. Changes in phenolic acid composition and associated enzyme activity in shoot and kernel fractions of brown rice during germination[J]. Food Chemistry,2018,256:163−170. doi: 10.1016/j.foodchem.2018.02.040
[39] WANG J F, BIAN Z X, WANG S, et al. Effects of ultrasonic waves, microwaves, and thermal stress treatment on the germination of tartary buckwheat seeds[J]. Journal of Food Process Engineering,2020,43(10):13494.
[40] TANG Y, XIAO L, WU X, et al. Impact of germination pretreatment on the polyphenol profile, antioxidant activities, and physicochemical properties of three color cultivars of highland barley[J]. Journal of Cereal Science,2021,97:103152. doi: 10.1016/j.jcs.2020.103152
-
期刊类型引用(4)
1. 王芳,马银花,祁存英,熊辉岩,段瑞君. 青稞品质及其环境因子影响研究进展. 食品研究与开发. 2025(02): 217-224 .  百度学术
百度学术
2. 朱镇华,李桂霞,徐晨希,尹慧,罗文,陈实. 醪糟黑青稞面包配方优化研究. 粮食加工. 2024(02): 59-64 .  百度学术
百度学术
3. 张玲,郑万财,兰永丽,张文刚. 藜麦富硒萌发工艺优化及抗氧化活性研究. 食品与机械. 2024(07): 175-182 .  百度学术
百度学术
4. 茹巧美,任国平,王艳. 酸化甘油-超声辅助提取杨梅花青素工艺优化及其抗氧化活性研究. 食品安全质量检测学报. 2024(13): 124-132 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:
 下载:
下载:



