Effects of Combined Treatments of Bacteria and Enzyme on the Degradation and Flavor Components of Body Wall of Sea Cucumber
-
摘要: 目的:为探究不同菌酶联用处理方式对刺参体壁降解效果及产物风味特性的影响。方法:采用不同处理方式:单菌(J)、单酶(M)、先菌后酶(JM)、先酶后菌(MJ)、菌酶同用(T)(菌为解淀粉芽孢杆菌,酶为复合蛋白酶)对刺参体壁进行降解,测定降解液中氨基酸组成、多肽相对分子质量分布等理化指标,同时利用气相色谱-离子迁移谱(GC-IMS)和电子舌分别测定不同处理方式下刺参体壁降解产物的挥发性和非挥发性风味成分。结果:刺参体壁经菌酶联合(JM、MJ、T)处理后,与单独作用相比,相对分子质量>1000 Da的肽含量减少了60.29%,<500 Da的肽含量增加了33.36%,联合处理下游离氨基酸总量与风味核苷酸总量的平均值较菌酶单独作用时分别增加了1.3倍和4.1倍,降解液中挥发性化合物由未处理时的43种增加到联合处理后的67种。表明刺参体壁经联合处理后风味成分变得更加复杂,联合处理可以降低小分子醛、不饱和醛等腥味成分的含量、增加酯类等愉悦性成分的含量。其中,多肽含量最高的处理组是M(34.770 mg/g),其次是JM(30.733 mg/g),感官评分最高的是JM(66.67分),其次是J(63.75分);鲜味和甜味氨基酸之和占总氨基酸的比例中J最高,JM和M次之,T最低;菌酶联合处理中,JM处理组呈酸臭味的丙酸、刺激性气味的2-甲基丙醛相对含量较低、呈酮香味的2-戊酮、芳香味的月桂烯相对含量较高。综合各指标测定结果来看,JM降解液的风味较佳。结论:菌酶联合处理(JM、MJ、T)均能去除刺参降解产物的腥味,同时提升风味,其中JM降解综合评价最高,作为一种技术对刺参体壁进行降解,可获得具有良好风味的多肽降解产物。Abstract: Objective: To investigate the effects of different combined treatments of bacteria and enzyme on the degradation and flavor components of body wall of sea cucumber. Methods: Different treatment methods: Single bacteria (J), single enzyme (M), bacteria before enzyme (JM), bacteria after enzyme (MJ), and bacteria with enzyme (T) (The bacterium was Bacillus amyloliticus and the enzyme was compound protease) were used to degrade the body wall of sea cucumber. Physical and chemical indexes such as amino acid composition and relative molecular mass distribution of polypeptides in the degradation solution were determined. Gas chromatography-ion mobility spectrometry (GC-IMS) and electronic tongue were used to determine the volatile and non-volatile flavor components of the degradation products of body wall of sea cucumber under different treatments. Results: After combined treatments of bacteria and enzyme (JM, MJ, T), compared with single action, the content of relative molecular mass of peptides larger than 1000 Da was decreased by 60.29%, while those smaller than 500 Da was increased by 33.36%. The content of total free amino acid and nucleotide of combined treatments were increased by 1.3 and 4.1 times, respectively, compared with that of bacterial enzyme alone. The volatile compounds in the degradation solution increased from 43 without treatment to 67 after combined treatments, indicating that the flavor components of body wall of sea cucumber became more complex after combined treatment. Combined treatment could reduce the content of small molecular aldehydes, unsaturated aldehydes and other fishy ingredients, increase the content of esters and other pleasant ingredients. Among them, the treatment group with the highest polypeptide content was M (34.770 mg/g), followed by JM (30.733 mg/g), and the sensory score was highest in JM (66.67), followed by J (63.75). In the proportion of the sum of umami and sweet amino acids to the total amino acids, J was the highest, followed by JM and M, and T was the lowest. In the combined treatments of bacterial and enzyme, the relative contents of propionic acid with sour odor and 2-methylpropionic aldehyde with pungent odor were lower, and the relative contents of 2-pentanone with ketone flavor and laurene with aromatic flavor were higher in the JM treatment group. According to the results of each index, the flavor of JM degradation solution was better. Conclusion: The combined treatments of bacteria and enzyme (JM, MJ, T) can remove the fishy taste of the degradation products of sea cucumber, and improve the aromatic flavor at the same time. JM has the highest evaluation of degradation. As a technology to degrade the body wall of sea cucumber, polypeptide degradation products with good flavor can be obtained.
-
刺参(Stichopus japonicus)是一种营养丰富、药用价值极高的深海棘皮动物,含有多种生物活性物质,如刺参多糖、刺参皂苷、刺参多肽、胶原蛋白、明胶、硫酸软骨素等[1]。刺参肽是通过生物降解从刺参中提取并纯化后得到的小分子肽,其具有抗糖尿病[2]、抗肿瘤[3]等多种活性,是开发新药和功能性食品的良好原料。刺参肽的主要制备方法为酶解法和发酵法。酶解法水解效率高、反应条件温和,但酶解液香味不足、异味较重[4];发酵法与酶法相比成本较低、同时可以提升原料的营养品质和降低抗营养因子含量,但存在水解效率较低、产酶不足、耗时严重等缺点[5]。研究表明,菌酶协同发酵可以结合二者的优点,对风味的改善优于单独酶解、对肽含量的提高优于单独发酵[6],在降低商业酶使用量的同时,能弥补微生物发酵水解程度低的不足,是一种有效的方法。王安凤[7]研究发现合浦珠母贝肉酶解液经米曲霉和鲁式酵母协同发酵处理后,酶解液的挥发性风味成分由29种增加到56种,发酵后风味成分更加复杂,愉悦性风味成分增加。汪韬等[8]通过乳酸菌发酵改善仿刺参酶解液的腥味和苦味,制得了具有仿刺参鲜味和良好发酵风味的仿刺参肽粉。闫泽文[9]研究也发现乳酸菌发酵降低了仿刺参内脏因酶解产生的苦味肽含量,从而降低样品的苦味。目前从刺参体壁、内脏、生殖腺等加工副产物中提取多肽均有研究,但多为单独酶解或者单独发酵方面的研究[10],菌酶联合使用降解刺参多肽的研究还比较少。
本文以盐渍刺参为原料,从水产品常用的菌种(枯草芽孢杆菌、植物乳杆菌、肠膜明串珠菌、解淀粉芽孢杆菌、鲁式酵母)和酶制剂(碱性蛋白酶、木瓜蛋白酶、中性蛋白酶、复合蛋白酶、风味蛋白酶)中筛选出效果最佳的菌和酶后,采用不同菌酶联用方式(先菌后酶、先酶后菌、菌酶同时加入)降解刺参体壁,通过测定降解液中氨基酸组成、多肽相对分子质量分布等理化指标和挥发性和非挥发性风味成分等风味指标,探究不同处理方式对刺参体壁降解效果及产物风味特性的影响,以期为开发风味良好的刺参多肽提供理论基础和技术支撑。
1. 材料与方法
1.1 材料与仪器
盐渍刺参(15~20 g、5~10 cm/个) 烟台万事如意食品有限公司;复合蛋白酶(1.6 AU-N/g) 丹麦诺维信公司;风味蛋白酶(2万U/g)、碱性蛋白酶(20万U/g)、木瓜蛋白酶(80万U/g) 南宁庞博生物工程有限公司;枯草芽孢杆菌(bio-59397)、植物乳杆菌(20265)、肠膜明串珠菌(21859)、解淀粉芽孢杆菌(10035)、鲁式酵母(32899) 中国工业菌种保藏中心;总氨基酸测定试剂盒 南京建成生物工程研究所;Lowry法蛋白浓度测定试剂盒、核苷酸标准品(5'-腺苷酸(5'-AMP)、5'-鸟苷酸(5'-GMP)、5'-肌苷酸(5'-IMP))、抑肽酶标准品、乙氨酸-乙氨酸-酪氨酸-精氨酸标准品 北京索莱宝科技有限公司;三氟乙酸 上海麦克林生化科技有限公司;甲醇(色谱纯)、乙腈(色谱纯)、三氯乙酸、高氯酸、磷酸二氢钾、氢氧化钾 均为分析纯,国药集团化学试剂有限公司。
JMF-365胶体磨 烟台星火轻工机械设备有限公司;METTLER TOLEDO电子分析天平 美国Ohaus公司;MQL-61R立式全温振荡培养箱 上海旻泉仪器有限公司;HH-4电热恒温水浴锅 山东省烟台龙口市先科仪器公司;GR60DA立式自动压力蒸汽灭菌器 厦门致微仪器有限公司;TGL-16M高速台式冷冻离心机 湖南湘仪实验室仪器开发有限公司;1510型酶标仪 赛默飞世尔(中国)有限公司;1260型高效液相色谱仪 安捷伦科技(中国)有限公司;FlavourSpec®风味分析仪 济南海能仪器股份有限公司;SuperTongue电子舌 上海瑞玢智能科技有限公司;日立L-8900全自动氨基酸分析仪 日本Hitachi公司;KQ-600B型超声波清洗器 昆山市超声仪器有限公司;XW-80A旋涡混合器 上海精科实业有限公司;FD-2A冷冻干燥机 北京博医康实验仪器有限公司。
1.2 实验方法
1.2.1 原料预处理
将盐渍刺参洗净,用去离子水浸泡脱盐。去除刺参的沙嘴,洗净、剪碎,加入同等质量的去离子水混匀,用150目胶体磨3000 r/min匀浆5 min[11],作为未处理匀浆(Y)备用。
1.2.2 不同处理方式处理刺参体壁匀浆样品
1.2.2.1 单菌筛选发酵实验
将冷冻干燥保存的菌种接种于按说明书配制的液体培养基中37 ℃培养18 h,活化2代后作为种子液,4 ℃条件下备用。每次使用之前都取种子液活化一代,待菌种长到OD600=0.40浓度后开始使用。
称取50 g匀浆样品,按料液比1:3(g/mL)加入去离子水,分别加入枯草芽孢杆菌、植物乳杆菌、肠膜明串珠菌、解淀粉芽孢杆菌、鲁式酵母,菌加量为3%(菌液与样品体积比)[12],每种菌在各自适宜的温度和pH条件下(表1),恒温振荡培养箱(180 r/min)发酵48 h,121 ℃灭菌20 min,7000 r/min离心10 min取上清液备用。
表 1 不同菌种的发酵条件Table 1. Fermentation conditions of different strains菌种种类 pH 温度(℃) 时间(h) 枯草芽孢杆菌 7.0 37 48 植物乳杆菌 6.8 37 48 肠膜明串珠菌 7.0 37 48 解淀粉芽孢杆菌 7.2 30 48 鲁氏酵母 7.0 28 48 1.2.2.2 单酶筛选酶解实验
称取50 g匀浆样品,按料液比1:3(g/mL)加入去离子水,分别加入碱性蛋白酶、木瓜蛋白酶、复合蛋白酶、风味蛋白酶,酶加量为500 U/g(以匀浆质量和酶活计算),每种酶在各自适宜的温度和pH条件下(表2),恒温振荡培养箱(180 r/min)酶解4 h,沸水浴灭酶10 min,7000 r/min离心10 min取上清液备用。
表 2 不同酶制剂的酶解条件Table 2. Enzymatic hydrolysis conditions of different enzyme preparations蛋白酶种类 pH 温度(℃) 时间(h) 风味蛋白酶 7.5 50 4 复合蛋白酶 6.0 50 4 木瓜蛋白酶 6.5 55 4 碱性蛋白酶 8.0 50 4 1.2.2.3 不同处理方式降解实验
称取50 g匀浆样品,按料液比1:3(g/mL)加入去离子水,以筛选出的解淀粉芽孢杆菌和复合蛋白酶为后续实验用菌和用酶,依次进行单菌发酵(J)、单酶酶解(M)、先菌后酶(JM)、先酶后菌(MJ)和菌酶同用(T)实验[9],其中JM和MJ的发酵条件参照1.2.2.1,酶解条件参照1.2.2.2。T在30 ℃下恒温振荡培养箱(180 r/min)发酵48 h后,121 ℃灭菌20 min,7000 r/min离心10 min取上清液备用。
1.2.3 多肽含量的测定
参考鲁伟等[13]的方法并作适当修改,取1 mL降解液,加入等体积质量分数10%的三氯乙酸溶液,静置10 min,4 ℃、10000 r/min离心10 min,采用Lowry法,在650 nm波长处测定吸光度。根据标准曲线y=0.8312x−0.0039,R2=0.991,得出多肽的含量。
1.2.4 感官评定
选择10位不同年龄段的经过培训且味觉、嗅觉正常的食品科研人员进行感官评分,分别从腥味、气味、滋味三个方面进行评价并打分,评价标准见表3,由于3个指标对降解液品质的贡献不一样,因此,将腥味、气味和滋味的权重系数分别设定为3,3和4,样品评分=(腥味得分)×3+(气味得分)×3+(滋味得分)×4,满分100分。每个样品重复3次,去掉每个样品的最高分和最低分,取平均分作为样品的感官评分。
表 3 感官评分标准Table 3. Sensory rating criteria项目 评分标准 1~2分 3~5分 6~8分 9~10分 腥味(30分) 腥味较重 腥味中等 腥味较淡 基本无腥味 气味(30分) 发酵味、酸味过重并伴随一定的异味 具有刺参固有的气味,无不良气味 具有刺参固有的气味,发酵产生的鲜香味 具有刺参固有的气味,令人愉悦的果香味和清爽的酸味 滋味(40分) 口感较差,过苦、过咸、有异味 口感一般,偏苦、偏咸 口感适宜,微甜、微咸 口感柔和,酸甜适宜、鲜香可口 1.2.5 游离氨基酸总量的测定
采用总氨基酸测定试剂盒说明书的比色法进行测定。
1.2.6 相对分子质量的测定
相对分子质量采用高效凝胶过滤色谱法(GB/T 27729-2008海洋鱼低聚肽粉),用高效液相色谱仪测定。
1.2.7 氨基酸的测定
氨基酸采用酸水解法(GB/T 18246-2019饲料中氨基酸的测定),用全自动氨基酸分析仪测定。
1.2.8 呈味核苷酸的测定
参照张倩等[14]的方法,并稍作修改。分别准确吸取5.0 g降解液样品(精确到0.001 g),加入15 mL预冷处理质量分数为5%的高氯酸(PCA),充分混匀静置20 min,4 ℃、5000 r/min离心15 min后取上清液,用1 mol/L和6 mol/L的氢氧化钾调节溶液pH至6.8,并用超纯水定容至50 mL,摇匀后经0.22 µm滤膜过滤,滤液供分析用。
色谱条件:ZORBAXSB-C18柱(250 mm×4.6 mm,5 μm),流动相A相为甲醇,B相为0.01 mol/L KH2PO4,梯度洗脱(0~10 min,1%~3% A;10~20 min,3%~20% A;20~30 min,20%~25% A),检测波长:UV 260 nm,流速为0.4 mL/min,柱温:25 ℃,进样体积:10 μL。根据样品与标准品的保留时间和峰面积确定AMP、GMP、IMP的含量。
1.2.9 GC-IMS的测定
参考Li等[15]的方法并作适当修改。准确称取2.0 g样品置于20 mL顶空瓶中,密封后置于50 ℃,500 r/min振荡器加热孵化15 min,顶空进样口温度为55 ℃,进样量为0.5 mL,载气为高纯N2。气相色谱柱为WAX,30 m,ID:0.53 mm,膜厚1 μm(美国RESTEK公司),柱温为60 ℃,运行时间30 min。离子迁移谱检测温度为45 ℃,漂移气为高纯N2,流速为150 mL/min。
1.2.10 电子舌的测定
取上清液30 mL加蒸馏水稀释至90 mL,倒入电子舌专用杯中。先用0.01 mol/L的KCl溶液将电子舌预热,预热完成后开始电子舌测试。每测一次需要将电子舌传感器清洗一遍,每个样品设置测4次,为保证结果的稳定性,删除第1次,取后3次的测量结果进行分析。
1.3 数据处理
数据均是3次重复试验取平均值,结果以平均值±标准差表示,采用SPSS Statistics 26.0软件对数据进行ANOVA差异显著性分析,P<0.05表示具有统计学意义,运用Origin8.0软件作图。
2. 结果与分析
2.1 不同菌对发酵液多肽含量和感官评分的影响
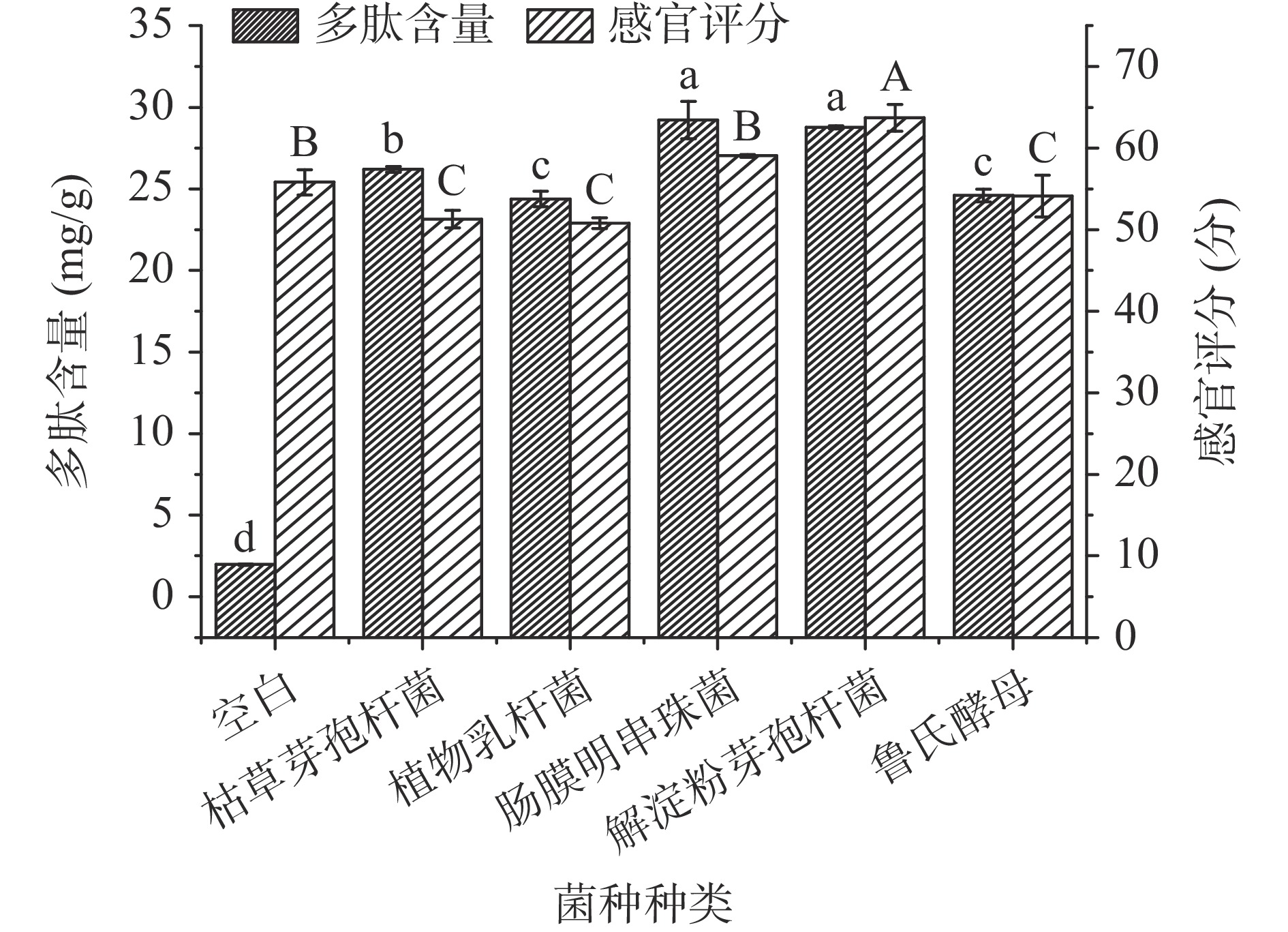
从图1可以看出,经菌发酵后发酵液中多肽含量显著增加(P<0.05),感官评分各不相同。采用不同的菌发酵刺参体壁,发酵液的多肽含量从高到低依次为肠膜明串珠菌、解淀粉芽孢杆菌、枯草芽孢杆菌、鲁氏酵母和植物乳杆菌,但肠膜明串珠菌和解淀粉芽孢杆菌没有显著差异(P>0.05)。发酵液的感官评分从高到低依次是解淀粉芽孢杆菌、肠膜明串珠菌、鲁式酵母、枯草芽孢杆菌和植物乳杆菌,其中解淀粉芽孢杆菌感官评分显著高于其他菌(P<0.05)。解淀粉芽孢杆菌可以产生多种酶,包括蛋白酶、淀粉酶和葡萄糖苷酶等,能将原料中的蛋白质、淀粉分解为单糖、寡糖、氨基酸和多肽,为多种风味物质的形成提供了前体物质[16]。赵彦珺[17]用复合菌发酵海参的肠和卵,发现发酵可以明显改善海参肠卵酶解液的风味,张涵[18]利用乳酸菌和甜酒曲发酵熟制海参,得到了具有酸香口味和醇香口味的海参制品。综合考虑多肽含量和感官评分两指标,选用解淀粉芽孢杆菌作为后续发酵菌。
2.2 不同蛋白酶对酶解液多肽含量和感官评分的影响
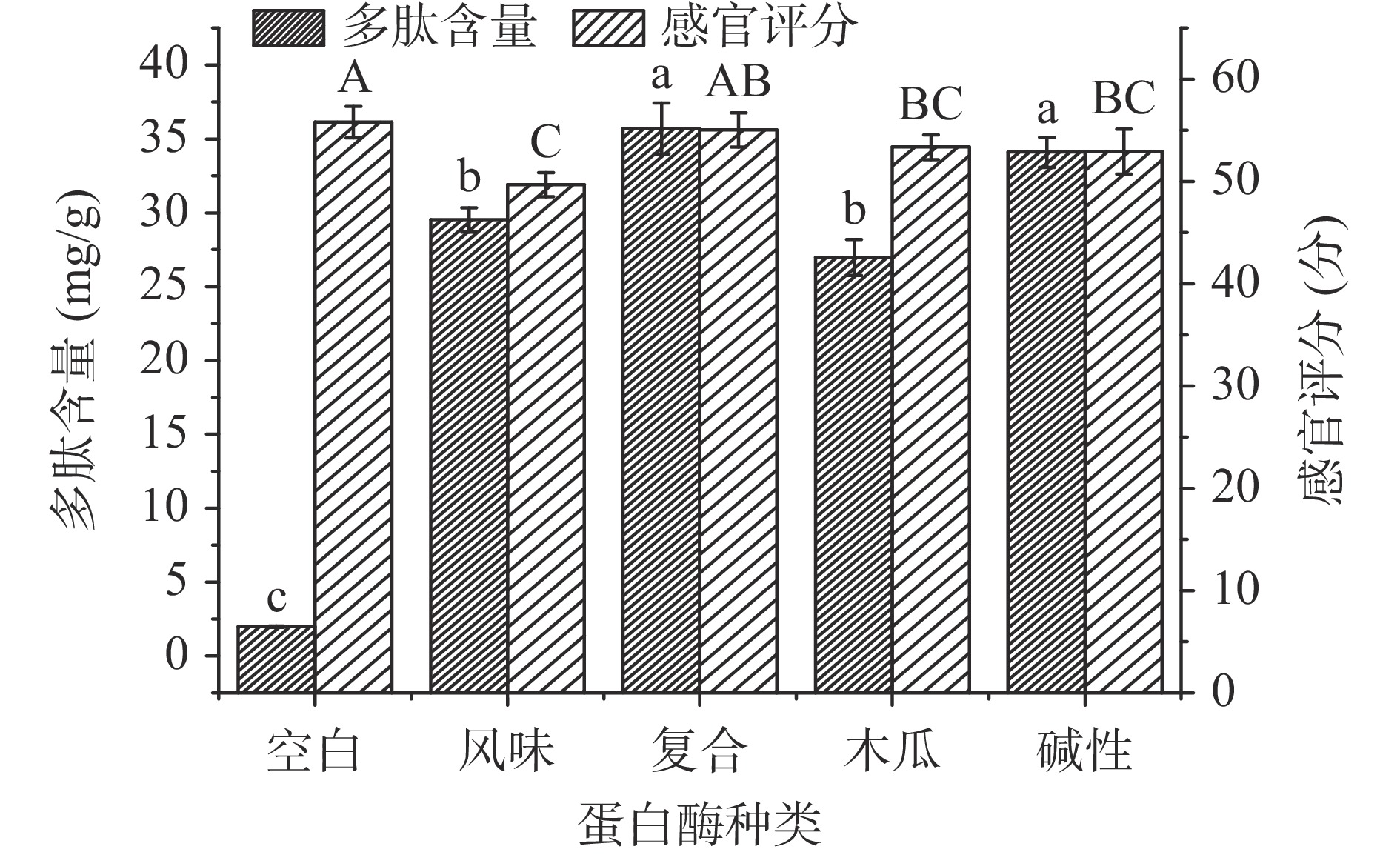
从图2可以看出,酶解液中多肽含量显著增加,感官评分除复合蛋白酶外均显著降低(P<0.05)。采用不同的蛋白酶酶解刺参体壁,酶解液的多肽含量从高到低依次是复合蛋白酶、碱性蛋白酶、风味蛋白酶和木瓜蛋白酶,其中复合蛋白酶和碱性蛋白酶差异不显著(P>0.05),但显著高于风味蛋白酶和木瓜蛋白酶(P<0.05),这与李学鹏等[19]用不同酶酶解刺参体壁,得到碱性蛋白酶水解效率大于木瓜蛋白酶的结果相似。酶解液的感官评分从高到低依次为复合蛋白酶、木瓜蛋白酶、碱性蛋白酶和风味蛋白酶,其中复合蛋白酶与木瓜蛋白酶、碱性蛋白酶差异不显著(P>0.05),但显著高于风味蛋白酶(P<0.05)。这种差异主要是由蛋白酶的特异性与酶切位点的差异性引起的[20]。复合蛋白酶是一种非特异性内切酶,有较多的切割位点,可通过水解蛋白质产生大量小片段多肽,从而表现出较高多肽含量的特点[21]。徐永霞等[22]研究发现用复合酶酶解蓝蛤,酶解液的水解度最大且整体风味较其他酶好。综合考虑多肽含量和感官评分两指标,选用复合蛋白酶作为后续酶解酶。
2.3 不同处理方式对降解液多肽含量、感官评分和游离氨基酸总量的影响
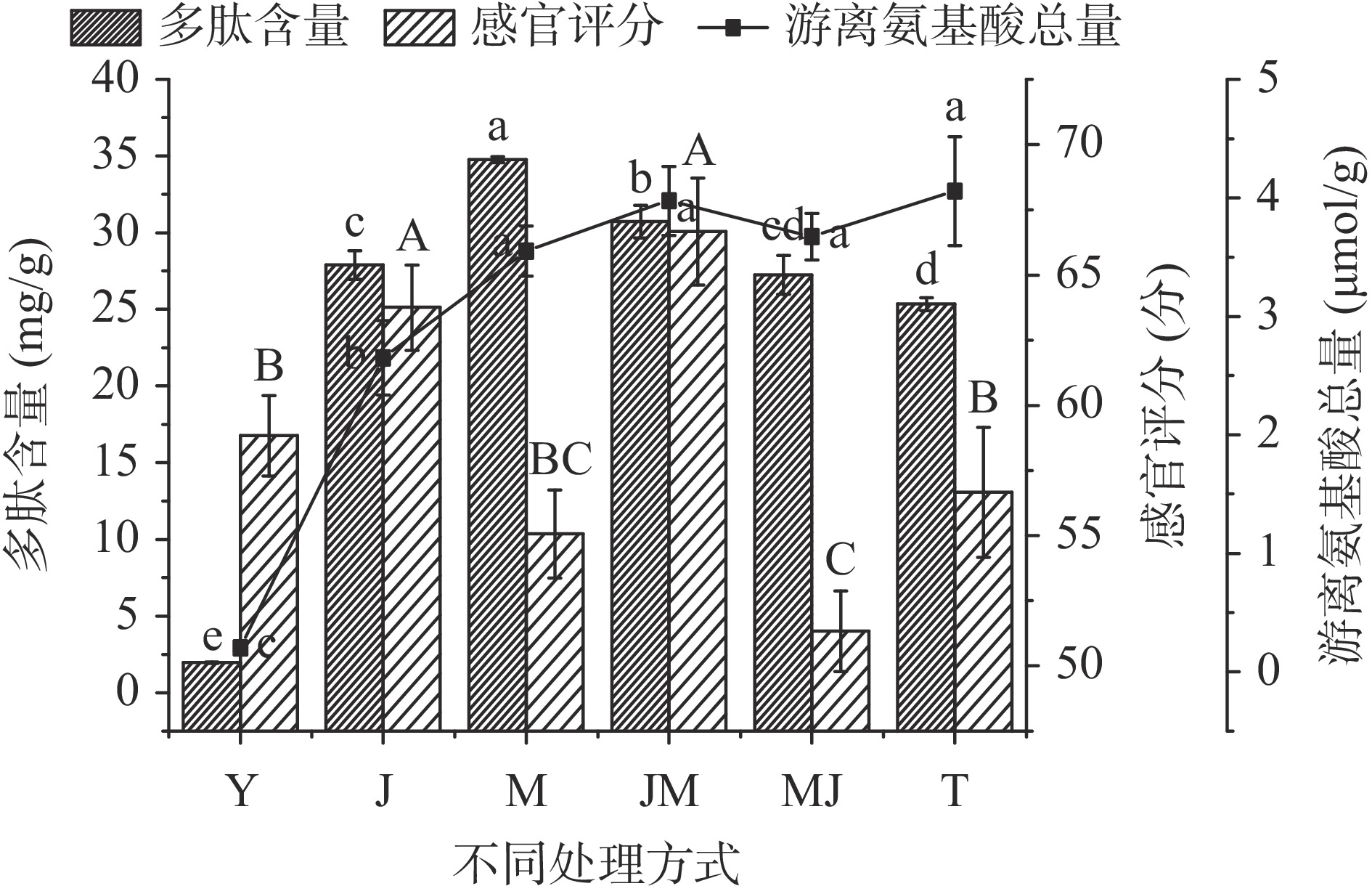
由图3可知,不同的菌酶联合方式对多肽含量、感官评分和游离氨基酸总量的影响不同,经处理后降解液中的多肽含量、游离氨基酸总量均显著高于Y(P<0.05),感官评分各不相同。与J相比,JM多肽含量和游离氨基酸总量显著增加(P<0.05),感官评分无显著变化(P>0.05);MJ多肽含量无显著变化(P>0.05),而感官评分显著降低(P<0.05),游离氨基酸总量显著增加(P<0.05);T多肽含量和感官评分显著降低(P<0.05),游离氨基酸总量显著增加(P<0.05)。与M相比,3种菌酶联合方式的多肽含量显著降低(P<0.05),JM的多肽含量最高,T的多肽含量最低;JM的感官评分显著增加(P<0.05),而MJ和T没有显著变化(P>0.05);游离氨基酸总量没有显著变化(P>0.05)。T多肽含量下降,可能是由于酶作用时间较长,部分多肽被进一步降解成游离氨基酸[23]。菌酶联合使用降低商业酶使用量的同时,弥补了微生物发酵水解程度低的不足,一般认为酶解易产生苦味肽、同时腥味较重,而发酵对去腥和风味提升具有良好的效果[5]。在3种菌酶联合方式中,JM的多肽含量和感官评分最高。
2.4 不同处理方式对降解液多肽相对分子质量分布的影响
如表4所示,经不同处理方式处理后水解物相对分子质量分布主要分为五个区间,但主要集中在<500 Da、500~1000 Da和1000~2000 Da范围内。其中,相对分子质量<1000 Da的小肽链占比在65.75%~96.30%之间,最高的是T(96.30%),最低的是J(65.75%)。这与Wang等[24]利用复合酶与风味酶酶解鳕鱼头得到80%以上的短肽(10肽以下)的结果相似。研究表明,降解液的呈味特性、营养价值及生物活性等与所含的小分子肽密切相关,水产品中的蛋白质、核酸等大分子物质分解转化为小分子的多肽、游离氨基酸和5'-核苷酸等后,滋味能得到更大化的呈现[25]。刘倩[26]采用醇提法从毛霉蛋白酶豆腐酶解液中提取大豆鲜味肽,得到鲜味最强的组分是相对分子质量在452.2~556.3 Da之间的短肽;Liu等[27]研究发现以二肽和三肽为基础的肠内配方比全蛋白配方对腹部手术患者的营养改善更有效、耐受性更好,小肽更利于患者的消化吸收。刺参体壁主要由胶原蛋白组成,相对分子质量在几万到十几万之间,经不同处理后,>3000 Da、2000~3000 Da、1000~2000 Da区段的肽含量减少,而<500 Da、500~1000 Da区段的肽含量增加,说明不同处理方式的降解效果均显著。
表 4 不同处理方式降解液的多肽相对分子质量分布Table 4. Relative molecular mass distribution of peptides in degradation solution with different treatment methods相对分子质量(Da) J(%) M(%) JM(%) MJ(%) T(%) >3000 5.921 0.051 0.109 0.091 0 2000~3000 8.885 0.813 1.175 1.297 0.11 1000~2000 19.445 9.575 10.324 9.919 3.592 500~1000 21.956 28.908 25.555 22.013 16.886 <500 43.794 60.653 62.837 66.680 79.412 2.5 不同处理方式对降解液氨基酸组成的影响
对不同处理方式降解液中的氨基酸组成和呈味特性进行分析比较。如表5所示,不同处理方式中均检测到17种常见氨基酸,表明5种刺参体壁降解液中氨基酸种类比较丰富,且不同处理方式下TAA含量差异显著(P<0.05),从高到低依次是M(62.61 g/100 g)、JM(54.78 g/100 g)、MJ(50.43 g/100 g)、J(47.48 g/100 g)、T(44.19 g/100 g)。从单一氨基酸上看,不同处理方式中含量最高的主要是甘氨酸和谷氨酸,最低的是蛋氨酸与组氨酸,这与张健等[28]对刺参卵和体壁营养成分分析的结果一致。由表5知,3类呈味氨基酸含量在不同降解液中的分布规律相似,均为甜味氨基酸最大,苦味氨基酸次之,鲜味氨基酸最小。从占TAA的百分比上看,T的鲜味与甜味氨基酸之和显著低于其他降解液,而苦味氨基酸显著高于其他降解液(P<0.05),M与JM的占比无显著差异(P>0.05)。
表 5 不同处理方式降解液的氨基酸组成Table 5. Amino acid composition of degradation solution by different treatment methods序号 氨基酸 含量(g/100 g干重) Y J M JM MJ T 1 天门冬氨酸Asp 6.04±0.04ab 4.99±0.11d 6.37±0.11a 5.78±0.25bc 5.67±0.14c 5.10±0.11d 2 苏氨酸Thr 3.13±0.02b 2.23±0.08d 3.35±0.04a 2.56±0.11c 1.98±0.05e 1.59±0.03f 3 丝氨酸Ser 3.08±0.03a 2.19±0.04c 3.18±0.04a 2.55±0.1b 2.20±0.05c 1.81±0.03d 4 谷氨酸Glu 9.82±0.11a 7.34±0.15c 10.01±0.15a 8.49±0.36b 7.35±0.17c 6.2±0.13d 5 甘氨酸Gly 10.32±0.14a 8.15±0.23d 9.65±0.18b 8.98±0.36c 8.6±0.17cd 7.43±0.16e 6 丙氨酸Ala 4.39±0.04a 2.98±0.03c 4.29±0.09a 3.48±0.14b 2.77±0.07d 2.22±0.05e 7 半胱氨酸Cys 1.39±0.09ab 1.50±0.18a 1.49±0.04ab 1.42±0.02ab 1.40±0.03ab 1.26±0.03b 8 缬氨酸Val 2.28±0.02b 1.84±0.03e 2.52±0.01a 2.14±0.06c 2.11±0.04c 1.97±0.05d 9 蛋氨酸Met 0.86±0.01bc 0.56±0.01cd 0.46±0.02d 0.98±0.28b 1.37±0.10a 1.11±0.14ab 10 异亮氨酸Ile 1.74±0.01b 1.23±0.04d 1.85±0.06a 1.45±0.05c 1.23±0.02d 1.19±0.03d 11 亮氨酸Leu 2.63±0.01b 2.04±0.01d 3.05±0.03a 2.45±0.10c 2.68±0.06b 2.57±0.05bc 12 酪氨酸Tyr 2.01±0.02bc 1.91±0.07c 2.35±0.02a 2.27±0.04ab 2.12±0.16abc 2.01±0.23bc 13 苯丙氨酸Phe 1.45±0.01c 1.41±0.03c 1.75±0.04ab 1.72±0.07b 1.82±0.01a 1.73±0.04ab 14 赖氨酸Lys 1.88±0.01c 1.80±0c 2.25±0.04a 2.16±0.08ab 2.19±0.03ab 2.12±0.05b 15 脯氨酸Pro 4.87±0.05a 3.77±0.05c 4.74±0.05a 4.27±0.13b 3.78±0.08c 3.29±0.08d 16 组氨酸His 0.60±0b 0.46±0.01c 0.74±0.01a 0.55±0.04b 0.41±0.04c 0.44±0.02c 17 精氨酸Arg 4.74±0.08a 3.07±0.07c 4.58±0.08a 3.54±0.18b 2.74±0.04d 2.12±0.04e 18 TAA 61.22±0.59a 47.48±0.92d 62.61±0.8a 54.78±1.77b 50.43±0.83c 44.19±0.93e 19 DAA 15.86±0.18a 12.33±0.32c 16.38±0.32a 14.27±0.76b 13.02±0.37c 11.30±0.29d 20 SAA 25.79±0.35a 19.33±0.55c 25.2±0.49a 21.84±1.03b 19.33±0.51c 16.35±0.43d 21 BAA 18.18±0.07b 14.33±0.03f 19.55±0.18a 17.25±0.34c 16.68±0.08d 15.28±0.38e 22 DAA+SAA 41.65±0.53a 31.65±0.87c 41.58±0.81a 36.11±1.78b 32.35±0.89c 27.65±0.72d 23 (DAA+SAA)/TAA 0.68±0a 0.67±0b 0.66±0b 0.66±0.01b 0.64±0c 0.63±0d 24 BAA/TAA 0.30±0d 0.30±0.01cd 0.31±0c 0.32±0c 0.33±0b 0.35±0a 注:TAA为总氨基酸;DAA为鲜味氨基酸(谷氨酸、天冬氨酸);SAA为甜味氨基酸(甘氨酸、丙氨酸、丝氨酸、脯氨酸、苏氨酸);BAA为苦味氨基酸(酪氨酸、苯丙氨酸、缬氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、精氨酸、甲硫氨酸);同行不同小写字母表示不同处理组差异显著(P<0.05)。 2.6 不同处理方式对降解液核苷酸含量的影响
由表6可知,菌酶联合处理后,核苷酸含量较单独作用有所增加,不同处理方式的影响不同。与J相比,JM的5'-AMP含量显著增加(P<0.05),其次MJ,而T没有显著变化(P>0.05);T的5'-GMP含量显著增加(P<0.05),其次MJ,而JM没有显著变化(P>0.05)。与M相比,JM、MJ和T的5'-AMP和5'-GMP含量均显著增加(P<0.05),其中,5'-AMP含量JM最高,5'-GMP含量T最高。不同联合方式下风味核苷酸总量从高到低依次是T、MJ、JM。原刺参体壁中不含有5'-GMP,经处理后产生5'-GMP,而M没有产生5'-GMP,是由于酶解超过1.5 h会破坏5'-GMP[29],但菌酶共同作用,5'-GMP大幅度增加,其中的原因还有待进一步探究。刺参体壁和降解液中没有检测到5'-IMP,这与孟凌玉[30]研究微生物混合发酵虾头酶解产物中呈味核苷酸的结果相一致。一般认为虾、蟹、贝等海洋无脊椎动物ATP分解不产生IMP,同时高温也会造成IMP的降解与损失[31]。核苷酸作为单品时并无鲜味,其呈鲜机制主要是通过与鲜味物质之间的协同效应来实现的,主要包括呈味核苷酸之间,以及呈味核苷酸与鲜味氨基酸之间的协同效应[32]。经处理后J、M、JM、MJ、T风味核苷酸总量较Y均显著增加(P<0.05),J与JM无显著变化(P>0.05),且菌酶联合处理风味核苷酸总量增加更多。
表 6 不同处理方式降解液的核苷酸含量Table 6. Nucleotide content of degradation solution by different treatment methods不同处理
方式鲜味物质含量(mg/100 g) 5’-AMP
(腺苷酸)5’-GMP
(鸟苷酸)5’-IMP
(肌苷酸)风味核苷酸 Y 0.43±0.00e − − 0.43±0.00e J 2.17±0.06c 11.33±0.78b − 13.50±0.84c M 0.76±0.00d − − 0.76±0.00d JM 2.45±0.07a 11.31±0.78b − 13.76±0.85c MJ 2.29±0.04b 32.90±1.36a − 35.19±1.4b T 2.20±0.02bc 36.39±2.31a − 38.59±2.33a 注:−表示未检出;风味核苷酸为5’-GMP、5’-IMP和5’-AMP之和;同列小写字母不同表示不同处理组差异显著(P<0.05)。 2.7 不同处理方式对降解液挥发性风味物质的影响
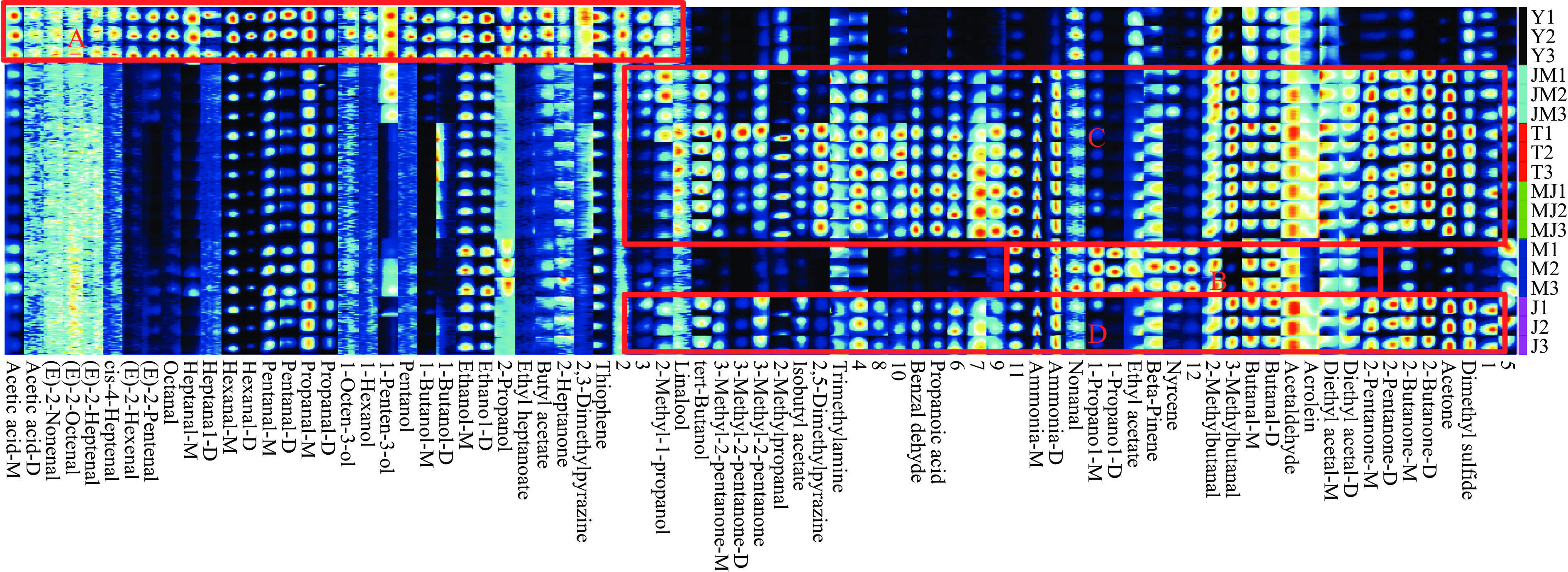
如图4所示,不同处理条件下的刺参样品中挥发性成分在种类和含量上均有差异。六组样品中共检测出77种挥发性成分,定性出来62种,包括14种醇类、24种醛类、8种酮类、2种酸类、4种酯类、1种醚类、4种烃类及其他类5种,含量最高的种类是醛类、醇类、酮类和烃类,这一结果与其他关于刺参挥发性风味物质的研究一致[33]。
Y(匀浆)中以醇和醛为主要成分,如图4A区域所示,例如E-2-辛烯醛、E-2-庚烯醛、E-2-己烯醛、辛醛、1-辛烯-3-醇、戊醇、己醇等,且含量明显高于酶解和发酵处理组。相关研究表明[34],醛的气味阈值和气味特性主要受醛的链长、饱和度和分子结构等的影响。低相对分子质量(<150 Da)的饱和脂肪醛通常呈刺激性气味、油脂味或鱼腥味,单不饱和醛与青草味和鱼腥味有关,而支链和直链会带来刺鼻的气味和提供青草味。阮秋凤等[35]的研究也表明,鱼类中的己醛、庚醛、Z-4-庚烯醛、E-2-辛烯醛等具有腥味。
刺参体壁经过处理后,低相对分子质量醛如己醛、庚醛、辛醛和壬醛的含量降低或消失,单不饱和醛也均消失,同时产生具有杏仁香味的苯甲醛,这可能是经处理后的样品腥味降低、风味改善的主要原因。而醇类物质中,1-丁醇、戊醇、1-己醇、1-戊烯-3-醇、1-辛烯-3-醇含量降低或消失,1-丙醇和芳樟醇、2-甲基-1-丙醇含量升高,新产生叔丁醇。其中,戊醇、己醇、1-辛烯-3-醇通常被认为是脂质氧化的产物[36],叔丁醇和芳樟醇具有清新、樟脑气味。
M中挥发性化合物种类最少,如图4B区域所示,其中壬醛、乙醇、1-丙醇、2-丙醇、月桂烯等物质的含量较其他处理组高,壬醛呈鱼腥味、醇类阈值较高对风味的改善作用不明显,且酶解常伴随苦味。
J、JM、MJ和T新增挥发性化合物种类最多,新产生酮类、酯类和烯类物质,如图4C区域所示,酮类物质阈值较低对风味贡献较大。经处理后2-丁酮、β-蒎烯的含量增加,新产生丙酮、2-戊酮、4-甲基-2-戊酮、苯甲醛、芳樟醇等。丙酮具有芳香气味,2-丁酮、2-戊酮气味与丙酮类似,4-甲基-2-戊酮呈令人愉快的酮香味[35]。发酵过程中这些物质相对含量的升高,说明发酵处理对刺参的风味起到了积极的作用,使刺参的整体风味得到改善。不同处理方式间4-甲基-2-戊酮、月桂烯、三甲胺、丙酸、二甲基硫醚、2-甲基丙醛等的含量差异比较大。呈芳香味的月桂烯仅在JM和M中检出,呈酸臭味的丙酸、刺激性气味的2-甲基丙醛在MJ、T中相对含量较高,在JM和M中相对含量较低,呈酮香味的丙酮、2-戊酮在JM和J中相对含量较高,在MJ和M中相对含量较低。相比于其他处理方式,JM中鱼腥味成分含量相对较低、愉悦性成分含量相对较高。
2.8 不同处理方式对降解液滋味的影响
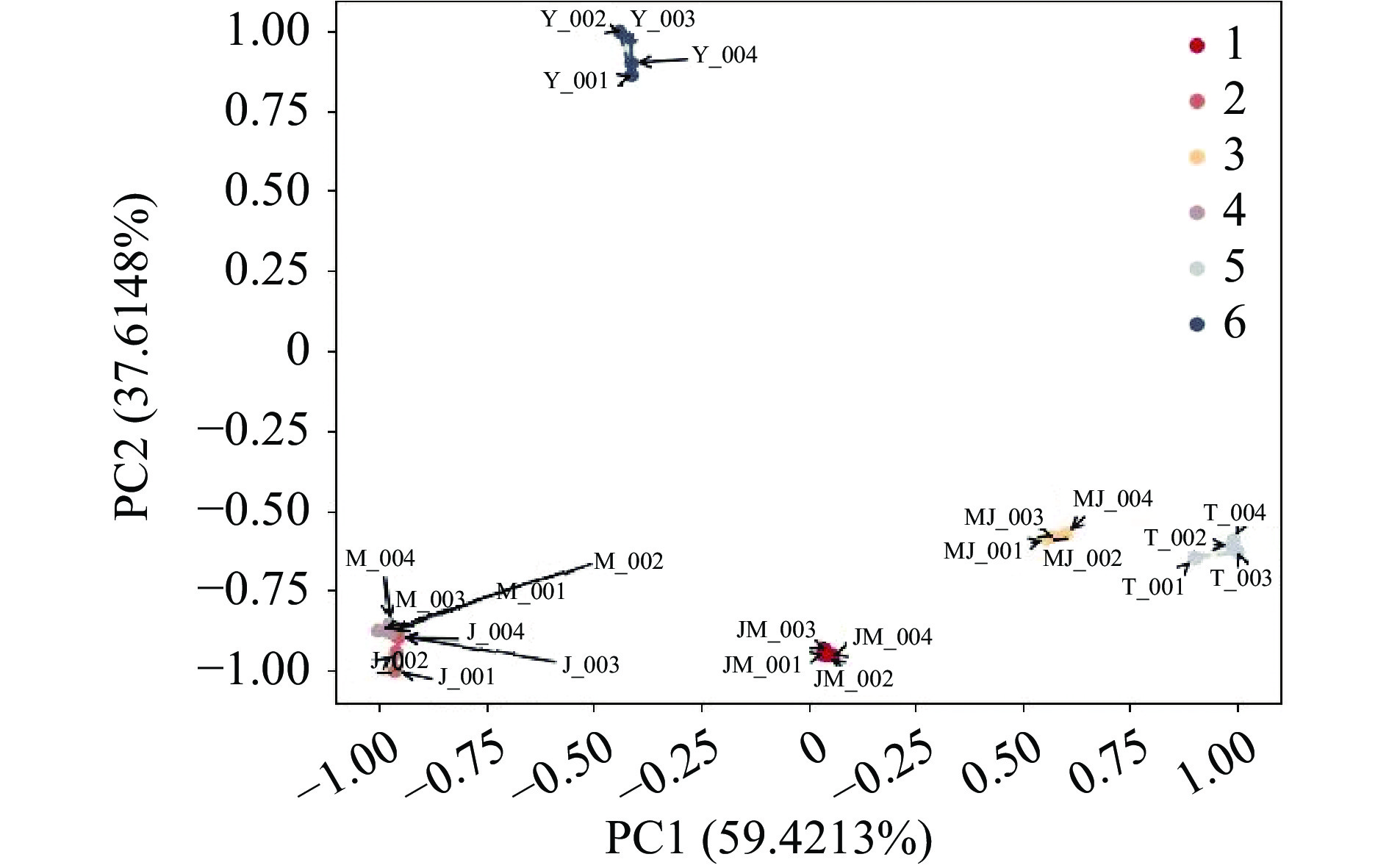
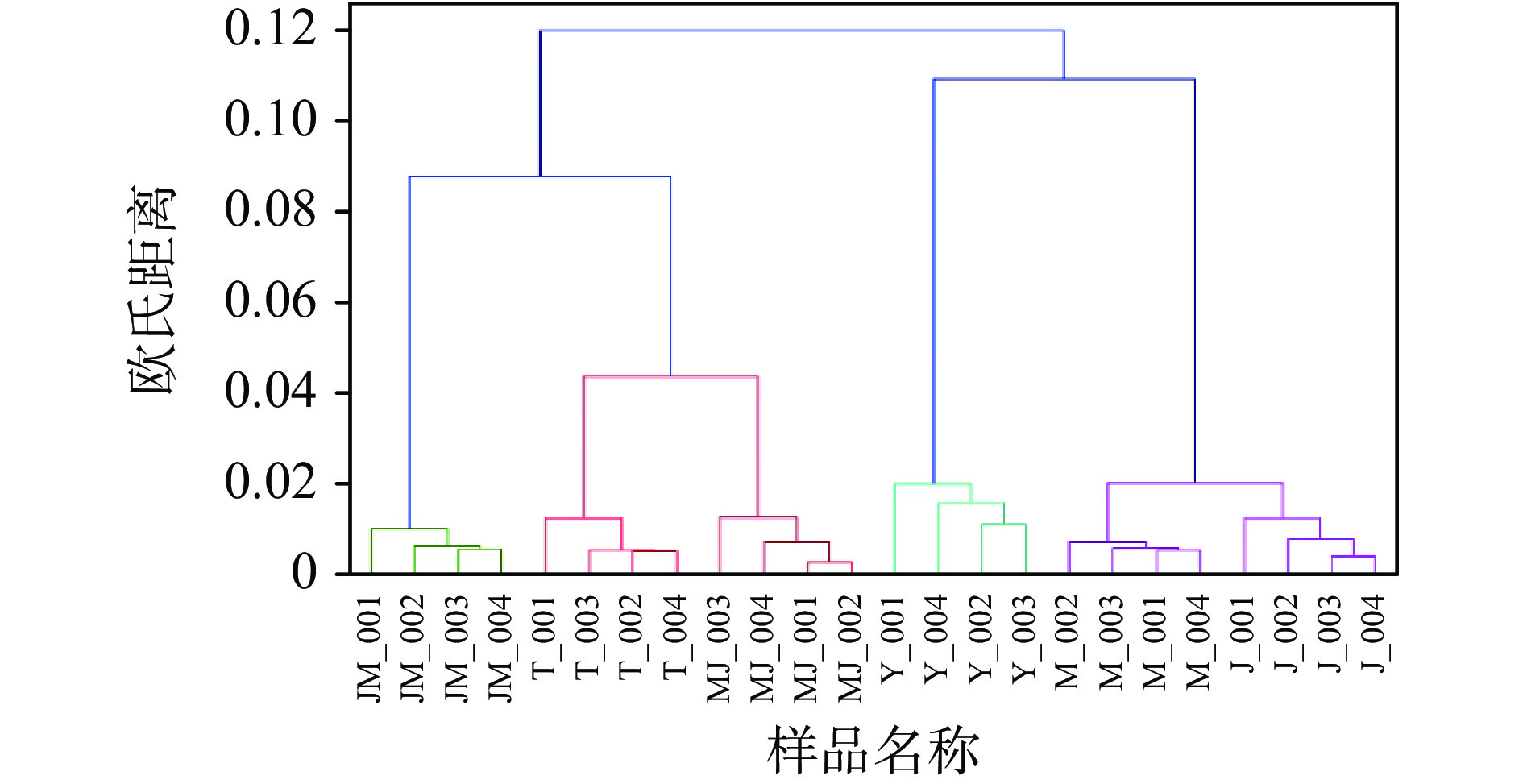
本实验使用主成分分析来分析不同处理方式下降解液中非挥发性化合物的变化。律诗等[37]通过主成分分析从九种食用菌中选出了鲜味评分最高的鹿茸菇;Li等[38]从主成分分析中清楚地将新鲜和干燥松茸不同部位的样品区分开来。如图5所示,PC1(59.42%)和PC2(37.61%)的累计方差贡献率为97.03%,说明二个主成分包含了较多的样品信息。刺参体壁降解液样品在图上有很好的区分性,说明不同处理方式下风味物质之间差异显著(P<0.05)。J与M样品滋味比较相似;同样,MJ与T样品风味也比较相似。JM风味介于二者之间,这也解释了感官评分差异产生的原因。刺参体壁样品在菌酶不同联用顺序下(JM与MJ),风味特征发生了二次变化,但MJ和T样品表现出相似的风味特征,其原因还需通过进一步的实验来确定。利用聚类分析进一步分析了不同处理的条件下刺参体壁的滋味物质(图6)。根据聚类树状图的垂直模式[39],所有样品被分为二类。Y、J、M样品被聚集在一起形成一组;菌酶联用的样品聚集在一起形成另外一组。每一类又可以分成二类,其中,共同作用中MJ和T被分在一组,另一边,J和M被分在同一组。结果表明,酶添加顺序对刺参体壁的滋味成分有较大影响,不同处理方式刺参体壁风味不同,这与主成分分析结果一致。
3. 结论
本研究表明,菌酶联合处理后刺参体壁降解产物的多肽含量与感官评分、总游离氨基酸与核苷酸含量都较处理前显著增加(P<0.05)。其中,多肽含量最高是M,其次是JM;感官评分最高是JM,其次是J;原体壁中的大分子胶原蛋白主要降解为相对分子质量<3000 Da的肽段;J的鲜味和甜味氨基酸之和占比最高、苦味占比最低,JM和M次之,T最低;T和MJ降解液的核苷酸总量最高;J、JM、MJ和T挥发性风味物质种类最多,新产生的酮类、酯类和烯类物质,其中JM与J风味轮廓最为相似,鱼腥味成分含量最低,酮香味成分含量最高、风味最好。
综上所述,菌酶联合跟单菌、单酶处理相比,风味改善的同时多肽含量增加,更适合降解刺参体壁,其中JM处理方式对风味的改善效果最为明显。可作为一种新的技术对刺参体壁进行降解,也为将来刺参肽功能食品、配方食品的开发和应用提供了一定参考。
-
表 1 不同菌种的发酵条件
Table 1 Fermentation conditions of different strains
菌种种类 pH 温度(℃) 时间(h) 枯草芽孢杆菌 7.0 37 48 植物乳杆菌 6.8 37 48 肠膜明串珠菌 7.0 37 48 解淀粉芽孢杆菌 7.2 30 48 鲁氏酵母 7.0 28 48 表 2 不同酶制剂的酶解条件
Table 2 Enzymatic hydrolysis conditions of different enzyme preparations
蛋白酶种类 pH 温度(℃) 时间(h) 风味蛋白酶 7.5 50 4 复合蛋白酶 6.0 50 4 木瓜蛋白酶 6.5 55 4 碱性蛋白酶 8.0 50 4 表 3 感官评分标准
Table 3 Sensory rating criteria
项目 评分标准 1~2分 3~5分 6~8分 9~10分 腥味(30分) 腥味较重 腥味中等 腥味较淡 基本无腥味 气味(30分) 发酵味、酸味过重并伴随一定的异味 具有刺参固有的气味,无不良气味 具有刺参固有的气味,发酵产生的鲜香味 具有刺参固有的气味,令人愉悦的果香味和清爽的酸味 滋味(40分) 口感较差,过苦、过咸、有异味 口感一般,偏苦、偏咸 口感适宜,微甜、微咸 口感柔和,酸甜适宜、鲜香可口 表 4 不同处理方式降解液的多肽相对分子质量分布
Table 4 Relative molecular mass distribution of peptides in degradation solution with different treatment methods
相对分子质量(Da) J(%) M(%) JM(%) MJ(%) T(%) >3000 5.921 0.051 0.109 0.091 0 2000~3000 8.885 0.813 1.175 1.297 0.11 1000~2000 19.445 9.575 10.324 9.919 3.592 500~1000 21.956 28.908 25.555 22.013 16.886 <500 43.794 60.653 62.837 66.680 79.412 表 5 不同处理方式降解液的氨基酸组成
Table 5 Amino acid composition of degradation solution by different treatment methods
序号 氨基酸 含量(g/100 g干重) Y J M JM MJ T 1 天门冬氨酸Asp 6.04±0.04ab 4.99±0.11d 6.37±0.11a 5.78±0.25bc 5.67±0.14c 5.10±0.11d 2 苏氨酸Thr 3.13±0.02b 2.23±0.08d 3.35±0.04a 2.56±0.11c 1.98±0.05e 1.59±0.03f 3 丝氨酸Ser 3.08±0.03a 2.19±0.04c 3.18±0.04a 2.55±0.1b 2.20±0.05c 1.81±0.03d 4 谷氨酸Glu 9.82±0.11a 7.34±0.15c 10.01±0.15a 8.49±0.36b 7.35±0.17c 6.2±0.13d 5 甘氨酸Gly 10.32±0.14a 8.15±0.23d 9.65±0.18b 8.98±0.36c 8.6±0.17cd 7.43±0.16e 6 丙氨酸Ala 4.39±0.04a 2.98±0.03c 4.29±0.09a 3.48±0.14b 2.77±0.07d 2.22±0.05e 7 半胱氨酸Cys 1.39±0.09ab 1.50±0.18a 1.49±0.04ab 1.42±0.02ab 1.40±0.03ab 1.26±0.03b 8 缬氨酸Val 2.28±0.02b 1.84±0.03e 2.52±0.01a 2.14±0.06c 2.11±0.04c 1.97±0.05d 9 蛋氨酸Met 0.86±0.01bc 0.56±0.01cd 0.46±0.02d 0.98±0.28b 1.37±0.10a 1.11±0.14ab 10 异亮氨酸Ile 1.74±0.01b 1.23±0.04d 1.85±0.06a 1.45±0.05c 1.23±0.02d 1.19±0.03d 11 亮氨酸Leu 2.63±0.01b 2.04±0.01d 3.05±0.03a 2.45±0.10c 2.68±0.06b 2.57±0.05bc 12 酪氨酸Tyr 2.01±0.02bc 1.91±0.07c 2.35±0.02a 2.27±0.04ab 2.12±0.16abc 2.01±0.23bc 13 苯丙氨酸Phe 1.45±0.01c 1.41±0.03c 1.75±0.04ab 1.72±0.07b 1.82±0.01a 1.73±0.04ab 14 赖氨酸Lys 1.88±0.01c 1.80±0c 2.25±0.04a 2.16±0.08ab 2.19±0.03ab 2.12±0.05b 15 脯氨酸Pro 4.87±0.05a 3.77±0.05c 4.74±0.05a 4.27±0.13b 3.78±0.08c 3.29±0.08d 16 组氨酸His 0.60±0b 0.46±0.01c 0.74±0.01a 0.55±0.04b 0.41±0.04c 0.44±0.02c 17 精氨酸Arg 4.74±0.08a 3.07±0.07c 4.58±0.08a 3.54±0.18b 2.74±0.04d 2.12±0.04e 18 TAA 61.22±0.59a 47.48±0.92d 62.61±0.8a 54.78±1.77b 50.43±0.83c 44.19±0.93e 19 DAA 15.86±0.18a 12.33±0.32c 16.38±0.32a 14.27±0.76b 13.02±0.37c 11.30±0.29d 20 SAA 25.79±0.35a 19.33±0.55c 25.2±0.49a 21.84±1.03b 19.33±0.51c 16.35±0.43d 21 BAA 18.18±0.07b 14.33±0.03f 19.55±0.18a 17.25±0.34c 16.68±0.08d 15.28±0.38e 22 DAA+SAA 41.65±0.53a 31.65±0.87c 41.58±0.81a 36.11±1.78b 32.35±0.89c 27.65±0.72d 23 (DAA+SAA)/TAA 0.68±0a 0.67±0b 0.66±0b 0.66±0.01b 0.64±0c 0.63±0d 24 BAA/TAA 0.30±0d 0.30±0.01cd 0.31±0c 0.32±0c 0.33±0b 0.35±0a 注:TAA为总氨基酸;DAA为鲜味氨基酸(谷氨酸、天冬氨酸);SAA为甜味氨基酸(甘氨酸、丙氨酸、丝氨酸、脯氨酸、苏氨酸);BAA为苦味氨基酸(酪氨酸、苯丙氨酸、缬氨酸、组氨酸、异亮氨酸、亮氨酸、赖氨酸、精氨酸、甲硫氨酸);同行不同小写字母表示不同处理组差异显著(P<0.05)。 表 6 不同处理方式降解液的核苷酸含量
Table 6 Nucleotide content of degradation solution by different treatment methods
不同处理
方式鲜味物质含量(mg/100 g) 5’-AMP
(腺苷酸)5’-GMP
(鸟苷酸)5’-IMP
(肌苷酸)风味核苷酸 Y 0.43±0.00e − − 0.43±0.00e J 2.17±0.06c 11.33±0.78b − 13.50±0.84c M 0.76±0.00d − − 0.76±0.00d JM 2.45±0.07a 11.31±0.78b − 13.76±0.85c MJ 2.29±0.04b 32.90±1.36a − 35.19±1.4b T 2.20±0.02bc 36.39±2.31a − 38.59±2.33a 注:−表示未检出;风味核苷酸为5’-GMP、5’-IMP和5’-AMP之和;同列小写字母不同表示不同处理组差异显著(P<0.05)。 -
[1] PANGESTUTI R, ARIFIN Z. Medicinal and health benefit effects of functional sea cucumbers[J]. Journal of Traditional and Complementary Medicine,2018,8(3):341−351. doi: 10.1016/j.jtcme.2017.06.007
[2] TINGTING W, LIN Z, TIANTIAN Z, et al. Anti-diabetic effects of sea cucumber (Holothuria nobilis) hydrolysates in streptozotocin and high-fat-diet induced diabetic rats via activating the PI3K/Akt pathway[J]. Journal of Functional Foods,2020,75:104224−104224. doi: 10.1016/j.jff.2020.104224
[3] JANAKIRAM N B, MOHAMMED A, RAO C V. Sea cucumbers metabolites as potent anti-cancer agents[J]. Marine Drugs,2015,13(5):2909−2923. doi: 10.3390/md13052909
[4] 林凯, 韩雪, 张兰威, 等. ACE抑制肽构效关系及其酶法制备的研究进展[J]. 食品科学,2017,38(3):261−270. [LIN K, HAN X, ZHANG L W, et al. Progress in structure-activity relationship and enzymatic preparation of ACE inhibitory peptides[J]. Food Science,2017,38(3):261−270. [5] CHAI K F, VOO A Y H, CHEN W N. Bioactive peptides from food fermentation: A comprehensive review of their sources, bioactivities, applications, and future development[J]. Comprehensive Reviews in Food Science and Food Safety,2020,19(6):3825−3885. doi: 10.1111/1541-4337.12651
[6] 梁丽芬, 叶泉清, 陈静, 等. 菌酶协同发酵生产蛋白饲料的研究进展及应用[J]. 饲料研究,2021,44(2):129−131. [LIANG L F, YE Q Q, CHEN J, et al. Research progress and application of bacterial enzyme co-fermentation in protein feed production[J]. Feed Research,2021,44(2):129−131. doi: 10.13557/j.cnki.issn1002-2813.2021.02.030 [7] 王安凤. 合浦珠母贝肉调味料的制备及风味研究[D]. 上海: 上海海洋大学, 2017. WANG A F. Study on preparation and flavor improvement of seasoning derived from Pinctada fucata muscle[D]. Shanghai: Shanghai Ocean University, 2017.
[8] 汪韬, 温运启, 于娇, 等. 富含乳酸菌的脱腥海参肽粉的制备[J]. 食品与发酵工业,2020,46(18):187−191. [WANG T, WEN Y Q, YU J, et al. Preparation of deodorized sea cucumber peptide powder rich in lactic acid bacteria[J]. Food and Fermentation Industries,2020,46(18):187−191. doi: 10.13995/j.cnki.11-1802/ts.023819 [9] 闫泽文. 不同菌种发酵对海参内脏酶解液风味的影响及抗肿瘤活性研究[D]. 烟台: 烟台大学, 2021. YAN Z W, Effects of different strains fermentation on flavor and antitumor activity of enzymatic hydrolysate of sea cucumber viscera[D]. Yantai: Yantai University, 2021.
[10] 王共明. 仿刺参卵多肽、多糖的制备及多肽活性研究[D]. 上海: 上海海洋大学, 2013. WANG G M. Preparation of peptide and polysaccharide and activity research of Apostichopus japonicus Spawn peptide[D]. Shanghai: Shanghai Ocean University, 2013.
[11] 井月欣, 乔瑞光, 张健, 等. 响应面试验优化盐渍仿刺参脱盐工艺[J]. 食品工业科技,2017,38(18):160−164, 172. [JING Y X, QIAO R G, ZHANG J, et al. Optimization of desalting process of salted Apostichopus japonicus by response surface methodology[J]. Science and Technology of Food Industry,2017,38(18):160−164, 172. doi: 10.13386/j.issn1002-0306.2017.18.031 [12] 王婷, 温子健, 季晓彤, 等. 海参卵纳豆菌发酵条件及产物生物活性[J]. 食品科学,2017,38(8):43−48. [WANG T, WEN Z J, JI X T, et al. Investigation of fermentation conditions for fibrinolysin production from sea cucumber ovum by Bacillus natto and bioactive activity of the fermentation product[J]. Food Science,2017,38(8):43−48. doi: 10.7506/spkx1002-6630-201708008 [13] 鲁伟, 任国谱, 宋俊梅. 蛋白水解液中多肽含量的测定方法[J]. 食品科学,2005(7):169−171. [LU W, REN G P, SONG J M. Determination of content of peptides in protein hydrolysates[J]. Food Science,2005(7):169−171. doi: 10.3321/j.issn:1002-6630.2005.07.039 [14] 张倩, 刘睿, 王欣之, 等. 高效液相色谱法测定四角蛤蜊、菲律宾蛤仔中呈味核苷酸[J]. 食品与发酵工业,2017,43(3):224−228. [ZHANG Q, LIU R, WANG X Z et al. Determination of flavor nucleotides in Mactra veneriformis and Ruditapes philippinarum by high performance liquid chromatography[J]. Food and Fermentation Industries,2017,43(3):224−228. doi: 10.13995/j.cnki.11-1802/ts.201703039 [15] LI X, DONG Y, JIANG P, et al. Identification of changes in volatile compounds in sea cucumber Apostichopus japonicus during seasonings soaking using HS-GC-IMS[J]. LWT-Food Science and Technology, 2022, 154.
[16] 王田田, 汪腾蛟, SAYTHON, 等. 菌、酶协同发酵对辣木茎叶粉的营养价值及抗氧化活性的影响[J]. 黑龙江畜牧兽医,2020(12):117−121. [WANG T T, WANG T J, SAYTHON, et al. The effect of nutritional value and antioxidant activity of Moringa oleifera Lam stem and leaf powder by cooperative fermentation of bacteria and enzymes doi: 10.13881/j.cnki.hljxmsy.2019.12.0100 J]. Heilongjiang Animal Science and Veterinary Medicine,2020(12):117−121. doi: 10.13881/j.cnki.hljxmsy.2019.12.0100
[17] 赵彦珺. 基于气相离子迁移谱研究酶解及发酵对海参肠卵挥发性物质的影响[D]. 烟台: 烟台大学, 2020. ZHAO Y J. The effect of enzymolysis and fermentation on the volatile compounds in the intestines and gonads of sea cucumber using headspace-gas chromatography-ion mobility spectroscopy (HS-GC-IMS)[D]. Yantai: Yantai University, 2020.
[18] 张涵. 海参及其发酵制品风味构成研究[D]. 大连: 大连工业大学, 2017. ZHANG H. Characterization of flavor composition in sea cucumber and fermented products[D]. Dalian: Dalian Polytechnic University, 2017.
[19] 李学鹏, 王祺, 励建荣, 等. 海参酶解液的体外抗氧化活性研究[J]. 食品工业科技,2014,35(24):100−103. [LI X P, WANG Q, LI J R, et al. Study on the in vitro inoxidizability of enzymatic hydrolysates from sea cucumber (Stichopus japonicus)[J]. Science and Technology of Food Industry,2014,35(24):100−103. doi: 10.13386/j.issn1002-0306.2014.24.012 [20] 周逢芳, 蔡彬新, 巫鑫睿, 等. 海参体壁蛋白ACE抑制肽酶解工艺及产物分子量分布研究[J]. 食品工业科技,2017,38(17):163−167, 173. [ZHOU P F, CAI B X, WU X R, et al. Study on hydrolysis condition and molecular weight distribution of ACE inhibitory peptide derived from sea cucumber protein[J]. Science and Technology of Food Industry,2017,38(17):163−167, 173. doi: 10.13386/j.issn1002-0306.2017.17.031 [21] 李学鹏, 刘晏玮, 谢晓霞, 等. 热预处理对蓝蛤酶解及酶解液呈味特性的影响[J]. 食品科学,2020,41(2):133−140. [LI X P, LIU Y W, XIE X X, et al. Effect of thermal pretreatment on enzymatic hydrolysis of clam (Aloididae aloidi) and flavor characteristics of hydrolysates[J]. Food Science,2020,41(2):133−140. doi: 10.7506/spkx1002-6630-20181206-086 [22] 徐永霞, 曲诗瑶, 李涛, 等. 不同蛋白酶对蓝蛤酶解液风味特性的影响[J]. 食品科学,2021,42(4):190−196. [XU Y X, QU S Y, LI T, et al. Effects of different proteases on the flavor characteristics of Aloididae aloidi muscle hydrolysates[J]. Food Science,2021,42(4):190−196. doi: 10.7506/spkx1002-6630-20190823-248 [23] 吴红洋, 姜太玲, 胡惠茗, 等. 响应面法优化酶解花椒籽蛋白制备降血压肽工艺[J]. 食品科学,2014,35(21):180−185. [WU H Y, JIANG T L, HU H M, et al. Response surface methodology for optimization of hydrolysis conditions for preparing antihypertensive peptides sichuan pepper (Zanthoxylum bungeanum) seed protein[J]. Food Science,2014,35(21):180−185. doi: 10.7506/spkx1002-6630-201421035 [24] WANG Y, TANG X, LUAN J, et al. Effects of ultrasound pretreatment at different powers on flavor characteristics of enzymatic hydrolysates of cod (Gadus macrocephalus) head[J]. Food Research International (Ottawa, Ont),2022,159:111612−111612. doi: 10.1016/j.foodres.2022.111612
[25] 于芳珠, 薄存美, 刘登勇. 食品中鲜味物质研究进展[J]. 食品安全质量检测学报,2020,11(16):5554−5561. [YU F Z, BO C M, LIU D Y. Research progress of umami substances in food[J]. Journal of Food Safety and Quality,2020,11(16):5554−5561. doi: 10.19812/j.cnki.jfsq11-5956/ts.2020.16.037 [26] 刘倩. 毛霉蛋白酶水解制备大豆鲜味肽的研究[D]. 广州: 华南理工大学, 2020. LIU Q. The study of extracting soybean umami peptides by mucro protease[D]. Guangzhou: South China Universityo of Technology. 2020.
[27] LIU M Y, TANG H C, HU S H, et al. Peptide-based enteral formula improves tolerance and clinical outcomes in abdominal surgery patients relative to a whole protein enteral formula[J]. World Journal of Gastrointestinal Surgery,2016,8(10):700−705. doi: 10.4240/wjgs.v8.i10.700
[28] 张健, 王茂剑, 马晶晶, 等. 仿刺参生殖腺营养成分分析[J]. 食品科学,2013,34(14):232−236. [ZHANG J, WANG M J, MA J J, et al. Nutrient composition of Apostichopus japonicas gonad[J]. Food Science,2013,34(14):232−236. doi: 10.7506/spkx1002-6630-201314047 [29] 李雪, 冯涛, 宋诗清, 等. 不同处理方法对蟹味菇呈味物质释放的影响[J]. 食品科学,2020,41(10):198−205. [LI X, FENG T, SONG S Q, et al. Effect of different pretreatment methods on the release of flavor substances from Hypsizygus marmoreus[J]. Food Science,2020,41(10):198−205. doi: 10.7506/spkx1002-6630-20190611-121 [30] 孟凌玉. 虾头酶解产物微生物混合发酵工艺及其风味成分的变化[D]. 湛江: 广东海洋大学, 2013. MENG L Y, Fermentation technology and flavor changes of shrimp head enzymatic hydrolysate with mixed starter cultures[D]. Zhanjiang: Guangdong Ocean University. 2013.
[31] 蔡路昀, 王亚茹, 王静, 等. 水产品中ATP及其关联化合物研究进展[J]. 食品工业科技,2019,40(7):278−284. [CAI L Y, WANG Y R, WANG J, et al. Research progress of ATP and Its related compounds in aquatic products[J]. Science and Technology of Food Industry,2019,40(7):278−284. doi: 10.13386/j.issn1002-0306.2019.07.048 [32] 谷镇. 食用菌呈香呈味物质分析及制备工艺研究[D]. 上海: 上海师范大学, 2012. GU Z. Study on the determination of flavor substances and preparation technology[D]. Shanghai: Shanghai Normal University, 2012.
[33] ZHANG H, GENG Y F, QIN L, et al. Characterization of volatile compounds in different dried sea cucumber cultivars[J]. Journal of Food Measurement and Characterization,2018,12(3):1439−1448. doi: 10.1007/s11694-018-9759-7
[34] 邵悦春, 付晓婷, 许加超, 等. 基于气相离子迁移谱的发酵海带风味分析[J]. 食品工业科技,2021,42(12):300−306. [SHAO Y C, FU X T, XU J C, et al. Flavor analysis of fermented Laminaria japonica based on gas chromatograph-ion mobility spectrometer (GC-IMS)[J]. Science and Technology of Food Industry,2021,42(12):300−306. doi: 10.13386/j.issn1002-0306.2020090210 [35] 阮秋凤, 安玥琦, 陈周, 等. 短时间微流水处理对草鱼鱼肉风味品质的影响[J]. 食品科学技术学报,2021,39(3):30−42, 51. [RUAN Q F, AN Y Q, CHEN Z, et al. Effect of short-time micro-flow water treatment on flavor quality of grass carp fish meat[J]. Journal of Food Science and Technology,2021,39(3):30−42, 51. doi: 10.12301/j.issn.2095-6002.2021.03.004 [36] LI X, WANG K, YANG R, et al. Mechanism of aroma compounds changes from sea cucumber peptide powders (SCPPs) under different storage conditions[J]. Food Research International, 2020, 128.
[37] 律诗, 代晹鑫, 刘野, 等. 食用菌鲜味强度评价及鲜味氨基酸和核苷酸提取工艺优化[J]. 食品科学技术学报,2022,40(1):100−108. [LU S, DAI Y X, LIU Y, et al. Evaluation of umami intensity of edible fungi and optimization of umami amino acid and nucleotide extraction[J]. Journal of Food Science and Technology,2022,40(1):100−108. doi: 10.12301/spxb202100376 [38] LI M, YANG R, ZHANG H, et al. Development of a flavor fingerprint by HS-GC-IMS with PCA for volatile compounds of Tricholoma matsutake Singer[J]. Food Chemistry,2019,290:32−39. doi: 10.1016/j.foodchem.2019.03.124
[39] ZHANG Q, DING Y, GU S, et al. Identification of changes in volatile compounds in dry-cured fish during storage using HS-GC-IMS[J]. Food Research International, 2020, 137.





 下载:
下载:
 下载:
下载:



