Bioinformatics Analysis and Gene Cloning of L-Lactate Dehydrogenase from Lactobacillus rhamnosus
-
摘要: 本研究以鼠李糖乳杆菌(Lactobacillus rhamnosus)L-乳酸脱氢酶(Lr-L-LDH)为研究对象,以研究较多的Lr-L-LDH1为对照,对基因组注释的两个Lr-L-LDH1和Lr-L-LDH2基因,进行异同分析。采用在线网站和专业软件对Lr-L-LDH1和Lr-L-LDH2的一级结构、基本特性、亲疏水性、二级结构进行分析和预测,对三级结构进行同源建模以及酶和底物的分子对接分析,并对酶的编码基因进行系统发育分析,克隆表达及酶活性检测。结果显示:相较于Lr-L-LDH1,Lr-L-LDH2有着相似的分子特性,二级和三级结构,但Lr-L-LDH2编码序列短,氨基酸序列同源性低(48.08%),有不同的进化地位;Lr-L-LDH2也含有乳酸脱氢酶催化活性位点序列和保守的NAD+结合位点序列(GXGXXG),能够形成典型的活性三维口袋域,是NAD+依赖型四聚体结构L-乳酸脱氢酶,在细胞中需要果糖1,6-二磷酸(FBP)来激活,催化丙酮酸还原为L-乳酸;体外克隆表达和酶学分析表明,Lr-L-LDH2酶活力极显著低于Lr-L-LDH1(P<0.01)。Lr-L-LDH1和Lr-L-LDH2都具有乳酸脱氢酶活性,推测二者在乳酸表达调控中相互作用,对鼠李糖乳杆菌L-乳酸脱氢酶的分子改造应同时考虑Lr-L-LDH1和Lr-L-LDH2的作用,研究对乳酸发酵工业的基因工程改造提供分子基础和科学依据。Abstract: In this study, L-lactate dehydrogenase (Lr-L-LDH) from Lactobacillus rhamnosus was investigated. The well-known Lr-L-LDH1 was taken as the control, differences between Lr-L-LDH1 and Lr-L-LDH2 annotated from the genome of L. rhamnosus were analyzed. The primary structure, basic properties, hydrophobicity, secondary structure of Lr-L-LDH1 and Lr-L-LDH2 were predicted and analyzed using online websites and professional software. Homology modeling of the tertiary structure, molecular docking of enzymes and substrates, phylogenetic analysis, in vitro cloning, expression, and enzyme activity assays were further studied. The results showed that, in comparison to Lr-L-LDH1, although Lr-L-LHD2 had similar molecular characteristics, secondary and tertiary structures, Lr-L-LHD2 exhibited differences: A shorter sequences, low amino acid identities (48.08%), and a different phylogenetic status. Lr-L-LHD2 also contained a catalytically active site, a highly conserved NAD+ binding site sequence (GXGXXG), a three-dimensional active pocket domain, was an NAD+ dependent tetrameric L-lactate dehydrogenase, and be activated by fructose 1,6-diphosphate in the cytoplasm for catalyzing the reduction of pyruvate to L-lactic acid. In vitro enzyme activity was significantly lower than Lr-L-LDH1 (P<0.01). In conclusion, both Lr-L-LDH1 and Lr-L-LHD2 showed enzyme activities of L-lactate dehydrogenase, indicating they may regulate the L-lactate metabolism pathway together. Considerations of both Lr-L-LDH1 and Lr-L-LHD2 should be taken for the future molecular modifications of L-LDH in L. rhamnosus, and the study provided the molecular and scientific basis for the gene engineering modifications of lactic acid fermentation industry.
-
L-乳酸是世界三大重要有机酸之一,被广泛应用于食品、医药、化妆品和农业等领域,以其为原料聚合成的聚乳酸(Polylactic acid, PLA)是国家重点支持的战略性生物降解和环境友好新材料,可替代石化基材料,消除环境“白色污染”[1-4]。目前乳酸的生产合成主要通过化学合成法、酶合成法和微生物发酵法等,其中微生物发酵法以来源丰富的生物资源为原料,其生产过程安全可靠,反应条件温和,能耗小,成本较低,且产品乳酸的光学纯度高,是乳酸生产行业主要的生产方法[5]。微生物菌种是发酵产业的核心,合成L-乳酸的乳酸菌大致分布在乳杆菌属、链球菌属、肠球菌属和片球菌属等[6-7],乳酸脱氢酶(Lactate dehydrogenase,LDH)是微生物乳酸合成代谢途径中催化丙酮酸转化生成乳酸的关键酶,微生物中的L-乳酸脱氢酶(L-lactate dehydrogenase,L-LDH,EC 1.1.1.27)是脱氢酶中十分重要且研究较多的一种酶[2,5,8-10]。乳酸脱氢酶是同源四聚体结构,含有4个相同的亚基,每个亚基均具有相对独立的催化功能,以丙酮酸为底物时,乳酸脱氢酶先结合辅酶NADH,再与丙酮酸结合,丙酮酸接受NADH提供的[H],发生氧化反应,生成乳酸和NAD+[11]。
在乳酸的微生物发酵法生产中,针对微生物的丙酮酸代谢通路进行改造,利用基因工程技术敲除丙氨酸脱氢酶基因或过量表达L-乳酸脱氢酶基因,以增强乳酸菌体内原有的L-乳酸合成代谢途径,并使所得菌株能够保持性状的稳定遗传,可以进行高产量和高纯度的L-乳酸生产[5,12-13],这是乳酸发酵工业化生产的保障。目前对于L-乳酸脱氢酶的研究,较多的是针对编码L-LDH1的L-ldh1基因的克隆表达和酶学分析,其目的是进行基因工程改造以增强L-乳酸的发酵表达[14-16]。乳酸菌基因组中一般存在两个L-乳酸脱氢酶基因:L-ldh1和L-ldh2,有研究推测L-ldh1和L-ldh2在细胞内乳酸(L-乳酸、D-乳酸)的表达调控中存在相互作用关系[17],但关于L-ldh2编码的L-LDH2的研究,以及针对L-LDH1和L-LDH2二者之间的比较研究较少,这种情况不利于乳酸菌L-乳酸发酵的基因工程改造。鼠李糖乳杆菌(Lactobacillus rhamnosus)是一类重要的L-乳酸生产菌株[4,18-19],本研究以鼠李糖乳杆菌Lactobacillus rhamnosus ATCC 11443菌株为研究对象,以其全基因组信息为参考,从核酸和蛋白质序列出发,对其L-LDH1和L-LDH2进行生物信息学分析和克隆表达分析,探讨两个酶的进化、性质、结构和生物学功能异同,以期为乳酸菌L-LDH的分子改造,基因工程菌株构建和L-乳酸发酵表达优化提供参考。
1. 材料与方法
1.1 材料与仪器
鼠李糖乳杆菌L. rhamnosus ATCC 11443(JCM 1553) 购自日本微生物保藏中心(JCM),现保藏于本实验室,该菌株的全基因组序列信息,以及相关菌株的L-乳酸脱氢酶基因序列信息从NCBI数据库中获取;菌株E. coli-Top10、E. coli-BL21(DE3)、pET-28a(+)质粒 由本实验室保藏;pMD18-T克隆质粒 购自TaKaRa公司;Taq DNA聚合酶、BamH I和Xho I限制性内切酶、T4 DNA连接酶、DNA Marker、Protein Marker 购自宝日医生物技术(北京)有限公司;DNA胶回收试剂盒、PCR产物纯化试剂盒、质粒提取试剂盒 购自天根生化科技(北京)有限公司;氨苄青霉素、卡那霉素、丙酮酸钠、异丙基-β-D-硫代半乳糖苷(Isopropyl-beta-D-thiogalactopyranoside,IPTG)、5-溴-4-氯-3-吲哚基-β-D-半乳糖苷(5-Bromo-4-chloro-3-indolyl-β-D-galactopyranoside,X-gal)、还原态烟酰胺腺嘌呤二核苷酸(Nicotinamide adenine dinucleotide,NADH) 购自生工生物工程(上海)股份有限公司;引物合成 由生工生物工程(上海)股份有限公司完成。
鼠李糖乳杆菌的培养采用MRS培养基:酵母提取物5 g/L、蛋白胨10 g/L、牛肉膏10 g/L、葡萄糖20 g/L、硫酸锰0.056 g/L、乙酸钠5 g/L、硫酸镁0.2 g/L、磷酸氢二钾2.62 g/L、柠檬酸二铵2 g/L、吐温80 1 mL,调pH至6.2。大肠杆菌的培养采用LB培养基:酵母提取物5 g/L、蛋白胨10 g/L、NaCl 10 g/L,调pH至7.4。
T100™ PCR扩增仪、PowerPac™通用电泳仪、MicroPulser电穿孔仪、ChemiDoc XRS+ System凝胶成像系统 美国Bio-Rad公司;MIKRO 200R高速冷冻离心机 德国Hettich公司;HVA-85高压蒸汽灭菌器 日本Hirayama公司;L6S紫外可见分光光度计 上海精密科学仪器有限公司;TS-120C卧式恒温振荡器 上海天呈实验仪器制造有限公司;SBA-40C型葡萄糖-乳酸生物传感分析仪 山东省科学院生物研究所。
1.2 实验方法
1.2.1 基因的系统进化分析
系统进化分析先用MAFFT程序对基因序列进行多重比对,将序列比对结果导入j ModelTest程序用于筛选核苷酸替代矩阵,再用PhyML程序生成ML(Maximum likelihood)最大似然树[20-22]。
1.2.2 酶的基本性质分析
鼠李糖乳杆菌L-乳酸脱氢酶的氨基酸序列同源性用Geneious软件进行分析,其蛋白质的理化性质用ExPASy-PortParam tool(http://web.expasy.org/protparam/)进行分析预测,功能位点和结构域用PROSITE(http://prosite.expasy.org)进行分析预测,跨膜区用TMHMM Server v. 2.0(https://services.healthtech.dtu.dk/service.php?TMHMM-2.0)进行分析预测,亲、疏水性用PortScale(http://web.expasy.org/protscale/)进行分析预测,信号肽用SignalP 5.0 Server(https://services.healthtech.dtu.dk/service.php?SignalP-5.0)进行分析预测。
1.2.3 二级结构预测、三维结构分析和分子对接分析
鼠李糖乳杆菌L-乳酸脱氢酶二级结构用SOPMA(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl?page=/NPSA/npsa_sopma.html)进行分析预测,三维结构用SWISS-MODEL(https://www.swissmodel.expasy.org)进行同源建模,酶与底物的分子对接用DISCOVERY STUDIO 2019软件进行分析预测。
1.2.4 L-乳酸脱氢酶基因的扩增
根据菌株基因组中L-乳酸脱氢酶基因序列设计特异引物,分别在上下游引物引入BamH I和Xho I酶切位点,引物如表1所示。PCR扩增目的基因。PCR反应程序:94 °C预变性反应5 min;94 °C变性反应30 s,56 °C退火反应30 s,72 °C延伸反应1 min,执行30次循环;72 ℃后延伸反应10 min。
表 1 本研究使用的引物Table 1. Primer used in this study引物 引物序列(5'-3') 用途 ldhL1-F CATGGATCCATGCACATAAGAAAGGATGAT 扩增Lr-L-ldh1基因 ldhL1-R GCACTCGAGTTACTGACGTGTTTCGATGTC 扩增Lr-L-ldh1基因 ldhL2-F CATGGATCCATGCAACATAGCGGAAATATT 扩增Lr-L-ldh2基因 ldhL2-R GCACTCGAGCTAGGCTTCCTGTGCCTTCTT 扩增Lr-L-ldh2基因 PCR产物按试剂盒操作说明纯化回收,用BamH I和Xho I限制性内切酶酶切,然后与同样双酶切处理的克隆载体pMD18-T用T4 DNA连接酶连接,连接产物经纯化后电转化E. coli-Top10感受态细胞,经过X-gal蓝白筛选,挑取白色菌落进行PCR验证和酶切验证,将验证正确的重组中间质粒送生工生物工程(上海)股份有限公司进行测序。
1.2.5 L-乳酸脱氢酶基因表达菌株的构建
分别将测序正确的重组中间质粒和pET-28a(+)质粒用BamH I和Xho I双酶切,经纯化回收后,用T4 DNA连接酶将酶切的目的基因片段与酶切的pET-28a(+)质粒连接,连接产物纯化回收后电转化E. coli BL21(DE3)感受态细胞,挑取菌落进行PCR验证和BamH I和Xho I双酶切验证,筛选得到重组表达菌株,表达菌株经测序验证后用于表达实验。
1.2.6 L-乳酸脱氢酶测定
挑取重组表达菌单菌落接种于5 mL含卡那霉素(100 μg/mL)的LB培养基中,37 °C,220 r/min,过夜培养。按1%的接种量转接于100 mL含卡那霉素(100 μg/mL)LB培养基中,37 °C,220 r/min培养至OD600为0.8,加入终浓度为0.5 mmol/L的IPTG溶液,16 °C诱导6 h。8000 r/min、5 min离心收集菌体,SDS-PAGE分析和酶活性检测[14]。
L-乳酸脱氢酶的酶活性测定参照李建武等[23]的方法改良:将收集的菌体用磷酸钾缓冲液(K2HPO4-KH2PO4、50 mmol/L、pH7.0)洗涤2次,经超声破碎菌体细胞后,4 °C,12000 r/min,离心10 min后取上清液即为待测酶液。酶活检测总反应体系包括50 mmol/L K2HPO4-KH2PO4缓冲液(pH7.5)、0.2 mmol/L NADH、5 mmol/L丙酮酸钠,对照组中不含NADH,其他成分相同。混匀后于30 °C保温5 min,加入适量的待测酶液。检测NADH在340 nm处吸收值的变化。酶活力单位(U)定义为:在上述条件下,每分钟催化氧化1 μmol NADH所需要的酶量。比活性定义为每毫升酶蛋白所含的酶活单位数(U/mL)。
1.3 数据处理
DNA序列和氨基酸序列数据用Geneious 10软件预处理。每组试验重复三次,使用Microsoft Excel 2016软件进行数据处理,采用T检验对数据进行显著性差异分析,P<0.05有显著差异,P<0.01有极显著差异。
2. 结果与分析
2.1 L. rhamnosus ATCC 11443的L-乳酸脱氢酶基因系统进化分析
鼠李糖乳杆菌L. rhamnosus ATCC 11443基因组(GenBank:NZ_CP022109)中功能注释为L-乳酸脱氢酶(EC number: 1.1.1.27)的基因有两个:Lr-L-ldh1和Lr-L-ldh2。两个基因在基因组中方向相反,Lr-L-ldh1基因DNA序列定位于2583870-2584877,ORF全长1008 bp,编码蛋白质产物为L-乳酸脱氢酶Lr-L-LDH1;Lr-L-ldh2基因DNA序列定位于607880-606942,ORF全长939 bp,编码蛋白质产物为L-乳酸脱氢酶Lr-L-LDH2。
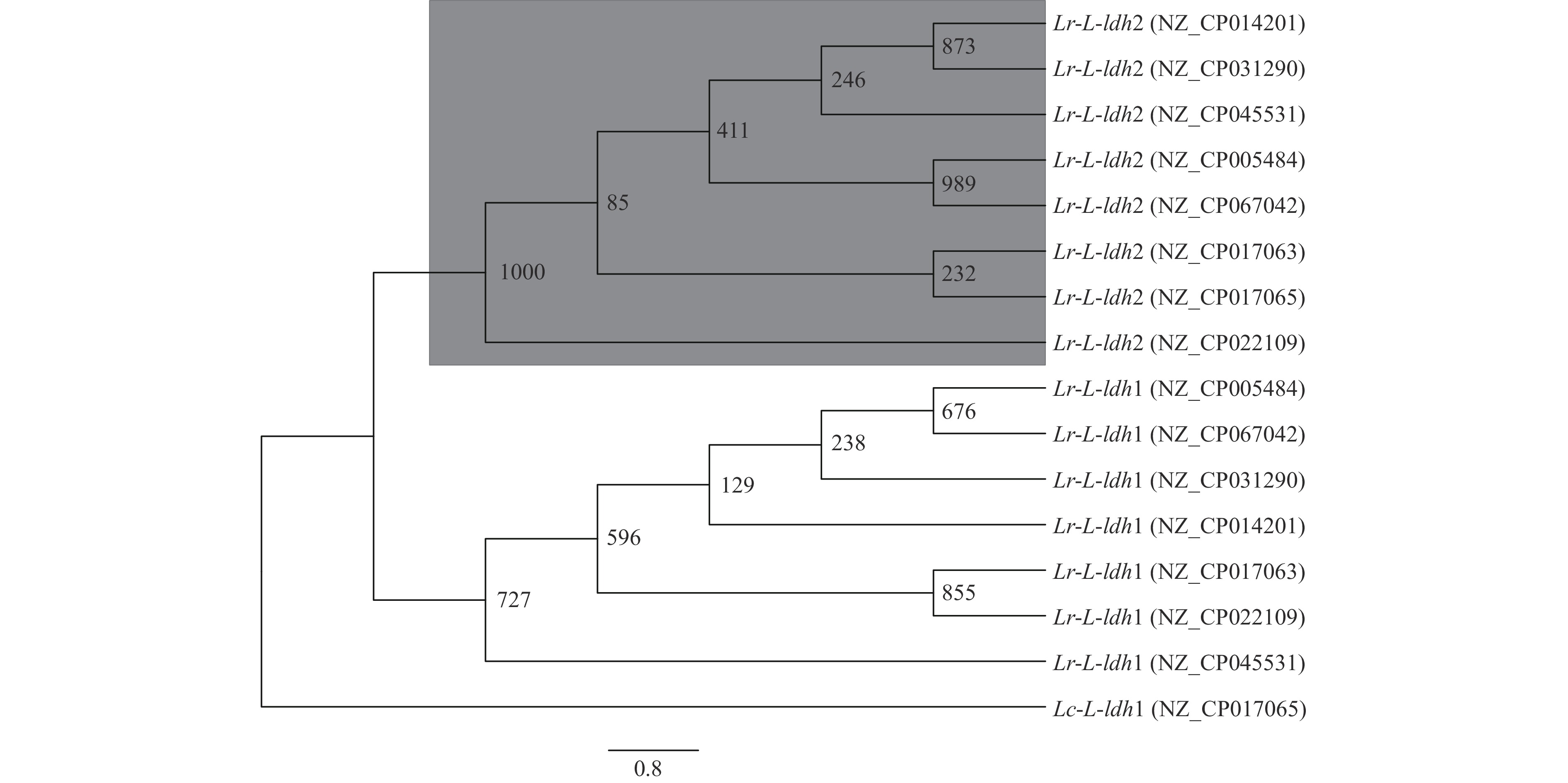
乳酸脱氢酶基因序列是一个研究物种进化的理想的分子指标[24-27]。以干酪乳杆菌(GenBank:NZ_CP017065)L-乳酸脱氢酶基因作为外类群,基于Lr-L-ldh1和Lr-L-ldh2的DNA序列进行系统进化分析,构建ML tree(Bootstrap values:1000),结果如图1所示,Lr-L-ldh1(NZ_CP022109)与不同来源的鼠李糖乳杆菌L-ldh1聚为一类,并与干酪乳杆菌的Lc-L-ldh1(NZ_CP017065)聚成一个分枝;Lr-L-ldh2(NZ_CP022109)与不同来源的鼠李糖乳杆菌L-ldh2聚为一类,并与干酪乳杆菌的Lc-L-ldh2(NZ_CP017065)聚成一个分枝。系统进化分析结果表明鼠李糖乳杆菌L. rhamnosus ATCC 11443基因组中的两个L-乳酸脱氢酶基因Lr-L-ldh1和Lr-L-ldh2分属不同的进化分枝,即Lr-L-LDH1和Lr-L-LDH2在进化中分别处于不同的地位。
2.2 Lr-L-LDH的基本性质分析
2.2.1 Lr-L-LDH理化性质分析
对Lr-L-LDH1和Lr-L-LDH2的基本理化特性,包括氨基酸残基数量、分子质量、等电点、带负电荷氨基酸、带正电荷氨基酸、分子式、原子总数、消光系数、不稳定指数、脂肪族指数和亲水性平均系数等进行分析,结果如表2所示,Lr-L-LDH1和Lr-L-LDH2的上述基本理化性质均存在差异。蛋白质的稳定性与二肽组成紧密相关,Lr-L-LDH1和Lr-L-LDH2的氨基酸序列同源性仅为48.08%,其氨基酸序列组成和数量的差异决定了二肽组成的差异,导致Lr-L-LDH1和Lr-L-LDH2的稳定性指数不同,但二者的不稳定指数均小于40,表明这两个蛋白质的结构是稳定的[28]。另外,不同氨基酸的解离系数存在差别,Lr-L-LDH1和Lr-L-LDH2的氨基酸组成不同,且带正、负电荷氨基酸总数也不相等,导致二者的等电点存在差别。上述分析对于Lr-L-LDH1和Lr-L-LDH2的分离纯化和催化特性研究具有一定的指导意义。
表 2 Lr-L-LDH基本性质分析Table 2. Analysis of the basic characteristics of the Lr-L-LDH基本性质 Lr-L-LDH1 Lr-L-LDH2 氨基酸残基数量 335 312 分子质量(Da) 36608.80 33557.10 等电点 5.34 5.12 带负电荷氨基酸(Asp+Glu) 45 39 带正电荷氨基酸(Arg+Lys) 36 28 分子式 C1639H2613N433O500S7 C1487H2377N407O461S7 原子总数 5192 4739 消光系数(mol/cm) 32890 26025 不稳定指数 30.10 37.35 脂肪族指数 99.88 104.17 亲水性平均系数 -0.096 -0.020 2.2.2 Lr-L-LDH的亲、疏水性分析
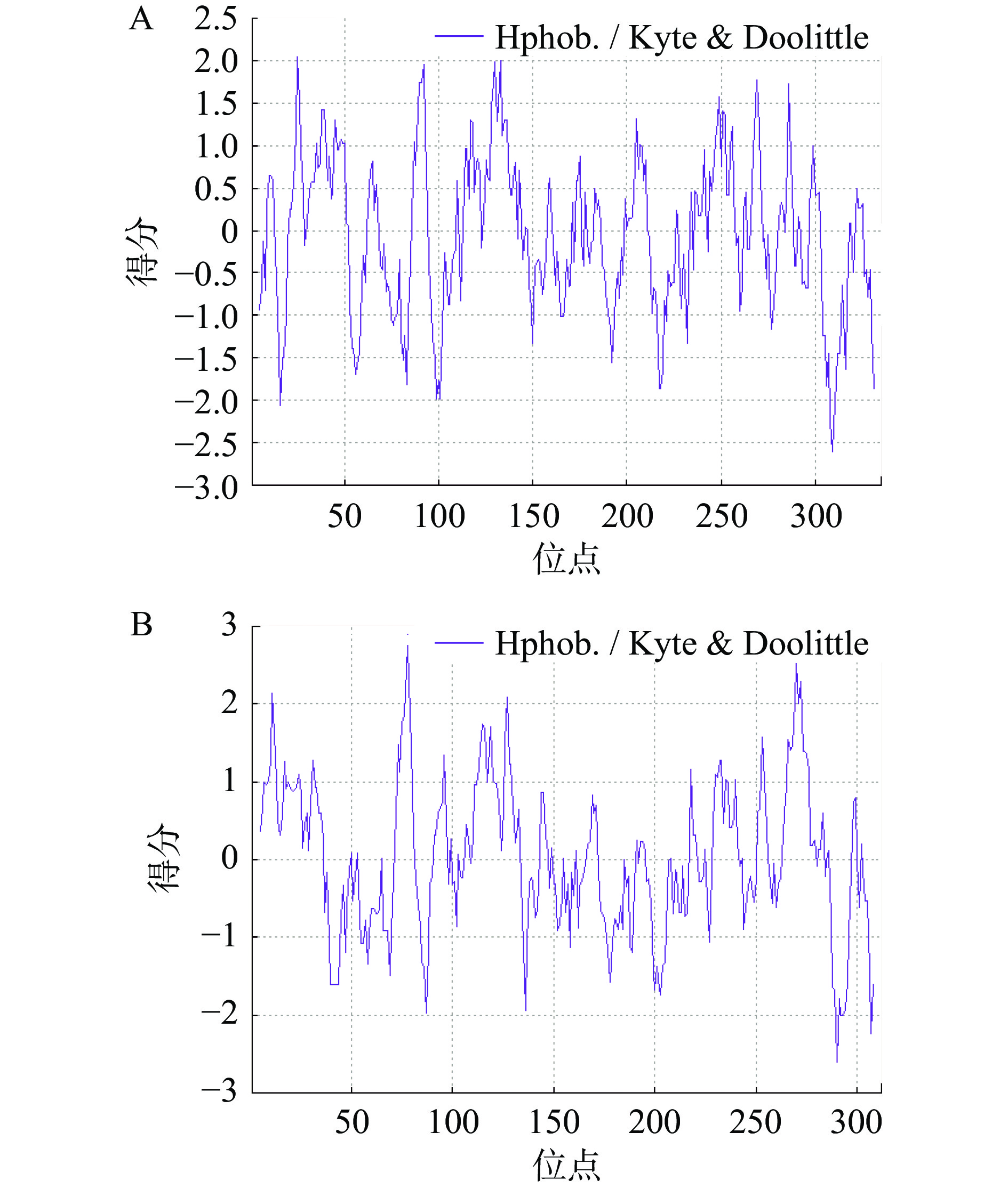
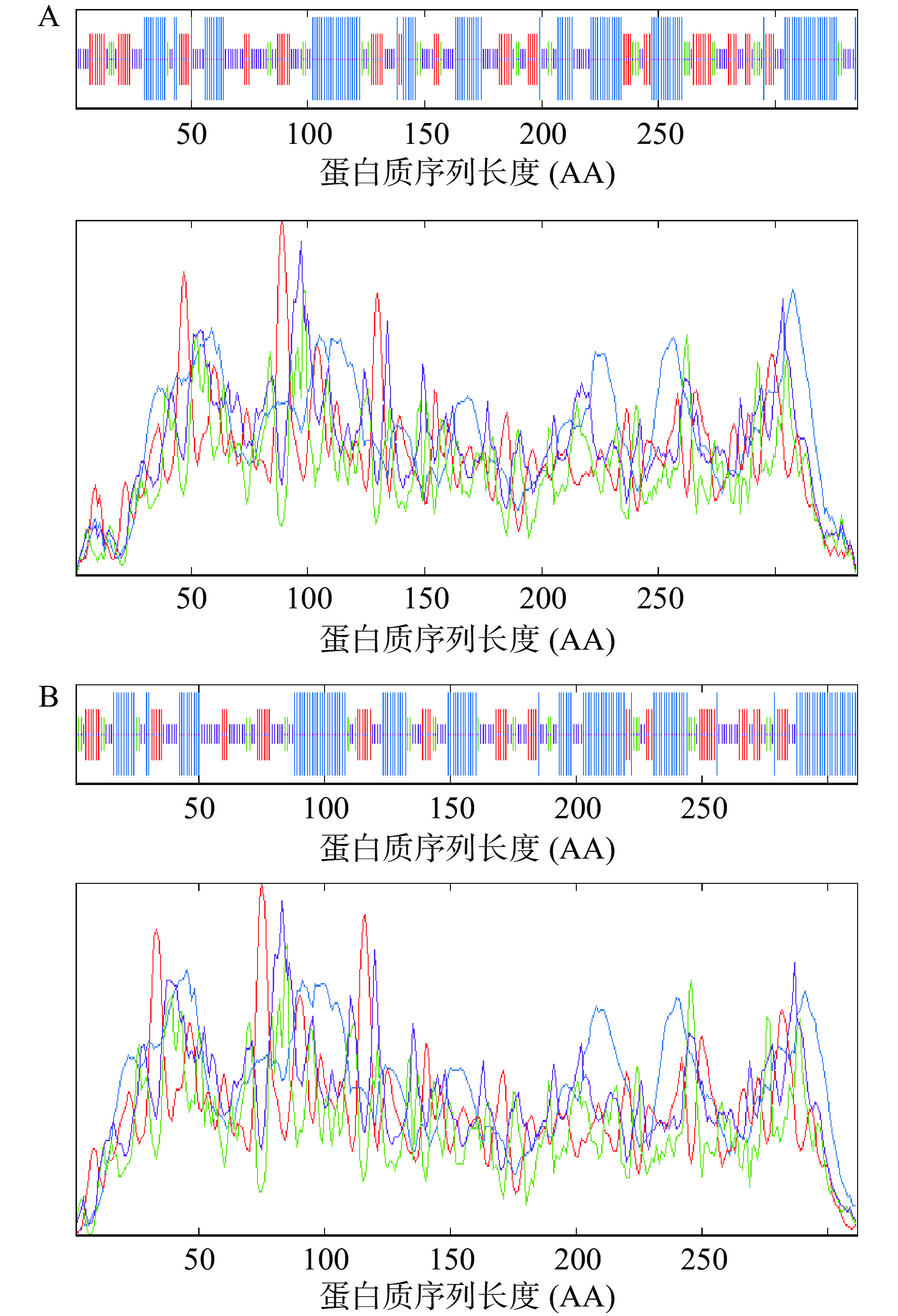
氨基酸的亲、疏水作用在很大程度上影响蛋白的稳定性,蛋白质的折叠主要由氨基酸的亲、疏水性驱动,因此氨基酸亲和疏水性分析对于通过定点突变或者区域的理性设计和改造,改善蛋白的稳定性具有重要指导作用。采用Hphob/Kyte & Doolittle算法计算Lr-L-LDH1和Lr-L-LDH1的亲、疏水性,结果如图2所示。特定位点的负值越大表示氨基酸亲水性越强,正值越大则表示疏水性越强[29]。Lr-L-LDH1的第309位谷氨酸残基亲、疏水指数最小为−2.611,亲水性最强,第25位甘氨酸残基亲、疏水指数最大为2.044,疏水性最强,亲水性平均系数(Grand average of hydropathicity,GRAVY)为−0.096(表2);Lr-L-LDH2的第290位谷氨酸残基亲、疏水指数最小为−2.600,亲水性最强,第78位苏氨酸残基亲、疏水指数最大为2.744,疏水性最强,GRAVY为−0.020(表2)。Lr-L-LDH1和Lr-L-LDH2在氨基酸残基亲、疏水性指数和亲水性平均系数均存在差异,但总平均亲水性指数均为负值,说明二者都表现为亲水性,推测为可溶性蛋白质。
2.2.3 Lr-L-LDH的跨膜区预测和信号肽预测
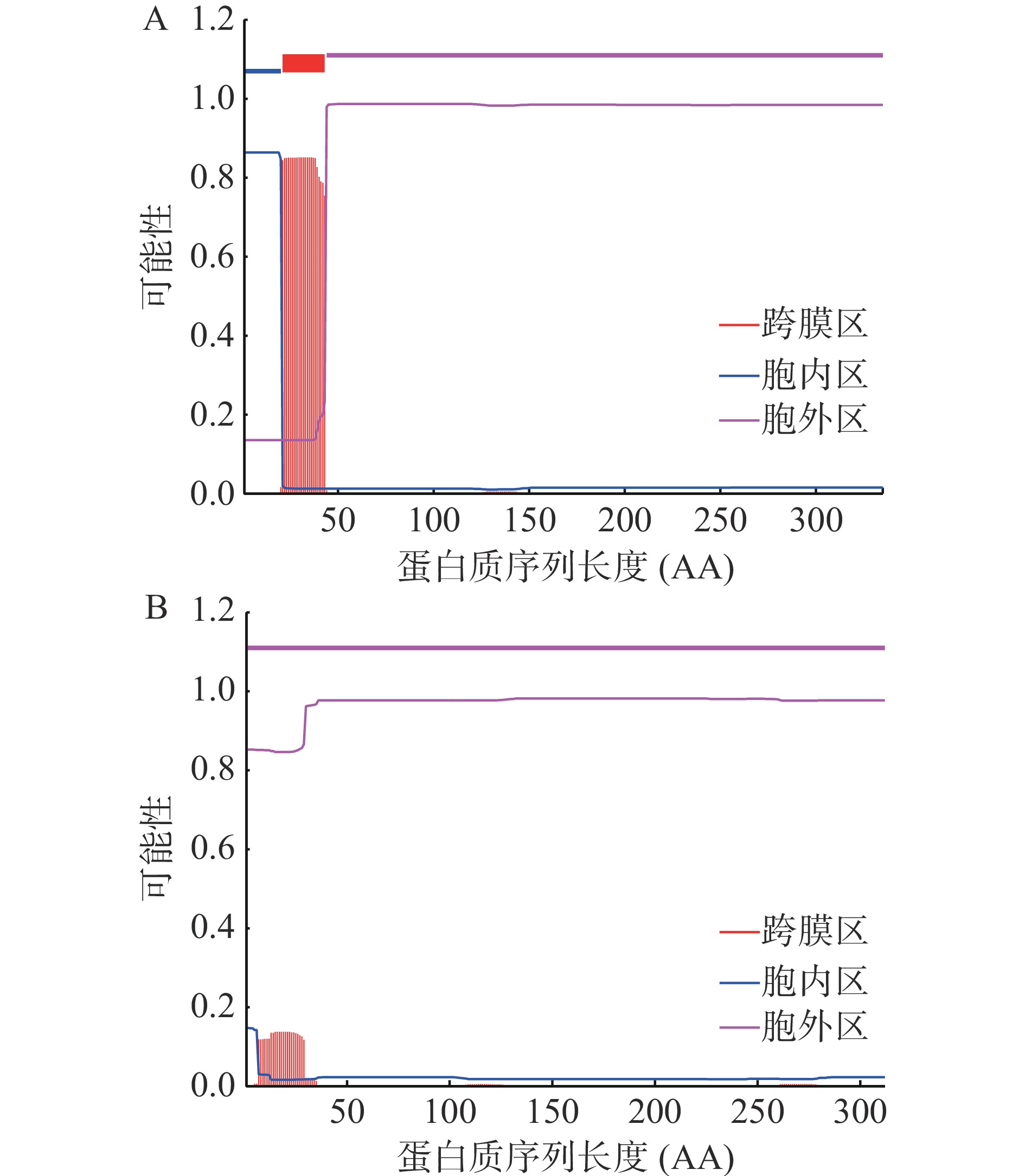
蛋白质的折叠将形成疏水性内核和亲水性表面,跨膜区具有高疏水性结构域,由强疏水的氨基酸组成,能使膜蛋白穿过膜的磷脂双分子层。Lr-L-LDH1和Lr-L-LDH2是亲水性蛋白质,经TMHMM Server v. 2.0和SignalP 5.0 Server分析,结果如表3和图3所示。Lr-L-LDH1可能存在一个跨膜区,Lr-L-LDH2没有明显的跨膜区,但分析预测二者的信号肽存在的概率很低,Signal Peptide(Sec/SPI)数值均小于0.5,故判定没有信号肽。一般认为,没有信号肽的蛋白质不能转运,翻译完成后的蛋白质将留在合成的区域,不会分泌到胞外,因此推测Lr-L-LDH1和Lr-L-LDH2均为胞内酶。
表 3 Lr-L-LDH信号肽预测Table 3. Signal peptide prediction of Lr-L-LDH蛋白类型 可能性 Lr-L-LDH1 Lr-L-LDH2 信号肽(Sec/SPI) 0.0116 0.1173 TAT信号肽(Tat/SPI) 0.0019 0.01 脂蛋白信号肽(Sec/SPII) 0.0009 0.039 其他 0.9856 0.8337 2.2.4 Lr-L-LDH的序列比对分析
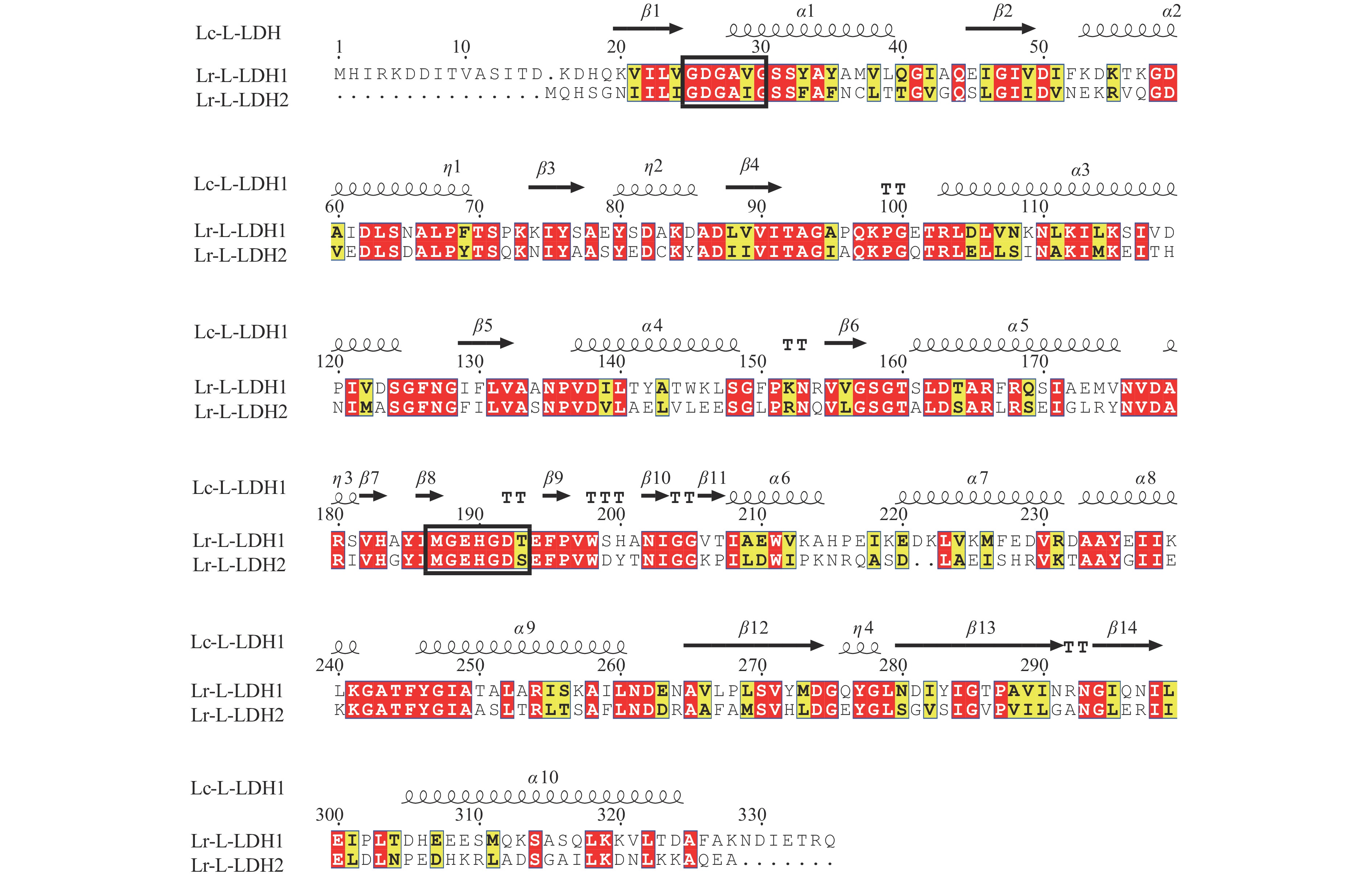
氨基酸序列比对和蛋白质功能位点分析显示,Lr-L-LDH1含有9个潜在的酪蛋白激酶II(CK2)磷酸化位点,4个潜在的蛋白激酶C(PKC)磷酸化位点,5个潜在的肉豆蔻基酰化位点,1个NAD+结合位点序列(GDGAVG),1个L-乳酸脱氢酶活性位点序列aa187~aa193(MGEHGDT);Lr-L-LDH2含有3个潜在的酪蛋白激酶II(CK2)磷酸化位点,3个潜在的蛋白激酶C(PKC)磷酸化位点,9个潜在的肉豆蔻基酰化位点,1个NAD+结合位点序列(GDGAIG),1个L-乳酸脱氢酶活性位点序列aa173~aa179(MGEHGDS),如图4所示。Lr-L-LDH1和Lr-L-LDH2都有典型的NAD+结合位点序列(GXGXXG,X为任意氨基酸),推测Lr-L-LDH1和Lr-L-LDH2为NAD+依赖型LDH。另外,Lr-L-LDH1和Lr-L-LDH2都有乳酸脱氢酶活性位点序列,是与底物结合并发挥催化作用的部位,与LDH的活性直接相关。Lr-L-LDH1和Lr-L-LDH2的NAD+结合位点序列和乳酸脱氢酶活性位点序列中都仅存在一个氨基酸残基的差异。
2.2.5 Lr-L-LDH的二级结构预测和三维结构同源建模分析
2.2.5.1 Lr-L-LDH的二级结构预测
Lr-L-LDH1和Lr-L-LDH2的二级结构分析结果如表4和图5所示,二者都以α-螺旋和无规则卷曲结构为主。蛋白质的空间结构决定了其功能,α-螺旋的化学键能高、不易变形、可塑性低,对骨架起稳定作用,β-转角和无规则卷曲易变形、可塑性高、无规则卷曲受侧链相互作用的影响很大,这类有序的非重复性结构经常构成酶活性部位和其他蛋白质特异的功能部位[30],前述蛋白质功能位点分析预测的Lr-L-LDH1活性位点序列 aa187~aa193 和 Lr-L-LDH2 活性位点序列 aa173~aa179就位于无规则卷曲构象区域。另外,无规则卷曲有明确而稳定的结构,使蛋白质的空间结构中的自由能达到最大,从而促进其内部结构的稳定性,提高蛋白质的热稳定性、溶剂耐受性等[31],因此推测Lr-L-LDH1和Lr-L-LDH2结构中比例较多的无规则卷曲能使其具有较高的热稳定性,该结果也与前述2.2.1中不稳定指数所预测的Lr-L-LDH1和Lr-L-LDH2为结构稳定性蛋白相一致。
表 4 二级结构中组件的比率Table 4. The proportion of components in a secondary structure二级结构 比率(%) Lr-L-LDH1 Lr-L-LDH2 α-螺旋 36.72 41.03 延伸链 22.99 20.19 β-转角 8.96 9.29 无规则卷曲 31.34 29.49 2.2.5.2 Lr-L-LDH的三维结构同源建模和分子对接分析
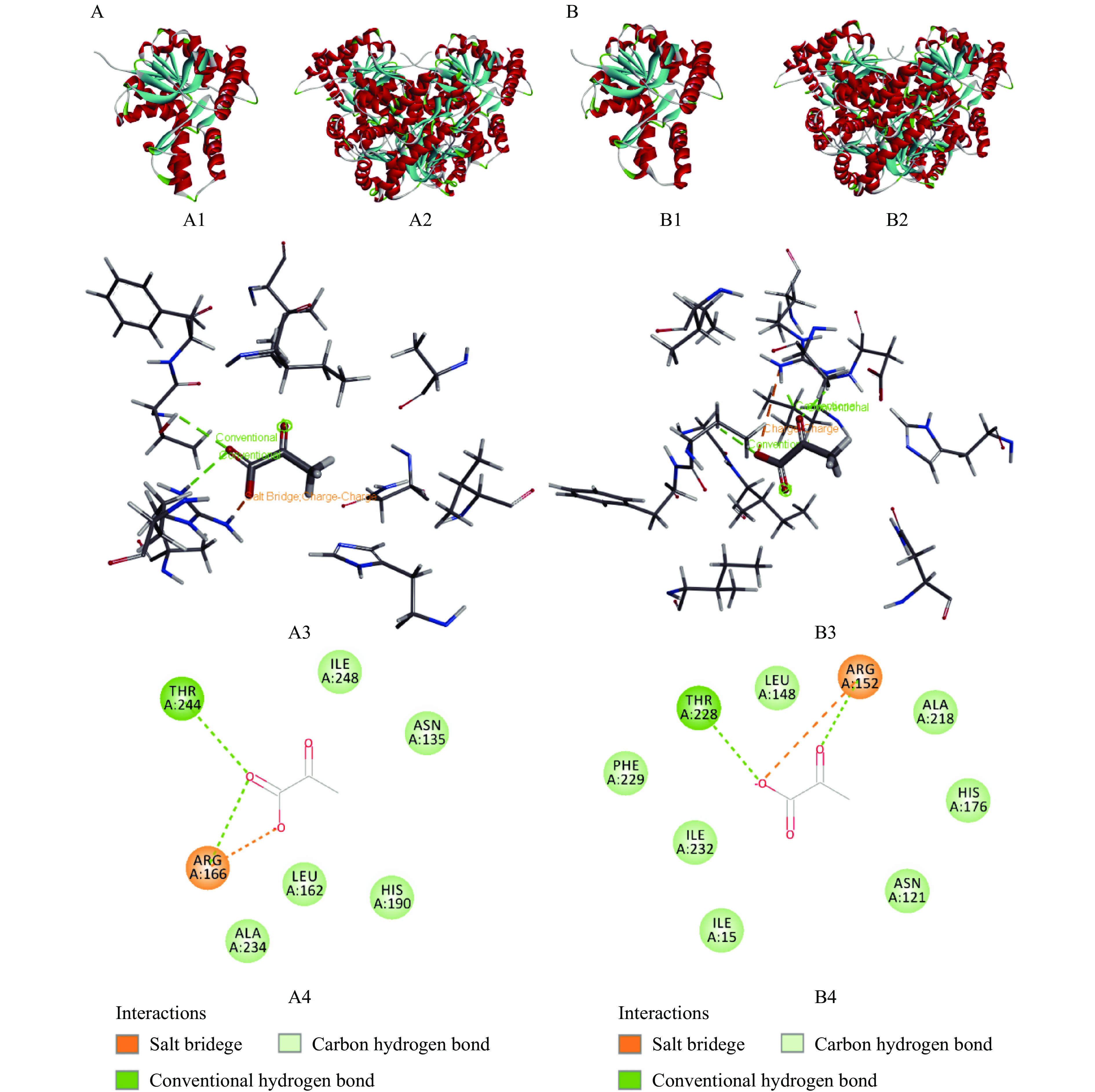
Lr-L-LDH1和Lr-L-LDH2的三维结构分析,SWISS-MODEL在蛋白质数据库中检索出了与Lr-L-LDH1同源性为99.69%,与Lr-L-LDH2同源性为48.39%,来源于干酪乳杆菌(Lactobacillus casei)的L-乳酸脱氢酶(Lc-L-LDH,PDB:2zqy)晶体结构。Lr-L-LDH1和Lr-L-LDH2是一种规则对称的四聚体结构(分别如图6中A2、B2所示),由4个相同的亚基组成(分别如图6中A1、B1所示)。基于Lc-L-LDH结构与功能的研究,推测Lr-L-LDH是变构酶,具有变构作用,通常需要果糖1,6-二磷酸(Fructose-1,6- bisphosphate, FBP)才能发挥催化活性,分别通过丙酮酸和果糖1,6-二磷酸的同向和异向激活作用被激活[31-33]。Lc-L-LDH的丙酮酸结合位点残基涉及精氨酸-169(Arg169)、组氨酸-193(His193)和苏氨酸-247(Thr247),以丙酮酸为配体分子,对受体分子Lr-L-LDH1和Lr-L-LDH2进行分子对接,分析酶与底物分子的结合及可能的成键。分析结果显示,在Lr-L-LDH1的三维构象活性口袋区域中底物分子丙酮酸的结合位点残基分别为精氨酸-166(Arg166)、组氨酸-190(His190)和苏氨酸-244(Thr244),如图6中A3、A4所示;在Lr-L-LDH2的三维构象活性口袋区域中底物分子丙酮酸的结合位点残基分别为精氨酸-152(Arg152)、组氨酸-190(His176)和苏氨酸-228(Thr228),如图6中B3、B4所示。该分析结果与之前的乳酸脱氢酶活性位点序列预测相一致,Lr-L-LDH1活性位点序列aa187~aa193和Lr-L-LDH2活性位点序列aa173~aa179中都存在保守的组氨酸残基,组氨酸是氨基酸中唯一一种侧链基团pKa值接近7.0的氨基酸,其在生物体内的氧化过程中可作为质子供体。
![]() 图 6 Lr-L-LDH1 和Lr-L-LDH2的三维结构预测和分子对接分析注:A:Lr-L-LDH1;B:Lr-L-LDH2;A1:Lr-L-LDH1单体三维结构模拟;A2:Lr-L-LDH1四聚体三维结构模拟;A3、A4:Lr-L-LDH1酶-丙酮酸底物作用关系分析;B1:Lr-L-LDH2单体三维结构模拟;B2:Lr-L-LDH2四聚体三维结构模拟;B3、B4:Lr-L-LDH2酶-丙酮酸底物作用关系分析;橙黄色虚线表示盐桥(Salt bridge),绿色虚线表示氢键(Conventional hydrogen bond)。Figure 6. Three-dimensional structure prediction and molecular docking analysis of Lr-L-LDH1 and Lr-L-LDH2
图 6 Lr-L-LDH1 和Lr-L-LDH2的三维结构预测和分子对接分析注:A:Lr-L-LDH1;B:Lr-L-LDH2;A1:Lr-L-LDH1单体三维结构模拟;A2:Lr-L-LDH1四聚体三维结构模拟;A3、A4:Lr-L-LDH1酶-丙酮酸底物作用关系分析;B1:Lr-L-LDH2单体三维结构模拟;B2:Lr-L-LDH2四聚体三维结构模拟;B3、B4:Lr-L-LDH2酶-丙酮酸底物作用关系分析;橙黄色虚线表示盐桥(Salt bridge),绿色虚线表示氢键(Conventional hydrogen bond)。Figure 6. Three-dimensional structure prediction and molecular docking analysis of Lr-L-LDH1 and Lr-L-LDH22.3 Lr-L-LDH的克隆和表达
2.3.1 L-乳酸脱氢酶基因的克隆和表达菌株构建
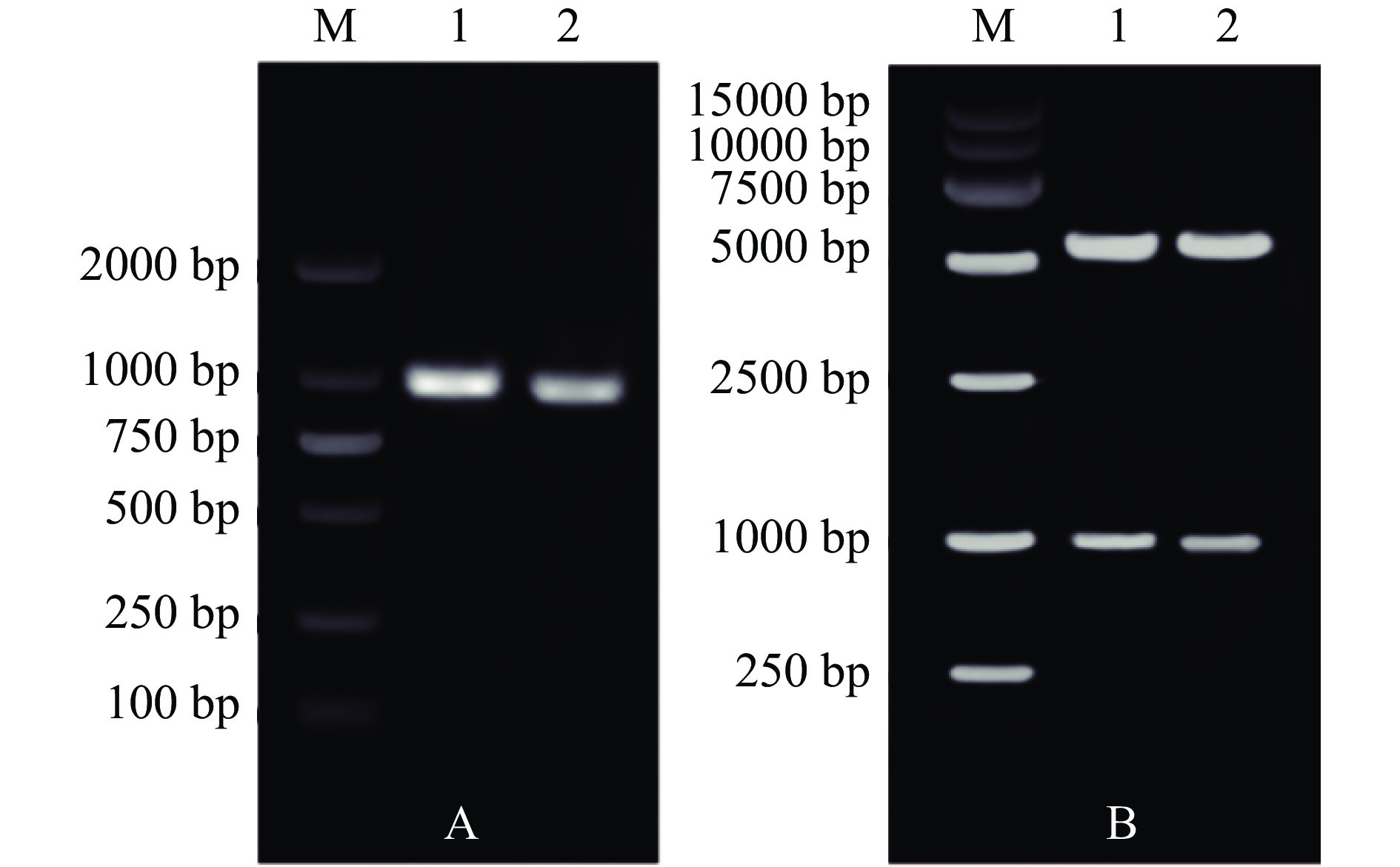
以L. rhamnosus ATCC 11443菌株基因组DNA为模板扩增目的基因Lr-ldh1和Lr-ldh2。PCR产物用0.8%琼脂糖凝胶电泳检测,检测结果如图7A所示。电泳检测结果表明扩增的Lr-ldh1和Lr-ldh2基因DNA片段大小分别约为1000和950 bp,与预期相符。构建的中间质粒为pMD18-Lr-ldh1和pMD18-Lr-ldh2,经DNA测序验证,克隆的Lr-ldh1和Lr-ldh2基因序列与GenBank所报道的L. rhamnosus ATCC 11443菌株L-乳酸脱氢酶基因序列完全一致,表明已克隆得到目的L-乳酸脱氢酶基因。
构建的表达质粒为pET-28a-Lr-ldh1和pET-28a-Lr-ldh2,表达质粒的BamH I和Xho I双酶切电泳验证结果如图7B所示。酶切的Lr-ldh1和Lr-ldh2基因DNA片段大小分别约为1000和950 bp,与预期相符。将表达质粒pET-28a-Lr-ldh1和pET-28a-Lr-ldh2电转化E. coli-BL21 (DE3)感受态细胞,得到E. coli-BL21(DE3)-pET-28a-Lr-ldh1和E. coli-BL21(DE3)-pET-28a-Lr-ldh2表达菌株,表达菌株中的目的基因经DNA测序验证正确后将用于表达实验。
2.3.2 L-乳酸脱氢酶基因诱导表达和酶活检测
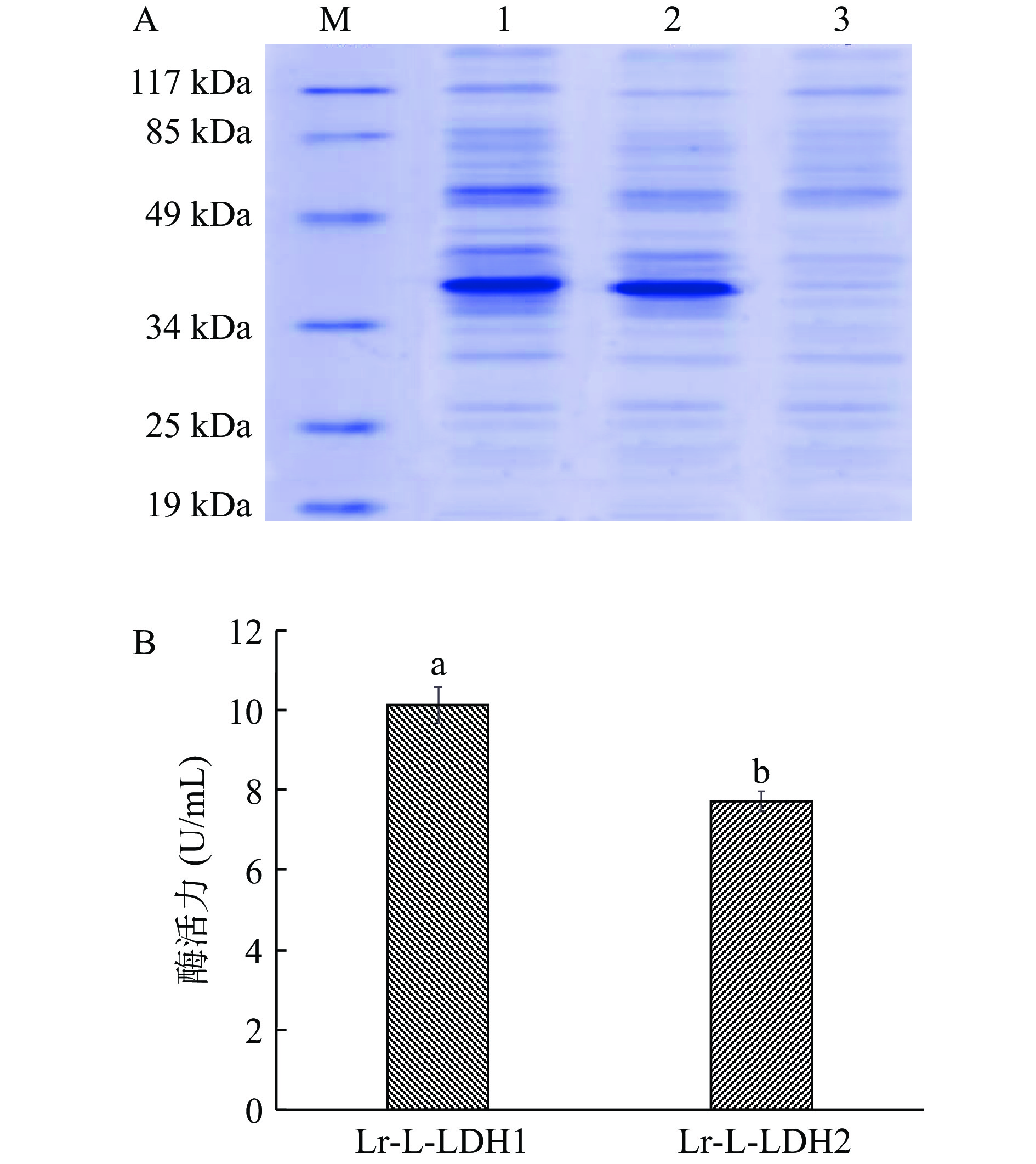
以E. coli-BL21(DE3)作为对照,将重组表达菌株E. coli-BL21(DE3)-pET-28a-Lr-L-ldh1和E. coli-BL21(DE3)-pET-28a-Lr-L-ldh2接种至LB培养基中培养,IPTG诱导表达后收集菌体,菌体经处理后进行SDS-PAGE电泳,检测L-乳酸脱氢酶基因的表达,表达结果如图8所示。结果表明,重组表达菌E. coli-BL21(DE3)-pET-28a-Lr-L-ldh1和E. coli-BL21(DE3)-pET-28a-Lr-L-ldh2经诱导表达后,在菌体中均检测到明显的相对分子质量约为40 kDa的目的蛋白条带,与预期相符,外源Lr-L-ldh1和Lr-L-ldh2基因在大肠杆菌中得到表达。
将重组表达菌株E. coli-BL21(DE3)-pET-28a-Lr-L-ldh1和E. coli-BL21(DE3)-pET-28a-Lr-L-ldh2接种至LB培养基中培养,IPTG诱导表达后收集菌体,菌体细胞经超声破碎后制备成待测酶液,用于酶活检测。菌株E. coli-BL21(DE3)-pET-28a-Lr-L-ldh1粗酶液的酶活力为10.07 U/mL,菌株E. coli-BL21(DE3)-pET-28a-Lr-L-ldh2粗酶液的酶活力为7.77 U/mL,Lr-L-LDH1和Lr-L-LDH2的酶活力存在极显著差异(P<0.01)。
3. 讨论与结论
乳酸菌中LDH均具有较强的稳定性和专一性,是糖酵解途径中的关键酶,主要存在于细胞质中,催化厌氧糖酵解的最后一步[34]。LDH分为非NAD+依赖的乳酸脱氢酶iLDHs(NAD-independent lactate dehydrogenases)和NAD+依赖的乳酸脱氢酶nLDHs(NAD-dependent lactate dehydrogenases),nLDHs以NAD+为辅酶,具有D型和L型两种构象,即D-乳酸脱氢酶(D-LDH;EC 1.1.1.28)和L-乳酸脱氢酶(L-LDH;EC 1.1.1.27)[35-36]。L-LDH在生理条件下需要果糖1,6-二磷酸(Fructose-1,6-bisphosphate, FBP)来激活,发酵生产L-乳酸,在缺少FBP时几乎没有活性[33,37-39]。L-LDH在生物催化丙酮酸生成L-乳酸的过程中具有十分重要的应用价值,通过基因工程改造实现L-LDH的高效表达是使其适应工业化生产应用的有效手段[40]。本研究对鼠李糖乳杆菌L. rhamnosus ATCC 11443菌株的Lr-L-LDH1和Lr-L-LDH2进行生物信息学分析、克隆表达分析和酶活检测,Lr-L-LDH2虽然在编码序列,二级和三级结构等性质上和Lr-L-LDH1相似,但其系统进化位置不同,体外表达酶活性差异显著。
本研究首先确证了L. rhamnosus ATCC 11443基因组功能注释中Lr-L-ldh1和Lr-L-ldh2为L-乳酸脱氢酶的编码基因,都具有典型的乳酸脱氢酶活性位点序列,而且,Lr-L-LDH1和Lr-L-LDH2酶催化丙酮酸生成L-乳酸的功能结构域中,其三维构象活性口袋区域中都具有典型的Arg、His、Thr丙酮酸结合位点残基,通过His将质子传递给丙酮酸,使其转化生成L-乳酸,该研究结果为进一步增强Lr-L-LDH酶活力的分子改造和酶学性质分析提供参考。
其次,在催化丙酮酸生成L-乳酸的过程中,Lr-L-LDH1和Lr-L-LDH2都是以NAD+为辅酶,并需要FBP的激活。相关研究发现,在一定范围内丙酮酸和NAD+浓度与L-乳酸脱氢酶的酶活性正相关,FBP的浓度决定细胞内乳酸的合成速率[15]。因此,如何调控L-乳酸发酵体系中底物浓度、还原力和FBP浓度以达到L. rhamnosus ATCC 11443菌株最优的L-乳酸发酵产率将是下一步研究的目标。
再次,Lr-L-LDH1和Lr-L-LDH2是结构稳定的可溶性蛋白,该特性能够保障其在细胞质中能够抵抗一定范围环境因素变化的影响,行使酶的催化功能,维持菌株的正常代谢,该结果也提示了在下一步的酶分子改造和酶活性分析中,如何增强Lr-L-LDH在特定工业生产环境中的稳定性是一个研究重点。
最后,Lr-L-LDH1和Lr-L-LDH2酶的编码DNA序列不同、大小不同,氨基酸同源性仅为48.08%,Lr-L-LDH1和Lr-L-LDH2的NAD+结合位点序列和乳酸脱氢酶活性位点序列中都存在一个氨基酸残基的差异,二者的进化地位不同。相同反应条件下,Lr-L-LDH1和Lr-L-LDH2都能催化丙酮酸生成L-乳酸,但Lr-L-LDH1的酶活力极显著高于Lr-L-LDH2。另外,在相关的乳酸菌D-乳酸表达的研究中发现,敲除乳酸菌L-ldh2基因后,L-乳酸产量和光学纯度显著上升,D-乳酸产量和光学纯度显著下降;敲除乳酸菌L-ldh1基因后,D-乳酸产量和光学纯度显著显著上升[41]。因此认为,Lr-L-ldh1和Lr-L-ldh2是两个不同的基因,共同主导乳酸菌的L-乳酸表达,在细胞的乳酸表达调控中也可能存在相互依存、互为限制的作用关系。该研究结果提示了有必要通过基因工程手段进一步分析Lr-L-ldh1和Lr-L-ldh2基因在细胞内的表达调控关系,同时,该结果也为Lr-L-ldh1和Lr-L-ldh2两个基因间的选择性敲除或多拷贝表达提供选择依据,为高效L. rhamnosus ATCC 11443乳酸基因工程表达菌株的构建工作奠定基础。
-
图 6 Lr-L-LDH1 和Lr-L-LDH2的三维结构预测和分子对接分析
注:A:Lr-L-LDH1;B:Lr-L-LDH2;A1:Lr-L-LDH1单体三维结构模拟;A2:Lr-L-LDH1四聚体三维结构模拟;A3、A4:Lr-L-LDH1酶-丙酮酸底物作用关系分析;B1:Lr-L-LDH2单体三维结构模拟;B2:Lr-L-LDH2四聚体三维结构模拟;B3、B4:Lr-L-LDH2酶-丙酮酸底物作用关系分析;橙黄色虚线表示盐桥(Salt bridge),绿色虚线表示氢键(Conventional hydrogen bond)。
Figure 6. Three-dimensional structure prediction and molecular docking analysis of Lr-L-LDH1 and Lr-L-LDH2
表 1 本研究使用的引物
Table 1 Primer used in this study
引物 引物序列(5'-3') 用途 ldhL1-F CATGGATCCATGCACATAAGAAAGGATGAT 扩增Lr-L-ldh1基因 ldhL1-R GCACTCGAGTTACTGACGTGTTTCGATGTC 扩增Lr-L-ldh1基因 ldhL2-F CATGGATCCATGCAACATAGCGGAAATATT 扩增Lr-L-ldh2基因 ldhL2-R GCACTCGAGCTAGGCTTCCTGTGCCTTCTT 扩增Lr-L-ldh2基因 表 2 Lr-L-LDH基本性质分析
Table 2 Analysis of the basic characteristics of the Lr-L-LDH
基本性质 Lr-L-LDH1 Lr-L-LDH2 氨基酸残基数量 335 312 分子质量(Da) 36608.80 33557.10 等电点 5.34 5.12 带负电荷氨基酸(Asp+Glu) 45 39 带正电荷氨基酸(Arg+Lys) 36 28 分子式 C1639H2613N433O500S7 C1487H2377N407O461S7 原子总数 5192 4739 消光系数(mol/cm) 32890 26025 不稳定指数 30.10 37.35 脂肪族指数 99.88 104.17 亲水性平均系数 -0.096 -0.020 表 3 Lr-L-LDH信号肽预测
Table 3 Signal peptide prediction of Lr-L-LDH
蛋白类型 可能性 Lr-L-LDH1 Lr-L-LDH2 信号肽(Sec/SPI) 0.0116 0.1173 TAT信号肽(Tat/SPI) 0.0019 0.01 脂蛋白信号肽(Sec/SPII) 0.0009 0.039 其他 0.9856 0.8337 表 4 二级结构中组件的比率
Table 4 The proportion of components in a secondary structure
二级结构 比率(%) Lr-L-LDH1 Lr-L-LDH2 α-螺旋 36.72 41.03 延伸链 22.99 20.19 β-转角 8.96 9.29 无规则卷曲 31.34 29.49 -
[1] JU S Y, KIM J H, LEE P C. Long-term adaptive evolution of Leuconostoc mesenteroides for enhancement of lactic acid tolerance and production[J]. Biotechnology for Biofuels,2016,9(1):240. doi: 10.1186/s13068-016-0662-3
[2] ABDEL-RAHMAN M A, TASHIRO Y, SONOMOTO K. Lactic acid production from lignocellulose-derived sugars using lactic acid bacteria: Overview and limits[J]. Journal of Biotechnology,2010,156(4):286−301.
[3] PARRA-RAMIREZ D, MARTINEZ A, CARDONA C A. Lactic acid production from glucose and xylose using the lactogenic Escherichia coli strain JU15: Experiments and techno-economic results[J]. Bioresource Technology,2018,273:86−92.
[4] 孙浩轩, 周卫强, 杨硕, 等. 微生物制备高光学纯度L-乳酸的研究进展[J]. 食品与发酵科技,2021,57(5):91−96, 112. [SUN H X, ZHOU W Q, YANG S, et al. Progress in microbiological preparation of L-lactic acid strain with high optical purity and its production[J]. Food and Fermentation Sciences & Technology,2021,57(5):91−96, 112. [5] 刘金熙, 李冠洋, 金清. 乳酸菌发酵生产D-/L-乳酸的研究进展[J]. 食品安全导刊,2021,33:146−148. [LIU J X, LI G Y, JIN Q. Research progress in production of D-/L-lactic acid by lactic acid bacteria[J]. China Food Safety Magazine,2021,33:146−148. doi: 10.3969/j.issn.1674-0270.2021.30.spaqdk202130085 [6] WESSELS S, AXELSSON L, HANSEN E B, et al. The lactic acid bacteria, the food chain, and their regulation[J]. Trends in Food Science & Technology,2004,15(10):498−505.
[7] BERNARD N, FERAIN T, GARMYN D, et al. Cloning of the D-lactate dehydrogenase gene from Lactobacillus delbrueckii subsp. bulgaricus by complementation in Escherichia coli[J]. FEBS Letters,1991,290:61−64. doi: 10.1016/0014-5793(91)81226-X
[8] ABDEL-RAHMAN M A, TASHIRO Y, SONOMOTO K. Recent advances in lactic acid production by microbial fermentation processes[J]. Biotechnology Advances,2013,31(6):877−902. doi: 10.1016/j.biotechadv.2013.04.002
[9] 吉林中粮生化有限公司. 产L-乳酸的重组菌株及其构建方法和发酵产L-乳酸的方法及应用: 中国, CN202010463397.3[P]. 2020-08-07 Jilin COFCO Biochemical Co. Ltd. Recombinant strain producing L-lactic acid and its construction method, fermentation method and application: China, CN202010463397.3[P]. 2020-08-07.
[10] 李雪晴, 袁风娇, 刘艳, 等. 不对称还原苯丙酮酸的L-乳酸脱氢酶L-LcLDH2的表达及生物信息学分析[J]. 食品与生物技术学报,2019,38(12):25−30. [LI X Q, YUAN F J, LIU Y, et al. Expression and bioinformatic analysis of an L-Lactate Dehydrogenase (L-LcLDH2) for the asymmetric reduction of phenylpyruvic acid[J]. Journal of Food Science and Biotechnology,2019,38(12):25−30. doi: 10.3969/j.issn.1673-1689.2019.12.004 [11] ANDRES J, MOLINER V, KRECHL J, et al. A PM3 quantum chemical study of the pyruvate reduction mechanism catalyzed by lactate dehydrogenase[J]. Bioorganic Chemistry,1993,21(3):260−274. doi: 10.1006/bioo.1993.1022
[12] KLEEREBEZEM M, HUGENHOLTZ J. Metabolic pathway engineering in lactic acid bacteria[J]. Current Opinion in Biotechnology,2003,14(2):232−237. doi: 10.1016/S0958-1669(03)00033-8
[13] 杨贞耐, 张雪. 乳酸菌代谢途径的基因工程调控[J]. 中国乳品工业,2007,35(11):44−47. [YANG Z N, ZHANG X. Genetic engineering of metabolic pathways in lactic acid bacteria[J]. China Dairy Industry,2007,35(11):44−47. doi: 10.3969/j.issn.1001-2230.2007.11.013 [14] 李倩, 王梦, 刘珞, 等. L-乳酸脱氢酶在大肠杆菌BL-21(DE3)中的表达[J]. 生物加工过程,2011,9(6):21−25. [LI Q, WANG M, LIU L, et al. Expression of L-lactate dehydrogenase in Escherichia coli BL-21 (DE3)[J]. Chinese Journal of Bioprocess Engineering,2011,9(6):21−25. doi: 10.3969/j.issn.1672-3678.2011.06.005 [15] 袁剑, 秦浩, 葛向阳, 等. 干酪乳杆菌L-乳酸脱氢酶在大肠杆菌中的表达、纯化及酶学性质[J]. 微生物学通报,2011,38(10):1482−1487. [YUAN J, QIN H, GE X Y, et al. Overexpression, purification and properties of ldhL gene from Lactobacillus casei in Escherichia coli[J]. Microbiology China,2011,38(10):1482−1487. [16] 杨登峰, 潘丽霞, 关妮, 等. 产高纯度L-乳酸大肠杆菌基因工程菌的初步研究[J]. 现代食品科技,2010,26(2):126−128,171. [YANG D F, PAN L X, GUAN N, et al. Construction of recombinant E. coli. strain for producing high-purity L-Lactate[J]. Modern Food Science and Technology,2010,26(2):126−128,171. [17] 王刚, 肖雨, 李义, 等. ldhL-ldb0094基因敲除对保加利亚乳杆菌产L-乳酸的影响[J]. 中国生物工程杂志,2019,39(8):66−73. [WANG G, XIAO Y, LI Y, et al. Effect of ldhL-ldb0094 gene knock out mutant on Lactobacillus delbrueckii subsp. blgaricus producing L-lactic acid[J]. China Biotechnology,2019,39(8):66−73. [18] 许黎明, 成春燕, 吕军. 鼠李糖乳杆菌D-乳酸脱氢酶基因ldhD的敲除[J]. 基因组学与应用生物学,2016,35(6):1421−1427. [XU L M, CHENG C Y, LÜ J. Knockout of D-Lactate dehydrogenase gene ldhD in Lactobacillus rhamnosus[J]. Genomics and Applied Biology,2016,35(6):1421−1427. [19] 金李玲, 孙丽霞, 陈思婷, 等. 鼠李糖乳杆菌半固态发酵法生产L-乳酸及发酵动力学分析[J]. 食品工业科技,2015,36(19):195−201. [JIN L L, SUN L X, CHEN S T, et al. Study on production of L-Lactic acid in semi-solid state fermentation by Lactobacillus rhamnosus and fermentation kinetics[J]. Science and Technology of Food Industry,2015,36(19):195−201. [20] JIANG G F, HINSINGER D D, STRIJK J S. Comparison of intraspecific, interspecific and intergeneric chloroplast diversity in Cycads[J]. Scientific Reports,2016,6:31473. doi: 10.1038/srep31473
[21] XU L M, HINSINGER D D, JIANG G F. The complete mitochondrial genome of the Agrocybe aegerita, an edible mushroom[J]. Mitochondrial Dna Part B,2017,2(2):791−792. doi: 10.1080/23802359.2017.1398618
[22] XU L M, HINSINGER D D, JIANG G F. The complete mitochondrial genome of the Basidiomycete fungus Pleurotus cornucopiae (Paulet) Rolland[J]. Mitochondrial DNA Part B,2018,3(1):73−75. doi: 10.1080/23802359.2017.1422405
[23] 李建武, 萧能, 余瑞元, 等. 生物化学实验原理和方法[M]. 北京: 北京大学出版社, 1997: 351−353 LI J W, XIAO N, YU R Y, et al. Principles and methods of biochemical experiment[M]. Beijing: Peking University Press, 1997: 351−353.
[24] 倪玉芳. 四种啮齿动物Ldha基因的克隆、原核表达与酶学性质研究[D]. 泸州: 西南医科大学, 2021 NI Y F. Cloning, prokaryotic expression and enzymatic properties of Ldha genes from four rodents[D]. Luzhou: Southwest Medical University, 2021.
[25] 申萍香, 黄艳, 黄江, 等. 生物信息学分析亚洲牛带绦虫乳酸脱氢酶基因及其蛋白的结构与特性[J]. 中国人兽共患病学报,2008,24(8):722−727. [SHEN P X, HUANG Y, HUANG J, et al. Bioinformatics analysis on the structures and properties of gene and the encoding protein of lactate dehydrogenase from Taeniasaginata asiatica[J]. Chinese Journal of Zoonoses,2008,24(8):722−727. doi: 10.3969/j.issn.1002-2694.2008.08.008 [26] 吕刚, 余新炳, 黄灿, 等. 日本血吸虫乳酸脱氢酶(SjLDH)结构与功能的生物信息学分析[J]. 中国寄生虫学与寄生虫病杂志,2007,25(3):202−205. [LÜ G, YU X B, HUANG C, et al. Bioinformatics analysis for the structure and function of lactate dehydrogenase from Schistosoma japonicum[J]. Chinese Journal of Parasitology and Parasitic Diseases,2007,25(3):202−205. doi: 10.3969/j.issn.1000-7423.2007.03.010 [27] 赵婷. 副干酪乳杆菌乳酸脱氢酶的克隆表达及酶学性质的研究[D]. 苏州: 苏州大学, 2012 ZHAO T. Cloning, overexpression and properties of ldh gene from Lactobacillus paracasei[D]. Suzhou: Soochow University, 2012.
[28] GURUPRASAD K, REDDY B V, PANDIT M W. Correlation between stability of a protein and its dipeptide composition: A novel approach for predicting in vivo stability of a protein from its primary sequence[J]. Protein Engineering, Design and Selection,1990,4(2):155−161. doi: 10.1093/protein/4.2.155
[29] GASTEIGER E, HOOGLAND C, GATTIKER A, et al. The proteomics protocols handbook: Protein identification and analysis tools on the ExPASy server[M]. Clifton: Humana Press, 2005: 571−607.
[30] WOODS H K R. Prediction of protein antigenic determinants from amino acid sequences[J]. Proceedings of the National Academy of Sciences of the United States of America,1981,78(6):3824−3828. doi: 10.1073/pnas.78.6.3824
[31] 陈琦, 李春秀, 郑高伟, 等. 工业蛋白质构效关系的计算生物学解析[J]. 生物工程学报,2019,35(10):1829−1842. [CHEN Q, LI C X, ZHENG G W, et al. Computational analysis of structure-activity relationship of industrial enzymes[J]. Chinese Journal of Biotechnology,2019,35(10):1829−1842. [32] ARAI K, ISHIMITSU T, FUSHINOBU S, et al. Active and inactive state structures of unliganded Lactobacillus casei allosteric L-lactate dehydrogenase[J]. Proteins-structure Function & Bioinformatics,2010,78(3):681−694.
[33] GARVIE E I. Bacterial lactate dehydrogenases[J]. Microbiological Reviews,1980,44(1):106. doi: 10.1128/mr.44.1.106-139.1980
[34] FELDMAN-SALIT A, HERING S, MESSIHA H L, et al. Regulation of the activity of lactate dehydrogenases from four lactic acid bacteria[J]. Journal of Biological Chemistry,2013,288(29):21295−21306. doi: 10.1074/jbc.M113.458265
[35] NEVES A R, POOL W A, KOK J, et al. Overview on sugar metabolism and its control in Lactococcus lactis-the input from in vivo NMR[J]. Fems Microbiology Reviews,2010,29(3):531−554.
[36] 钱国军, 陈彩平, 翟如英, 等. 极耐热性乳酸脱氢酶高效表达、纯化及酶学性质[J]. 生物工程学报,2014,30(4):545−553. [QIAN G J, CHEN C P, ZHAI R Y, et al. Expression, purification and characterization of a thermostable lactate dehydrogenase from Thermotoga maritima[J]. Chinese Journal of Biotechnology,2014,30(4):545−553. [37] ZHAO R, ZHENG S, DUAN C, et al. NAD-dependent lactate dehydrogenase catalyses the first step in respiratory utilization of lactate by Lactococcus lactis[J]. Febs Open Bio,2013,3:379−386. doi: 10.1016/j.fob.2013.08.005
[38] CROW V L, PRITCHARD G G. Fructose-1, 6-diohosphate activated L-lactate dehydrogenase from Streptococcus lactis kinetic properties and factors affecting activation[J]. Journal of Bacteriology,1977,131(1):82−91. doi: 10.1128/jb.131.1.82-91.1977
[39] THOMAS T D, TURNER K W, CROW V L. Galactose fermentation by Streptococcus lactis and Streptococcus cremoris: Pathways, products, and regulation[J]. Journal of Bacteriology,1980,144(2):672−682. doi: 10.1128/jb.144.2.672-682.1980
[40] CARREA G, RIVA S. Properties and synthetic applications of enzymes in organic solvents[J]. Cheminform,2000,39(13):2226−2254.
[41] 王希庆. 产高光学纯度D-乳酸保加利亚乳杆菌工程菌的构建及在生物炼制中的应用[D]. 长春: 吉林农业大学, 2018 WANG X Q. Construction of Lactobacillus delbrueckii sp. bulgaricus engineering for high optical purity D-lactic acid and application in biorefinery[D]. Changchun: Jilin Agricultural University, 2018.
-
期刊类型引用(4)
1. 季佳琪,李明初,李冬霞,谭雅宁,高爽,王颉,牟建楼. 高温蒸煮结合蜗牛酶法改性葡萄皮不溶性膳食纤维工艺优化及体外降血糖作用. 食品工业科技. 2024(16): 249-258 .  本站查看
本站查看
2. 林良美,肖少香,张丽红. 响应面优化复合酶法提取红薯皮膳食纤维. 粮食科技与经济. 2024(04): 96-100+115 .  百度学术
百度学术
3. 竹娟,王译晗,陈立莉,曲文鑫,刘荣. 芍药花提取物中黄酮的测定及其体外抗氧化和降脂活性研究. 天然产物研究与开发. 2024(11): 1838-1844+1899 .  百度学术
百度学术
4. 赵习爱,傅婧,任娟蕊. 燕麦萌动对膳食纤维结构和功能的影响. 食品与发酵工业. 2024(24): 229-237 .  百度学术
百度学术
其他类型引用(2)





 下载:
下载:
 下载:
下载:
