Improvement of CaSO4-Induced Gelation Properties of Soybean Protein Isolate by Pre-crosslinking with Transglutaminase
-
摘要: 酶法改性能够有效提升大豆蛋白的凝胶性。为了探讨谷氨酰胺转氨酶(transglutaminase, TGase)预交联对盐诱导大豆分离蛋白凝胶性的影响,通过控制酶浓度、预交联时间制备不同预交联程度的大豆分离蛋白(soy protein isolate,SPI)溶液,并研究其在CaSO4作用下的成胶性能。结果显示,与未经TGase处理的SPI相比,TGase适度预交联能够显著提升SPI的凝胶品质。经3~5 U/g TGase预交联20 min或3 U/g TGase预交联20~30 min后,SPI凝胶性得到了不同程度的提升,其中弹性模量、屈服应力、屈服应变、持水率最大分别提高了124.5%、269.0%、135.0%及53.0%。然而,过度预交联产生过大的蛋白聚集体,导致最终形成的凝胶结构粗糙、多孔,凝胶强度、持水力等均显著下降(P<0.05)。由此可见,合理利用TGase对蛋白进行预交联处理能够改善SPI凝胶制品品质,对于TGase在食品工业中的应用及传统豆制品质构改良具有重要的指导意义。Abstract: Enzymatic modification can effectively improve the gel property of soybean protein. In order to study the effect of transglutaminase (TGase) pre-crosslinking on the properties of salt induced soy protein isolate (SPI) gel, SPI dispersions with different crosslinking degree were prepared by controlling the enzyme concentration and the pre-crosslinking time, and their gelation properties under the action of CaSO4 were studied. The results showed that compared with SPI without TGase treatment, appropriate pre-crosslinking of protein could significantly improve the quality of SPI gels. After 3~5 U/g TGase crosslinking for 20 min or 3 U/g TGase crosslinking for 20~30 min, the properties of SPI gel were improved to different degrees, among which the elastic modulus, yield stress, yield strain and water holding capacity were increased by 124.6%, 269.0%, 135.0% and 53.0%, respectively. However, excessive crosslinking produced protein aggregates with too large size, resulting in coarse and porous gel structure and significantly decreased (P<0.05) in gel strength and water holding capacity. It can be seen that proper utilization of TGase can improve the quality of SPI gel products, which has important guiding significance for the application of TGase in food industry and the improvement of texture of traditional soybean products.
-
Keywords:
- soy protein isolate /
- transglutaminase /
- pre-crosslinking /
- gel property
-
近年来,豆制品及相关素肉产品在国内发展迅速,豆腐、百叶、豆干和素鸡等传统豆制品以及植物蛋白肉等新型含大豆制品,因其对健康有益、对环境友好等优点逐渐得到消费者的重视,使得大豆制品需求越来越大。豆制品的品质(口感、持水性、风味等)很大程度上取决于大豆蛋白的凝胶性,研究表明,凝胶的结构和强度与产品持水率、抗破裂性能等具有显著正相关关系,产品在加工中蛋白颗粒能否相互粘结、水分能否很好的被包裹并保持在凝胶基质中是形成良好豆制品凝胶的关键要素[1-3]。传统豆制品(如豆腐、豆干等)通常采用盐(CaSO4、MgSO4、MgCl2等)[4-5]或酸(葡萄糖内酯、乳酸等)[6-7]等作为凝固剂进行加工,凝胶结构主要是通过非共价相互作用(如静电相互作用、疏水相互作用、氢键等)来维持,普遍存在结构弱、韧性低及保水能力不高等问题[8-9]。
谷氨酰胺转氨酶又称转谷氨酰胺酶(TGase,TG酶),可以进行酰基转移、交联和脱酰胺作用对蛋白进行改性,因其具有蛋白选择范围广、交联聚合度高、安全性良好等优点被广泛应用于食品加工[10]。TGase可以催化蛋白质中谷氨酰胺残基的γ-羧胺基团和赖氨酸残基的ε-氨基之间发生酰基转移反应,形成ε-(γ-谷酰胺)-赖氨酸的异型肽键,引起蛋白质分子间或分子内的发生交联,促进蛋白与食品中其他组分的相互作用,对于提高豆制品[11-12]、肉制品[8-9]、乳制品[13]等食品的凝胶性能,改善食品的品质和风味具有重要的作用。因此,可以通过利用TGase引入共价键的方法来对蛋白凝胶的结构和性能进行改善,从而达到提高传统豆制品品质的目的。然而,有研究表明,TGase处理对蛋白凝胶性的影响与蛋白的交联程度显著相关,如在牛奶蛋白酸诱导凝胶的研究中,Eissa等[14]发现TGase处理对凝胶的模量没有影响,但断裂应变和应力明显增加;Jaros等[15]报道体系中交联的酪蛋白过量时,凝胶强度变弱,脱水率升高;Guo等[16]研究了TGase处理对花生豆腐凝胶品质的影响,发现低浓度(0.75 mg/g)的TGase显著改善了花生豆腐的质地,形成较致密的网状结构,而过量(1.25 mg/g)TGase处理则导致不连续网络的形成,使凝胶变软。而有关TGase预交联对传统凝固剂诱导大豆蛋白凝胶性影响的研究较少,相关机制尚不明确,需进一步探究。
针对上述问题,本研究以大豆分离蛋白(SPI)为原料,利用TGase对SPI溶液进行预交联处理,通过控制酶浓度、交联时间调控SPI的预交联程度,进而研究其在传统凝固剂(CaSO4,适合制备填充型凝胶)作用下的成胶性能,探讨能有效改善SPI凝胶性的TGase预处理最优条件,以期为大豆蛋白凝胶制品的优化加工和品质控制提供理论基础和科学依据。
1. 材料与方法
1.1 材料与仪器
脱脂大豆豆粕 YP901C型,山东禹王生态食品有限公司;谷氨酰胺转氨酶(酶活力为120 U/g) 江苏泰兴东圣食品科技公司;十二烷基苯磺酸钠、丙烯酰胺、N,N-亚甲基双丙烯酰胺、β-巯基乙醇、三羟基氨基甲烷、四甲基乙二胺、溴酚蓝、过硫酸铵 分析纯,国药集团;甘油、甲醇、冰醋酸、硫酸钙 分析纯,西陇科学;甘氨酸 分析纯,上海源叶;低分子量Marker 分析纯,索莱宝试剂公司;考马斯亮蓝 分析纯,阿拉丁试剂公司;罗丹明-B 分析纯,Sigma公司。
JA2003N型电子分析天平 上海精密科学仪器有限公司;TG16-WS型高速离心机 长沙湘智离心机仪器有限公司;FE20型pH计 梅特勒-托利多仪器公司;HH-501型恒温水浴锅 常德市鸿科仪器厂;Big Squid型磁力搅拌器 德国IKA公司;MS3000型激光粒度分析仪 美国马尔文公司;Fluoromax-4型高灵敏度荧光光谱仪 法国Horiba Instrument公司;MCR302型旋转流变仪 奥地利安东帕有限公司;Nikon A1型激光共聚焦显微镜 日本Nikon公司。
1.2 实验方法
1.2.1 SPI的提取
参照Wan等[17]的方法并略有改动,脱脂豆粕与去离子水按1:15的比例混合搅拌,用 2 mol/L 的 NaOH 调节 pH 至 8.0,室温下搅拌 2 h,高速离心(10000 g,4 ℃,20 min)去除不溶物后得到上清液,将所得上清液中加入2 mol/L HCl调节pH至4.5,室温静置30 min,3300 g离心10 min得到蛋白沉淀物。所得的蛋白沉淀物按1:2的质量比与去离子水复溶,并用2 mol/L的NaOH调节pH至7.0,充分搅拌,至其全部溶解。所制得的蛋白溶液经过冷冻干燥得到SPI粉末,其蛋白湿基含量通过凯氏定氮法测得为90%。将所制得的SPI粉末置于−80 ℃冰箱中密封保存备用。
1.2.2 SPI溶液的制备
将SPI粉末溶于去离子水中,室温下搅拌2 h,使其充分溶解,调节pH为7.0,加入0.02%(w/v)NaN3防止微生物的生长,接着在10000 g离心力,4 ℃下离心10 min去除溶液中不溶的杂质,再利用去离子水将SPI溶液浓度调节至60 mg/mL,存至4 ℃冰箱,水合过夜。将SPI溶液用密封黑盖瓶密封,利用循环水浴锅95 ℃加热15 min,冷却至室温备用。
1.2.3 TGase交联SPI聚集体的制备
1.2.3.1 不同TGase浓度的SPI聚集体的制备
将1.2.2所制得的溶液分装于烧杯中,分别添加TGase悬浊液,使得溶液中酶浓度分别为0(空白对照组)、1、3、5、7 U/g蛋白质。然后置于50 ℃水浴锅中反应交联20 min。
1.2.3.2 不同TGase交联时间的SPI聚集体的制备
将1.2.2所制得的溶液分装于烧杯中,分别添加TGase悬浊液,使得溶液中酶浓度为3 U/g。然后置于50 ℃水浴锅中分别交联反应0(空白对照组)、10、20、30、40 min。
1.2.4 SPI聚集体粒径的测定
利用Mastersizer 3000型激光粒度仪测定TGase作用下大豆分离蛋白聚集体的粒径,将SPI聚集体溶液缓慢加入分测量池中,至遮光度到7%左右停止加样。折光系数取1.45,分散相折光系数为1.33。
1.2.5 SPI聚集体SDS-PAGE的测定
参照Hsieh等[18]的方法并略有改动,通过SDS-PAGE测定TGase交联前后SPI亚基的变化。将1.2.3所制得的SPI样品稀释至2 mg/mL,与含有2%(w/v)十二烷基苯磺酸钠(SDS)、10%(w/v)甘油、10%(w/v)β-巯基乙醇及0.05%(w/v)溴酚蓝的0.125 mol/L、pH8.0的Tris-HCl缓冲液进行等体积混合,然后在沸水中煮沸5 min,冰水中冷却。浓缩胶和分离胶的浓度分别为5%和12.5%,每孔进样20 μL,初始电流设置为10 mA,样品到达分离胶时,电流调整为20 mA。电泳结束后用含1 mg/mL考马斯亮蓝,45%甲醇和10%冰醋酸的染色液进行染色,染色30 min后,用含有25%甲醇,8%冰醋酸的脱色液进行脱色。脱色完成后的凝胶进行拍照分析。
1.2.6 流变性质测定
分别向1.2.3中所制备的聚集体溶液中加入CaSO4分散液至盐离子终浓度为25 mmol/L,磁力搅拌均匀后利用MCR 302旋转流变仪振荡模式测定SPI溶液凝胶的流变性质[4],选用的转子为PP 50平板,间隙值为1 mm。
1.2.6.1 温度扫描
温度扫描参数为:应变1%(线性范围区内),频率为1 Hz。温度首先从25 ℃升温至80 ℃,在80 ℃恒温保持30 min,然后再从80 ℃降温至25 ℃。记录弹性模量G′粘性模量G′′随温度和时间的变化情况,升降温速率均为5 ℃/min。
1.2.6.2 频率扫描
温度扫描结束后,在25 ℃条件下对凝胶进行频率扫描,应变设为1%,频率扫描的角频率区间为1~100 rad/s,记录G'、G''随角频率的变化情况。
1.2.6.3 大形变振荡扫描
SPI凝胶的大形变测试采用振幅扫描的模式进行,在1 Hz振荡频率下,凝胶的应变从0.1%逐渐增大直至剪切应力开始降低(凝胶开始破裂),记录应变随应力的变化情况。
1.2.7 CaSO4诱导TGase预交联SPI凝胶的制备
向1.2.3所制备SPI聚集体溶液添加25 mmol/L CaSO4溶液,搅拌均匀后,置于80 ℃水浴锅中水浴加热凝固30 min,取出,冰水冷却后储藏与4 ℃冰箱中等待下一步分析。
1.2.8 SPI凝胶持水力的测定
准确称取5 g 1.2.7 中制备的 SPI 凝胶于 10 mL 离心管中,在 4 ℃、8000 g条件下离心10 min。将离心管倒置,沥干析出的水分,称量。记录离心前后离心管和凝胶的总重量,持水力(%)被定义为离心后凝胶中的水分含量与离心前总水分含量的百分比。
1.2.9 微观结构分析
使用激光共聚焦显微镜(CLSM,Nikon A1)对1.2.7所制备的SPI凝胶进行微观结构观察[4]。具体操作过程如下:向TGase预处理后的蛋白溶液中加入配制好的0.1%的罗丹明B(10 mL的SPI液中加入0.1 mL染液),再加入凝固剂(CaSO4),搅拌混合均匀后,吸取适量混合液放入单凹载玻片的凹槽中,小心盖上盖玻片,在盖玻片四周涂上一层指甲油防止水分蒸发,然后按照1.2.7所描述的方法制备凝胶,并在4 ℃条件下避光储藏12 h后进行激光共聚焦显微镜观察。罗丹明B的激发波长为552 nm,物镜倍数为100倍(油镜)。
1.3 数据处理
所有数据至少重复测定2次,每次至少3个平行,结果用平均值±SD表示。使用IBM SPSS Statistics 26软件进行方差及相关性分析,采用LSD法对实验所得数据进行显著性分析(P<0.05)。
2. 结果与分析
2.1 不同TGase预交联程度对SPI粒径的影响
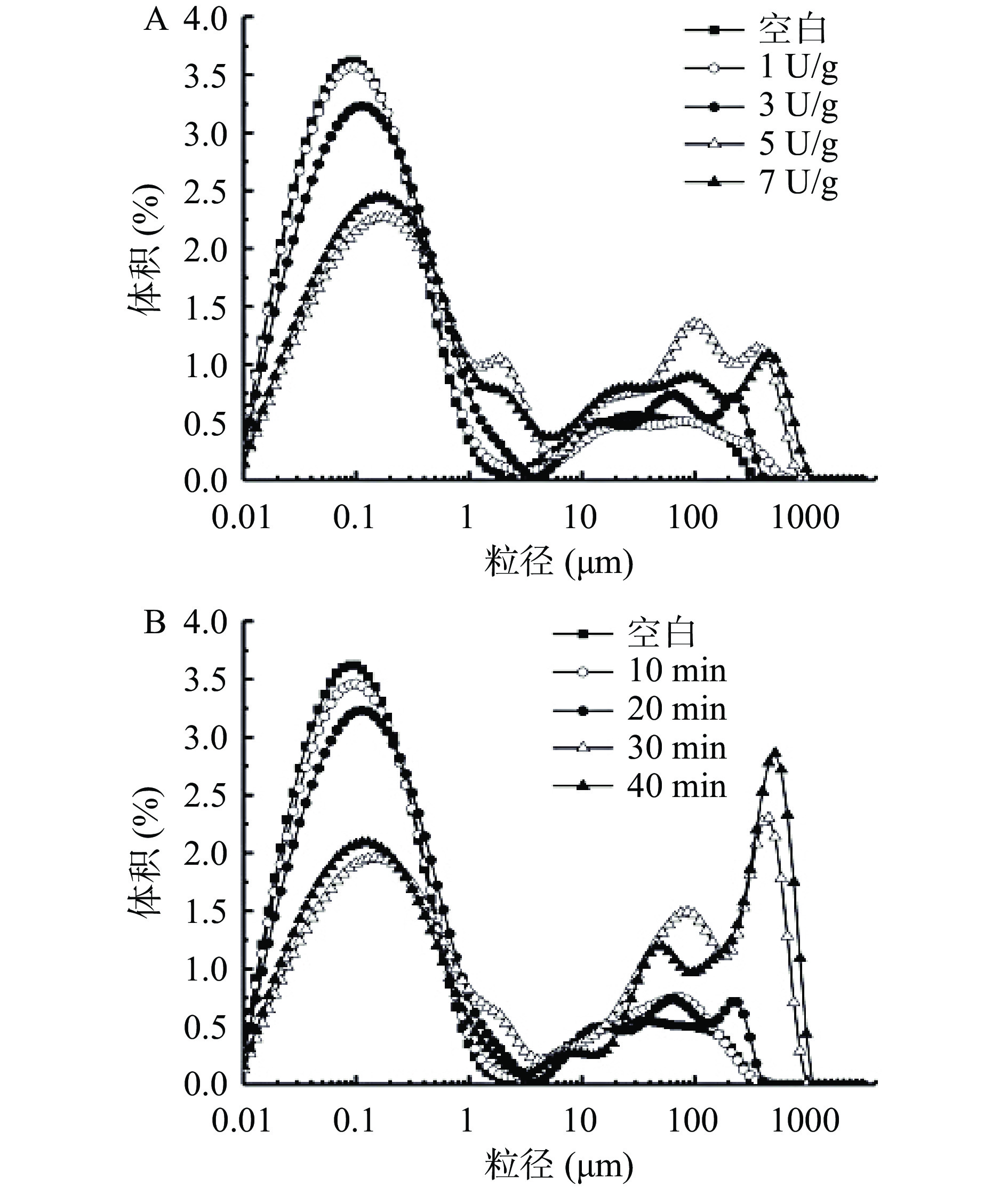
利用激光光散射技术测定不同TGase预交联程度的SPI粒径分布,如图1所示,随着TGase浓度的增大和交联时间的延长,蛋白颗粒的峰向分子更大的尺寸移动,在0.1 μm处的峰逐渐降低,而>100 μm的峰逐渐增大,当TGase的浓度最大为7 U/g或者TGase预交联时间为40 min时,粒径分布的峰面积最宽。此时,蛋白质中的赖氨酸ε-氨基作为酰基受体,与Gln的γ-酰氨基在TGase催化下分子内和分子间都会形成异肽键,多肽和蛋白之间发生共价交联产生更大粒径的蛋白聚集体[19-20],并随着TGase预交联程度的增加,蛋白分子聚集现象越剧烈,聚集体粒径逐渐变大[21]。
2.2 不同TGase预交联程度的SPI电泳
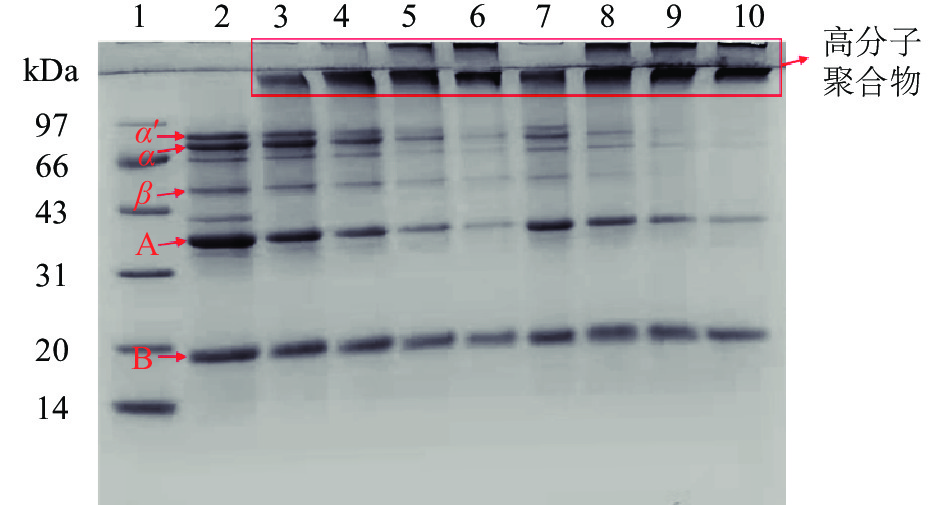
热处理后的SPI溶液在不同TGase浓度和不同交联时间下的SDS-PAGE如图2所示。未添加TGase的天然SPI,可以从分离胶中清晰地看到7S(α′、α、β)和11S(A、B)亚基条带分布。当添加TGase后,分离胶上部及浓缩胶中开始出现高分子聚合物条带。随着酶浓度的增加及预交联时间的延长,7S亚基(α′、α、β)及11S的A亚基条带颜色明显变浅,且大分子量的聚集体条带颜色逐渐加深,说明这些组分逐渐被TGase交联,生成聚合物。然而,11S的B亚基条带在反应过程中变化不明显,即使在7 U/g交联20 min或3 U/g交联40 min条件下,条带颜色仍然较深。电泳结果表明,大豆蛋白中的7S亚基及11S的A亚基是TGase的良好底物,而B亚基则难以被TGase交联,这可能与11S球蛋白的四级结构及11S的B亚基中谷氨酰胺/赖氨酸含量较低有关[22]。从条带消失的速度和程度来看,TGase交联SPI各组分的优先次序推断为7S>11S A亚基>11S B亚基。Hsieh等[18]也发现,与11S碱性蛋白相比,TGase交联11S酸性蛋白及7S速度更快,这与本研究的结果保持一致。
2.3 不同TGase预交联程度SPI凝胶的流变特性分析
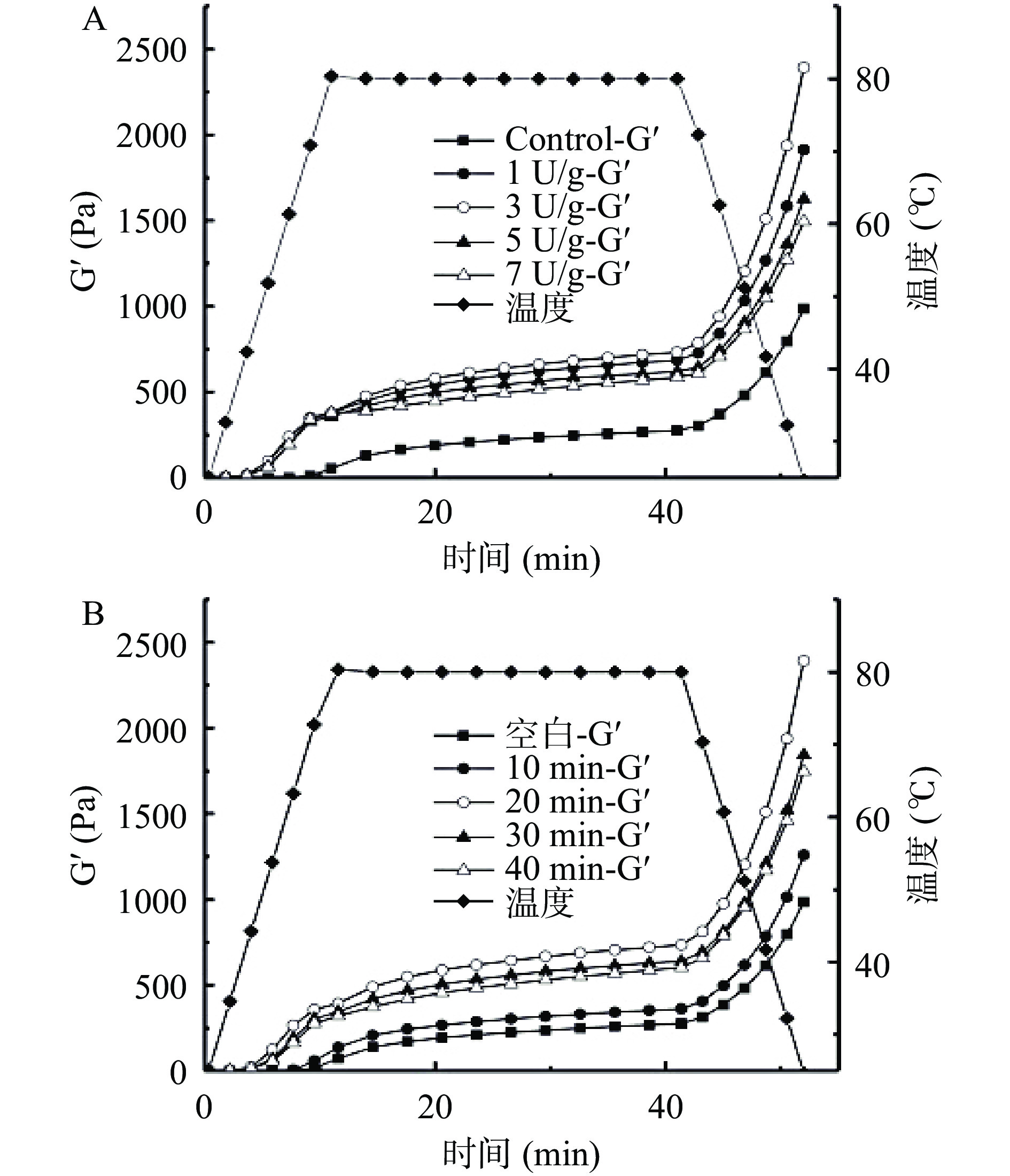
不同TGase预交联处理SPI在CaSO4诱导成胶过程中弹性模量(G')变化如图3所示,在升温和保温过程中疏水相互作用随温度的升高不断增加,蛋白分子进一步交联,凝胶的结构开始重排,SPI聚集体溶液逐渐从溶液状态变为固态凝胶结构,但这一阶段凝胶的弹性模量增加还较为缓慢。而在降温过程中,G′上升极为快速,此时体系内熵的降低,加强了凝胶网络中蛋白颗粒之间的氢键、范德华力等一些作用力,导致蛋白的弹性模量急剧增大[23-24]。
将温度扫描的终点值G′作为蛋白凝胶最终的弹性模量,如表1所示,对比未加入TGase的SPI样品,TGase催化了蛋白分子之间形成共价交联增强凝胶弹性和强度,显著提高凝胶的弹性模量(P<0.05),当TGase浓度为3 U/g或者当TGase交联时间为20 min时,凝胶的G′值最大,较未添加TGase CaSO4诱导形成的SPI凝胶提高了124.5%,这与Ozcan等[25]的研究结果相似。继续增加酶量或者延长交联时间,TGase的过度交联产生大的聚集体,会限制后续CaSO4成胶过程中蛋白分子的重排和其他分子间的相互作用,凝胶的网络结构受到损伤,结构不均匀,凝胶的弹性性能降低[26]。因此,适当的TGase预交联程度能提高CaSO4诱导SPI凝胶的弹性模量,增加凝胶强度,但过度交联反而使CaSO4诱导SPI凝胶变得更弱。
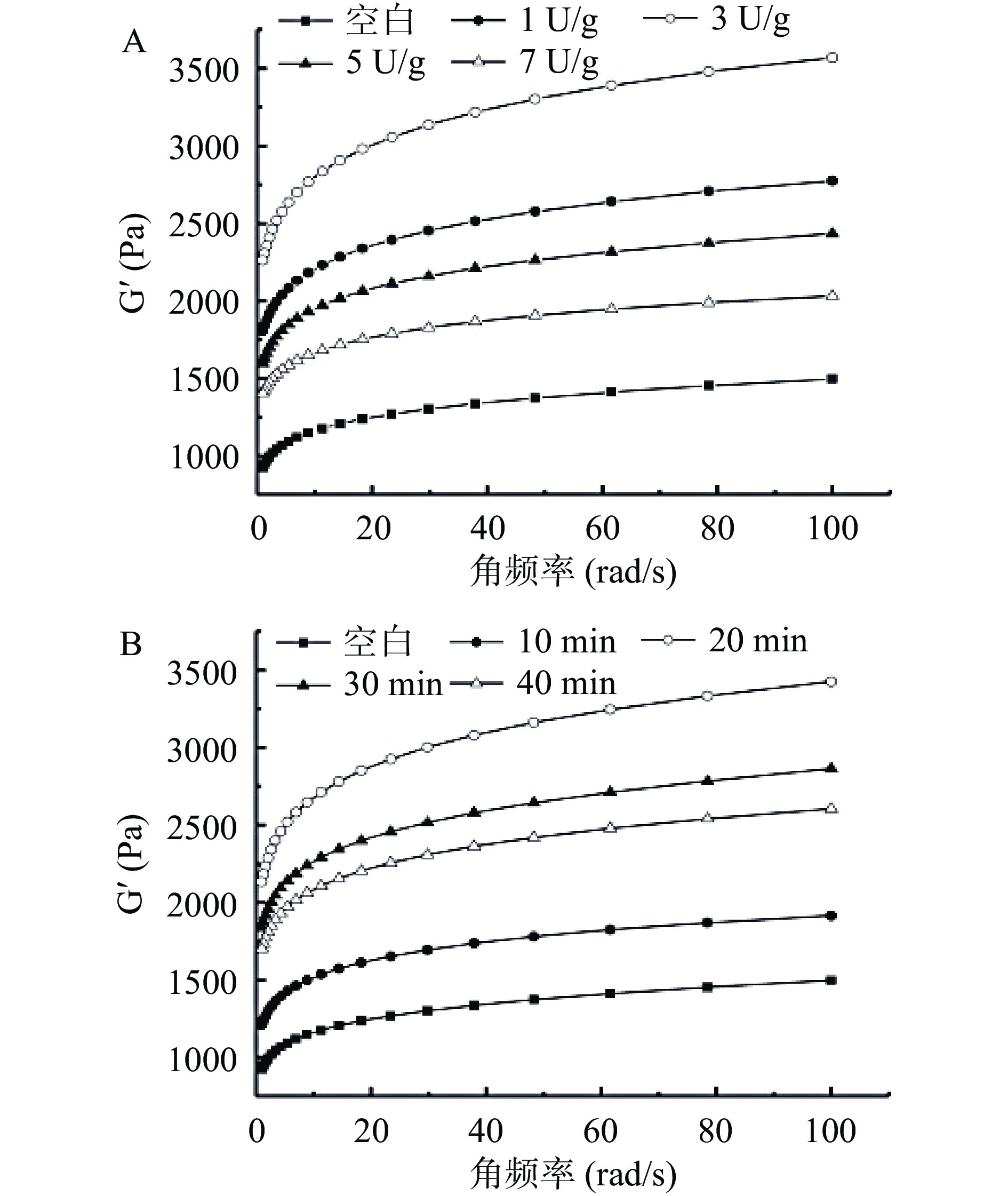
表 1 不同TGase预交联处理SPI凝胶温度扫描终点G′、频率扫描幂律模型拟合的n值、屈服应力和屈服应变Table 1. The G′ value, n value of power law model fitting, fracture stress and strain of SPI gels with different TGases pre-crosslinking treatments预交联程度 G′ (Pa) n 应力(Pa) 应变(%) 空白 1059.85±105.80d 0.1040±0.0001 a 508.00±62.80d 43.83±5.78d 1 U/g 2056.90±884.60b 0.1020±0.0014 a 1163.60±55.44c 65.65±1.48c 浓度 3 U/g 2379.15±18.00a 0.0937±0.0005b 1474.60±126.70b 91.00±5.80b 5 U/g 1617.50±12.02c 0.0903±0.0001c 1874.50±72.80a 103.00±2.83a 7 U/g 1417.00±18.38c 0.0013±0.0001d 1742.95±215.00ab 99.05±2.76ab 10 min 1377.45±129.40c 0.0980±0.0016a 620.67±98.10cd 50.55±5.73cd 时间 20 min 2379.15±18.00a 0.0937±0.0005a 1474.67±126.70a 91.00±5.80a 30 min 1792.67±138.90b 0.1011±0.0031a 1252.00±89.10b 70.70±5.66b 40 min 1830.95±120.30b 0.0936±0.0013b 762.50±53.03c 62.65±5.73bc 注:不同小写字母(a~d)表示同组内不同样品之间存在显著性差异(P<0.05)。 为了进一步探讨不同TGase预交联程度对CaSO4诱导的SPI凝胶的粘弹性及形成作用力性质差异,对凝胶进行了频率扫描实验,结果如图4。所有样品在1~100 rad/s的频率变化范围内,凝胶的G′都随着角频率ω的增大而逐渐增加,呈现弱的频率依赖性。使用幂律模型:G′=K·ωn来对G′和ω的关系进行拟合,指数n反映弹性模量对ω的依赖程度。n值大小可以用来表示形成凝胶结构中作用力的性质,n=0说明凝胶为化学性凝胶,由较强的共价键组成(例如二硫键、异肽键等),而n>0则表示物理性凝胶,即主要作用力为弱的非共价键(例如范德华力、氢键、疏水和静电相互作用)[27-28],拟合所得n值如表1。可以看到未加入TGase的蛋白样品n值接近于0.1,这是典型的物理性凝胶,即主要作用力为弱的非共价键。随着TGase浓度的增大和预交联时间的延长,n值逐渐降低,当TGase达到7 U/g时或交联时间为40 min时,n值达到最低值,更接近于0,说明TGase诱导SPI中更多ε-(-γ-Glu)Lys形成,在SPI凝胶网络中形成了化学共价键,此时蛋白凝胶结构中更多的化学性凝胶参与,凝胶结构更为复杂。
图5为不同凝胶样品的大形变实验结果,曲线上应力开始降低的点即凝胶的断裂点,此时的应力和应变值分别称为样品的屈服应力和屈服应变,结果如表1。相比未经TGase预交联的SPI凝胶,添加TGase进行预交联处理能促进蛋白凝胶内部的共价交联,增强SPI凝胶的结构,显著提高了凝胶的抗形变能力(P<0.05)。随着TGase浓度增大,预交联时间延长,凝胶的抗形变的能力呈现先增大后减小的变化趋势。当TGase浓度为5 U/g,预交联时间为20 min时,此时SPI凝胶的屈服应力和应变达到最高,为1874.50 Pa和103%,相较于未经TGase预交联处理的SPI凝胶分别提高了269.0%和135.0%,这与Tsevdou等[26]的研究结果相一致,进一步证明了适度TGase预交联能够显著改善CaSO4诱导形成的SPI凝胶性能。继续增大TGase浓度或延长预交联时间,凝胶的屈服应力和应变降低,凝胶结构变差,抵抗形变的能力减弱[29]。
2.4 不同TGase预交联程度SPI凝胶的凝胶持水力
图6显示了不同TGase预交联处理后CaSO4诱导形成的SPI凝胶的持水力。由图可知,未经TGase处理的SPI凝胶持水力为57.9%,TGase预交联能够显著提高SPI凝胶的持水力(P<0.05)。随着酶浓度的增加和预交联时间的延长,持水力呈先增大后下降的趋势,分别在5 U/g、20 min和3 U/g、30 min时达到最大,这与前文中凝胶流变特性和凝胶结构结果中的最优预交联条件不一致,可能原因是影响蛋白凝胶持水力的因素较为复杂,包括凝胶强度、凝胶结构、分子间作用力等,多种因素相互作用,共同决定了凝胶持水能力的大小[23]。在本研究中,适度的TGase预处理能显著提高凝胶的弹性模量,形成致密且均匀的凝胶结构,从而锁住凝胶中的水分[30-32]。虽然结果显示,当TGase浓度>5 U/g(预交联时间20 min)或预交联时间>20 min(3 U/g)时,SPI凝胶弹性模量开始降低(表1)、结构较为粗糙(图7),但此时凝胶内部较高含量的共价键(异肽键)及强分子间作用力可能有利于水分的保持。同时,TGase预交联过程中谷氨酰胺残基的脱酰胺反应也能够增加蛋白质的亲水性,提高凝胶的持水力[33]。然而,进一步延长预交联时间(40 min),SPI凝胶持水力显著下降(P<0.05),这可能主要取决于凝胶的结构,由图7e可知,经3 U/g的TGase交联40 min后形成的凝胶结构过于粗糙,疏松多孔,难以有效地将水分截留在凝胶基质中,从而凝胶持水力大幅度下降。
2.5 不同TGase预交联程度下CaSO4诱导SPI凝胶的微观结构
不同TGase预交联处理的SPI凝胶的微观结构如图7所示。对于未经TGase预处理的SPI凝胶,蛋白颗粒较小,孔隙多但分布均匀。TGase预交联后,明显观察到蛋白块状的聚集体出现,并随着TGase预交联程度的增大,TGase预交联形成的蛋白聚集体逐渐增大,蛋白颗粒间的孔隙明显的减少。当TGase浓度为3 U/g,预交联时间为20 min时,可以观察到此时凝胶结构最为均匀、致密。继续增加TGase浓度或延长预交联时间,发现凝胶结构开始逐渐变得粗糙,特别是经7 U/g TGase预交联20 min或3 U/g TGase预交联40 min时,形成的凝胶出现大的孔隙。这可能是由于蛋白过度交联,形成大的块状聚集体,不利于盐凝固剂的进一步作用,从而导致最终凝胶结构不均匀。这与流变的数据结果相印证,TGase过度预交联使CaSO4诱导形成的SPI凝胶的品质降低,粘弹性及抗形变能力减弱。
3. 结论
TGase能够催化谷氨酰胺与赖氨酸残基之间形成异肽键,促进蛋白质分子内或分子间的共价交联,形成高分子聚合物,进而影响CaSO4诱导的SPI凝胶的性质。相较于未经TGase预交联处理的SPI凝胶,适度的TGase的预交联处理(如3~5 U/g TGase预交联20 min或3 U/g TGase预交联20~30 min)能显著增强CaSO4诱导SPI凝胶的性能,包括凝胶的弹性模量、屈服应力、屈服应变、持水率,最高分别提升了124.5%、269.0%、135.0%及53.0%,同时使凝胶结构更加均匀、致密。但过度TGase预交联处理,包括TGase浓度过高,预交联时间过长,都会导致产生的蛋白聚集体过大,不利于后续均匀凝胶网络的形成,造成最终SPI凝胶结构粗糙、疏松多孔,凝胶弹性性能及持水率降低。研究结果对于大豆蛋白乃至植物蛋白凝胶制品的加工与质构改良具有重要的参考价值。
-
表 1 不同TGase预交联处理SPI凝胶温度扫描终点G′、频率扫描幂律模型拟合的n值、屈服应力和屈服应变
Table 1 The G′ value, n value of power law model fitting, fracture stress and strain of SPI gels with different TGases pre-crosslinking treatments
预交联程度 G′ (Pa) n 应力(Pa) 应变(%) 空白 1059.85±105.80d 0.1040±0.0001 a 508.00±62.80d 43.83±5.78d 1 U/g 2056.90±884.60b 0.1020±0.0014 a 1163.60±55.44c 65.65±1.48c 浓度 3 U/g 2379.15±18.00a 0.0937±0.0005b 1474.60±126.70b 91.00±5.80b 5 U/g 1617.50±12.02c 0.0903±0.0001c 1874.50±72.80a 103.00±2.83a 7 U/g 1417.00±18.38c 0.0013±0.0001d 1742.95±215.00ab 99.05±2.76ab 10 min 1377.45±129.40c 0.0980±0.0016a 620.67±98.10cd 50.55±5.73cd 时间 20 min 2379.15±18.00a 0.0937±0.0005a 1474.67±126.70a 91.00±5.80a 30 min 1792.67±138.90b 0.1011±0.0031a 1252.00±89.10b 70.70±5.66b 40 min 1830.95±120.30b 0.0936±0.0013b 762.50±53.03c 62.65±5.73bc 注:不同小写字母(a~d)表示同组内不同样品之间存在显著性差异(P<0.05)。 -
[1] ZHAO H, CHEN J, HEMAR Y, et al. Improvement of the rheological and textural properties of calcium sulfate-induced soy protein isolate gels by the incorporation of different polysaccharides[J]. Food Chemistry,2020,310:125983. doi: 10.1016/j.foodchem.2019.125983
[2] ZHU Q, ZHAO L, ZHANG H, et al. Impact of the release rate of magnesium ions in multiple emulsions (water-in-oil-in-water) containing BSA on the resulting physical properties and microstructure of soy protein gel[J]. Food Chemistry,2017,220:452−459. doi: 10.1016/j.foodchem.2016.10.016
[3] ZHAO Y Y, CAO F H, LI X J, et al. Effects of different salts on the gelation behaviour and mechanical properties of citric acid-induced tofu[J]. International Journal of Food Science & Technology,2020,55(2):785−794.
[4] 王旭峰. CaSO4诱导大豆分离蛋白乳状液凝胶性质影响因素的研究[D]. 无锡: 江南大学, 2017. WANG X F. Study of influencing factors on the properties of soy protein isolate emulsion gels induced by CaSO4[D]. Wuxi: Jiangnan University, 2017.
[5] 孟旭, 吴立业, 程超. 豆腐凝固过程的研究进展[J]. 中国调味品,1992(7):2−5. [MENG X, WU L Y, CHENG C. Research progress in tofu solidification process[J]. China Condiment,1992(7):2−5. [6] MYLLARINEN P, BUCHERT J, AUTIO K. Effect of transglutaminase on rheological properties and microstructure of chemically acidified sodium caseinate gels[J]. International Dairy Journal,2007,17(7):800−807. doi: 10.1016/j.idairyj.2005.10.031
[7] 任凯. 豆腐的物性评价模型构建及感官品质优化研究[D]. 南昌: 南昌大学, 2019. REN K. Establishment of tofu physical property evaluation model and sensory quality optimization[D]. Nanchang: Nanchang University, 2019.
[8] ERDEM N, BABAOGLU A S, POCAN H B, et al. The effect of transglutaminase on some quality properties of beef, chicken, and turkey meatballs[J]. Journal of Food Processing and Preservation,2020,44(10):14158.
[9] ALVES M C, PAULA M M D O, COSTA C G C D, et al. Restructured fish cooked ham: Effects of the use of carrageenan and transglutaminase on textural properties[J]. Journal of Aquatic Food Product Technology,2021,30(4):451−461. doi: 10.1080/10498850.2021.1895942
[10] 汪长青. 预处理对TG酶促小麦与大豆蛋白混合凝胶性质的影响[D]. 合肥: 合肥工业大学, 2018. WANG C Q. Effect of physicochemical pretreatment on transglutaminase-set wheat gluten and soy protein isolate mixture gel[D]. Hefei: Hefei University of Technology, 2018.
[11] 臧学丽, 陈光. 转谷氨酰胺酶对大豆蛋白凝胶特性及结构的影响[J]. 西北农林科技大学学报(自然科学版),2018,46(1):86−94. [ZANG X L, CHEN G. Influence of transglutaminase on soybean protein gel preparation and structure[J]. Journal of Northwest A & F University (Natural Science Edition),2018,46(1):86−94. [12] YASIR S B M, SUTTON K H, NEWBERRY M P, et al. The impact of transglutaminase on soy proteins and tofu texture[J]. Food Chemistry,2007,104(4):1491−1501. doi: 10.1016/j.foodchem.2007.02.026
[13] DUARTE L, MATTE C R, BIZARRO C V, et al. Review transglutaminases: Part II-industrial applications in food, biotechnology, textiles and leather products[J]. World Journal of Microbiology & Biotechnology,2019,36(1):1−20.
[14] EISSA A S, KHAN S A. Acid-induced gelation of enzymatically modified, preheated whey proteins[J]. Journal of Agricultural & Food Chemistry,2005,53(12):5010−5017.
[15] JAROS D, JACOB M, OTTO C, et al. Excessive cross-linking of caseins by microbial transglutaminase and its impact on physical properties of acidified milk gels[J]. International Dairy Journal,2010,20(5):321−327. doi: 10.1016/j.idairyj.2009.11.021
[16] GUO Y, HU H, WANG Q, et al. A novel process for peanut tofu gel: its texture, microstructure and protein behavioral changes affected by processing conditions[J]. LWT-Food Science and Technology,2018,96:140−146. doi: 10.1016/j.lwt.2018.05.020
[17] WAN Y, LIU J, GUO S. Effects of succinylation on the structure and thermal aggregation of soy protein isolate[J]. Food Chemistry,2018,245:542−550. doi: 10.1016/j.foodchem.2017.10.137
[18] HSIEH J F, YU C J, CHANG J Y, et al. Microbial transglutaminase-induced polymerization of beta-conglycinin and glycinin in soymilk: A proteomics approach[J]. Food Hydrocolloids,2014,35:678−685. doi: 10.1016/j.foodhyd.2013.08.020
[19] NOGUEIRA S N F, CASANOVA F, GAUCHERON F, et al. Combined effect of transglutaminase and sodium citrate on the microstructure and rheological properties of acid milk gel[J]. Food Hydrocolloids,2018,82:304−311. doi: 10.1016/j.foodhyd.2018.03.038
[20] DICKINSON E. Enzymic crosslinking as a tool for food colloid rheology control and interfacial stabilization[J]. Trends in Food Science & Technology,1997,8(10):334−339.
[21] 邓涵. 转谷氨酰胺酶交联协同热加工对豆腐品质特性和潜在致敏性的影响[D]. 南昌: 南昌大学, 2018. DENG H. Effect of cross-linking with transglutaminase and thermal processing on quality and potential allergenicity of tofu[D]. Nanchang: Nanchang University, 2018.
[22] CHANYONGVORAKUL Y, MATSUMURA Y, SAKAMOTO H, et al. Gelation of bean 11S globulins by Ca2+-independent transglutaminase[J]. Bioscience, Biotechnology, and Biochemistry,1994,58(5):864−869. doi: 10.1271/bbb.58.864
[23] LUO K, LIU S, MIAO S, et al. Effects of transglutaminase pre-crosslinking on salt-induced gelation of soy protein isolate emulsion[J]. Journal of Food Engineering,2019,263:280−287. doi: 10.1016/j.jfoodeng.2019.07.008
[24] HESARINEJAD M A, KOOCHEKI A, RAZAVI S M A. Dynamic rheological properties of Lepidium perfoliatum seed gum: Effect of concentration, temperature and heating/cooling rate[J]. Food Hydrocolloids,2014,35:583−589. doi: 10.1016/j.foodhyd.2013.07.017
[25] OZCAN Y T, LEE W J, HORNE D, et al. Effect of trisodium citrate on rheological and physical properties and microstructure of yogurt[J]. Journal of Dairy Science,2007,90(4):1644−1652. doi: 10.3168/jds.2006-538
[26] TSEVDOU M S, ELEFTHERIOU E G, TAOUKIS P S. Transglutaminase treatment of thermally and high pressure processed milk: Effects on the properties and storage stability of set yoghurt[J]. Innovative Food Science and Emerging Technologies,2013,17:144−152. doi: 10.1016/j.ifset.2012.11.004
[27] MAO L, ROOS Y H, MIAO S. Study on the rheological properties and volatile release of cold-set emulsion-filled protein gels[J]. Journal of Agricultural and Food Chemistry,2014,62(47):11420−11428. doi: 10.1021/jf503931y
[28] NAJI T S, RAZAVI S M A. New studies on basil (Ocimum bacilicum L.) seed gum: Part II-Emulsifying and foaming characterization[J]. Carbohydrate Polymers,2016,149:140−150. doi: 10.1016/j.carbpol.2016.04.088
[29] RENZETTI S, DAL B F, ARENDT E K. Microstructure, fundamental rheology and baking characteristics of batters and breads from different gluten-free flours treated with a microbial transglutaminase[J]. Journal of Cereal Science,2008,48(1):33−45. doi: 10.1016/j.jcs.2007.07.011
[30] ERCILI C D, LILLE M, LEGLAND D, et al. Structural mechanisms leading to improved water retention in acid milk gels by use of transglutaminase[J]. Food Hydrocolloids,2013,30(1):419−427. doi: 10.1016/j.foodhyd.2012.07.008
[31] LIU Y, ZHANG Y, GUO Z, et al. Enhancing the functional characteristics of soy protein isolate via cross-linking catalyzed by Bacillus subtilis transglutaminase[J]. Journal of the Science of Food and Agriculture,2021,101(10):4154−4160. doi: 10.1002/jsfa.11052
[32] LIU Y, HUANG L, ZHENG D, et al. Characterization of transglutaminase from Bacillus subtilis and its cross-linking function with a bovine serum albumin model[J]. Food and Function,2018,9(11):5560−5568. doi: 10.1039/C8FO01503A
[33] DOMAGALA J, NAJGEBAUER L D, WIETESKA S I, et al. Influence of milk protein cross-linking by transglutaminase on the rennet coagulation time and the gel properties[J]. Journal of the Science of Food and Agriculture,2016,96(10):3500−3507. doi: 10.1002/jsfa.7534
-
期刊类型引用(0)
其他类型引用(1)





 下载:
下载:



 下载:
下载:



