Preparation of Curcumin Nanoemulsion and Its in Vitro Simulated Digestion Characteristics
-
摘要: 为提高姜黄素的水溶性和生物可利用度,本研究以选择性水解大豆蛋白为乳化剂,构建了稳定的姜黄素纳米乳液运载体系,对纳米乳液的制备过程中均质压力的影响进行研究,并对纳米乳液的粒径、Zeta-电位、浊度、微观结构以及胃肠消化特性进行表征。结果表明,姜黄素的溶解度与油相有显著关系(P<0.05) ,溶解度从大到小分别为中链甘油三酯(MCT)>菜籽油>玉米油>橄榄油>大豆油。以50 MPa为均质压力,制备得到的乳液平均粒径最小(265.00±4.14 nm)、Zeta-电位绝对值较大(−30.77±0.71 mV)、浊度最低。分别以菜籽油和MCT为油相制备得到载姜黄素纳米乳能抵抗胃蛋白酶的消化,在胃部保持一定的界面张力使乳液维持原有形态,而在小肠中消化,游离脂肪酸释放率达60%。将菜籽油和MCT以不同比例进行复配,发现随着菜籽油比例的增加,姜黄素的生物可利用度和保留率显著降低,其中,以菜籽油:MCT=3:7为油相的乳液具备与以纯MCT为油相的乳液几乎相同的姜黄素生物可利用度和保留率,接近70%。研究结果对封装和释放高亲脂性功能成分的传递系统的设计具有重要指导意义。Abstract: In this study, a stable curcumin nanoemulsion delivery system was constructed using selectively hydrolyzed soy protein as the emulsifier to enhance the aqueous solubility and bioavailability of curcumin. The effect of homogenization pressure on nanoemulsions was investigated, and the particle size, zeta-potential, turbidity, microstructure, and the in vitro gastrointestinal digestion properties of nanoemulsions were determined. The solubility of curcumin was significantly (P<0.05) dependent on the type of oil, the solubility in four oil was medium chain triglycerides (MCT) > canola oil > corn oil > olive oil > soybean oil. The emulsions prepared under 50 MPa showed the smallest mean particle size (265.00±4.14 nm), larger zeta-potential (-30.77±0.71 mV), and the lowest turbidity. The curcumin-loaded nanoemulsions prepared with rapeseed oil and MCT could resist pepsin digestion and maintain a certain interfacial tension in the stomach to keep the emulsion in its original form, while being digested in the small intestine with a 60% release rate of free fatty acids. The bioavailability and retention of curcumin decreased significantly with the increasing in the ratio of canola oil to MCT. Among them, the emulsions formed with rapeseed oil:MCT=3:7 oil phase possessed almost the same bioavailability and retention of curcumin as those with pure MCT oil phase, close to 70%. The study would provide guide for the design of delivery systems to encapsulate and release high lipophilic functional components.
-
Keywords:
- curcumin /
- nanoemulsion /
- grease composition /
- in vitro digestion
-
姜黄素是姜黄根茎中提取的天然黄色色素,具有独特的风味和强烈的色泽,主要用作香料或食用色素[1],此外,其还因在抗菌、抗炎[2]、抗氧化、抗肿瘤、抗诱变、抗风湿、降血脂[3-4]等方面表现的突出生物活性及在糖尿病、骨质疏松、创伤性脑损伤、神经退行性疾病、肝损伤等疾病的治疗上表现的促进作用[5-6],而引起了人们的广泛关注。然而,与其他亲脂生物活性化合物(如β-胡萝卜素、辅酶Q10、植物甾醇)相比,姜黄素的生物利用度低、易于氧化和化学降解等特性使其应用受到了限制[7]。水包油乳液是姜黄素最有效的运载体之一,姜黄素溶解在油滴中,通过抑制其暴露于周围水中的氧和羟基离子,保护姜黄素免受化学降解[8]。乳液是由两种不混溶液体在机械剪切作用下形成的[9]。若只是简单的分散(如纯油相分散在纯水相中),即使在高能量条件下,也只会形成瞬态乳液。通过添加蛋白质可以起到稳定乳液的作用,但蛋白质的结构易受到环境影响而改变(如pH),从而影响乳液的稳定效果。根据热力学定律和能量最小原理,体系总会向着能量最低的状态发展,乳液会迅速发生分离以减少界面接触面积和自由能,导致絮凝、聚结、乳析、沉降等失稳现象的产生[10]。
在前期研究中[11],为了克服蛋白质乳液稳定性差的缺陷,本课题组对大豆蛋白进行选择性水解,发现部分水解后得到的多肽分子量较小,能够有效提高大豆蛋白的乳化活性,并且具有较高的表面活性,在油水界面灵活性高。许多研究表明,采用水解大豆蛋白作为乳化剂能够提高大豆蛋白的乳化性质和稳定性[12]。另外,利用酶法将大豆蛋白进行部分水解,大分子蛋白部分转化为小分子肽,更易于被人体消化吸收,并且可能产生一些特殊的生理功能,提高大豆蛋白的功能特性。乳液粒径的大小对包封姜黄素的化学稳定性起着至关重要的作用。尽管姜黄素是一种相对疏水的分子(lgP=3.29)[13],主要位于水包油乳液的油相中,但仍有一小部分姜黄素存在于水相中,这部分姜黄素在水相中更容易被化学降解。Kharat等[14]研究表明,随着乳液粒径尺寸的减小,乳液中油滴的比表面积增大,姜黄素在液滴内外的转移速率可能受到影响,进而影响其包封率。理想情况下,为了保护姜黄素,乳液的粒径应该相对较大,但这可能会降低乳化稳定性和生物可利用度。据报道,纳米乳液由于液滴尺寸小,对颗粒聚集和重力分离具有更好的稳定性并且能够提高胃肠道中包裹的亲脂成分的稳定性[15-17]。因此,合理控制乳液粒径大小对包封姜黄素,增强其稳定性有重要影响。此外,控制油相类型可以优化姜黄素在乳状液中的包封率[18-19]。Liang等[20]的研究表明,脂质消化率依次为:长链三酰甘油(LCT)<中链三酰甘油(MCT)<短链三酰甘油(SCT);Li等[21]也发现由MCT组成的脂质比由LCT组成的脂质消化更快,这可能与小肠环境中油脂(长链、中链或短链游离脂肪酸)中的脂肪酸组成不同有关。然而,这些研究只是提供了一些粗略的结论,并没有分析小肠消化过程中油脂组成对亲脂成分消化特性的影响。
因此本研究选用选择性水解大豆蛋白作为壁材,选择姜黄素溶解度较高的油相作为包材,采用不同的均质压力制备载姜黄素纳米乳液并进行表征,并探究油脂组成对油水乳剂中姜黄素消化特性的影响,为合理设计传递系统、提高姜黄素和其他具有生理活性的亲脂成分的生物可利用度提供理论依据。
1. 材料与方法
1.1 材料与仪器
低温脱脂豆粕 山东禹王集团;姜黄素(纯度95%)、中链甘油三酯(Medium chain triacylglycerol,MCT) 源叶生物科技有限公司;大豆油、玉米油、菜籽油 益海(泰州)粮油工业有限公司;葵花籽油、橄榄油 上海嘉里食品工业有限公司;胆盐、胃蛋白酶、胰酶 Sigma-Aldrich;其他试剂 分析纯,国药集团化学试剂有限公司。
FE28 pH计 梅特勒-托利多仪器(上海)有限公司;BSA224S-CW电子分析天平 赛多利斯科学仪器(北京)有限公司;CR21N高速离心机 Hinac;GYB高压均质机 上海东华高压均质机厂;DK-S26电热恒温水浴锅 上海森信实验仪器有限公司;FJ200-SH高速均质分散机 上海标本模型厂;Nano ZSE纳米粒度及Zeta电位仪 Malvern Panalytical;Ti-E-A1R激光共聚焦扫描显微镜 Nikon;BX43F光学显微镜 OLYMPUS。
1.2 实验方法
1.2.1 大豆分离蛋白及其选择性水解产物的制备
参考李伟伟[11]的方法采用碱溶酸沉和酶法制备大豆选择性水解产物(SPH)。豆粕和超纯水以1:10的比例混合。在pH保持在8.0的情况下搅拌2 h,将混合物离心(10000×g,4 ℃,25 min),取上清液。调上清液的pH=4.5,离心(10000×g,4 ℃,15 min)取沉淀。沉淀用适量超纯水复溶并将pH调至2.0,搅拌2 h使其完全溶解。再次离心(10000×g,4 ℃,10 min)取上清液,用双缩脲法测定溶液中蛋白浓度,并将蛋白溶液稀释至50 mg/mL,添加胃蛋白酶(E/S=1:10000)在37 ℃下水浴搅拌1 h,然后立即将pH调至7.0,溶液离心(10000×g,4 ℃,15 min)取上清液,冷冻干燥后得到选择性水解产物SPH。
1.2.2 姜黄素在不同油相中的溶解度
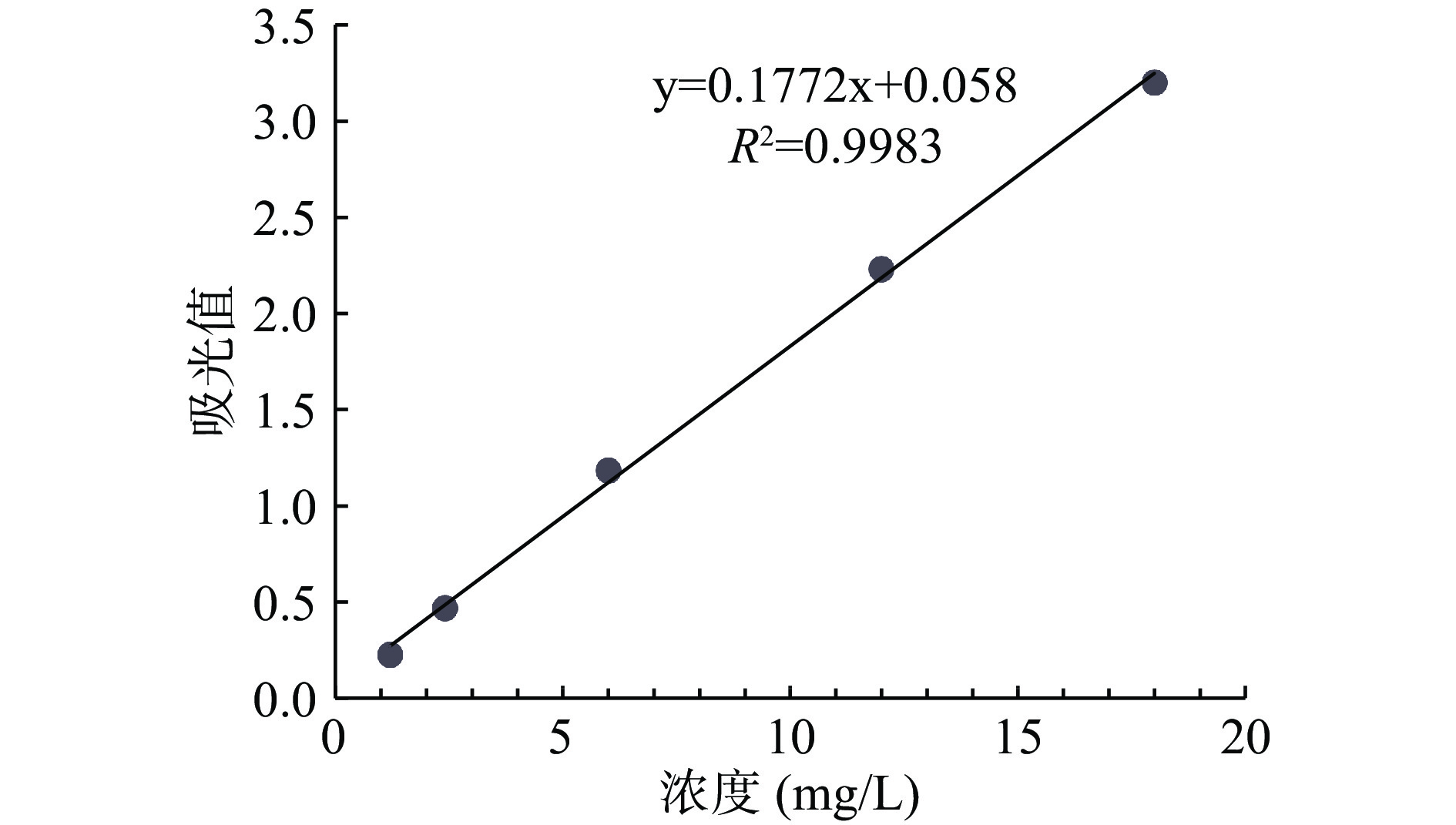
参考刘红星等[22]的方法,建立姜黄素浓度标准曲线:3 mg姜黄素溶解在50 mL的95%乙醇,取0.2、0.5、1.0、2.0和3.0 mL溶液,并依次用95%乙醇稀释至10 mL(姜黄素浓度从1.2 mg/L到18 mg/L,使用95%的乙醇作为空白),在425 nm处测定吸光度。以吸光度为Y轴,姜黄素浓度为X轴,得到姜黄素含量的标准曲线如图1。
分别取中碳链甘油三酯(MCT),大豆油,玉米油,菜籽油、橄榄油各50 mL,将其水浴加热至100 ℃,将0.75 g姜黄素溶解于五种不同的油相中,在100 ℃水浴中搅拌3 min,持续搅拌直至溶解完全后冷却到室温,再于3500×g条件下离心5 min取上清液,上清液需在室温避光储存24 h待用。吸取少量上清液并用95%乙醇适当稀释,在425 nm处测定吸光度,根据绘制的标准曲线将吸光值代入,得到姜黄素在各油相中的溶解度。
溶解度(mg/mL)=A−0.00580.1772 (1) 1.2.3 不同均质压力对乳液形成的影响
选用1.2.2筛选出的姜黄素溶解度较大的油相,与蛋白质水溶液以1:9(w/w)混合,配制2%(w/w)SPH溶液,以20000 r/min的速度进行高速剪切3 min后获得粗乳液[23],粗乳液分别采取30、40、50、60 MPa的均质压力经高压均质机循环两次,收集乳液进行后续测试。
1.2.3.1 平均粒径和粒径分布
采用动态激光光散射法(DLS)测定乳液的平均粒径和粒径分布。取10 µL乳液,用10 mmol/L磷酸缓冲溶液(pH7.0)将其稀释1000倍[22],取适量样品装入聚苯乙烯比色皿(折光指数1.330)中,测定温度为25±1 ℃,测定波长为658 nm,散射角度为133°,测定并记录平均粒径、粒径分布和多分散指数。所测样品均为新鲜配置,所有测量均重复三次,并取平均值。
1.2.3.2 Zeta-电位
取10 µL乳液,用10 mmol/L 磷酸缓冲溶液(pH7.0)将其稀释1000倍[24],将乳液加入毛细管样品池中,通过Nano ZSE纳米粒度及Zeta电位仪测定样品的Zeta-电位。
1.2.3.3 浊度
乳液的浊度采用透射光浊度法测定[25]。将待测样品稀释500倍,利用紫外分光光度计在500 nm处测定待测样品的吸光度[26]。
R=2.303A⋅VI (2) 式中:R为浊度;A为吸光值;V为稀释倍数;I为比色皿宽度。
1.2.3.4 乳液的微观结构
采用激光共聚焦扫描显微镜(CLSM)测定乳液的微观结构,在10×目镜和60×油镜下进行观测。用1 mg/mL 尼罗红溶液对脂质染色,用1 mg/mL FITC溶液对蛋白质染色,样品染色30 min后进行观测。尼罗红和 FITC 的激发波长分别为561和488 nm,发射波长分别为605和515 nm。
1.2.4 载姜黄素纳米乳液的体外消化特性
1.2.4.1 载姜黄素纳米乳液的制备
选择将MCT与菜籽油以不同比例进行复配作为油相来溶解姜黄素,并采用50 MPa的均质压力制备载姜黄素纳米乳,考察油相组成对载姜黄素纳米乳液的体外消化特性的影响。设置五组MCT与菜籽油不同配比的油相,其中菜籽油分别占0、30%、50%、70%、100%。将0.75 g姜黄素分别加载溶解在五组油相中,浓度为1 mg/g油脂,制备姜黄素负载乳状液。将得到的混合物加热到60 ℃,以1200 r/min搅拌2 h,然后超声处理20 min[27]。直至观察到油相中的姜黄素颗粒完全消失,即姜黄素在油相中完全溶解,否则应该重复此过程。制备乳液时油相与水相的比例为1:9,水相中溶解2%(w/w)的SPH。将混合物在高速剪切仪的作用下(20000 r/min)高速分散3 min后获得粗乳液,再将粗乳液通过高压均质机,在合适的均质压力均质两遍获得纳米乳。
1.2.4.2 体外模拟消化试验
由于乳液在口腔停留时间短,姜黄素纳米乳液在体内的消化用一个包含胃-肠阶段的体外模拟消化模型模拟。参考Peng等[28]、Zheng等[29]的方法制备模拟消化液。
胃消化阶段:将氯化钠(2 g/L)和盐酸(83.3 mmol/L或7 mL/L)在室温下完全溶解在双蒸馏水中制备模拟胃液(SGF)。实验开始前40 min将胃蛋白酶(3.2 mg/g)加入到SGF中,之后在室温下搅拌10 min,制备模拟胃液工作液(SGFWS)。实验前将剩余的SGF溶液放入冰箱(4 ℃)。
每次研究前,将1.2.4.1中制备的姜黄素纳米乳液和SGFWS预热至37 ℃,预热10 min。样品乳液(40 g)与SGFWS(40 g)混合,然后用0.25 mol/L盐酸调整pH为2.5,37 ℃水浴100 r/min连续搅拌2 h。
肠消化阶段:准备三种含有肠道成分的溶液,分别模拟肠道液体(SIF)、胆盐溶液、脂肪酶溶液。用150 mL双蒸馏水充分溶解氯化钙(5.5 g)和氯化钠(32.87 g),制得SIF。将胆盐(53.57 mg/mL)与磷酸盐缓冲液(5 mmol/L,pH7.0)在室温下连续搅拌过夜制备胆盐溶液。肠期反应前30 min制备脂肪酶溶液(24 mg/mL),将粉状脂肪酶与磷酸盐缓冲液(5 mmol/L,pH7.0)混合。使用前将其在水浴(37 ℃)中孵育。
取胃期采集的食糜(60 g)放入37 ℃水浴中。先调整样品pH7.0,再加入3 mL SIF(0.5 mol/L CaCl2,7.5 mol/L NaCl)和7 mL胆盐溶液(含375 mg胆盐),再调整样品pH7.0。最后加入5 mL脂肪酶溶液(含120 mg脂肪酶),在整个消化过程中记录维持中性pH所需的碱性溶液(0.25 mol/L NaOH溶液)的体积。
1.2.4.3 消化过程中乳液微观结构的观察
胃期和肠期在连续搅拌过程中在第30、60、90和120 min各取1 mL样品用于显微镜观察,观测前取5 μL样品,简单地进行搅拌,然后小心地放在载玻片上,盖上盖玻片,制片应避免产生气泡,用光学显微镜在100×物镜下进行观察。
1.2.4.4 游离脂肪酸(FFAs)释放的测定
用肠期中和溶液所需的NaOH体积(VNaOH)计算游离脂肪酸的释放百分比(方程假设,如果反应完成,每个甘油三酯分子会释放两种脂肪酸):
FFAs释放率(%)=VNaOHmNaOHMlipid2Wlipid (3) 式中:Mlipid为所用油的分子量;mNaOH为氢氧化钠溶液的量浓度(0.25 mol/L);Wlipid是消化系统中使用的油脂的重量(g)。
1.2.4.5 生物可利用率和保留率的测定
小肠阶段的体外消化过程结束后,样品分为两部分:一部分离心获得胶束样品,一部分无需处理作为总消化样品。
首先,取一部分消化后的总样品转移到离心管中,离心(18000×g,25 ℃,50 min)[30]后收集中间层所得的上清液作为混合胶束样品,总消化样品和初始样品无需进一步处理。使用氯仿萃取姜黄素,3500×g离心10 min。然后用紫外可见分光光度计在波长为425 nm测定姜黄素的浓度,并根据标准曲线,计算消化前初始样品中姜黄素的浓度(Cinitial)、混合胶束样品中姜黄素的浓度(Cmicelle)和总消化液样品中姜黄素的浓度(Cdigest)。
计算含姜黄素样品的生物可利用度和保留率。总消化液样品姜黄素含量值表示消化后小肠阶段姜黄素的总含量。
根据以下公式计算生物可利用度:
生物可利用度(%)=CmicelleCdigest×100 (4) 根据以下公式计算保留率:
保留率(%)=CdigestCinitial×100 (5) 1.3 数据处理
所有结果均以3个重复的平均值±标准差进行记录。所有图形都是用Origin软件绘制。样本比较采用单因素方差分析(ANOVA),使用IBM SPSS Statistics 23进行显著性差异分析。
2. 结果与分析
2.1 姜黄素在不同油相中的溶解度
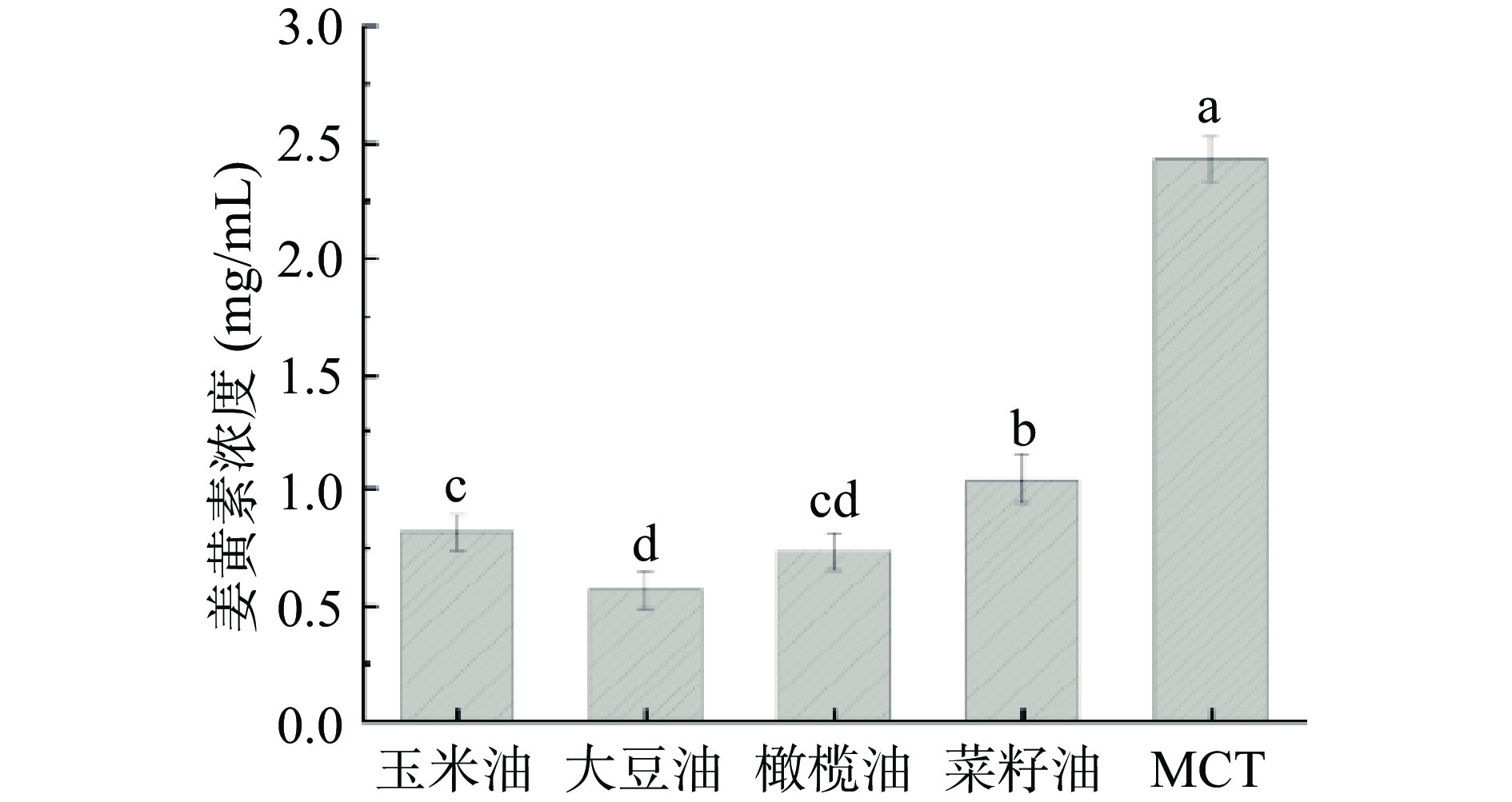
姜黄素在五种油相中的溶解度如图2所示:在100 ℃条件下,姜黄素在MCT中的溶解度为2.52±0.056 mg/mL,明显高于其他四种油相。相较于普通植物油,MCT的碳链较短,单位质量的MCT含有较多的极性基团,有利于其与姜黄素分子中的偶极基团形成偶极-偶极相互作用,促进其溶解[31]。此外,姜黄素分子加入脂质相也存在排斥体积效应[32]。当姜黄素分子被引入脂质相时,它周围会有一个区域,脂质分子的中心会被排除在外。因此,在这个被排除的区域内,脂质分子的浓度实际上为零,而它们在体脂相中的浓度等于单位体积内脂质分子的数量。在热力学上,由于与这个浓度梯度有关的渗透效应,脂质排除区域的存在其实是不利的。耗损脂质相的区域厚度随着脂质分子的分子量的增加而增加,因此MCT的影响更大一些,用MCT作为油相能够提高姜黄素的加载量。鉴于安全性和成本的考量,工业加工生产一般使用食用油作为原料。为给工业加工提供有效的参考,选用食用油中姜黄素溶解度最高的菜籽油作为油相来制备纳米乳液,探究均质压力对纳米乳液形成的影响。
2.2 均质压力对乳液形成的影响
2.2.1 平均粒径和粒径分布
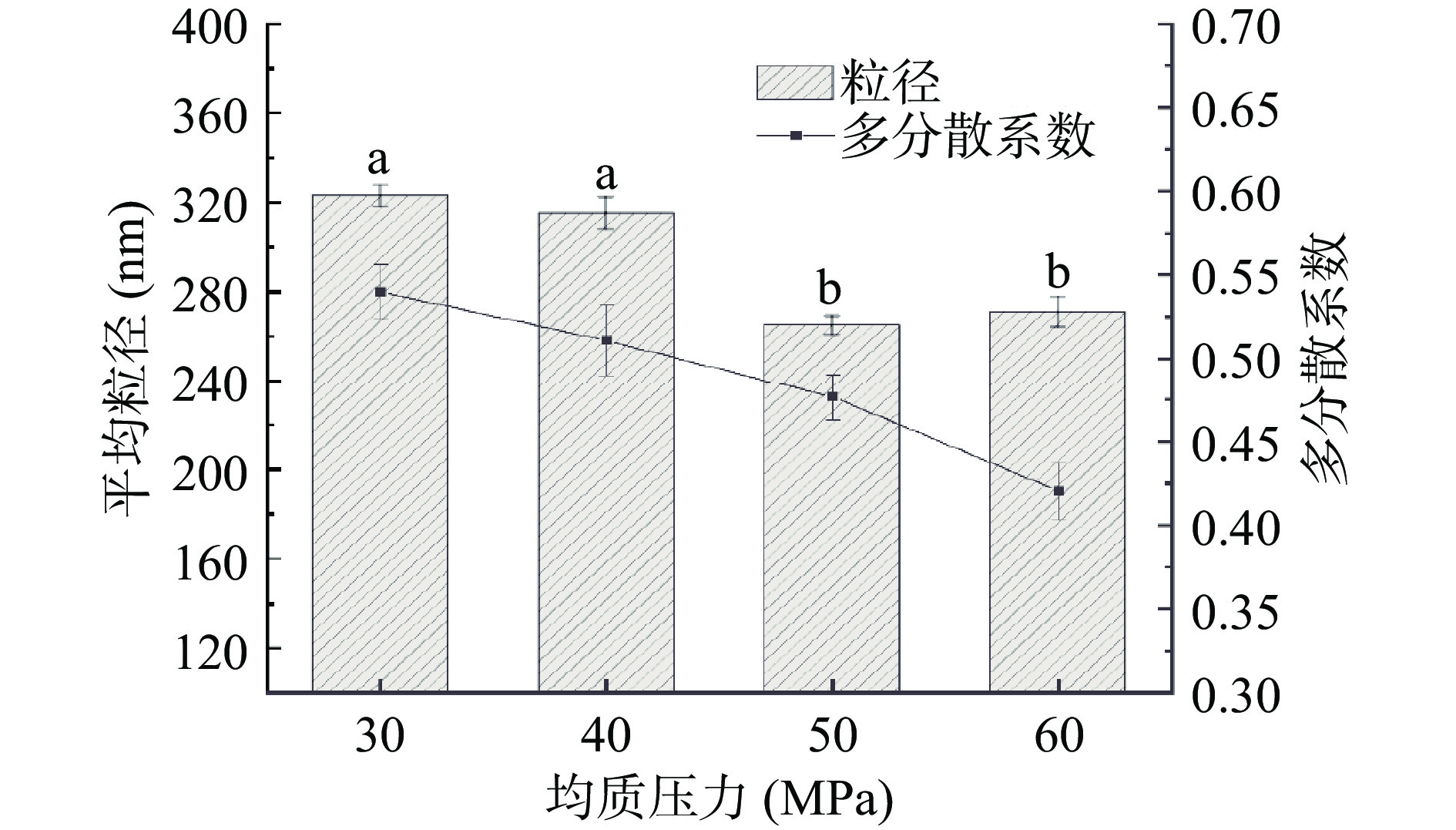
均质压力是影响纳米乳液粒径的重要因素,图3显示,随着均质压力的增加,液滴平均粒径减小,在均质压力为50 MPa时,获得的乳液平均粒径最小,为265.0±3.71 nm,当均质压力继续增加到60 MPa时,乳液平均粒径有增大的趋势,但不显著。高压均质过程中剪切力、空穴效应和撞击都会对乳液粒径造成影响,这些机械作用越强,液滴的粒径越小,分布越均匀。但均质压力过大时,乳液受到的冲击力就会过大,颗粒之间相互碰撞的次数增加,从而可能破坏界面膜而引发聚集现象[33]。与此同时,高压可能会引起蛋白质变性,变性的蛋白质分子互相作用形成聚集体,从界面脱落,溶解度下降,阻碍液滴被均质分散,从而降低均质效果[34]。
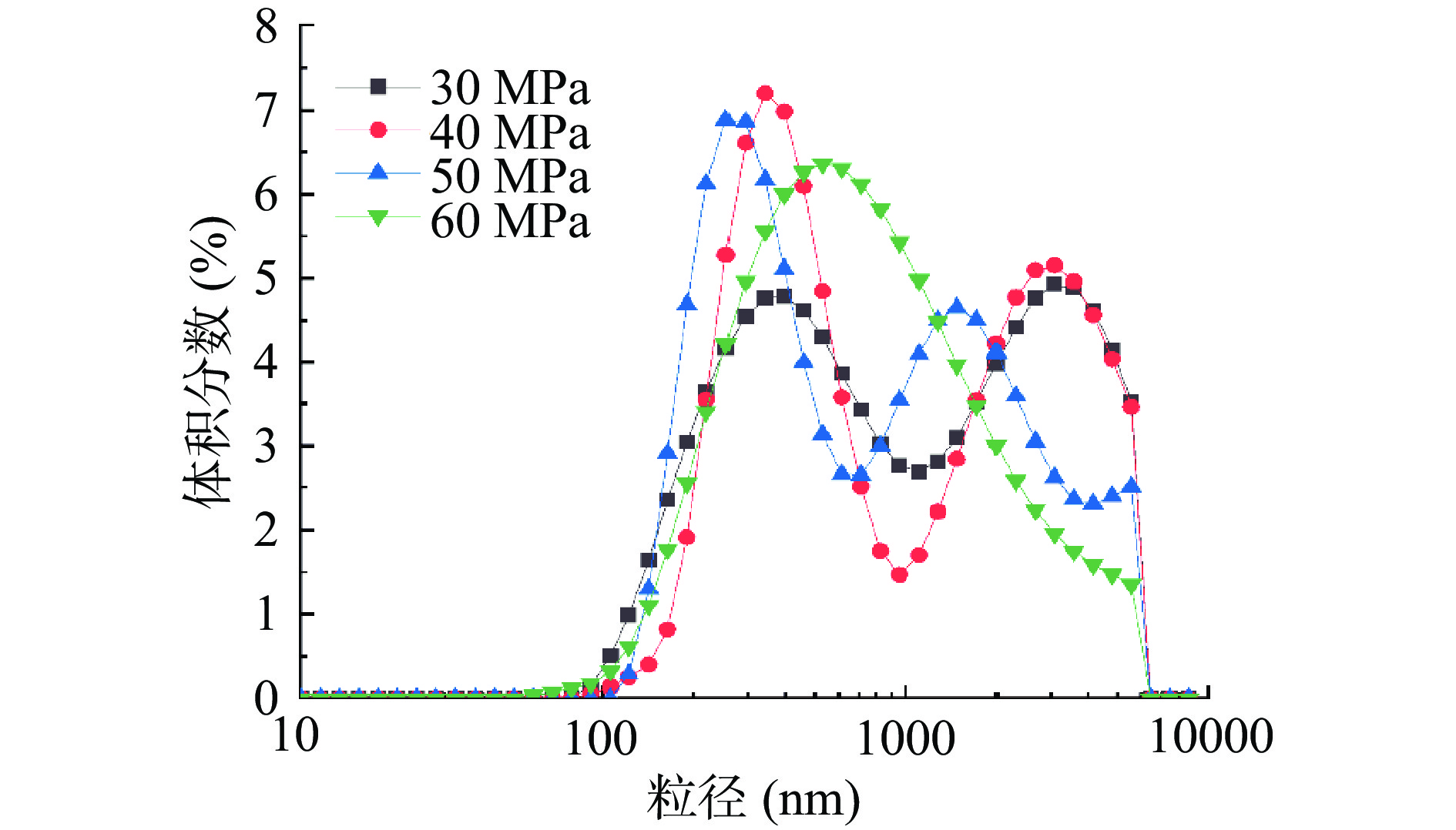
不同均质压力下的乳液粒径分布如图4。在30、40、50 MPa的压力下,乳液粒径都呈双峰分布,随着均质压力增大,大粒径逐渐减少,峰分布变窄,双峰靠拢,乳液的多分散系数也逐渐降低(图3),说明乳液中液滴尺寸差距逐渐缩小。乳液的粒径减小,不仅可以提升乳液的稳定性,还有助于提高非水溶性营养成分的生物利用率[35]。当均质压力增大到60 MPa时,粒径呈现单峰分布,说明此时乳液中的液滴大小分布均匀。
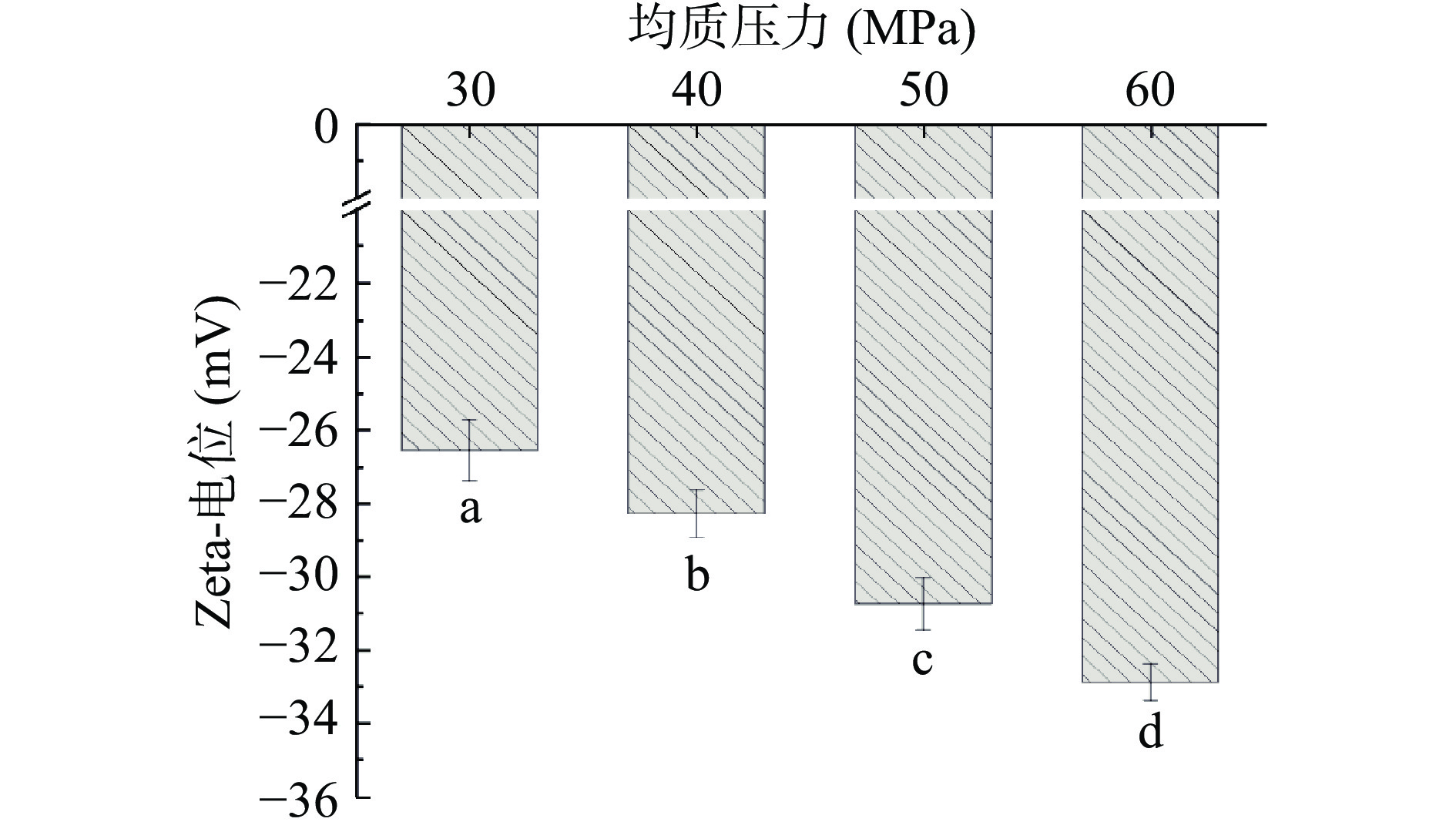
2.2.2 Zeta-电位
Zeta-电位与溶液中粒子表面的电势有关。通常情况下,表面电位的绝对值越大,粒子因强静电斥力而对聚集的阻力越大。根据乳滴在施加电场下移动的速率和方向来确定它携带的电位值,一般认为乳液净电位值大于30 mV时就能够提供足够的静电斥力稳定乳液[32]﹐故依据电位值可以初步分析乳液的稳定性。大豆蛋白结构中存在的亲水基团可与水分子间形成氢键,在纳米乳的表面形成水膜层,使乳滴表面带负电。从图5中可以看出,随着均质压力增大,乳液的Zeta-电位绝对值也增大。在50 MPa和60 MPa的均质压力下制备的乳液,其Zeta-电位绝对值都大于30 mV,说明它们都具有一定的稳定性。
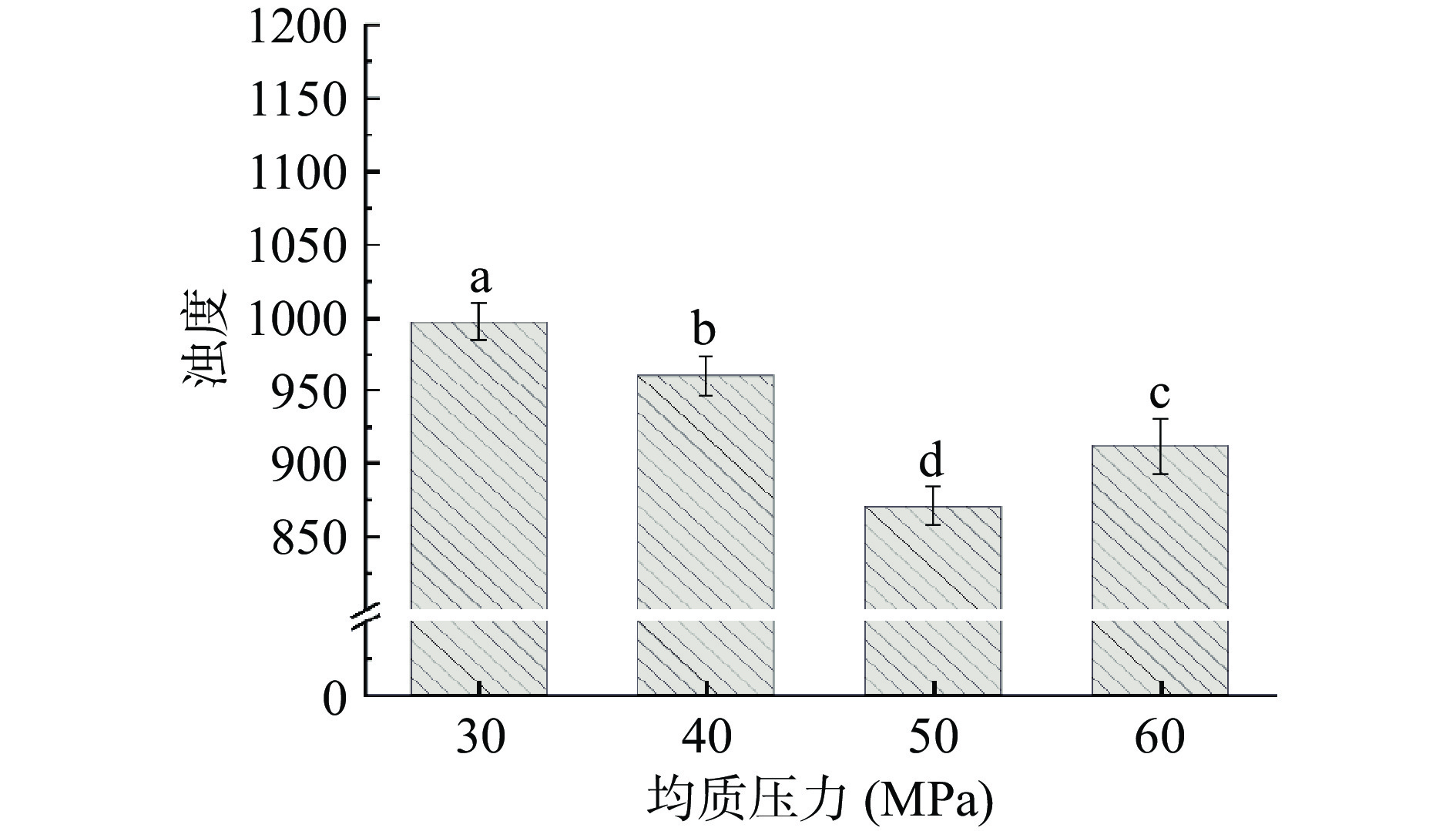
2.2.3 乳液浊度
分散相的浊度受粒径大小影响。粒径越大,纳米乳液的透明度越低,浊度越大[36]。同时,分散相的浊度受浓度影响,浓度越高,光散射效应越强,可见光的穿透率越低,浊度越大。如图6所示,乳液的浊度在均质压力从30 MPa增大到50 MPa时逐渐减小,而在均质压力继续增大到60 MPa,乳液浊度反而增大,这样的变化极有可能是受乳液的粒径大小影响的。结合图3,随着均值压力从30 MPa增大到50 MPa,乳液的平均粒径在逐渐减小,因此浊度也在逐渐减小。而在均质压力继续增大至60 MPa时,乳液中的蛋白质分子形成了聚集体,导致粒径增大,因此浊度也增大。
2.2.4 乳液的微观结构
采用激光共聚焦显微镜对乳液的微观结构进行表征,如图7所示。脂质液滴与尼罗红结合呈红色,蛋白质与FITC结合呈现荧光绿色。当均质压力从30 MPa增大到50 MPa,得到的乳液粒径更小,分布更均匀。然而,均质压力继续增大到60 MPa,液滴聚集程度有所增加,有部分蛋白形成了明显的聚集体。综上结果,均质压力为50 MPa得到的纳米乳液粒径较小且分布均匀,因此采用该均质压力进行后续实验。
2.3 载姜黄素纳米乳的体外消化特性
根据前面得到的结果,选择将MCT与菜籽油以不同比例进行复配作为油相来溶解姜黄素,并采用50 MPa的均质压力来制备载姜黄素纳米乳液,该姜黄素纳米乳液的包埋率达90%以上,具有较好的包埋效果。并用一个包含胃-肠阶段的体外消化模型模拟消化环境,考察姜黄素在胃肠消化过程中的释放情况。
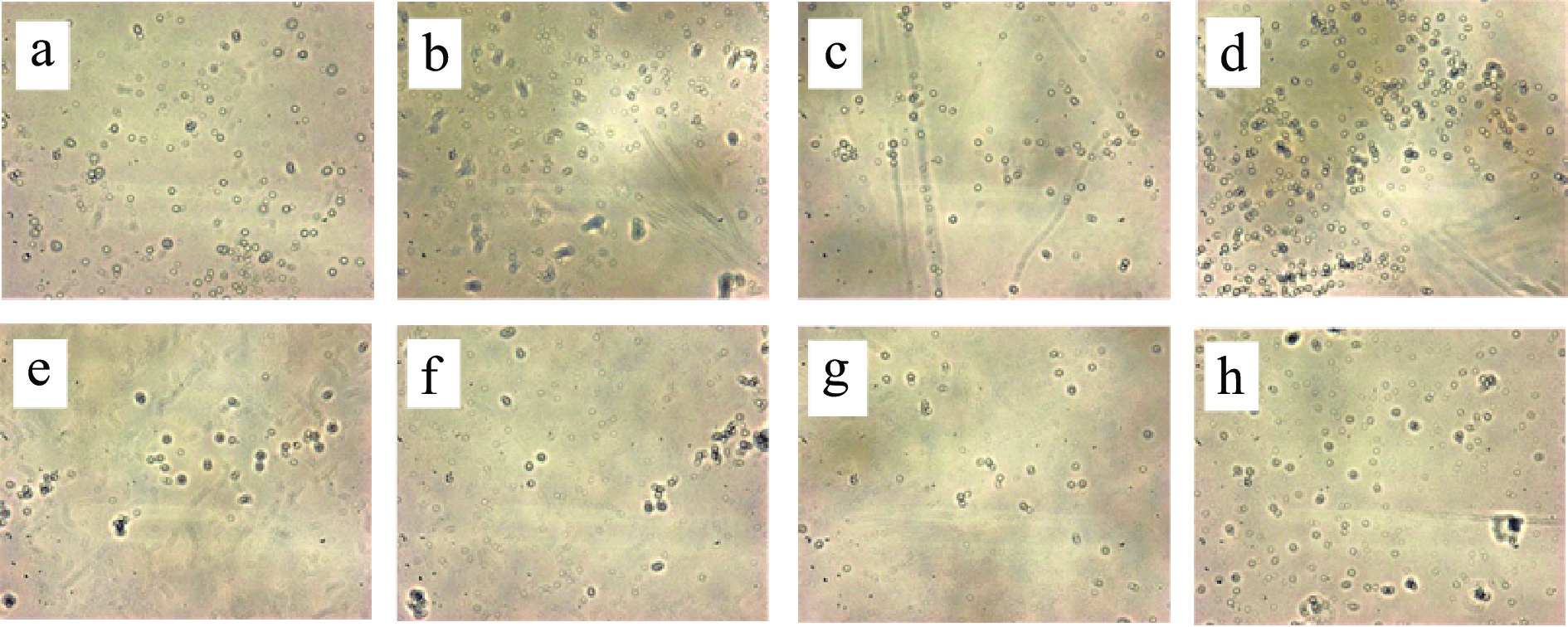
2.3.1 乳液微观结构(胃期)
分别以菜籽油和MCT为油相,在50 MPa的均质压力下制备载姜黄素纳米乳,考察其在模拟体外消化过程中微观结构的变化。由图8可见,纳米乳在SGFWS中消化时并没有发生明显的絮凝,说明在胃部消化阶段,纳米乳能抵抗胃蛋白酶的消化,保持一定的界面张力使乳液维持原有形态。而以未改性大豆蛋白为乳化剂制备的纳米乳液滴在此期间会发生絮凝(结果未展示),可能是油体之间的范德华效应和疏水引力导致的[37],同时磷脂和蛋白质在胃液的高酸性环境中都会发生质子化,导致负电荷减少,正电荷增加,胃液中的电解质通过静电屏蔽作用来降低表面电位的大小,作用于液滴之间的远程静电斥力减弱导致絮凝。不同油相制备的纳米乳在胃部消化中没有表现出明显的差异。
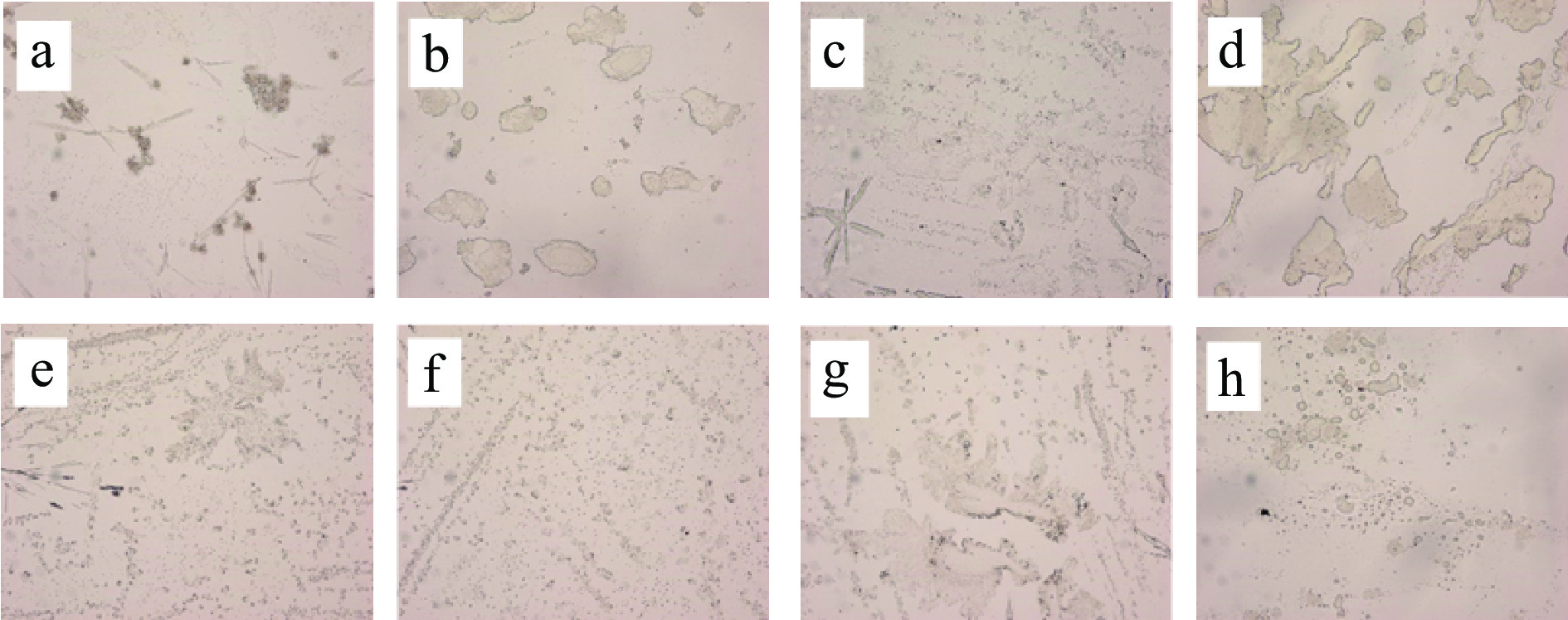
2.3.2 乳液微观结构(肠期)
图9显示,纳米乳在小肠中开始发生消化。消化前期脂滴分散,因为胃糜进入小肠后,胆盐快速结合到脂滴表面起乳化作用。随着消化时间增长,在消化结束时都出现了大油滴,可能是胰酶催化蛋白质水解产生小肽或氨基酸,不足以维持液滴形态,油脂不断凝结。乳液体系在消化过程中逐渐瓦解,脂质消化产生的游离脂肪酸和单甘油酯形成了胶束、钙皂、囊泡和其他胶体颗粒。30 min后MCT纳米乳分散均匀,而菜籽油纳米乳还存在大块聚集,说明MCT纳米乳的在小肠的消化比较快。消化结束后菜籽油消化程度低,形成油滴更大。
选择将MCT与菜籽油以不同比例进行复配作为油相来溶解姜黄素,并继续采用50 MPa的均质压力制备载姜黄素纳米乳,考察油相组成对游离脂肪酸释放以及姜黄素生物可利用度和保留率的影响。
2.3.3 FFAs的释放
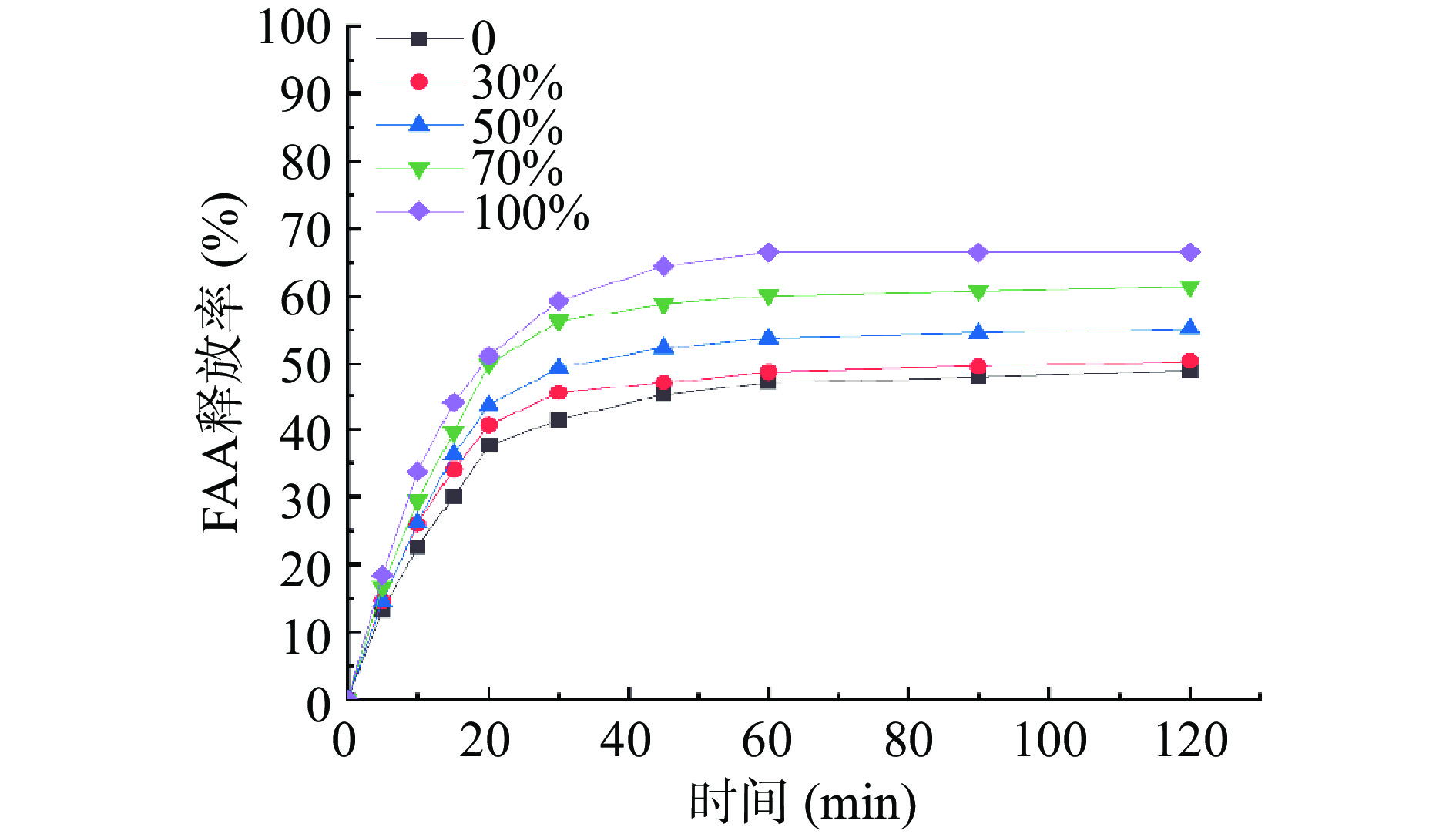
游离脂肪酸(FFAs)释放率受脂质在消化液中的分散特性影响,脂肪酶需要结合到油水界面才能发挥消化作用,油脂与脂肪酶的接触面积大,有利于脂肪水解反应速率和消化程度的提升。前20 min五组乳液FFAs释放速率均较快(图10),这段时间胆盐吸附在油水界面发挥作用,脂肪酶大量接触脂质并催化水解其内部的甘油三脂。释放速率随消化时间增加而减缓,可能是由于油水界面的胆盐趋向饱和,脂解产物在乳状液表面堆积阻碍了脂肪酶接触脂质[29]。菜籽油在油相中占比越大,纳米乳最终的FFAs释放率越低,可能是受乳液粒径和粘度的影响。姚艳玉等[38]、李朝阳等[39]发现油相种类会影响乳液粒径,相比含LCT的乳液,以MCT为油相的纳米乳具有更小的粒径。菜籽油中甘油三酯多为LCT,因此油相中菜籽油含量高,乳液的粒径可能更大,不利于消化。同时菜籽油粘度较大,蛋白和脂质的水解物更易被覆在油水界面,这种竞争吸附阻碍脂肪酶催化脂质水解,同时粘度大造成的粘连和聚集也会抑制脂质水解。
随着菜籽油的比重增加,FFAs释放率变得越来越低也可能是由于菜籽油当中有较多长链脂肪酸积聚在液滴表面[40],从而抑制脂肪酶对乳化甘油三酯的消化。中链游离脂肪酸比长链游离脂肪酸更容易在水相中分散,因此不容易在液滴表面聚集,抑制脂质消化[37],故FFAs释放率更高一些。
2.3.4 姜黄素生物可利用度和保留率
在小肠消化阶段,随着脂质水解,姜黄素可从脂滴中释放出来,进入由胆盐、游离脂肪酸和磷脂组成的混合胶束中,混合胶束再将姜黄素转运至小肠上皮细胞吸收,胶束化是姜黄素生物可利用的前提条件[41]。
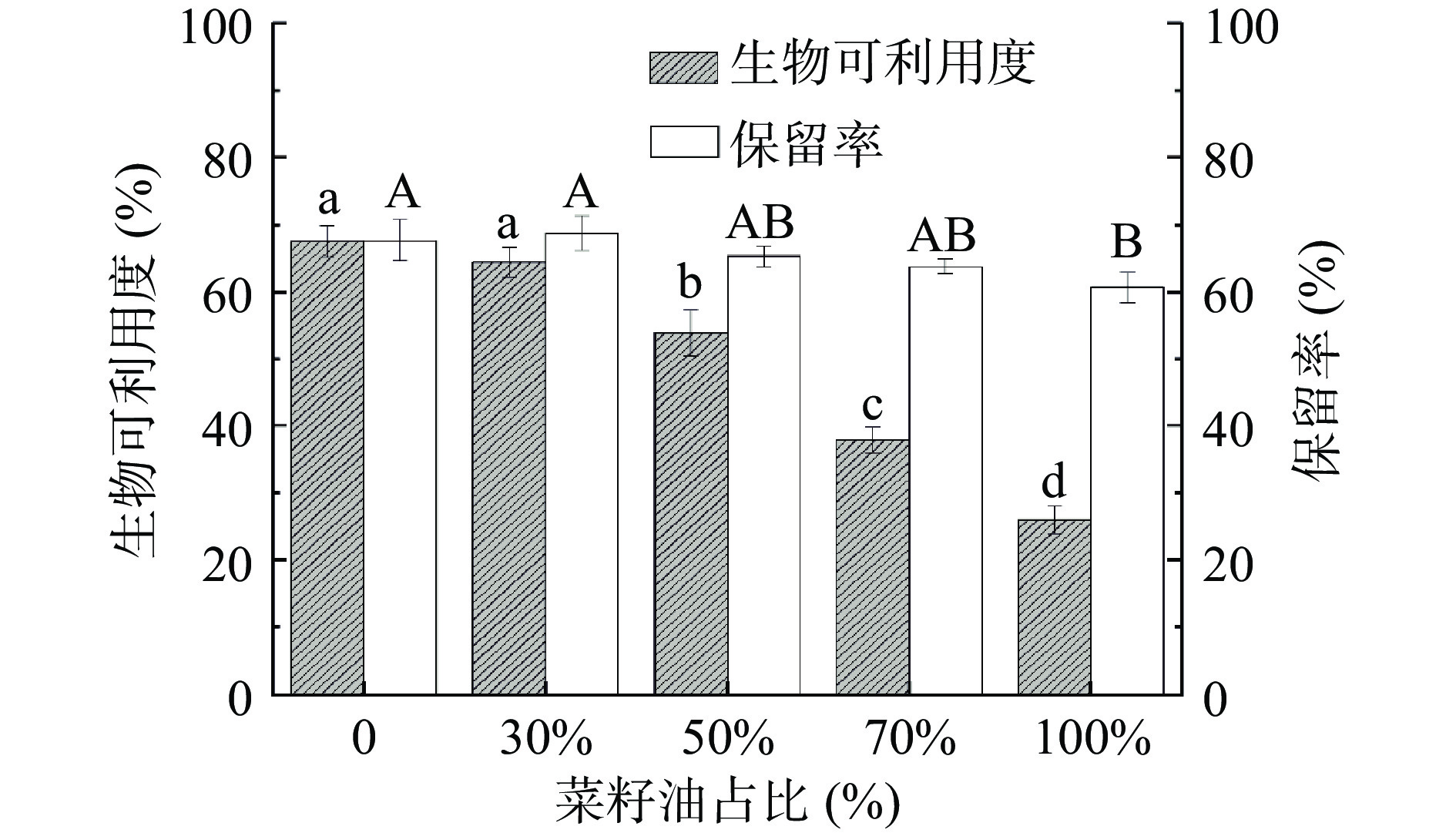
改变油相中菜籽油、MCT的配比,考察乳液消化后的生物可利用度和保留率。从图11可知,随着菜籽油在油相中占比升高,姜黄素的生物可利用度降低。据报道[42],生物可利用度和FFAs释放率呈正相关。油相的水解产物是胶束相的主要成分,水解程度低不利于胶束相形成,也不利于姜黄素从油相中释放,导致较低的生物可利用度[43]。脂肪酸酰基链的长度也会影响营养素的生物可利用度。影响研究表明[44],长链脂肪酸通常有助于改善类胡萝卜素的生物可利用度。当菜籽油:MCT=3:7时,姜黄素的生物可利用度和保留率都与纯MCT乳液无显著差异(P>0.05)。
考察乳液消化后的保留率实则是为了反映乳液的稳定性。图11显示,随着菜籽油在油相中占比升高,姜黄素的保留率降低。该结果与生物可利用度的结果相一致,说明在载体脂质中包含MCT能够显著提高姜黄素的生物可利用度,这是因为它能够形成混合胶束,溶解高亲脂性组分[28]。
3. 结 论
课题组发现,姜黄素在MCT中的溶解度最大,为2.52±0.056 mg/mL,其次是菜籽油。制备的姜黄素纳米乳液具有原料廉价易得,较高的乳化活性和较好的稳定性等突出的优势,对乳液制备条件进行优化,得到最适均质压力为50 MPa,此时乳液平均粒径最小、Zeta-电位较大,可以形成较为稳定的运载体系。以菜籽油或者MCT为油相来制备纳米乳液,在胃消化过程中都可以保持结构的稳定,并在肠道中被消化。油相的组成对姜黄素的生物可利用度和保留率有显著影响,姜黄素生物可利用度以及保留率依赖于油相组成。随着菜籽油占比的增加,纳米乳液FFAs释放率降低,这种现象可能是受乳液粒径和粘度的影响,并且蛋白和脂质的水解物覆在油水界面,造成粘连和聚集会抑制脂质水解,不利于消化。相反,菜籽油占比减少时,MCT占比增加,更多的混合胶束来溶解释放的姜黄素形成,从而增加了姜黄素的生物可利用度。本研究利用大豆蛋白水解物制备了纳米乳液来作为姜黄素的递送体系,具有独特的优势。利用纳米乳液进行包埋递送增强了姜黄素的生物相容性和生物可利用率,基于递送系统对不同功能性活性物质进行包埋对于活性物质的有效利用和功能最大化具有重要的意义,研究结果为合理设计传递系统,并提高姜黄素和其他具有生理活性的亲脂成分的消化特性提供理论指导。另外,除了油相组成,油相的含量以及壁材的组成对姜黄素的生物可利用度和保留率也有影响,这也是本课题组后期继续研究的方向。
-
-
[1] TAYYEM R F, HEATH D D, AL-DELAIMY W K, el al. Curcumin content of turmeric and curry powders[J]. Nutrition and Cancer-An International Journal,2006,55(2):126−131. doi: 10.1207/s15327914nc5502_2
[2] 魏雨菲, 于海川, 刘雪玲, 等. 姜黄主要化学成分及药理作用研究进展[J]. 新乡医学院学报,2020,37(10):990−995. [WEI Y F, YU H C, LIU X L, et al. Research progress on main chemical constituents and pharmacological effects of curcuma longa[J]. Journal of Xinxiang Medical College,2020,37(10):990−995. doi: 10.7683/xxyxyxb.2020.10.020 [3] HATCHER H, PLANALP R, CHO J, et al. Curcumin: From ancient medicine to current clinical trials[J]. Cellular and Molecular Life Sciences,2008,65(11):1631−1652. doi: 10.1007/s00018-008-7452-4
[4] HAMAGUCHI T, ONO K, YAMADA M. Review: Curcumin and alzheimer's disease[J]. CNS Neuroscience & Therapeutics,2010,16(5):285−297.
[5] ABD EL-HAKIM Y M, EL-HOUSEINY W, EL-MURR A E, et al. Melamine and curcumin enriched diets modulate the haemato-immune response, growth performance, oxidative stress, disease resistance, and cytokine production in oreochromis niloticus[J]. Aquatic Toxicology,2020,220:105406. doi: 10.1016/j.aquatox.2020.105406
[6] ABDELSAMIA E M, KHALEEL S A, BALAH A, et al. Curcumin augments the cardioprotective effect of metformin in an experimental model of type I diabetes mellitus; Impact of Nrf2/HO-1 and JAK/STAT pathways[J]. Biomedicine & Pharmacotherapy,2019,109:2136−2144.
[7] MCCLEMENTS D J, JAFARI S M. Improving emulsion formation, stability and performance using mixed emulsifiers: A review[J]. Advances in Colloid and Interface Science,2018,251:55−79. doi: 10.1016/j.cis.2017.12.001
[8] JIANG T, LIAO W, CHARCOSSET C. Recent advances in encapsulation of curcumin in nanoemulsions: A review of encapsulation technologies, bioaccessibility and applications[J]. Food Research International,2020,132:109035. doi: 10.1016/j.foodres.2020.109035
[9] SUN L H, LV S W, CHEN C H, et al. Preparation and characterization of rice bran protein-stabilized emulsion by using ultrasound homogenization[J]. Cereal Chemistry,2019,96(3):478−486. doi: 10.1002/cche.10147
[10] SARKAR A, HORNE D S, SINGH H. Interactions of milk protein-stabilized oil-in-water emulsions with bile salts in a simulated upper intestinal model[J]. Food Hydrocolloids,2010,24(2−3):142−151.
[11] 李伟伟. 高乳化性大豆蛋白的制备及其界面流变性质的研究[D]. 无锡: 江南大学, 2017 LI W W. Preparation of high-emulsifying soy protein and study on the interfacial shear rheology[D]. Wuxi: Jiangnan University, 2017.
[12] SHEN P, ZHOU F, ZHANG Y, et al. Formation and characterization of soy protein nanoparticles by controlled partial enzymatic hydrolysis[J]. Food Hydrocolloids, 2020, 105: 105844.
[13] ZEMBYLA M, MURRAY B S, SARKAR A. Water-in-oil Pickering emulsions stabilized by water-insoluble polyphenol crystals[J]. Langmuir,2018,34(34):10001−10011. doi: 10.1021/acs.langmuir.8b01438
[14] KHARAT M, ABERG J, DAI T T, et al. Comparison of emulsion and nanoemulsion delivery systems: The chemical stability of curcumin decreases as oil droplet size decreases[J]. Journal of Agricultural and Food Chemistry,2020,68(34):9205−9212. doi: 10.1021/acs.jafc.0c01877
[15] SOLANS C, IZQUIERDO P, NOLLA J, et al. Nano-emulsions[J]. Current Opinion in Colloid & Interface Science, 2005, 10(3–4): 102−110.
[16] SONNEVILLE-AUBRUN O, SIMONNET J T, L'ALLORET F. Nanoemulsions: A new vehicle for skincare products[J]. Advances in Colloid and Interface Science,2004,108:145−149.
[17] PATEL D, SAWANT K K. Oral bioavailability enhancement of acyclovir by self-microemulsifying drug delivery systems (SMEDDS)[J]. Drug Development and Industrial Pharmacy,2007,33(12):1318−1326. doi: 10.1080/03639040701385527
[18] KSHIRSAGAR A C, YENGE V B, SARKA A, et al. Efficacy of pullulan in emulsification of turmeric oleoresin and its subsequent microencapsulation[J]. Food Chemistry,2009,113(4):1139−1145. doi: 10.1016/j.foodchem.2008.09.002
[19] MAREFATI A, BERTRAND M, SJOO M, et al. Storage and digestion stability of encapsulated curcumin in emulsions based on starch granule Pickering stabilization[J]. Food Hydrocolloids,2017,63:309−320. doi: 10.1016/j.foodhyd.2016.08.043
[20] LIANG R, JIANG Y W, YOKOYAMA W, et al. Preparation of Pickering emulsions with short, medium and long chain triacylglycerols stabilized by starch nanocrystals and their in vitro digestion properties[J]. RSC Advances,2016,6(101):99496−99508. doi: 10.1039/C6RA18468E
[21] LI X, LI H, XIAO Q, et al. Two-way effects of surfactants on Pickering emulsions stabilized by the self-assembled microcrystals of alpha-cyclodextrin and oil[J]. Physical Chemistry Chemical Physics,2014,16(27):14059−14069. doi: 10.1039/C4CP00807C
[22] 刘红星, 陈福北, 黄初升, 等. 紫外分光光度法在姜黄素类化合物提取中的应用[J]. 广西师范学院学报(自然科学版),2008(3):68−72. [LIU H X, CHEN F B, HUANG C S, et al. UV-visible absorption and its application to extraction curcuminoids[J]. Journal of Guangxi Teachers Education University (Natural Science Edition),2008(3):68−72. doi: 10.3969/j.issn.1002-8743.2008.03.014 [23] PAN Y, XIE Q T, ZHU J, et al. Study on the fabrication and in vitro digestion behavior of curcumin-loaded emulsions stabilized by succinylated whey protein hydrolysates[J]. Food Chemistry,2019,287:76−84. doi: 10.1016/j.foodchem.2019.02.047
[24] WEI Z H, GAO Y X. Physicochemical properties of beta-carotene bilayer emulsions coated by milk proteins and chitosan-EGCG conjugates[J]. Food Hydrocolloids,2016,52:590−599. doi: 10.1016/j.foodhyd.2015.08.002
[25] ZHANG Z P, ZHANG R J, DECKER E A, et al. Development of food-grade filled hydrogels for oral delivery of lipophilic active ingredients: pH-triggered release[J]. Food Hydrocolloids,2015,44:345−352. doi: 10.1016/j.foodhyd.2014.10.002
[26] WANG B, LI D, WANG L J, et al. Ability of flaxseed and soybean protein concentrates to stabilize oil-in-water emulsions[J]. Journal of Food Engineering,2010,100(3):417−426. doi: 10.1016/j.jfoodeng.2010.04.026
[27] KHARAT M, ZHANG G D, MCCLEMENTS D J. Stability of curcumin in oil-in-water emulsions: Impact of emulsifier type and concentration on chemical degradation[J]. Food Research International,2018,111:178−186. doi: 10.1016/j.foodres.2018.05.021
[28] PENG S F, LI Z L, ZOU L Q, et al. Enhancement of curcumin bioavailability by encapsulation in sophorolipid-coated nanoparticles: An in vitro and in vivo study[J]. Journal of Agricultural and Food Chemistry,2018,66(6):1488−1497. doi: 10.1021/acs.jafc.7b05478
[29] ZHENG B J, ZHANG X Y, PENG S F, et al. Impact of curcumin delivery system format on bioaccessibility: Nanocrystals, nanoemulsion droplets, and natural oil bodies[J]. Food & Function,2019,10(7):4339−4349.
[30] ZHENG B J, PENG S F, ZHANG X Y, et al. Impact of delivery system type on curcumin bioaccessibility: Comparison of curcumin-loaded nanoemulsions with commercial curcumin supplements[J]. Journal of Agricultural and Food Chemistry,2018,66(41):10816−10826. doi: 10.1021/acs.jafc.8b03174
[31] AHMED K, LI Y, MCCLEMENTS D J, et al. Nanoemulsion- and emulsion-based delivery systems for curcumin: Encapsulation and release properties[J]. Food Chemistry,2012,132(2):799−807. doi: 10.1016/j.foodchem.2011.11.039
[32] RUIZ-ALVAREZ J M, DEL CASTILLO-SANTAELLA T, MALDONADO-VALDERRAMA J, et al. pH influences the interfacial properties of blue whiting (M. poutassou) and whey protein hydrolysates determining the physical stability of fish oil-in-water emulsions[J]. Food Hydrocolloids,2021,122:107075.
[33] MCCLEMENTS D J. Theoretical analysis of factors affecting the formation and stability of multilayered colloidal dispersions[J]. Langmuir,2005,21(21):9777−9785. doi: 10.1021/la0512603
[34] 毕爽, 李杨, 隋晓楠, 等. 高压均质对大豆蛋白-磷脂复合体系结构及理化/功能性质的影响[J]. 食品科学,2017,38(5):148−153. [BI S, LI Y, SUI X N, et al. Effect of high pressure homogenization on structural, physicochemical and functional properties of soybean protein-lecithin composite system[J]. Food Science,2017,38(5):148−153. doi: 10.7506/spkx1002-6630-201705024 [35] BI C H, WANG P L, SUN D Y, et al. Effect of high-pressure homogenization on gelling and rheological properties of soybean protein isolate emulsion gel[J]. Journal of Food Engineering,2020,277:109923. doi: 10.1016/j.jfoodeng.2020.109923
[36] HA T V A, KIM S, CHOI Y, et al. Antioxidant activity and bioaccessibility of size-different nanoemulsions for lycopene-enriched tomato extract[J]. Food Chemistry,2015,178:115−121. doi: 10.1016/j.foodchem.2015.01.048
[37] OZTURK B, MCCLEMENTS D J. Progress in natural emulsifiers for utilization in food emulsions[J]. Current Opinion in Food Science,2016,7:1−6.
[38] 姚艳玉, 马培华, 曾庆晗, 等. 油相种类对姜黄素纳米乳液稳定性的影响[J]. 食品科技,2017,42(9):238−242. [YAO Y Y, MA P H, ZENG Q H, et al. Effect of oil phase on the stability of curcumin nanoemulsion[J]. Food Technology,2017,42(9):238−242. doi: 10.13684/j.cnki.spkj.2017.09.046 [39] 李朝阳, 窦中友, 张丽萍, 等. 载体油对槲皮素纳米乳液理化稳定性和生物利用度的影响[J]. 食品科学,2020,42(12):1−10. [LI Z Y, DOU Z Y, ZHANG L P, et al. Effect of carrier oil on physicochemical stability and bioavailability of quercetin nanoemulsion[J]. Food Science,2020,42(12):1−10. doi: 10.7506/spkx1002-6630-20190127-346 [40] SEK L, PORTER C J H, KAUKONEN A M, et al. Evaluation of the in-vitro digestion profiles of long and medium chain glycerides and the phase behaviour of their lipolytic products[J]. Journal of Pharmacy and Pharmacology,2002,54(1):29−41.
[41] LI Y X, QARIA M A, SIVASAMY S, et al. Curcumin production and bioavailability: A comprehensive review of curcumin extraction, synthesis, biotransformation and delivery systems[J]. Industrial Crops and Products,2021,172:114050. doi: 10.1016/j.indcrop.2021.114050
[42] 余振宇. OSA改性芋头淀粉基Pickering乳液运载体系稳定机制及特性研究[D]. 合肥: 合肥工业大学, 2020 YU Z Y. Stabilization mechanism and characteristics of Pickering emulsion delivery system based on OSA modified taro starch[D]. Hefei: Hefei University of Technology, 2020.
[43] LIU CH, WANG R C, HE S H, et al. The stability and gastro-intestinal digestion of curcumin emulsion stabilized with soybean oil bodies[J]. LWT-Food Science and Technology,2020,131:109663. doi: 10.1016/j.lwt.2020.109663
[44] HOMERO-MENDEZ D, MINGUEZ-MOSQUERA M I. Bioaccessibility of carotenes from carrots: Effect of cooking and addition of oil[J]. Innovative Food Science & Emerging Technologies,2007,8(3):407−412.
-
期刊类型引用(2)
1. 左云会,胡腾根,朱永清,徐玉娟,唐语谦,余元善. 石榴皮活性物质提取及其W/O/W乳液稳态化包埋研究. 中国食品学报. 2024(09): 167-183 .  百度学术
百度学术
2. 黄小倩,李佳琪,郭梦雪,张卉悦,张伟敏,夏光华. 忧遁草多糖乳液体外消化特性研究. 食品工业科技. 2023(19): 1-9 .  本站查看
本站查看
其他类型引用(7)





 下载:
下载:






 下载:
下载:



