Study on the Improvement of Symptoms of DSS-induced Colitis in Mice by Pasteurized Fermented Milk
-
摘要: 本研究采用3.5%的葡聚糖硫酸钠(DSS)构建小鼠结肠炎症动物模型,旨在阐明巴氏杀菌发酵乳对结肠炎小鼠的缓解作用及可能的机制。通过评估小鼠疾病活动指数(disease activity index,DAI),HE染色观察结肠组织病理切片,气相色谱-质谱联用(GC/MS)分析肠道短链脂肪酸含量,ELISA检测结肠组织中的炎症因子水平,检测髓过氧化物酶(MPO)含量和采用免疫组化进行紧密连接蛋白的表达,来研究巴氏杀菌发酵乳的作用。结果表明,巴氏杀菌发酵乳可以降低结肠炎小鼠疾病活动指数DAI、缓解结肠组织损伤、增加小鼠肠道短链脂肪酸乙酸、异丙酸、戊酸和总酸的含量,同时降低小鼠促炎细胞因子肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)的分泌、增加抗炎细胞因子白细胞介素-10(IL-10)的分泌和降低MPO活性。进一步的研究表明,巴氏杀菌发酵乳可以增加小鼠肠道紧密连接蛋白的表达,增强肠道上皮屏障功能。因此,巴氏杀菌发酵乳可以缓解小鼠肠道炎症症状,并且可能是通过调节免疫功能和增强肠道屏障发挥其作用。Abstract: In this study, 3.5% DSS was used to construct an animal model of colonic inflammation in mice, in order to study the relieving effect of commercially available pasteurized fermented milk on colitis mice and the possible mechanism. The effect of pasteurized fermented milk was studied by evaluating the disease activity index (DAI) in mice, observing colon tissue structure by HE staining, analyzing intestinal short-chain fatty acid content by gas chromatography-mass spectrometry (GC/MS), detecting inflammatory factors in colon tissue by ELISA levels, measuring myeloperoxidase (MPO) content and using immunohistochemistry for tight junction protein expression. The results of the study showed that pasteurized fermented milk could reduce the disease activity index DAI, alleviate colon tissue damage, increase the content of acetic acid, isopropionic acid, valerate acid and total acid in the intestinal short-chain fatty acids of mice, reduce the secretion of anti-inflammatory cytokines tumor necrosis factor-α (TNF-α) and leukocyte-mediated interleukin-1β (IL-1β) in mice, and increase the anti-inflammatory cytokines interleukin-10 (IL-10) secretion and decrease MPO activity. Further research showed that pasteurized fermented milk could increase the expression of tight junction proteins in the mouse gut and enhance intestinal epithelial barrier function. Therefore, pasteurized fermented milk could not only alleviate the symptoms of intestinal inflammation in mice, but might play its role by regulating the body's immunity and strengthening the intestinal barrier.
-
Keywords:
- pasteurized fermented milk /
- colitis /
- immune activity /
- intestinal barrier /
- alleviation
-
肠道作为机体重要的消化器官,会与食物中的外来细菌、病毒和有害物质接触,是保护并维持机体免疫平衡的重要屏障。炎症性肠病(Inflammatory bowel disease,IBD)是一种原因尚不明确的慢性胃肠道疾病,主要包括克罗恩病和溃疡性结肠炎,其临床症状表现为持续性的腹泻、腹痛、发热和呕吐等,且粪便中常伴随血液和黏液[1]。IBD由于病程长、易复发、并发症多且难治愈等原因,会直接影响患者的生活。临床对于溃疡性结肠炎主要应用以柳氮磺胺吡啶(SASP)为代表的氨基水杨酸类药物作为主要的治疗药物,对于大部分轻、中度患者有较好的疗效,但对部分长期服药的患者存在较大的副作用如呼吸困难、恶心、呕吐等不良反应[2]。鉴于现有治疗方法存在的多种问题,替代传统方法能够缓解IBD的方案显得尤为重要。新的治疗物质包括益生元、益生菌、部分微生物代谢物如不饱和脂肪酸(共轭亚油酸和共轭亚麻酸)和短链脂肪酸等[3-5]。
巴氏杀菌发酵乳在其生产工艺流程中存在二次巴氏杀菌,并且在4~25 ℃条件下可保质大约半年左右,也称长保质期酸奶。近年来由于这一细分品类的出现,以保存期较长的优点满足了冷链不完善的消费需求,所以销量和受众较好。世界乳品联合会专家指出,酸奶的营养不仅来自活性乳酸菌,还来自牛奶在发酵过程中所产生的一系列化学产物[6]。研究发现,与活菌相比,灭活导致乳酸菌细胞壁破裂,脂磷壁酸和胞外多糖等释放出来,可以穿过黏液层到达肠道上皮,增强肠道黏膜的完整性,所以灭活乳酸菌具有黏附抗性、增强免疫能力和肠道黏膜屏障功能等多种生理功能[7]。发酵过程中产生的一些微生物代谢物如不饱和脂肪酸等具有免疫调节活性,对肠道免疫屏障有积极影响[8]。
目前,关于活菌型发酵乳以及活性益生菌对肠道炎症的作用研究比较多,但是关于巴氏杀菌型发酵乳对肠道健康的研究相对较少且尚未明确。本研究以巴氏杀菌发酵乳为研究对象,通过构建葡聚糖硫酸钠(dextran sodium sulfate,DSS)诱导的肠炎小鼠模型组,灌胃巴氏杀菌型发酵乳进行干预,探究其对结肠炎小鼠肠道形态、结肠功能和免疫活性的影响,揭示其对结肠炎小鼠炎症的缓解作用以及发挥作用的可能机制。同时为灭活型发酵乳缓解肠道疾病提供参考。
1. 材料与方法
1.1 材料与仪器
巴氏杀菌发酵乳(安慕希利乐钻原味产品) 购自大型超市;SPF级雄性Balb/c小鼠(6周龄) 购自北京维通利华试验动物技术有限公司,实验动物生产许可证号:SCXK(京)2016-0006;葡聚糖硫酸钠(DSS) 美国MP公司;0.9%氯化钠、柳氮磺吡啶 北京索莱宝科技有限公司;HE染色相关试剂(伊红、苏木精、二甲苯、石蜡等)、ELLSA试剂盒、髓过氧化物酶(MPO)试剂盒 上海酶联生物科技有限公司;乙醚、乙酸、丁酸、异丁酸、戊酸 美国Sigma公司;紧密连接蛋白-1(ZO-1)、紧密连接组分闭合蛋白(Occludin) 美国Abcam公司。
HWS12恒温水浴锅 上海一恒科学技术有限公司;BX53F荧光显微镜 赛默飞世尔有限公司;MLS-3750高压蒸汽灭菌锅 日本Sanyo公司;Beta1-8 LDplus真空冷冻干燥机 德国Christ公司;Thermo TRACE 1310-ISQ LT 气-质联用仪 美国Thermo公司;TGL-16M台式高速冷冻离心机 上海卢湘仪离心机仪器有限公司。
1.2 实验方法
1.2.1 动物分组及模型的构建
本实验采用SPF级雄性Balb/c小鼠(44只),随机分为4组,保持恒温(22~24 ℃),并保持在12 h亮/暗循环的环境中,自由饮食和饮水。动物在此条件下饲养,经过7 d的适应生长后用于实验。具体分组见表1,除空白对照组外,其余各组均给予3.5% DSS(w/v)溶液,连续自由饮用14 d,用以建立急性IBD炎症动物模型[9]。而后进入7 d干预期,根据组别,连续7 d分别灌胃,灌胃方法:空白对照组、模型组分别给予200 μL生理盐水,阳性对照组给予200 μL柳氮磺吡啶水溶液(0.45 g/kg),巴氏杀菌发酵乳组给予巴氏杀菌发酵乳(26 mL/kg),其中巴氏杀菌发酵乳干预组小鼠灌胃量参考20 g小鼠与70 kg成人体表面积比例参数0.0026进行换算,其中按照成人每天饮用200 g/d进行换算。第28 d,腹腔注射1%戊巴比妥钠溶液麻醉后,颈椎脱臼法处死所有小鼠。动物实验严格遵守实验动物福利伦理与保护相关规定,随时接受实验动物伦理委员会的监督与检查。
表 1 动物实验分组Table 1. Animal experiment group组别 造模 干预7 d 剂量 空白对照组(C) 自由饮食14 d 生理盐水 10 mL/kg 模型组(M) DSS 14 d 生理盐水 10 mL/kg 阳性对照组(P) DSS 14 d 柳氮磺吡啶 0.45 g/kg 巴氏杀菌发酵乳组(AN) DSS 14 d 巴氏杀菌发酵乳 26 mL/kg 1.2.2 小鼠体征观察
于诱导及治疗期间,每天观察小鼠体重变化情况,同时记录粪便性状,便血情况,按照表2所述标准进行评分,DAI=(体重下降分值+粪便性状分值+便血情况分值)/3。
表 2 疾病活动指数(DAI评分表)Table 2. Disease activity index (DAI scale)计分(分) 体重下降(%) 粪便性状 便血情况 0 0 正常 阴性 1 1~5 形成粪便但易粘附 弱阳性 2 6~10 半成型软粪便 阳性 3 11~15 粪浆状,但不粘附于肛门 强阳性 4 ≥15 腹泻,粘附肛门 肉眼可见血便 1.2.3 结肠系数和长度
动物实验结束后处死小鼠,取出无盲肠的结肠,称取其质量及小鼠体重,结肠重量除以小鼠体重为结肠系数。拍摄结肠整体形态照片,用游标卡尺测量结肠长度。
1.2.4 结肠病理组织HE染色及评分
将于4%多聚甲醛溶液中固定24 h的结肠组织取出,依次经过脱水、浸蜡、包埋、切片、捞片和烤片,脱蜡复水等步骤处理后,进行HE染色,最后在光学显微镜下观察结肠组织结构。结肠组织学损伤标准评分参考Jang等[10]的方法,按照表3进行。
表 3 HE切片组织学评分Table 3. HE section histological scoring评分(分) 描述 病变范围 0 正常结肠形态结构,无上皮破坏,隐窝缺失 1 病变范围占所有检查视野1%~25% 2 病变范围占所有检查视野26%~50% 3 病变范围占所有检查视野51%~75% 4 病变范围占所有检查视野75%~100% 病变深度 0 无炎症细胞浸润 1 炎症细胞浸润局限于黏膜层 2 炎症细胞浸润至黏膜下层 3 炎症细胞浸润突破黏膜下层,到达肌层 4 炎症细胞浸润结肠全层 1.2.5 短链脂肪酸检测
采取乙醚萃取法提取粪便中的短链脂肪酸。提前配制标准品,量取乙酸、丁酸、异丁酸、戊酸纯标准品适量,用乙醚配制成0.02、0.1、0.5、2、5、10、50、100、250、500 μg/mL 10个混合标准浓度梯度。母液及工作标准溶液均保存于0 ℃。取小鼠粪便标样于2 mL离心管中,加50 μL 15%磷酸,再加125 μg/mL的内标(异己酸)溶液100 μL和乙醚400 μL匀浆1 min,于4 ℃ 12000 r/min离心10 min,取上清上机测试。GC-MS测定:色谱柱选用 Agilent HP-INNOWAX 毛细管柱(30 m×0.25 mm ID×0.25 μm)。程序升温,初始温度为60 ℃,在此温度下保持3 min ,然后以5 ℃/min的速度升温至165 ℃,保持3 min,后运行3 min。载气(He)恒定流速为1.2 mL/min,进样口温度180 ℃,分流比为5:1。质谱条件:电子电离源,电子能量70 eV,传输线温度280 ℃,离子源温度230 ℃,四极杆温度150 ℃,质量扫描范围m/z 40~250。
1.2.6 小鼠炎性指标检测
取约1 cm的小鼠结肠组织以1:9的比例加入预冷的无菌PBS溶液置于玻璃研磨器中研磨成匀浆后,3000 r/min离心20 min 收集上清于−20 ℃保存。根据酶联免疫试剂盒说明书测定小鼠结肠中细胞因子TNF-α、IL-1β和IL-10的含量。
1.2.7 髓过氧化物酶(MPO)测定
准备结肠组织,依据MPO试剂盒进行测定。
1.2.8 紧密连接蛋白测定
采用的是免疫组化对小鼠结肠黏膜的紧密蛋白ZO-1和Occludin进行测定。取结肠溃疡处约1 cm,10%甲醛固定72 h,乙醇脱水后石蜡包埋,固定于切片机,切片厚度20 μm,脱蜡,用3%过氧化氢阻断内源性过氧化物酶,滴加一抗4 ℃过夜,TBS洗涤后滴
加二抗,37 ℃孵育 30 min,TBS 洗涤,DAB显色,苏木素复染,梯度酒精溶液和二甲苯脱水,盖玻片封片。显微镜400倍观察,使用Image-Pro 6.0对400×图片进行光密度值分析。
1.3 数据处理
数据以平均值±标准误表示,采用Excel、SPSS和Origin软件进行处理。P<0.05表示差异具有统计学意义。
2. 结果与分析
2.1 巴氏杀菌发酵乳对小鼠生长性能的影响
DSS诱导结肠炎小鼠的典型特征包括体重下降、DAI指数增加、结肠长度缩短、肠道黏膜损伤等,因此这些特征一般作为常规指标进行测定[9]。图1显示了造模期间各组小鼠的体重和DAI指数变化情况。DAI综合评分能够反映小鼠体重变化、血便情况及大便性状,DAI值越大,反映出肠道的炎症越严重[11]。由图可以看出空白对照组小鼠体重与造模前相比呈现轻微上升趋势,DAI指数趋近于0,同时观察到小鼠粪便状态正常,精神状态良好。与空白对照组相比,模型组小鼠出现明显的结肠炎症状,包括体重明显下降,出现稀便,肉眼可见血便等症状,DAI显著上升(P<0.05)。通过巴氏杀菌发酵乳干预7 d后小鼠体重恢复效果较好,毛色逐渐恢复光泽,活动量逐渐增加,DAI指数也低于模型组小鼠。说明巴氏杀菌发酵乳在一定程度上可以改善小鼠的炎症反应。
2.2 巴氏杀菌发酵乳对小鼠结肠长度和结肠系数的影响
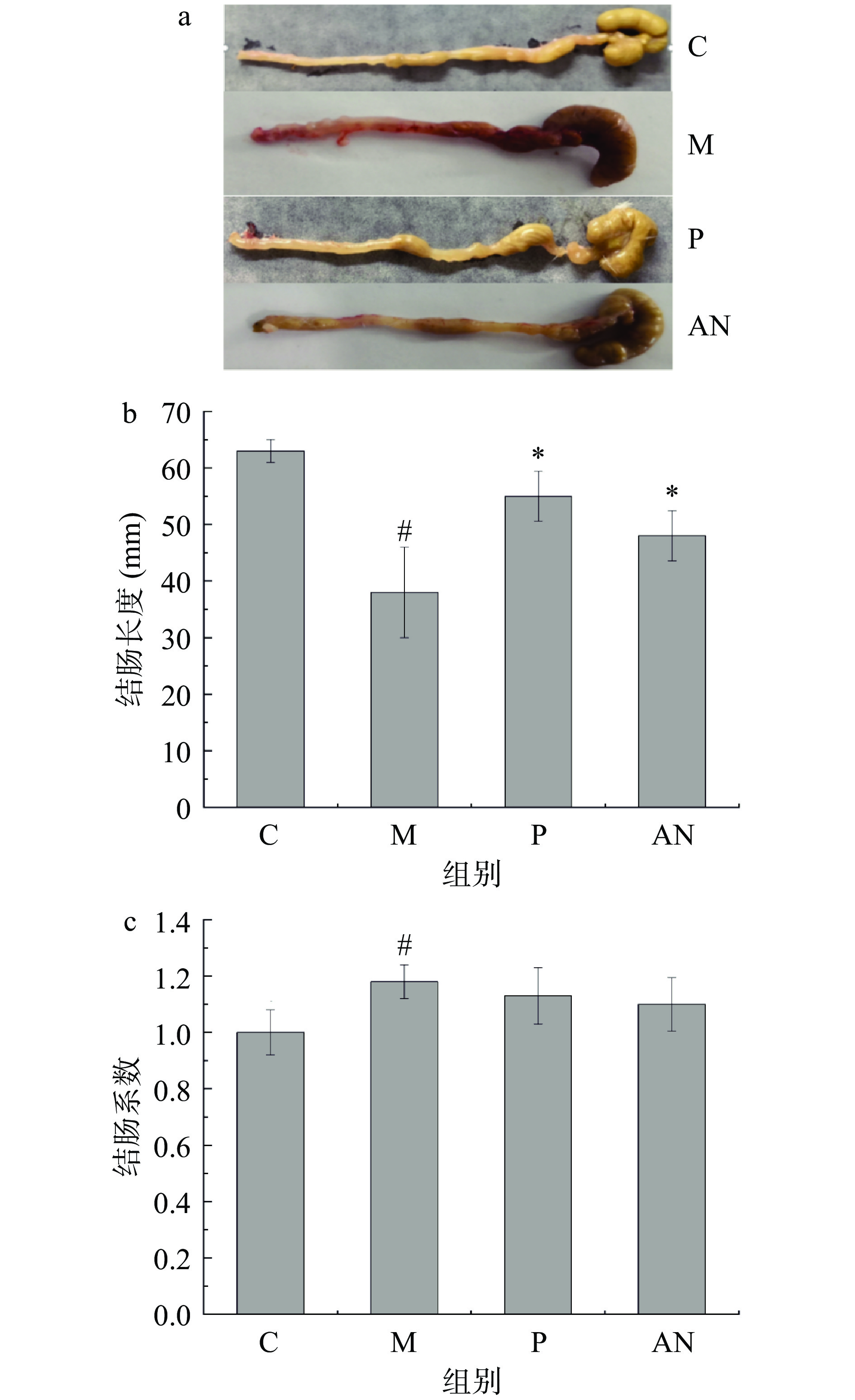
研究表明,DSS诱导的结肠炎会引起结肠充血水肿、肠壁增厚和结肠长度缩短等,因此结肠系数和结肠长度是评估DSS诱导结肠炎严重程度的重要指标之一[12]。对每只小鼠的结肠长度进行测量并拍照,如图2所示,与空白对照组比较,模型组小鼠结肠肉眼可见结肠水肿充血,结肠长度显著缩短,组织变厚,脆性增加,缺少弹性,且结肠系数最大,说明DSS成功诱导小鼠出现结肠炎症状,模型建立成功。而巴氏杀菌发酵乳组的结肠水肿、长度均有不同程度的恢复,结肠系数下降。说明巴氏杀菌发酵乳可以有效预防结肠的缩短,降低结肠系数,减轻小鼠结肠充血、水肿、增厚等炎症反应,这与DAI指数的结果相一致。
2.3 小鼠结肠病理学分析
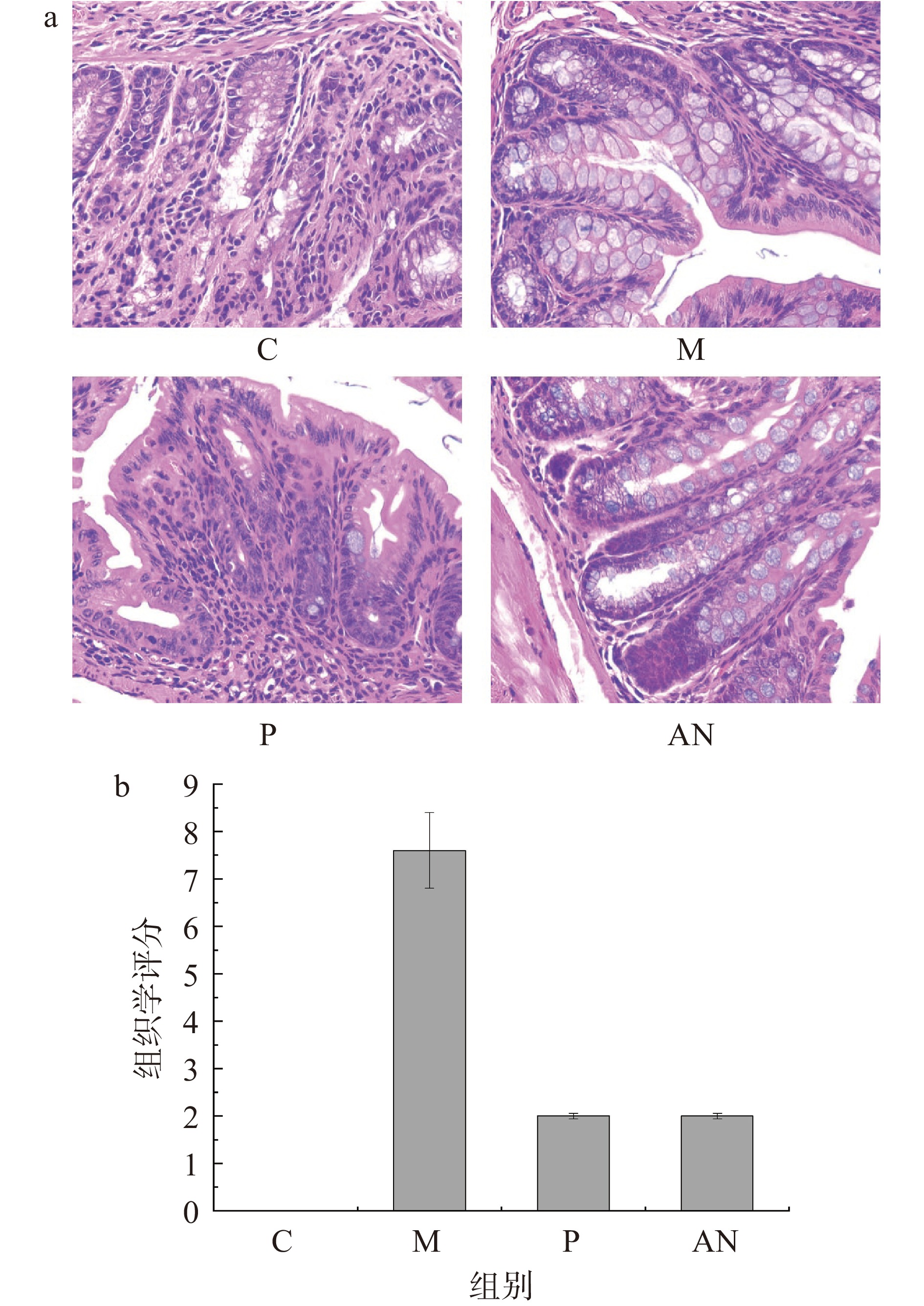
如图3所示,空白对照组小鼠结肠黏膜结构完整,腺体排列整齐,未见黏膜溃烂和炎性细胞浸润。模型组小鼠结肠黏膜缺损,隐窝缺失,黏膜及黏膜下层大量中性粒细胞及淋巴细胞浸润。巴氏杀菌发酵乳组结肠黏膜层轻微损伤,上皮细胞形态正常,肠腺数量丰富,炎症面积大范围减少,表明巴氏杀菌发酵乳对IBD小鼠结肠黏膜组织受损有缓解作用,具有良好的抗炎效果。结肠组织学评分是以结肠病变范围和病变深度为评价指标对每个组的H&E切片进行组织学评分,评分越高,结肠组织的病变程度越大。关于缓解结肠炎的大量研究中,H&E病理评分一直都是评价缓解结肠炎效果的关键指标[13-15]。可见巴氏杀菌发酵乳对小鼠结肠炎有缓解效果。
2.4 短链脂肪酸含量分析
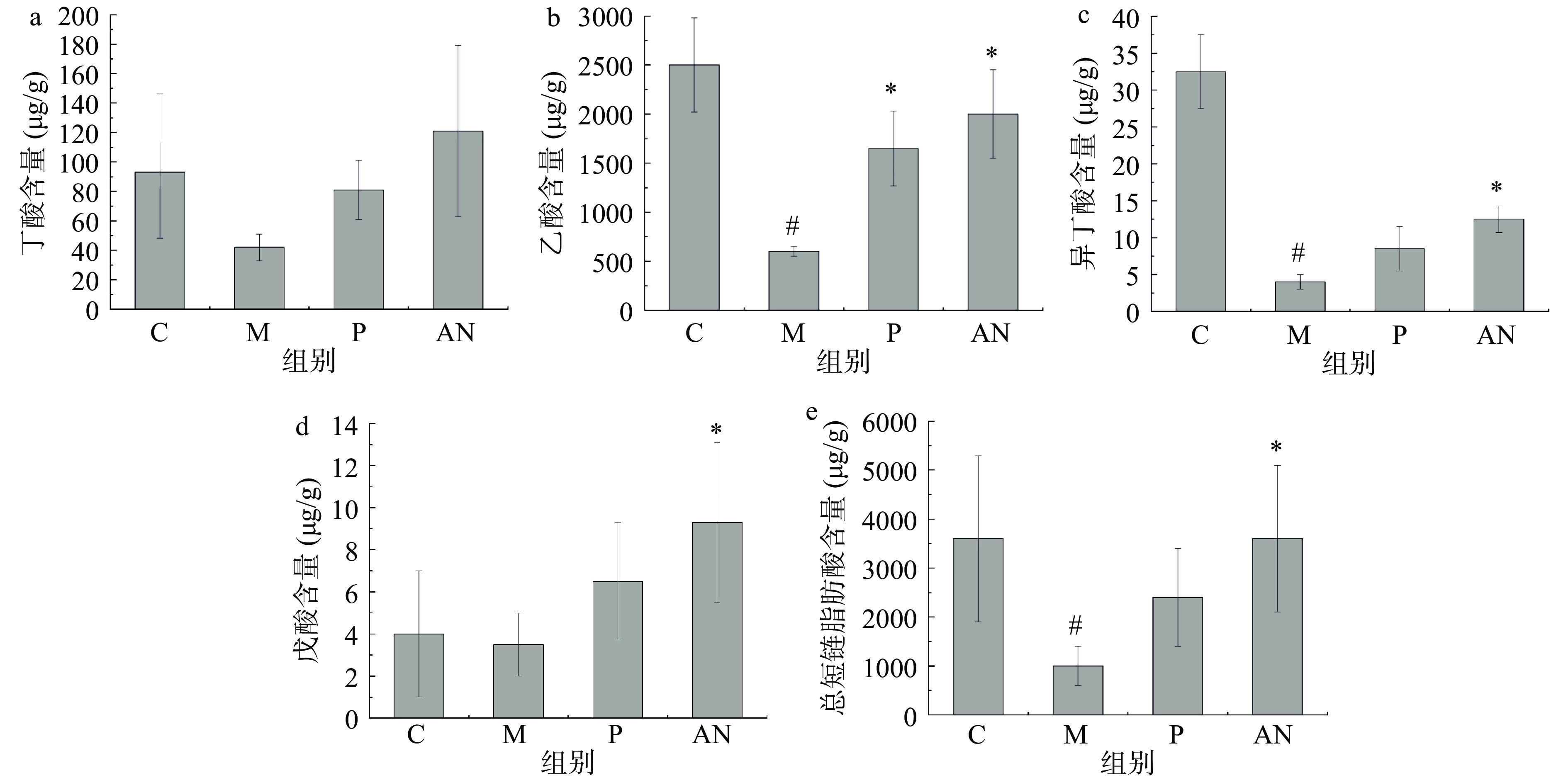
短链脂肪酸(short-chain fatty acids,SCFAs)是肠道菌群的代谢产物,能够为结肠细胞提供能量,调节肠腔内的pH,增强肠道屏障功能[16]。同时还能通过调节免疫细胞趋化性、活性氧(reactive oxygen,ROS)释放以及细胞因子释放,具有抗炎功能。其中,丁酸通过抑制促炎因子TNF-α、IL-1β和一氧化氮的产生,并降低NF-ĸB的活性[17]。早有研究显示丁酸制剂的应用可以缓解溃疡性结肠炎的病症[18]。本文测定了小鼠粪便中乙酸、丁酸、异丁酸、戊酸以及总短链脂肪酸的含量,以探究巴氏杀菌发酵乳对短链脂肪酸含量的影响。Vinolo等[19]研究发现结肠炎可引起肠道短链脂肪酸浓度下降。本研究结果如图4所示,DSS组肠道内的SCFAs浓度均有不同程度的降低,可能是由于DSS导致小鼠肠道菌群失调。与模型组相比,经过巴氏杀菌发酵乳干预7 d后,小鼠粪便中的短链脂肪酸丁酸、乙酸、异丁酸、戊酸和总短链脂肪酸含量均有不同程度的提升,其中乙酸、异丁酸、戊酸和总短链脂肪酸含量与模型组相比具有显著性差异(P<0.05)。这可能是由于巴氏杀菌发酵乳在肠道内发挥了益生调节作用,这与早前研究发现的灭活型常温酸奶能够提高短链脂肪酸含量的结果相似[20]。由此可见,巴氏杀菌发酵乳能够在一定程度上显著增加小鼠粪便中短链脂肪酸的含量,起到减轻炎症的保护作用,从而促进肠道健康。
2.5 小鼠炎症因子指标分析
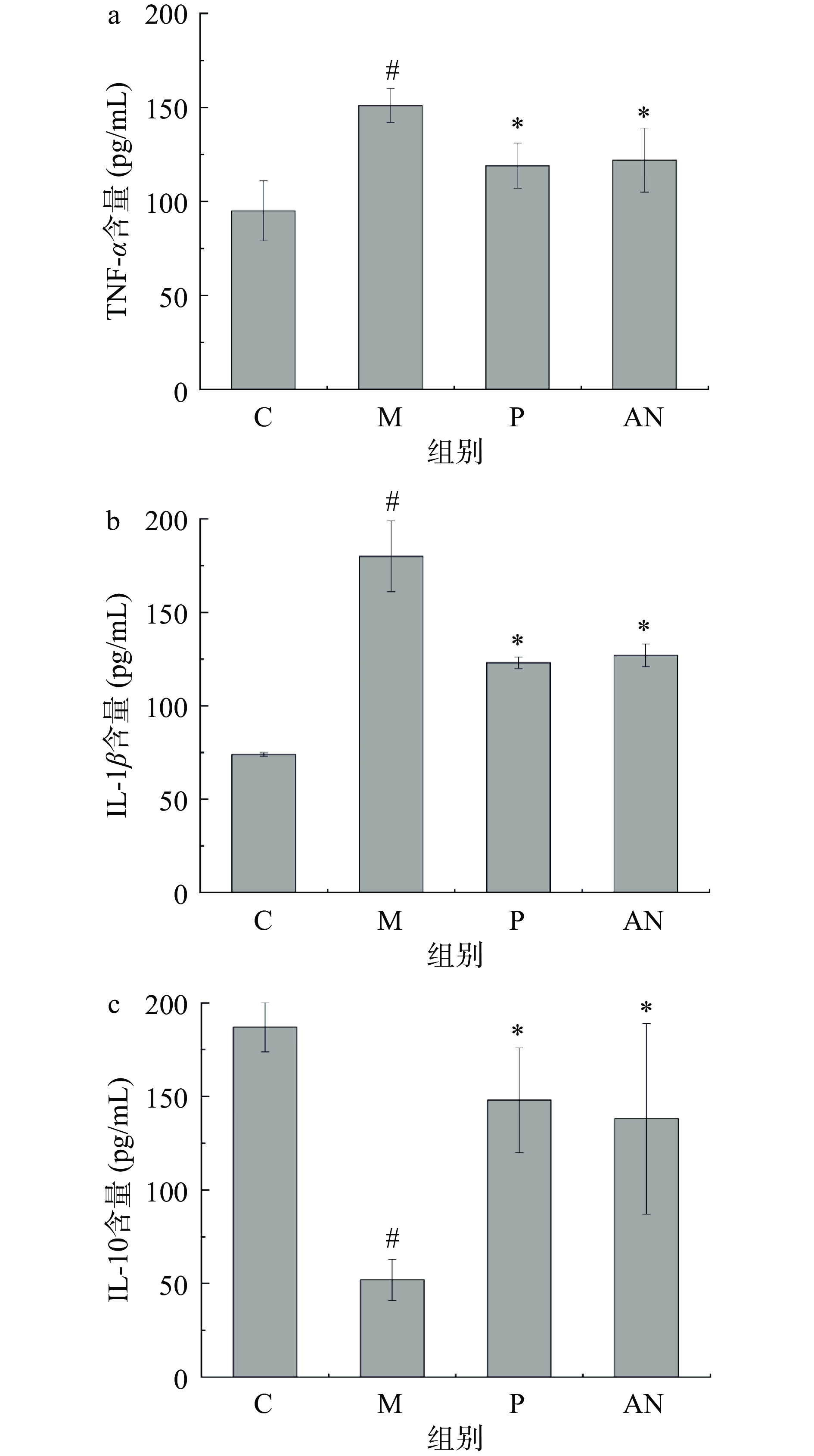
组织中的抗炎及促炎因子水平能够直接反映出机体的炎症水平。研究证明,炎症细胞因子对肠道屏障也有着一定影响,促炎因子TNF-α、IFN-γ、IL-1β、IL-12分泌增加能够损坏肠道黏膜,增加病原体的易感染性和上皮通透性,激活或甚至扩大感染反应[21]。而抗炎细胞因子IL-10、TGF-β等则具有相反的生理功能,缓解炎症和黏膜损伤[22]。炎症发作时会促使PAMPS信号过度活化,导致TLR信号下游靶基因异常转录,IL-1、IL-6及TNF-α等炎症细胞因子大量释放,造成靶器官损害。而IL-10分泌减少,造成促炎症因子和抗炎因子平衡打破,故结肠炎发病[23]。因此下调促炎因子水平和上调抗炎因子水平是治疗该病的一种策略。本研究收集小鼠结肠组织并检测细胞因子,如图5所示,与空白对照组相比,模型组中抗炎因子IL-10的水平降低,促炎因子TNF-α和IL-1β的水平升高,表明模型组小鼠的免疫功能异常,有明显的炎症反应。经巴氏杀菌发酵乳干预7 d后,与模型组相比,实验组小鼠IL-10含量显著增加,TNF-α和IL-1β含量显著降低(P<0.05)。已有研究发现,灭活双歧杆菌发酵乳能够抑制TNF-α、IFN-γ、IL-6表达,增加抗炎因子IL-4和IL-10表达[24]。干酪乳杆菌TK1501发酵的灭活型红枣饮品能够上调结肠炎小鼠细胞中抗炎因子IL-4的含量,下调促炎因子IL-1β、IL-6含量[25]。这可能是因为灭活菌细胞壁中的肽聚糖、脂多糖、脂壁磷酸等成分刺激了巨噬细胞分泌抗炎因子、抗菌肽等功能因子,从而提高机体的免疫能力所致。与本研究结果相似,说明巴氏杀菌发酵乳对DSS诱导的结肠炎的有益作用与调节促炎因子和抗炎因子的表达有关。
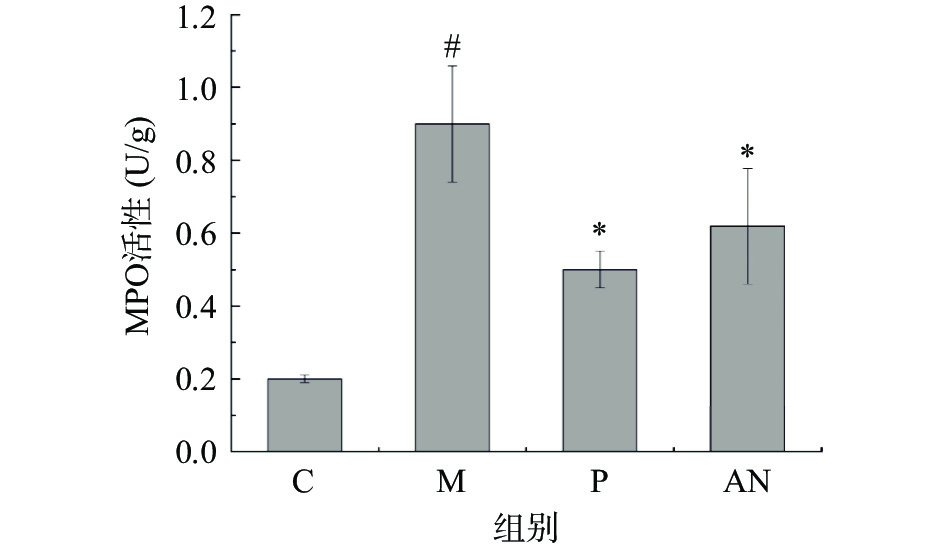
2.6 对小鼠MPO的影响
髓过氧化物酶(MPO)属于血红素蛋白,其活性变化与相关组织的中性粒细胞的浸润情况相关[26]。肠道炎症是DSS引起结肠炎的病理表现,MPO与炎症呈正相关,所以MPO可以作为反映结肠炎炎症程度的重要指标之一[27]。在炎性状态下,MPO被释放到细胞外液,进入循环。Yorulmaz等[28]测定血清和结肠组织的MPO,结果显示MPO活性显著升高,而在鱼油和美沙拉嗪的干预下均降低。本研究通过测定结肠组织中MPO活性变化来探究巴氏杀菌发酵乳对结肠炎小鼠MPO活性的变化。结果如图6所示,模型组小鼠组织中的MPO活性显著增加(P<0.05),给予巴氏杀菌发酵乳干预后能够降低小鼠组织中的MPO活性,表明巴氏杀菌发酵乳具有减轻DSS引起的肠道损伤,可以在一定程度上缓解结肠炎小鼠的炎症水平。
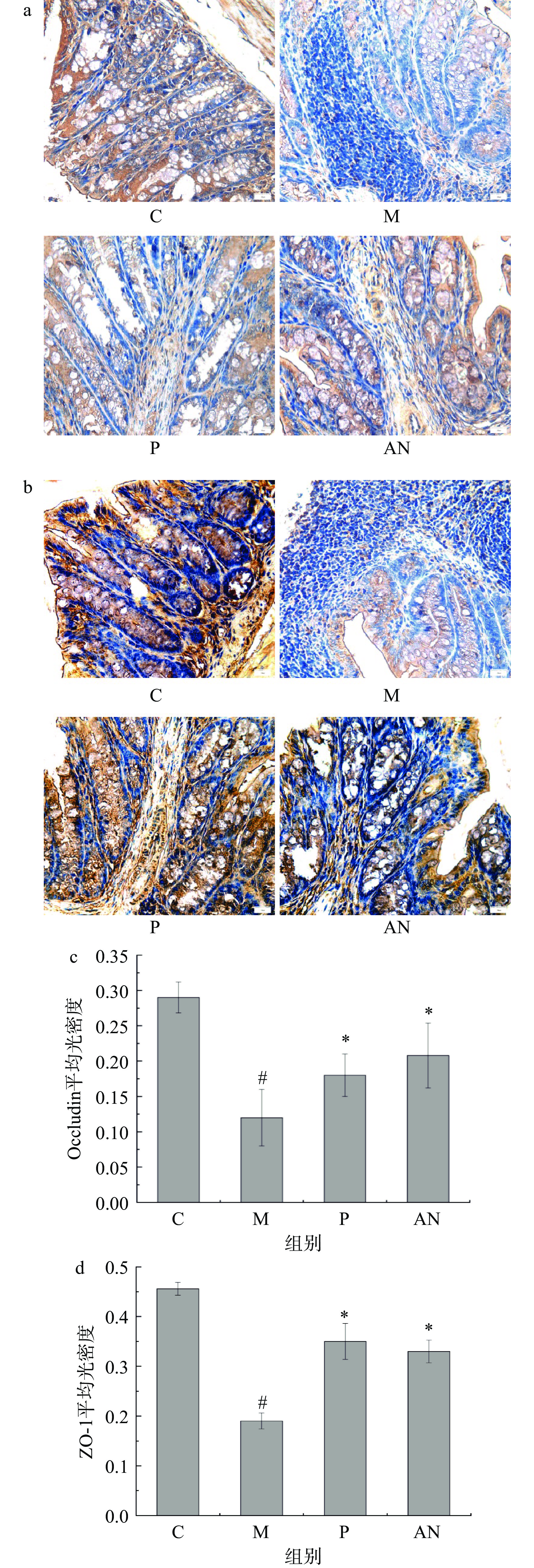
2.7 对小鼠肠道屏障的影响
肠道上皮细胞间的紧密连接(Tight junction,TJ)由一系列紧密连接蛋白组成,包括Occludin、Claudin以及ZO-1、ZO-2、ZO-3等。紧密连接蛋白形成肠道的防御屏障,可以将肠腔中的有害微生物和化学物质隔离,起到保护肠道的作用[29]。当IBD产生时,肠黏膜屏障功能表现异常,抗原物质激活免疫细胞,产生大量炎性细胞因子及介质,间接破环紧密连接蛋白的结构,影响ZO-1、Occludin、E-cadherin的表达,造成肠道屏障功能受损严重[30]。本研究测定了巴氏杀菌发酵乳对炎症小鼠紧密连接蛋白Occludin和ZO-1的影响。结果如图7所示,空白对照组小鼠结肠ZO-1和Occludin蛋白在管腔上皮细胞、隐窝上皮细胞及上皮细胞连接处顶端均可观察到表达。与空白对照组相比,DSS诱导的模型组Occludin和ZO-1表达量均显著降低(P<0.05)。给予巴氏杀菌发酵乳干预后,ZO-1和Occludin蛋白表达量显著增加(P<0.05),其表达多位于管腔上皮细胞、隐窝上皮细胞、上皮细胞连接处顶端及少部分胞浆,且与SASP药物组结果相似。Patel等[31]研究表明,灭活益生菌能够通过Toll样受体信号通路诱导紧密连接蛋白表达,提高肠道黏膜屏障完整性,预防结肠炎产生。干酪乳杆菌TK1501发酵的灭活型红枣饮品干预后的结肠炎小鼠结肠中链接蛋白和黏蛋白的表达量增加,肠道屏障功能也有所恢复[25]。本研究结果表明巴氏杀菌发酵乳可能通过增强机体的防御机制降低炎症因子的表达,缓解紧密连接蛋白的损伤,达到预防IBD的作用。
3. 结论
本实验对巴氏杀菌发酵乳具有改善结肠炎这一生物学功能进行了研究。巴氏杀菌发酵乳灌胃小鼠后,在一定程度上降低了IBD小鼠疾病活动指数DAI和结肠组织伤损评分,改善小鼠组织病理变化。小鼠肠道短链脂肪酸中乙酸、丁酸、异丁酸、戊酸以及总短链脂肪酸含量均有不同程度的提高,MPO活性也有所降低,促炎性细胞因子IL-1β和TNF-α分泌的降低和抗炎因子IL-10分泌的提高,对结肠炎起到了抑制作用。同时可以增加小鼠肠道紧密连接蛋白ZO-1和Occludin的表达,增强肠道上皮的屏障功能。综合以上结果,巴氏杀菌发酵乳具有减轻DSS诱导的结肠炎症症状的功效,使小鼠机体各项指标向正常状态转换,为灭活型发酵乳治疗肠道疾病提供了理论支持。但目前对于灭活型发酵乳的临床实验少之又少,所以需要对灭活型发酵乳缓解IBD的机制进行深入研究,建立更多严格的实验来验证灭活发酵乳的临床价值,以便对处于不同阶段、不同症状的IBD患者采用适合条件进行治疗,最后开发新型、功能强大的乳制品,开启治疗IBD的新局面。
-
表 1 动物实验分组
Table 1 Animal experiment group
组别 造模 干预7 d 剂量 空白对照组(C) 自由饮食14 d 生理盐水 10 mL/kg 模型组(M) DSS 14 d 生理盐水 10 mL/kg 阳性对照组(P) DSS 14 d 柳氮磺吡啶 0.45 g/kg 巴氏杀菌发酵乳组(AN) DSS 14 d 巴氏杀菌发酵乳 26 mL/kg 表 2 疾病活动指数(DAI评分表)
Table 2 Disease activity index (DAI scale)
计分(分) 体重下降(%) 粪便性状 便血情况 0 0 正常 阴性 1 1~5 形成粪便但易粘附 弱阳性 2 6~10 半成型软粪便 阳性 3 11~15 粪浆状,但不粘附于肛门 强阳性 4 ≥15 腹泻,粘附肛门 肉眼可见血便 表 3 HE切片组织学评分
Table 3 HE section histological scoring
评分(分) 描述 病变范围 0 正常结肠形态结构,无上皮破坏,隐窝缺失 1 病变范围占所有检查视野1%~25% 2 病变范围占所有检查视野26%~50% 3 病变范围占所有检查视野51%~75% 4 病变范围占所有检查视野75%~100% 病变深度 0 无炎症细胞浸润 1 炎症细胞浸润局限于黏膜层 2 炎症细胞浸润至黏膜下层 3 炎症细胞浸润突破黏膜下层,到达肌层 4 炎症细胞浸润结肠全层 -
[1] SULTAN S, EL-MOWAFY M, ELGAML A, et al. Metabolic influences of gut microbiota dysbiosis on inflammatory bowel disease[J]. Frontiers in Physiology,2021,12:715506. doi: 10.3389/fphys.2021.715506
[2] YASUTOMI E, HIRAOKA S, YAMAMOTO S, et al. Switching between three types of mesalazine formulation and sulfasalazine in patients with active ulcerative colitis who have already received high-dose treatment with these agent[J]. Journal of Clinical Medicine,2019,8(12):2109. doi: 10.3390/jcm8122109
[3] 李陶, 刘雁冰, 靳晓宇. 肠道微生态调节在炎症性肠病中的应用进展[J]. 解放军预防医学杂志,2020,236(11):101−103. [LI T, LIU Y B, JIN X Y. Application progress of intestinal microecological regulation in inflammatory bowel disease[J]. J Prev Med Chin PLA,2020,236(11):101−103. [4] 查睿, 尹辉, 刘涛. DHA及其衍生物对肠道炎症作用的研究进展[J]. 食品工业科技, 2020, 41(24): 314-320. ZHA R, YIN H, LIU T. Research progress of DHA and its derivatives on intestinal inflammation[J]. Science and Technology of Food Industry, 2020, 41(24): 314-320. ]
[5] ZHUANG X J, LI T, LI M Y, et al. Systematic review and meta-analysis: Short-chain fatty acid characterization in patients with inflammatory bowel disease[J]. Inflammatory Bowel Diseases,2019,25(11):1751−1763. doi: 10.1093/ibd/izz188
[6] 吕文君, 王占东, 李凯峰, 等. 长保质期酸奶的发展现状[J]. 科技创新导报,2011,183(3):209−211. [LÜ W J, WANG Z D, LI K F, et al. Current situation of long shelf-life yoghurt[J]. Science and Technology Innovation Herald,2011,183(3):209−211. [7] 张宏福, 夏冰, 陈亮, 等. 灭活乳酸菌研究与应用前沿进展[J]. 饲料工业,2021,636(15):1−8. [ZHANG H F, XIA B, CHEN L, et al. Frontier advances on research and application of inactivated lactic bacteria[J]. Feed Industry,2021,636(15):1−8. [8] CHEN Y, YANG B, ROSS R P, et al. Alleviation effects of Bifidobacterium breve on DSS-induced colitis depends on intestinal tract barrier maintenance and gut microbiota modulation[J]. European Journal of Nutrition,2021,60(1):369−387. doi: 10.1007/s00394-020-02252-x
[9] CHASSAING B, AITKEN J D, MALLESHAPPA M, et al. Dextran sulfate sodium (DSS)-induced colitis in mice[J]. Curr Protoc Immunol,2014,104:15.25.1−15.25.14.
[10] JANG Y J, KIM W K, HAN D H, et al. Lactobacillus fermentum species ameliorate dextran sulfate sodium-induced colitis by regulating the immune response and altering gut microbiota[J]. Gut Microbes,2019,10(6):696−711. doi: 10.1080/19490976.2019.1589281
[11] 赵亚妮, 李瑶, 张妍, 等. 葡聚糖硫酸钠不同给药方式建立小鼠溃疡性结肠炎模型[J]. 实验动物与比较医学,2021,185(1):33−39. [ZHAO Y N, LI Y, ZHANG Y, et al. Establishment of ulcerative colitis model in mice by different drug delivery methods of dextran sodium sulfate[J]. Laboratory Animal and Comparative Medicine,2021,185(1):33−39. [12] ZHANG M, HAO X N, AZIZ T, et al. Exopolysaccharides from Lactobacillus plantarum YW11 improve immune response and ameliorate inflammatory bowel disease symptoms[J]. Acta Biochimica Polonica,2020,67(4):485−493.
[13] RUI Y, ZUO F L, MA H Q, et al. Exopolysaccharide-producing Bifidobacterium adolescentis strains with similar adhesion property induce differential regulation of inflammatory immune response in Treg/Th17 axis of DSS-colitis mice[J]. Nutrients,2019,11(4):782. doi: 10.3390/nu11040782
[14] DOGI C, GARCIA G, DE-LEBLANC A D, et al. Lactobacillus rhamnosus RC007 intended for feed additive: Immune-stimulatory properties and ameliorating effects on TNBS-induced colitis[J]. Beneficial Microbes,2016,7(4):539−547. doi: 10.3920/BM2015.0147
[15] CUI L J, YUAN W, CHEN F Y, et al. Pectic polysaccharides ameliorate the pathology of ulcerative colitis in mice by reducing pyroptosis[J]. Annals of Translational Medicine,2022,10(6):347. doi: 10.21037/atm-22-877
[16] 曹永强, 张健, 郑喆, 等. 副干酪乳杆菌N1115发酵乳对小鼠便秘的改善作用[J]. 食品科学,2018,39(1):185−191. [CAO Y Q, ZHANG J, ZHENG Z, et al. Therapeutic effect of Lactobacillus paracasei N1115 fermented milk in constipated mice[J]. Food Science,2018,39(1):185−191. [17] 曾霖, 张鹏翔, 黄倩, 等. 基于短链脂肪酸防治代谢性疾病的研究进展[J]. 中国全科医学,2022,25(9):1141−1147. [ZENG L, ZHANG P X, HUANG Q, et al. Research progress of the prevention and treatment of metabolic diseases based on short chain fatty acids[J]. Chinese General Practice,2022,25(9):1141−1147. [18] 伊曼, 孙素霞. 丁酸作用机制研究新进展[J]. 重庆医学,2017,46(17):2422−2425. [YI M, SUN S X. New progress in the mechanism of action of butyric acid[J]. Chongqing Medicine,2017,46(17):2422−2425. [19] VINOLO M A, RODRIGUES H G, NACHBAR R T, et al. Regulation of inflammation by short chain fatty acids[J]. Nutrients,2011,3(10):858−876. doi: 10.3390/nu3100858
[20] 王然, 李桂花, 王鹏杰, 等. 灭活型副干酪乳杆菌L9常温酸奶调节肠道菌群缓解便秘作用研究[J]. 食品科学技术学报,2020,38(3):95−101. [WANG R, LI G H, WANG P J, et al. Effect of non-viable Lactobacillus paracasei L9 in normal temperature yogurt on modulating gut microbiota and relieving constipation[J]. Journal of Food Science and Technology,2020,38(3):95−101. [21] LIU Y, LI B G, SU Y H, et al. Potential activity of traditional Chinese medicine against ulcerative colitis: A review[J]. Journal of Ethnopharmacology,2022,289:115084. doi: 10.1016/j.jep.2022.115084
[22] 姚晓翠, 王静. 炎症性肠病患者体内Treg细胞及TGFβ、IL-10的检测及临床意义[J]. 山东医学高等专科学校学报,2017,39(2):107−110. [YAO X C, WANG J. Expression level of Treg, TGFβ and IL-10 in IBD patients and their clinical value[J]. Journal of Shandong Medical College,2017,39(2):107−110. [23] 杨妍. IL-6、IL-10、TNF-α 联合检测在溃疡性结肠炎临床诊断中的意义[J]. 社区医学杂志,2012,10(2):35−36. [YANG Y. Significance of combined detection of IL-6, IL-10 and TNF-α in the clinical diagnosis of ulcerative colitis[J]. Chinese Journal of Cancer Prevention and Treatment,2012,10(2):35−36. [24] 马瑞娟, 刘治麟, 谢晓丽, 等. 灭活乳双歧杆菌U9发酵乳对小鼠溃疡性结肠炎的预防作用[J]. 营养学报,2021,43(2):180−185. [MA R J, LIU Z L, XIE X L, et al. Preventive effect of inactivated Bifidobacterium Animalis subsp. Lactis U9 fermented milk on ulcerative colitis in mice[J]. Acta Nutrimenta Sinica Apr,2021,43(2):180−185. [25] 刘成琪, 霍姝伊, 王宁宇, 等. 灭活副干酪乳杆菌TK1501发酵红枣饮品对葡聚糖硫酸钠诱导的慢性结肠炎改善作用[J]. 食品与发酵工业,2022,48(7):58−63. [LIU C Q, HUO S Y, WANG N Y, et al. Improved effect of inactivated Lactobacillus paracasei TK1501 fermented red jujube drink on chronic colitis induced by DSS[J]. Food and Fermentation Industries,2022,48(7):58−63. [26] 高翔, 张伟. 髓过氧化物酶在宿主防御和炎症中的作用[J]. 中国高原医学与生物学杂志,2021,146(1):69−72. [GAO X, ZHANG W. The role of myeloperoxidase in host defense and inflammation[J]. Chinese High Altitude Medicine and Biology,2021,146(1):69−72. [27] KHAN A A, ALSAHLI M A, RAHMANI A H. Myeloperoxidase as an active disease biomarker: Recent biochemical and pathological perspectives[J]. Med Sci (Basel), 2018, 6(2); 33-53.
[28] YORULMAZ E, YORULMAZ H, GÖKMEN E S, et al. Therapeutic effectiveness of rectally administered fish oil and mesalazine in trinitrobenzenesulfonic acid-induced colitis[J]. Biomedicine & Pharmacotherapy,2019,118:109247.
[29] 李雨芯, 余雪嫣, 黄雪. 白芨多糖上调溃疡性结肠炎小鼠肠黏膜紧密连接蛋白occludin的表达[J]. 基础医学与临床,2021,41(7):941−945. [LI Y X, YU X Y, HUANG X. Bletilla striata polysaccharide up-regulates the expression of tight junction protein occludin in intestinal mucosa of mice with ulcerative colitis[J]. Basic and Clinical Medicine,2021,41(7):941−945. doi: 10.16352/j.issn.1001-6325.2021.07.001 [30] 吴巍芸. 实验性结肠炎小鼠结肠紧密连接蛋白的变化及意义[J]. 广东医学院学报,2016,34(5):467−470. [WU W Y. The changes in tight juction protein of colon of mice with DSS-induced colitis[J]. Journal of Guangdong Medical University,2016,34(5):467−470. [31] PATEL R M, MYERS L S, KURUNDKAR A R, et al. Probiotic bacteria induce maturation of intestinal claudin 3 expression and barrier function[J]. Am J Pathol,2012,180:626−635. doi: 10.1016/j.ajpath.2011.10.025
-
期刊类型引用(9)
1. 向芳. 食品减盐策略研究进展. 食品与发酵工业. 2024(06): 350-358 .  百度学术
百度学术
2. 赵亚丽,张香美,卢涵,杨贝,文港. 传统腌腊肉制品质量安全管理研究. 食品与机械. 2023(01): 55-60+156 .  百度学术
百度学术
3. 刘东,夏金龙. 低钠酱鹿肉的配方优化及贮藏期特性研究. 中国调味品. 2023(03): 67-74 .  百度学术
百度学术
4. 李智,牛超杰,邹爱军,常超. 肉制品加工减盐技术及其应用. 武汉轻工大学学报. 2023(04): 31-38 .  百度学术
百度学术
5. 张彦慧,郑红霞,刘楠,高彦祥,毛立科. 胶体结构设计在减盐食品中的应用. 食品科学. 2022(01): 213-222 .  百度学术
百度学术
6. 吕广英,孔君,郑润愽. 一种低钠休闲香肠的加工技术研究. 肉类工业. 2022(05): 16-19 .  百度学术
百度学术
7. 芮李彤,李海静,张婷婷,郭琦,李子豪,夏秀芳. 食盐对肉制品品质形成的作用及减盐技术研究进展. 肉类研究. 2022(07): 61-67 .  百度学术
百度学术
8. 孙悦,李震,王鹏,徐幸莲. 响应面优化减盐鸡肉松热加工工艺及品质测定. 食品工业科技. 2022(20): 263-273 .  本站查看
本站查看
9. 周平萍. 咸味剂咸度分析研究方法进展. 现代食品. 2022(17): 23-26+37 .  百度学术
百度学术
其他类型引用(5)





 下载:
下载:

 下载:
下载:



