Screening of Three Chitinase-producing Strains, Optimization of Their Chitinase-producing Conditions and Application in the Hydrolysis of Shrimp Shells
-
摘要: 目的:筛选鉴定产几丁质酶的菌株并优化其发酵条件,最终应用于虾壳降解研究。方法:以盐城市滩涂海泥为样品,利用平板筛选水解几丁质的菌株,运用生物信息学方法鉴定菌株,通过单因素优化其发酵条件,并将筛选得到的菌株和优化后的发酵条件用于虾壳发酵。结果:鉴定得到三株显著降解胶体几丁质的菌,分别是发光杆菌(Photobacterium sp. LYM-1)、需钠弧菌(Vibrio sp. WM-1)和希瓦氏菌(Shewanella sp. ZXY-1);优化发酵条件:发光杆菌的碳源为几丁质10 g/L,氮源为NH4Cl 2.0 g/L,接种量为3%,发酵液pH为6.5,温度为32 ℃,发酵1 d酶活最高为15.37±0.55 U/mL,是优化前的4.37倍;需钠弧菌的碳源为几丁质10 g/L,氮源为NH4Cl 2.0 g/L,接种量为3%,发酵液pH为7.5,温度为22 ℃,发酵2 d酶活最高为40.82±6.03 U/mL,是优化前的1.60倍;希瓦氏菌的碳源为几丁质10 g/L,氮源为(NH4)2SO4 2.0 g/L,接种量为3%,发酵液pH为6.5,温度为22 ℃,发酵1 d酶活最高为25.64±3.29 U/mL,是优化前的2.47倍;三株菌均能利用虾壳产几丁质酶,但利用效率均低于几丁质,酶活力分别为10.25±0.95、32.16±2.25和21.81±4.27 U/mL。结论:本研究从盐碱地筛选得到三株产几丁质酶的菌株,优化后酶活力均得到提高,且均能利用虾壳产几丁质酶,为发酵虾壳制备几丁质酶提供新的菌株来源。Abstract: Objective: This study aimed to screen and identify chitinase-producing strains and optimize the fermentation conditions of the target bacteria, which were eventually applied to the degradation fermentation of shrimp shells. Methods: The chitin degradation bacteria were screened on chitin hydrolysis zone taking marine mud from beach in Yancheng as samples, identified via bioinformatics technology, and analyzed in the form of phylogenetic tree. Fermentation conditions for the target strains were modified depending on the single-factor experiment. Results: Photobacterium sp. LYM-1, Vibrio sp. WM-1, and Shewanella sp. ZXY-1 were isolated and identified via 16S rDNA sequence analysis. The optimal fermentation conditions were determined as follows: For Photobacterium sp. LYM-1, chitin (10 g/L) as the carbon source, NH4Cl (2.0 g/L) as the nitrogen source, the inoculated quantified of 3%, initial medium pH6.5, and 32 ℃ for 1 d, in which the highest chitinase activity in the supernatant reached 15.37±0.55 U/mL, achieving 4.37 times higher than that before optimization. For Vibrio sp. WM-1, chitin (10 g/L) as the carbon source, NH4Cl (2.0 g/L) as the nitrogen source, the inoculated quantified of 3%, initial medium pH7.5, and 22 ℃ for 2 d, in which the highest chitinase activity reached 40.82±6.03 U/mL, achieving 1.60 times higher than that before optimization. For Shewanella sp. ZXY-1, chitin (10 g/L) as the carbon source, (NH4)2SO4 (2.0 g/L) as the nitrogen source, the inoculated quantified of 3%, initial medium pH6.5, and 22 ℃ for 1 d, which contributed the highest chitinase activity to reaching 25.64±3.29 U/mL, achieving 2.47 times higher than that before optimization. All three strains in this study could realize chitinase production under optimized conditions using shrimp shell powder as the sole substrate. The chitinase activities of Photobacterium sp. LYM-1, Vibrio sp. WM-1, and Shewanella sp. ZXY-1 on shrimp shell powders were 10.25±0.95, 32.16±2.25 and 21.81±4.27 U/mL, respectively, which was lower than those on chitin powder. Conclusion: Three chitinase-producing strains were successfully screened from saline-alkali soil, of which the enzyme activity was elevated after optimization. All of them could produce chitinase with the shrimp shell utilized as the substrate, serving as potential strains for chitinase production from the fermentation of shrimp shell.
-
几丁质别名甲壳素、甲壳质等,是一种由N-乙酰糖胺通过β-(1,4)糖苷键连接形成的生物大分子物质[1]。大量存在于虾、蟹等水生生物的外壳中,是大部分昆虫外骨骼的重要组成物质[2],同时广泛分布于真菌和藻类等植物的细胞壁中[3]。几丁质在自然界中含量仅次于纤维素,是第二大丰富的多糖物质[1, 3]。1811年,该物质首次由Henri Braconnot在真菌中发现,但由于该物质难以溶于常见的溶剂,因而其应用价值也被严重限制[4]。
现今,人类生活经常用到的几丁质系列产品,大多是通过使用化工方式处理虾壳所得到的,而且在其生产过程中还必须用到大批的浓酸、浓碱等,极易导致环境污染[5],这与二十一世纪提出的低碳经济、环保生态的宗旨完全相悖;而使用生物酶的方式来降解几丁质类物质具备反应条件较缓和,对周围环境污染较小等优势,得到了人们的重视[6-7]。使用微生物几丁质酶,不但能够更全面地开发和利用宝贵的几丁质资源,并且还可在节能环保的要求下制造壳聚糖等更具高附加值的产物,并且几丁质酶自身在生物虫害防治等领域也有着很大的意义[2, 8-9]。沿海地区每年都有大量的虾、蟹壳类废物产生,如长时间不经处理会污染环境卫生,影响城市美观,利用几丁质酶对这些废物进行处理,不仅可以变废为宝,还可以减轻环境的压力,具有十分深远的意义[10]。
几丁质酶广泛存在于细菌、真菌、动物和植物中。研究发现,许多陆地来源的微生物可以产几丁质酶,包括粘质沙雷氏菌[11]、纤维弧菌[12]、假交替单胞菌[13]等细菌,灰盖鬼伞[14]、玉米黑粉菌[15]、金龟子绿僵菌[16]等真菌,以及古菌[17]和病毒[18]等。苏云金芽胞杆菌产生的几丁质酶能够有效杀死害虫,因此具有开发为环保杀虫剂的应用价值[19]。海洋覆盖地球70%的面积,生态环境温和,微生物资源丰富,具有较大的开发潜力。为挖掘更多的产几丁质酶菌株,研究人员将研究对象逐渐转移至海洋来源微生物。丁志雯等[20]从连云港海域沙泥中筛选获得产几丁质酶海洋细菌Dyadobacter sp. CZW019。陈立功等[21]从渤海海域海泥筛选获得产低温几丁质酶菌株Photobacterium sp.。张奇等[22]从广西合浦县大神木海鸭场附近滩涂沉积物筛选获得产几丁质酶菌株Lysobacter firmicutimachus。但上述研究均未将筛选得到的菌株应用于虾壳等富含几丁质的天然物质的发酵,使用自然界资源发酵产几丁质酶才能更好地达到绿色环保的目的。
因此,本研究拟从盐城海滨盐碱地筛选高效水解几丁质的菌株,运用分子生物学技术鉴定菌株类型,并构建系统发育树分析菌的进化模式。通过单因素实验优化菌株的碳源、氮源、pH和温度等发酵条件,并将优化的条件应用于虾壳的发酵,分析菌株降解虾壳的效果,以期为虾壳等废弃物的高值化利用提供新的菌种。
1. 材料与方法
1.1 材料与仪器
从盐城海边滩涂地,不同的地方采集样品,主要包括植物根部附近的土壤、贝壳样品以及滩涂污泥沉积物等20处,将样品立即放入保鲜盒中并带回实验室。几丁质、壳聚糖 分析纯,阿拉丁试剂(上海)有限公司;纤维素、淀粉 分析纯,上海麦克林生化科技有限公司;酵母提取物、胰蛋白胨 分析纯,生工生物(上海)股份有限公司;牛肉膏 分析纯,国药集团化学试剂有限公司;引物 通用生物公司合成;虾壳粉 盐城市农贸市场;蔗糖、乙醇、尿素、K2HPO4、KH2PO4、MgSO4·7H2O、FeSO4·7H2O、NaCl、(NH4)2SO4、NH4Cl等其他试剂 均为国产分析纯。
T100 Thermal Cycler聚合酶链式反应(PCR)仪 BIO-RAD;DYY-8C型电泳仪 北京市六一仪器厂;YXQ-50A立式高压蒸汽灭菌锅 上海博迅医疗生物仪器股份有限公司;HZQ-X300恒温振荡培养箱 上海一恒科学仪器有限公司;Multiskan Skyhigh全波长酶标仪 赛默飞世尔科技(中国)有限公司;GWA UN1-F20超纯水系统 北京普析通用仪器有限责任公司。
1.2 实验方法
1.2.1 培养基配制
LB培养基:胰蛋白胨10.0 g/L,NaCl 5.0 g/L,酵母膏5.0 g/L,pH7.0~8.0,121 ℃灭菌20 min。
混合盐离子溶液[23]:MgSO4·7H2O 50.0 g/L,FeSO4·7H2O 1.0 g/L,K2HPO4 70.0 g/L,KH2PO4 30.0 g/L,pH7.0。
液体富集培养基:混合盐离子溶液10 mL,几丁质粉末8.0 g/L,(NH4)2SO4 2.0 g/L,pH7.2~7.5,121 ℃灭菌20 min。
胶体几丁质培养基:混合盐离子溶液10 mL,胶体几丁4.0 g/L,(NH4)2SO4 2.0 g/L,琼脂15.0 g/L,pH7.0,121 ℃灭菌20 min。
种子培养基:混合盐离子溶液10 mL,几丁质粉末10.0 g/L,酵母粉5.0 g/L,蛋白胨5.0 g/L,pH7.0,121 ℃灭菌20 min。
发酵培养基:混合盐离子溶液10 mL,几丁质粉末10.0 g/L,(NH4)2SO4 2.0 g/L,pH7.0,121 ℃灭菌20 min。
1.2.2 产几丁质酶菌株的筛选
分别称取5.0 g采集的样品,加入25 mL无菌水中,混匀后于30 ℃、180 r/min培养4 h,取1 mL上清液加入到29 mL液体富集培养基中,混匀后于30 ℃、200 r/min培养3~4 d后,取样1 mL培养液并梯度稀释至10−3、10−4、10−5,分别吸取200 μL稀释液涂布于胶体几丁质培养皿上,30 ℃倒置培养3~5 d,期间每天按时观察菌落生长及透明圈产生情况。挑取周围产透明圈的菌株至无菌水中,混匀后用接种环划线涂布至胶体几丁质培养基上,纯化出具有透明圈的单菌落。
1.2.3 产几丁质酶菌株菌株的鉴定
挑取划线培养皿中的单菌落至5 mL灭菌的LB培养基试管中,37 ℃,220 r/min振荡过夜培养。培养结束后向试管中添加2 mL甘油,混匀分装至无菌冻存管,−80 ℃保存。配制如下细胞裂解液:50 mmol/L NaCl,10% SDS,EDTA 500 mmol/L,1% Triton-X100和50 mmol/L Tris-HCl,调整pH至8.0。分别取−80 ℃保存的菌体,离心收集菌体沉淀。取150 uL细胞裂解缓冲液到菌体沉淀中,同时加入5 µL蛋白酶K。在55 ℃条件下放置3 h,90 ℃高温灭活,DNA模板制备完成。设计16S rDNA通用引物,由通用生物公司合成,表1是通用引物序列。
表 1 16S rDNA通用引物序列Table 1. 16S rDNA universal primer sequence引物名称 引物序列 27F AGAGTTTGATCCTGGCTCAG 1492R GGTTACCTTGTTACGACTT PCR反应:95 ℃预变性5 min,95 ℃变性30 s,55 ℃复性30 s,72 ℃延伸1.5 min,变性、复性和延伸循环30次,72 ℃终延伸10 min,最后4 ℃保温。使用琼脂制备1%的核酸胶。然后用凝胶成像仪拍照切胶,使用胶回收试剂盒纯化回收PCR产物,将PCR产物送至通用生物公司进行测序分析。将测序结果提交BLAST,与数据库中同源性较高的序列比对,挑选相关的序列导入MEGA11软件进行16S rDNA序列的比对分析,从而构建系统发育树。
1.2.4 菌株种子液的制备及初始发酵工艺
从超低温冰箱中取出前面筛选鉴定得到的菌株,接种到10 mL灭菌的种子培养基中,37 ℃、200 r/min培养至OD600值0.8,得种子液,取种子培养基并接种于灭菌的发酵培养基中进行发酵。发酵条件为:3% (v/v)接种量,100 mL发酵培养基,几丁质粉末10.0 g/L,(NH4)2SO4 2.0 g/L,pH7.0,32 ℃、200 r/min发酵培养2 d,取发酵液上清测定酶活。
1.2.5 酶活测定方法
参考傅丽君等[24]的方法进行几丁质酶活的测定。发酵完成后,取1 mL发酵液,4000 r/min离心10 min,取100 μL上清液,与100 μL胶体几丁质[24]混匀,在45 ℃水浴中反应30 min,反应结束后加入300 μL DNS[25]混匀,置于95 ℃水浴中煮10 min,冷却后加入500 μL去离子水并混匀,取200 μL于96孔板中,用酶标仪测540 nm处吸光值,以预先加热灭活的发酵液上清作为阴性对照。在45 ℃反应条件下每分钟产生1 μmol N-乙酰-D-氨基葡萄糖需要的酶量定义为1个酶活力单位(1 U)。初始发酵工艺中的酶活测定,以及后续单因素优化实验中的酶活测定均采用此方法。
1.2.6 单因素优化产酶发酵条件
最适发酵产酶时间:3% (v/v)接种量,100 mL发酵培养基,几丁质粉末10.0 g/L,(NH4)2SO4 2.0 g/L,pH7.0,32 ℃、200 r/min发酵,分别在发酵的第1、2、3、4、5、6、7 d检测酶活。
碳源添加种类:碳源分别为10 g/L几丁质、壳聚糖、纤维素、蔗糖、淀粉和酵母提取物,3% (v/v)接种量,100 mL发酵培养基,(NH4)2SO4 2.0 g/L,pH7.0,32 ℃、200 r/min发酵2 d,测定酶活。
氮源添加种类:氮源分别为2.0 g/L硫酸铵、氯化铵、蛋白胨、牛肉膏和尿素,3% (v/v)接种量,100 mL发酵培养基,几丁质10.0 g/L,pH7.0,32 ℃、200 r/min发酵2 d,测定酶活。
发酵培养温度:温度分别为16、22、28、32、37、42和50 ℃,3% (v/v)接种量,100 mL发酵培养基,硫酸铵2.0 g/L,几丁质10.0 g/L,pH7.0,200 r/min发酵2 d,测定酶活。
发酵液初始pH:使用3 mol/L的HCl和NaOH调节发酵液初始pH,分别为5.5、6.0、6.5、7.0、7.5、8.0、8.5和9.0,定容至100 mL,3% (v/v)接种量,硫酸铵2.0 g/L,几丁质10.0 g/L,32 ℃、200 r/min发酵2 d,测定酶活。
1.2.7 降解虾壳粉产几丁质酶的应用
使用优化得到的最佳发酵条件,将种子液接种到以虾壳粉为碳源的培养基中,取不同时间点(1、2、3、4、5、6和7 d)的发酵液,并保存于-20 ℃,最后同时测定酶活。
1.3 数据处理
单因素实验数据处理将三株菌株中酶活最高的设定为100%,相对酶活(%)=样品酶活/最高酶活×100。所有实验均为三组平行,采用Excel 2019对试验数据进行统计分析,以Origin 8.0制图,系统发育树的构建使用MEGA11软件。
2. 结果与分析
2.1 产几丁质酶菌株的筛选
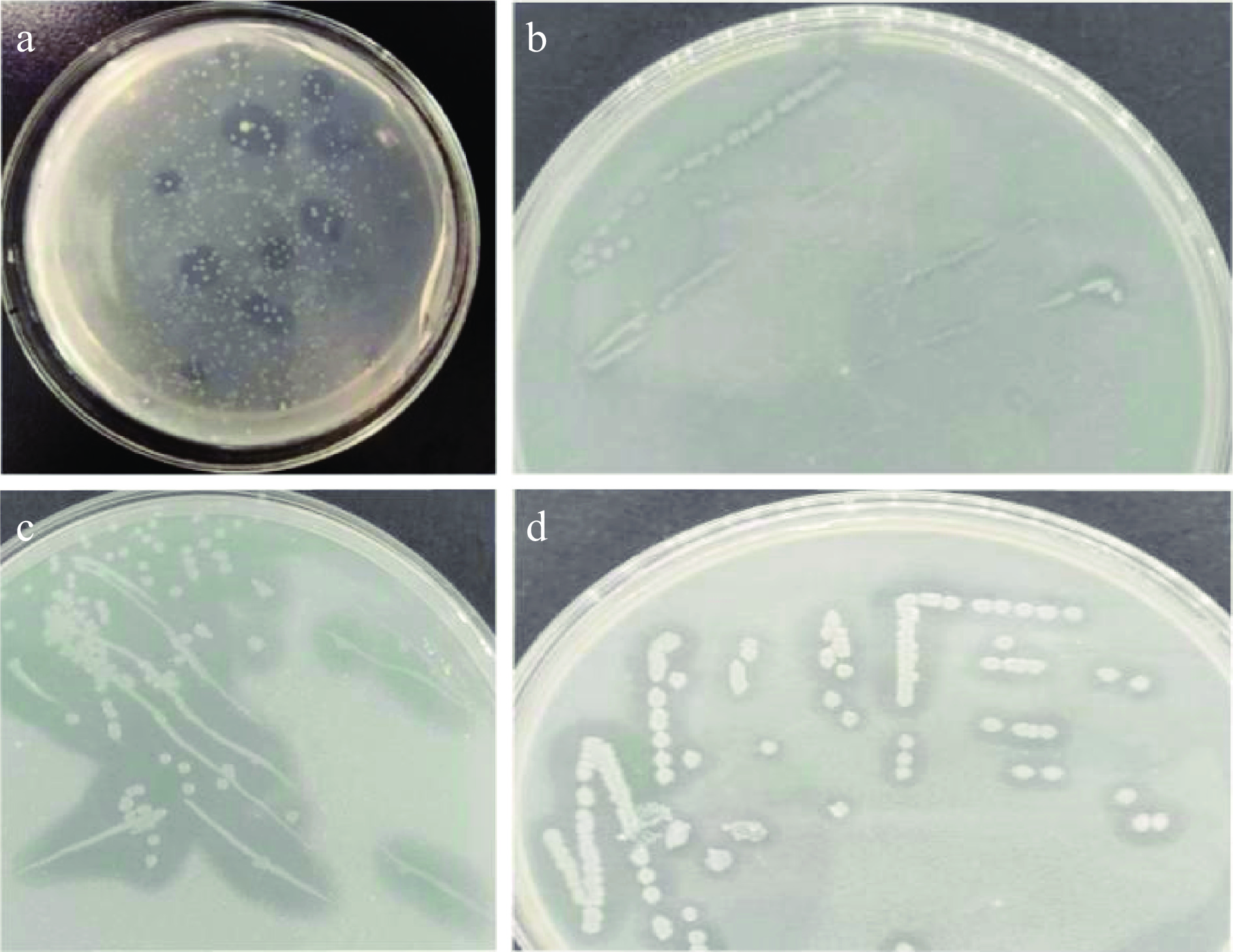
胶体几丁质固体培养基倒置培养3 d后,胶体几丁质固体培养基上长出大量菌株,并产生无色透明圈,结果如图1a所示。挑选有透明圈的菌株进行划线纯化,从而得到单菌落,如图1b、1c和1d所示,共得到14株可能的菌株。
2.2 菌株16S rDNA的扩增及序列分析
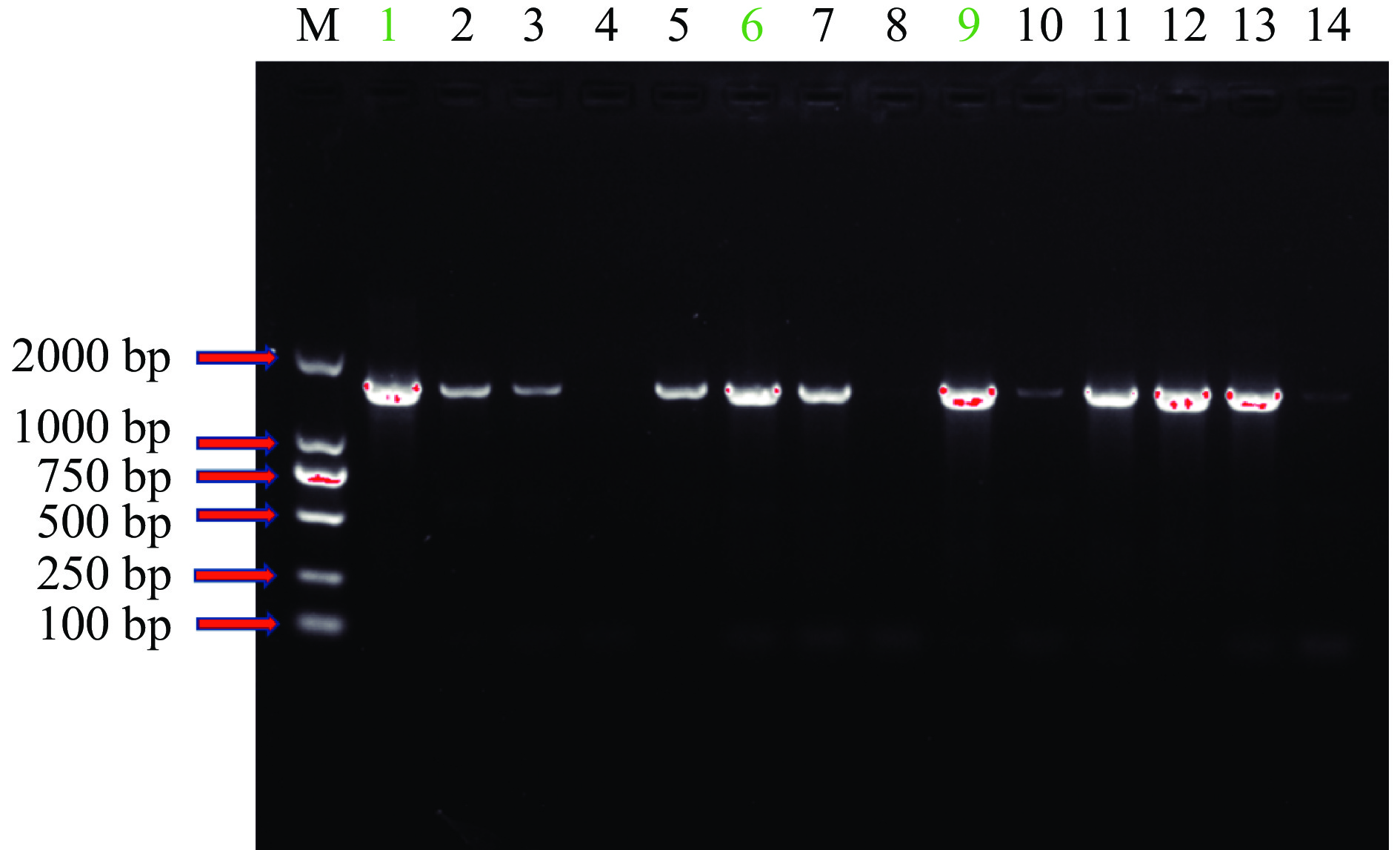
使用16S rDNA通用引物,对纯化得到的14株细菌进行PCR扩增,结果如图2所示。将PCR产物送至通用生物公司进行测序鉴定,通过对序列比对分析,发现图2中编码1、6和9分别是三株不同的菌,分别命名为ZXY-1、WM-1和LYM-1,其余序列均与其相同。
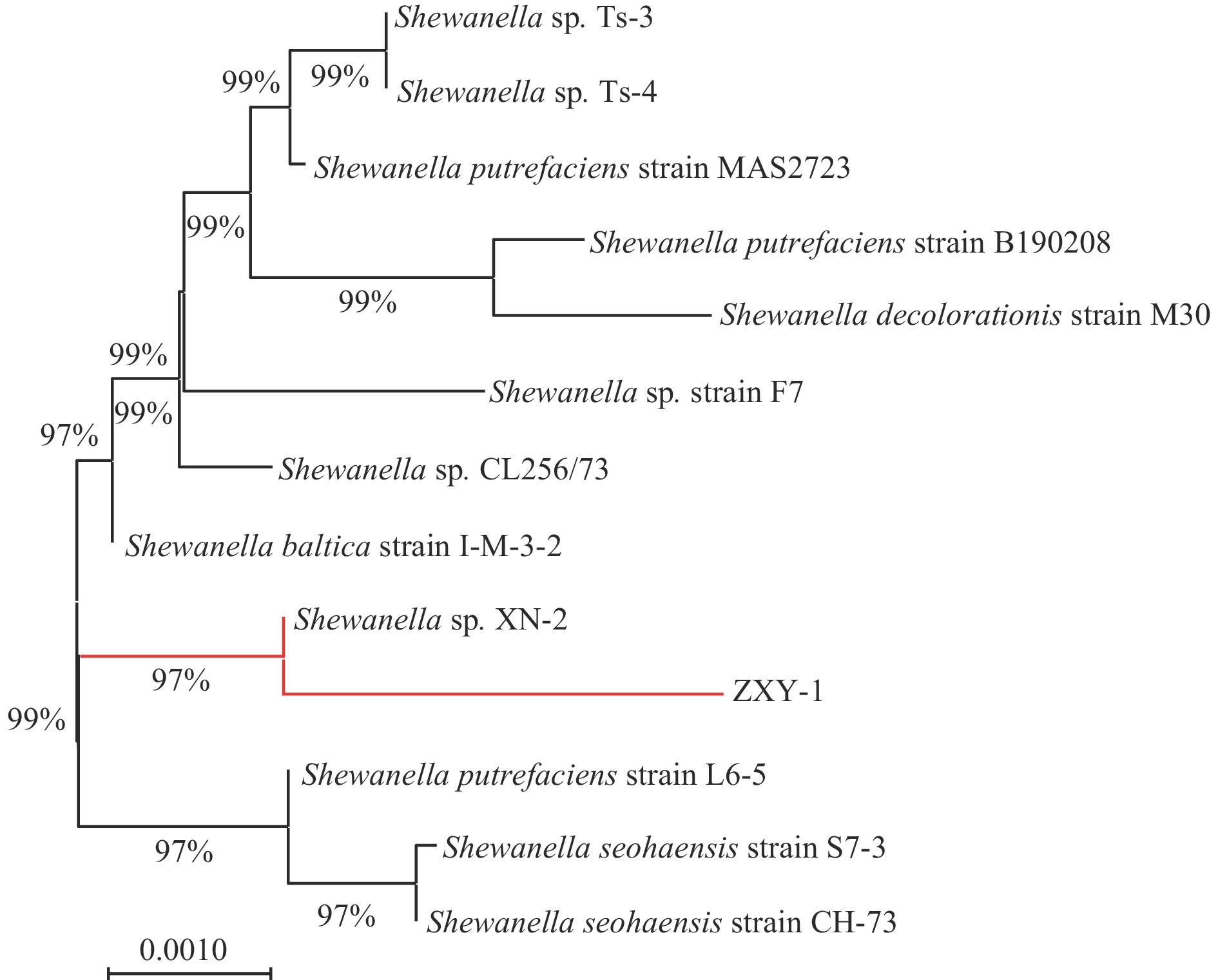
运用MEGA11软件进行16Sr DNA序列的对比分析,挑选GenBank数据库里的基因序列进行同源比对,并构建系统发育树,如图3。由图可知ZXY-1与Shewanella sp. XN-2(登录号:KP265975)菌株亲缘关系最接近,16S rDNA相似度为97%,可初步判断ZXY-1为希瓦氏菌。
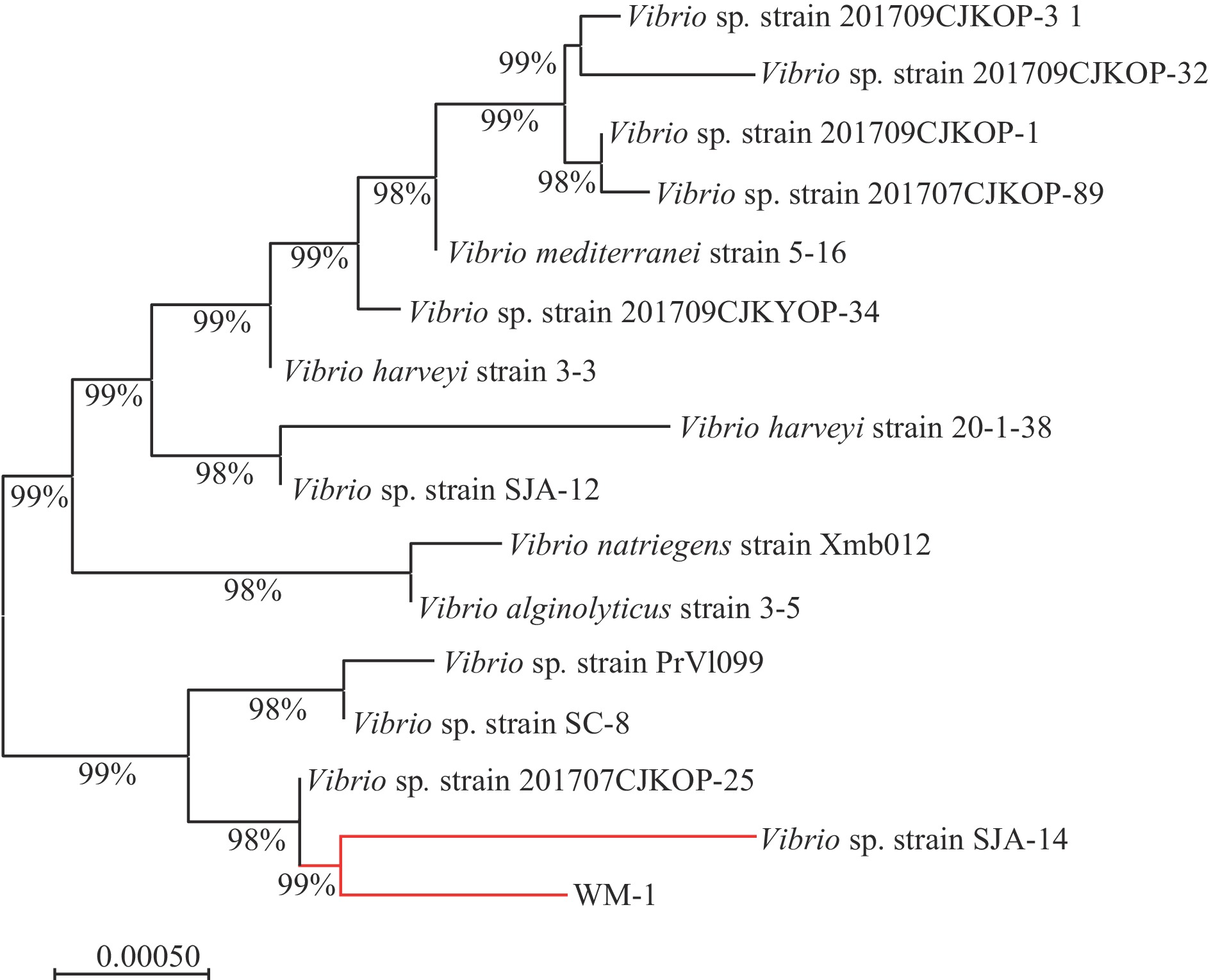
运用MEGA11软件进行16S rDNA序列的对比分析,挑选GenBank数据库里的基因序列进行同源比对,并构建系统发育树,如图4。由图可知WM-1与Vibrio sp. strain SJA-14(登录号:MN635999)菌株亲缘关系最接近,16S rDNA相似度为99%,可初步判断WM-1为需钠弧菌。
运用MEGA11软件进行16S rDNA序列的对比分析,挑选GenBank数据库里的基因序列进行同源比对,并构建系统发育树,如图5。由图可知LYM-1与Photobacterium sp. SY4(登录号:MN635999)菌株亲缘关系最接近,16S rDNA相似度为95%,可初步判断LYM-1为发光杆菌。
将上述3株菌株寄往广东省微生物菌种保藏中心进行保藏(GDMCC)。保藏信息分别为:希瓦氏菌Shewanella sp. ZXY-1,GDMCC编号1.3007;需钠弧菌Vibrio sp. WM-1,GDMCC编号1.3008;发光杆菌Photobacterium sp. LYM-1,GDMCC编号1.3009。
2.3 发酵工艺优化前酶活测定结果
标准曲线的绘制以N-乙酰-D-氨基葡萄糖为标准品,设置浓度梯度,得到标曲的方程式为:Y=0.146X−0.1018,R2=0.9931。以发酵24 h为标准,测定菌株LYM-1优化前酶活力为3.52±0.22 U/mL,菌株WM-1优化前酶活力为25.47±0.35 U/mL,菌株ZXY-1优化前酶活力为10.36±0.19 U/mL。
2.4 单因素发酵产酶条件优化
2.4.1 最适产酶发酵时间
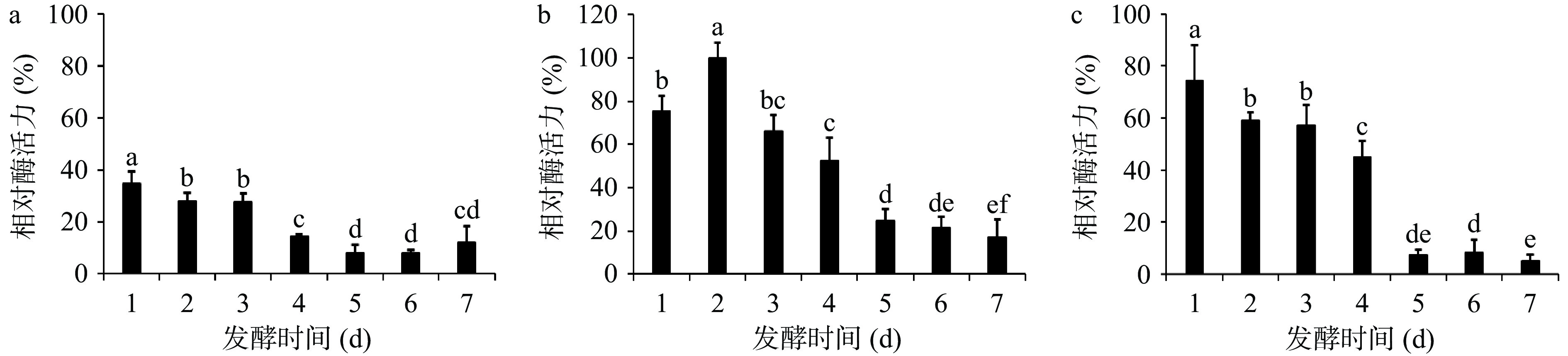
发酵时间对三株菌产酶的结果影响如图6所示。发光杆菌LYM-1(图6a)在发酵条件下培养 1 d酶活力达最大,随着发酵时间的延长,酶活力逐渐降低,发酵1 d和2 d差异显著(P<0.05),发酵2~3 d差异不显著(P>0.05)。需钠弧菌WM-1(图6b)在发酵条件下培养2 d酶活力达最大,然后酶活力也逐渐降低,差异显著(P<0.05);希瓦氏菌ZXY-1(图6c)在发酵条件下培养1 d酶活力达最大,发酵2~3 d,酶活力差异不显著(P>0.05),其他发酵时长的酶活力变化差异显著(P<0.05)。造成酶活力达到最大以后又降低的原因可能是:由于发酵液中营养成分减少,产物的浓度增大、pH降低等不利因素的影响[26],菌株繁殖受到抑制,因而酶活力开始减弱。三株菌的发酵时间依次选定为:1、2和1 d。
2.4.2 最适碳源
生物体代谢的核心是碳代谢,碳代谢过程为生物活动提供能力,为有机物的合成提供碳骨架,是生物体生命活动的最基础能源物质之一[27]。由图7可知,以不同的碳源为底物发酵,三株菌产几丁质酶的活力从大到小顺序为:几丁质>酵母提取物>壳聚糖>淀粉>蔗糖>纤维素。由此确定几丁质为三株菌发酵产酶的最佳碳源,酵母提取物是一种富含蛋白质、多肽、核苷酸、维生素、矿物质、游离氨基酸的功能性营养物质[28],也有较强的促进生长和产酶能力。而三株菌可能因为不产内切酶β-1,4-葡聚糖酶(EGs,EC 3.2.1.4)、外切β-1,4-葡聚糖酶(CBHs,EC 3.2.1.91)和β-1,4-葡萄糖苷酶(BGs,EC 3.2.1.21)3类纤维素酶[29-30],无法利用纤维素作为碳源。而蔗糖作为碳源,可能因为基质浓度过高而抑制菌体生长和酶活,进而导致出现蔗糖利用率不高的现象[1]。因此,三株菌均选定几丁质为最适碳源。
2.4.3 最适氮源
氮源是微生物生长必需的营养成分之一,也是构成生物体蛋白质的重要元素[1],可以前体物质的形式直接参与次生代谢活动[27]。无机氮源是微生物生长的速效氮源,而有机氮源对发酵起着关键的调控作用,可提高生长速率;控制生长水平,促进次级代谢产物产生;控制生长速率,影响菌的生长状态,从而影响发酵效率[31-32]。三株菌发酵的最适氮源筛选结果如图8所示,结果显示发光杆菌LYM-1(图8a)和需钠弧菌WM-1(图8b)的最适氮源均为氯化铵;希瓦氏菌ZXY-1(图8c)最适碳源为硫酸铵。这三株菌均能利用有机氮源和无机氮源,利用无机氮源的效果均优于有机氮源。三株菌的最适氮源依次选定为:氯化铵、氯化铵和硫酸铵。
2.4.4 最适温度
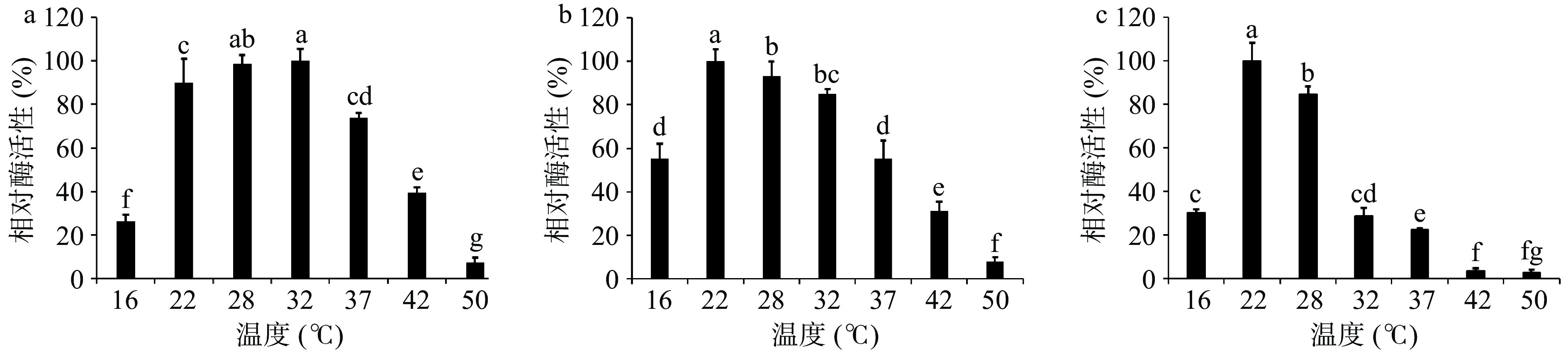
三株菌最适温度优化结果如图9所示。低温菌体繁殖速度减缓,且总体酶活力也不高。在到达最适温度前,随着温度的上升,代谢强度增大,促进细菌生长繁殖[33],几丁质酶活力也随之上升。发光杆菌LYM-1(图9a)在32 ℃时几丁质酶活达到最高,与28 ℃的发酵结果差异不显著(P>0.05);需钠弧菌WM-1(图9b)在22 ℃时几丁质酶活达到最高,之后酶活力降低,差异显著(P<0.05);希瓦氏菌ZXY-1(图9c)在22 ℃时几丁质酶活力达到最高,温度再升高,酶活力降低较快,且差异显著(P<0.05)。随着温度升高,细菌生长速率减小,高温也会使酶蛋白变性失活,整体酶活力也不断下降。三株菌的最适温度依次选定为:32 、22 和22 ℃。
2.4.5 发酵液最适初始pH
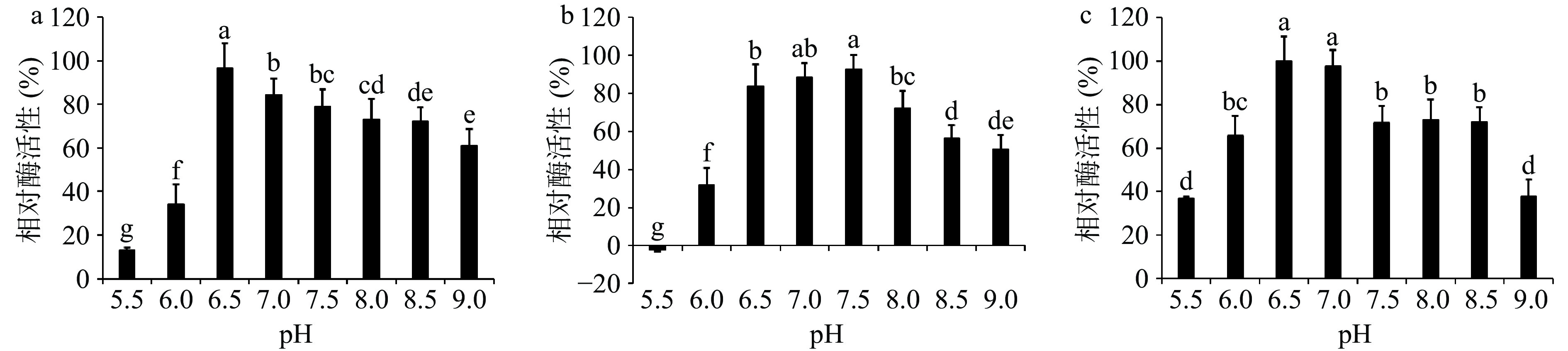
三株菌发酵液最适初始pH优化结果如图10所示。pH偏低或偏高都不利于细菌的繁殖,且酶活性也不高。发光杆菌LYM-1(图10a)在pH6.5~9.0范围内均有较高的活性,最适pH为6.5;需钠弧菌WM-1(图10b)在pH6.5~8.0范围内均有较高的活性,最适pH为7.5;希瓦氏菌ZXY-1(图10c)在pH6.5~8.5范围内均有较高的活性,最适pH为6.5。结果显示3种菌均适应于中性的产酶环境,与大部分细菌最适发酵产酶的pH(6.3~7.5)范围吻合[34-35]。三株菌的最适pH依次选定为:6.5、7.5和6.5。
使用单因素实验得到的最优发酵工艺条件再次发酵,结果见表2,最优发酵条件产几丁质酶活为:Photobacterium sp. LYM-1酶活为15.37±0.55 U/mL,是优化前酶活力的4.37倍;Vibrio sp. WM-1酶活达到40.82±6.03 U/mL,是优化前酶活力的1.60倍;Shewanella sp. ZXY-1酶活达到25.64±3.29 U/mL,是优化前酶活力的2.47倍。张奇等[22]发现菌株GXUN-20,优化发酵工艺后酶活达到0.965 U/mL,而本研究中三株菌几丁质酶活明显高于菌株GXUN-20。
表 2 优化前后酶活力对比Table 2. Comparison of enzyme activity before and after optimization菌株 优化前(U/mL) 优化后(U/mL) 提高倍数 发光杆菌LYM-1 3.52±0.22 15.37±0.55 4.37 需钠弧菌WM-1 25.47±0.35 40.82±6.03 1.60 希瓦氏菌ZXY-1 10.36±0.19 25.64±3.29 2.47 2.5 降解虾壳粉产几丁质酶的应用
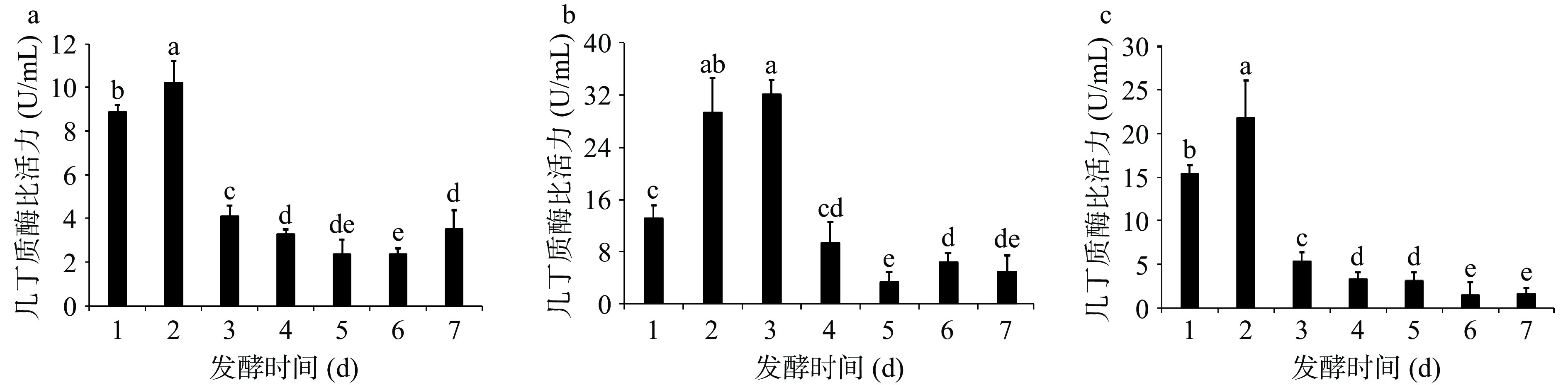
将虾壳粉作为发酵碳源,以优化后的最适发酵条件进行发酵,检测三株菌1~7 d酶活。结果显示三株菌均在培养1~3 d几丁质酶活达最高,后期酶活逐渐下降,4 d后酶活变化不显著(P
>0.05)。发光杆菌LYM-1(图11a)和希瓦氏菌ZXY-1(图11c)在2 d时降解虾壳粉产几丁质酶酶活达最高;需钠弧菌WM-1(图11b)在3 d时降解虾壳粉产几丁质酶酶活达最高。与优化后的几丁质发酵结果相比,虾壳粉最适发酵产酶时间推迟1 d,原因可能是干燥虾壳除甲壳素外,还含有碳酸钙、蛋白质以及微量脂类物质等[36],在开始阶段利用碳源(几丁质)的速率较低,减缓了菌株产酶效率。 用优化后的发酵条件发酵虾壳粉,结果见表3,可以看到三株菌降解几丁质和虾壳粉产几丁质酶的能力从大到小依次为:需钠弧菌WM-1>希瓦氏菌ZXY-1>发光杆菌LYM-1。几丁质酶是一类特性差异较大的水解酶类,不同菌种来源,酶学性质存在较大的差异[37]。三株菌以几丁质为底物生产的几丁质酶活力均优于虾壳粉,虾壳粉中甲壳素不易与几丁质酶直接结合,影响酶促反应效率,是发酵虾壳粉产几丁质酶的活性低于发酵纯几丁质粉末产几丁质酶的主要原因之一[20],这也是利用天然几丁质产物的难点。目前鲜有关于菌株直接利用虾壳的报道,而本研究成功获得三株可以利用虾壳产几丁质酶的菌株,具有较强的应用价值。
表 3 几丁质和虾壳粉为底物的酶活力对比Table 3. Comparison of enzyme activity between chitin and shrimp shell powder substrates菌株 几丁质(U/mL) 虾壳粉(U/mL) 发光杆菌LYM-1 15.37±0.55 10.25±0.95 需钠弧菌WM-1 40.82±6.03 32.16±2.25 希瓦氏菌ZXY-1 25.64±3.29 21.81±4.27 3. 结论
本研究从盐城海滨盐碱地采集样本,筛选得到高效水解几丁质的菌株,利用分子生物学技术鉴定筛选得到三株不同属的菌株,分别为发光杆菌Photobacterium sp. LYM-1、需钠弧菌Vibrio sp. WM-1和希瓦氏菌Shewanella sp. ZXY-1。通过单因素实验,以几丁质酶活力为指标,优化了包括发酵时间、碳源、氮源、温度和pH在内的几个关键发酵条件,确定了三株菌的最佳发酵工艺,优化后三株菌产生的几丁质酶酶活均得到较大提高。使用虾壳粉作为碳源,同时使用最佳发酵工艺进行发酵。三株菌均可利用虾壳粉产几丁质酶,酶活与发酵几丁质相比稍低,其中Vibrio sp. WM-1的产几丁质酶能力明显优于另两株。本研究发现了新的降解几丁质的菌种,为降解利用虾壳等富含几丁质的废弃物提供了重要菌株,也为其降解机制的研究奠定基础。
-
表 1 16S rDNA通用引物序列
Table 1 16S rDNA universal primer sequence
引物名称 引物序列 27F AGAGTTTGATCCTGGCTCAG 1492R GGTTACCTTGTTACGACTT 表 2 优化前后酶活力对比
Table 2 Comparison of enzyme activity before and after optimization
菌株 优化前(U/mL) 优化后(U/mL) 提高倍数 发光杆菌LYM-1 3.52±0.22 15.37±0.55 4.37 需钠弧菌WM-1 25.47±0.35 40.82±6.03 1.60 希瓦氏菌ZXY-1 10.36±0.19 25.64±3.29 2.47 表 3 几丁质和虾壳粉为底物的酶活力对比
Table 3 Comparison of enzyme activity between chitin and shrimp shell powder substrates
菌株 几丁质(U/mL) 虾壳粉(U/mL) 发光杆菌LYM-1 15.37±0.55 10.25±0.95 需钠弧菌WM-1 40.82±6.03 32.16±2.25 希瓦氏菌ZXY-1 25.64±3.29 21.81±4.27 -
[1] HARMSEN R A G, TUVENG T R, ANTONSEN S G, et al. Can we make chitosan by enzymatic deacetylation of chitin?[J]. Molecules (Basel, Switzerland),2019,24(21):3862. doi: 10.3390/molecules24213862
[2] MATANO C, KOLKENBROCK S, HAMER S N, et al. Corynebacterium glutamicum possesses β-N-acetylglucosaminidase[J]. BMC Microbiology,2016,16(1):177. doi: 10.1186/s12866-016-0795-3
[3] YAN Q, HONG E, FONG S S, et al. Study of ChiR function in Serratia marcescens and its application for improving 2,3-butanediol from crystal chitin[J]. Applied Microbiology and Biotechnology,2017,101(20):7567−7578. doi: 10.1007/s00253-017-8488-x
[4] 张岩, 关菲菲, 伍宁丰, 等. 几丁质脱乙酰酶的研究进展[J]. 生物技术通报,2019,35(11):179−186. [ZHANG Y, GUAN F F, WU N F, et al. Research progress on chitin deacetylase[J]. Biotechnology Bulletin,2019,35(11):179−186. doi: 10.13560/j.cnki.biotech.bull.1985.2019-0449 [5] MA X, GÖZAYDIN G, YANG H, et al. Upcycling chitin-containing waste into organonitrogen chemicals via an integrated process[J]. Proceedings of the National Academy of Sciences of the United States of America,2020,117(14):7719−7728. doi: 10.1073/pnas.1919862117
[6] WENDISCH V F, BRITO L F, LOPEZ M, et al. The flexible feedstock concept in industrial biotechnology: Metabolic engineering of Escherichia coli, Corynebacterium glutamicum, Pseudomonas, Bacillus and yeast strains for access to alternative carbon sources[J]. Journal of Biotechnology,2016,234:139−157. doi: 10.1016/j.jbiotec.2016.07.022
[7] COMA M, MARTINEZ-HERNANDEZ E, ABELN F, et al. Organic waste as a sustainable feedstock for platform chemicals[J]. Faraday Discussions,2017,202:175−195. doi: 10.1039/C7FD00070G
[8] GHORMADE V, PATHAN E K, DESHPANDE M V, et al. Can fungi compete with marine sources for chitosan production?[J]. International Journal of Biological Macromolecules, 2017, 104 (Pt B): 1415-1421.
[9] NOYES N R, WEINROTH M E, PARKER J K, et al. Enrichment allows identification of diverse, rare elements in metagenomic resistome-virulome sequencing[J]. Microbiome,2017,5(1):142. doi: 10.1186/s40168-017-0361-8
[10] ARNOLD N D, BRÜCK W M, GARBE D, et al. Enzymatic modification of native chitin and conversion to specialty chemical products[J]. Marine Drugs,2020,18(2):93. doi: 10.3390/md18020093
[11] 何迎春, 李小湘, 高必达, 等. 含粘质沙雷氏菌几丁质酶SchiA基因的植物转化质粒pBG1112构建和水稻遗传转化[J]. 农业生物技术学报,2003(2):121−126. [HE Y C, LI X X, GAO B D, et al. Construction of a new plant transformation vector pBG1112 with a chitinase gene SchiA from Serratia marcescens and its genetic transformation in rice[J]. Journal of Agricultural Biotechnology,2003(2):121−126. doi: 10.3969/j.issn.1674-7968.2003.02.003 [12] MONGE E C, TUVENG T R, VAAJE-KOLSTAD G, et al. Systems analysis of the glycoside hydrolase family 18 enzymes from Cellvibrio japonicus characterizes essential chitin degradation functions[J]. Journal of Biological Chemistry,2018,293(10):3849−3859. doi: 10.1074/jbc.RA117.000849
[13] WANG Y J, JIANG W X, ZHANG Y S, et al. Structural insight into chitin degradation and thermostability of a novel endochitinase from the glycoside hydrolase family 18[J]. Frontiers in Microbiology,2019(10):2457.
[14] ZHOU Y, KANG L, NIU X, et al. Purification, characterization and physiological significance of a chitinase from the pilei of Coprinopsis cinerea fruiting bodies[J]. FEMS Microbiology Letters,2016,363(12):120. doi: 10.1093/femsle/fnw120
[15] LANGNER T, ÖZTÜRK M, HARTMANN S, et al. Chitinases are essential for cell separation in Ustilago maydis[J]. Eukaryotic Cell,2015,14(9):846−857. doi: 10.1128/EC.00022-15
[16] STAATS C C, FAU K L, FAU L I, et al. Metarhizium anisopliae chitinase CHIT30 is involved in heat-shock stress and contributes to virulence against Dysdercus peruvianus[J]. Fungal Biology,2013,117(2):137−144. doi: 10.1016/j.funbio.2012.12.006
[17] ZHANG Y, AN R. , YATSUNAMI R, et al. Characterization of a haloarchaeal GH family 18 chitinase with additional acidic amino acids on its protein surface[J]. Journal of Japanese Society for Extremophiles,2010,9(2):72−74. doi: 10.3118/jjse.9.72
[18] WENNMANN J T, FAU G A G, JEHLE J A, et al. The genome sequence of Agrotis segetum nucleopolyhedrovirus B (AgseNPV-B) reveals a new baculovirus species within the Agrotis baculovirus complex[J]. Virus Genes,2015,50(2):260−276. doi: 10.1007/s11262-014-1148-7
[19] 冯俊丽, 朱旭芬. 微生物几丁质酶的分子生物学研究[J]. 浙江大学学报(农业与生命科学版),2004(1):105−111. [FENG J L, ZHU X F. Study on molecular biology of microbial chitinase[J]. Journal of Zhejiang University (Agriculture and Life Sciences),2004(1):105−111. doi: 10.3321/j.issn:1008-9209.2004.01.022 [20] 丁志雯, 刘耀东, 黄志发, 等. 产几丁质酶海洋细菌Dyadobacter sp. CZW019的筛选、鉴定及酶学性质研究[J]. 江苏海洋大学学报(自然科学版),2021,30(2):22−29. [DING Z W, LIU Y D, HUANG Z F, et al. Screening, identification and enzymic properties of a chitinase-producing marine bacterium Dyadobacter sp. CZW019[J]. Journal of Jiangsu Ocean University (Natural Science Edition),2021,30(2):22−29. [21] 陈立功, 吴家葳, 张庆芳, 等. 产低温几丁质酶菌株的筛选、鉴定与产酶条件优化[J]. 食品工业科技,2020,41(23):85−90, 98. [CHEN L G, WU J W, ZHANG Q F, et al. Screening and identification of a cold-adapted chitinolytic bacterium strain and optimization of its chitinase fermentation conditions[J]. Science and Technology of Food Industry,2020,41(23):85−90, 98. doi: 10.13386/j.issn1002-0306.2019120158 [22] 张奇, 王一兵, 申乃坤, 等. 产几丁质酶菌株GXUN-20的筛选、鉴定及其产酶条件优化[J]. 食品工业科技,2021,42(24):119−127. [ZHANG Q, WANG Y B, SHEN N K, et al. Screening and identification of chitinase-producing strain GXUN-20 and optimization of its enzyme producing conditions[J]. Science and Technology of Food Industry,2021,42(24):119−127. doi: 10.13386/j.issn1002-0306.2021040118 [23] LIU C, SHEN N, WU J, Cloning, et al. Expression and characterization of a chitinase from Paenibacillus chitinolyticus strain UMBR 0002[J]. Peer J,2020,8:e8964. doi: 10.7717/peerj.8964
[24] 傅丽君, 杨磊, 黄锦泉, 等. 产几丁质酶Bt-016菌株发酵条件优化探究[J]. 莆田学院学报,2019,26(5):46−50, 99. [FU L J, YANG L, HUANG J Q, et al. Optimization of Fermentation conditions of chitinase producing Bt-016 strain[J]. Journal of Putian University,2019,26(5):46−50, 99. doi: 10.3969/j.issn.1672-4143.2019.05.013 [25] 王海东, 陈飚, 伦镜盛, 等. 产几丁质酶菌株SWCH-6的筛选、鉴定及其产酶条件的优化研究[J]. 微生物学通报,2008(5):705−711. [WANG H D, CHEN B, LUN J S, et al. Screening, identification of a chitinolytic bacterium strain SWCH-6 and its optimal chitinase fermentation conditions[J]. Microbiology China,2008(5):705−711. [26] 田曼丽, 王杰. 微生物生长特性的试验研究[J]. 科学技术创新,2021(8):81−82. [TIAN M L, WANG J. Experimental study on microbial growth characteristics[J]. Scientific and Technological Innovation,2021(8):81−82. doi: 10.3969/j.issn.1673-1328.2021.08.038 [27] 张雷, 张蕾, 王玲莉, 等. γ-聚谷氨酸生产菌株的鉴定及发酵培养基优化[J]. 食品工业科技,2020,41(20):64−71. [ZHANG L, ZHANG L, WANG L L, et al. Identification and optimization of fermentational condition of γ-polyglutamic acid producing strain[J]. Science and Technology of Food Industry,2020,41(20):64−71. [28] 杨龙, 邢为国. 酵母提取物对白对虾生长性能、抗氧化及机体成分的影响[J]. 中国饲料,2021(12):70−73. [YANG L, XING W G. Effects of yeast extract on growth performance, antioxidation and body composition of Penaeus vannamei[J]. China Feed,2021(12):70−73. doi: 10.15906/j.cnki.cn11-2975/s.20211218 [29] 王丰园, 金海炎, 丁凌飞, 等. 纤维素酶及其活性提升研究进展[J]. 现代农村科技,2022(3):65−68. [WANG F Y, JIN H Y, DING L F, et al. Advances in cellulase and its activity enhancement[J]. Modern Rural Science and Technology,2022(3):65−68. doi: 10.3969/j.issn.1674-5329.2022.03.051 [30] 陈艳, 田康明, 李玉, 等. 以蔗糖为底物利用重组大肠杆菌合成甘露醇[J]. 微生物学通报,2014,41(11):2182−2189. [CHEN Y, TIAN K M, LI Y, et al. Mannitol biotransformation from sucrose with recombinant Escherichia coli[J]. Microbiology China,2014,41(11):2182−2189. doi: 10.13344/j.microbiol.china.140075 [31] 许尚华. 硝酸钠促地衣芽胞杆菌WX-02高产聚γ-谷氨酸的蛋白质组学研究[D]. 武汉: 华中农业大学, 2013. XU S H. Comparative proteomic study of effect of sodium nitrate on poly-gamma-glutamic acid biosynthesis by Bacillus licheniformis WX-02[D]. Wuhan: Huazhong Agricultural University, 2013.
[32] 李朝波, 翟秀超, 温琦, 等. 添加不同有机氮源对L-赖氨酸发酵的作用[J]. 粮食与食品工业,2021,28(3):44−47. [LI C B, ZHAI X C, WEN Q, et al. Effects of feeding different organic nitrogen sources on L-lysine fermentation[J]. Cereal & Food Industry,2021,28(3):44−47. doi: 10.3969/j.issn.1672-5026.2021.03.012 [33] 马璐, 杨驰, 肖冬来, 等. 碳氮源对广叶绣球菌液体发酵的影响[J]. 中国食用菌,2020,39(10):37−41, 45. [MA L, YANG C, XIAO D L, et al. Liquid fermentation of Sparassis latifolia on different carbon and nitrogen source combinations[J]. Edible Fungi of China,2020,39(10):37−41, 45. doi: 10.13629/j.cnki.53-1054.2020.10.007 [34] 汪伟, 蔡海波, 谭文松, 等. pH调控方式和温度对透明质酸发酵过程的影响[J]. 现代食品科技,2019,35(8):207−213. [WANG W, CAI H B, TAN W S, et al. Effects of pH control modes on hyaluronic acid fermentation process[J]. Modern Food Science and Technology,2019,35(8):207−213. doi: 10.13982/j.mfst.1673-9078.2019.8.030 [35] 朱伟, 冯培功, 马君军, 等. 温度对粪便发酵过程中耗氧气量和有害气体排放量的影响[J]. 黑龙江畜牧兽医,2018(20):43−45, 49. [ZHU W, FENG P G, MA J J, et al. The effect of environment temperature on the emission of harmful gases from faecal fermentation[J]. Heilongjiang Animal Science and Veterinary Medicine,2018(20):43−45, 49. doi: 10.13881/j.cnki.hljxmsy.2018.04.0383 [36] 程小飞, 宋锐, 洪波, 等. 虾壳粉氨基酸和脂肪酸营养成分分析[J]. 中国饲料,2020(23):66−70. [CHEN X F, SONG R, HONG B, et al. Analysis of nutritional components of amino acids and fatty acids in Procrustus clarkii crawfish shell meal[J]. China Feed,2020(23):66−70. doi: 10.15906/j.cnki.cn11-2975/s.20202315 [37] 王敏, 辛二娜, 王瑶, 等. 几丁质降解菌的分离鉴定与产酶条件探究[J]. 山西农业科学,2021,49(4):420−424. [WANG M, XIN E N, WANG Y, et al. Isolation and identification of chitin-degrading bacterium and exploration of the optimal culture conditions for enzyme production[J]. Journal of Shanxi Agricultural Sciences,2021,49(4):420−424. doi: 10.3969/j.issn.1002-2481.2021.04.05 -
期刊类型引用(2)
1. 谢啟发,薛小旭,黄志发,米浩宇,贺福祥,房耀维,刘姝. 海洋产几丁质酶厦门加西利亚单胞菌Chi34的筛选、鉴定及酶学性质分析. 食品工业科技. 2023(12): 116-123 .  本站查看
本站查看
2. 权淑静,杨文玲,雷高,王佰涛,刁文涛,梁博,刘德海. 产几丁质酶高原菌的分离鉴定及酶学性质初步研究. 中国酿造. 2023(11): 152-156 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:



 下载:
下载:



