A Review of the Molecular Interaction between Plant Polyphenols and Starch
-
摘要: 淀粉是食品工业的重要原料之一,同时也是人体主要的供能物质。植物多酚是一类广泛存在于植物中且对人体健康有益的活性物质。植物多酚与淀粉的分子相互作用会影响淀粉基食品在加工和贮藏过程中的品质(如质构、风味及色泽等)及营养特性。本文在查阅和整理国内外有关文献和研究的基础上,对植物多酚与淀粉的分子相互作用及其对淀粉和植物多酚相关性质的影响进行综述,包括植物多酚与淀粉的复合物形成方式(以疏水作用力为主的V型复合物和以氢键为主的非V型复合物),其相互作用对淀粉理化性质(糊化性质、回生性质和流变性质等)、微观结构和消化特性的改变及其对植物多酚的保护及缓释作用,以期为植物多酚在淀粉的加工、贮藏及其他相关领域的资源化利用提供有益的帮助与参考。Abstract: Starch is the important raw material for food industry, and it is also the main bioenergy source for human body. Plant polyphenols are a kind of active substances that widely exist in plants, and they are beneficial to human health. And the molecular interaction between plant polyphenols and starch can affect the quality (such as texture, flavor, color and so on) and nutrition of starch food during processing and storage. On the basis of consulting a lot of literature and studies, this paper reviews the molecular interaction between plant polyphenols and starch and its influence on the related properties of starch and plant polyphenols, these include the formation of complexes between plant polyphenols and starch (including V-type inclusion facilitated by hydrophobic effect and complex most through hydrogen bonds), the change of their interaction on the physicochemical properties (such as pasting, retrogradation, rheological properties, etc.), microstructure and digestive properties of starch, as well as the effect of protection and slow release on plant polyphenols, which would provide useful guidance for the resource utilization of plant polyphenols in starch processing and storage and other related fields.
-
淀粉是食品工业中一种重要的原料,其性质对面制品、米制品等食品的感官和营养等品质有十分重要的影响。淀粉是一种以α-D-吡喃葡萄糖为基本单位,通过糖苷键连接而成的生物大分子,根据其结构可分为直链淀粉和支链淀粉。其中,直链淀粉是由葡萄糖单元通过α-1,4糖苷键连接而成,基本上呈线型,分子量在1×104~1×105 Da之间。支链淀粉则是由许多小的直链淀粉分子通过α-1,6糖苷键连接形成分支,分子量在1×105~1×106 Da之间。食品中天然存在的淀粉呈颗粒状,并由有序的结晶区与无序的无定形区交替构成其微观结构[1-2]。实际生产中,淀粉因其来源广、成本低、营养高、易加工等优点而被广泛应用。但是,淀粉及其制品也存在一些明显的不足,如易老化回生、冻融稳定性差、保水性差等,这在一定程度上影响了淀粉制品的品质与货架期。同时,淀粉制品的的加工通常不只有淀粉一种组分存在,而是淀粉与食品中其他组分共同存在的混合体系[3-4]。近年来,食品中淀粉与其他组分的相互作用引起了食品科学工作者的关注。统计显示,2011~2021年SCI(Science Citation Index)收录的科学论文中约7万篇的研究主题是淀粉,占同期食品领域论文总数的5%,其中约20%是关于淀粉与其他物质相互作用的研究。研究发现,淀粉与食品中其他组分的相互作用既对淀粉类食品的感官、风味等品质有影响,也在一定程度上改变着淀粉的消化吸收特性[5]。
植物多酚是一类存在于植物体内具有多个酚羟基结构的化合物,是植物的次生代谢产物,广泛分布于植物的叶、皮、根和果实中。根据化学结构和特征,植物多酚可大致分为水解类多酚(聚没食子酸酯类多酚)、缩合类多酚(聚黄烷醇类多酚)和复杂类多酚(同时含有水解类和缩合类成份)。水解类多酚是多个没食子酸或与其有生源关系的酚羧酸与多元醇通过分子内酯键连接形成的酯类化合物,具有C6-C1的结构特征;缩合类多酚是多个黄烷醇单体以C-C键连接形成的聚合物,具有C6-C3-C6的结构特征[6-7]。植物多酚作为一种重要的生物活性成分,具有抗氧化、抗菌、抗肿瘤等多种有益人体健康的保健作用,在食品、生物、医药和化工领域得到了广泛的应用[8]。
近年来,植物多酚与淀粉之间的分子相互作用引起了人们的关注。一方面,植物多酚可作为生物活性成分用于功能性淀粉食品的开发;另一方面,淀粉食品的加工往往会涉及到植物性原料的细胞及组织的破坏,导致其细胞及组织中植物多酚的释放,而内源性植物多酚与淀粉之间的分子相互作用,对淀粉类食品的品质会产生影响。其实,植物多酚在我国传统淀粉食品的生产中有着悠久而广泛的使用历史。在长期的生产中,人们积累了大量有关植物多酚与淀粉相分子互作用的经验与成果,并在实践中不断发展。植物多酚与食品中其他组分的相互作用对食品的色泽、风味、质构等有积极影响,可提升食品的品质和延长食品的货架期[9-10]。随着科技的发展,植物多酚与淀粉之间分子相互作用的化学本质开始逐渐被人们揭示和认识,对相互作用的研究也开始从传统的食品加工领域向化学及生物等领域拓展,逐渐成为食品及相关领域的研究热点[11]。本文在查阅和整理大量有关文献和研究的基础上,对植物多酚与淀粉的分子相互作用及其对淀粉和植物多酚的影响进行介绍,以期为植物多酚在淀粉的加工与贮藏及其他相关领域的资源化利用提供有益的帮助与参考。
1. 植物多酚与淀粉复合物的形成方式
大量研究表明,植物多酚能与淀粉分子之间发生相互作用以形成复合物,从而影响淀粉的理化特性以及多酚的生物活性。植物多酚与淀粉形成复合物的机理及结合方式可大致分为两种。
1.1 V型复合物
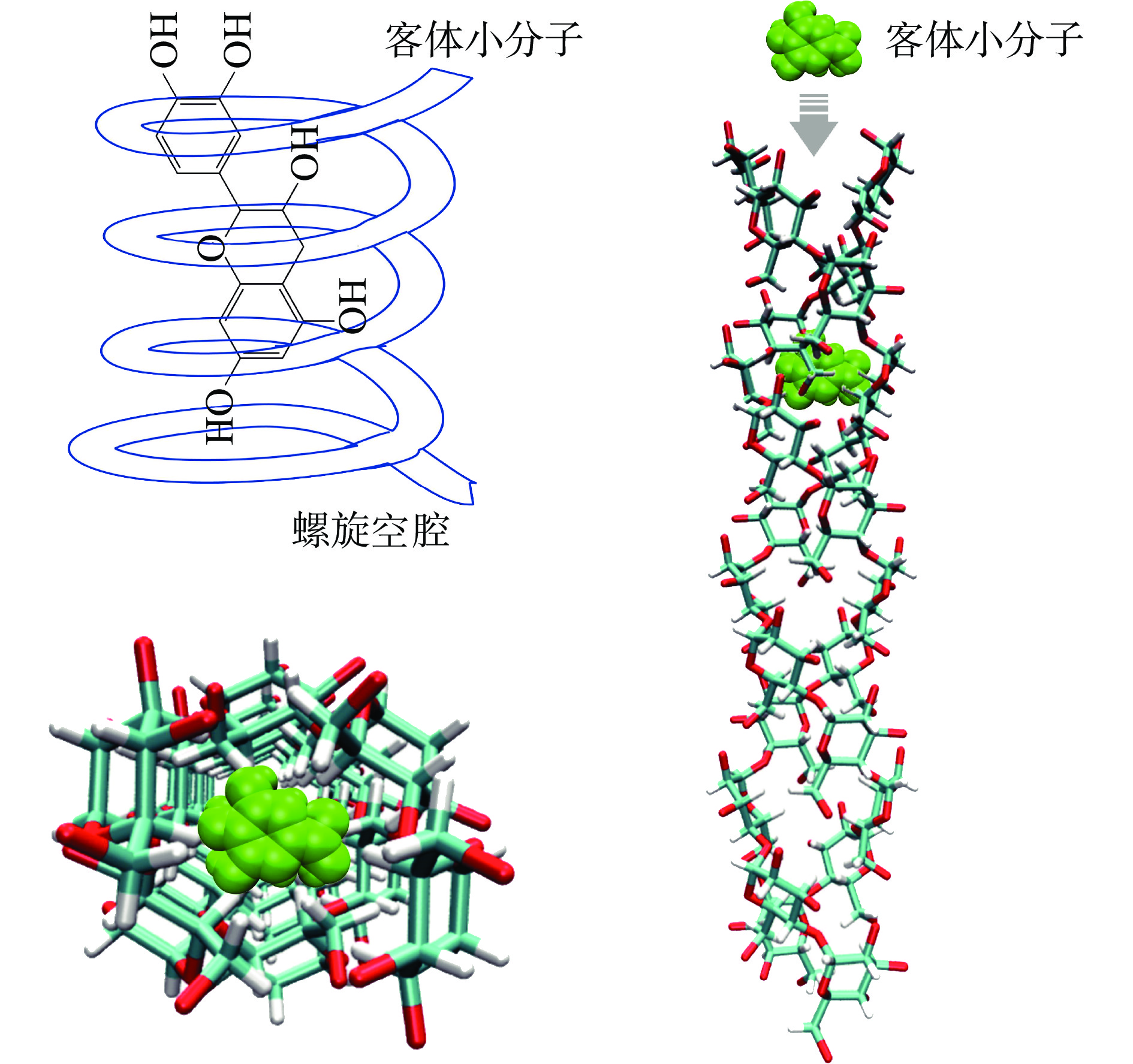
一些分子量较小的酚类物质进入淀粉链的螺旋空腔内形成V型复合物(如图1所示)。该类复合物的制备可通过热处理、溶剂处理及酶处理等方式完成。热处理和溶剂处理所制备的样品的多酚包埋率较高,但高温条件及较高的pH环境可能会导致酚类化合物的降解或氧化;酶处理可避免热处理和溶剂处理的弊端,但合成率较低。此外,V型复合物的形成原理是由于直链淀粉呈单一左手螺旋结构,疏水基团位于螺旋内侧,故螺旋空腔内的疏水相互作用可作为主要驱动力,牵引分子量较小、含疏水基团的酚类物质进入空腔内,从而形成带有两亲性或疏水性配体的V型直链淀粉-多酚复合物[12-13]。有研究表明,通过热处理方式,4-O-棕榈酰绿原酸成功进入直链淀粉的疏水空腔内形成V型复合物[14];结合热处理及溶剂处理的方式,使用氢氧化钠溶液制备了金雀异黄素和高直链玉米淀粉的V型复合物[5]。目前,V型复合物的判定可借助广角X射线衍射仪、拉曼散射技术、傅里叶变换红外光谱、固态核磁共振光谱等手段[15]。由于V型复合物的形成受限于直链淀粉螺旋空腔的尺寸以及酚类物质的大小及疏水性能,故绝大部分多酚类物质和淀粉的结合方式为第二种。
1.2 非V型复合物
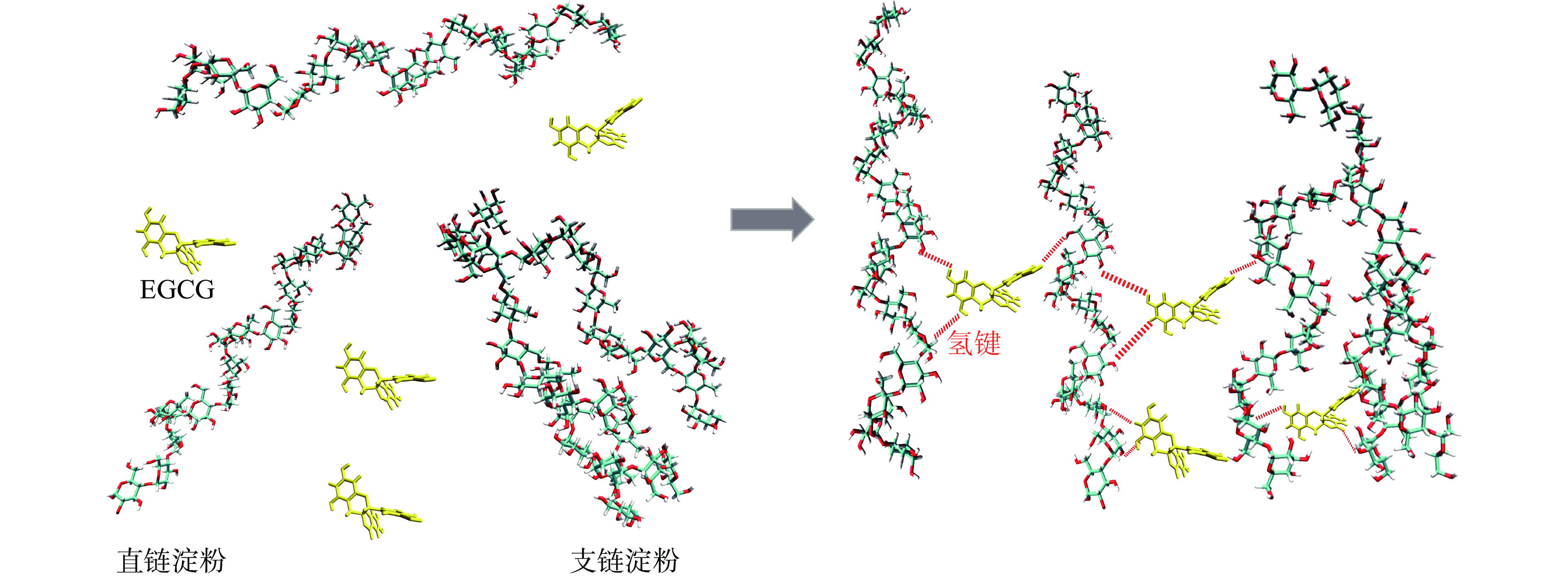
多酚的羰基结构和酚羟基结构能够与淀粉分子的羟基产生相互作用,并以非共价键(氢键和范德华力)诱导淀粉分子聚集(如图2所示)。此类非包容性的复合物通常以氢键结合,形成的主要原因是由于尺寸较大的酚类物质无法进入淀粉的螺旋空腔内[16]。有研究表明,芦丁、阿魏酸等酚类物质不能与高直链玉米淀粉形成V型复合物[5]。目前,通过分光光度法、动态激光散射分析和核磁共振氢谱分析等多种方法可以从分子水平上揭示形成非包容性复合物的相互作用机理[17-18]。
由此可见,植物多酚的分子尺寸、空间位阻、酚羟基数目等均会影响其与淀粉的结合方式和相互作用能力。分子尺寸较小的酚类物质能够通过与淀粉侧链羟基基团形成氢键,并在氢键和疏水相互作用的“牵引”下进入淀粉螺旋链的空腔中形成V型复合物[5],在这一相互作用过程中,淀粉的疏水空腔和植物多酚的苯环之间的疏水相互作用在两者的结合过程中占据了更为主要的地位[5,9]。同时,V型复合物的形成改变了淀粉分子的空间构型,从而影响了淀粉的糊化特性、回生特性及流变特性等。此外,空间位阻较大的植物多酚受到淀粉疏水空腔尺寸的限制,无法通过疏水作用进入淀粉螺旋空腔,因此氢键的形成在维系此类植物多酚与淀粉的稳定结合过程中发挥了重要作用[9]。同时,两者间氢键的形成数目及强度受到植物多酚的酚羟基数量的影响[7],植物多酚的酚羟基数目越多,其与淀粉形成的氢键数目更大,两者间的的结合强度越大,而具有较大空间位阻和较多酚羟基数目的植物多酚更能够以自身为核心聚集周围游离的淀粉链,从而干预淀粉分子间的缠绕和重结晶,进而改变淀粉的理化特性和消化特性[7,18]。
2. 植物多酚与淀粉的分子相互作用对淀粉理化性质的影响
2.1 对淀粉糊化性质的影响
淀粉的糊化是淀粉颗粒结构发生瓦解,由有序状态转变为无序状态,分子分散于水中形成具有一定黏性的糊状溶液的一类热力学过程[19]。多酚类物质因其多酚羟基结构的存在,能与淀粉侧链发生氢键相互作用,促进淀粉颗粒的水合,从而影响淀粉的糊化性质。大量研究表明,淀粉-多酚复合物的形成可以影响淀粉的糊化特性,这与酚类物质对结晶胶束结构内耦合力的削减有关,使得糊化所需温度及热能降低[20]。此外,酚类物质对淀粉糊化特性的影响与酚类物质的来源、多酚添加量以及淀粉的来源等密切相关。
2.1.1 不同来源多酚对淀粉糊化性质的影响
多酚是广泛存在于植物体中的次生代谢产物,分布于植物的叶、皮、根、果实和果壳中,由于不同植物自身代谢及生长环境具有差异,使得不同植物来源的多酚具有不同的结构特征,按照其构成单元骨架,可大致分为缩合类多酚(C6-C3-C6结构)、水解类多酚(C6-C1结构)和复杂类多酚(含有以上两种结构)。同时,缩合类多酚按照分子量大小,又可细分为黄烷醇单体(主要为黄烷-3-醇和黄烷-3,4-二醇)及其聚合物,而水解类多酚按照水解种类的不同,又可细分为棓单宁和鞣花单宁;按照其植物来源,可初步分为茶多酚、葡萄多酚、苹果多酚和石榴多酚等[7]。植物来源的差异使得其对淀粉的糊化特性会产生不同程度的影响。从绿茶、山楂、石榴皮、五倍子这四种植物中提取的植物多酚都能够降低小麦淀粉的终值黏度。其中,五倍子来源的植物多酚的作用最为显[21]。借助快速黏度计对淀粉糊化过程黏度的变化进行分析,红茶多酚和绿茶多酚都能不同程度上降低玉米、小麦、马铃薯和大米这四种植物来源的淀粉的热浆黏度和终值黏度,但红茶多酚表现出更为显著的效果。这可能是由于红茶是发酵茶,发酵过程使得其中的酚类物质发生了氧化聚合反应,从而增大了红茶多酚的分子量及分子结构的复杂性[22]。借助差示扫描量热仪对淀粉糊化过程凝胶化温度的变化进行分析,发现五倍子、石榴皮及山楂中提取的酚类物质都可以影响小麦淀粉的糊化。但是同等条件下,五倍子提取物降低了小麦淀粉的糊化初始温度、峰值温度和终值温度,略微增大其糊化焓,而石榴皮和山楂提取物显著增大了小麦淀粉的糊化初始温度、峰值温度和终值温度,略微降低其糊化焓,这可能是由于不同来源的植物多酚中酚羟基的数量及分布位置、分子量以及体系pH具有一定差异[21-23]。通常来说,植物多酚的酚羟基数目及分子量越大,其以自身为核心,通过氢键聚集周围淀粉分子的能力就越强,且较强的氢键作用能够改变淀粉颗粒结晶区和无定形区之间的耦合强度,从而改变淀粉的糊化温度和糊化焓值;而酚羟基在酚类物质上的分布位置,会影响酚类物质的电子云分布,改变其表面静电势,从而影响其反应活性及其与淀粉的亲和力;此外,植物多酚可以与水分子相互作用,改变水溶液的pH和离子强度,从而改变淀粉颗粒“周围的环境”,而pH降低程度的差异可能使得酸性分子对淀粉颗粒的无定形区域造成不同程度的改变,从而影响淀粉的糊化过程[21-23]。
2.1.2 多酚添加量对淀粉糊化性质的影响
多酚的添加量对淀粉糊化特性具有显著的影响,较低浓度植物多酚的添加对体系pH的影响较小,主要以多酚与淀粉间的氢键、范德华力及疏水相互作用等分子间作用力为主。当然,低剂量酚类物质所能提供的有效酚羟基数目较少,可能对淀粉颗粒半结晶结构的影响较弱;而较高剂量的植物多酚不仅会较大程度改变淀粉所处“环境”的pH,还能通过较强的氢键作用影响淀粉颗粒的缔合强度,并阻碍游离淀粉链之间的碰撞及缠绕[5,7,9]。利用快速黏度仪发现茶多酚能够影响大米淀粉的糊化过程,且随着茶多酚添加量的增大,大米淀粉糊的终值黏度逐渐下降,这可能由于茶多酚浓度的增大阻碍了淀粉链间的有序排列[24]。此外,借助差示扫描量热仪发现大米淀粉的糊化温度和糊化焓均随茶多酚添加量的增加而呈现下降趋势[25]。阿魏酸能够改变玉米淀粉的糊化性质,显著降低玉米淀粉的糊化起始温度和糊化终值温度,但却对糊化峰值温度没有显著影响;不同剂量(5%、10%和15%,w/w,基于淀粉质量)的阿魏酸使得玉米淀粉的糊化焓值略有下降,而当阿魏酸的添加量提高至20%(w/w,基于淀粉质量)时,玉米淀粉的糊化焓值显著降低[26]。
2.1.3 同种多酚对不同植物来源淀粉糊化性质的影响
淀粉按照植物来源可分为谷类淀粉(如小麦淀粉)、薯类淀粉(如马铃薯淀粉)、豆类淀粉(如豌豆淀粉)和其他淀粉(如百合淀粉)等四类,而不同植物来源的淀粉在晶型、形状以及粒径等方面有一定的差异,如:玉米淀粉等谷类淀粉的晶型为A型,马铃薯淀粉等块茎类淀粉为B型,而豆类淀粉为C型(A型和B型的混合结晶);不同植物来源的淀粉颗粒形状各异,有圆球形、椭圆形、多角形和不规则形等,而其粒径更是不尽相同,但天然淀粉的尺寸均是微米级[1-3]。同种多酚对不同植物来源的淀粉的糊化性质具有不同程度的影响。研究表明,红茶多酚能够提高玉米淀粉和大米淀粉的糊化温度,降低其糊化焓值,但是却对马铃薯淀粉的糊化温度和糊化焓值没有显著影响。这可能是由于玉米淀粉和大米淀粉中的磷酸单酯含量高于马铃薯淀粉,且玉米淀粉和大米淀粉的粒径更小,从而导致红茶多酚对这三种植物来源的淀粉的糊化特性产生了不同程度的影响[27]。苦荞来源的多酚提取物能够显著影响苦荞淀粉、小麦淀粉的糊化初始温度和峰值温度,但却对两种淀粉的终值温度影响并不显著。此外,随着苦荞多酚浓度的增大(1%~4%),苦荞淀粉的糊化焓值呈先增大后减小的趋势,而小麦淀粉的糊化焓值逐渐减小[28],这可能是由于苦荞淀粉和小麦淀粉在粒径及直/支链淀粉比例上的差异所致,苦荞淀粉的粒径相比于小麦淀粉的更小,且苦荞淀粉中直链淀粉的占比小于小麦淀粉的,这使得两种淀粉的结晶度、颗粒结构等都有所不同,从而导致了它们与苦荞源多酚在结合亲和力或相互作用能力上的差异。绿茶多酚的添加能够显著减低大米淀粉、玉米淀粉和马铃薯淀粉这三种不同植物来源淀粉的糊化初始温度、峰值温度、终值温度以及糊化焓值[29],三种淀粉原始的糊化焓的大小顺序为:马铃薯淀粉>玉米淀粉>大米淀粉,而直链淀粉含量的顺序为:马铃薯淀粉<玉米淀粉<大米淀粉,这表明三种淀粉中直链淀粉占比越低,其糊化所需的热能越高。由此可见,不同植物来源的淀粉受晶型、结晶度、形状、粒径及直/支链淀粉比例等多方面因素的影响,其与同种植物多酚的相互作用能力不尽相同,从而导致其糊化特性受到不同程度的影响。
2.2 对淀粉回生性质的影响
淀粉的回生是已糊化淀粉分子在低温下重新排列并形成结晶体的过程,该过程不可逆[5]。淀粉的回生是淀粉分子链间疏水相互作用和强氢键作用所导致的。大量研究表明,植物多酚与淀粉间的相互作用能够一定程度上抑制淀粉的回生,这是由于酚类化合物的高活性酚羟基基团能与淀粉的羟基形成氢键,从而阻碍直链淀粉分子间的缠绕,抑制淀粉聚合物链的排列[30]。淀粉和多酚之间的氢键相互作用越强,对淀粉回生过程的抑制能力越高。因此,酚类物质的来源、多酚添加量以及淀粉的来源等因素可能会影响酚类物质对淀粉回生性质的作用。
2.2.1 不同来源多酚对淀粉回生性质的影响
不同来源的植物多酚具有不同的分子结构和反应活性,对淀粉的回生性质会产生不同程度的影响。来源于绿茶、山楂、石榴皮、五倍子四种植物的多酚类提取物与小麦淀粉进行共同糊化及48 h的常温储存后,质构分析结果表明四种酚类提取物在不同程度上降低了淀粉凝胶的硬度,凝胶硬度越低表明淀粉的回生程度越小。其中,五倍子多酚提取物对淀粉凝胶硬度增长的抑制效果最为显著,而石榴皮多酚提取物所表现出的能力最差[21],这可能是由于五倍子多酚提取物含有高浓度的五倍子单宁,而石榴皮多酚提取物以鞣花单宁为主,五倍子单宁是以D-葡萄糖为基本骨架的棓单宁,具有较多的棓酰基结构,而鞣花单宁是多元醇与六羟基联苯二酸或与六羟基联苯二酸有生源关系的酚羧酸结合形成的酯类化合物,这两类物质具有不同的分子结构和分子量[7],与淀粉分子的相互结合能力也不尽相同。同时福林酚试剂测定结果表明,五倍子多酚提取物的总酚含量远高于石榴皮多酚提取物的,这也使得五倍子多酚提取物对淀粉凝胶硬化速度及回生程度的抑制能力更强。利用差示扫描量热仪和X射线衍射仪分析绿茶多酚和红茶多酚对马铃薯淀粉回生能力的影响,结果显示绿茶多酚对马铃薯淀粉的回生过程表现出了较好的抑制效果(回生焓值和结晶程度的降低),而红茶多酚的作用效果并不显著[22],这可能是由于这两种茶多酚来源于不同发酵程度的茶叶。绿茶为非发酵茶,绿茶提取物以儿茶素类物质为主(如:表儿茶素,Epicatechin,EC;表没食子儿茶素,Epigallocatechin,EGC;表儿茶素没食子酸酯,Epicatechin gallate,ECG和表没食子儿茶素没食子酸酯,Epigallocatechin gallate,EGCG);红茶为全发酵茶,发酵程度越高,儿茶素类物质发生氧化聚合形成茶黄素和茶红素,导致其活性酚羟基数目降低,而酚羟基数目对多酚与淀粉之间氢键作用的强度具有重要影响。
2.2.2 多酚添加量对淀粉回生性质的影响
多酚添加量的变化使得体系内活性基团数量及pH发生改变,对淀粉的回生性质会产生不同程度的影响。有研究表明,茶多酚能够抑制大米淀粉的老化,在相同条件下,茶多酚的添加量由5%(w/w,基于淀粉质量)增大至20%(同上)时,茶多酚的添加会显著降低大米淀粉储存周期内的回生焓值和回生率,表明茶多酚能抑制大米淀粉的老化,且茶多酚的添加量越大,回生抑制效果越明显[31]。将不同含量(1%,2%,3%,6%,9%和12%,w/w,基于淀粉质量)的芦丁添加到淀粉中进行共糊化和回生处理,发现芦丁添加量较高的样品其回生程度更低,这可能是因为高添加量组内淀粉和多酚间的相互作用更为强烈,多酚通过强氢键作用显著阻碍了淀粉分子链的交联和缠绕[25, 32]。
2.2.3 同种多酚对不同植物来源淀粉回生性质的影响
不同植物来源的淀粉具有不同长度的淀粉分子链以及不同大小的结晶度,故多酚对不同植物来源淀粉的老化过程所造成的影响会有所差异。研究发现,绿茶多酚能够显著降低糊化后大米淀粉、玉米淀粉和马铃薯淀粉的回生焓值和回生率,但绿茶多酚对大米淀粉和玉米淀粉回生过程的抑制效果优于马铃薯淀粉[29,33]。此外,有研究表明,在4 ℃的储藏条件下,红茶多酚提取物的添加能够显著抑制玉米淀粉和大米淀粉回生过程的发生,但对马铃薯淀粉的回生过程未产生显著影响,这可能是由于不同种类淀粉的颗粒粒径以及结晶致密度存在差异。三种淀粉颗粒粒径的大小顺序为:马铃薯淀粉>玉米淀粉>大米淀粉,且其支链链淀粉含量的顺序为:马铃薯淀粉>玉米淀粉>大米淀粉[27,34]。通常来说,淀粉颗粒粒径越大,其大分子量的支链淀粉的含量越高,而在淀粉回生过程中,支链淀粉的老化缔合速度远小于直链淀粉,这也使得不同来源的淀粉的回生特性有所不同。此外,不同来源的淀粉其结晶致密度有所差异,这表明淀粉颗粒内直链淀粉和支链淀粉的比例以及它们之间的作用强度有所不同。直链淀粉分子在高温下结构较为舒展,极性基团易外露,而支链淀粉分子呈树状分支形,具有较大的空间阻碍作用,这也使得同种植物多酚对直链淀粉和支链淀粉具有不同的结合亲和力,从而导致其对不同植物来源的淀粉的回生性质产生不同的作用效果[5,9,27,34]。
2.3 对淀粉流变性质的影响
淀粉糊的流变性包含流动特性和黏度特性。糊化过程中,淀粉颗粒内直链淀粉分子链因结构的灵活性能够不断运动,并能连接到由分子间双螺旋缠绕所生成的网络结构上,而植物多酚与淀粉间的相互作用能够影响淀粉分子的流动性,改变反应体系的黏度参数值,从而影响淀粉的流变性质[35]。研究表明,芦丁的添加增大了大米淀粉糊的屈服应力和相关系数,降低了大米淀粉的流动特性[25]。此外,植物多酚还能影响淀粉糊的黏度特性。有研究表明,茶多酚会阻碍淀粉分子链的结合缠绕,从而降低淀粉糊黏度[31]。同时,茶多酚的添加,显著降低了高直链玉米淀粉糊的储能模量和损耗模量,但对蜡质玉米淀粉糊的并未产生显著作用,这表明茶多酚对玉米淀粉糊流变性质的影响主要是酚类和直链淀粉间的相互作用[36]。由此可见,淀粉颗粒内直链淀粉和支链淀粉的比例会影响多酚对其流变性质的作用效果[31,35-36]。槲皮素和芦丁这两类多酚均能降低小麦淀粉糊的储能模量和损耗模量,削弱小麦淀粉的凝胶体系,但芦丁对小麦淀粉糊流变特性的影响强于槲皮素。相比于槲皮素的分子结构,芦丁在C环的3号位上多连接了一个葡萄糖苷和鼠李糖苷,而芦丁C环上糖苷配体的存在使得其极性大于槲皮素。同时,糖羟基的引入使得芦丁能与淀粉之间形成更多的氢键,从而导致芦丁对淀粉流变性质的影响强于槲皮素,这也表明酚类物质结构的差异会影响其与淀粉的相互作用能力[32,37]。
2.4 对淀粉其他理化性质的影响
植物多酚不仅可以影响淀粉的糊化性质、回生性质和流变性质,还能改变淀粉的颗粒大小、透明度和凝胶性质等。研究表明,茶多酚的添加增大了淀粉中直链淀粉的流体力学半径,这可能是由于茶多酚对直链淀粉的桥接作用增大了淀粉的分子量,降低了溶液内淀粉分子的多分散性[31,35,38]。苦荞多酚的添加显著降低了小麦淀粉糊和苦荞淀粉糊的透明度,这可能是由于苦荞多酚的存在,促使糊化后分散于溶液中的淀粉分子链之间发生缔合,淀粉分子的不断聚合阻碍了光线的透过,从而降低了淀粉的透明度[28,32]。茶多酚的添加改变了淀粉的凝胶性质,这可能是茶多酚的酚羟基基团阻碍了淀粉链之间的结合,影响了凝胶网络结构的生成,从而削弱了淀粉的凝胶强度,且与茶多酚的添加量呈明显的剂量效应关系[39]。
3. 植物多酚与淀粉的分子相互作用对淀粉微观结构的影响
小麦淀粉颗粒的外观在自然状态下近似为椭球形或扁球形,但其形态可能会随着糊化和短期回生过程的发生而改变,这分别涉及淀粉颗粒在高温下的破裂以及糊化后淀粉分子在冷却过程中的重结晶[40]。一定浓度的淀粉颗粒充分水合并发生糊化作用时,颗粒吸水,体积膨胀并破裂,直链淀粉所构成的无定形区和支链淀粉构成的结晶区被破坏,直链淀粉溶解于水溶液中,支链淀粉结合水分发生膨胀,并使得溶液黏度发生显著变化[5]。随着温度的降低,淀粉分子游动速度下降,淀粉分子彼此碰撞并缠绕,形成三维立体网状结构,并将周围水分子束缚于其中形成具有一定黏性和弹性的淀粉水凝胶[41]。可见,淀粉凝胶的内在结构为立体纤维网状凝胶结构,中间分布了许多有规则的空隙,它们填充于淀粉类食品中,正是由于淀粉的这种三维网状结构的存在,使得它能够吸附和承载食品中的风味成分和功能性物质,而淀粉凝胶结构的变化会影响食品的口感、质构及营养价值[42-43]。在植物多酚与淀粉的相互作用中,酚类物质在分子尺寸、羟基数目及空间构型方面的差异使得酚类物质的性质具有较大差异,从而使得两者间的分子相互作用强度有明显差异,进而对淀粉及其凝胶的微观结构产生不同的影响[44]。
相关研究表明,没食子酸、绿原酸、表没食子儿茶素没食子酸酯(EGCG)及单宁酸等酚类物质对淀粉微观结构的影响有明显的差异[45]。没食子酸分子尺寸较小,可经由氢键及疏水相互作用的牵引,从淀粉螺旋链两端进入淀粉疏水空腔内,空腔内的没食子酸分子像“瓶塞”一样占据空腔入口,故其余的没食子酸分子无法进入空腔内部,仅与淀粉分子侧链结合。此外,没食子酸分子上的连苯三酚羟基与羧基的分布可能导致它与淀粉的结合程度并不高,具有平面构型的没食子酸分子并不能稳定地连接于淀粉链上,故在淀粉重结晶过程中,部分没食子酸仅堆积在淀粉表层。绿原酸的分子构型呈单链状,空间位阻较小,且活性基团分布于分子链两端,绿原酸分子首先通过分子链一端的活性基团结合于淀粉侧链上,再借由另一端的活性基团聚集周围游离的淀粉分子,这样的结合方式可能使得分子的堆积和层叠较为均匀,从而使得其形貌较为光滑。EGCG的分子尺寸较为适中,且酚羟基数目较多,这使得它与淀粉分子侧链的结合更为紧密。此外,EGCG分子A环、B环及D环上的酚羟基能够同时与周围的淀粉链相结合,形成以多酚为“桥梁”的柱状连接。单宁酸的分子尺寸较大,具有大量的酚羟基,在与淀粉的相互作用过程中,它的多酚羟基结构能够聚集游离的淀粉分子链。同时,它以葡萄糖为中心的五条分子链上的酚羟基能够结合不同位置的淀粉链,使得周围的淀粉链较大程度地发生聚集,形成更为明显的不均匀涂层结构[46-47]。此外,相关研究还指出,茶多酚可占据淀粉分子间的结合位点,影响淀粉分子间的排列和缠绕,从而影响淀粉凝胶层间的交联程度,使得淀粉凝胶微观结构的孔隙增大[48]。茶多酚还能够与淀粉链发生明显的分子相互作用,逐渐结合周围的游离淀粉分子,使得自身被包埋于淀粉分子内,从而增大淀粉凝胶表层的粗糙度[49]。
4. 植物多酚与淀粉的分子相互作用对多酚的保护及缓释作用
植物多酚具有多种对人体健康有益的生物活性功能,然而植物多酚必须先经过人体消化道,再经循环运输以到达靶组织才能更好地发挥其生物活性[6]。该摄食及吸收过程经历了不同pH消化液及多种消化酶的接触,酚类物质的分子结构及生物活性可能会发生变化[50]。包埋可以保护植物多酚,有利于延长活性物质的释放,并提高其稳定性和生物活性。研究表明,来源广泛、无毒无害以及价格低廉的淀粉经糊化后,淀粉分子间交联所产生的物理空隙能够包裹和负载多种酚类物质。同时,淀粉分子还能通过氢键及疏水相互作用等方式与酚类物质(如茶多酚、花青素、白藜芦醇及单宁酸等)结合形成V型或非V型复合物,而随着淀粉添加量的增加(或糖羟基的增加)以及植物多酚酚羟基数目的增大,淀粉与酚类物质之间能形成更连续的氢键网络结构,从而强化淀粉-多酚复合物的稳定性[5,9,12,16],复合物的形成可保护多酚免受消化液及消化酶的损害,并在一定程度上调控多酚在人体消化道的释放,从而提高多酚的生物可及性和生物利用度[51-52]。复合物的形成还可以提高溶解度较低的酚类物质(如槲皮素、姜黄素等)的水溶性,并有效地将多酚释放至特定部位,从而控制多酚的给药剂量[53]。此外,通过物理、化学及生物方法改性的淀粉对酚类物质具有更高效的负载能力,如经非晶态辛烯基琥珀酸酐改性的蜡质玉米淀粉能够更好地包裹茶多酚,并在体内消化过程中将儿茶素逐渐从复合物中释放出来[54];经乙酰化的淀粉纳米颗粒可以增强姜黄素的稳定性和更高的封装效率[55];经4-α-葡萄糖基转移酶修饰的大米淀粉能够极大地改善姜黄素的溶解度,从而提高其在人体的可利用率[56]。可见,利用植物多酚与淀粉之间的相互作用来控制酚类活性物质在人体的释放是一种具有研究前景及意义的方法与途径。
5. 植物多酚与淀粉的分子相互作用对淀粉消化特性的影响
淀粉的消化涉及到淀粉酶和葡萄糖苷酶等消化酶的酶水解作用。因此,植物多酚对淀粉消化特性的影响涉及“淀粉-消化酶-植物多酚”三类物质。根据淀粉在人体消化道的消化吸收速度,可将淀粉分为三个类别:快消化淀粉、慢消化淀粉和抗性淀粉。其中,快消化淀粉是指在人体小肠内能够被快速消化和吸收的部分(20 min内释放葡萄糖),其摄入会导致餐后血糖的急剧增长;慢消化淀粉指能在人体小肠内被彻底消化但消化速度较慢的部分(20~120 min内释放葡萄糖);抗性淀粉指不能被人体小肠消化的部分[9]。研究表明,没食子酸与淀粉之间通过氢键、疏水相互作用及静电作用等形成非V型复合物,使得淀粉的酶解速度降低[57];咖啡酸-淀粉非V型复合物的形成降低了淀粉的消化特性,且与咖啡酸的浓度呈正相关[58]。可见,植物多酚通过非共价键作用力与淀粉分子发生相互作用,形成非V型复合物,能够增强淀粉对消化酶的抗性。这可能是因为植物多酚的加入改变了淀粉的物理化学特性,降低了淀粉的水动力学半径,且以氢键的方式“桥连”并进一步聚集游离淀粉分子,阻碍了淀粉消化酶的进入及其与淀粉分子的接触[9,31,57-58];还有一方面原因是植物多酚能够改变淀粉消化酶的空间构型,从而降低消化酶的活性[59]。此外,有研究表明,绿茶多酚-淀粉的V型复合物的形成增加了抗性淀粉的含量,降低了体外酶水解试验中葡萄糖的生成量[17];以茶多酚-蜡质玉米淀粉复合物喂食小鼠,发现茶多酚的加入降低了小鼠的餐后血糖值[60],这可能是因为该类多酚以疏水相互作用等方式占据了淀粉链的螺旋空腔,从而改变了淀粉的空间构型,并以氢键的方式占据了淀粉和酶的结合位点,进而导致了淀粉消化特性的降低[19,17,60]。总的来说,植物多酚与淀粉的相互作用对淀粉消化特性的影响可分为两方面:一是植物多酚通过氢键、疏水相互作用等非共价键作用力与淀粉形成非V型或V型复合物,从而改变了淀粉的空间构象,阻碍了淀粉消化酶和淀粉的充分接触;二是体系内游离的植物多酚与淀粉消化酶结合,从而抑制了酶的活性。植物多酚这两个方面的作用在“淀粉-消化酶-植物多酚”的三元体系中同时发生,密不可分。
6. 结语与展望
植物多酚与淀粉的分子相互作用受到植物多酚的分子尺寸及空间构型等化学特征及淀粉的来源和种类等因素的影响,呈现出明显的差异,从而对淀粉的老化、回生、流变性质、颗粒大小、透明度、凝胶性质和微观结构等理化特性、加工特性以及消化特性产生不同的影响,进而对淀粉基食品在加工和贮藏过程中的品质及营养特性产生影响。同时,两者的分子相互作用对植物多酚的生物活性及生物利用度也有积极的影响。可见,利用植物多酚与淀粉的分子相互作用调控淀粉基食品及植物多酚的加工特性、功能特性和消化特性,对改善淀粉基食品的品质,开发健康的功能型淀粉制品和提升植物多酚在食品工业的资源化利用价值有积极的作用。
随着食品科学及相关学科领域研究理论与技术的发展,对植物多酚与淀粉的分子相互作用还需要进一步开展下述的研究工作:采用计算化学与多光谱分析技术相结合,进一步分析植物多酚的结构参数(酚羟基位置与数目、分子量、酯化程度)对两者间分子相互作用的影响与规律,明确其构效关系;通过分子动力学模拟的方法,研究植物多酚与淀粉的分子相互作用的动态变化过程,并对其分子相互作用模式、分子作用力、作用位点及分子反应自由能等分子反应参数进行分析;基于生理学、营养学、分析化学和代谢组学技术的耦合,探究植物多酚对淀粉消化和营养特性的影响及规律,并进一步分析淀粉对植物多酚在生物体内代谢的影响。
-
[1] 杨景峰, 罗志刚, 罗发兴. 淀粉晶体结构研究进展[J]. 食品工业科技,2007,28(7):240−243. [YANG J F, LUO Z G, LUO F X. The review: starch crystal structure[J]. Science and Technology of Food Industry,2007,28(7):240−243. [2] TESTER R F, KARKALAS J, QI X. Starch composition, fine structure and architecture[J]. Journal of Cereal Science,2004,39(2):151−165. doi: 10.1016/j.jcs.2003.12.001
[3] FU Z, CHEN J, LUO S J, et al. Effect of food additives on starch retrogradation: A review[J]. Starch-Starke,2015,67(1):69−78.
[4] KHLESTKIN V K, PELTEK S E, KOLCHANOV N A. Review of direct chemical and biochemical transformations of starch[J]. Carbohydrate Polymers,2018,181(1):460−476.
[5] ZHU F. Interactions between starch and phenolic compound[J]. Trends in Food Science and Technology,2015,43(2):129−143. doi: 10.1016/j.jpgs.2015.02.003
[6] CROZIER A, JAGANATH I B, CLIFFORD M N. Dietary phenolics: chemistry, bioavailability and effects on health[J]. Natural Product Reports,2009,26(8):1001−1043. doi: 10.1039/b802662a
[7] 石碧, 曾维才, 狄莹. 植物单宁化学及应用[M]. 北京: 科学出版社, 2020 SHI B, ZENG W C, DI Y. Plant tannin chemistry and applications[M]. Beijing: Science Press, 2020.
[8] DEL R D, RODRIGUEZ M A, SPENCER J P E, et al. Dietary (poly) phenolics in human health: structures, bioavailability, and evidence of protective effects against chronic diseases[J]. Antioxidants and Redox Signaling,2013,18(14):1818−1892. doi: 10.1089/ars.2012.4581
[9] DENG N, DENG Z, TANG C, et al. Formation, structure and properties of the starch-polyphenol inclusion complex: A review[J]. Trends in Food Science and Technology,2021,112:667−675. doi: 10.1016/j.jpgs.2021.04.032
[10] ARAÚJO F F, FARIAS D P, NERI-NUMA I A, et al. Polyphenols and their applications: An approach in food chemistry and innovation potential[J]. Food Chemistry,2021,338(15):127535.
[11] AMOAKO D B, AWIKA J M. Polyphenol interaction with food carbohydrates and consequences on availability of dietary glucose[J]. Current Opinion in Food Science,2016,8:14−18.
[12] AMOAKO D B, AWIKA J M. Resistant starch formation through intrahelical V-complexes between polymeric proanthocyanidins and amylose[J]. Food Chemistry,2019,285:326−333. doi: 10.1016/j.foodchem.2019.01.173
[13] WANG S, KONG L, ZHAO Y, et al. Lipophilization and molecular encapsulation of p-coumaric acid by amylose inclusion complex[J]. Food Hydrocolloids,2019,93:270−275. doi: 10.1016/j.foodhyd.2019.02.044
[14] LORENTZ C, PENCREAC'H G, SOULTANI-VIGNERON S, et al. Coupling lipophilization and amylose complexation to encapsulate chlorogenic acid[J]. Carbohydrate Polymers,2012,90(1):152−158. doi: 10.1016/j.carbpol.2012.05.008
[15] SUN B, TIAN Y, CHEN L, et al. Linear dextrin as curcumin delivery system: Effect of degree of polymerization on the functional stability of curcumin[J]. Food Hydrocolloids,2018,77:911−920. doi: 10.1016/j.foodhyd.2017.11.038
[16] LIU Y, CHEN L, XU H, et al. Understanding the digestibility of rice starch-gallic acid complexes formed by high pressure homogenization[J]. International Journal of Biological Macromolecules,2019,134:856−863. doi: 10.1016/j.ijbiomac.2019.05.083
[17] ZHAO B, SUN S, LIN H, et al. Physicochemical properties and digestion of the lotus seed starch-green tea polyphenol complex under ultrasound-microwave synergistic interaction[J]. Ultrasonics Sonochemistry,2019,52:50−61. doi: 10.1016/j.ultsonch.2018.11.001
[18] WANG C, CHEN X, LIU S. Encapsulation of tangeretin into debranched-starch inclusion complexes: Structure, properties and stability[J]. Food Hydrocolloids,2020,100:105409. doi: 10.1016/j.foodhyd.2019.105409
[19] DONMEZ D, PINHO L, PATEL B, et al. Characterization of starch-water interactions and their effects on two key functional properties: Starch gelatinization and retrogradation[J]. Current Opinion in Food Science,2021,39:103−109. doi: 10.1016/j.cofs.2020.12.018
[20] LIU B, ZHONG F, YOKOYAMA W, et al. Interactions in starch co-gelatinized with phenolic compound systems: Effect of complexity of phenolic compounds and amylose content of starch[J]. Carbohydrate Polymers,2020,247:116667. doi: 10.1016/j.carbpol.2020.116667
[21] ZHU F, CAI Y Z, SUN M, et al. Effect of phytochemical extracts on the pasting, thermal, and gelling properties of wheat starch[J]. Food Chemistry,2009,112(4):919−923. doi: 10.1016/j.foodchem.2008.06.079
[22] GUZAR I, RAGAEE S, SEETHARAMAN K. Mechanism of hydrolysis of native and cooked starches from different botanical sources in the presence of tea extracts[J]. Journal of Food Science,2012,77(11):1192−1196. doi: 10.1111/j.1750-3841.2012.02929.x
[23] ALEIXANDRE A, ROSELL C M, et al. Starch gels enriched with phenolics: Effects on paste properties, structure and digestibility[J]. LWT-Food Science and Technology,2022,161:113350. doi: 10.1016/j.lwt.2022.113350
[24] WU Y, CHEN Z, LI X, et al. Effect of tea polyphenols on the retrogradation of rice starch[J]. Food Research International,2009,42(2):221−225. doi: 10.1016/j.foodres.2008.11.001
[25] ZHU F, WANG Y J. Rheological and thermal properties of rice starch and rutin mixtures[J]. Food Research International,2012,49(2):757−762. doi: 10.1016/j.foodres.2012.09.031
[26] KARUNARATNE R, ZHU F. Physicochemical interactions of maize starch with ferulic acid[J]. Food Chemistry,2016,199:372−379. doi: 10.1016/j.foodchem.2015.12.033
[27] XIAO H X, LIN Q L, LIU G Q, et al. Evaluation of black tea polyphenol extract against the retrogradation of starches from various plant sources[J]. Molecules,2012,17(7):8147−8158. doi: 10.3390/molecules17078147
[28] WU X J, FU G M, LI R Y, et al. Effect of thermal processing for rutin preservation on the properties of phenolics & starch in Tartary buckwheat achenes[J]. International Journal of Biological Macromolecules,2020,164:1275−1283. doi: 10.1016/j.ijbiomac.2020.07.135
[29] XIAO H, LIN Q, LIU G, et al. Inhibitory effects of green tea polyphenols on the retrogradation of starches from different botanical sources[J]. Food and Bioprocess Technology,2013,6(8):2177−2181. doi: 10.1007/s11947-011-0739-8
[30] WANG S, LI C, COPELAND L, et al. Starch retrogradation: A comprehensive review[J]. Comprehensive Reviews in Food Science and Food Safety,2015,14(5):568−585. doi: 10.1111/1541-4337.12143
[31] CHEN N, CHEN L, GAO H X, et al. Mechanism of bridging and interfering effects of tea polyphenols on starch molecules[J]. Journal of Food Processing and Preservation,2020,44:e14576.
[32] WANG L B, WANG L J, LI Z G, et al. Diverse effects of rutin and quercetin on the pasting, rheological and structural properties of tartary buckwheat starch[J]. Food Chemistry,2021,335:127556. doi: 10.1016/j.foodchem.2020.127556
[33] LI H, ZHAI F Y, LI J F, et al. Physicochemical properties and structure of modified potato starch granules and their complex with tea polyphenols[J]. International Journal of Biological Macromolecules,2021,166:521−528. doi: 10.1016/j.ijbiomac.2020.10.209
[34] HE W, WEI C X. Progress in C-type starches from different plant sources[J]. Food Hydrocolloids,2017,73:162−175. doi: 10.1016/j.foodhyd.2017.07.003
[35] WU Y, LIN Q L, CHEN Z X, et al. The interaction between tea polyphenols and rice starch during gelatinization[J]. Food Science and Technology International,2011,17(6):569−577. doi: 10.1177/1082013211430294
[36] CHAI Y W, WANG M Z, ZHANG G Y. Interaction between amylose and tea polyphenols modulates the postprandial glycemic response to high-amylose maize starch[J]. Journal of Agricultural and Food Chemistry,2013,61(36):8608−8615. doi: 10.1021/jf402821r
[37] BARROS F, AWIKA J M, ROONEY L W. Interaction of tannins and other sorghum phenolic compounds with starch and effects on in vitro starch digestibility[J]. Journal of Agricultural and Food Chemistry,2012,60(46):11609−11617. doi: 10.1021/jf3034539
[38] DU J J, YANG Z K, XU X N, et al. Effects of tea polyphenols on the structural and physicochemical properties of high-hydrostatic-pressure-gelatinized rice starch[J]. Food Hydrocolloids,2019,91:256−262. doi: 10.1016/j.foodhyd.2019.01.035
[39] LV Y Z, ZHANG L M, LI M N, et al. Physicochemical properties and digestibility of potato starch treated by ball milling with tea polyphenols[J]. International Journal of Biological Macromolecules,2019,129:207−213. doi: 10.1016/j.ijbiomac.2019.02.028
[40] HUANG J H, WANG Z, FAN L, et al. A review of wheat starch analyses: Methods, techniques, structure and function[J]. International Journal of Biological Macromolecules,2022,203:130−142. doi: 10.1016/j.ijbiomac.2022.01.149
[41] MA Y S, ZHANG H, JIN Y M, et al. Impact of superheated steam on the moisture transfer, structural characteristics and rheological properties of wheat starch[J]. Food Hydrocolloids,2022,122:107089. doi: 10.1016/j.foodhyd.2021.107089
[42] RONG L Y, SHEN M Y, WEN H L, et al. Effects of xanthan, guar and Mesona chinensis Benth gums on the pasting, rheological, texture properties and microstructure of pea starch gels[J]. Food Hydrocolloids,2022,125:107391. doi: 10.1016/j.foodhyd.2021.107391
[43] CHI C D, LI X X, ZHANG Y P, et al. Modulating the in vitro digestibility and predicted glycemic index of rice starch gels by complexation with gallic acid[J]. Food Hydrocolloids,2019,89:821−828. doi: 10.1016/j.foodhyd.2018.11.016
[44] HAN X, ZHANG M, ZHANG R, et al. Physicochemical interactions between rice starch and different polyphenols and structural characterization of their complexes[J]. LWT-Food Science and Technology,2020,125:109227. doi: 10.1016/j.lwt.2020.109227
[45] CHEN N, GAO H X, HE Q, et al. Interaction and action mechanism of starch with different phenolic compounds[J]. International Journal of Food Sciences and Nutrition,2020,71(6):726−737. doi: 10.1080/09637486.2020.1722074
[46] OBIRO W C, RAY S S, EMMAMBUX M N. V-amylose structural characteristics, methods of preparation, significance, and potential applications[J]. Food Reviews International,2012,28(4):412−438. doi: 10.1080/87559129.2012.660718
[47] WEI X, LI J, LI B. Multiple steps and critical behaviors of the binding of tannic acid to wheat starch: Effect of the concentration of wheat starch and the mass ratio of tannic acid to wheat starch[J]. Food Hydrocolloids,2019,94:174−182. doi: 10.1016/j.foodhyd.2019.03.019
[48] WU Y, NIU M, XU H L, et al. Pasting behaviors, gel rheological properties, and freeze-thaw stability of rice flour and starch modified by green tea polyphenols[J]. LWT-Food Science and Technology,2020,118:108796. doi: 10.1016/j.lwt.2019.108796
[49] LV Y J, LI M, PAN J X, et al. Interactions between tea products and wheat starch during retrogradation[J]. Food Bioscience,2020,34:100523. doi: 10.1016/j.fbio.2019.100523
[50] VELDERRAIN R G R, PALAFOX C H, WALL-MEDRANO A, et al. Phenolic compounds: Their journey after intake[J]. Food and Function,2013,5(2):189−197.
[51] GUO Z B, ZHAO B B, CHEN J, et al. Insight into the characterization and digestion of lotus seed starch-tea polyphenol complexes prepared under high hydrostatic pressure[J]. Food Chemistry,2019,297:124992. doi: 10.1016/j.foodchem.2019.124992
[52] COHEN R, SCHWARTZ B, PERI I, et al. Improving bioavailability and stability of genistein by complexation with high-amylose corn starch[J]. Journal of Agricultural and Food Chemistry,2011,59(14):7932−7938. doi: 10.1021/jf2013277
[53] COHEN R, ORLOVA Y, KOVALEV M, et al. Structural and functional properties of amylose complexes with genistein[J]. Journal of Agricultural and Food Chemistry,2008,56(11):4212−4218. doi: 10.1021/jf800255c
[54] WEI G, JIE Z A, PLA B, et al. Preparation and characterization of octenyl succinylated starch microgels via a water-in-oil (W/O) inverse microemulsion process for loading and releasing epigallocatechin gallate[J]. Food Chemistry,2021,355:129661. doi: 10.1016/j.foodchem.2021.129661
[55] ACEVEDO-GUEVARA L, NIETO-SUAZA L, SANCHEZ L T, et al. Development of native and modified banana starch nanoparticles as vehicles for curcumin[J]. International Journal of Biological Macromolecules,2018,111:498−504. doi: 10.1016/j.ijbiomac.2018.01.063
[56] KANG J, KIM Y H, CHOI S J, et al. Improving the stability and curcumin retention rate of curcumin-loaded filled hydrogel prepared using 4αGTase-treated rice starch[J]. Foods,2021,10(1):150. doi: 10.3390/foods10010150
[57] CHI C, LI X, ZHANG Y, et al. Digestibility and supramolecular structural changes of maize starch by non-covalent interactions with gallic acid[J]. Food & Function,2017,8(2):720−730.
[58] LI M, PERNELL C, FERRUZZI M G. Complexation with phenolic acids affect rheological properties and digestibility of potato starch and maize amylopectin[J]. Food Hydrocolloids,2018,77:843−852. doi: 10.1016/j.foodhyd.2017.11.028
[59] LS A, YW A, MING M B. Inhibition of α-amylase by polyphenolic compounds: Substrate digestion, binding interactions and nutritional intervention[J]. Trends in Food Science & Technology,2020,104:190−207.
[60] LIU J, WANG M, PENG S, et al. Effect of green tea catechins on the postprandial glycemic response to starches differing in amylose content[J]. Journal of Agricultural and Food Chemistry,2011,59:4582−4588. doi: 10.1021/jf200355q
-
期刊类型引用(6)
1. 许津阁,郑卓琦,侯鹏颉,马高兴,熊彦娣,马壮,刘萌,赵靓,廖小军. 不同产地酱用卡宴辣椒原料品质评价. 食品工业科技. 2025(01): 317-332 .  本站查看
本站查看
2. 熊岑,阮沛仪,郭晓刚,刘大千,曾丽娴. 辣椒中多酚的提取工艺和抗氧化活性研究. 中国调味品. 2024(02): 89-94 .  百度学术
百度学术
3. 金怀慷,杨灿,刘力. 云南5种辣椒加工适应性分析与比较. 天津农业科学. 2024(06): 77-82 .  百度学术
百度学术
4. 田筱,涂德辉,梁传静,王永平,李伟,邢丹. 贵州五地辣椒矿物质含量及果实品质分析. 北方园艺. 2024(18): 7-15 .  百度学术
百度学术
5. 杨娅,吴康云,黄冬福,周鹏,付文婷,王楠艺,何建文. 基于主成分分析对不同地区辣椒品质的综合评价. 食品工业科技. 2024(23): 264-271 .  本站查看
本站查看
6. 付文婷,王楠艺,周鹏,杨娅,彭世清,黄冬福,何建文. 不同产区辣椒果实品质差异及其与气象因子的相关性. 南方农业学报. 2024(09): 2763-2771 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:
 下载:
下载:



