Aroma Characteristics of Cold/Hot Tomato Paste and Their Relationships with Non-volatile Components
-
摘要: 番茄酱是一种重要的调味品,因其独特的口感和风味而广受消费者喜爱。本文以通过冷破(cold break,CB)、热破(hot break,HB)生产的8种番茄酱作为研究对象,采用顶空固相微萃取-气相色谱-质谱联用(headspace solid-phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)技术对其挥发性风味化合物的组成及相对含量进行分析,计算香气活度值(odor activity value,OAV)确定特征风味化合物,结合主成分分析(principal component analysis,PCA)以及相关性分析确定番茄酱中的香气成分与还原糖、有机酸、抗坏血酸以及果胶含量之间的关系。结果表明:不同破碎方法的番茄酱中挥发性风味化合物的组成及相对含量存在明显差别,8个样品中共鉴定出61种挥发性风味化合物,以醛类、醇类和酮类为主,其中22种为OAV≥1的香气活性化合物;CB番茄酱中的挥发性风味化合物组成及相对含量要显著(P<0.05)高于HB番茄酱,并且CB处理有利于保持番茄酱中较高的还原糖、有机酸含量,但会导致果胶浓度下降;通过PCA可以将CB、HB番茄酱较好区分;Pearson相关性分析结果表明β-环柠檬醛、苯乙醛、芳樟醇、α-松油醇、大马士酮、2-戊基呋喃、2-异丁基噻唑这几种化合物与非挥发性成分之间表现出较强的相关性,因此推测它们之间可能存在相互作用。
-
关键词:
- 番茄酱 /
- 破碎方式 /
- 顶空固相微萃取-气相色谱-质谱联用(HS-SPME-GC-MS) /
- 挥发性风味化合物 /
- 相关性
Abstract: Tomato paste is an important condiment, which is popular among consumers due to its unique taste and flavor. In this paper, headspace solid-phase microextraction-gas chromatography-mass spectrometry (HS-SPME-GC-MS) technology was used to measure the composition and relative content of volatile flavor compounds in eight kinds of tomato paste produced by cold break (CB) and hot break (HB) methods. The odor activity value (OAV) was calculated to determine odor active compounds. The relationship between the odor active compounds and the contents of reducing sugars, organic acids, ascorbic acid and pectin were analyzed by principal component analysis (PCA) and correlation analysis. The results showed that there were significant (P<0.05) differences in the composition and relative contents of flavor compounds in CB and HB tomato pastes. A total of 61 volatile compounds were identified in 8 samples, including aldehydes, alcohols and ketones, and 22 compounds belonged to odor active compounds (OAV≥1). The composition and relative contents of volatile compounds in CB tomato paste were significantly higher than that in HB tomato paste. At the same time, CB treatment was beneficial to keep high reducing sugars and organic acids content in tomato paste but would lead to the decrease of pectin concentration. Notably, the CB and HB tomato pastes could be distinguished by PCA of odor active compounds. Pearson correlation analysis suggested that β-cyclocitral, phenylacetaldehyde, linalool, α-terpineol, damascenone, 2-pentylfuran, 2-isobutylthiazole showed strong correlation with non-volatile components, so it was speculated that there might be interactions between them. -
番茄(Lycopersicum esculentum)是世界上生产最多、最重要的农产品之一[1],因其独特风味以及丰富的营养物质,在食品工业中具有广泛的应用价值[2]。番茄除了被当作新鲜果蔬食用外,还被加工成各种各样的番茄加工制品,如番茄汁、番茄罐头、番茄丁、番茄酱等[3]。番茄酱作为最受消费者喜爱的番茄制品之一,其生产工艺简单,制作成本低,在减少新鲜番茄贮藏损失的同时还创造了额外经济价值。番茄酱的生产主要包括原料清洗、筛选、破碎、预热、精制、浓缩、杀菌、罐装等工艺。根据破碎温度的不同,番茄酱可通过冷破(cold break,CB)和热破(hot break,HB)两种方式生产,热破过程中,温度一般在85~90 ℃之间,当热破温度超过90 ℃时,即为超热破番茄酱(super-hot break,SHB),这会导致果胶酶和果胶甲酯酶等酶活力降低,阻碍番茄中果胶物质的降解,提升产品的粘度;而冷破温度一般低于70 ℃,这有利于保留酶的活性,降低产品粘度,使产品色泽更加自然,风味特征更加鲜明[4-5]。预热处理工艺与破碎温度保持一致,因此会导致热破番茄酱中的酶活进一步降低,产品粘度进一步提升。在热加工处理过程中,番茄中的番茄红素由反式结构向顺式结构转变,而人体对于顺式结构具有更高的生物利用率,因此番茄酱是比新鲜番茄更优质的番茄红素来源[6]。此外,Gao等[7]研究发现,热破番茄酱中9,13-di-cis-lycopene,9-cis-lycopene,5-cis-lycopene这几种顺式番茄红素含量显著高于冷破番茄酱,因此热破工艺产生的番茄红素具有更高的生物利用度。
风味是食品非常重要的一个感官属性,不仅可以反映食品整体品质的高低,也是影响消费者接受程度的重要因素[8-9]。与新鲜番茄相比,番茄酱在生产过程中由于温度的升高会发生氨基酸降解、类胡萝卜素氧化、以及美拉德反应[10],从而导致整体风味轮廓发生显著变化。目前,已经从番茄及其加工制品中鉴定出400多种风味化合物[11],但能够显著影响我们对番茄风味感知的香气活性化合物只有几十种。早在1993年,Buttery等[12]对新鲜番茄以及番茄酱中的风味化合物进行提取以及定性定量分析,结果发现,与新鲜番茄相比,番茄酱中的(Z)-3-己烯醛和己醛含量降低了约400倍,而一些酮类(如6-甲基-5庚烯-2-酮)以及萜烯类(如芳樟醇)化合物的浓度显著提升;Kelebek等[13]采取溶剂辅助蒸发提取(solvent assisted flavor evaporation,SAFE)结合香气提取稀释分析(aroma extract dilution analysis,AEDA)对冷破、热破番茄酱不同加工阶段的风味进行比较,发现(Z)-3-己烯醛、4-甲基-5(H)-呋喃-2-酮、β-紫兰酮是新鲜番茄中的关键香气成分,糠醛是热破番茄酱中的关键香气成分,甲基庚烯酮是冷破番茄酱中的关键香气成分,且在破碎、加热、蒸发阶段这些化合物的含量有所不同。
目前,对于番茄酱风味的研究主要集中在挥发性香气成分方面,然而,风味是挥发性化合物与糖、酸、果胶以及其它一些非挥发性成分相互作用的结果,这些非挥发性成分可能通过调控香气化合物的保留和释放来影响番茄酱的整体风味特征[14]。对于番茄酱中香气化合物和非挥发性成分的对比以及它们之间相互作用的研究还未见报道。因此,本研究以冷破、热破番茄酱作为研究对象,通过顶空固相微萃取-气相色谱-质谱联用(HS-SPME-GC-MS)技术对其香气成分进行检测,同时对番茄酱中的还原糖、有机酸、果胶、抗坏血酸含量进行测定,分析它们与香气成分之间的相关性,以期为番茄酱加工方法的改善以及风味品质的提升提供理论依据。
1. 材料与方法
1.1 材料与仪器
8种番茄酱样品 来自于中粮屯河生产线,具体信息如表1所示,样品采集后立即运回实验室,并放在−80 ℃的超低温冰箱内进行贮存备用;盐酸、氢氧化钠、无水乙醇、咔唑、磷酸、磷酸二氢钠 分析纯,国药集团化学试剂有限公司;标准品:柠檬酸、苹果酸、葡萄糖、果糖、蔗糖 HPLC≥98.0%,上海源叶生物公司;半乳糖醛酸标准品 质量分数≥97.0%,上海麦克林公司;1-庚醇(色谱纯)、C7~C30系列烷烃(质量分数≥99.0%) 美国Sigma-Aldrich公司。
表 1 8种番茄酱的信息参数Table 1. Information parameters of eight kinds of tomato paste样品编号 产地 固形物含量 破碎方式 1 昌吉 32%~34% CB 2 昌吉 36%~38% CB 3 乌苏 28%~30% CB 4 乌苏 36%~38% CB 5 昌吉 30%~32% HB 6 乌苏 28%~30% HB 7 乌苏 30%~32% HB 8 昌吉 28%~30% SHB 紫外分光光度计 美国PerkinElmer公司;高效液相色谱仪 美国Waters公司;7890B-5977A气相色谱-质谱联用仪 美国Agilent公司;固相微萃取装置、57330-U萃取头 美国Supelco公司;HH-2型数显恒温水浴锅 常州国华电器有限公司。
1.2 实验方法
1.2.1 挥发性成分的萃取
采取SPME法提取番茄酱中的挥发性风味成分:称取5.0 g番茄酱样品加入到40 mL顶空瓶中,并用10 μL微量注射器向样品瓶中准确的加入1 μL内标1-庚醇(0.822 mg/mL),旋紧顶空瓶瓶盖后将其放入50 ℃的水浴中进行平衡,平衡时间为15 min,与此同时将萃取头插入250 ℃的进样口进行老化,老化时间为5 min,老化结束后,将其插入到顶空瓶中进行萃取,萃取时间为40 min。
1.2.2 GC-MS 参数设置
色谱(GC)条件:柱子采用DB-Wax MS(30 m×320 μm,0.25 μm),进样口温度250 ℃,柱温箱升温程序:40 ℃,保持3 min;3 ℃/min升温至180 ℃,10 ℃/min升温至230 ℃,保持3 min;不分流进样;载气:99.999%高纯度氦气,载气流速:3.0751 mL/min。
质谱(MS)条件:离子源EI源;电子能量70 eV;接口温度250 ℃;离子源温度230 ℃;四级杆温度150 ℃,进样口温度250 ℃,质量扫描范围50~500 u,采集方式Scan,每种条件测定重复5次。
1.2.3 葡萄糖、果糖、蔗糖含量的测定
参考邸太菊等[8]的方法进行。
1.2.4 有机酸(苹果酸、柠檬酸)含量的测定
按照GB 5009.157-2016的方法进行。
1.2.5 抗坏血酸含量的测定
参考付晓伟等[15]的方法进行。
1.2.6 果胶含量的测定
参考李晓等[16]的方法进行。
1.2.7 感官评价分析
选取10名经过培训筛选的感官评价员(5名男生,5名女生,年龄在23~30岁之间)对8种不同加工因素下的番茄酱样品进行风味的评定,培训筛选方法如下:让所有人员对经过一定梯度稀释的标准品如6-甲基-5-庚烯-2-酮、芳樟醇、柠檬烯等进行嗅闻,对气味可以准确描述者即为合格。正式评价前让感官评价员熟悉番茄酱的风味,以保证可以做出客观评价[17],参考牟琴等[18]的方法稍作修改,制定番茄酱的感官评价标准(0~5分),如表2所示。
表 2 番茄酱的感官评价标准Table 2. Sensory evaluation criteria for tomato pastes项目 感官得分(分) 0 1 2 3 4 5 青草味 无 极微 轻微 中等 强 极强 果味 花香味 青草味 酸味 蒸煮味 异味 喜好程度 1.2.8 香气成分的定性分析
采取质谱库检索(MS)、保留指数(RI)相结合的方法对番茄酱中的香气成分进行定性分析[9]。
1.2.9 香气成分的定量分析
采取内标半定量的方法计算每种化合物在不同番茄酱样品中的相对含量。将1 μL内标1-庚醇(0.822 mg/mL)标准品加入到待测样品,按照1.2.2中的升温程序进行全扫描检测,根据以下公式计算待测物浓度[9]:
ρx=Ax×ρ1A1 式中:ρx和Ax表示待测物的浓度和峰面积;ρ1和A1表示内标物的浓度和峰面积。
1.2.10 香气活性值(OAV)计算
OAV值为香气成分的浓度与其阈值之间的比值,其大小可以反映各香气成分对样品整体贡献率的高低,OAV≥1,说明该物质对样品的整体风味具有重要作用,OAV<1,代表该物质对样品的整体风味具有辅助作用[19]。
1.3 数据处理
采用Microsoft Office 2019软件进行表格制作,采用SPSS 18.0软件进行单因素方差分析和显著性分析,显著性分析采用Duncan检验,利用SIMCA 14.1进行主成分分析,采用Origin 2022进行Pearson相关性分析。
2. 结果与分析
2.1 番茄酱的挥发性化合物组成分析
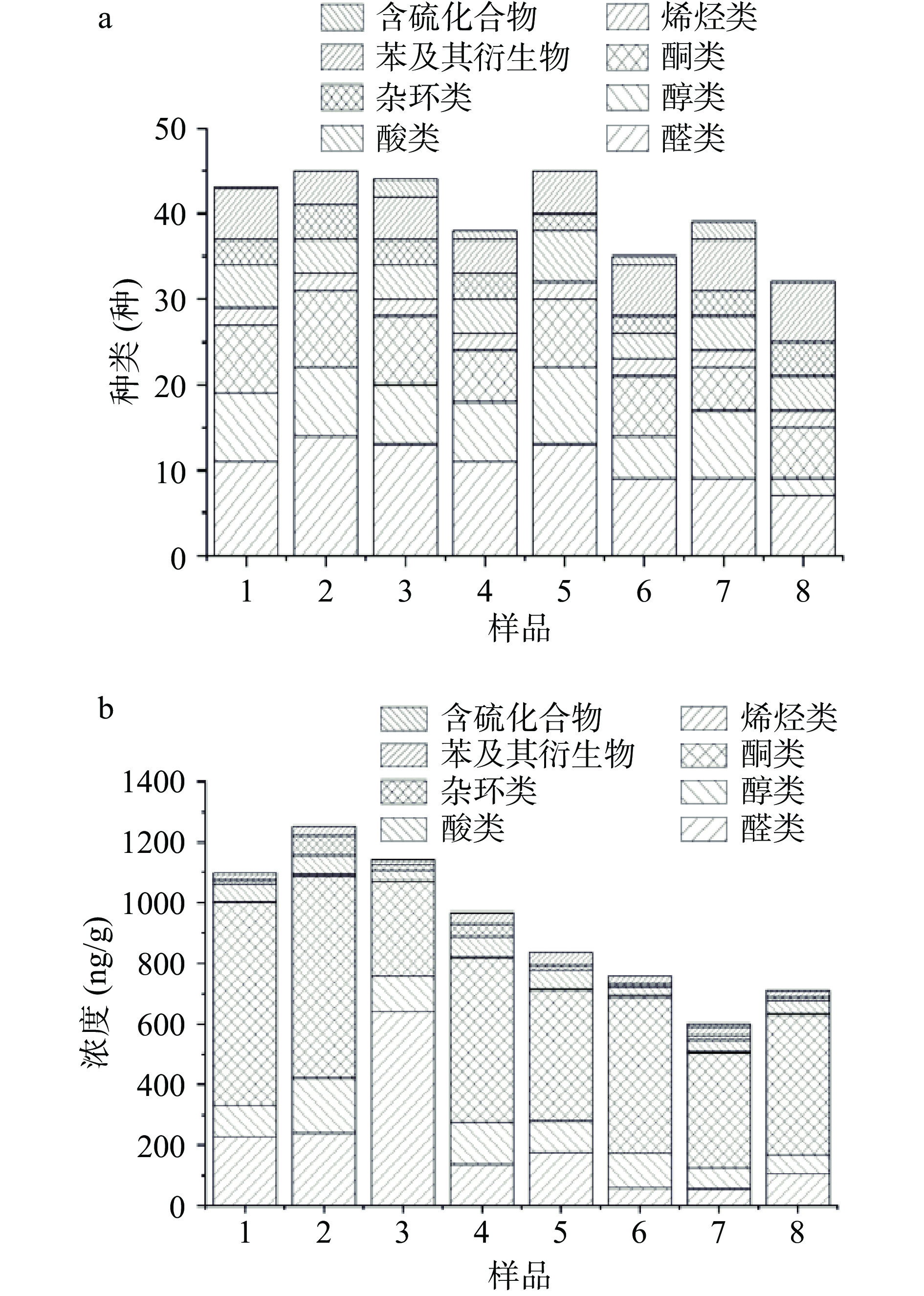
挥发性化合物是影响番茄酱感官品质的重要因素,同时对消费者的购买行为也具有先导性作用[20]。以来自不同地区(昌吉、乌苏),不同固形物含量(28%~38%)以及不同破碎方式(冷破、热破、超热破)的8种番茄酱样品为原料,对其挥发性风味化合物的组成以及行对含量进行分析,结果如表3和图1所示,共鉴定出61种化合物,其中包括16种醛类、11种醇类、10种酮类、2种烯烃类、6种酸类、5种杂环类、9种苯及其衍生物、2种含硫类化合物。经过冷破处理的番茄酱(1~4号)中所鉴定出的化合物种类在38~45种之间,而经过热破处理(5~8号)番茄酱中鉴定出的化合物种类在32~45种之间。
表 3 8种番茄酱中挥发性风味组分Table 3. Volatile components in eight tomato paste序号 化合物名称 RI值 化合物浓度(ng/g) 1号 2号 3号 4号 5号 6号 7号 8号 醛类 1 己醛 1084 5.04±2.63b 9.14±0.68a 1.57±0.41cd 3.18±0.84bc 3.43±0.92bc − − 9.44±1.52a 2 辛醛 1280 0.75±0.06d 1.46±0.13c 0.96±0.08d 2.11±0.10b 2.53±0.65a − − − 3 2,6-二甲基-5-庚烯醛 1389 − − − 2.75±0.31 − − − − 4 (E)-2-庚烯醛 1342 − 3.12±0.31 − − − − − − 5 壬醛 1385 3.17±0.4b 2.33±0.31bc 2.23±0.28bc 2.90±0.13bc 4.64±1.5abc 1.83±0.10c 2.92±0.19bc 4.66±0.15a 6 (E)-2-辛烯醛 1345 3.55±0.53a 2.47±0.08b 1.78±0.29c 2.61±0.26b 1.89±0.32c 1.79±0.13c 1.94±0.03c 1.65±0.04c 7 糠醛 1455 18.46±0.97d 78.99±2.43a 25.16±0.81c 56.95±1.36b 8.32±0.30f 6.56±0.00f 10.86±0.31e 7.40±0.44f 8 苯甲醛 1495 121.88±8.61b 81.15±20.51b 574.08±208.93a − 88.00±4.97b − − 49.78±3.29b 9 (E)-2-壬烯醛 1521 2.61±0.18a 2.06±0.13b 0.94±0.35c − 2.05±0.32b − 1.83±0.25b − 10 β-环柠檬醛 1598 4.48±0.36b 5.03±0.16a 1.55±0.34e 4.98±0.45a 3.47±0.05c 2.77±0.02d 2.70±0.16d − 11 苯乙醛 1625 55.12±7.11a 41.42±1.87b 25.03±3.59c 47.51±5.8ab 49.93±8.16ab 30.7±1.43c 26.13±2.67c 30.18±2.59c 12 2,3-二氢-2,2,6-三甲基苯甲醛 1198 − 5.14±0.12b 2.44±0.07d 8.52±0.38a 2.39±0.23d 1.84±0.05e 2.98±0.07c − 13 (E)-2-癸烯醛 1647 − − − − 2.16±0.51 − − − 14 4-乙基苯甲醛 1719 2.99±0.66a 2.61±0.10a 1.21±0.08c 2.80±0.54a 1.56±0.05bc 1.48±0.03bc − 1.95±0.17b 15 柠檬醛 1720 7.89±1.28b 4.37±1.45c 3.49±0.30c − 7.33±1.29b 9.51±1.31a 4.42±0.48c − 16 5-甲基-2-噻吩甲醛 1785 − 0.70±0.16b 1.38±0.30a 1.56±0.09a − 1.56±0.05a 0.74±0.00b − 小计 225.94±10.52b 240±21.14b 641.81±206.22a 135.87±6.43bc 177.7±12.64bc 58.15±1.24c 54.51±2.66c 105.06±4.91bc 醇类 1 己醇 1360 − − − − 2.22±0.31 − − − 2 2-乙基己醇 1474 0.98±0.18b − − − 1.44±0.15a − − − 3 芳樟醇 1537 81.13±7.08c 130.3±8.8a 81.4±3.82c 108.52±4.76b 61.93±2.35d 81.71±1.01c 45.24±3.98e 56.57±2.20d 4 脱氢芳樟醇 1583 2.44±0.2cd 6.22±1.13b 3.77±0.99c 10.32±0.51a 1.78±0.16d − 2.51±0.15cd − 5 α-松油醇 1692 10.94±0.71c 18.83±0.99a 13.42±0.14b 13.34±0.7b 10.2±0.9c 11.47±0.47c 5.24±0.65d 5.61±0.18d 6 3-甲硫基丙醇 1701 − 9.37±0.62a 2.79±0.14c 2.83±0.22c 6.84±0.74b 6.04±0.23b 2.13±0.04d − 7 橙花醇 1804 1.09±0.12b 1.72±0.08a − − 1.17±0.13b − − − 8 2-(4-甲基苯基)丙-2-醇 1844 0.86±0.04b 0.82±0.04b 0.54±0.05c 1.08±0.02a − − − − 9 香叶醇 1854 2.00±0.57c 2.84±0.17a 2.40±0.13b − 1.84±0.07c 2.12±0.00bc − − 10 十二醇 1970 − − − − − − 0.24±0.42 − 11 苯乙醇 1883 4.16±0.23d 11.21±0.38c 11.83±0.72c 3.56±0.08d 13.62±0.88ab 14.35±0.05a 13.05±0.93b − 小计 103.6±7.98d 181.32±10.19a 116.15±5.24c 139.66±4.62b 101.04±2.66d 116.34±1.42c 68.42±4.25e 62.18±2.13e 酮类 1 2-庚酮 1174 − 11.00±1.99 − − − − − − 2 仲辛酮 1285 0.61±0.08f 2.83±0.27d 1.32±0.15ef 6.81±0.69b 5.79±0.57c 1.79±0.27e 6.22±0.33bc 10.12±0.77a 3 1-庚烯-3-酮 1290 − − 0.12±0.11 − − − − − 4 甲基庚烯酮 1336 635.53±45.11a 609.91±26.35a 277.55±53.12d 494.56±78.92b 402.52±59.97bc 446.9±75.43b 352.94±70.99cd 431.25±69.43bc 5 对甲基苯乙酮 1759 7.56±0.59b 7.90±0.09b 4.69±0.54e 9.95±0.56a 6.11±0.43c 6.02±0.01cd 5.50±0.46cde 5.14±0.78de 6 大马士酮 1813 8.09±0.81c 14.21±0.83a 9.93±0.68b 14.55±0.35a 4.62±0.08e 5.47±0.45d 4.75±0.6de 4.26±0.28e 7 香叶基丙酮 1840 16.31±2.1a 18.01±0.24a 14.48±1.28b 13.45±0.75bc 11.88±0.55cd 13.1±0.49bc 12.18±0.82cd 10.83±0.94d 8 β-紫罗酮 1913 0.89±0.04b 1.21±0.07a 0.67±0.02c − 0.90±0.09b − − 0.61±0.11c 9 呋喃酮 2064 0.61±0.06a 0.45±0.04b − − 0.49±0.03b 0.37±0.02c − − 10 法尼基丙酮 2083 1.47±0.23b 1.47±0.07b 3.45±0.48a 0.91±0.05c 0.58±0.05cd 0.29±0.03de − − 小计 671.07±45.16a 666.98±25.78a 312.2±51.98 540.24±79.96b 432.88±59.81bc 515.48±89.19b 381.59±70.46 462.21±70.11bc 烃类 1 (+)-柠檬烯 1178 1.38±0.54d 2.79±0.27bc 1.36±0.44d 4.36±0.69a 2.68±0.26c 2.33±0.56cd 2.35±0.58cd 3.76±1.03ab 2 紫苏烯 1295 1.19±0.19cd 1.63±0.1bc 1.07±0.09d 2.31±0.44a 2.29±0.48a 1.86±0.06b 1.59±0.09bc 1.64±0.02bc 小计 2.57±0.71d 4.42±0.3bc 2.42±0.47d 6.67±0.55a 4.97±0.75bc 4.18±0.6c 3.93±0.49c 5.4±1.00b 酸类 1 乙酸 1450 34.98±3.94a 36.00±0.87a 17.82±2.90c 23.29±1.03b 24.86±0.87b 14.32±1.09c 22.9±2.99b 10.18±0.32d 2 丙酸 1525 − − − − 2.91±0.34 − − − 3 丁酸 1652 2.23±0.18b − − − 2.88±0.10a − − − 4 异戊酸 1665 9.16±0.82e 20.11±0.35c 12.49±0.99de 33.68±2.96a 26.11±3.43b 12.32±0.8de 13.1±2.50d 23.87±1.05b 5 辛酸 2083 2.95±0.24a 2.43±0.13ab 2.33±0.06b 2.75±0.28ab 1.61±0.05c − 1.39±0.31c 2.92±0.69a 6 壬酸 2164 8.46±1.08a 4.34±0.88b 1.57±0.34cd 4.2±0.77b 2.31±0.62c 0.93±0.10d 0.96±0.12d 3.74±0.14b 小计 57.78±3.34b 62.88±1.20ab 34.2±3.18d 63.92±4.09a 60.69±3.81ab 28.01±0.89e 38.35±3.84cd 40.71±0.32c 杂环类化合物 1 2-戊基呋喃 1240 6.33±1.44e 42.88±2.14a 9.14±0.81cd 14.99±2.06b 11.07±0.19c 6.97±0.39de 6.74±1.13e 6.66±0.34e 2 2-乙酰基呋喃 1490 3.65±0.35cd 18.95±1.22a 6.99±0.31b 19.5±0.76a 4.38±0.12c 3.17±0.11d 3.75±0.27cd 1.91±0.14e 3 2-异丁基噻唑 1391 3.37±1.24b 4.19±1.32b 3.12±0.32b 9.49±1.51a − − 4.50±0.07b 4.58±0.33b 4 2-乙基-5-甲基吡嗪 1402 − 0.65±0.01 − − − − − − 5 3-甲基吲哚 1500 − − − − − − − 0.06±0.05 小计 13.35±0.62de 66.66±2.93a 19.25±0.92c 43.98±3.68b 15.45±0.27d 10.16±0.35e 14.99±1.29d 13.21±0.36de 苯及其衍生物 1 甲苯 1042 10.01±1.57c 15.85±0.91b 6.66±0.59c 24.88±3.87a 24.09±4.32a 18.64±1.37b 20.39±5.53ab 6.13±1.89c 2 间二甲苯 1150 3.40±0.52d 6.70±0.57c 2.91±0.30d − 10.39±0.90a − − 8.61±1.50b 3 4-异丙基甲苯 1261 1.96±0.28b 3.64±0.33b 2.85±0.46b 8.51±2.29a 3.25±0.06b 2.40±0.43b 3.19±0.79b 3.18±0.30b 4 1,2,4-三甲基苯 1293 2.24±0.27a − − − 1.71±0.42b 1.26±0.06c 1.72±0.04b 1.42±0.01bc 5 烯丙苯酚 1380 − − − − − − 1.41±0.02 − 6 对甲酚 2080 − − − − − 0.11±0.00 − 0.27±0.01 7 丁香酚 2163 0.32±0.05b − 0.25±0.01c 0.23±0.02c − − 0.27±0.04bc 0.68±0.09a 8 4-乙基苯酚 2185 − − − − − 0.25±0.02 − − 9 4-乙烯基-2-甲氧基苯酚 2230 5.66±0.73a 3.66±0.29b 2.79±0.29c 2.69±0.18c 2.61±0.34c 2.4±0.11c 1.46±0.20d 1.24±0.07d 小计 23.59±2.00bc 29.85±1.39b 15.47±0.12d 36.31±3.52a 42.04±5.84a 24.33±1.57bc 28.43±6.18b 21.52±0.59c 含硫化合物 1 二甲基二硫 1058 − − 0.17±0.00b − − 1.38±0.22 4.71±1.12a − 2 二甲基三硫 1366 − − 1.57±0.25b 1.36±0.24b − − 4.74±0.64a − 小计 − − 1.74±0.25b 1.36±0.24b − 1.36±0.16b 9.45±1.75a − 总计 548.95±27.47ab 626.06±17.18a 571.62±98.94a 484.01±40.76bc 417.38±25.18cd 379±44.94de 299.84±37.26e 355.15±36.37de 注:不同字母代表风味化合物含量存在显著性差异(P<0.05)。 图1反应了8种番茄酱样品中的挥发性化合物种类(图1a)和浓度(图1b),从图中可以看出,除样品5外,冷破番茄酱中鉴定出的挥发性化合物种类显著高于热破番茄酱,2号样品的挥发性化合物种类也是8种样品中最多的,为45种,同时,破碎温度最高的8号样品中鉴定出的挥发性化合物种类最少;冷破番茄酱(样品1~4号)的总挥发性化合物浓度也要显著高于热破番茄酱(5~8号),其中2号样品的总挥发性化合物浓度最高,为626.02 ng/g;醛类化合物是番茄及其制品中重要的风味化合物,3号样品中发现的醛类化合物最多,为14种,在经过超热处理的番茄酱中发现的醛类化合物最少,为7种,辛醛、(E)-2-庚烯醛、(E)-2-壬烯醛、β-环柠檬醛以及柠檬醛等重要的风味化合物在超热处理的番茄酱中均未发现。C6~C9的醛类化合物可以赋予番茄及其制品青草味和生青味,主要通过脂肪氧合酶(LOX)途径生成。热破番茄酱的加工温度较高,这会导致与脂肪氧化相关酶的活性受到抑制甚至失活,从而降低醛类化合物的含量[21]。
番茄中的醇类化合物主要是由C6的醛类在醇脱氢酶(ADH)的作用下转化生成[22],其阈值一般较高,因此对番茄酱的整体风味贡献较小,但它可以作为一种重要前体物参与长链酯类化合物的生成[23]。从表3可以看出,2号样品中的醇类化合物含量最高,为181.32 ng/g,样品8号中仅鉴定出芳樟醇和α-松油醇两种醇类化合物,总浓度也只有62.18 ng/g,这与热处理过程中ADH活性下降有关。芳樟醇主要呈现出一种玫瑰花香,也有研究发现芳樟醇与番茄制品中煮熟的味道有关[24]。α-松油醇则主要表现出一种薄荷的清香味,是新鲜番茄的特征风味物质之一。以往有研究表明,热处理通过降低番茄中呈现植物风味的挥发性化合物的含量而使番茄酱中具有更加浓郁的煮熟味[25]。
碳数在7以下的酮是脂类衍生的挥发性化合物,其可以赋予番茄酱青草香、花香以及甜香[26]。值得注意的是,甲基庚烯酮在8种番茄酱样品中均有较高的浓度,浓度在277.55~635.53 ng/g之间,这与Kelebek等[13]的研究结果一致。有学者发现类胡萝卜素和番茄红素含量较高的番茄品种中含有较高的甲基庚烯酮,因此推断甲基庚烯酮以番茄红素和类胡萝卜素为前体物通过类胡萝卜素途径生成[27-28]。
乙酸、丙酸、丁酸、异戊酸、辛酸及壬酸均为番茄酱中的羧酸,其中,乙酸、异戊酸以及壬酸在8种不同的番茄酱中均被检测到,并且乙酸和异戊酸具有较高的浓度。乙酸主要是由加工过程中发酵所产生,主要赋予番茄酱类似于葡萄酒的风味,异戊酸主要为番茄酱提供酸味。
除此之外,番茄酱中也鉴定出一些烯烃类、杂环类、苯及其衍生物以及一些含硫类化合物,相对于醇、醛类、酮类化合物来说,这些化合物的种类和浓度相对较低,但有些化合物因其阈值较低(如含硫化合物),对番茄酱的整体风味仍具有较大贡献。
2.2 番茄酱中香气活性化合物分析
挥发性风味化合物对番茄酱的贡献程度由其含量和阈值共同决定,因此通过计算每种化合物的OAV进行对比分析,得到OAV≥1的香气活性化合物共22种,结果如表4所示。从表4中可以看出,22种香气活性化合物包括7种醛、4种醇、6种酮、2种杂环化合物、2种含硫化合物、1种烯烃。OAV较大的化合物为酮类、醇类以及含硫化合物。其中大马士酮(OAV=7276)最大,其次是β-紫罗酮(OAV=1734),苯乙醇(OAV=957)、二甲基三硫(OAV=948)以及芳樟醇(OAV=592),它们的OAV均大于100,说明这几种化合物对于番茄酱的风味具有重要贡献作用。大马士酮、β-紫罗酮、芳樟醇以及苯乙醇它们均能赋予番茄酱水果香、花香、以及甜香等风味特征,这些化合物同时也是新鲜番茄的特征风味的重要组成成分。而二甲基三硫在番茄酱中的浓度较低,但因其阈值极低,因此也是番茄酱中的香气活性化合物,它主要来自于含硫氨基酸的降解,可以赋予番茄酱硫磺、卷心菜的风味,对其蒸煮风味贡献较大[29]。
表 4 番茄酱中的香气活性化合物汇总Table 4. Aroma active compounds in tomato paste序号 化合物名称 CAS 风味特征 阈值(ng/g) 最高OAV 1 大马士酮 23726-93-4 苹果香,花香 0.002 7276 2 β-紫罗酮 79-77-6 花香,甜香 0.0007 1734 3 苯乙醇 22258.00 甜香,丁香花 0.015 957 4 二甲基三硫 3658-80-8 卷心菜,硫磺 0.005 948 5 芳樟醇 78-70-6 薰衣草,花香 0.22 592 6 二甲基二硫 624-92-0 洋葱,卷心菜 0.16 29 7 呋喃酮 3658-77-3 奶油,甜香 0.03 20 8 甲基庚烯酮 110-93-0 蘑菇味,蒸煮味 68 9 9 (E)-2-壬烯醛 18829-56-6 黄瓜味,青草味 0.19 11 10 苯乙醛 122-78-1 蜂蜜,甜香 6.3 8 11 2-戊基呋喃 3777-69-3 青草味,黄油味 5.8 7 12 苯甲醛 100-52-7 焦糖香,苦杏仁 24 5 13 辛醛 124-13-0 青草香,脂肪香 0.58 4 14 壬醛 124-19-6 柑橘香,青草香 1.1 4 15 α-松油醇 98-55-5 薄荷香,脂肪香 4.6 4 16 1-庚烯-3-酮 2918-13-0 铁锈味 0.04 3 17 2-异丁基噻唑 18640-74-9 番茄叶味 3.5 3 18 己醛 66-25-1 青草香,脂肪香 5 2 19 β-环柠檬醛 432-25-7 薄荷香 3 2 20 仲辛酮 111-13-7 汽油味,肥皂味 5 2 21 (E)-2-辛烯醛 2548-87-0 青草香,脂肪香 3 1 22 香叶醇 106-24-1 玫瑰,天竺葵 2.5 1 结合表3中化合物的浓度以及表4中的阈值信息可知,大马士酮、β-紫罗酮、芳樟醇这几种化合物在冷破番茄酱中的OAV要显著高于热破样品,因此冷破工艺可以最大限度保留新鲜番茄的果香、花香以及甜香等风味特征;而热破番茄酱中二甲基三硫的OAV更高,因此热破工艺更容易产生蒸煮风味。
Kelebek等[13]通过溶剂辅助蒸发提取(SAFE)的方法萃取番茄酱中的挥发性风味化合物,并进行稀释分析,确定出冷破、热破番茄酱的香气活性化合物为甲基庚烯酮(FD=1024)和糠醛(FD=512)。这与本文的研究结果有所差异,这可能是由于香气化合物萃取方法的不同所导致的。
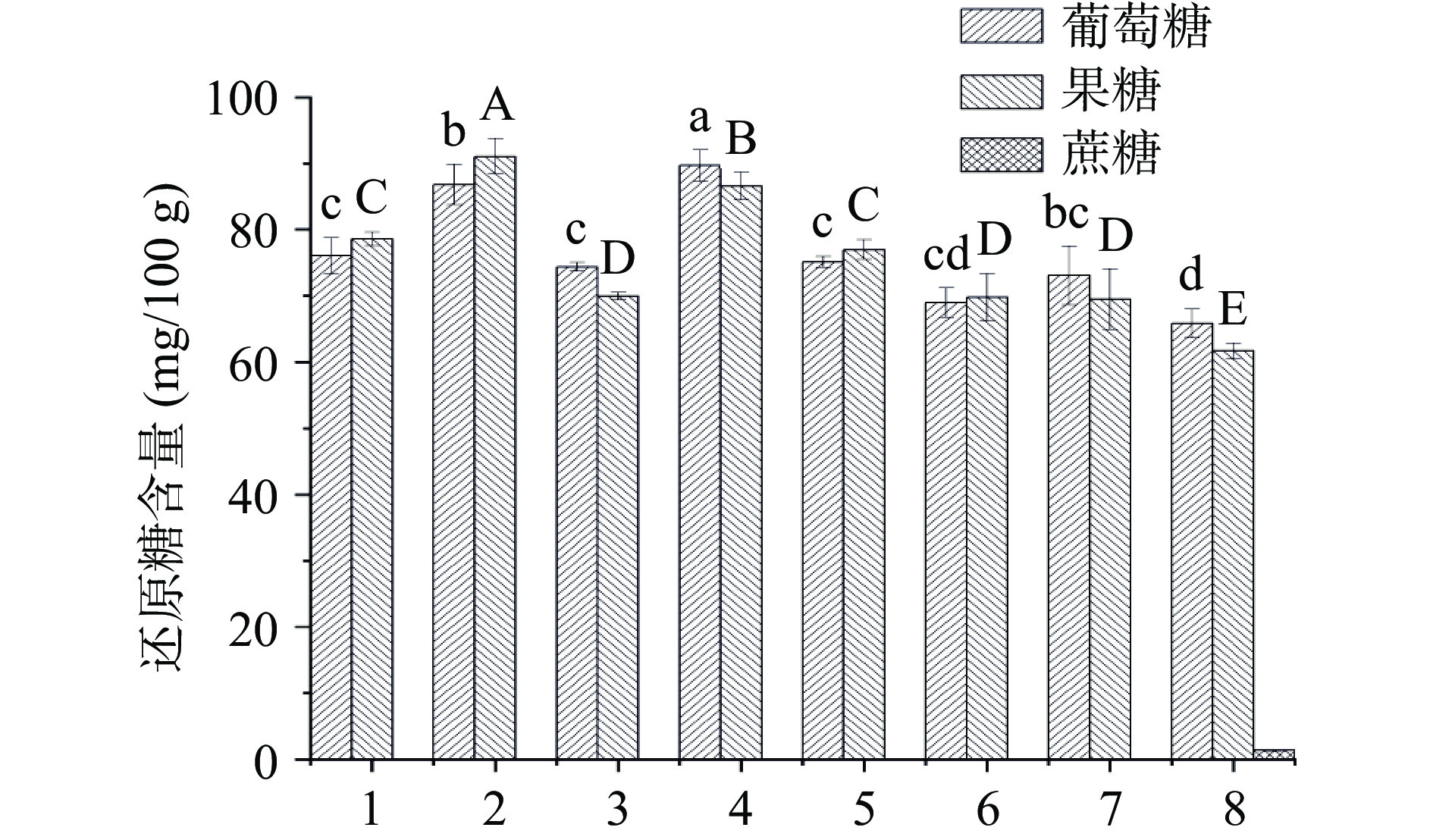
2.3 番茄酱中还原糖含量分析
在番茄酱中还原糖含量的鉴定结果中发现,番茄酱主要含有果糖及葡萄糖两种糖,大部分番茄酱样品中不含有蔗糖,这与之前报道的研究结果相一致[30]。由图2可以看出,冷破处理的番茄酱中果糖和葡萄糖的含量基本高于热破处理的番茄酱,但是3号样品显示出一定的差异性,这一现象可能是其番茄原料本身的差异所导致的。Kelebek等[4]的研究显示冷破处理与热破处理的番茄酱之间的还原糖含量并不存在显著性差异,这可能是由于番茄的个体差异导致的。
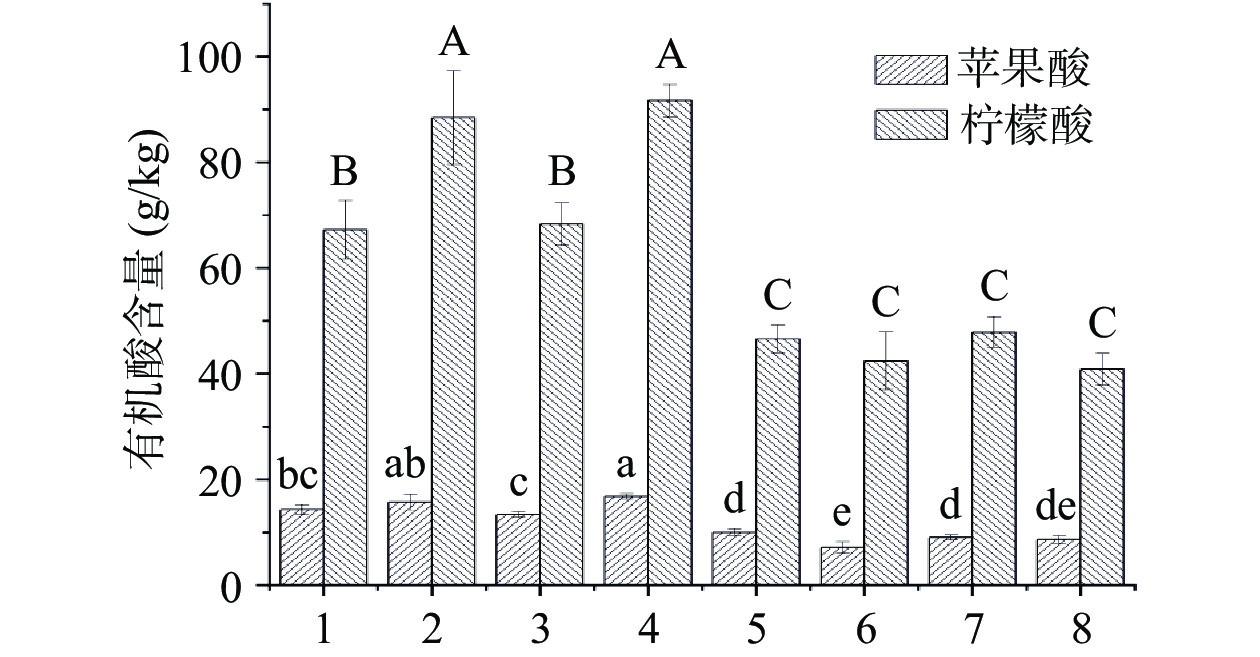
2.4 番茄酱中有机酸含量分析
柠檬酸和苹果酸是番茄酱中主要的两种有机酸,柠檬酸被认定是番茄中最丰富的有机酸,是番茄总酸的最主要的贡献物质,同时,番茄酱加工生产过程总酸的降低被认为主要是由于柠檬酸的损失所致。通过高效液相色谱对8种番茄酱中的苹果酸、柠檬酸进行定性、定量分析,由图3可以看出,对比发现冷破处理的番茄酱中苹果酸、柠檬酸的含量较高,而热破处理的番茄酱样品中的含量较低并且存在着明显的差异,这一结果与Kelebek等[4]的研究结果相一致。同时,观察发现破碎温度最高的样品8号中苹果酸、柠檬酸含量均处于最低值,同样印证了加热蒸发能够造成机酸含量的损失。
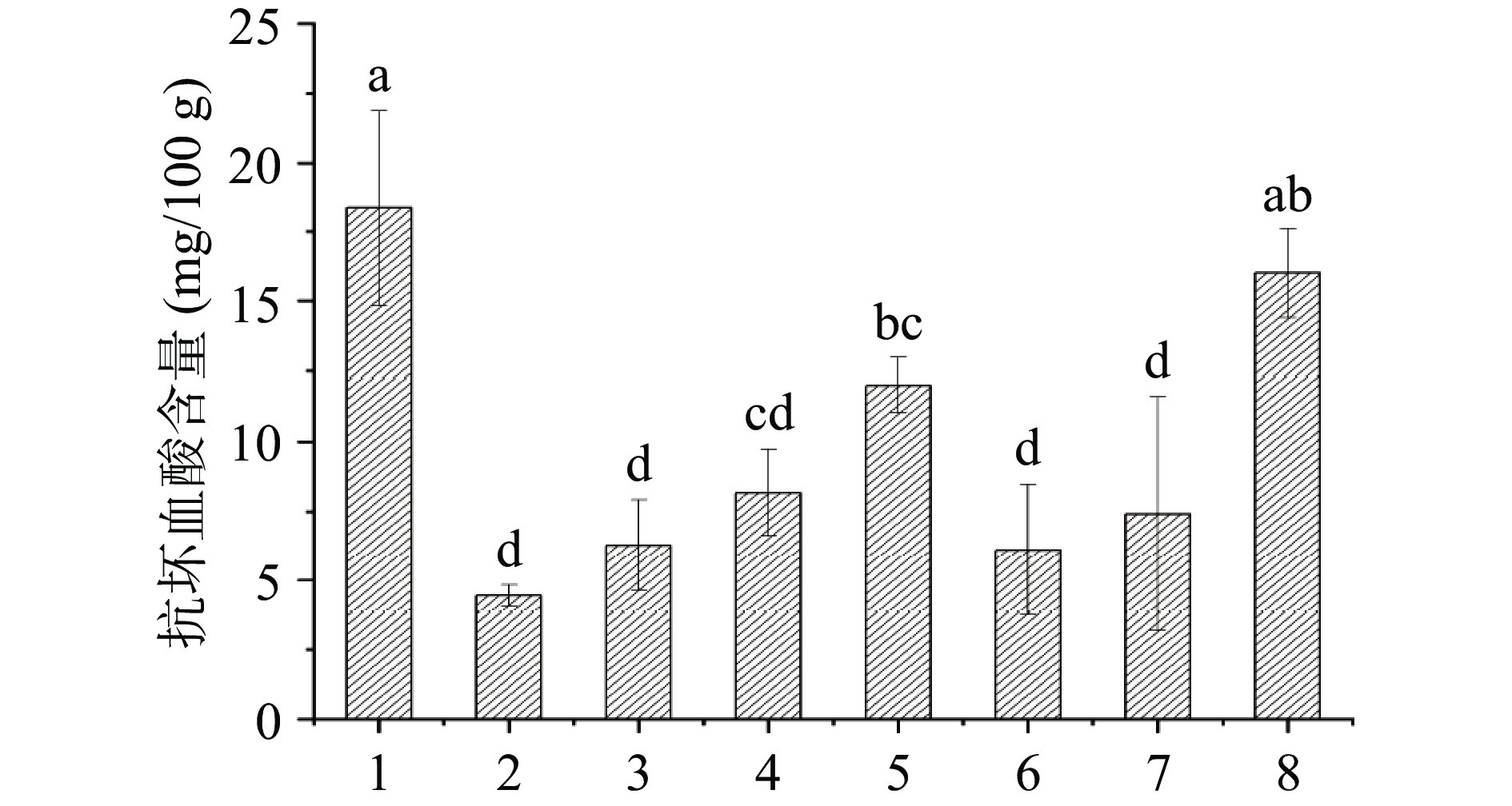
2.5 番茄酱中抗坏血酸含量分析
抗坏血酸是番茄中主要的抗氧化剂,对人体健康具有益处,由图4可以看出,8种不同加工因素下的番茄酱中,样品1中含有的抗坏血酸的含量最高,而样品2号的抗坏血酸的含量最低,由上述数据并没有发现破碎方式与抗坏血酸含量之间具有明显关系,导致这一现象的原因可能是各个样品的生产加工存在一定差异。由于抗坏血酸对于各个生产加工过程较为敏感,因此,在番茄酱的加工生产过程中抗坏血酸很容易被破坏。Gahler等[31]研究发现热处理、均质、杀菌及装瓶等连续加工过程均会对抗坏血酸的含量造成损失,在这些过程中抗坏血酸发生氧化或者热降解,损失率可达56%[32]。
2.6 番茄酱果胶含量分析
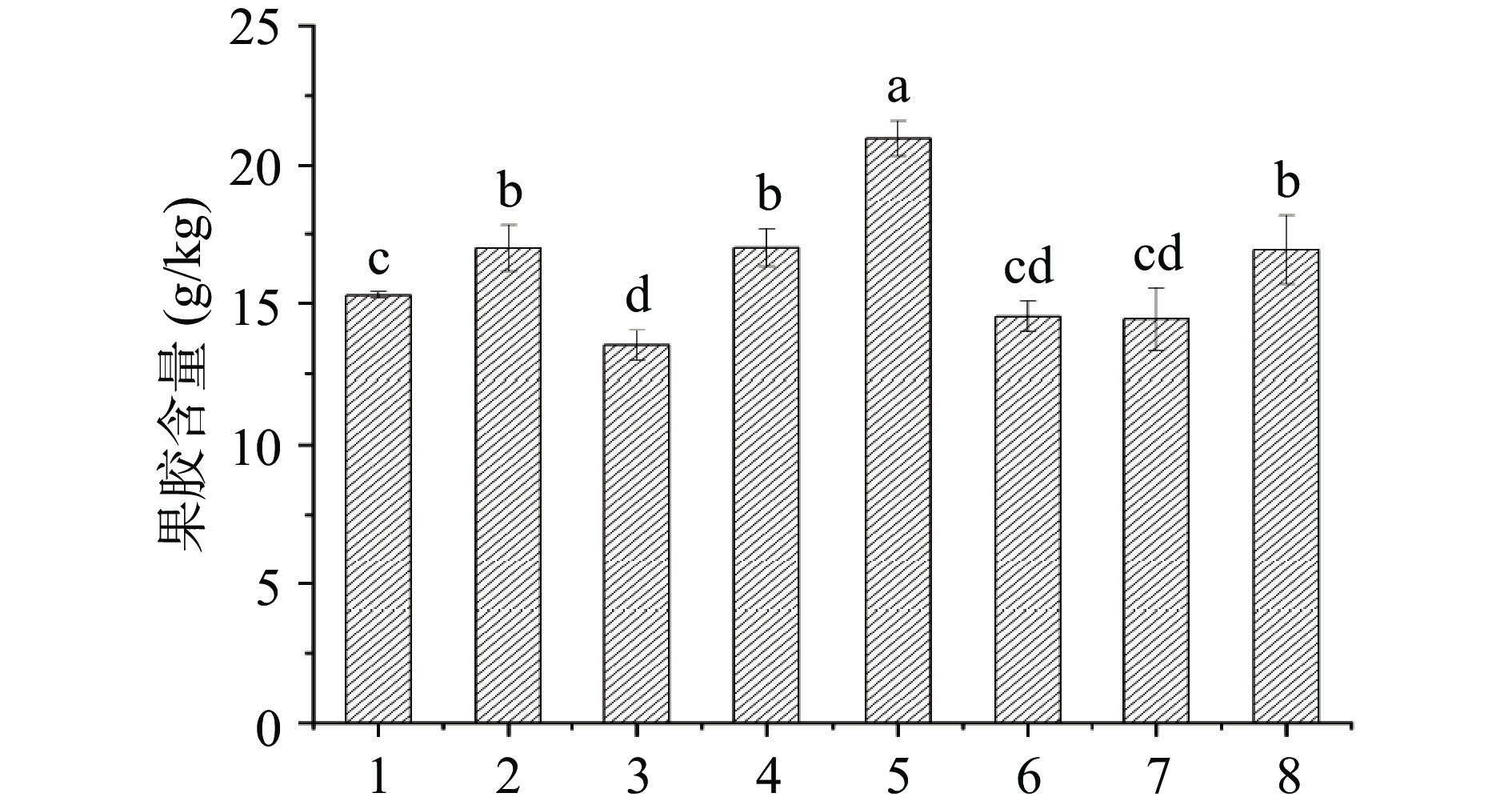
果胶的本质是一种多糖聚合物,普遍存在与植物的根、茎、叶以及果实当中,本研究对不同加工因素下番茄酱中果胶进行测定,由图5发现经热破处理的番茄酱中的果胶含量较高,而冷破处理的番茄酱中果胶的含量较低,这可能是由于热破处理的温度在85 ℃以上,番茄中果胶酶在高温下被灭活,从而阻止了果胶降解,而在65 ℃冷破处理的温度下,果胶酶刚好保持着较高活性,促使果胶分解形成果胶酸。
2.7 8种番茄酱的感官评价分析
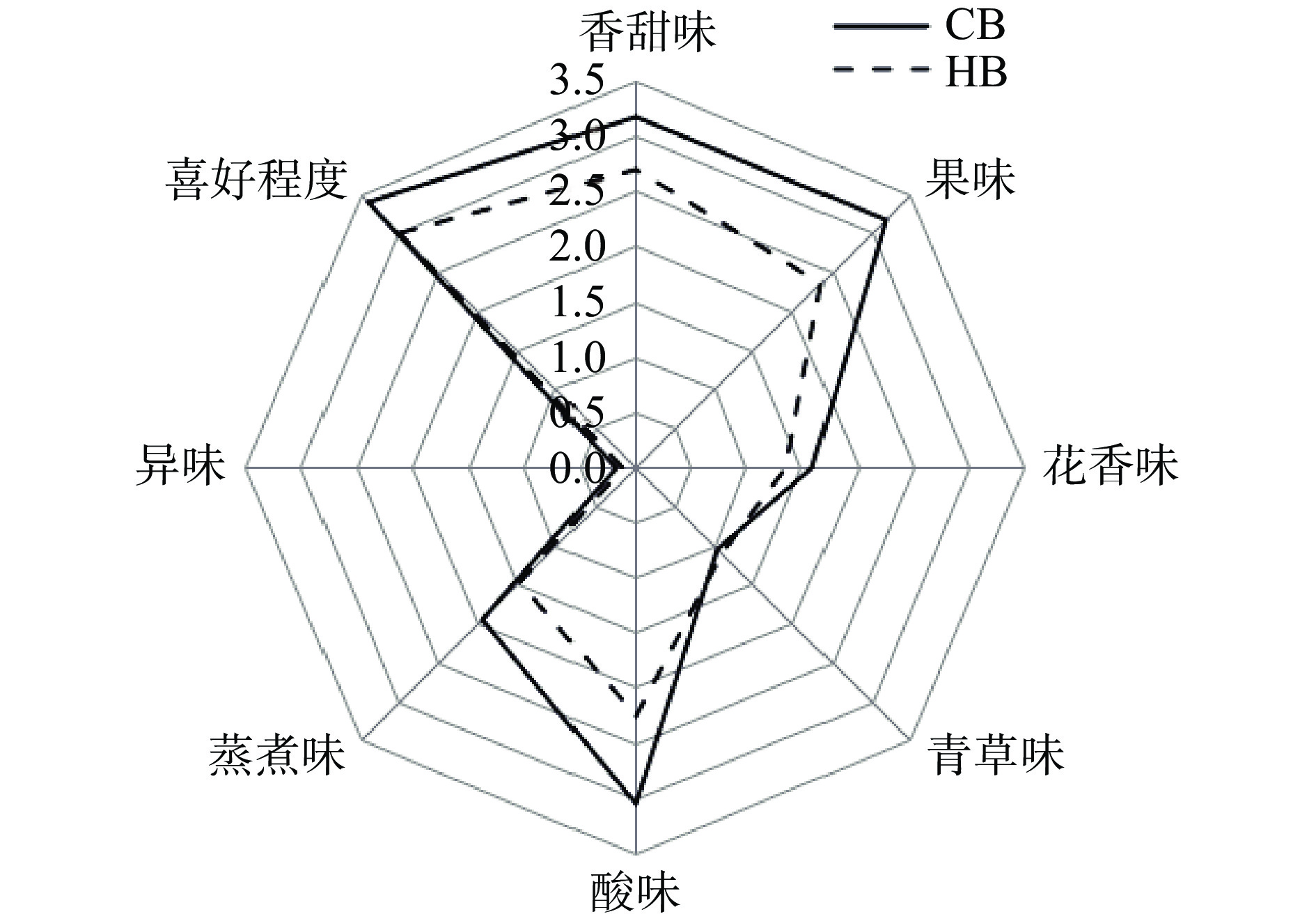
感官小组的成员对8种不同加工因素下的番茄酱的8个指标(果味、花香味、青草味、酸味、蒸煮味、异味、香甜味、喜好程度)进行评定,将1~4号样品的感官得分计算平均值作为CB番茄酱的代表值,5~8号样品的感官得分计算平均值作为HB番茄酱的代表值,绘制感官风味轮,结果如图6所示。从图6中可以看出,冷破番茄酱冷破番茄酱在香甜味、果味、花香味、酸味、蒸煮味、喜好程度方面的得分均高于热破番茄酱,其它感官属性之间差异较小,说明冷破番茄酱的风味特征更加鲜明,与2.1中冷破番茄酱的风味化合物浓度较高的结果相一致。
2.8 8种番茄酱香气活性化合物的主成分分析(PCA)
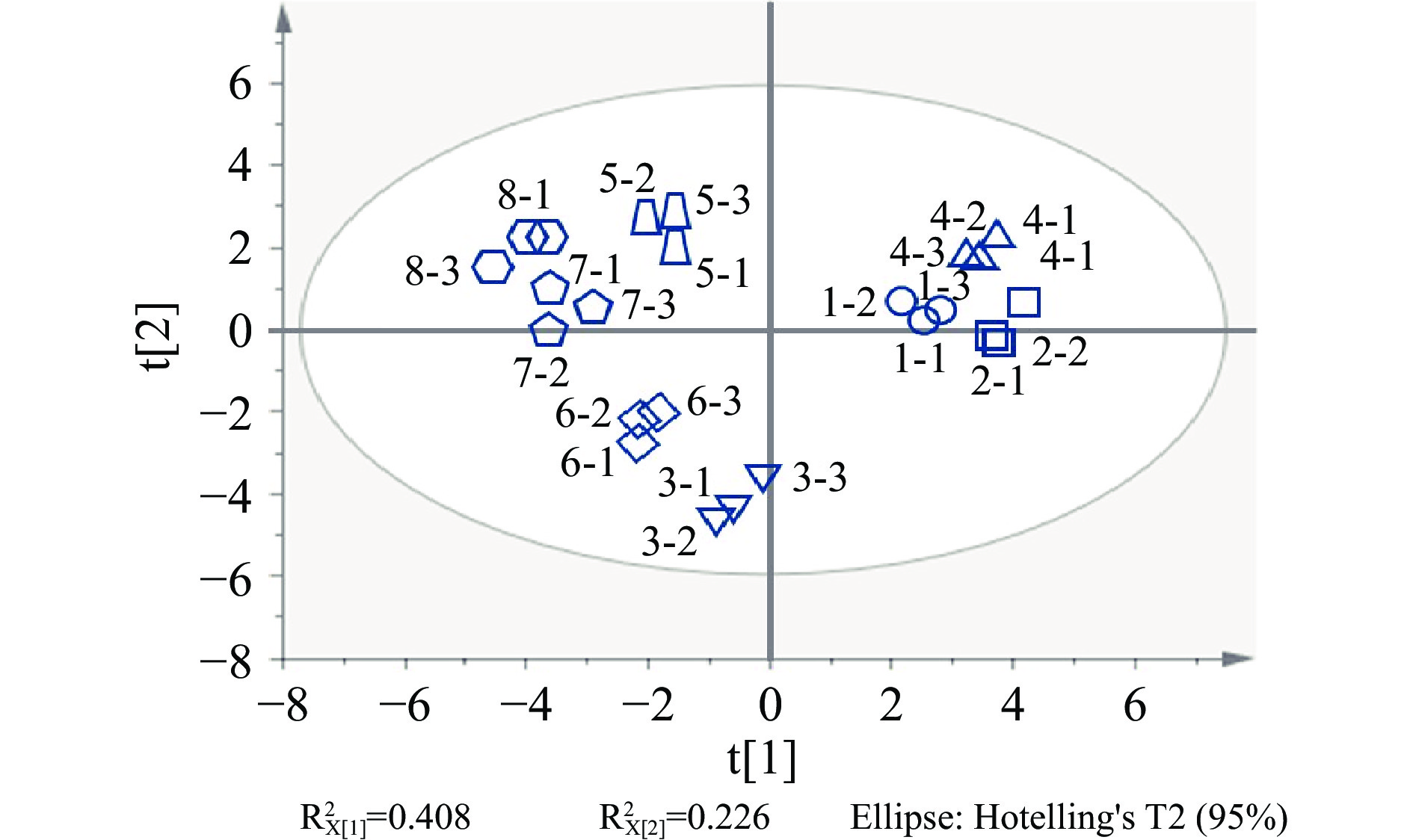
根据香气活性化合物的浓度对8种番茄酱进行主成分分析,结果如图7所示。从图7中可以看出,主成分1的方差贡献率为40.8%,主成分2的方差贡献率为22.6%,两者累计方差贡献率为63.4%,PC1和PC2在一定程度上可以反应大部分样品信息。除3号样品(CB,乌苏,28%~30%)外,冷破番茄酱(1~4号)主要位于1、4象限,热破番茄酱(5~8号)主要位于2、3象限,它们在第一主成分上可以被明显区分开,即冷破番茄酱和热破番茄酱在风味上差异显著。对于样品3未能与其它3个冷破番茄酱样品归类到一起,这可能是番茄原料的差异性导致的。
2.9 挥发性香气化合物与非挥发性成分的相关性分析
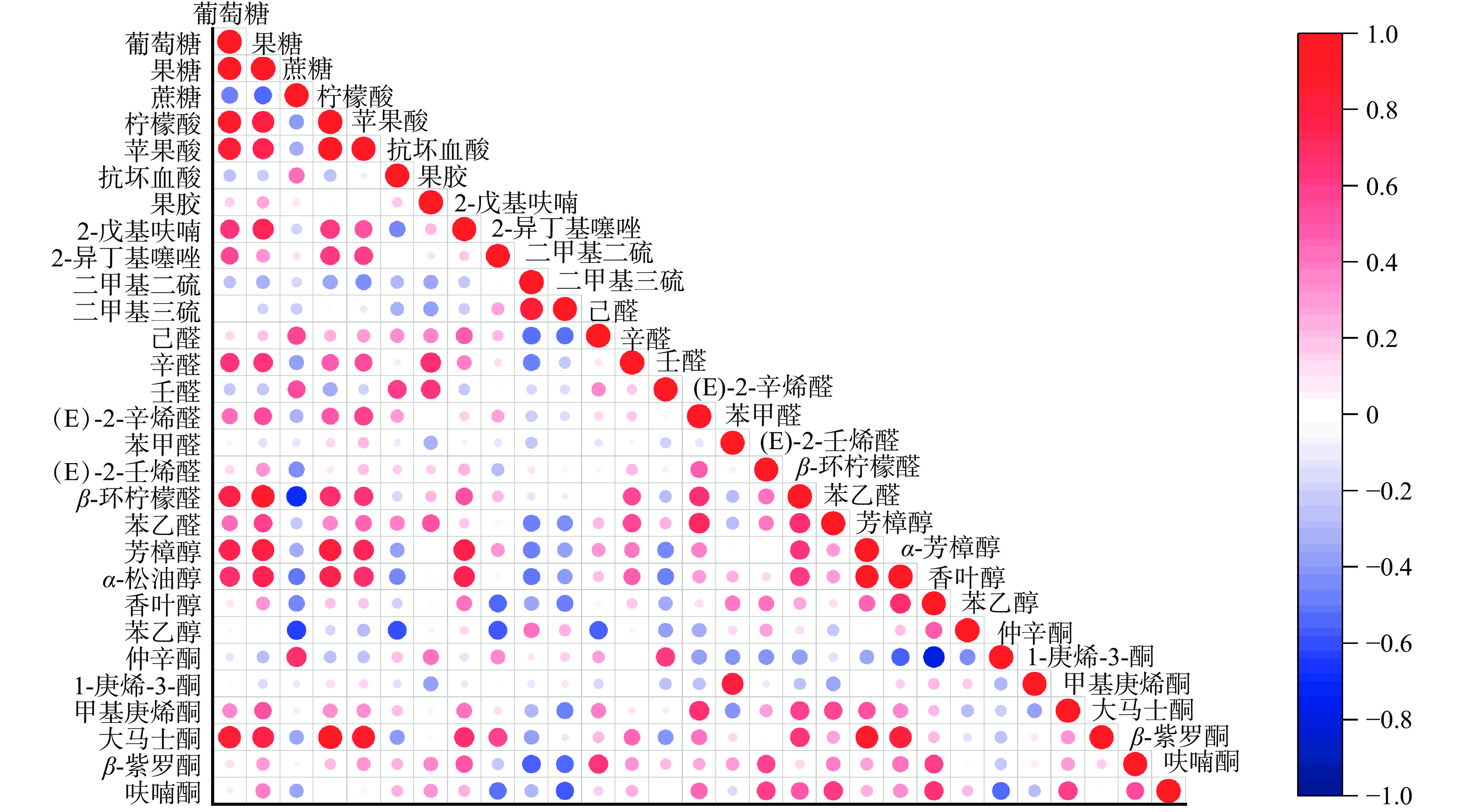
为了探究番茄酱中的香气活性化合物与糖、酸、果胶以及抗坏血酸等非挥发性成分之间的相关性,进行Pearson相关性分析,结果如图8所示。从图8中可以看出,果糖和葡萄糖与大部分醛类化合物以及酮类化合物之间表现出较强的正相关;苹果酸和柠檬酸则与醛、醇、酮类化合物表现出正相关,其中与芳樟醇、大马士酮的相关性最强;抗坏血酸与苯乙醇、芳樟醇、α-松油醇之间表现出负相关;果胶与含硫化合物之间存在负相关,与己醛、辛醛、壬醛化合物之间存在正相关。对于香气活性化合物而言,β-环柠檬醛、苯乙醛、芳樟醇、α-松油醇、大马士酮、2-戊基呋喃、2-异丁基噻唑与非挥发性化合物之间的相关性较强,推测这几种香气活性化合物与非挥发性组分之间可能存在一定的相互作用。
3. 结论
通过SPME-GC-MS技术对8种冷破、热破番茄酱中的挥发性成分进行鉴定分析,计算OAV确定番茄酱中的香气活性化合物。结果表明,8个番茄酱品种中共鉴定出61种挥发性风味化合物,包括醛类、醇类、酮类、酸类、烯烃类、杂环类、苯及其衍生物以及含硫化合物,其中22种为香气活性化合物,大马士酮(OAV=7276)贡献最大,其次是β-紫罗酮(OAV=1734),苯乙醇(OAV=957)、二甲基三硫(OAV=948)以及芳樟醇(OAV=592)。不同破碎方法对番茄酱的风味影响较大,热破处理由于较高的破碎温度导致一些酶活力下降,从而使一些化合物的生物合成途径受阻,因此热破番茄酱的风味较差。冷破热破的处理方式也会对番茄酱中的还原糖、有机酸、抗坏血酸、果胶等非挥发性组分的含量产生影响,通过相关性分析发现,某些香气活性化合物与这些非挥发性成分之间相关性较高,它们之间可能存在一定的相互作用,这些将成为以后的重点研究方向。本文为番茄酱加工方法的改善以及风味品质的提升提供了一定的理论依据。
-
表 1 8种番茄酱的信息参数
Table 1 Information parameters of eight kinds of tomato paste
样品编号 产地 固形物含量 破碎方式 1 昌吉 32%~34% CB 2 昌吉 36%~38% CB 3 乌苏 28%~30% CB 4 乌苏 36%~38% CB 5 昌吉 30%~32% HB 6 乌苏 28%~30% HB 7 乌苏 30%~32% HB 8 昌吉 28%~30% SHB 表 2 番茄酱的感官评价标准
Table 2 Sensory evaluation criteria for tomato pastes
项目 感官得分(分) 0 1 2 3 4 5 青草味 无 极微 轻微 中等 强 极强 果味 花香味 青草味 酸味 蒸煮味 异味 喜好程度 表 3 8种番茄酱中挥发性风味组分
Table 3 Volatile components in eight tomato paste
序号 化合物名称 RI值 化合物浓度(ng/g) 1号 2号 3号 4号 5号 6号 7号 8号 醛类 1 己醛 1084 5.04±2.63b 9.14±0.68a 1.57±0.41cd 3.18±0.84bc 3.43±0.92bc − − 9.44±1.52a 2 辛醛 1280 0.75±0.06d 1.46±0.13c 0.96±0.08d 2.11±0.10b 2.53±0.65a − − − 3 2,6-二甲基-5-庚烯醛 1389 − − − 2.75±0.31 − − − − 4 (E)-2-庚烯醛 1342 − 3.12±0.31 − − − − − − 5 壬醛 1385 3.17±0.4b 2.33±0.31bc 2.23±0.28bc 2.90±0.13bc 4.64±1.5abc 1.83±0.10c 2.92±0.19bc 4.66±0.15a 6 (E)-2-辛烯醛 1345 3.55±0.53a 2.47±0.08b 1.78±0.29c 2.61±0.26b 1.89±0.32c 1.79±0.13c 1.94±0.03c 1.65±0.04c 7 糠醛 1455 18.46±0.97d 78.99±2.43a 25.16±0.81c 56.95±1.36b 8.32±0.30f 6.56±0.00f 10.86±0.31e 7.40±0.44f 8 苯甲醛 1495 121.88±8.61b 81.15±20.51b 574.08±208.93a − 88.00±4.97b − − 49.78±3.29b 9 (E)-2-壬烯醛 1521 2.61±0.18a 2.06±0.13b 0.94±0.35c − 2.05±0.32b − 1.83±0.25b − 10 β-环柠檬醛 1598 4.48±0.36b 5.03±0.16a 1.55±0.34e 4.98±0.45a 3.47±0.05c 2.77±0.02d 2.70±0.16d − 11 苯乙醛 1625 55.12±7.11a 41.42±1.87b 25.03±3.59c 47.51±5.8ab 49.93±8.16ab 30.7±1.43c 26.13±2.67c 30.18±2.59c 12 2,3-二氢-2,2,6-三甲基苯甲醛 1198 − 5.14±0.12b 2.44±0.07d 8.52±0.38a 2.39±0.23d 1.84±0.05e 2.98±0.07c − 13 (E)-2-癸烯醛 1647 − − − − 2.16±0.51 − − − 14 4-乙基苯甲醛 1719 2.99±0.66a 2.61±0.10a 1.21±0.08c 2.80±0.54a 1.56±0.05bc 1.48±0.03bc − 1.95±0.17b 15 柠檬醛 1720 7.89±1.28b 4.37±1.45c 3.49±0.30c − 7.33±1.29b 9.51±1.31a 4.42±0.48c − 16 5-甲基-2-噻吩甲醛 1785 − 0.70±0.16b 1.38±0.30a 1.56±0.09a − 1.56±0.05a 0.74±0.00b − 小计 225.94±10.52b 240±21.14b 641.81±206.22a 135.87±6.43bc 177.7±12.64bc 58.15±1.24c 54.51±2.66c 105.06±4.91bc 醇类 1 己醇 1360 − − − − 2.22±0.31 − − − 2 2-乙基己醇 1474 0.98±0.18b − − − 1.44±0.15a − − − 3 芳樟醇 1537 81.13±7.08c 130.3±8.8a 81.4±3.82c 108.52±4.76b 61.93±2.35d 81.71±1.01c 45.24±3.98e 56.57±2.20d 4 脱氢芳樟醇 1583 2.44±0.2cd 6.22±1.13b 3.77±0.99c 10.32±0.51a 1.78±0.16d − 2.51±0.15cd − 5 α-松油醇 1692 10.94±0.71c 18.83±0.99a 13.42±0.14b 13.34±0.7b 10.2±0.9c 11.47±0.47c 5.24±0.65d 5.61±0.18d 6 3-甲硫基丙醇 1701 − 9.37±0.62a 2.79±0.14c 2.83±0.22c 6.84±0.74b 6.04±0.23b 2.13±0.04d − 7 橙花醇 1804 1.09±0.12b 1.72±0.08a − − 1.17±0.13b − − − 8 2-(4-甲基苯基)丙-2-醇 1844 0.86±0.04b 0.82±0.04b 0.54±0.05c 1.08±0.02a − − − − 9 香叶醇 1854 2.00±0.57c 2.84±0.17a 2.40±0.13b − 1.84±0.07c 2.12±0.00bc − − 10 十二醇 1970 − − − − − − 0.24±0.42 − 11 苯乙醇 1883 4.16±0.23d 11.21±0.38c 11.83±0.72c 3.56±0.08d 13.62±0.88ab 14.35±0.05a 13.05±0.93b − 小计 103.6±7.98d 181.32±10.19a 116.15±5.24c 139.66±4.62b 101.04±2.66d 116.34±1.42c 68.42±4.25e 62.18±2.13e 酮类 1 2-庚酮 1174 − 11.00±1.99 − − − − − − 2 仲辛酮 1285 0.61±0.08f 2.83±0.27d 1.32±0.15ef 6.81±0.69b 5.79±0.57c 1.79±0.27e 6.22±0.33bc 10.12±0.77a 3 1-庚烯-3-酮 1290 − − 0.12±0.11 − − − − − 4 甲基庚烯酮 1336 635.53±45.11a 609.91±26.35a 277.55±53.12d 494.56±78.92b 402.52±59.97bc 446.9±75.43b 352.94±70.99cd 431.25±69.43bc 5 对甲基苯乙酮 1759 7.56±0.59b 7.90±0.09b 4.69±0.54e 9.95±0.56a 6.11±0.43c 6.02±0.01cd 5.50±0.46cde 5.14±0.78de 6 大马士酮 1813 8.09±0.81c 14.21±0.83a 9.93±0.68b 14.55±0.35a 4.62±0.08e 5.47±0.45d 4.75±0.6de 4.26±0.28e 7 香叶基丙酮 1840 16.31±2.1a 18.01±0.24a 14.48±1.28b 13.45±0.75bc 11.88±0.55cd 13.1±0.49bc 12.18±0.82cd 10.83±0.94d 8 β-紫罗酮 1913 0.89±0.04b 1.21±0.07a 0.67±0.02c − 0.90±0.09b − − 0.61±0.11c 9 呋喃酮 2064 0.61±0.06a 0.45±0.04b − − 0.49±0.03b 0.37±0.02c − − 10 法尼基丙酮 2083 1.47±0.23b 1.47±0.07b 3.45±0.48a 0.91±0.05c 0.58±0.05cd 0.29±0.03de − − 小计 671.07±45.16a 666.98±25.78a 312.2±51.98 540.24±79.96b 432.88±59.81bc 515.48±89.19b 381.59±70.46 462.21±70.11bc 烃类 1 (+)-柠檬烯 1178 1.38±0.54d 2.79±0.27bc 1.36±0.44d 4.36±0.69a 2.68±0.26c 2.33±0.56cd 2.35±0.58cd 3.76±1.03ab 2 紫苏烯 1295 1.19±0.19cd 1.63±0.1bc 1.07±0.09d 2.31±0.44a 2.29±0.48a 1.86±0.06b 1.59±0.09bc 1.64±0.02bc 小计 2.57±0.71d 4.42±0.3bc 2.42±0.47d 6.67±0.55a 4.97±0.75bc 4.18±0.6c 3.93±0.49c 5.4±1.00b 酸类 1 乙酸 1450 34.98±3.94a 36.00±0.87a 17.82±2.90c 23.29±1.03b 24.86±0.87b 14.32±1.09c 22.9±2.99b 10.18±0.32d 2 丙酸 1525 − − − − 2.91±0.34 − − − 3 丁酸 1652 2.23±0.18b − − − 2.88±0.10a − − − 4 异戊酸 1665 9.16±0.82e 20.11±0.35c 12.49±0.99de 33.68±2.96a 26.11±3.43b 12.32±0.8de 13.1±2.50d 23.87±1.05b 5 辛酸 2083 2.95±0.24a 2.43±0.13ab 2.33±0.06b 2.75±0.28ab 1.61±0.05c − 1.39±0.31c 2.92±0.69a 6 壬酸 2164 8.46±1.08a 4.34±0.88b 1.57±0.34cd 4.2±0.77b 2.31±0.62c 0.93±0.10d 0.96±0.12d 3.74±0.14b 小计 57.78±3.34b 62.88±1.20ab 34.2±3.18d 63.92±4.09a 60.69±3.81ab 28.01±0.89e 38.35±3.84cd 40.71±0.32c 杂环类化合物 1 2-戊基呋喃 1240 6.33±1.44e 42.88±2.14a 9.14±0.81cd 14.99±2.06b 11.07±0.19c 6.97±0.39de 6.74±1.13e 6.66±0.34e 2 2-乙酰基呋喃 1490 3.65±0.35cd 18.95±1.22a 6.99±0.31b 19.5±0.76a 4.38±0.12c 3.17±0.11d 3.75±0.27cd 1.91±0.14e 3 2-异丁基噻唑 1391 3.37±1.24b 4.19±1.32b 3.12±0.32b 9.49±1.51a − − 4.50±0.07b 4.58±0.33b 4 2-乙基-5-甲基吡嗪 1402 − 0.65±0.01 − − − − − − 5 3-甲基吲哚 1500 − − − − − − − 0.06±0.05 小计 13.35±0.62de 66.66±2.93a 19.25±0.92c 43.98±3.68b 15.45±0.27d 10.16±0.35e 14.99±1.29d 13.21±0.36de 苯及其衍生物 1 甲苯 1042 10.01±1.57c 15.85±0.91b 6.66±0.59c 24.88±3.87a 24.09±4.32a 18.64±1.37b 20.39±5.53ab 6.13±1.89c 2 间二甲苯 1150 3.40±0.52d 6.70±0.57c 2.91±0.30d − 10.39±0.90a − − 8.61±1.50b 3 4-异丙基甲苯 1261 1.96±0.28b 3.64±0.33b 2.85±0.46b 8.51±2.29a 3.25±0.06b 2.40±0.43b 3.19±0.79b 3.18±0.30b 4 1,2,4-三甲基苯 1293 2.24±0.27a − − − 1.71±0.42b 1.26±0.06c 1.72±0.04b 1.42±0.01bc 5 烯丙苯酚 1380 − − − − − − 1.41±0.02 − 6 对甲酚 2080 − − − − − 0.11±0.00 − 0.27±0.01 7 丁香酚 2163 0.32±0.05b − 0.25±0.01c 0.23±0.02c − − 0.27±0.04bc 0.68±0.09a 8 4-乙基苯酚 2185 − − − − − 0.25±0.02 − − 9 4-乙烯基-2-甲氧基苯酚 2230 5.66±0.73a 3.66±0.29b 2.79±0.29c 2.69±0.18c 2.61±0.34c 2.4±0.11c 1.46±0.20d 1.24±0.07d 小计 23.59±2.00bc 29.85±1.39b 15.47±0.12d 36.31±3.52a 42.04±5.84a 24.33±1.57bc 28.43±6.18b 21.52±0.59c 含硫化合物 1 二甲基二硫 1058 − − 0.17±0.00b − − 1.38±0.22 4.71±1.12a − 2 二甲基三硫 1366 − − 1.57±0.25b 1.36±0.24b − − 4.74±0.64a − 小计 − − 1.74±0.25b 1.36±0.24b − 1.36±0.16b 9.45±1.75a − 总计 548.95±27.47ab 626.06±17.18a 571.62±98.94a 484.01±40.76bc 417.38±25.18cd 379±44.94de 299.84±37.26e 355.15±36.37de 注:不同字母代表风味化合物含量存在显著性差异(P<0.05)。 表 4 番茄酱中的香气活性化合物汇总
Table 4 Aroma active compounds in tomato paste
序号 化合物名称 CAS 风味特征 阈值(ng/g) 最高OAV 1 大马士酮 23726-93-4 苹果香,花香 0.002 7276 2 β-紫罗酮 79-77-6 花香,甜香 0.0007 1734 3 苯乙醇 22258.00 甜香,丁香花 0.015 957 4 二甲基三硫 3658-80-8 卷心菜,硫磺 0.005 948 5 芳樟醇 78-70-6 薰衣草,花香 0.22 592 6 二甲基二硫 624-92-0 洋葱,卷心菜 0.16 29 7 呋喃酮 3658-77-3 奶油,甜香 0.03 20 8 甲基庚烯酮 110-93-0 蘑菇味,蒸煮味 68 9 9 (E)-2-壬烯醛 18829-56-6 黄瓜味,青草味 0.19 11 10 苯乙醛 122-78-1 蜂蜜,甜香 6.3 8 11 2-戊基呋喃 3777-69-3 青草味,黄油味 5.8 7 12 苯甲醛 100-52-7 焦糖香,苦杏仁 24 5 13 辛醛 124-13-0 青草香,脂肪香 0.58 4 14 壬醛 124-19-6 柑橘香,青草香 1.1 4 15 α-松油醇 98-55-5 薄荷香,脂肪香 4.6 4 16 1-庚烯-3-酮 2918-13-0 铁锈味 0.04 3 17 2-异丁基噻唑 18640-74-9 番茄叶味 3.5 3 18 己醛 66-25-1 青草香,脂肪香 5 2 19 β-环柠檬醛 432-25-7 薄荷香 3 2 20 仲辛酮 111-13-7 汽油味,肥皂味 5 2 21 (E)-2-辛烯醛 2548-87-0 青草香,脂肪香 3 1 22 香叶醇 106-24-1 玫瑰,天竺葵 2.5 1 -
[1] TORBICA A, BELOVIC M, MASTILOVIC J, et al. Nutritional, rheological, and sensory evaluation of tomato ketchup with increased content of natural fibres made from fresh tomato pomace[J]. Food and Bioproducts Processing,2016,98:299−309. doi: 10.1016/j.fbp.2016.02.007
[2] 赵文启. 冷热破工艺对番茄酱贮藏期间品质变化影响的研究[D]. 石河子: 石河子大学, 2018 ZHAO W Q. Effects of cold break process and hot break process on quality change of tomato paste during storage[D]. Shihezi: Shihezi University, 2018.
[3] LENUCCI M S, DURANTE M, ANNA M, et al. Possible use of the carbohydrates present in tomato pomace and in byproducts of the supercritical carbon dioxide lycopene extraction process as biomass for bioethanol production[J]. Journal of Agricultural and Food Chemistry,2013,61(15):3683−3692. doi: 10.1021/jf4005059
[4] KELEBEK H, SELLI S, KADIROGLU P, et al. Bioactive compounds and antioxidant potential in tomato pastes as affected by hot and cold break process[J]. Food Chemistry,2017,220:31−41. doi: 10.1016/j.foodchem.2016.09.190
[5] GOODMAN C L, FAWCETT S, BARRINGER S A. Flavor, viscosity, and color analyses of hot and cold break tomato juices[J]. Journal of Food Science,2010,67(1):404−408.
[6] SCHIERLE J, BRETZEL W, BUEHLER I, et al. Content and isomeric ratio of lycopene in food and human blood plasma[J]. Food Chemistry,1997,59(3):459−465. doi: 10.1016/S0308-8146(96)00177-X
[7] GAO R P, WU Z, MA Q, et al. Effects of breaking methods on the viscosity, rheological properties and nutritional value of tomato paste[J]. Foods,2021,10(10):2395. doi: 10.3390/foods10102395
[8] 邸太菊, 李学杰, 李健, 等. 猕猴桃货架期品质及关键风味物质分析[J]. 食品科学技术学报,2020,38(3):51−59. [DI T J, LI X J, LI J, et al. Analysis on quality and key flavor compounds of kiwifruit during shelf life[J]. Journal of Food Science and Technology,2020,38(3):51−59. doi: 10.3969/j.issn.2095-6002.2020.03.007 [9] 李学杰, 宋焕禄, 王中江, 等. 基于SPME-GC-O-MS及质构分析对烤牛肉和植物蛋白肉的感官品质探究[J]. 食品工业科技,2021,42(12):8−18. [LI X J, SONG H L, WANG Z J, et al. Research on sensory quality of roasted beef and plant-based meat analogues based on SPME-GC-O-MS and texture analysis[J]. Science and Technology of Food Industry,2021,42(12):8−18. doi: 10.13386/j.issn1002-0306.2021030081 [10] SERVILI M, SELVAGGINI R, TATICCHI A, et al. Relationships between the volatile compounds evaluated by solid phase microextraction and the thermal treatment of tomato juice: Optimization of the blanching parameters[J]. Food Chemistry,1999,71(3):407−415.
[11] MARTHA P T. Flavor of tomato and tomato products[J]. Food Reviews International,2009,2(3):309−351.
[12] BUTTERY R G, TERANISHI R, LING L C, et al. Quantitative and sensory studies on tomato paste volatiles[J]. Journal of Agricultural and Food Chemistry,1990,38(1):336−340. doi: 10.1021/jf00091a074
[13] KELEBEK H, KESEN S, SONMEZDAG A S, et al. Characterization of the key aroma compounds in tomato pastes as affected by hot and cold break process[J]. Journal of Food Measurement and Characterization,2018,12(4):2461−2474. doi: 10.1007/s11694-018-9863-8
[14] BOLAND A B, DELAHUNTY C M, RUTH S. Influence of the texture of gelatin gels and pectin gels on strawberry flavour release and perception[J]. Food Chemistry,2006,96(3):452−460. doi: 10.1016/j.foodchem.2005.02.027
[15] 付晓伟, 吴晓, 姜莉莉, 等. 紫外分光光度法测定水果中维生素C含量[J]. 山东化工,2020,49(24):3. [FU X W, WU X, JIANG L L, et al. Deter mination of vitamin C in fruits by UV spectrophotometry[J]. Shandong Chemical Industry,2020,49(24):3. doi: 10.3969/j.issn.1008-021X.2020.24.039 [16] 李晓, 王文亮, 王月明, 等. 外源性果胶甲酯酶对低盐腌渍黄瓜质构性质的影响[J]. 食品科学技术学报,2018,36(6):88−94. [LI X, WANG W L, WANG Y M, et al. Effects of exogenous pectin methylesterase on texture and texture properties of low-salt pickled cucumber[J]. Journal of Food Science and Technology,2018,36(6):88−94. doi: 10.3969/j.issn.2095-6002.2018.06.013 [17] 随新平, 朱庆珍, 张宁, 等. 阿胶的香气活性物质分析[J]. 食品科学技术学报,2021,39(3):89−100. [SUI X P, ZHU Q Z, ZHANG N, et al. Analysis of aroma active compounds of Ejiao[J]. Journal of Food Science and Technology,2021,39(3):89−100. doi: 10.12301/j.issn.2095-6002.2021.03.010 [18] 牟琴, 徐俐. 不同品种番茄对发酵番茄酱品质的影响[J]. 中国酿造,2018,37(10):130−134. [MOU Q, XU L. Effects of different tomato varieties on the quality of fermented tomato paste[J]. China Brewing,2018,37(10):130−134. doi: 10.11882/j.issn.0254-5071.2018.10.025 [19] 刘欢, 张德权, 王振宇, 等. 北京烤鸭腿皮与腿肉关键挥发性风味物质解析[J]. 中国食品学报,2021,21(2):308−318. [LIU H, ZHANG D Q, WANG Z Y, et al. Analysis of aroma compounds in leg skin and leg meat from Beijing roasted duck[J]. Journal of Chinese Institute of Food Science and Technology,2021,21(2):308−318. doi: 10.16429/j.1009-7848.2021.02.037 [20] 范霞, 崔心平. 基于HS-SPME-GC-MS和电子鼻技术研究不同肉质桃子采后贮藏期的香气成分[J]. 食品科学,2021,42(20):222−229. [FAN X, CUI X P. Analysis of aroma compounds of different peach flesh types during postharvest storage by headspace solid-phase microextraction combined with gas chromatography-mass spectrometry and electronic nose[J]. Food Science,2021,42(20):222−229. doi: 10.7506/spkx1002-6630-20201026-261 [21] KOLTUN S J, MACINTOSH A J, GOODRICH-SCHNEIDER R M, et al. Effects of thermal processing on flavor and consumer perception using tomato juice produced from florida grown fresh market cultivars[J]. Journal of Food Processing and Preservation,2021,46(1):e16164.
[22] BOUKOBZA F, DUNPHY P J, TAYLOR A J. Measurement of lipid oxidation-derived volatiles in fresh tomatoes[J]. Postharvest Biology and Technology,2001,23(2):117−131. doi: 10.1016/S0925-5214(01)00122-3
[23] 扈莹莹, 王妍, 于晶, 等. 脂肪添加量对发酵香肠脂质和蛋白质氧化及挥发性化合物形成的影响[J]. 食品科学,2019,40(18):8−14. [HU Y Y, WANG Y, YU J, et al. Effect of fat addition on lipid and protein oxidation and volatile compound formation in fermented sausages[J]. Food Science,2019,40(18):8−14. doi: 10.7506/spkx1002-6630-20181022-233 [24] 苗爱清, 吕海鹏, 孙世利, 等. 乌龙茶香气的HS-SPME-GC-MS/GC-O研究[J]. 茶叶科学,2010(S1):583−587. [MIAO A Q, LIU H P, SUN S L, et al. Aroma components of oolong tea by HS-SPME-GC-MS and GC-O[J]. Journal of Tea Science,2010(S1):583−587. doi: 10.3969/j.issn.1000-369X.2010.z1.015 [25] BHATKAR N S, SHIRKOLE S S, MUJUMDAR A S, et al. Drying of tomatoes and tomato processing waste: A critical review of the quality aspects[J]. Drying Technology,2021,39(11):1720−1744. doi: 10.1080/07373937.2021.1910832
[26] KALUA C M, ALLEN M S, BEDGOOD D R, et al. Olive oil volatile compounds, flavour development and quality: A critical review[J]. Food Chemistry,2007,100(1):273−286. doi: 10.1016/j.foodchem.2005.09.059
[27] AONO Y, ASIKIN Y, WANG N, et al. High-throughput chlorophyll and carotenoid profiling reveals positive associations with sugar and apocarotenoid volatile content in fruits of tomato varieties in modern and wild accessions[J]. Metabolites,2021,11(6):398. doi: 10.3390/metabo11060398
[28] BUTTERY R G, TERANISHI R, LING L C, et al. Quantitative studies on origins of fresh tomato aroma volatiles[J]. Journal of Agricultural and Food Chemistry,1988,36(6):1247−1250. doi: 10.1021/jf00084a030
[29] DU X F, SONG M, BALDWIN E, et al. Identification of sulphur volatiles and GC-olfactometry aroma profiling in two fresh tomato cultivars[J]. Food Chemistry,2015,171(15):306−314.
[30] SERGR Y, HEWITT J D, ROBINSON N L, et al. Sink metabolism in tomato fruit 1[J]. Plant Physiology,1988,87:727−730. doi: 10.1104/pp.87.3.727
[31] GAHLER S, OTTO K, BOHM V. Alterations of vitamin C, total phenolics, and antioxidant capacity as affected by processing tomatoes to different products[J]. Journal of Agricultural and Food Chemistry,2003,51(27):7962−7968. doi: 10.1021/jf034743q
[32] BOONPANGRAK S, LATITMANAT S, SUWANWONG Y, et al. Analysis of ascorbic acid and isoascorbic acid in orange and guava fruit juices distributed in Thailand by LC-IT-MS/MS[J]. Food Analytical Methods,2016,9(6):1616−1626. doi: 10.1007/s12161-015-0337-x
-
期刊类型引用(6)
1. 闫昱辛,何美军,李宇,袁晓曼,谭旭辉,程名,罗凯,廖璐婧. 铁皮石斛叶多糖美白和抗氧化活性. 植物研究. 2025(01): 111-118 .  百度学术
百度学术
2. 代丽丽,王景,魏许瑞,马庆亚,王娜,都治香. 基于PI3K/Akt信号通路研究灯盏花乙素对子宫内膜癌Ishikawa细胞的影响. 中国临床药理学杂志. 2024(01): 27-31 .  百度学术
百度学术
3. 张琦,包小波,田冲冲. 灯盏花乙素增强4T1乳腺癌细胞对顺铂敏感性的体内外研究. 食品工业科技. 2024(05): 331-340 .  本站查看
本站查看
4. 王佳恩,殷子喻,马莉,李双良,符德欢. 灯盏乙素抗肿瘤作用机制研究进展. 中草药. 2024(13): 4608-4621 .  百度学术
百度学术
5. 张琦,田冲冲,张洋,方晨曦,卜薇,李凤. 灯盏花乙素通过PPARγ-PGC1α-UCP1通路改善小鼠肥胖作用及机制. 药物评价研究. 2024(08): 1787-1796 .  百度学术
百度学术
6. 田冲冲,张琦,陈延绅. 基于肠道微生态探讨灯盏花乙素对乳腺癌小鼠的化疗增敏作用及其机制. 中国微生态学杂志. 2024(12): 1374-1381+1387 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:

 下载:
下载:



