Characterization of Key Aroma Compounds of Apple Slices Dried by Hot-air at Different Temperatures by GC-MS and Electronic Nose
-
摘要: 为明确富士苹果的关键香气化合物以及干燥温度对富士苹果关键香气化合物的影响,采用顶空固相微萃取气质联用(headspace solid-phase micro-extraction gas chromatography-mass spectrometer,HS-SPME-GC-MS)技术结合电子鼻对富士苹果鲜样、50、60、70和80 ℃热风干燥苹果脆片的挥发性化合物进行表征。结果表明,苹果鲜样和4种干燥样品共鉴定出64种挥发性化合物,包括酯类23种、醇类18种、醛类8种、烯烃类2种、酮类2种、内酯类3种、酸类1种、含硫化合物3种和杂环化合物4种。不同样品各类挥发性化合物的种类及含量均存在较大差异,鲜样香气化合物含量为397.059 mg/kg,不同温度热风干燥样品挥发性化合物含量由高到低分别为64.189 mg/kg(50 ℃处理)、57.703 mg/kg(80 ℃处理)、32.124 mg/kg(70 ℃处理)、32.020 mg/kg(60 ℃处理)。气味活性值(odor-active value,OAV)分析表明,苹果鲜样与热风干燥样品共有关键香气化合物8种,分别为α-法尼烯(12746.11~1597.75)、2-甲基丁酸己酯(755.62~6.90)、己醇(2988.00~168.54)、1-辛烯-3-醇(53.12~12.08)、壬醛(1534.99~47.36)、反式-2-壬烯醛(1202.98~189.38)、芳樟醇(1264.30~212.75)和6-甲基-5-庚烯-2-酮(11.27~3.90)。除此以外,热风干燥样品独有的关键香气化合物包括2-甲基-1-丁醇(32.26~7.16)、3-甲基-4-庚醇(14.39~6.90)、苯乙醇(11.11~4.67)、辛醛(211.25~84.36)、3-羟基-2-丁酮(64.57~21.86)、3-甲硫基丙醇(13.52~5.88)和2-戊基呋喃(26.44~14.88)。电子鼻分析表明鲜样与热风处理苹果脆片香气轮廓存在差异,通过主成分分析(principle component analysis,PCA)可以对鲜样和脱水苹果脆片进行有效区分。综合考虑香气、能耗,相比于50 ℃热风处理,80 ℃可以在短时间内使苹果片呈现热风脱水制品的特征性风味。因此,80 ℃热风干燥条件最佳。
-
关键词:
- 苹果脆片 /
- 热风干燥 /
- 关键香气化合物 /
- 气相色谱-质谱法(GC-MS) /
- 电子鼻 /
- 香气活性值(OAV) /
- 主成分分析(PCA)
Abstract: To clarify the key aroma compounds of Fuji apples and the influence of drying temperatures, the volatile compounds of Fuji apple slices dried by hot-air at 50, 60, 70 and 80 ℃ were characterized by head space solid-phase micro-extraction gas chromatography-mass spectrometer (HS-SPME-GC-MS) combined with electronic nose. The results showed that 64 volatile compounds were identified in fresh and four kinds of dried apple samples, including 23 esters, 18 alcohols, 8 aldehydes, 2 alkenes, 2 ketones, 3 lactones, 1 acid, 3 sulfur-containing compounds and 4 heterocyclic compounds. The differences between types and contents of volatile compounds in different samples were great. The content of aroma compounds in fresh samples was 397.059 mg/kg. Total volatile compounds contents in four hot-air dried samples from high to low were 64.189 mg/kg at 50 ℃, 57.703 mg/kg at 80 ℃, 32.124 mg/kg at 70 ℃ and 32.020 mg/kg at 60 ℃, respectively. Odor-active value (OAV) analysis showed that there were 8 key aroma compounds both in fresh apple sample and hot-air dried apple samples. They were α-farnesene (12746.11~1597.75), hexyl 2-methylbutyrate (755.62~6.90), hexanol (2988.00~168.54), 1-octene-3-ol (53.12~12.08), nonanal (1534.99~47.36), trans-2-nonenal (1202.98~189.38), linalool (1264.30~212.75) and 6-methy-5-hepten-2-one (11.27~3.90). The key aroma compounds identified in hot-air dried samples included 2-methyl-1-butanol (32.26~7.16), 3-methyl-4-heptanol (14.39~6.90), phenylethanol (11.11~4.67), octanal (211.25~84.36), 3-hydroxy-2-butanone (64.57~21.86), 3-methylthiopropanol (13.52~5.88) and 2-pentylfuran (26.44~14.88). Electronic nose analysis showed that there were differences in aroma profiles between fresh apple and apple slices dried by hot-air at different temperatures. The fresh samples and dried apple slices could be effectively distinguished by principle component analysis (PCA). Considering aroma and energy consumption, 80 ℃ hot air dehydration apple slices had better characteristic aroma than 50 ℃ hot air treatments. Therefore, 80 ℃ hot air drying was the optimal drying condition. -
苹果脆片是畅销的脱水果蔬脆片之一,营养丰富,富含维生素、纤维素以及多种矿物质元素,具有低热量、低脂肪含量、口感酥脆、酸甜可口及便于携带等特点,深受广大消费者的喜爱[1]。热风干燥是一种传统有效的干燥方法,具有操作简便、处理量大、成本低等优势,广泛应用于脱水果蔬的加工过程中[2]。但热处理过程会导致香气发生改变,从而影响产品风味品质,因此得到了学者们的广泛关注[3]。水果及其加工制品中的挥发性成分是评估产品品质的重要参数,是产品香气特征和感官质量的重要影响因素[4]。到目前为止,已经从不同品种苹果中鉴定出300余种挥发性化合物,包括酯类、醇类、醛类、酸类、酮类和萜类化合物等。然而,只有少数物质对苹果风味有重要贡献,这些物质决定了苹果的风味属性[5-6]。因此对果蔬原料及其制品的关键香气化合物进行研究具有重要意义。
顶空固相微萃取气相色谱-质谱联用技术(headspace solid-phase micro-extraction gas chromatography-mass spectrometer,HS-SPME-GC-MS)对香气物质的检测具有较高的精度和良好的重现性[7]。电子鼻具有操作简单、快速等优势,可以对挥发性样品进行有效区分,但无法对挥发性化合物进行定量分析,GC-MS与电子鼻结合使用可极大地发挥各仪器的优势[8]。目前,采用顶空固相微萃取气质联用技术以及电子鼻技术对不同水果及其制品的挥发性成分进行了大量研究。Timoumi等[9]采用GC-MS研究了红外干燥时间和温度对苹果片香气含量的影响,明确了干燥时间和温度会影响挥发性化合物的含量。Krokida等[10]通过气相色谱-质谱联用技术分析了苹果在对流干燥过程中几种典型挥发性成分的变化,明确了较高温度对流干燥会导致挥发性成分快速损失。Song等[11]采用电子鼻结合顶空固相微萃取气相色谱-质谱技术明确了不同干燥方式对枣香气轮廓的影响。曹有芳等[12]采用电子鼻结合HS-SPME-GC-MS技术成功区分不同品种苹果酿造苹果酒的挥发性成分。但热风干燥作为一种常见的加工方式,其对苹果脆片关键香气化合物的影响研究尚未见报道。
因此,本研究以富士苹果为原料,采用HS-SPME-GC-MS对苹果鲜样、50、60、70和80 ℃热风干燥苹果脆片的挥发性化合物进行定性、定量分析,通过OAV鉴定关键香气化合物,结合电子鼻表征不同样品的香气轮廓差异,旨在明确不同温度热风干燥处理对苹果关键香气化合物的影响。
1. 材料与方法
1.1 材料与仪器
栖霞富士 果径约80 mm,初始水分含量86.4%±0.6%,购于山东烟台栖霞蛇窝堡镇果园,采摘后迅速运到北京存于4 ℃冷库,干燥前从冷库取出,室温下(25 ℃)放置24 h;正构烷烃混合物(C7~C30)标准品 美国Sigma-aldrich公司;丙位癸内酯标准品(色谱纯,98%) Macklin公司;甲醇(色谱纯,95%) 赛默飞世尔科技有限公司。
DHG-9123A型电热恒温鼓风干燥箱 上海一恒科技有限公司;HR1848榨汁机 珠海飞利浦电子有限公司;电子天平 上海梅特勒-托利多有限公司;PEN3型便携式电子鼻 德国Airsense公司;PAL RTC自动进样装置 广州智达实验室科技有限公司;GC-MS-QP2020气相色谱质谱联用仪 日本岛津公司;固相微萃取进样器、萃取针65 μm PDMS/DVB 美国Supelco公司;DB-WAX毛细管柱(30 m×250 μm,0.25 μm) 美国Agilent公司。
1.2 实验方法
1.2.1 样品制备
热风干燥苹果脆片制备方法及标准参考《NY/T 2779-2015苹果脆片》[13]。具体操作如下:选择成熟度好,无病虫害、无腐烂变质的苹果,经清洗、去皮、去核、切片(厚度5±0.2 mm);称取500 g苹果片,将其均匀平铺在不锈钢网盘,确保苹果片均为单层且之间无交叉重叠,然后迅速放入已经预热至设定温度的恒温鼓风干燥箱中,干燥至含水率<8%,50、60、70和80 ℃分别用时720、480、360和240 min。苹果脆片含水率的测定参考《GB 5009.3-2016 食品安全国家标准 食品中水分的测定》第一法,直接干燥法。将多次制备的苹果脆片混合均匀,用液氮冷冻后研磨为粉状,用于香气分析。
1.2.2 挥发性化合物提取
参考曾辉[14]的挥发性成分提取方法,并稍作修改。采用顶空固相微萃取技术进行提取。取2.0 g样品置于20 mL顶空进样瓶中,加入20 μL丙位癸内酯(925.12 μg/mL,溶于甲醇)作为内标,用聚四氟乙烯硅塞将顶空瓶口密封。萃取前将萃取头在250 ℃老化30 min;样品在50 ℃,平衡40 min后,萃取30 min;萃取完成后在进样口解吸3 min。
1.2.3 GC-MS分析
1.2.3.1 检测条件
参考曾辉[14]的GC-MS分析条件,并稍作修改。
色谱条件:DB-WAX毛细管柱(30 m×250 μm,0.25 μm);升温程序:初始柱温40 ℃,保持3 min,以5 ℃/min升温至120 ℃,然后以10 ℃/min升至230 ℃,并保持5 min;进样口温度250 ℃;载气为氦气,流速1.0 mL/min,不分流模式进样。质谱条件(MS):质谱接口温度250 ℃;离子源温度为200 ℃;EI电离源,能量70 eV;检测器电压0.2 kV;质量扫描范围35~350 m/z;溶剂延迟3 min。
1.2.3.2 定性分析
质谱库检索(MS)和保留指数(RI)两种方法。质谱库检索(MS):将GC-MS分析获得的挥发性化合物质谱与NIST 17数据库中标准化合物质谱进行比较,相似度在80以上,初步确定化合物。保留指数法是根据混合正构烷烃(C7~C30)标准品,在与样品相同的GC-MS条件下,获得的保留时间来计算挥发性化合物的保留指数,并将计算所获得的RI值与参考文献报道的RI值进行比较,二者相差20以内,对化合物进行进一步定性。RI计算公式如下[15]:
式中:n和n+1表示系列烷烃的原子个数;Ta为样品中化合物a的保留时间(化合物a的保留时间在Cn和Cn+1之间);Tn为正构烷烃Cn的保留时间;Tn+1为正构烷烃Cn+1的保留时间。
1.2.3.3 定量分析
采用内标法进行半定量[16],结果以干基计(dry basis,d.b)。内标法定量计算公式如下:
式中:Ci为待测化合物的质量浓度(μg/mL);C0为加入内标化合物的质量浓度(μg/mL);Ai为待测化合物的峰面积;A0为加入内标化合物的峰面积;V为每次进样样品的质量(g);V0为加入内标化合物的体积(mL)。
1.2.4 关键香气化合物评定方法
采用气味活度值法(odor-activity value,OAV)[17]。
式中:OAVi为某挥发性化合物的气味活度值;Ci为某挥发性化合物的含量;Ti为某挥发性化合物的阈值。
1.2.5 电子鼻分析
PEN3型电子鼻由10种金属氧化物气体传感器阵列组成。表1为各传感器阵列的响应特征。准确称取2.0 g样品于20 mL顶空瓶中,用聚四氟乙烯硅塞密封,25 ℃放置30 min后进行分析。电子鼻参数:样品测定间隔时间1 s,传感器冲洗持续180 s,自动调零持续10 s,预采样时间5 s,样品测试时间60 s,载气流速、进样流速300 mL/min。传感信号在48 s后基本稳定,采集信号时间为48~52 s。
表 1 PEN3电子鼻传感器性能描述Table 1. Description of PEN3 electronic nose sensor performance阵列序号 传感器 性能描述 R1 W1C 对芳烃成分,苯类灵敏 R2 W5S 对氮氧化合物灵敏 R3 W3C 对芳香成分灵敏,氨类灵敏 R4 W6S 主要对氢类灵敏 R5 W5C 对短链烷烃、芳香成分灵敏 R6 W1S 对甲基类灵敏 R7 W1W 对硫化物灵敏 R8 W2S 对醇类,醛酮类灵敏 R9 W2W 对芳香成分,有机硫化物灵敏 R10 W3S 对长链烷烃灵敏 1.3 数据处理
数据使用Excel 2003软件进行统计分析,使用SPSS 19.0软件进行单因素方差分析及多重比较,结果以平均值±标准偏差表示,P<0.05为显著相关,采用Origin 2018软件进行绘图。每个样品重复测定3次。
2. 结果与分析
2.1 热风干燥对苹果香气化合物的影响
采用HS-SPME-GC-MS技术对苹果鲜样和4种不同温度热风干燥苹果脆片挥发性化合物分析结果见表2。苹果鲜样和4种干燥样品中共检测出64种挥发性化合物,包括酯类23种、醇类18种、醛类8种、烯烃类2种、酮类2种、内酯类3种、酸类1种、含硫化合物3种和杂环化合物4种。不同样品各类挥发性化合物的种类及含量均存在较大差异。其中,苹果鲜样中检测到41种挥发性化合物,50、60、70和80 ℃热风干燥样品中分别检测到43、42、38和33种挥发性化合物。鲜样挥发性化合物含量最高,为397.059 mg/kg,4种热风干燥样品挥发性化合物含量由高到低分别是64.189 mg/kg(50 ℃处理)、57.703 mg/kg(80 ℃处理)、32.124 mg/kg(70 ℃处理)、32.020 mg/kg(60 ℃处理)。苹果经热风干燥后,挥发性化合物含量降低,这与Timoumi等[9]研究发现一致,热处理的时间和温度会对苹果片挥发性成分的种类和含量产生影响,推断与香气物质热分解及伴随水分蒸发有关。而相对于60和70 ℃热风干燥样品,50和80 ℃热风干燥苹果片挥发性化合物含量较高,结合苹果片制备温度和时间分析,说明低温、短时干燥有利于物质的保留。
表 2 苹果鲜样以及热风干燥苹果脆片挥发性化合物定性、定量结果Table 2. Identification and quantification of volatile compounds in fresh apple and hot-air dried apple slices序号 化合物名称 保留时间
(min)CAS 保留指数 含量(mg/kg d.b) 定性方法 参考值 实验值 鲜样 50 ℃ 60 ℃ 70 ℃ 80 ℃ 酯类 1 丁酸乙酯 5.361 105-54-4 1034 1034 13.552±1.791a − − − − MS/RI 2 2-甲基丁酸乙酯 5.723 7452-79-1 1050 1049 12.176±1.551a − − − − MS/RI 3 乙酸丁酯 6.178 123-86-4 1071 1069 7.949±1.361a − − − − MS/RI 4 2-甲基丁基乙酸酯 7.367 624-41-9 1120 1117 46.815±8.915a − − − − MS/RI 5 乙酸戊酯 8.804 628-63-7 1172 1171 0.699±0.195a − − − − MS/RI 6 己酸甲酯 9.166 106-70-7 1181 1184 3.669±1.293a 0.099±0.033b − − − MS/RI 7 丁酸丁酯 10.049 109-21-7 1219 1217 8.567±1.555a − − − − MS/RI 8 己酸乙酯 10.505 123-66-0 1233 1233 4.484±1.847a 0.46±0.062b 0.082±0.019b − − MS/RI 9 乙酸己酯 11.587 142-92-7 1271 1273 29.713±5.194a 0.483±0.067b 0.167±0.031b 0.199±0.008b − MS/RI 10 2-甲基丁酸2-甲基丁酯 11.859 2445-78-5 1285 1283 0.546±0.351a − − − − MS/RI 11 己酸丙酯 12.85 626-77-7 1322 1319 1.335±0.280a − − − − MS/RI 12 异丁酸己酯 13.555 2349-07-7 1339 1346 0.364±0.126a 0.044±0.006b − − − MS/RI 13 辛酸甲酯 14.74 111-11-5 1390 1390 − 0.110±0.032a 0.03±0.012b 0.035±0.008b 0.033±0.002b MS/RI 14 己酸丁酯 15.405 626-82-4 1412 1416 1.429±0.890a 0.058±.0b 0.010±0.002b − − MS/RI 15 丁酸己酯 15.484 2639-63-6 1412 1419 22.895±4.245a 0.408±0.034b 0.169±0.031b 0.236±0.031b 0.352±0.004b MS/RI 16 2-甲基丁酸己酯 15.771 10032-15-2 1429 1430 16.623±3.066a 2.533±0.187b 1.692±0.274b 2.343±0.273b 2.204±0.032b MS/RI 17 辛酸乙酯 15.937 106-32-1 1434 1437 − 0.091±0.009a 0.048±0.019b − − MS/RI 18 丙酸庚酯 16.1 2216-81-1 1446 1443 0.168±0.056a − − − − MS/RI 19 壬酸甲酯 17.412 1731-84-6 1485 1494 2.303±0.407a − 0.075±0.005b 0.171±0.016b 0.198±0.067b MS/RI 20 3-羟基丁酸乙酯 18.046 5405-41-4 1515 1521 − 1.564±0.163a 0.428±0.080b − − MS/RI 21 己酸己酯 20.18 6378-65-0 1603 1615 5.480±1.262a 0.526±0.021b 0.117±0.018b 0.082±0.011b 0.188±0.007b MS/RI 22 月桂酸甲酯 23.27 111-82-0 1798 1806 0.230±0.062a − − − MS/RI 23 棕榈酸甲酯 27.854 112-39-0 2207 2224 0.059±0.029b 0.173±0.048a 0.104±0.022b 0.217±0.068a 0.383±0.278a MS/RI 醇类 24 丁醇 8.297 71-36-3 1146 1152 2.363±0.762a − − − − MS/RI 25 2-甲基-1-丁醇 9.868 137-32-6 1208 1210 − 0.513±0.055a 0.264±0.046b 0.316±0.041b 0.114±0.063c MS/RI 26 戊醇 11.075 71-41-0 1248 1254 − 0.076±0.053a 0.012±0.002b − − MS/RI 27 2-庚醇 13.054 543-49-7 1312 1327 0.253±0.047a − − − − MS/RI 28 己醇 13.935 111-27-3 1351 1360 16.733±3.468a 2.855±0.332b 1.179±0.216b 1.871±0.152b 0.944±0.057b MS/RI 29 3-辛醇 15.011 589-98-0 1388 1400 0.579±0.196a − − − − MS/RI 30 1-辛烯-3-醇 16.435 3391-86-4 1448 1456 0.080±0.026a 0.043±0.008b 0.018±0.003c 0.070±0.003a 0.078±0.005a MS/RI 31 庚醇 16.587 111-70-6 1449 1462 0.560±0.113a 0.156±0.016b − − − MS/RI 32 6-甲基-5-庚烯-2-醇 16.788 1569-60-4 1466 1470 4.836±0.809a 0.155±0.020b 0.071±0.013b 0.109±0.009b 0.190±0.012b MS/RI 33 2,3-丁二醇 18.639 513-85-9 1553 1546 − 0.81±0.058a 0.440±0.070b 0.404±0.047b 0.425±0.01b MS/RI 34 芳樟醇 18.846 78-70-6 1542 1555 0.278±0.045a 0.067±0.008c 0.047±0.008c 0.133±0.02b 0.137±0.005b MS/RI 35 辛醇 19.125 111-87-5 1554 1567 0.403±0.083a 0.351±0.023a 0.179±0.030b 0.360±0.004a − MS/RI 36 4-萜烯醇 20.012 562-74-3 1603 1605 0.109±0.017a − − − − MS/RI 37 3-甲基-4-庚醇 21.856 1838-73-9 / 1709 − 0.865±0.03d 0.538±0.106c 0.689±0.050b 1.123±0.035a MS 38 香茅醇 22.807 106-22-9 1764 1774 0.147±0.042a 0.046±0a 0.029±0.016a 0.043±0a 0.030±0a MS/RI 39 苯甲醇 24.232 100-51-6 1865 1882 − 0.049±0.018ab 0.031±0.007b 0.056±0.007a 0.055±0.008a MS/RI 40 苯乙醇 24.666 60-12-8 1907 1918 − 0.141±0.01a 0.056±0.010d 0.113±0.009b 0.099±0.003c MS/RI 41 1,3-辛二醇 27.051 23433-05-8 2128 2141 0.514±0.176d 9.020±1.169b 4.564±1.102c 8.248±0.717b 12.506±1.086a MS/RI 醛类 42 己醛 6.347 66-25-1 1078 1076 71.273±18.000a 0.693±0.251b 0.265±0.098b − − MS/RI 43 反式-2-己烯醛 9.965 6728-26-3 1218 1214 18.580±6.466a − − − − MS/RI 44 辛醛 11.972 124-13-0 1287 1287 − 0.124±0.029a 0.052±0.011b 0.069±0.007b 0.050±0.000b MS/RI 45 反式-2-庚烯醛 12.877 18829-55-5 1325 1320 − 0.050±0.014a − 0.038±0.002a 0.040±0.013a MS/RI 46 壬醛 14.83 124-19-6 1390 1393 1.535±0.230a 0.117±0.052b 0.047±0.012b 0.079±0.011b 0.074±0.009b MS/RI 47 癸醛 17.532 112-31-2 1493 1499 0.416±0.083a − 0.076±0.013c 0.179±0.025b − MS/RI 48 反式-2-壬烯醛 18.401 18829-56-6 1533 1536 0.229±0.041a 0.062±0.009cd 0.036±0.007d 0.095±0.011bc 0.101±0.005a MS/RI 49 橙花醛 22.217 141-27-5 1726 1733 − 0.051±0.005a − 0.038±0.002a 0.052±0.000ab MS/RI 烯烃类 50 柠檬烯 9.395 138-86-3 1197 1193 − 0.149±0.072a 0.031±0.000bc 0.139±0.057a 0.106±0.017ab MS/RI 51 α-法尼烯 22.494 502-61-4 1737 1752 98.145±16.616a 37.474±1.425a 19.353±2.875b 12.303±1.811b 33.565±0.367a MS/RI 酮类 52 3-羟基-2-丁酮 11.821 513-86-0 1285 1281 − 0.904±0.091a 0.306±0.053d 0.527±0.045c 0.660±0.064b MS/RI 53 6-甲基-5-庚烯-2-酮 13.347 110-93-0 1339 1338 0.660±0.070b 0.592±0.078b 0.266±0.053c 0.598±0.044b 0.766±0.036a MS/RI 内酯类 54 γ-己内酯 21.691 695-06-7 1691 1698 − 0.138±0.012a 0.088±0.016c 0.088±0.012b 0.125±0.011b MS/RI 55 γ-壬内酯 25.989 104-61-0 2027 2037 − − 0.054±0.020a 0.111±0.003a − MS/RI 56 δ-癸内酯 27.719 705-86-2 2193 2209 − 0.060±0.052a 0.030±0.001b − − MS/RI 酸类 57 2-羟基-2-甲基丁酸 20.879 3739-30-8 / 1653 − 0.161±0.014c 0.114±0.019d 0.255±0.026a 0.214±0.010b MS 含硫化合物 58 2-甲硫基乙醇 18.276 5271-38-5 1537 1531 − 0.058±0.010a 0.033±0.005b 0.036±0.001b 0.027±0.002b MS/RI 59 3-甲硫基丙酸乙酯 19.203 13327-56-5 1566 1570 0.19±0.024a − − − − MS/RI 60 3-甲硫基丙醇 22.059 505-10-2 1722 1723 0.12±0.039d 1.666±0.063a 0.725±0.124c 0.837±0.093c 1.135±0.029b MS/RI 杂环类化合物 61 2-戊基呋喃 10.42 3777-69-3 1235 1230 − 0.153±0.035a 0.086±0.027b 0.183±0.030a 0.136±0.020a MS/RI 62 糠醛 16.555 98-01-1 1463 1461 − − 0.099±0.016c 0.814±0.080b 1.56±0.061a MS/RI 63 2-呋喃甲醇 21.095 98-00-0 1651 1665 − 0.039±0.004a 0.009±0.001c 0.021±0.002b − MS/RI 64 5-羟甲基糠醛 30.411 67-47-0 2505 2511 − − − 0.019±0.003b 0.031±0.001a MS/RI 注:“−”表示未检测到该种物质;“/”表示未查询到该物质的参考RI值;不同小写字母代表每种化合物P<0.05水平下不同样品间含量差异显著。 酯类物质主要是酸类和醇类物质酯化反应的产物,赋予水果香甜气味。在所有样品中共检测到23种酯,主要是乙酸酯类、丁酸酯类和己酸酯类挥发性成分,这与文献报道结果相一致[18-20]。苹果鲜样检测到20种酯类物质,其中2-甲基丁基乙酸酯是鲜样中含量最高的酯类物质,为46.815 mg/kg。其次为乙酸己酯、丁酸己酯、2-甲基丁酸己酯、丁酸乙酯、2-甲基丁酸乙酯和丁酸丁酯,这些酯类均具有典型的果香、花香和甜香气味。与鲜样相比,4种热风干燥样品酯类化合物种类均减少,50 ℃样品检测到12种、60 ℃样品检测到11种、70 ℃样品检测到7种、80 ℃检测到6种,这可能与小分子挥发性成分在干燥过程中随热空气流动损失,同时高温导致热敏性化合物的分解有关[21]。仅在个别的干燥样品中检测到较低含量的辛酸甲酯、辛酸乙酯、3-羟基丁酸乙酯,分别呈现柑橘味、果香、酒香,是发酵酒中的常见风味成分,一般来源于氨基酸和糖无氧代谢途径生成的高级醇与酸之间的缩合反应[22-24]。丁酸己酯、2-甲基丁酸己酯、己酸己酯和棕榈酸甲酯是鲜样与4种干燥样品共有的酯类物质。除棕榈酸甲酯以外,其他三种酯类经过热风干燥后含量显著降低(P<0.05),而棕榈酸甲酯在4种干燥样品中含量高于鲜样,其含量增加可能与脂肪酸氧化降解有关[25]。
醇类化合物一般带有清香、果香、草木香、醇味。己醇是鲜样中含量最高的醇类物质,为16.733 mg/kg。己醇主要与花香、青草味和果香相关[12,24],经过热风干燥后,含量显著降低(P<0.05)。己醇、1-辛烯-3-醇、6-甲基-5-庚烯-2-醇、芳樟醇、香茅醇和1,3-辛二醇是所有样品中共有的醇类物质。1-辛烯-3-醇为不饱和脂肪醇,具有蘑菇、玫瑰和干草香气[26]。6-甲基-5-庚烯-2-醇、芳樟醇、香茅醇分别呈现清香、花香和柑橘香[27-29],这三种醇类物质经过热处理后含量显著降低(P<0.05),1,3-辛二醇呈现相反趋势。2,3-丁二醇、2-甲基-1-丁醇、3-甲基-4-庚醇、苯甲醇和苯乙醇仅在热风干燥样品中检出,苯甲醇是一种糖苷前体,呈现杏仁、花香和烤面包味,加热后释放[30]。2-甲基-1-丁醇是2-甲基丁醛的还原产物,而2-甲基丁醛是一种支链短链醛,是异亮氨酸Strecker降解反应产物[31-32]。
在所有样品中共检测到7种醛类物质,己醛是苹果鲜样中含量最高的醛类物质,为71.273 mg/kg,表现为青草、清新、脂肪气味,是苹果的特征性香气成分[18-19]。醛类物质受热易分解[33-34],在50和60 ℃较低的干燥温度下,己醛含量分别降低至0.693、0.265 mg/kg,70和80 ℃干燥样品均未检出,表明随着温度的升高,己醛含量显著降低(P<0.05),干燥苹果样品中清新、青草味减弱。反式-2-己烯醛只在鲜样中检测到,为18.580 mg/kg,是脂肪氧合酶和氢过氧化物裂解酶对亚油酸和亚麻酸作用的产物[35],表现为脂肪味。壬醛具有脂肪味、花香、柑橘等香气,经过热风干燥处理,含量显著降低(P<0.05)。辛醛仅存在与干燥样品中,表现为脂肪味、清香、柠檬香。
萜烯类物质是果蔬中常见的一类物质,风味阈值较高,一般对产品整体风味贡献并不明显,但在产品整体香气的维持和协调中起着重要作用。α-法尼烯表现为甜香、柑橘香、花香,是所有样品中含量最高的萜烯类化合物,经过热风干燥处理后,α-法尼烯含量降低。此外,检测出2种酮类化合物,分别是3-羟基-2-丁酮和6-甲基-5-庚烯-2-酮。其中,3-羟基-2-丁酮,呈现黄油味,仅在4种干制样品中检出,猜测其形成可能与不饱和脂质的氧化降解或美拉德反应有关。在干燥样品中检测到3种内酯和1种酸类物质,包括γ-己内酯、γ-壬内酯、δ-癸内酯和2-羟基-2-甲基丁酸。内酯类物质是多种水果和水果产品中的重要芳香成分,呈现多种香气特征,如椰子味、水果味、甜味、焦糖味、桃味、杏味、干果味和脂肪味等,一般对水果的香气轮廓起积极作用。
热处理过程中,含硫化合物形成可能与含硫氨基酸(胱氨酸、半胱氨酸、甲硫氨酸)Strecter降解有关,是美拉德反应的重要产物,广泛存在于热加工食品中[25]。除此以外,含硫化合物形成还包括酶促反应路径,其前体物为生物体本身存在的含硫化合物,以及与一些含硫农药在生物体内的转化有关,同时,温度和光照也是植物生长过程中含硫化合物形成的重要影响因素[36]。在所有样品中共检测出3种含硫化合物,分别为2-甲硫基乙醇、3-甲硫基丙酸乙酯和3-甲硫基丙醇。3-甲硫基丙酸乙酯仅存在于苹果鲜样中,表现为薄荷味、青草味、焦糖味和药物气味[36]。经过干燥处理,3-甲硫基丙醇含量显著增加(P<0.05),据文献报道,3-甲硫基丙醇的形成与甲硫氨酸Strecter降解有关[25]。呋喃类物质是具有芳香特性的小环状醚类,通常具有甜香及谷物香,在食品加工和烹饪过程中,其生成途径包括美拉德反应、脂质氧化以及碳水化合物的热降解和重排等。2-戊基呋喃表现为焦香气味,是美拉德反应产物,广泛存在于熟制三文鱼、烤鸭和干制芒果皮等热加工食品中[25,36-37]。糠醛和5-羟甲基糠醛是美拉德反应初级阶段产物,是表征食品热处理过程中发生美拉德反应的重要检测指标[38]。糠醛表现为杏仁味、熟土豆味、面包味,对温度和水分有高度敏感性[39-40]。50 ℃样品未检出糠醛,但2-呋喃甲醇含量显著高于60、70 ℃样品(P<0.05),80 ℃未检出,呈现焦糖味、烧焦味,推测可能与50 ℃热风干燥时间较长有关,糠醛进一步被还原为2-呋喃甲醇[28]。5-羟甲基糠醛仅在70和80 ℃样品中检出,呈现焦糖味、脂肪味、香料味[41]。鲜样中未检测出杂环类化合物。
2.2 热风干燥对苹果关键香气化合物的影响
大量研究表明,食物基质中的一些挥发性化合物可能只有一小部分参与香气感知,对香气轮廓具有重要贡献。OAV是评价挥发性化合物在食品基质中贡献大小的重要标准。研究表明,OAV大于1的物质对该样品呈现出的整体香气有重要贡献[17]。因此,根据GC-MS分析结果进一步筛选香气活性化合物,为确定苹果鲜样及苹果脆片关键挥发性成分提供重要依据。本研究参考书籍[42]及相关文献[20-21],确定了挥发性化合物的阈值及OAV,从而判定不同样品的关键香气化合物。阈值、气味特征描述以及OAV如表3所示,主要为酯类、醇类、醛酮类、烯烃类、含硫化合物以及杂环类化合物。
表 3 苹果鲜样以及4种不同温度热风干燥苹果脆片挥发性化合物OAVTable 3. OAV of volatile compounds in fresh apple and four hot air dried apple slices at different temperatures化合物 气味特征 阈值(mg/kg) OAV 鲜样 50 ℃ 60 ℃ 70 ℃ 80 ℃ 丁酸乙酯 苹果味、果香 0.0005 27103.34 − − − − 2-甲基丁酸乙酯 苹果香、果香 0.000013 936583.12 − − − − 乙酸丁酯 苹果香、甜香 0.058 137.06 − − − − 2-甲基丁基乙酸酯 苹果香、梨香 0.008 5851.91 − − − − 乙酸戊酯 香蕉味、果香、甜香 0.043 16.25 − − − − 己酸甲酯 果香、新鲜、甜香 0.07 52.41 1.42 − − − 丁酸丁酯 花香 0.4 21.42 − − − − 己酸乙酯 香蕉味、苹果皮味 0.0022 2038.17 209.29 37.46 − − 乙酸己酯 苹果香、浆果香 0.115 258.37 4.20 1.45 1.73 − 2-甲基丁酸2-甲基丁酯 水果味 0.075 7.28 − − − − 异丁酸己酯 nd 0.0173 21.02 2.56 − − − 丁酸己酯 苹果皮香、柑橘香 0.203 112.78 2.01 <1 1.16 1.73 2-甲基丁酸己酯 草莓味 0.022 755.61 115.16 76.90 106.50 100.18 辛酸乙酯 香蕉味、菠萝味 0.0193 − 4.72 2.49 − − 丙酸庚酯 nd 0.004 41.99 − − − − 壬酸甲酯 椰子味、果香 0.046 50.07 − 1.63 3.72 4.31 月桂酸甲酯 椰子味、脂肪味 0.002 115.08 − − − − 正丁醇 酒精味 0.4592 5.15 − − − − 2-甲基-1-丁醇 燃料味、麦芽味 0.0159 − 32.26 16.58 19.89 7.16 2-庚醇 柑橘味 0.065235 3.88 − − − − 己醇 清香、草本香、木香 0.0056 2988.00 509.90 210.55 334.09 168.54 3-辛醇 柑橘味、坚果味 0.15 3.86 − − − − 1-辛烯-3-醇 蘑菇味 0.0015 53.12 28.97 12.08 46.57 51.80 正庚醇 腐臭味 0.0054 103.71 28.86 − − − 6-甲基-5-庚烯-2-醇 清香 2 2.42 <1 <1 <1 <1 芳樟醇 花香 0.00022 1264.30 302.31 212.75 605.14 623.18 辛醇 脂肪味 0.11 3.66 3.19 1.63 3.28 − 3-甲基-4-庚醇 nd 0.078 − 11.09 6.90 8.83 14.39 香茅醇 柑橘味、玫瑰香 0.062 2.37 <1 <1 <1 <1 苯乙醇 玫瑰香、甜苹果味 0.012 − 11.77 4.67 9.40 8.25 己醛 青草味、脂肪味 0.005 14254.57 138.59 52.92 − − 反式-2-己烯醛 脂肪味、绿色 0.03 619.33 − − − − 辛醛 脂肪香、坚果味 0.000587 − 211.25 88.42 117.30 84.36 壬醛 柑橘香、脂肪味 0.001 1534.99 116.94 47.36 79.36 73.63 癸醛 脂肪味、花香 0.003 138.76 − 25.42 59.74 − 反式-2-壬烯醛 黄瓜味、青草味 0.00019 1202.98 328.67 189.38 500.73 533.78 橙花醛 花香、果香、柠檬味 0.037 − 1.39 − 1.04 1.41 3-羟基-2-丁酮 黄油味、奶油味 0.014 − 64.57 21.86 37.61 47.17 6-甲基-5-庚烯-2-酮 柑橘味、胡椒味 0.068 9.71 8.70 3.90 8.80 11.27 γ-壬内酯 可可香、桃香 0.0097 − − 5.58 11.44 − 3-甲硫基丙酸乙酯 卷心菜、青草味 0.00845 22.54 − − − − 3-甲硫基丙醇 熟牛奶味、熟土豆味、泥土味 0.12323 − 13.52 5.88 6.79 9.21 2-戊基呋喃 黄油味、花香、果香 0.0058 − 26.44 14.88 31.54 23.52 α-法尼烯 柑橘香、花香、甜香 0.0077 12746.11 4866.72 2513.41 1597.75 4359.11 Total 1008125 7044 3554 3592 6123 注:“−”表示未检测到该种物质;“nd”表示未查阅到该种化合物的气味特征描述词;气味特征描述参照Vcf Home网站[43]和Flavornet网站[44]。 由表3可知,与鲜样相比,4种干燥样品中关键香气化合物的种类减少,总OAV降低。苹果鲜样、50、60、70和80 ℃热风干燥样品中OAV>1的挥发性化合物分别有33种(总OAV=1008125)、24种(总OAV=7044)、23种(总OAV=3554)、22种(总OAV=3592)和18种(总OAV=6123)。苹果鲜样独有的OAV>1的化合物16种,主要是酯类物质,包括2-甲基丁酸乙酯(936583.12)、丁酸乙酯(27103.34)、乙酸丁酯(137.06)、己酸乙酯(2038.17)和乙酸己酯(258.37)等。这些物质阈值较低,因此具有较高的OAV,是苹果鲜样中关键香气化合物,对苹果鲜样香气轮廓起到决定性作用,这与文献报道的研究结果相一致[6]。其次为己醛(14254.37)、α-法尼烯(12716.11)、己醇(2988.00),表现为青草味、果香、花香、甜香、柑橘香,对苹果鲜样香气轮廓的形成具有重要贡献。
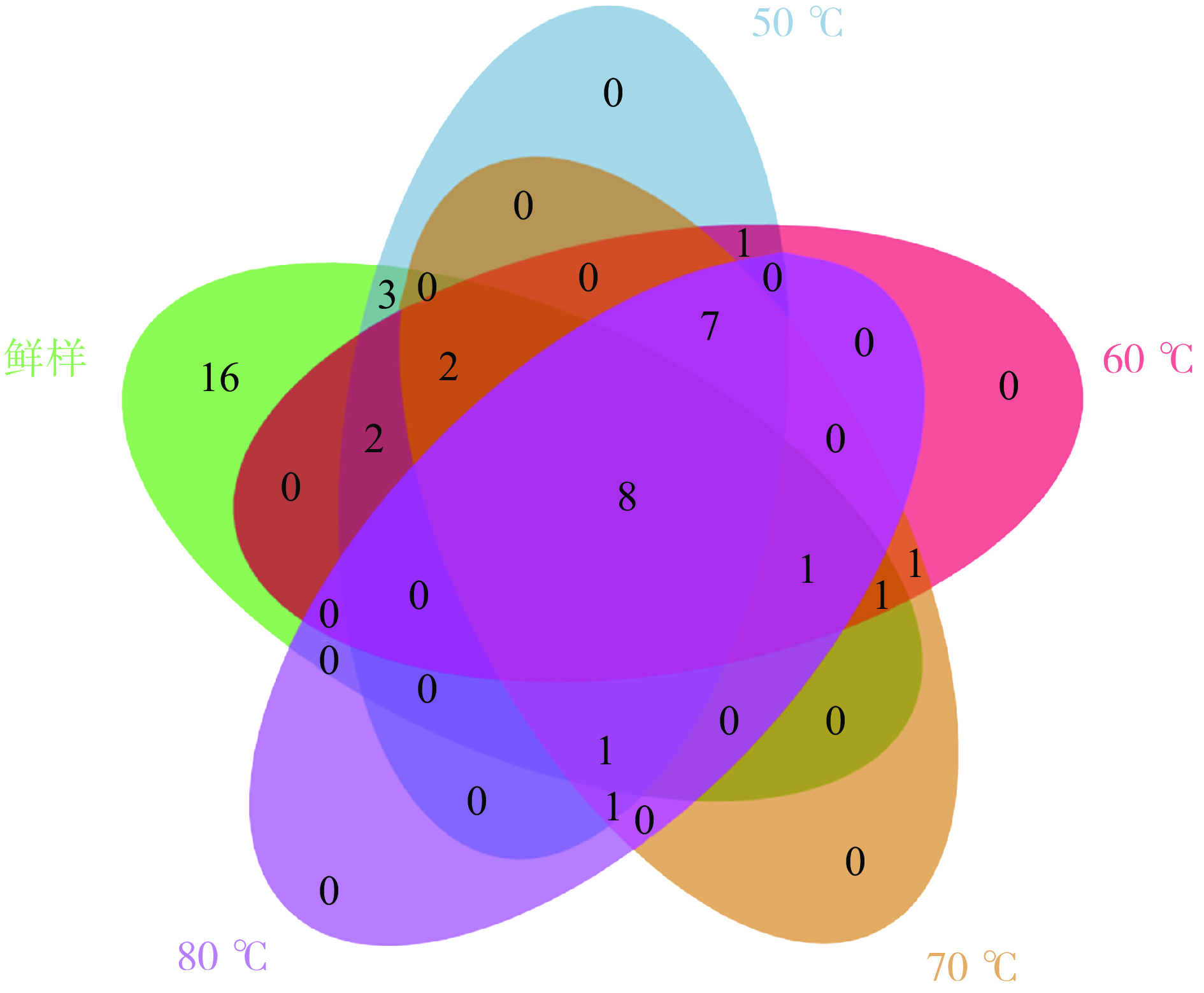
鲜样以及不同温度干燥样品中关键香气化合物的关系如图1所示,可以看出样品关键香气化合物存在差异。鲜样与干燥样品共有OAV>1的挥发性化合物8种,分别为α-法尼烯(12746.11~1597.75)、2-甲基丁酸己酯(755.617~6.90)、己醇(2988.00~168.54)、1-辛烯-3-醇(53.12~12.08)、壬醛(1534.99~47.36)、反式-2-壬烯醛(1202.98~189.38)、芳樟醇(1264.30~212.75)和6-甲基-5-庚烯-2-酮(11.27~3.90),表现为柑橘香、花香、果香、甜香。除6-甲基-5-庚烯-2-酮以外,其他7种化合物在鲜样中的OAV值均大于干燥样品中,而在四种干燥样品的OAV值差异较小,这与苹果经过热风干燥后化合物含量降低有关。如鲜样中,丁酸己酯OAV为755.61,50、60、70和80 ℃样品中分别为115.16、76.90、106.50和100.18,说明经过干燥处理后,干燥样品中与鲜样香气轮廓上仍保持一定的相似性,但是在香气强度上有所减弱。仅存在4种干燥样品中OAV>1的组分共7种,包括3种醇类、1种醛类、1种酮类、1种含硫化合物和1种杂环化合物,分别为2-甲基-1-丁醇(7.16~32.26)、3-甲基-4-庚醇(6.90~14.39)、苯乙醇(4.67~11.11)、辛醛(84.36~211.25)、3-羟基-2-丁酮(21.86~64.57)、3-甲硫基丙醇(5.88~13.52)和2-戊基呋喃(14.88~26.44),是经过热风干燥后新生成的化合物,这些化合物被认为是脱水苹果片特征香气成分。
总体而言,苹果鲜样的关键挥发性成分主要是酯类、醇类、醛类以及烯烃类化合物,包括丁酸乙酯、2-甲基丁酸乙酯、乙酸丁酯、2-甲基丁酸乙酸酯、己酸乙酯、乙酸己酯、丁酸己酯、2-甲基丁酸己酯、己醇、芳樟醇、己醛、反式-2-己烯醛、壬醛、反式-2-壬烯醛和α-法尼烯。这些物质以酯类为主,且具有较高的OAV,使新鲜苹果整体表现强烈的果香、香甜、清新、柑橘香、花香风味。与鲜样相比,热风干燥样品关键香气化合物酯类物质种类减少,OAV值降低。醛类、醇类物质种类增加,还包括一些酮类化合、含硫化合物、杂环化合物。4种干燥样品共有关键香气化合物包括2-甲基丁酸己酯、2-甲基-1-丁醇、己醇、1-辛烯-3-醇、芳樟醇、3-甲基-4庚醇、苯乙醇、己醛、辛醛、壬醛、反式-2-壬烯醛、α-法尼烯、3-羟基-2-丁酮、3-甲硫基丙醇和2-戊基呋喃。与鲜样相比,苹果脆片果香、青草味和清香味减弱,同时醛类物质提供了脂肪味,3-羟基-2-丁酮、3-甲硫基丙醇和2-戊基呋喃表现为黄油味、熟牛奶味、焦香味。4种干燥样品在风味轮廓上具有较高的相似度,而四种样品之间主要香气差异体现在各物质OAV值的微小差别,因为相比于60和70 ℃,50和80 ℃热风处理后新生成化合物,含量较高,OAV较大,体现了不同温度热风处理可以在不同程度上影响苹果脆片的感官特性及特征风味,使苹果脆片的风味轮廓更加丰富,同时也说明50和80 ℃热风干燥处理的苹果脆片更具有热风干燥特点。
2.3 电子鼻分析
2.3.1 传感器响应值变化
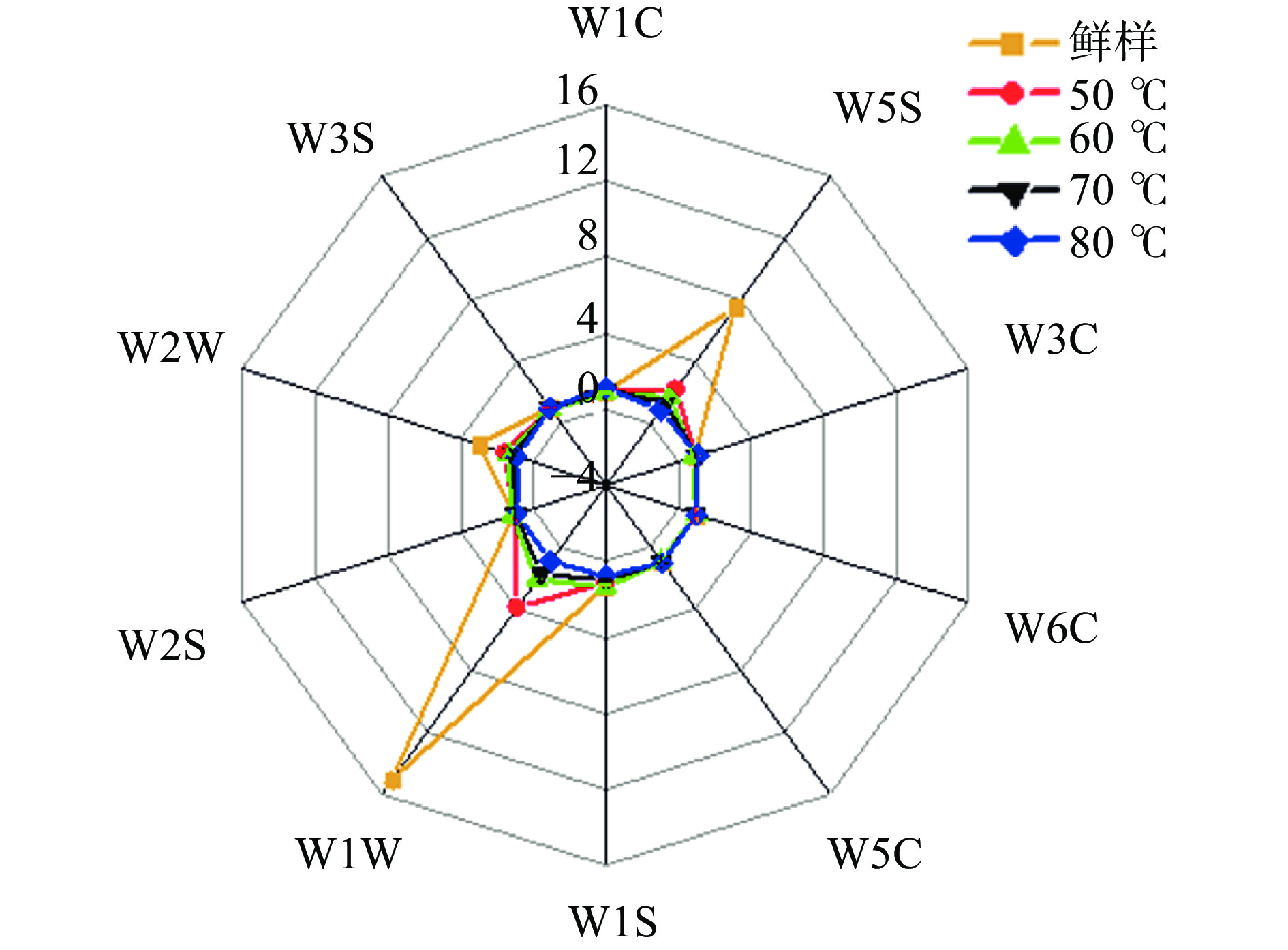
PEN3电子鼻中的10个金属传感器能分别针对不同气体产生响应信号。苹果鲜样与不同温度热风干燥苹果片样品电子鼻传感器的响应值雷达图见图2。由图2可知,苹果鲜样和干燥样品响应较强的传感器为W1W、W5S、W2W,说明萜烯类化合物、氮氧类化合物、芳香成分在苹果鲜样和干燥样品中的含量较高,表明鲜样与不同干燥样品香气轮廓存在显著差异。鲜样与干燥样品在W1W传感器响应值差异显著(P<0.05),推测W1W传感器与样品中α-法尼烯的含量有关,苹果鲜样的响应值最高,其次为50、80、60和70 ℃,说明相对于60 ℃、干燥温度较低(70、50 ℃)和干燥时间短(80 ℃)均较好地保留了苹果中的萜烯类挥发性成分。与鲜样相比,不同温度热风干燥样品W1W、W5S、W2W传感器响应值显著降低(P<0.05),说明经过热风干燥处理,萜烯类化合物、氮氧化合物含量降低,这与GC-MS结果具有很好的一致性,同时表明干燥温度对苹果片中的有机硫化物、萜烯类、醇类、醛酮类和甲基类物质等挥发性成分有较大的影响。W1C、W3C对芳烃成分、苯类敏感,热风干燥苹果片样品W1C、W3C传感器响应值高于鲜样,在干燥样品中,80 ℃干燥样品响应值最大,表明干燥后芳烃成分、苯类化合物含量显著增加(P<0.05),这与GC-MS结果中苯甲醇、苯乙醇仅在干样中检出结果相一致。W6S、W5C、W1S、W2S、W3S传感器对样品中挥发性气味的响应均较低,在0.01~2之间,表明样品中氨类、氢类、短链烷烃、甲基类、醇类、醛酮类、长链烷烃类挥发性组分含量较低,且不同温度热风干燥样品之间响应值差异较小,说明干燥温度对该类挥发性组分的影响不大。
2.3.2 主成分分析
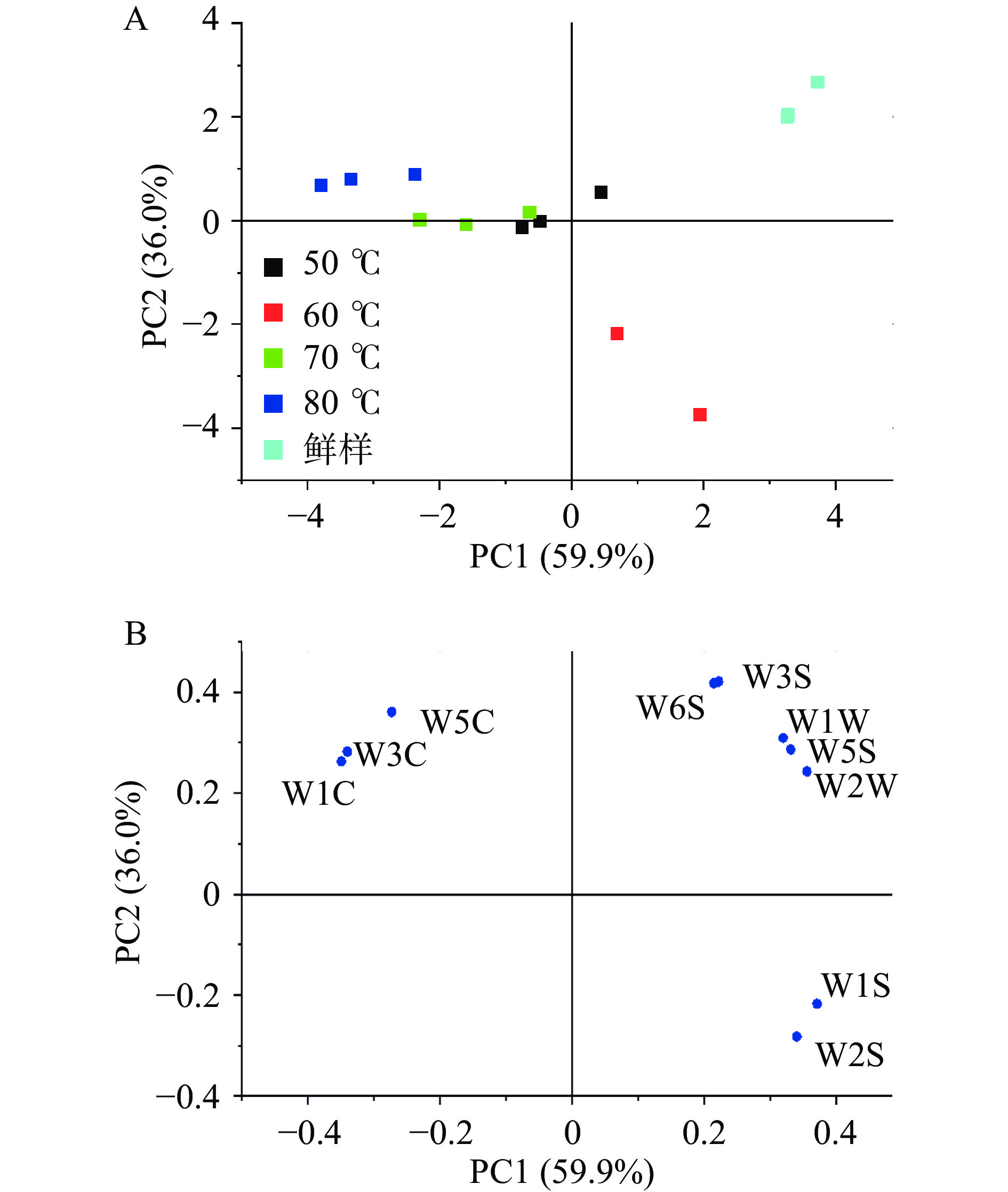
为了更好地可视化电子鼻数据,对电子鼻数据进行了主成分分析(PCA),以确定不同苹果片样品之间是否存在可察觉的嗅觉差异。图3为电子鼻数据主成分分析得分图(A)和载荷图(B),由图可以看出,两个主成分(第一主成分PC1的贡献率为59.9%,第二主成分PC2的贡献率为36.0%)累计方差95.9%,说明前两个主成分覆盖了样品的绝大多数气味信息[8]。如图3A所示,鲜样与干燥样品之间得到区分,说明干燥处理使苹果的挥发性风味物质发生改变,导致鲜样与干燥样品呈现不同的风味特征。鲜样和60 ℃热风处理样品都位于PC1的右侧区域,50、70和80 ℃样品在左侧区域,并且4种干燥样品之间没有重叠,表明其在挥发性成分上有一定差异,可能与样品香气化合物的种类和含量差异有关,与OAV分析结果相一致。载荷图是利用所有传感器的信号研究样品所属类别的一种统计方法。载荷分析如图3B所示,挥发性物质第一主成分以萜烯类和有机硫化合物为主,第二主成分以芳烃、苯类物质为主。W1C、W2W、W5S、W3S、W6S传感器与苹果鲜样相关联,与鲜样中含有较高含量的α-法尼烯有关。W1C、W3CS、W5C传感器与50、70和80 ℃样品相关联,与50、70和80 ℃样品在干燥过程中生成苯甲醇、苯乙醇有关及与含硫化合物的形成有关,进一步验证了鲜样与热风干燥苹果脆片之间香气轮廓的差异。
3. 结论
本研究采用HS-SPME-GC-MS结合电子鼻对苹果鲜样和不同温度热风干燥苹果脆片关键香气化合物进行了表征。GC-MS分析表明,苹果鲜样和4种热风干燥样品香气种类和含量存在较大的差异。苹果鲜样主体香气成分为酯类、烯烃类、醛类,其中2-甲基丁酸乙酯、丁酸乙酯、2-甲基丁基乙酸酯、α-法尼烯、己醛、壬醛、反式-2-壬烯醛是主要成分。与苹果鲜样相比,热风干燥样品酯类和烯烃类含量降低,杂环化合物和含硫化合物种类和含量增加。OAV分析表明,苹果鲜样与热风干燥样品关键香气化合物存在差异。2-甲基丁酸己酯、己醇、1-辛烯-3-醇、芳樟醇、壬醛、6-甲基-5-庚烯-2-酮、α-法尼烯是鲜样与4种干燥样品共有的关键香气化合物,在热风干燥样品中OAV值小于鲜样,表明干燥样品果香、花香、柑橘香减弱。除此以外,苹果鲜样关键香气化合物还包括2-甲基丁酸乙酯、2-甲基丁基乙酸酯、乙酸丁酯、丁酸丁酯、己酸乙酯、乙酸己酯。热风干燥样品关键香气化合物还包括3-甲硫基丙醇、2-戊基呋喃,增强苹果脆片的脂肪香、焦香风味,丰富了苹果脆片的香气轮廓。电子鼻响应雷达图分析表明不同温度热风处理的苹果脆片香气轮廓存在差异。PCA结果显示,鲜样与干燥样品之间通过电子鼻能够进行很好的区分。通过对鲜样及不同温度热风干燥苹果脆片挥发性化合物分析及关键香气成分的研究,为苹果脆片热风干燥工艺的改进提供了理论依据。综合考虑香气、能耗,相比于50 ℃热风处理,80 ℃可以在短时间内使苹果片呈现热风脱水制品的特征性风味。因此,80 ℃热风干燥条件最佳。
-
表 1 PEN3电子鼻传感器性能描述
Table 1 Description of PEN3 electronic nose sensor performance
阵列序号 传感器 性能描述 R1 W1C 对芳烃成分,苯类灵敏 R2 W5S 对氮氧化合物灵敏 R3 W3C 对芳香成分灵敏,氨类灵敏 R4 W6S 主要对氢类灵敏 R5 W5C 对短链烷烃、芳香成分灵敏 R6 W1S 对甲基类灵敏 R7 W1W 对硫化物灵敏 R8 W2S 对醇类,醛酮类灵敏 R9 W2W 对芳香成分,有机硫化物灵敏 R10 W3S 对长链烷烃灵敏 表 2 苹果鲜样以及热风干燥苹果脆片挥发性化合物定性、定量结果
Table 2 Identification and quantification of volatile compounds in fresh apple and hot-air dried apple slices
序号 化合物名称 保留时间
(min)CAS 保留指数 含量(mg/kg d.b) 定性方法 参考值 实验值 鲜样 50 ℃ 60 ℃ 70 ℃ 80 ℃ 酯类 1 丁酸乙酯 5.361 105-54-4 1034 1034 13.552±1.791a − − − − MS/RI 2 2-甲基丁酸乙酯 5.723 7452-79-1 1050 1049 12.176±1.551a − − − − MS/RI 3 乙酸丁酯 6.178 123-86-4 1071 1069 7.949±1.361a − − − − MS/RI 4 2-甲基丁基乙酸酯 7.367 624-41-9 1120 1117 46.815±8.915a − − − − MS/RI 5 乙酸戊酯 8.804 628-63-7 1172 1171 0.699±0.195a − − − − MS/RI 6 己酸甲酯 9.166 106-70-7 1181 1184 3.669±1.293a 0.099±0.033b − − − MS/RI 7 丁酸丁酯 10.049 109-21-7 1219 1217 8.567±1.555a − − − − MS/RI 8 己酸乙酯 10.505 123-66-0 1233 1233 4.484±1.847a 0.46±0.062b 0.082±0.019b − − MS/RI 9 乙酸己酯 11.587 142-92-7 1271 1273 29.713±5.194a 0.483±0.067b 0.167±0.031b 0.199±0.008b − MS/RI 10 2-甲基丁酸2-甲基丁酯 11.859 2445-78-5 1285 1283 0.546±0.351a − − − − MS/RI 11 己酸丙酯 12.85 626-77-7 1322 1319 1.335±0.280a − − − − MS/RI 12 异丁酸己酯 13.555 2349-07-7 1339 1346 0.364±0.126a 0.044±0.006b − − − MS/RI 13 辛酸甲酯 14.74 111-11-5 1390 1390 − 0.110±0.032a 0.03±0.012b 0.035±0.008b 0.033±0.002b MS/RI 14 己酸丁酯 15.405 626-82-4 1412 1416 1.429±0.890a 0.058±.0b 0.010±0.002b − − MS/RI 15 丁酸己酯 15.484 2639-63-6 1412 1419 22.895±4.245a 0.408±0.034b 0.169±0.031b 0.236±0.031b 0.352±0.004b MS/RI 16 2-甲基丁酸己酯 15.771 10032-15-2 1429 1430 16.623±3.066a 2.533±0.187b 1.692±0.274b 2.343±0.273b 2.204±0.032b MS/RI 17 辛酸乙酯 15.937 106-32-1 1434 1437 − 0.091±0.009a 0.048±0.019b − − MS/RI 18 丙酸庚酯 16.1 2216-81-1 1446 1443 0.168±0.056a − − − − MS/RI 19 壬酸甲酯 17.412 1731-84-6 1485 1494 2.303±0.407a − 0.075±0.005b 0.171±0.016b 0.198±0.067b MS/RI 20 3-羟基丁酸乙酯 18.046 5405-41-4 1515 1521 − 1.564±0.163a 0.428±0.080b − − MS/RI 21 己酸己酯 20.18 6378-65-0 1603 1615 5.480±1.262a 0.526±0.021b 0.117±0.018b 0.082±0.011b 0.188±0.007b MS/RI 22 月桂酸甲酯 23.27 111-82-0 1798 1806 0.230±0.062a − − − MS/RI 23 棕榈酸甲酯 27.854 112-39-0 2207 2224 0.059±0.029b 0.173±0.048a 0.104±0.022b 0.217±0.068a 0.383±0.278a MS/RI 醇类 24 丁醇 8.297 71-36-3 1146 1152 2.363±0.762a − − − − MS/RI 25 2-甲基-1-丁醇 9.868 137-32-6 1208 1210 − 0.513±0.055a 0.264±0.046b 0.316±0.041b 0.114±0.063c MS/RI 26 戊醇 11.075 71-41-0 1248 1254 − 0.076±0.053a 0.012±0.002b − − MS/RI 27 2-庚醇 13.054 543-49-7 1312 1327 0.253±0.047a − − − − MS/RI 28 己醇 13.935 111-27-3 1351 1360 16.733±3.468a 2.855±0.332b 1.179±0.216b 1.871±0.152b 0.944±0.057b MS/RI 29 3-辛醇 15.011 589-98-0 1388 1400 0.579±0.196a − − − − MS/RI 30 1-辛烯-3-醇 16.435 3391-86-4 1448 1456 0.080±0.026a 0.043±0.008b 0.018±0.003c 0.070±0.003a 0.078±0.005a MS/RI 31 庚醇 16.587 111-70-6 1449 1462 0.560±0.113a 0.156±0.016b − − − MS/RI 32 6-甲基-5-庚烯-2-醇 16.788 1569-60-4 1466 1470 4.836±0.809a 0.155±0.020b 0.071±0.013b 0.109±0.009b 0.190±0.012b MS/RI 33 2,3-丁二醇 18.639 513-85-9 1553 1546 − 0.81±0.058a 0.440±0.070b 0.404±0.047b 0.425±0.01b MS/RI 34 芳樟醇 18.846 78-70-6 1542 1555 0.278±0.045a 0.067±0.008c 0.047±0.008c 0.133±0.02b 0.137±0.005b MS/RI 35 辛醇 19.125 111-87-5 1554 1567 0.403±0.083a 0.351±0.023a 0.179±0.030b 0.360±0.004a − MS/RI 36 4-萜烯醇 20.012 562-74-3 1603 1605 0.109±0.017a − − − − MS/RI 37 3-甲基-4-庚醇 21.856 1838-73-9 / 1709 − 0.865±0.03d 0.538±0.106c 0.689±0.050b 1.123±0.035a MS 38 香茅醇 22.807 106-22-9 1764 1774 0.147±0.042a 0.046±0a 0.029±0.016a 0.043±0a 0.030±0a MS/RI 39 苯甲醇 24.232 100-51-6 1865 1882 − 0.049±0.018ab 0.031±0.007b 0.056±0.007a 0.055±0.008a MS/RI 40 苯乙醇 24.666 60-12-8 1907 1918 − 0.141±0.01a 0.056±0.010d 0.113±0.009b 0.099±0.003c MS/RI 41 1,3-辛二醇 27.051 23433-05-8 2128 2141 0.514±0.176d 9.020±1.169b 4.564±1.102c 8.248±0.717b 12.506±1.086a MS/RI 醛类 42 己醛 6.347 66-25-1 1078 1076 71.273±18.000a 0.693±0.251b 0.265±0.098b − − MS/RI 43 反式-2-己烯醛 9.965 6728-26-3 1218 1214 18.580±6.466a − − − − MS/RI 44 辛醛 11.972 124-13-0 1287 1287 − 0.124±0.029a 0.052±0.011b 0.069±0.007b 0.050±0.000b MS/RI 45 反式-2-庚烯醛 12.877 18829-55-5 1325 1320 − 0.050±0.014a − 0.038±0.002a 0.040±0.013a MS/RI 46 壬醛 14.83 124-19-6 1390 1393 1.535±0.230a 0.117±0.052b 0.047±0.012b 0.079±0.011b 0.074±0.009b MS/RI 47 癸醛 17.532 112-31-2 1493 1499 0.416±0.083a − 0.076±0.013c 0.179±0.025b − MS/RI 48 反式-2-壬烯醛 18.401 18829-56-6 1533 1536 0.229±0.041a 0.062±0.009cd 0.036±0.007d 0.095±0.011bc 0.101±0.005a MS/RI 49 橙花醛 22.217 141-27-5 1726 1733 − 0.051±0.005a − 0.038±0.002a 0.052±0.000ab MS/RI 烯烃类 50 柠檬烯 9.395 138-86-3 1197 1193 − 0.149±0.072a 0.031±0.000bc 0.139±0.057a 0.106±0.017ab MS/RI 51 α-法尼烯 22.494 502-61-4 1737 1752 98.145±16.616a 37.474±1.425a 19.353±2.875b 12.303±1.811b 33.565±0.367a MS/RI 酮类 52 3-羟基-2-丁酮 11.821 513-86-0 1285 1281 − 0.904±0.091a 0.306±0.053d 0.527±0.045c 0.660±0.064b MS/RI 53 6-甲基-5-庚烯-2-酮 13.347 110-93-0 1339 1338 0.660±0.070b 0.592±0.078b 0.266±0.053c 0.598±0.044b 0.766±0.036a MS/RI 内酯类 54 γ-己内酯 21.691 695-06-7 1691 1698 − 0.138±0.012a 0.088±0.016c 0.088±0.012b 0.125±0.011b MS/RI 55 γ-壬内酯 25.989 104-61-0 2027 2037 − − 0.054±0.020a 0.111±0.003a − MS/RI 56 δ-癸内酯 27.719 705-86-2 2193 2209 − 0.060±0.052a 0.030±0.001b − − MS/RI 酸类 57 2-羟基-2-甲基丁酸 20.879 3739-30-8 / 1653 − 0.161±0.014c 0.114±0.019d 0.255±0.026a 0.214±0.010b MS 含硫化合物 58 2-甲硫基乙醇 18.276 5271-38-5 1537 1531 − 0.058±0.010a 0.033±0.005b 0.036±0.001b 0.027±0.002b MS/RI 59 3-甲硫基丙酸乙酯 19.203 13327-56-5 1566 1570 0.19±0.024a − − − − MS/RI 60 3-甲硫基丙醇 22.059 505-10-2 1722 1723 0.12±0.039d 1.666±0.063a 0.725±0.124c 0.837±0.093c 1.135±0.029b MS/RI 杂环类化合物 61 2-戊基呋喃 10.42 3777-69-3 1235 1230 − 0.153±0.035a 0.086±0.027b 0.183±0.030a 0.136±0.020a MS/RI 62 糠醛 16.555 98-01-1 1463 1461 − − 0.099±0.016c 0.814±0.080b 1.56±0.061a MS/RI 63 2-呋喃甲醇 21.095 98-00-0 1651 1665 − 0.039±0.004a 0.009±0.001c 0.021±0.002b − MS/RI 64 5-羟甲基糠醛 30.411 67-47-0 2505 2511 − − − 0.019±0.003b 0.031±0.001a MS/RI 注:“−”表示未检测到该种物质;“/”表示未查询到该物质的参考RI值;不同小写字母代表每种化合物P<0.05水平下不同样品间含量差异显著。 表 3 苹果鲜样以及4种不同温度热风干燥苹果脆片挥发性化合物OAV
Table 3 OAV of volatile compounds in fresh apple and four hot air dried apple slices at different temperatures
化合物 气味特征 阈值(mg/kg) OAV 鲜样 50 ℃ 60 ℃ 70 ℃ 80 ℃ 丁酸乙酯 苹果味、果香 0.0005 27103.34 − − − − 2-甲基丁酸乙酯 苹果香、果香 0.000013 936583.12 − − − − 乙酸丁酯 苹果香、甜香 0.058 137.06 − − − − 2-甲基丁基乙酸酯 苹果香、梨香 0.008 5851.91 − − − − 乙酸戊酯 香蕉味、果香、甜香 0.043 16.25 − − − − 己酸甲酯 果香、新鲜、甜香 0.07 52.41 1.42 − − − 丁酸丁酯 花香 0.4 21.42 − − − − 己酸乙酯 香蕉味、苹果皮味 0.0022 2038.17 209.29 37.46 − − 乙酸己酯 苹果香、浆果香 0.115 258.37 4.20 1.45 1.73 − 2-甲基丁酸2-甲基丁酯 水果味 0.075 7.28 − − − − 异丁酸己酯 nd 0.0173 21.02 2.56 − − − 丁酸己酯 苹果皮香、柑橘香 0.203 112.78 2.01 <1 1.16 1.73 2-甲基丁酸己酯 草莓味 0.022 755.61 115.16 76.90 106.50 100.18 辛酸乙酯 香蕉味、菠萝味 0.0193 − 4.72 2.49 − − 丙酸庚酯 nd 0.004 41.99 − − − − 壬酸甲酯 椰子味、果香 0.046 50.07 − 1.63 3.72 4.31 月桂酸甲酯 椰子味、脂肪味 0.002 115.08 − − − − 正丁醇 酒精味 0.4592 5.15 − − − − 2-甲基-1-丁醇 燃料味、麦芽味 0.0159 − 32.26 16.58 19.89 7.16 2-庚醇 柑橘味 0.065235 3.88 − − − − 己醇 清香、草本香、木香 0.0056 2988.00 509.90 210.55 334.09 168.54 3-辛醇 柑橘味、坚果味 0.15 3.86 − − − − 1-辛烯-3-醇 蘑菇味 0.0015 53.12 28.97 12.08 46.57 51.80 正庚醇 腐臭味 0.0054 103.71 28.86 − − − 6-甲基-5-庚烯-2-醇 清香 2 2.42 <1 <1 <1 <1 芳樟醇 花香 0.00022 1264.30 302.31 212.75 605.14 623.18 辛醇 脂肪味 0.11 3.66 3.19 1.63 3.28 − 3-甲基-4-庚醇 nd 0.078 − 11.09 6.90 8.83 14.39 香茅醇 柑橘味、玫瑰香 0.062 2.37 <1 <1 <1 <1 苯乙醇 玫瑰香、甜苹果味 0.012 − 11.77 4.67 9.40 8.25 己醛 青草味、脂肪味 0.005 14254.57 138.59 52.92 − − 反式-2-己烯醛 脂肪味、绿色 0.03 619.33 − − − − 辛醛 脂肪香、坚果味 0.000587 − 211.25 88.42 117.30 84.36 壬醛 柑橘香、脂肪味 0.001 1534.99 116.94 47.36 79.36 73.63 癸醛 脂肪味、花香 0.003 138.76 − 25.42 59.74 − 反式-2-壬烯醛 黄瓜味、青草味 0.00019 1202.98 328.67 189.38 500.73 533.78 橙花醛 花香、果香、柠檬味 0.037 − 1.39 − 1.04 1.41 3-羟基-2-丁酮 黄油味、奶油味 0.014 − 64.57 21.86 37.61 47.17 6-甲基-5-庚烯-2-酮 柑橘味、胡椒味 0.068 9.71 8.70 3.90 8.80 11.27 γ-壬内酯 可可香、桃香 0.0097 − − 5.58 11.44 − 3-甲硫基丙酸乙酯 卷心菜、青草味 0.00845 22.54 − − − − 3-甲硫基丙醇 熟牛奶味、熟土豆味、泥土味 0.12323 − 13.52 5.88 6.79 9.21 2-戊基呋喃 黄油味、花香、果香 0.0058 − 26.44 14.88 31.54 23.52 α-法尼烯 柑橘香、花香、甜香 0.0077 12746.11 4866.72 2513.41 1597.75 4359.11 Total 1008125 7044 3554 3592 6123 注:“−”表示未检测到该种物质;“nd”表示未查阅到该种化合物的气味特征描述词;气味特征描述参照Vcf Home网站[43]和Flavornet网站[44]。 -
[1] 王崧百. 苹果脆片产业发展研究[J]. 食品安全导刊,2021(26):166−168. [WANG S B. Study on the development of apple chips industry[J]. China Food Safety Magazine,2021(26):166−168. doi: 10.16043/j.cnki.cfs.2021.26.111 WANG S B. Study on the development of apple chips industry[J]. China Food Safety Magazine, 2021(26): 166-168. doi: 10.16043/j.cnki.cfs.2021.26.111
[2] 楚倩倩, 任广跃, 段续, 等. 过热蒸汽和热风干燥在食品领域中的应用对比[J/OL]. 食品与发酵工业: 1−12[2022-01-08] CHU Q Q, REN G Y, DUAN X, et al. Application comparison of superheated steam and hot-air drying in the food field[J/OL]. Food and Fermentation Industries: 1−12[2022-01-08].
[3] 莫一凡, 姚凌云, 冯涛, 等. 水果干风味物质及干燥方式的影响研究[J]. 中国果菜,2020,40(6):23−28,40. [MO Y F, YAO L Y, FENG T, et al. Study on flavor substances of dried fruits and the effects of drying methods[J]. China Fruit & Vegetable,2020,40(6):23−28,40. 6): 23-28, 40. MO Y F, YAO L Y, FENG T, et al. Study on flavor substances of dried fruits and the effects of drying methods[J]. China Fruit & Vegetable, 2020, 40(6): 23-28, 40.
[4] 郭卫芸, 李光辉, 张珍珍, 等. 香椿中特征性香气成分定量分析及其在热风干燥过程中的变化规律[J]. 食品研究与开发,2021,42(3):14−19. [GUO W Y, LI G H, ZHANG Z Z, et al. Quantitative analysis of Toona sinensis aroma components and viariation rule during hot air dry process[J]. Food Research and Development,2021,42(3):14−19. GUO W Y, LI G H, ZHANG Z Z, et al. Quantitative analysis of Toona sinensis aroma components and viariation rule during hot air dry process[J]. Food Research and Development, 2021, 42(3): 14-19.
[5] DIMICK P S, HOSKIN J C, ACREE T E. Review of apple flavor-State of the art[J]. C R C Critical Reviews in Food Science & Nutrition,1983,18:387−409.
[6] REIS S, ROCHA S, BARROS A, et al. Establishment of the volatile profile of ‘Bravo de Esmolfe’ apple variety and identification of varietal markers[J]. Food Chemistry,2009,113(2):513−521. doi: 10.1016/j.foodchem.2008.07.093
[7] 石芬, 徐军, 姜宗伯, 等. HS-SPME-GC-MS结合多元统计分析初榨椰子油常温储藏过程中挥发性风味成分[J]. 食品工业科技, 2022, 43(10):314-322. SHI F, XU J, JIANG Z B, et al. Analysis of volatile flavor components of virgin coconut oil during normal temperature storage based on HS-SPME-GC-MS and multivariate statistical analysis[J]. Science and Technology of Food Industry, 2022, 43(10):314-322.
[8] 王铁儒, 郭丽, 马曼, 等. SPME-GC-MS与电子鼻结合分析不同酵母混菌发酵猕猴桃酒的挥发性香气物质[J]. 食品工业科技,2021,42(16):119−128. [WANG T R, GUO L, MA M, et al. Analysis of volatile aroma compounds in kiwi wine co-fermentation with different yeasts by SPME-GC-MS combined with electronic nose[J]. Science and Technology of Food Industry,2021,42(16):119−128. doi: 10.13386/j.issn1002-0306.2021010133 WANG T R, GUO L, MA M, et al. Analysis of volatile aroma compounds in kiwi wine co-fermentation with different yeasts by SPME-GC-MS combined with electronic nose[J]. Science and Technology of Food Industry, 2021, 42(16): 119-128. doi: 10.13386/j.issn1002-0306.2021010133
[9] TIMOUMI S, MIHOUBI D, ZAGROUBA F. Shrinkage, vitamin C degradation and aroma losses during infra-red drying of apple slices[J]. LWT-Food Science and Technology,2007,40:1648−1654. doi: 10.1016/j.lwt.2006.11.008
[10] KROKIDA M K, PHILIPPOPOULOS C. Volatility of apples during air and freeze drying[J]. Journal of Food Engineering,2006,73(2):135−141. doi: 10.1016/j.jfoodeng.2005.01.012
[11] SONG J, CHEN Q, BI J, et al. GC/MS coupled with MOS e-nose and flash GC e-nose for volatile characterization of Chinese jujubes as affected by different drying methods[J]. Food Chemistry,2020,331:127201. doi: 10.1016/j.foodchem.2020.127201
[12] 曹有芳, 刘丹, 徐俊南, 等. 基于电子鼻和气相色谱-质谱联用技术分析不同品种苹果酒香气物质[J]. 中国酿造,2020,39(2):182−188. [CAO Y F, LIU D, XV J N, et al. Analysis of aroma substances in apple wines brewed with different varieties of apple by electronic nose combined with GC-MS[J]. China Brewing,2020,39(2):182−188. doi: 10.11882/j.issn.0254-5071.2020.02.034 CAO Y F, LIU D, XV J N, et al. Analysis of aroma substances in apple wines brewed with different varieties of apple by electronic nose combined with GC-MS[J]. China Brewing, 2020, 39(2): 182-188. doi: 10.11882/j.issn.0254-5071.2020.02.034
[13] 农业部农产品加工局. NY/T 2779-2015 苹果脆片[S]. 北京: 中国人民共和国农业部, 2015. Agricultural Products Processing Bureau of Ministry of Agriculture. NY/T 2779-2015 Apple crisp chips[S]. Beijing: The Ministry of Agriculture of the People’s Republic of China, 2015.
[14] 曾辉. 不同品种苹果特征香气的表征与识别[D]. 长沙: 湖南农业大学, 2016. ZENG H. Research on representation and recognition of characteristic aroma of different apple cultivars[D]. Changsha: Hunan Agricultural University, 2016.
[15] 于怀龙, 马永昆, 张荣, 等. 不同品种桑椹香气成分的主成分分析[J]. 食品工业科技,2016,37(10):62−66,71. [YU H L, MA Y K, ZHANG R, et al. Principal component analysis of aroma components in mulberry from different varieties[J]. Science and Technology of Food Industry,2016,37(10):62−66,71. doi: 10.13386/j.issn1002-0306.2016.10.003 YU H L, MA Y K, ZHANG R, et al. Principal component analysis of aroma components in mulberry from different varieties[J]. Science and Technology of Food Industry, 2016, 37(10): 62-66, 71. doi: 10.13386/j.issn1002-0306.2016.10.003
[16] 万鹏, 梁国平, 马丽娟, 等. 19个苹果品种果实香气成分的GC-MS分析[J]. 食品工业科技,2019,40(14):227−232. [WAN P, LIANG G P, MA L J, et al. GC-MS analysis of fruit aroma components in 19 apple varieties[J]. Science and Technology of Food Industry,2019,40(14):227−232. WAN P, LIANG G P, MA L J, et al. GC-MS analysis of fruit aroma components in 19 apple varieties[J]. Science and Technology of Food Industry, 2019, 40(14): 227-232.
[17] ZHU J, CHEN F, WANG L, et al. Characterization of the key aroma volatile compounds in cranberry (Vaccinium macrocarpon Ait. ) using gas chromatography–olfactometry (GC-O) and odor activity value (OAV)[J]. Journal of Agricultural and Food Chemistry,2016,64:4990−4999. doi: 10.1021/acs.jafc.6b01150
[18] DIXON J, HEWETT E W. Factors affecting apple aroma/flavour volatile concentration: A review[J]. New Zealand Journal of Crop and Horticultural Science,2000,28(3):155−173. doi: 10.1080/01140671.2000.9514136
[19] GIRARD B, LAU O L. Effect of maturity and storage on quality and volatile production of “Jonagold” apples[J]. Food Research International,1995,28(5):465−471. doi: 10.1016/0963-9969(96)81393-7
[20] APREA E, COROLLARO M L, BETTA E, et al. Sensory and instrumental profiling of 18 apple cultivars to investigate the relation between perceived quality and odour and flavour[J]. Food Research International,2012,49(2):677−686. doi: 10.1016/j.foodres.2012.09.023
[21] ZHANG J, CAO Z, PEI P, et al. Volatile flavour components and the mechanisms underlying their production in golden pompano (Trachinotus blochii) fillets subjected to different drying methods: A comparative study using an electronic nose, an electronic tongue and SDE-GC-MS[J]. Food Research International,2019,123:217−225. doi: 10.1016/j.foodres.2019.04.069
[22] 张志兵, 连琛, 詹瑞玲, 等. 气相色谱-质谱联用法分析不同品种苹果酿造蒸馏酒中香气成分及特征[J]. 中国酿造,2021,40(9):191−195. [ZHANG Z B, LIAN S, ZHAN R L, et al. Analysis of aroma components and characteristics in apple distillations brewed with different varieties of apple by GC-MS[J]. China Brewing,2021,40(9):191−195. doi: 10.11882/j.issn.0254-5071.2021.09.034 ZHANG Z B, LIAN S, ZHAN R L, et al. Analysis of aroma components and characteristics in apple distillations brewed with different varieties of apple by GC-MS[J]. China Brewing, 2021, 40(9): 191-195. doi: 10.11882/j.issn.0254-5071.2021.09.034
[23] 赵志聪, 白启正, 连琛, 等. 苹果白兰地原酒蒸馏过程中挥发性香气成分的变化[J]. 现代食品,2021(15):80−85. [ZHAO Z C, BAI Q Z, LIAN C, et al. Changes of volatile aroma components during distillation of apple brandy[J]. Modern Food,2021(15):80−85. doi: 10.16736/j.cnki.cn41-1434/ts.2021.15.021 ZHAO Z C, BAI Q Z, LIAN C, et al. Changes of volatile aroma components during distillation of apple brandy[J]. Modern Food, 2021(15): 80-85. doi: 10.16736/j.cnki.cn41-1434/ts.2021.15.021
[24] 裴鹏正, 贠建民, 贾琦, 等. 软儿梨果酒发酵过程中挥发性风味物质变化分析[J]. 生物技术进展,2021,11(6):758−769. [PEI P Z, YUN J M, JIA Q, et al. Analysis on changes of volatile flavor compounds in Zuan’er pear wine during fermentation[J]. Current Biotechnology,2021,11(6):758−769. doi: 10.19586/j.2095-2341.2021.0086 PEI P Z, YUN J M, JIA Q, et al. Analysis on changes of volatile flavor compounds in Zuan’er pear wine during fermentation[J]. Current Biotechnology, 2021, 11(6): 758-769. doi: 10.19586/j.2095-2341.2021.0086
[25] CHUNG H Y, YUNG I, MA W, et al. Analysis of volatile components in frozen and dried scallops (Patinopecten yessoensis) by gas chromatography/mass spectrometry[J]. Food Research International,2002,35(1):43−53. doi: 10.1016/S0963-9969(01)00107-7
[26] LIU H, WANG Z, ZHANG D, et al. Characterization of key aroma compounds in Beijing Roasted Duck by gas chromatography-olfactometry-mass spectrometry, odor activity values and aroma recombination experiments[J]. Journal of Agricultural and Food Chemistry, 2019, 67(20):5847−5856.
[27] TAIRU A O, HOFMANN T, SCHIEBERLE P. Characterization of the key aroma compounds in dried fruits of the West African peppertree Xylopia aethiopica (Dunal) A. Rich (Annonaceae) using aroma extract dilution analysis[J]. Journal of Agricultural & Food Chemistry,1999,47(8):3285−3287.
[28] JORRY, DHARMAWAN, STEFAN, et al. Evaluation of aroma-active compounds in pontianak orange peel oil (Citrus nobilis Lour. Var. microcarpa Hassk.) by gas chromatography olfactometry, aroma reconstitution, and omission test[J]. Journal of Agricultural and Food Chemistry,2009,57(1):239−244. doi: 10.1021/jf801070r
[29] VANOLI M, VISAI C, RIZZOLO A. The influence of harvest date on the volatile composition of 'Starkspur Golden' apples[J]. Postharvest Biology and Technology,1995,6(3):225−234.
[30] VARMING C, ANDERSEN M L. Influence of thermal treatment on black currant (Ribes nigrum L.) juice aroma[J]. Journal of Agricultural & Food Chemistry,2004,52(25):7628−7636.
[31] BERDAGUE J L, MONTEIL P, MONTEL M C, et al. Talon effects of starter cultures on the formation of flavour compounds in dry sausage[J]. Meat Science,1993,35:275−287. doi: 10.1016/0309-1740(93)90033-E
[32] BARBIERI G, BOLZONI L, PAROLARI G, et al. Flavor compounds of dry-cured ham[J]. Journal of Agricultural & Food Chemistry,1992,40(12):2389−2394.
[33] PELLEGRINO, CONTE, GENNARO, et al. Comparing different processing methods in apple slice drying. Part 2 solid-state fast field cycling 1H-NMR relaxation properties, shrinkage and changes in volatile compounds[J]. Biosystems Engineering,2019,188:345−354. doi: 10.1016/j.biosystemseng.2019.10.020
[34] MISHARINA T A, MUHUTDINOVA S M, ZHARIKOVA G G, et al. Formation of flavor of dry champignons (Agaricus bisporus L.)[J]. Applied Biochemistry & Microbiology,2010,46(1):108−113.
[35] VALAPPIL Z A, FAN X, ZHANG H Q, et al. Impact of thermal and nonthermal processing technologies on unfermented apple cider aroma volatiles[J]. J Agric Food Chem,2009,57(3):924−929. doi: 10.1021/jf803142d
[36] MOREIRA N, MENDES F, PEREIRA O, et al. Volatile sulphur compounds in wines related to yeast metabolism and nitrogen composition of grape musts[J]. Analytica Chimica Acta,2002,458(1):157−167. doi: 10.1016/S0003-2670(01)01618-X
[37] METHVEN L, MARIA. Influence of sulfur amino acids on the volatile and nonvolatile components of cooked salmon (Salmo salar)[J]. Journal of Agricultural and Food Chemistry,2007,55(4):1427−1436. doi: 10.1021/jf0625611
[38] RODRIGO O S, CONSUELO D M, SOLEDAD P C, et al. Viability of pre-treatment drying methods on mango peel by-products to preserve flavouring active compounds for its revalorisation-ScienceDirect[J]. Journal of Food Engineering,2020,279:109953. doi: 10.1016/j.jfoodeng.2020.109953
[39] GOKMEN V, MORALES F. Processing contaminants: Hydroxymethylfurfural[J]. Encyclopedia of Food Safety,2014,2:404−408.
[40] RANNOU C, LAROQUE D, RENAULT E, et al. Mitigation strategies of acrylamide, furans, heterocyclic amines and browning during the maillard reaction in foods[J]. Food Research International,2016,90(PT.3):154−176.
[41] AMEUR L A, REGA B, GIAMPAOLI P, et al. The fate of furfurals and other volatile markers during the baking process of a model cookie[J]. Food Chemistry,2008,111(3):758−763. doi: 10.1016/j.foodchem.2007.12.062
[42] 里奥·范海默特. 化合物香味阈值汇编[M]. 北京: 科学出版社, 2015. VAN GEMERT J L. Compilations of flavour threshold values in water and other media[M]. Beijing: Science Press, 2015.
[43] VCF online by BeWiDo BV Inc. Volatile compounds in food[DB/OL]. [2021-11-30].https://www.vcf-online.nl/VcfHome.cfm.
[44] Gas chromatography-olfactometry (GCO) of natural products sponsored by DATU Inc. Flavornet and human odor space[DB/OL]. [2021-11-30]. http://www.flavornet.org/flavornet.html.
-
期刊类型引用(5)
1. 潘冠均,段淋渊,赵嘉科,帅平,戴国礼,田维素,王金源,黄佳鹏,闭晓彤,林恩照,秦垦,郝志龙,张波. 摊放程度对枸杞芽叶茶风味品质的影响. 食品工业科技. 2025(04): 117-126 .  本站查看
本站查看
2. 吴宗杰,欧晓西,林宏政,余欣茹,程守悦,吴晴阳,李鑫磊,孙云. 武夷肉桂加工中挥发性成分糖苷结合物和香气品质形成研究. 茶叶科学. 2024(01): 84-100 .  百度学术
百度学术
3. 潘冠均,封娇,段淋渊,张炫鹂,戴国礼,帅平,秦垦,郝志龙,张波. 不同单株枸杞芽叶茶风味品质分析. 食品工业科技. 2024(15): 264-273 .  本站查看
本站查看
4. 徐晓俞,李程勋,李爱萍,郑开斌,潘键,侯明香. 肉桂茶纯露挥发性成分分析. 福建农业科技. 2024(06): 49-55 .  百度学术
百度学术
5. 占鑫怡,杨云,陈彬,黄慧清,赵梦莹,李鑫磊,孙云. 不同摇青程度春闺闽北乌龙茶品质差异分析. 食品工业科技. 2023(11): 271-279 .  本站查看
本站查看
其他类型引用(2)








 下载:
下载:
 下载:
下载:



