The Improvement of Lactobacillus plantarum Fermented Milk in Characterization and Anti-Bacillus cereus Activity by Galactooligosacchari
-
摘要: 为探究低聚半乳糖对植物乳杆菌发酵乳特性及抗菌活性的影响,本文采用单因素法考察影响发酵乳特性的主要因素,并以响应面法优化发酵乳最佳发酵条件;以产肠毒素蜡样芽孢杆菌HN001为指示菌,探究低聚半乳糖的添加对植物乳杆菌ZDY2013发酵乳抑菌活性的改善作用。结果表明:植物乳杆菌能有效利用低聚半乳糖进行体外代谢,并抑制蜡样芽孢杆菌生长;牛奶中添加适量低聚半乳糖能够增加植物乳杆菌发酵乳中的活菌数、降低发酵乳的pH,并提高其持水力;响应面分析发现低聚半乳糖发酵乳的最佳制备条件为:2.0%的植物乳杆菌接种量、1.0%的低聚半乳糖添加量、发酵时间为24 h及发酵温度为42 ℃;添加低聚半乳糖的发酵乳能有效控制产肠毒素蜡样芽孢杆菌浓度在106 CFU/mL以下。该研究结果为低聚半乳糖及植物乳杆菌ZDY2013在发酵乳中的应用奠定了理论基础。Abstract: In order to test the effect of galactooligosaccharide (GOS) on the characterization and antibacterial activity of milk fermented by Lactobacillus plantarum, the main factors affecting the fermented milk were investigated and the most suitable fermentation conditions for improving the characterization of fermented milk were obtained with response surface analysis. The enterotoxigenic Bacillus cereus HN001 was used as an indicator to study the effect of GOS addition on the antibacterial activity of L. plantarum ZDY2013 fermented milk. The results showed that L. plantarum could use GOS for metabolism in vitro and inhibit the growth of B. cereus effectively. The proper addition of GOS in milk could increase the number of viable bacteria, reduce the pH and enhance the water holding capacity of L. plantarum fermented milk. The result from response surface analysis was found that the best fermentation conditions for fermented milk were 2.0% inoculums of L. plantarum, 1.0% GOS, fermented at 42 ℃ for 24 h. Additionally, GOS addition in fermented milk could effectively control the concentration of enterotoxigenic B. cereus HN001 to below 106 CFU/mL. The results of this study provide the foundation for the application of GOS and L. plantarum ZDY2013 in fermented milk.
-
益生乳酸菌因具有调节宿主健康并改善发酵食品风味的特点而得到广泛的应用[1-2]。乳制品作为乳酸菌应用最常规的载体[3-4],具有为乳酸菌提供保护剂的功能,同时可以为菌株发酵提供丰富的营养物质。乳酸菌代谢产生的代谢物,如乳糖酶和蛋白分解酶,可分别分解牛奶里的乳糖和蛋白质,并产生有机酸等小分子代谢产物,有利于人体消化吸收[5-7]。
植物乳杆菌ZDY2013是一株分离于自然发酵酸豆角中,且具有自主知识产权的优势菌株,具有耐受胃肠道环境并调节宿主肠道菌群的能力[8-9]。前期研究表明,植物乳杆菌ZDY2013展现了良好乳制品发酵剂的作用,能用于牛奶发酵,并能抑制污染各类乳制品的食源致病蜡样芽孢杆菌在发酵过程中的生长[10],同时该菌发酵的牛奶可有效预防由产肠毒素蜡样芽孢杆菌引起的肠道菌群稳态失衡[11]。因此,该植物乳杆菌应用于乳制品生产将有效防止发酵乳被该致病菌污染,从而提升发酵乳的安全性。
低聚半乳糖(Galactooligosaccharide,GOS)是一类肠道微生物可获得性碳水化合物(Microbiota-accessible carbohydrate,MAC),能不被肠道消化吸收,直接进入大肠供肠道固有乳酸菌代谢使用,具有益生元特性[12-13]。研究表明,低聚半乳糖在动物的乳汁中有微量的存在,而人母乳中含量相对较多[14],被认为是一种乳源性功能低聚糖,可以改善肠道菌群的稳定性,为婴幼儿健康发育不可或缺的成分[15-16]。研究发现低聚半乳糖可以降低多种类型腹泻疾病的风险,包括旅行者腹泻、渗透性腹泻和艰难梭菌相关复发性腹泻[17-19],还可以通过改善优势益生菌属的定植来达到促进肠道健康,进而预防炎症性肠病以及便秘等[20-22]的目的。
目前,低聚半乳糖主要应用于婴儿配方奶粉、糕点、面包等。据报道,添加低聚半乳糖在奶粉中可促进宿主体内双歧杆菌和鼠李糖乳杆菌的生长[13];摄入添加了低聚半乳糖的酸奶能够提高肠道菌群的丰度、短链脂肪酸的产量以及钙的利用率[23]。因此,开发兼具益生菌和益生元功能,或协同功能的乳制品是丰富该领域产品的有效策略。为此,本文在确定低聚半乳糖能促进植物乳杆菌ZDY2013体外代谢的基础上,进一步采用响应面法分析多种因素对发酵乳特性的影响,并考察低聚半乳糖对植物乳杆菌发酵乳抑制食源性产肠毒素蜡样芽孢杆菌的改善作用。本研究将为低聚半乳糖在发酵乳中的应用,及植物乳杆菌ZDY2013的功能开发提供理论基础。
1. 材料与方法
1.1 材料与仪器
植物乳杆菌(Lactobacillus plantarum)ZDY2013、产肠毒素蜡样芽孢杆菌(Bacillus cereus)HN001 均保存于食品科学与技术国家重点实验室;葡萄糖、低聚半乳糖、胰蛋白胨、牛肉膏、酵母提取物、MRS培养基 北京索莱宝科技有限公司;氯化铵、四水硫酸镁、磷酸氢二钾、磷酸二氢钾、半胱氨酸盐酸盐、七水硫酸镁、吐温-80 西陇化工股份有限公司;其他有机试剂均为国产分析纯。
Anaerobox IV型厌氧培养箱 美国Gene Science公司;ZXSD-B1090型恒温培养箱 中国上海智城分析仪器有限公司;ST 16R型台式高速冷冻离心机 德国Eppendorf公司;MultiskanGO型全波长酶标仪 美国Thermo Fisher Scientific公司;PHS-3E型pH计 中国上海仪电科学仪器有限公司。
1.2 实验方法
1.2.1 培养基的配制
MRS培养基:称取48 g MRS培养基粉末,加蒸馏水溶解并定容至1 L,锥形瓶分装,121 ℃高温灭菌15 min;LB培养基:称取NaCl 10 g、胰蛋白胨10 g、酵母提取物5 g、加蒸馏水溶解并定容至1 L,121 ℃高压灭菌15 min;Basal MRS(BMRS)培养基[24]:称取胰蛋白胨10.0 g、牛肉膏5.0 g、酵母提取物5.0 g、氯化铵3.0 g、四水硫酸镁0.05 g、磷酸氢二钾4.0 g、磷酸二氢钾2.6 g、半胱氨酸盐酸盐0.5 g、七水硫酸镁0.102 g和吐温-80 1.0 g,加去离子水至1 L,溶解并调pH至6.2±0.1,于121 ℃灭菌15 min。BMRS用于后续改良培养基的配制。
1.2.2 菌株活化
从−80 ℃冰箱取出植物乳杆菌ZDY2013,在MRS固体培养基上划线,于37 ℃静置厌氧培养24 h,将单菌落挑至5 mL液体MRS培养基中,37 ℃静置厌氧培养24 h,以1.0% (v/v)接种量传代两次,使得菌液浓度为1.5×109 CFU/mL。蜡样芽孢杆菌HN001需在LB固体培养基上划线,并传代至5 mL LB培养基中,在37 ℃、180 r/min条件下培养12 h。
1.2.3 低聚半乳糖对植物乳杆菌生长的影响
在BMRS培养基中添加无菌的低聚半乳糖或者葡萄糖溶液,使其终浓度为2.0%(v/v),获得不同改良MRS培养基,其中葡萄糖组作为对照组。取上述活化后的菌液以1.0%(v/v)接种到改良培养基中,于37 ℃条件静置厌氧培养,从2 h开始,每隔2 h取样一次,进行活菌计数。pH测定:取上述传代两次后的菌液1.0%(v/v),添加到含有2.0%葡萄糖或低聚半乳糖的改良MRS培养基中培养,每隔2 h取一次,测量其pH。
1.2.4 植物乳杆菌发酵液的抑菌活性测定
将上述活化后的植物乳杆菌以1.0%(v/v)接种到添加了葡萄糖或低聚半乳糖(2.0%,w/v)的改良MRS培养基中,37 ℃静置厌氧培养24 h,于8000×g离心10 min,发酵上清液备用。将上述活化后的蜡样芽孢杆菌HN001按1%(v/v)的接种量接种至5 mL LB培养中,在37 ℃、180 r/min条件下培养12 h,再用1×PBS对培养液进行10倍稀释,后取100 μL涂布到LB固体培养基上,待菌液晾干后,加入上述150 μL植物乳杆菌发酵上清液于牛津杯,静置20 min,37 ℃培养12 h,记录抑菌圈直径。
1.2.5 不同发酵条件对低聚半乳糖发酵乳特性的影响
1.2.5.1 单因素实验设计
a. 菌株接种量:以接种量0.5%、1.0%、2.0%和3.0% (v/v)的植物乳杆菌重悬液分别接种至已灭菌的10%的脱脂乳(含1.0%的葡萄糖或低聚半乳糖)中,在37 ℃下静置发酵24 h,测定发酵乳中植物乳杆菌的活菌数、pH和持水力;b. 低聚半乳糖浓度:配制含0.5%、1.0%、2.0%和4.0%的葡萄糖或低聚半乳糖的10%的脱脂乳,再接种1.0%的植物乳杆菌重悬液,于37 ℃条件下发酵24 h,测定发酵乳中植物乳杆菌活菌数、pH和持水力;c. 发酵时间:以接种量为1.0%的植物乳杆菌重悬液接种至已灭菌的10%的脱脂乳(含1.0%的葡萄糖或低聚半乳糖)中,在37 ℃条件下分别发酵6、12、24和48 h,测定发酵乳中植物乳杆菌活菌数、pH和持水力;d. 发酵温度:以接种量为1.0%的植物乳杆菌重悬液接种至已灭菌的10%的脱脂乳(含1.0%的葡萄糖或低聚半乳糖)中,分别在27、32、37、42 ℃条件下静置发酵24 h,测定发酵乳中植物乳杆菌活菌数、pH和持水力。
1.2.5.2 发酵乳特性的测定
a. 活菌数:用1×PBS对发酵乳样品进行10倍梯度稀释,接着在MRS固体培养基上涂板,于37 ℃条件下厌氧培养24 h,计算活菌数;b. pH:用PHS-3E型pH计测定不同条件下发酵乳样品的pH;c. 持水性:称取发酵乳样品5 g(M0),在5000×g,4 ℃下离心15 min,除去上清后再称重(M1)。发酵乳持水力计算公式如下:持水力(%)=(M1/M0)×100。
1.2.6 响应面试验优化发酵乳制备条件
根据单因素实验结果,以植物乳杆菌活菌数为响应值,以菌液接种量(X1)、糖添加质量浓度(X2)、发酵时间(X3)、发酵温度(X4)为考察指标,利用Designexpert 8.0.6软件设计四因素三水平试验,其中Box-Behnken试验因素与水平见表1。
表 1 Box-Behnken试验因素与水平Table 1. Factors and levels of Box-Behnken test因素 水平 -1 0 1 X1接种量(%) 1 2 3 X2糖浓度(%) 1 2 3 X3发酵时间(h) 12 24 36 X4发酵温度(℃) 32 37 42 1.2.7 低聚半乳糖发酵乳的抑菌活性
参考前期研究方法[10],在含有1.0%低聚半乳糖的10%脱脂乳粉溶液中接种产肠毒素蜡样芽孢杆菌HN001,使其终浓度为103 CFU/mL,模拟较低浓度的污染,再接种植物乳杆菌ZDY2013至其终浓度为105 CFU/mL,静置培养。分别在0、24、36和48 h取发酵液1.0 mL,用1×PBS进行10倍梯度稀释,在MRS固体平板上进行涂布,计算活菌数。试验进行三次重复。
1.3 数据处理
上述实验均重复三次,结果用均数±标准差(Mean±SD)表示。采用GraphPad Prism 8.0软件对数据进行处理和统计分析,各组总体均数采用双因素方差分析(Two-way ANOVA)进行显著性比较,其中P<0.05,表示差异显著。
2. 结果与分析
2.1 低聚半乳糖对植物乳杆菌体外代谢的影响
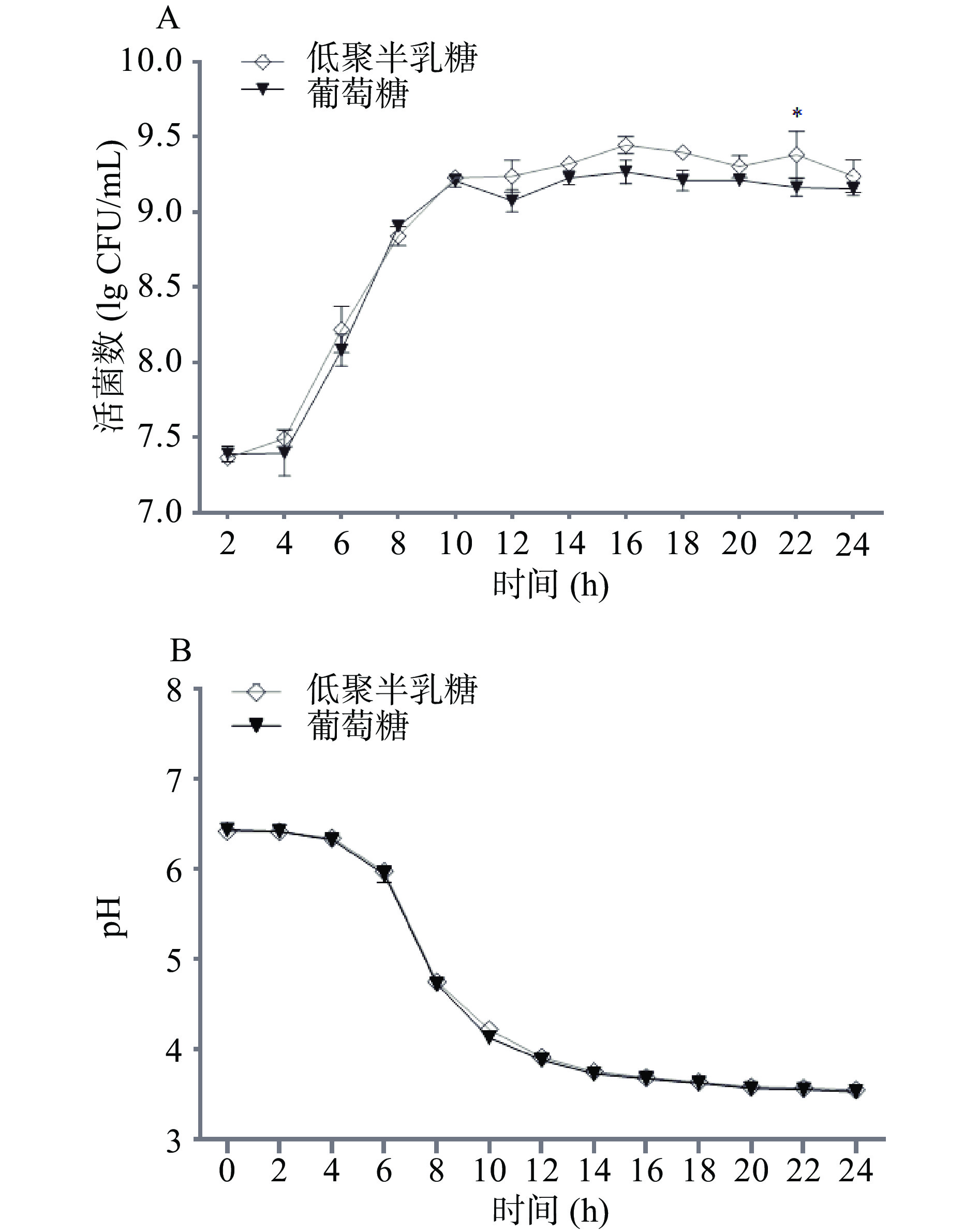
根据前期植物乳杆菌ZDY2013全基因组测序结果,可知其具有代谢多种碳水化合物的相关酶[25]。本研究采用低聚半乳糖制作改良MRS,评价植物乳杆菌ZDY2013体外发酵特点。结果发现,接种量为1.0%的植物乳杆菌能很好的利用低聚半乳糖进行代谢,生长能力类似碳源为葡萄糖的对照组(图1A)。其中,前4 h为代谢调整期,植物乳杆菌利用两种碳源代谢的浓度变化较少;在4~10 h间为指数生长期,细菌浓度能达到109 CFU/mL;在10 h之后为代谢稳定期,低聚半乳糖组的植物乳杆菌浓度要高于葡萄糖组,且在第22 h时有显著差异(P<0.05),说明低聚半乳糖在促进植物乳杆菌代谢方面要优于葡萄糖。另外,植物乳杆菌代谢两种不同碳水化合物后发酵液的pH变化趋势非常相似(图1B)。其中,前4 h的pH变化均不明显,4~12 h后pH急速下降,与菌株代谢的浓度结果基本一致,随后pH慢慢趋于稳定并维持在3.8左右,说明植物乳杆菌利用低聚半乳糖代谢能力较强,能降低发酵液pH,这和前期研究发现的植物乳杆菌ZDY2013利用商业化MRS代谢产酸降低pH结果一致[10]。综上所述,植物乳杆菌ZDY2013可以利用具有益生元特性的低聚半乳糖进行良好生长代谢。
2.2 低聚半乳糖对植物乳杆菌发酵上清液抑菌能力的影响
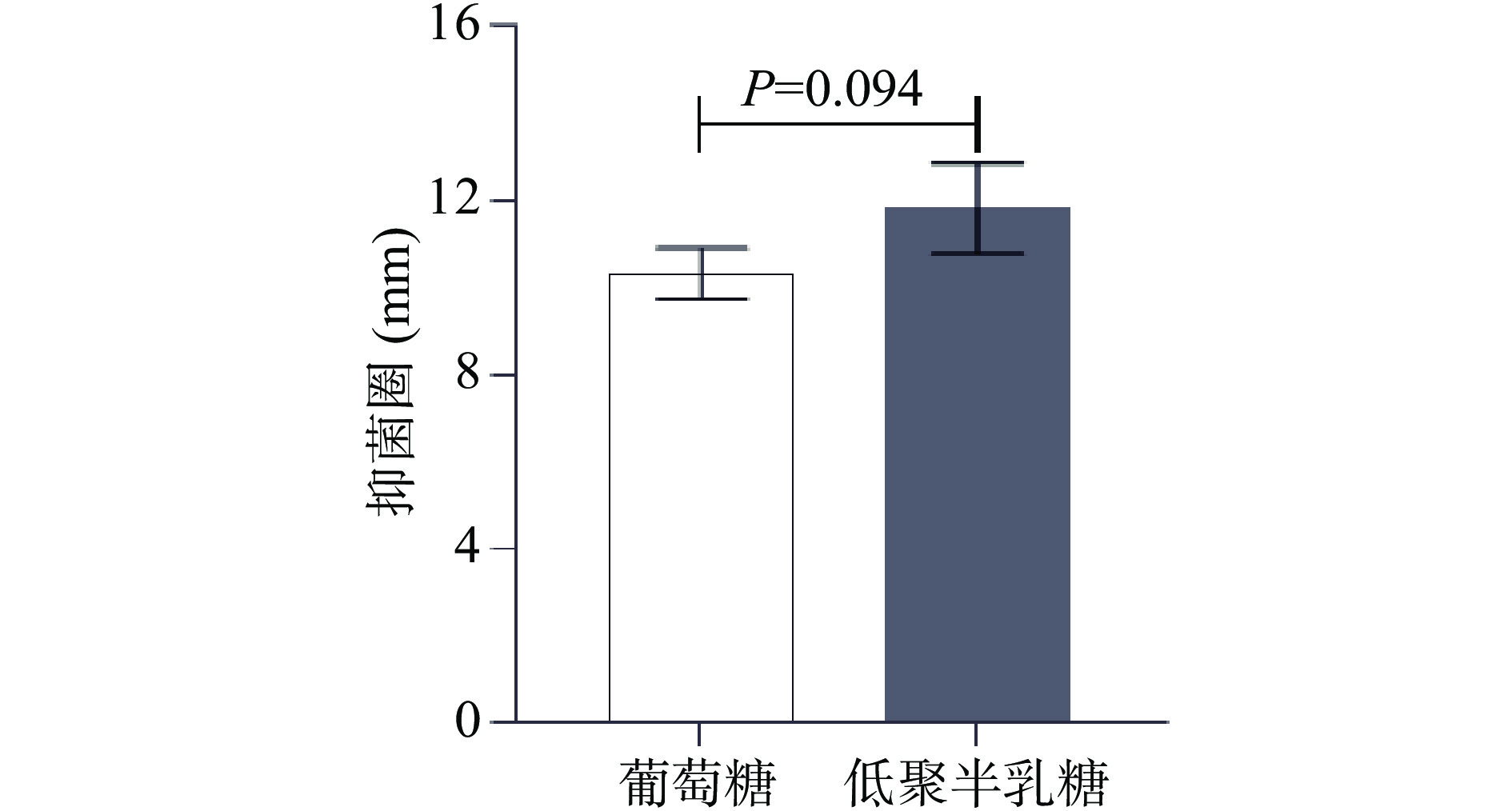
植物乳杆菌代谢碳水化合物发挥抗菌活性对其在食品中的开发应用具有重要意义。本研究采用食品中可引起呕吐和腹泻食源性疾病的蜡样芽孢杆菌作为指示菌[26],考察植物乳杆菌发酵低聚半乳糖后上清的抑菌能力。结果发现植物乳杆菌利用改良培养基发酵后的上清对产肠毒素蜡样芽孢杆菌HN001具有良好的抑制作用,抑菌圈均在10 mm以上,且低聚半乳糖组的抑菌效果优于对照的葡萄糖组(图2)。上述结果与前期植物乳杆菌利用MRS培养基发酵上清的抑菌效果相似,说明采用低聚半乳糖改良的培养基进行发酵也产生了能抑菌的有机酸[10]。
2.3 影响低聚半乳糖发酵乳特性的因素
2.3.1 不同菌液接种量对发酵乳特性的影响
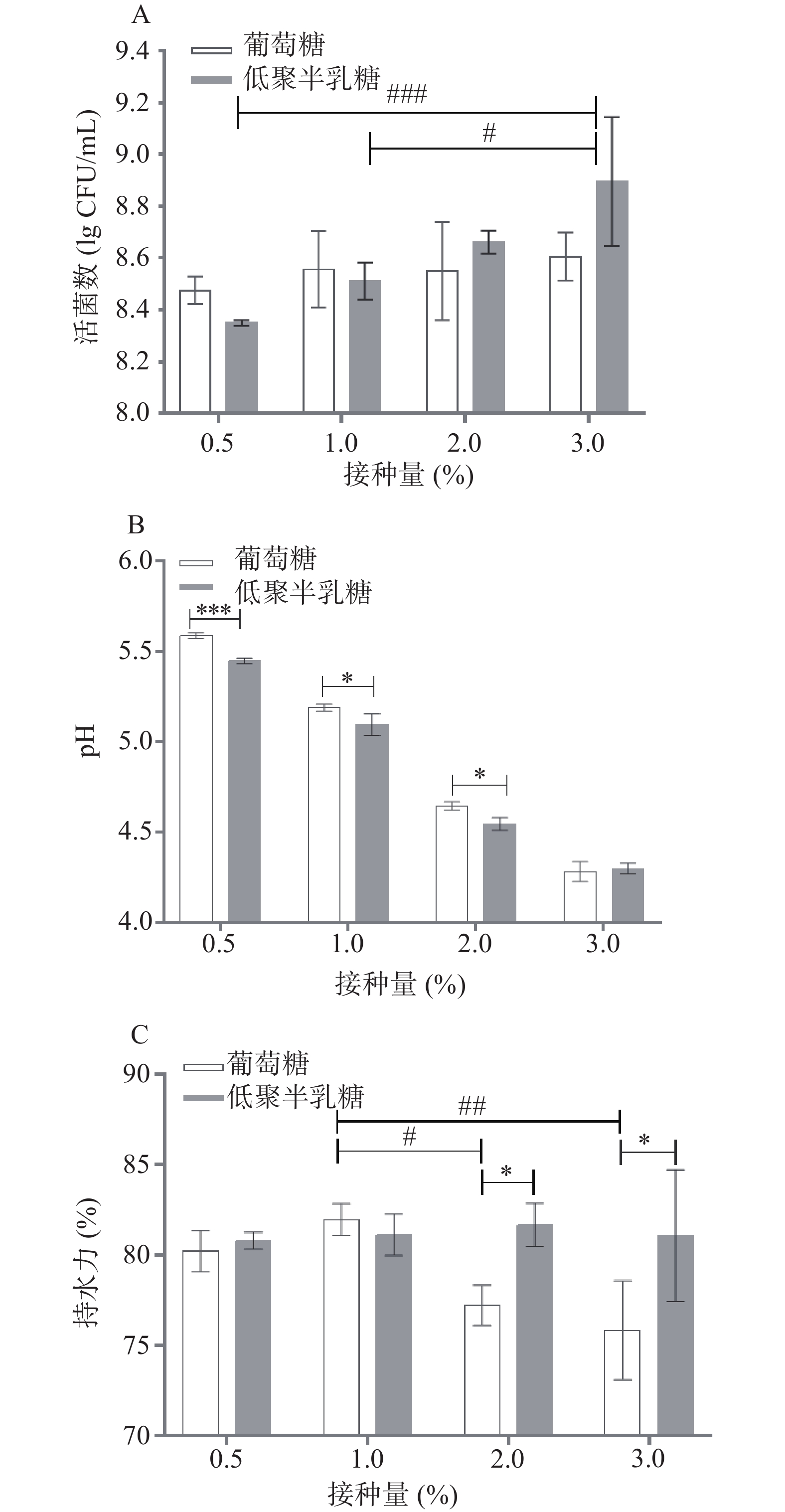
植物乳杆菌作为乳品发酵菌剂,对发酵乳的特性具有决定性的影响作用。在低聚半乳糖添加量一定的条件下,乳品中接种不同比例的植物乳杆菌菌液对发酵乳中活菌数有一定的影响,表现为随着接种量的升高(0.5%~3.0%),最终活菌数不断提高,且最高浓度达8.9 lg CFU/mL,与接种量为0.5%时,有高度显著差异(P<0.001;图3A);然而,葡萄糖添加量一定时,乳品中接种不同比例的植物乳杆菌菌液对发酵乳中活菌数没有特别的影响(均低于8.6 lg CFU/mL),这可能是因为1.0%(m/v)葡萄糖浓度较低,难以促使植物乳杆菌在发酵乳中高效生长,这也说明接种高浓度植物乳杆菌时,低聚半乳糖相比葡萄糖更有利于提高发酵乳中植物乳杆菌活菌数。与发酵乳中活菌数变化相对应的是,当乳品中添加一定量低聚半乳糖时,发酵乳pH随菌液接种量升高而降低(图3B),这主要是由于发酵液中高浓度活菌会产生更多的有机酸,从而导致发酵乳的pH高度显著下降(P<0.001)。类似地,葡萄糖对照组pH也不断下降,推测可能是由高含量接种量促使植物乳杆菌快速进入稳定期,并不断积累有机酸导致的。发酵乳的持水力体现了发酵乳体系对水的截留能力,与其微观结构有关[27],影响发酵乳的品质。本研究发现当接种较高浓度的植物乳杆菌时,葡萄糖组的发酵乳持水力比较差(75%),这可能与菌株在发酵乳中过早进入稳定期,并不断积累有机酸影响发酵乳的渗透压有关;而低聚半乳糖组未发生此类现象,接种量变化不会影响发酵乳较高的持水力(图3C),这可能是低聚糖更有利于发酵乳中酪蛋白生成,从而在酸性的环境下相互作用形成三维空间胶体结构,包容更多的水分子[24,28]。综上,说明添加了低聚半乳糖的发酵乳对菌液接种量变化的适应性更佳,且当菌液接种量为2%或3%时,更有利于改善发酵乳的特性。
2.3.2 不同低聚半乳糖浓度对发酵乳特性的影响
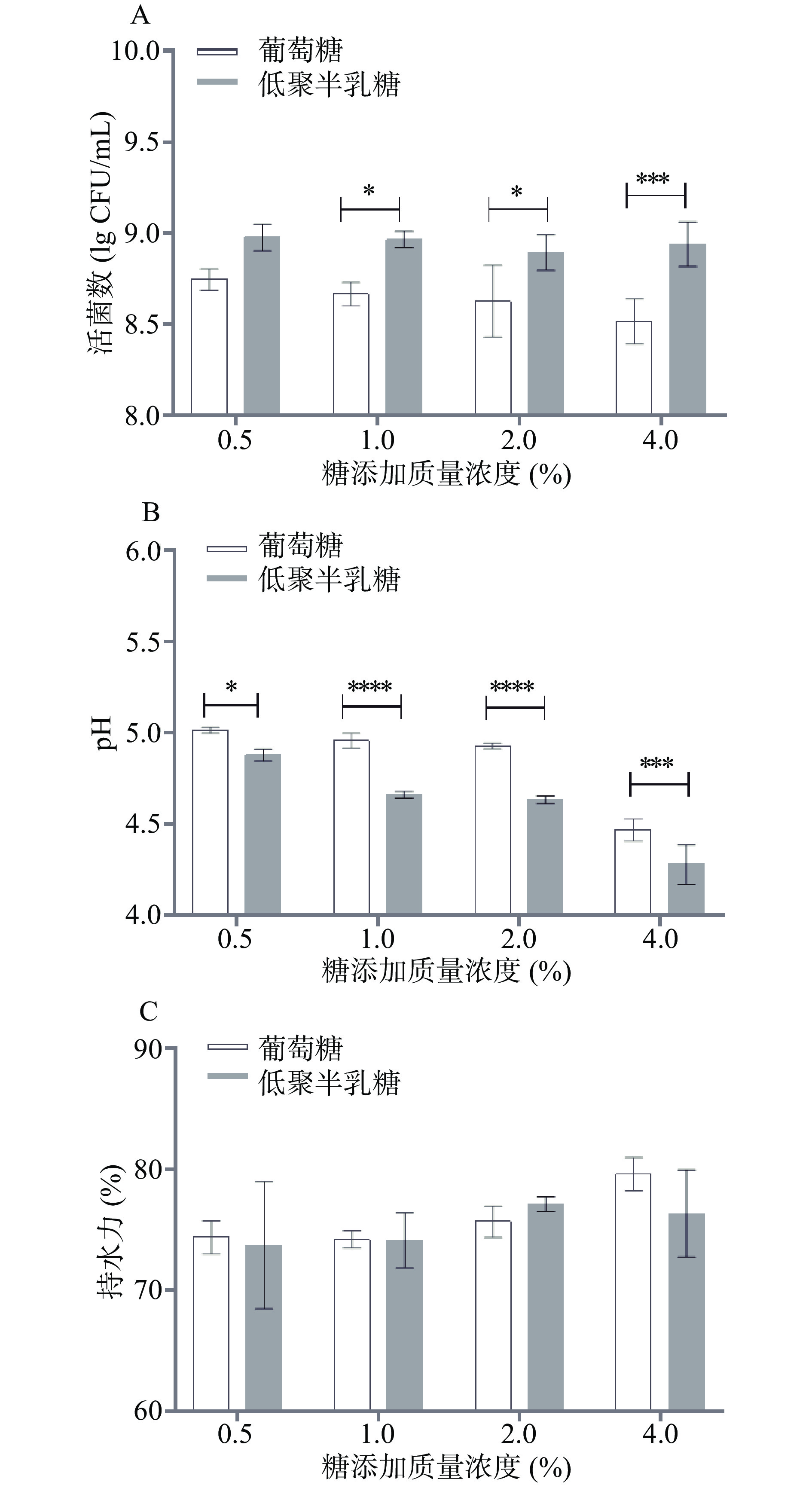
低聚半乳糖是一种具有优良益生元特性的功能低聚糖,其能被肠道内乳酸菌所利用,开发含有益生元的发酵乳制品具有重要意义。由前面结果已知,低聚半乳糖能促进植物乳杆菌在发酵乳中的代谢,为此进一步探究不同浓度的低聚半乳糖添加量对发酵乳特性的影响。从图4A结果可知,发酵乳中糖添加浓度的变化对植物乳杆菌活菌数无明显影响,但低聚糖组的活菌数均高于葡萄糖组,其中添加浓度为1.0%~4.0%时,有显著差异(P<0.05),这主要是因为低聚半乳糖在发酵乳中更有利于促进植物乳杆菌生长,从而提高了其在稳定期的浓度;由图4B可知,随着糖浓度的增加,pH有下降趋势,且低聚半乳糖组的pH均低于葡萄糖组,在糖浓度为1.0%~4.0%时有高度显著差异(P<0.001),结合图4A,说明随着糖浓度的升高,植物乳杆菌在发酵乳中产有机酸的能力变强。另外,当低聚半乳糖浓度为4.0%时,pH低于4.5,将有利于抑制发酵食品中病原微生物的繁殖。由图4C可知,随着糖浓度的增加,发酵乳的持水力有上升的趋势,但是低聚半乳糖组与葡萄糖对照组均无显著差异(P>0.05),说明糖浓度不是发酵乳持水力变化的决定因素。综上所述,不同浓度的糖对发酵乳特性有一定的影响,且糖质量浓度超过1.0%时优于葡萄糖。
2.3.3 发酵时间对发酵乳特性的影响
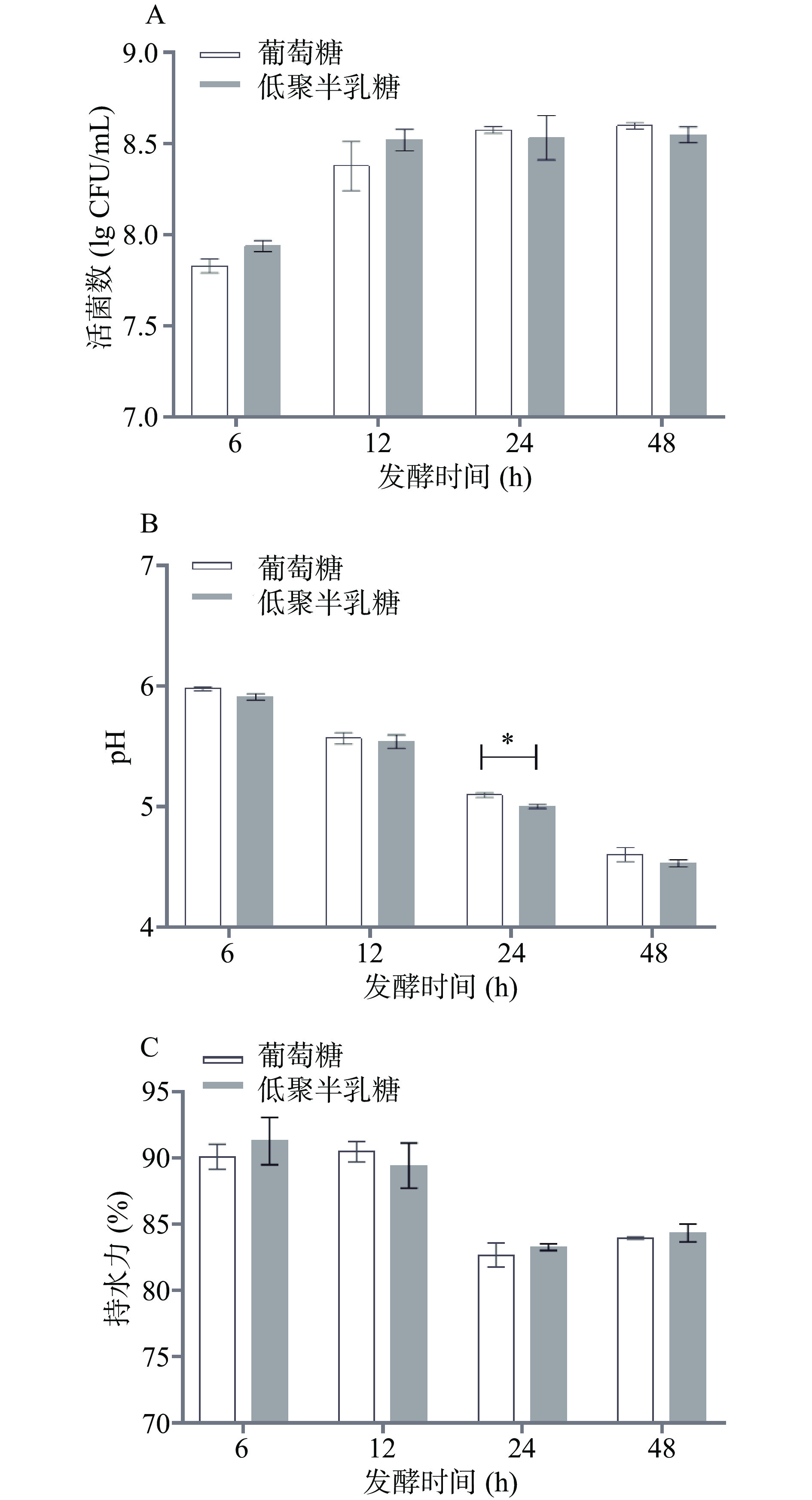
乳酸菌发酵时间长短的选择对发酵食品质量控制至关重要。如图5A所示,发酵结束时间的不同,发酵乳中的植物乳杆菌活菌数是有差异的,尤其是发酵6 h结束时,活菌浓度均不及108 CFU/mL,只有发酵12 h后,低聚半乳糖组的菌株开始进入生长稳定状态,且低聚半乳糖和葡萄糖组之间没有显著差异(P>0.05)。然而,低聚半乳糖和葡萄糖组在发酵24 h时,pH有显著差异(P<0.05),整体上发酵乳pH随发酵时间的延长而不断下降,这主要是活菌在发酵乳中快速代谢,积累有机酸导致的,且在24 h后pH降到5.0以下,能有效预防病原微生物污染。另外,发酵乳持水力在发酵前12 h很强,无论低聚半乳糖组还是葡萄糖组均超过85%,而发酵24 h之后会降低并趋于平稳(图5C)。综上,说明发酵24 h为发酵乳综合特性最适时间。
2.3.4 发酵温度对发酵乳特性的影响
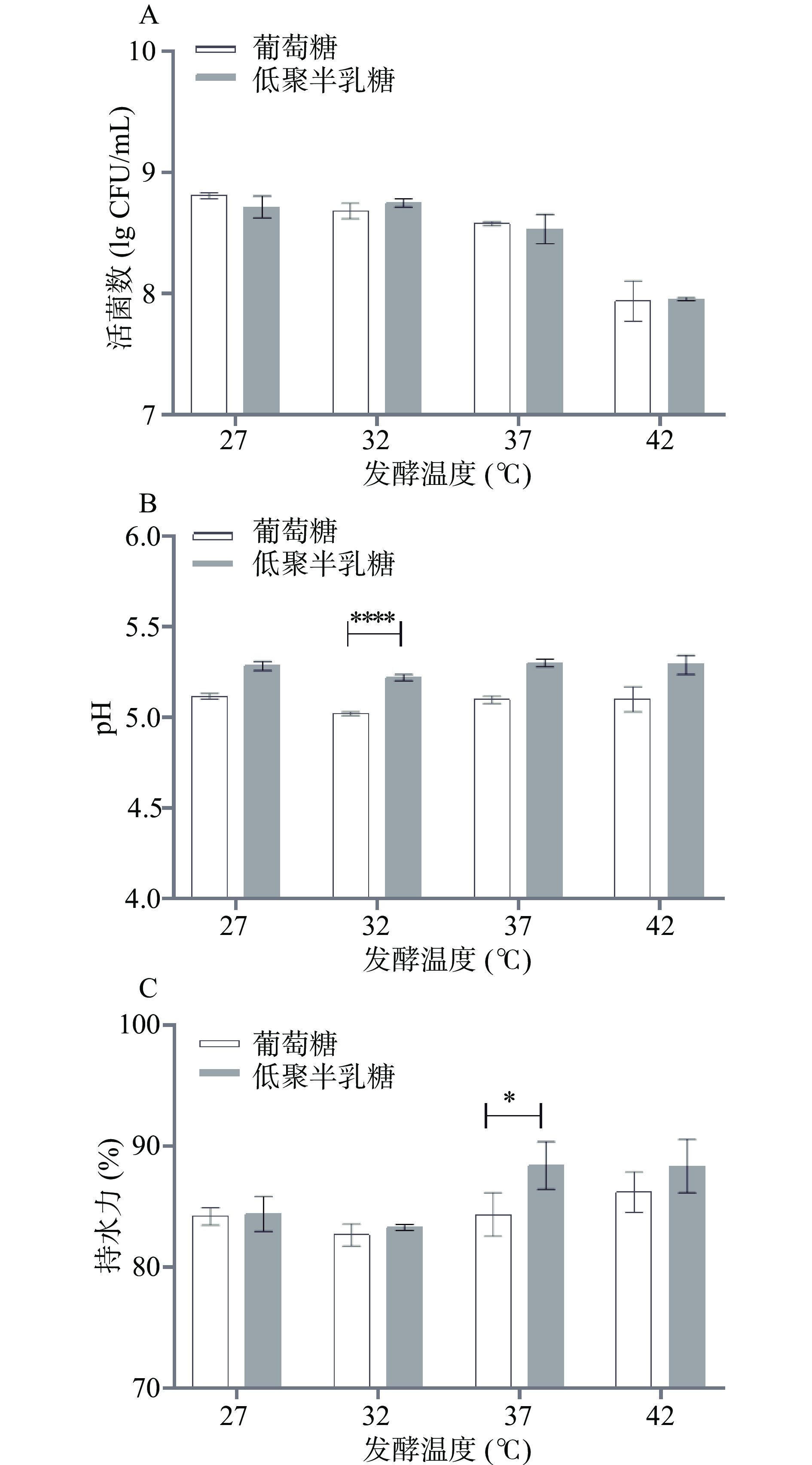
发酵温度是影响乳酸菌发酵乳品质的另一个因素,因此评估植物乳杆菌发酵的最适温度有重要意义。根据植物乳杆菌的最适生长温度为37 ℃的特点,本研究选择27、32、37和42 ℃温度指标来探究发酵温度对发酵乳特性的影响。由图6A可知,发酵温度为27~37 ℃时,发酵乳最终活菌浓度较高,接近109 CFU/mL;而温度为42 ℃时,对发酵乳最终活菌数有一定影响,但浓度也高于108 CFU/mL。另外,由图6B可知,不同发酵温度对发酵乳pH影响不大,这主要取决于发酵乳中活菌数和发酵时间的影响,和图6A结果相似。此外,从图6C可知,发酵温度变化对发酵乳的持水力影响也不明显,且只有当发酵温度在37 ℃时,低聚半乳糖组的持水力显著高于葡萄糖组(P<0.05)。综上,发酵温度在一定范围内变化对发酵乳特性影响不大,说明该发酵乳的制备对温度要求不太苛刻。
2.4 植物乳杆菌与低聚半乳糖在牛奶中发酵的条件优化
2.4.1 Box-Behnken试验结果与分析
发酵乳中活菌数为影响发酵乳特性的最主要因素,其可以影响发酵乳的pH和持水性。因此,在单因素实验的基础上,以发酵乳活菌数为响应值,以影响发酵乳特性的接种量(X1)、低聚半乳糖浓度(X2)、发酵时间(X3)和发酵温度(X4)为考量因素,获得Box-Behnken试验结果与分析(表2),再运用Design Expert V8.0.6对表2中的数据进行二次多元线性回归拟合,得到活菌数Y=8.74+0.057X1+0.062X2+0.14X3−0.27X4−0.063X1X2−0.040X1X3−0.0025X1X4−0.045X2X3−0.0075X2X4−0.005X3X4+0.010X12+0.015X22−0.22X32−0.28X42的回归方程,接着对回归方程进行方差分析,结果见表3。
表 2 Box-Behnken试验设计与结果Table 2. Design and results of Box-Behnken test实验号 X1 X2 X3 X4 活菌数(lg CFU/mL) 1 1 1 24 37 8.65 2 3 1 24 37 8.79 3 1 3 24 37 8.93 4 3 3 24 37 8.82 5 2 2 12 32 8.51 6 2 2 36 32 8.58 7 2 2 12 42 7.95 8 2 2 36 42 8.04 9 1 2 24 32 8.70 10 3 2 24 32 8.74 11 1 2 24 42 8.18 12 3 2 24 42 8.21 13 2 1 12 37 8.39 14 2 3 12 37 8.63 15 2 1 36 37 8.51 16 2 3 36 37 8.57 17 1 2 12 37 7.97 18 3 2 12 37 8.34 19 1 2 36 37 8.78 20 3 2 36 37 8.99 21 2 1 24 32 8.69 22 2 3 24 32 8.77 23 2 1 24 42 8.17 24 2 3 24 42 8.22 25 2 2 24 37 8.67 26 2 2 24 37 8.78 27 2 2 24 37 8.97 28 2 2 24 37 8.67 29 2 2 24 37 8.63 表 3 回归方程的方差分析Table 3. Variance analysis of regression equation方差来源 偏差平方和 自由度 均方 F值 P值 显著性 模型 2.02 14 0.14 4.56 0.0038 ** X1 0.039 1 0.039 1.22 0.2886 X2 0.046 1 0.046 1.44 0.2499 X3 0.24 1 0.24 7.43 0.0164 * X4 0.86 1 0.86 27.28 0.0001 *** X1X2 0.016 1 0.016 0.49 0.4940 X1X3 0.0064 1 0.0064 0.20 0.6599 X1X4 0.000025 1 0.000025 0.0007893 0.9780 X2X3 0.0081 1 0.0081 0.26 0.6209 X2X4 0.000225 1 0.000225 0.007104 0.9340 X3X4 0.0001 1 0.0001 0.003157 0.9560 X12 0.0006595 1 0.0006595 0.021 0.8873 X22 0.001476 1 0.001476 0.047 0.8322 X32 0.31 1 0.31 9.91 0.0071 ** X42 0.52 1 0.52 16.34 0.0012 ** 残差 0.44 14 0.032 0.0080 失拟项 0.37 10 0.37 1.92 0.2764 纯误差 0.076 4 0.019 总和 2.47 28 注:*表示P<0.05;**表示P<0.01;***表示P<0.001。 结果显示,模型组P值小于0.01(P=0.0038),说明试验回归方程模型显著。失拟项P值为0.2764,不显著,证明模型选择正确;决定系数R2=0.8201,校正决定系数R2Adj=0.6402,证明该预测模型结果与实验结果的拟合性较好。综上,说明此模型可预测最佳发酵条件。
2.4.2 响应面分析
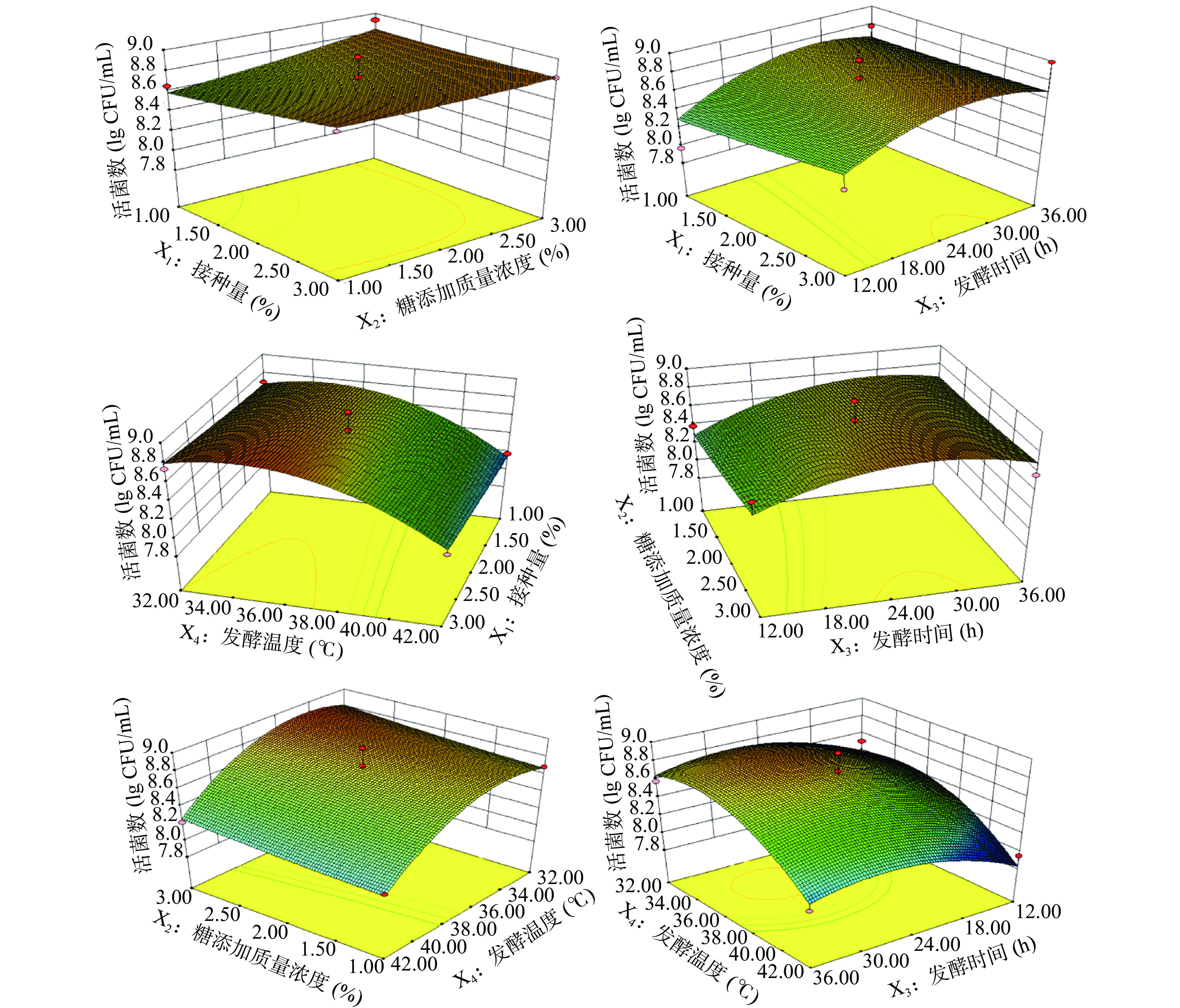
响应面中图形的陡峭程度反映了两两因素之间交互作用对响应值变化情况的影响。当响应曲面越陡峭,说明交互作用越明显;当等高线越趋于椭圆,表明因素之间的交互作用越是显著,呈圆形则说明交互作用不显著。由图7可知,除了接种量和糖添加质量浓度这两因素之间的交互作用外,其余各图都呈现凸形曲面,即X1(接种量)和X3(发酵时间)、X1(接种量)和X4(发酵温度)、X2(糖添加质量浓度)和X3(发酵时间)、X2(糖添加质量浓度)和X4(发酵温度)、X3(发酵时间)和X4(发酵温度)之间有一定的相互作用。此外,可以从图中看出,各因素对活菌数的影响依次为X4>X3>X2>X1。
根据软件Design Expert V8.0.6预测以菌液接种量为2.0%、糖添加质量浓度为1.0%、发酵时间为24 h、发酵温度为42 ℃是最佳发酵条件,对应理论活菌数最大值为1.42×108 CFU/mL。进一步对最优条件进行试验验证,三次重复的活菌数分别为1.24×108、1.06×108 和1.04×108 CFU/mL,与通过响应面试验预测的理论值很接近,说明本模型在模拟发酵条件上具有可靠性。该发酵条件是否同样有利于改善乳品口感、风味、营养价值及肠道健康有待进一步探究。
2.5 低聚半乳糖发酵乳对蜡样芽孢杆菌的抑制作用
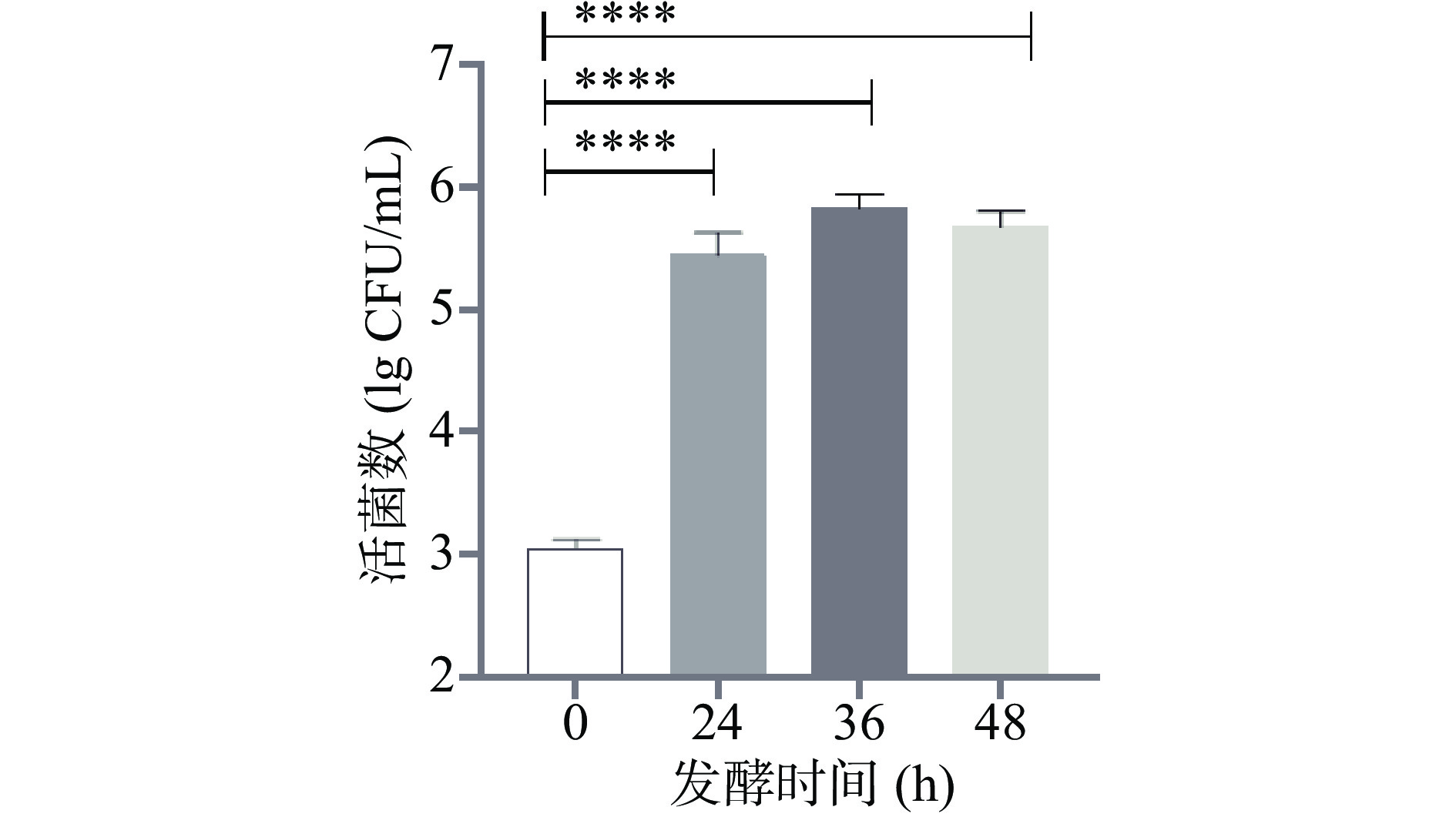
前面研究结果表明低聚半乳糖改良的培养基能改善植物乳杆菌ZDY2013发酵上清抑制蜡样芽孢杆菌的能力,且前期研究发现该菌在牛奶发酵过程中可有效抑制蜡样芽孢杆菌的繁殖[10]。本研究进一步以乳品中常见污染微生物蜡样芽孢杆菌作为指示菌,考察乳品中添加低聚半乳糖后进行植物乳杆菌发酵是否能有效抑制较低浓度蜡样芽孢杆菌的生长。结果如图8所示,蜡样芽孢杆菌的总活菌数在牛奶发酵24 h后达到5×105 CFU/mL,并在随后的发酵过程中维持该数量级,而该数量级的蜡样芽孢杆菌被认为是不会引起食源性疾病的[29]。另外,105 CFU/mL低于前期研究发酵乳中无添加低聚半乳糖时蜡样芽孢杆菌的最高浓度(1.8×106 CFU/mL)[10],说明添加低聚半乳糖有利于提高植物乳杆菌发酵乳拮抗蜡样芽孢杆菌的活性。综上所述,低聚半乳糖的添加提高了植物乳杆菌发酵乳预防蜡样芽孢杆菌污染的潜力,摄入该发酵乳可能对肠道健康具有一定的促进作用。
3. 结论
植物乳杆菌ZDY2013能抑制病原微生物并维护宿主肠道菌群的稳态,同时具有代谢多种碳水化合物并应用于发酵乳的良好潜力。本研究选取具有益生元特性的低聚半乳糖作为植物乳杆菌发酵乳添加成分,经体外代谢评价和单因素实验确定了植物乳杆菌的接种量、碳源的添加量、发酵时间和发酵温度对发酵乳的活菌数、pH和持水力有一定影响;综合各因素的交互作用,获得发酵乳制备的最佳条件:菌液接种量为2%、糖添加质量浓度为1.0%、发酵时间为24 h、发酵温度为42 ℃,并经实验得到验证。另外,添加了低聚半乳糖的发酵乳对产肠毒素蜡样芽孢杆菌的抑制能力较强。本研究将为开发一种具有益生菌、益生元特性,并抑制病原微生物的功能发酵乳奠定基础。
-
表 1 Box-Behnken试验因素与水平
Table 1 Factors and levels of Box-Behnken test
因素 水平 -1 0 1 X1接种量(%) 1 2 3 X2糖浓度(%) 1 2 3 X3发酵时间(h) 12 24 36 X4发酵温度(℃) 32 37 42 表 2 Box-Behnken试验设计与结果
Table 2 Design and results of Box-Behnken test
实验号 X1 X2 X3 X4 活菌数(lg CFU/mL) 1 1 1 24 37 8.65 2 3 1 24 37 8.79 3 1 3 24 37 8.93 4 3 3 24 37 8.82 5 2 2 12 32 8.51 6 2 2 36 32 8.58 7 2 2 12 42 7.95 8 2 2 36 42 8.04 9 1 2 24 32 8.70 10 3 2 24 32 8.74 11 1 2 24 42 8.18 12 3 2 24 42 8.21 13 2 1 12 37 8.39 14 2 3 12 37 8.63 15 2 1 36 37 8.51 16 2 3 36 37 8.57 17 1 2 12 37 7.97 18 3 2 12 37 8.34 19 1 2 36 37 8.78 20 3 2 36 37 8.99 21 2 1 24 32 8.69 22 2 3 24 32 8.77 23 2 1 24 42 8.17 24 2 3 24 42 8.22 25 2 2 24 37 8.67 26 2 2 24 37 8.78 27 2 2 24 37 8.97 28 2 2 24 37 8.67 29 2 2 24 37 8.63 表 3 回归方程的方差分析
Table 3 Variance analysis of regression equation
方差来源 偏差平方和 自由度 均方 F值 P值 显著性 模型 2.02 14 0.14 4.56 0.0038 ** X1 0.039 1 0.039 1.22 0.2886 X2 0.046 1 0.046 1.44 0.2499 X3 0.24 1 0.24 7.43 0.0164 * X4 0.86 1 0.86 27.28 0.0001 *** X1X2 0.016 1 0.016 0.49 0.4940 X1X3 0.0064 1 0.0064 0.20 0.6599 X1X4 0.000025 1 0.000025 0.0007893 0.9780 X2X3 0.0081 1 0.0081 0.26 0.6209 X2X4 0.000225 1 0.000225 0.007104 0.9340 X3X4 0.0001 1 0.0001 0.003157 0.9560 X12 0.0006595 1 0.0006595 0.021 0.8873 X22 0.001476 1 0.001476 0.047 0.8322 X32 0.31 1 0.31 9.91 0.0071 ** X42 0.52 1 0.52 16.34 0.0012 ** 残差 0.44 14 0.032 0.0080 失拟项 0.37 10 0.37 1.92 0.2764 纯误差 0.076 4 0.019 总和 2.47 28 注:*表示P<0.05;**表示P<0.01;***表示P<0.001。 -
[1] MARKOWIAK P, SLIZEWSKA K. Effects of probiotics, prebiotics, and synbiotics on human health[J]. Nutrients,2017,9(9):1−30.
[2] 曹振辉, 刘永仕, 潘洪彬, 等. 乳酸菌的益生功能及作用机制研究进展[J]. 食品工业科技,2015,36(24):366−377. [CAO Z H, LIU Y S, PAN H B, et al. Research progress on probiotic function and mechanism of lactic acid bacteria[J]. Science and Technology of Food Industry,2015,36(24):366−377. CAO Z H, LIU Y S, PAN H B, et al. Research progress on probiotic function and mechanism of lactic acid bacteria[J]. Science and Technology of Food Industry, 2015, 36(24): 366-377.
[3] OH N S, JOUNG J Y, LEE J Y, et al. A synbiotic combination of Lactobacillus gasseri 505 and Cudrania tricuspidata leaf extract prevents hepatic toxicity induced by colorectal cancer in mice[J]. Journal of Dairy Science,2020,103(4):2947−2955. doi: 10.3168/jds.2019-17411
[4] SAVAIANO D A, HUTKINS R W. Yogurt, cultured fermented milk, and health: A systematic review[J]. Nutrition Reviews,2021,79(5):599−614. doi: 10.1093/nutrit/nuaa013
[5] OAK S J, JHA R. The effects of probiotics in lactose intolerance: A systematic review[J]. Critical Reviews in Food Science Nutrition,2019,59(11):1675−1683. doi: 10.1080/10408398.2018.1425977
[6] ZHONG Z, HU R, ZHAO J, et al. Acetate kinase and peptidases are associated with the proteolytic activity of Lactobacillus helveticus isolated from fermented food[J]. Food Microbiology,2021,94:103651.
[7] 张彦位, 路江浩, 鄢梦洁, 等. 益生菌对微生态系统的改善作用及其应用研究进展[J]. 食品工业科技,2021,42(4):369−379. [ZHANG Y W, LU J H, YAN M J, et al. Research progress of probiotics on improving microecosystem and its application[J]. Science and Technology of Food Industry,2021,42(4):369−379. ZHANG Y W, LU J H, YAN M J, et al. Research progress of probiotics on improving microecosystem and its application[J]. Science and Technology of Food Industry, 2021, 42(4): 369-379.
[8] HUANG H R, TAO X, WAN C X, et al. In vitro probiotic characteristics of Lactobacillus plantarum ZDY 2013 and its modulatory effect on gut microbiota of mice[J]. Journal of Dairy Science,2015,98(9):5850−5861. doi: 10.3168/jds.2014-9153
[9] WANG Y Y, GUO Y L, CHEN H, et al. Potential of Lactobacillus plantarum ZDY2013 and Bifidobacterium bifidum WBIN03 in relieving colitis by gut microbiota, immune, and anti-oxidative stress[J]. Canadian Journal of Microbiology,2018,64(5):327−337. doi: 10.1139/cjm-2017-0716
[10] ZHANG Z H, TAO X, SHAH N P, et al. Antagonistics against pathogenic Bacillus cereus in milk fermentation by Lactobacillus plantarum ZDY2013 and its anti-adhesion effect on Caco-2 cells against pathogens[J]. Journal Dairy of Science,2016,99(4):2666−2674. doi: 10.3168/jds.2015-10587
[11] ZHANG Z H, JIN M L, WANG K M, et al. Short-term intake of Lactiplantibacillus plantarum ZDY2013 fermented milk promotes homoeostasis of gut microbiota under enterotoxigenic Bacillus cereus challenge[J]. Food & Function,2021,12(11):5118−5129.
[12] SONNENBURG E D, SONNENBURG J L. Starving our microbial self: The deleterious consequences of a diet deficient in microbiota-accessible carbohydrates[J]. Cell Metabolism,2014,20(5):779−786. doi: 10.1016/j.cmet.2014.07.003
[13] GOPAL P K, SULLIVAN P A, SMART J B. Utilisation of galacto-oligosaccharides as selective substrates for growth by lactic acid bacteria including Bifidobacterium lactis DR10 and Lactobacillus rhamnosus DR20[J]. International Dairy Journal,2001,11(1):19−25.
[14] 薛雅莺, 袁卫涛, 杨海军. 低聚半乳糖的特性及应用前景[J]. 发酵科技通讯,2011,40(3):50−52. [XUE Y Y, YUAN W T, YANG H J. Characteristics and application prospect of galactose oligomeric[J]. Bulletin of Fermentation Science and Technology,2011,40(3):50−52. doi: 10.3969/j.issn.1674-2214.2011.03.020 XUE Y Y, YUAN W T, YANG H J. Characteristics and application prospect of galactose oligomeric[J]. Bulletin of Fermentation Science and Technology, 2011, 40(3): 50-52. doi: 10.3969/j.issn.1674-2214.2011.03.020
[15] MA C C, WASTI S, HUANG S, et al. The gut microbiome stability is altered by probiotic ingestion and improved by the continuous supplementation of galactooligosaccharide[J]. Gut Microbes,2020,12(1):1785252. doi: 10.1080/19490976.2020.1785252
[16] 孙思睿, 张晟, 孟祥晨. 低聚半乳糖对植物乳杆菌生长及部分代谢的影响[J]. 食品工业科技,2017,38(17):95−98. [SUN S R, ZHANG C, MENG X C. Effects of galactose oligomeric on growth and partial metabolism of Lactobacillus plantarum[J]. Science and Technology of Food Industry,2017,38(17):95−98. SUN S R, ZHANG C, MENG X C. Effects of galactose oligomeric on growth and partial metabolism of Lactobacillus plantarum[J]. Science and Technology of Food Industry, 2017, 38(17): 95-98.
[17] AZAGRA B I, MASSOT C M, KNIPPING K, et al. Supplementation with 2'-FL and scGOS/lcFOS ameliorates rotavirus-induced diarrhea in suckling rats[J]. Front Cell Infect Microbiol,2018,8:372. doi: 10.3389/fcimb.2018.00372
[18] SUN J W, LIANG W X, YANG X F, et al. Cytoprotective effects of galacto-oligosaccharides on colon epithelial cells via up-regulating miR-19b[J]. Life Sciences,2019,231:116589.
[19] HASLE G, RAASTAD R, BJUNE G, et al. Can a galacto-oligosaccharide reduce the risk of traveller's diarrhoea? A placebo-controlled, randomized, double-blind study[J]. Journal of Travel Medicine,2017,24(5):1−9.
[20] KWON J I, PARK Y, NOH D O, et al. Complex-oligosaccharide composed of galacto-oligosaccharide and lactulose ameliorates loperamide-induced constipation in rats[J]. Food Science and Biotechnology,2018,27(3):781−788. doi: 10.1007/s10068-017-0300-2
[21] KIM M G, JO K Y, CHANG Y B, et al. Changes in the gut microbiome after galacto-oligosaccharide administration in loperamide-induced constipation[J]. Journal of Personalized Medicine,2020,10(4):1−15.
[22] CHU H Q, TAO X, SUN Z G, et al. Galactooligosaccharides protects against DSS-induced murine colitis through regulating intestinal flora and inhibiting NF-κB pathway[J]. Life Sciences,2020,242:117220.
[23] SEIJO M, BONANNO M S, VENICA C I, et al. A yoghurt containing galactooligosaccharides and having low-lactose level improves calcium absorption and retention during growth: Experimental study[J]. International Journal of Food Science & Technology,2021,57(1):48−56.
[24] 张娜, 占英, 孟迎平, 等. 功能低聚糖对植物乳杆菌ZDY2013发酵乳发酵特性及冷藏效果的影响[J]. 现代食品科技,2021,37(11):34−42. [ZHANG N, ZHAN Y, MENG Y P, et al. Effects of functional oligosaccharides on fermentation characteristics and refrigeration effect of Lactobacillus plantarum ZDY2013 fermented milk[J]. Modern Food Science and Technology,2021,37(11):34−42. ZHANG N, ZHAN Y, MENG Y P, et al. Effects of functional oligosaccharides on fermentation characteristics and refrigeration effect of Lactobacillus plantarum ZDY2013 Fermented milk[J]. Modern Food Science and Technology, 2021, 37(11): 34-42.
[25] PENG L, ZHAO K, CHEN S, et al. Whole genome and acid stress comparative transcriptome analysis of Lactiplantibacillus plantarum ZDY2013[J]. Archives of Microbiology,2021,203:2795−2807. doi: 10.1007/s00203-021-02240-7
[26] 张志鸿, 许恒毅, 魏华. 基于PCR方法检测蜡样芽孢杆菌的研究进展[J]. 食品工业科技,2013,34(22):335−342. [ZHANG Z H, XU H Y, WEI H. Progress in the detection of Bacillus cereus based on PCR[J]. Science and Technology of Food Industry,2013,34(22):335−342. ZHANG Z H, XU H Y, WEI H. Progress in the detection of Bacillus cereus based on PCR[J]. Science and Technology of Food Industry, 2013, 34(22): 335-342.
[27] 蔡淼, 郝晓娜, 罗天淇, 等. 植物乳杆菌YW11胞外多糖对酸乳加工特性的影响[J]. 食品科学,2021,42(14):39−45. [CAO M, HAO X N, LUO T Q, et al. Effects of extracellular polysaccharide of Lactobacillus plantarum YW11 on processing characteristics of yoghurt[J]. Food Science,2021,42(14):39−45. doi: 10.7506/spkx1002-6630-20200511-115 CAO M, HAO X N, LUO T Q, et al. Effects of extracellular polysaccharide of Lactobacillus plantarum YW11 on processing characteristics of yoghurt[J]. Food Science, 2021, 42(14): 39-45. doi: 10.7506/spkx1002-6630-20200511-115
[28] WANG H, WANG C, WANG M, et al. Chemical, physiochemical, and microstructural properties, and probiotic survivability of fermented goat milk using polymerized whey protein and starter culture kefir mild 01[J]. Journal of Food Science,2017,82(11):2650−2658. doi: 10.1111/1750-3841.13935
[29] ARNESEN L P, FAGERLUND A, GRANUM P E. From soil to gut: Bacillus cereus and its food poisoning toxins[J]. FEMS Microbiology Reviews,2008,32(4):579−606. doi: 10.1111/j.1574-6976.2008.00112.x





 下载:
下载:
 下载:
下载:
