Isolation and Identification of Antibacterial Lpopeptides from Bacillus subtilis KC-WQ Fermentation Broth and Optimization of Fermentation Conditions
-
摘要: 本文研究了一株枯草芽孢杆菌KC-WQ的胞外分泌物的抑菌效果及功效成分。实验发现枯草芽孢杆菌KC-WQ对大肠杆菌(Escherichia coli)、沙门氏菌(Salmonella enterica subsp. enterica)和嗜水气单胞菌(Aeromonas hydrophila)均有明显的抑菌效果,其中对沙门氏菌的抑制效果最为显著。在此基础上,采用酸沉淀法分离抗菌成分,通过薄层色谱法(TLC)、高效液相色谱法(HPLC)、基质辅助激光解吸电离飞行时间质谱(MALDI-TOF-MS)分析结构发现,该菌株分泌抗菌物质为脂肽类,分子量分布在1030.5~1491.4 Da之间,主要由伊枯草菌素(Iturin)、表面活性素(Surfactin)和芬荠素(Fengycin)组成,最小抑菌浓度为0.8 mg/mL。该脂肽成分经热处理(105 ℃,20 min)后,仍保持良好的抗菌效果。采用响应面法对KC-WQ的发酵条件进行优化,得到最佳发酵条件为:初始pH为6.0,发酵温度为36 ℃,摇床转速为208 r/min,预测粗产物产量为1.311 g/L,后经实验验证,实际产量可达1.236 g/L。上述结果表明,枯草芽孢杆菌KC-WQ具有良好的抗菌性能和加工性能,可作为抑菌成分,在食品保藏和抗菌包装材料开发中具有应用前景。Abstract: This paper studied the antibacterial effect and functional components of the extracellular secretions of a strain of Bacillus subtilis KC-WQ. The experiment found that KC-WQ had obvious antibacterial effect on Escherichia coli, Salmonella enterica subsp. enterica and Aeromonas hydrophila, among which it had the most significant antibacterial effect on Salmonella. On this basis, the acid precipitation method was used to separate the antibacterial components, and the structure was found through thin layer chromatography (TLC), high performance liquid chromatography (HPLC) and matrix-assisted laser desorption ionization time-of-flight mass spectrometry (MALDI-TOF-MS). The antibacterial substances secreted by this strain were lipopeptides with a molecular weight distribution between 1030.5 and 1491.4 Da, mainly composed of Iturin, Surfactin and Fengycin, and the minimum inhibitory concentration was 0.8 mg/mL. The lipopeptide component still maintained a good antibacterial effect after heat treatment (105 ℃, 20 min). The response surface method was used to optimize the culture conditions of KC-WQ, and the best fermentation conditions were obtained: The initial pH was 6.0, the fermentation temperature was 36 ℃, the shaker speed was 208 r/min, and the predicted crude product yield was 1.311 g/L. Later verified by experiments, the actual yield was 1.236 g/L. The above results indicated that Bacillus subtilis KC-WQ had good antibacterial and processing properties, could be used as a good antibacterial ingredient, and had a good application prospect in the development of antibacterial and preservation materials in food industry.
-
沙门氏菌、大肠杆菌以及金黄色葡萄球菌作为常见的食源性致病菌,危害着公共食品安全[1],寻找安全有效的抗菌物质刻不容缓。脂肽作为一种来源于微生物的表面活性剂,具有抗菌、抗病毒等多种功效[2]。与传统抗生素不同,抗菌脂肽具有易降解、热稳定性高、不易形成耐药性、绿色安全等优势[3]。高晓平等[4]研究表明,表面活性素具有抑制乳中大肠埃希菌O157的功效,延长乳的保质期。具有环状结构的抗菌脂肽防腐剂可以抑制其本身对蛋白酶的敏感性,同时抑制病原菌如黄曲霉等生长繁殖[5],有效控制食品中有害微生物的滋生,具有一定食品防腐保鲜功能[6]。
自然界中酵母菌、真菌、细菌等多种微生物都可以产生脂肽,目前已发现的主要有隐杆菌属、类芽孢杆菌属、梭菌属、游动放线菌属、芽孢杆菌属、假单胞菌属、沙雷氏菌属、镰孢霉属、链霉菌属、节杆菌属、分支杆菌属、短杆菌属和解硫胺素芽孢杆菌属[7-13]等,包含陆地和海洋微生物。枯草芽孢杆菌(Bacillus subtilis)能产生多种抗菌脂肽[14],主要包括伊枯草菌素(Iturin)、芬荠素(Fengycin)和表面活性素(Surfactin)三大家族;其中Iturin和Fengycin相比于其他抗菌脂肽,有较强的抗菌活性;而Surfactin在抑制病毒、支原体等方面有较好的效果[15-18]。这些抗菌脂肽大多可以通过发酵条件优化实现增产[19]。目前,喻钢等[20]建立了基于制备型反相色谱柱分离纯化枯草芽孢杆菌细菌素类抗菌活性物质方法。抗菌脂肽的分离纯化主要通过电荷差异、疏水性质以及分子量不同实现杂质去除,从而达到纯化的目的[21]。
抗菌脂肽作为一种天然的抗菌成分,目前仍面临产率低、成本高等问题[22],在食品、医疗的应用缺少进一步的研究。本实验自主筛选得到一株枯草芽孢杆菌KC-WQ作为出发菌株,考察其胞外发酵产物的抑菌特性,分离其中的抗菌脂肽并解析其结构,通过耐高温测试评价其用于食品加工[23]的潜力。最后优化发酵条件,建立响应面预测模型,旨在提高产量,并为生产流程、实际应用提供理论基础。
1. 材料与方法
1.1 材料与仪器
枯草芽孢杆菌KC-WQ 从发酵豆粕中分离得到,经16S鉴定后保藏于中国典型培养物保藏中心(武汉大学保藏中心,保藏号CCTCC NO:M 2021799);BL21大肠杆菌(Escherichia coli BL21)、鼠伤寒沙门氏菌TA97a(Salmonella TA97a)和嗜水气单胞菌ATCC35654(Aeromonas hydrophila ATCC35654) 均由南京工业大学微生物实验室提供;三氯甲烷 上海凌峰化学试剂有限公司;甲醇 上海迈瑞尔化学技术有限公司;盐酸 永华化学科技有限公司;Surfactin标准品 上海麦克林生化科技有限公司;LB液体培养基、PDA培养基 青岛海博生物技术有限公司。
D-78532隔水式培养箱 上海一恒科学仪器有限公司;UNIVERSAL320(R)离心机 德祥科技有限公司;BKQ-B100II高压蒸汽灭菌锅 赛锶钛氪贸易有限公司;ZQZY-88CN振荡培养箱 上海知楚仪器有限公司;DH100-2干式恒温器 杭州瑞诚仪器有限公司;S210 pH计 梅特勒-托利多仪器有限公司;RE-52AA旋转蒸发器 上海亚荣生化仪器厂;752S紫外可见分光光度计 上海棱光技术有限公司。
1.2 实验方法
1.2.1 菌株活化和培养
将枯草芽孢杆菌KC-WQ接种于LB液体培养基37 ℃、200 r/min条件下培养24 h作为种子液,将种子液以3%浓度接种在Landy改良培养基[19]内,37 ℃、200 r/min条件下发酵48 h。Landy改进培养基:葡萄糖20.0 g,谷氨酸钠5.0 g,酵母提取物1.0 g,MgSO4 0.5 g,KCl 0.5 g,KH2PO4 1.0 g,FeSO4 0.15 mg,MnSO4 0.5 mg,CuSO4 0.16 mg,蒸馏水定容至1.0 L。
1.2.2 牛津杯抑菌圈实验
取出提前制备的平板,划分区域,将50 μL活化接种量为1.5%的沙门氏菌作为指示菌液滴加于PDA平板上,用一次性涂布棒涂布均匀。取出灭菌后的牛津杯放置在平板四个区域,设置只添加100 μL LB培养基作为空白对照,其余三个牛津杯中分别滴加除去菌体的KC-WQ发酵液,加样体积依次为50、100、150 μL。随后平板置于37 ℃培养箱内培养12 h后,观察并测量抑菌圈大小,重复三次,取平均值。
1.2.3 抗菌脂肽的制备
在灭完菌的Landy培养基里按照3%接种量接种,200 r/min,37 ℃发酵48 h,发酵液8000 r/min,4 ℃离心10 min,取上层清夜备用。用6 mol/L HCl调节上层清液pH至4.0,4 ℃、12 h过夜沉淀,8000 r/min,4 ℃离心10 min。离心弃去上层清液,收集沉淀,将得到的沉淀加入过量甲醇溶解。将溶解后的液体过有机膜抽滤除去杂质,45 ℃旋转蒸发浓缩,得到甲醇粗提液。将粗提液用65 ℃烘箱烘干,收集黄色沉淀,即为抗菌脂肽粗提物[22]。
1.2.4 粗提物成分和结构分析
1.2.4.1 TLC薄层色谱分析
称取脂肽粗提物50 mg,溶于1500 μL甲醇作为待测样品溶液。取一块硅胶薄层板,在距离一边1 cm处用铅笔画线,作为样品起始点,设置A、B两组平行实验。按照薄层色谱法,使用毛细管蘸取溶液,分别点于两点上,每次10 μL,点样5次,每次点完用吹风机吹干,备用。配置展开剂为甲醇:三氯甲烷:水=25:65:4。将展开剂、薄层板放入展缸中展开、挥干,观察在紫外灯下的条带。
1.2.4.2 高效液相色谱分析
本部分采用安捷伦1260高效液相色谱仪和ZORBAX Eclipse XDB-C18色谱柱(5 μm,150 mm×4.6 mm)进行分析,样品与标准品均溶于20%乙腈水溶液,流动相A为乙腈(含0.1% 三氟乙酸),流动相B为超纯水(含0.1%三氟乙酸),流动相比例A:B为8:2,流速为1 mL/min,检测波长为214 nm,样品浓度为5 mg/mL,进样体积为60 μL。
1.2.4.3 MALDI-TOF-MS质谱分析
质谱检测条件:粗提物10 mg溶于10 mL甲醇溶剂,正离子检测,DHB基质。使用UltrafleXtreme MALDI-TOF质谱仪(Bruker Daltonics)在反射正离子模式下进行MALDI仪器质谱分析。用智能束激光辐照产生的离子在100~1700 Da的质量范围内获得了质谱,照射频率为1000 Hz,PIE为120 ns,透镜电压为7 kV。第一离子源电压为20 kV,第二离子源电压为17.65 kV。每个光谱由平均1000次激光发射产生,并且激光辐照度被设置为50%~55%。使用FlexAnalysis软件(version:3.3,Bruker)处理质谱图。
1.2.5 耐热性测定
将用上述方法提取的抗菌脂肽配制成1.0 mg/mL的溶液,在45、65、85、105 ℃条件下加热20 min,以未经处理的原样品作为对照组,以沙门氏菌为指示菌评价其抑菌效果,测量抑菌圈直径,重复三次,取平均值。
1.2.6 最小抑菌浓度测定
将由方法1.2.3提取的抗菌脂肽样品做浓度递减稀释,分别为25、12.2、6.2 、3.1、1.6、0.8、0.4 mg/mL,对沙门氏菌做抑菌试验,以抑菌圈大于10 mm为依据确定最小抑菌浓度[21],重复三次,取平均值。
1.2.7 发酵条件优化
1.2.7.1 碳源优化
根据初始发酵培养基,以添加2%碳源进行优化实验,分别选取单一碳源葡萄糖、麦芽糖、蔗糖和混合碳源(葡萄糖1%+淀粉1%)进行单因素实验,保持其余发酵条件一致。使用紫外可见分光光度计测在600 nm处测定OD并按照方法1.2.3所述测定抗菌脂肽粗提物产量,以OD600和抗菌脂肽粗提物产量作为实验评价指标,重复三次,取平均值。
1.2.7.2 氮源优化
在初始发酵培养基的基础上加入0.25%的不同氮源进行单因素实验设计。选取尿素,胰蛋白胨作为氮源,另外设计无氮源对照组同步进行,实验保持其余发酵条件一致。评价方法同上,重复三次,取平均值。
1.2.7.3 摇床转速优化
选择发酵温度为37 ℃,pH为7,装液量为200 mL,发酵时间为48 h,选择转速分别为150、180、200、250 r/min,其余条件保持一致。评价方法同上,重复三次,取平均值。
1.2.7.4 发酵温度优化
选择发酵pH为7,装液量为200 mL,发酵时间为48 h,转速为200 r/min,温度分别为30、33、35、37 ℃,其余条件保持一致。评价方法同上,重复三次,取平均值。
1.2.7.5 发酵初始pH优化
选择发酵温度为37 ℃,装液量为200 mL,发酵时间为48 h,转速为200 r/min,初始pH为5.0、6.0、7.0、8.0,其余条件保持一致。评价方法同上,重复三次,取平均值。
1.2.7.6 响应面试验
在单因素实验培养基优化的基础之上,以抗菌脂肽粗产量Y作为响应值,对初始pH(X1)、发酵温度(X2)、摇床转速(X3)构建三因素三水平的响应面优化分析(表1)。
表 1 各变量及其高低水平设计Table 1. Variables and their high and low level design编号 因素 −1 0 +1 X1 初始pH 6 7 8 X2 发酵温度(℃) 33 35 37 X3 摇床转速(r/min) 150 200 250 1.3 数据处理
数据分统计学析实验重复3次,数据结果用“平均值±标准差”表示,IBM SPSS Statistics 19.0软件进行分析,方差分析(ANOVA)判断多重平均值的显着性,显著性水平P<0.05表示具有统计学意义。
2. 结果与分析
2.1 抑菌活性验证
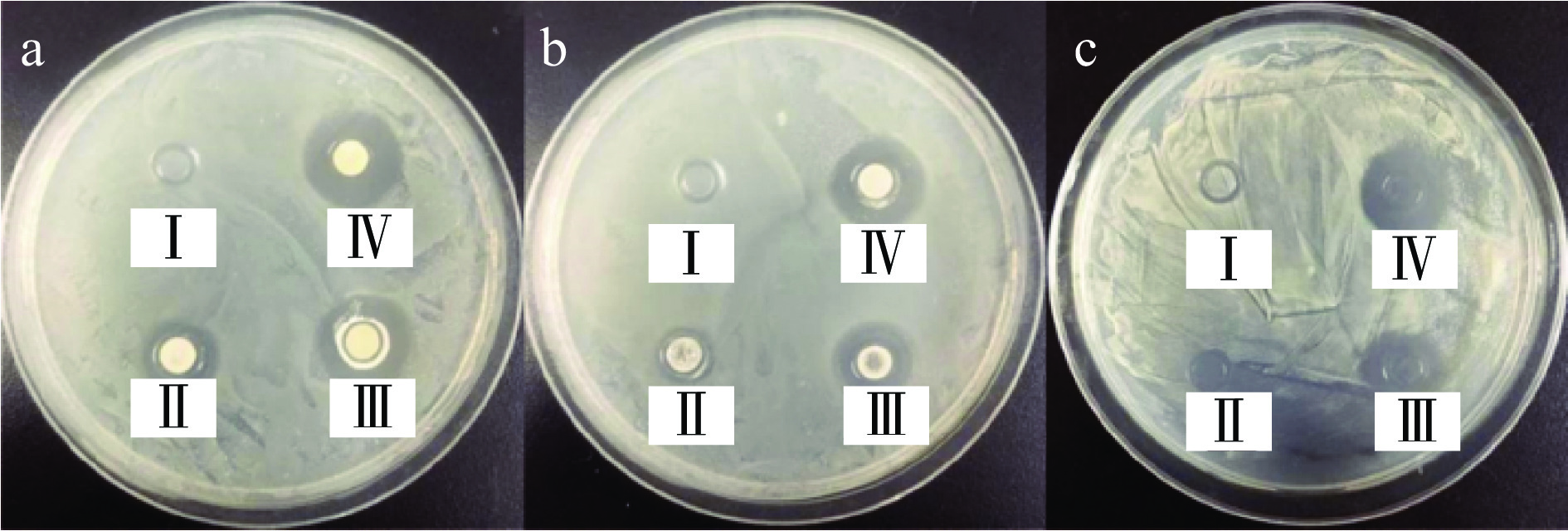
如图1所示,枯草芽孢杆菌KC-WQ发酵液对三种致病菌增殖具有明显的抑菌效果。对比抑菌圈平均值直径的大小发现(表2),发酵液抑菌效果与剂量呈正相关,相同剂量下的发酵液对沙门氏菌的抑制效果最为显著,抑菌圈直径最高达到了(16.50±2.18)mm;对大肠杆菌和嗜水气单胞菌也有较好的抑制效果,最大抑菌圈直径分别为(12.83±2.37)mm和(15.77±1.57)mm。相比白杰等[21]报道的枯草B3菌株,KC-WQ发酵液抑菌效果更为明显,因此为进一步验证抑菌效果,采用沙门氏菌作为指示菌进行后续评价实验。
表 2 枯草芽孢杆菌KC-WQ抑菌圈直径Table 2. Inhibition zone diameter of Bacillus subtilis KC-WQ抑菌圈直径(mm) Ⅰ Ⅱ Ⅲ Ⅳ 沙门氏菌 0.00 11.00±1.00a 14.83±2.47b 16.50±2.18c 大肠杆菌 0.00 11.33±1.53a 12.00±2.65b 12.83±2.37c 嗜水气单胞菌 0.00 10.00±2.00a 14.40±1.04b 15.77±1.57c 注:具有显著性差异的组用不同的字母标记。 2.2 脂肽粗提物产量及结构分析
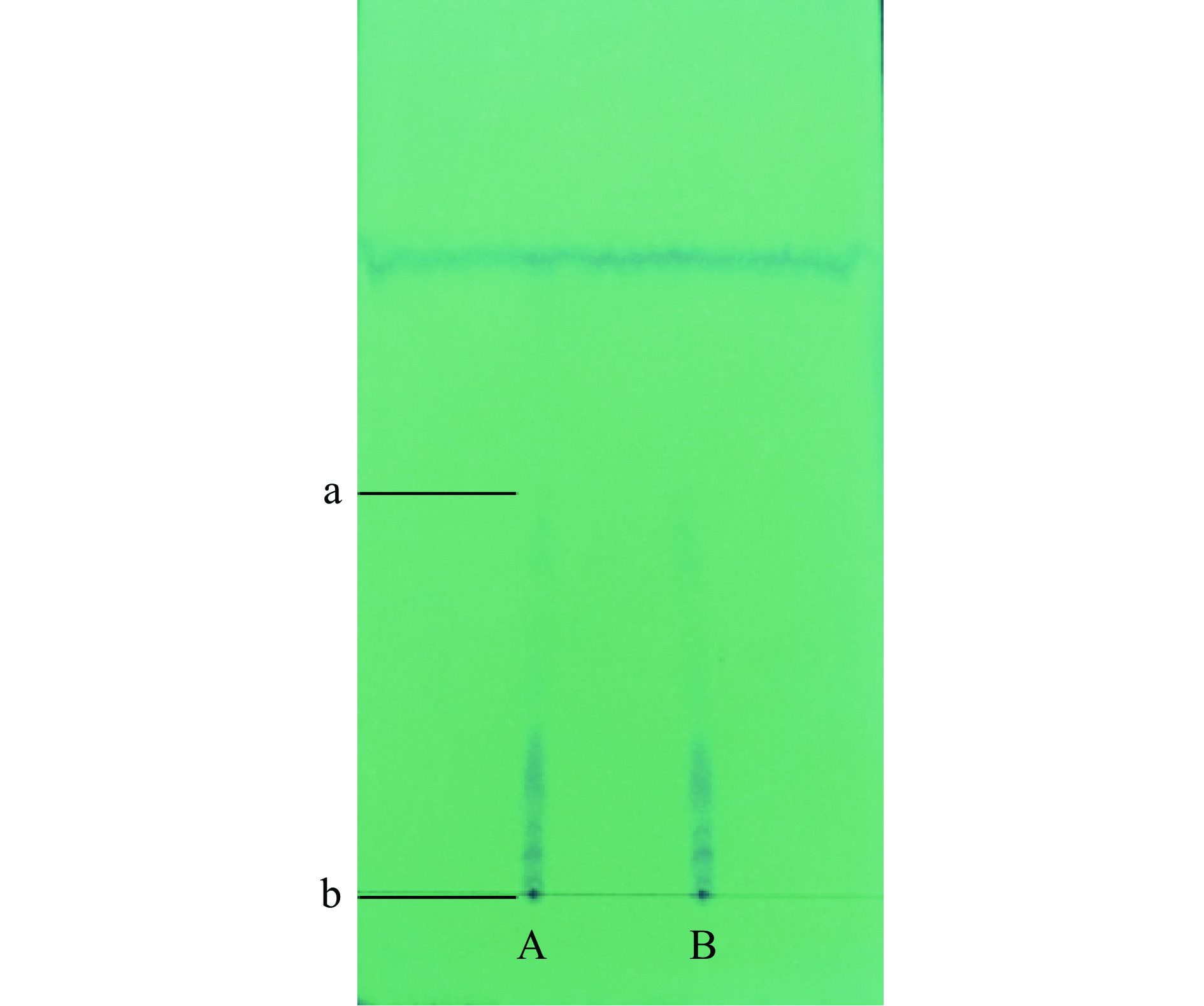
将上述枯草菌株发酵培养,酸沉淀法制得抗菌脂肽,产量为(0.763±0.03)g/L。TCL法对脂肽粗提物进行初步分析,紫外灯下显色后在a、b之间有多段活性成分的显色印迹(图2),表明其组分较为复杂。
2.3 HPLC结果分析
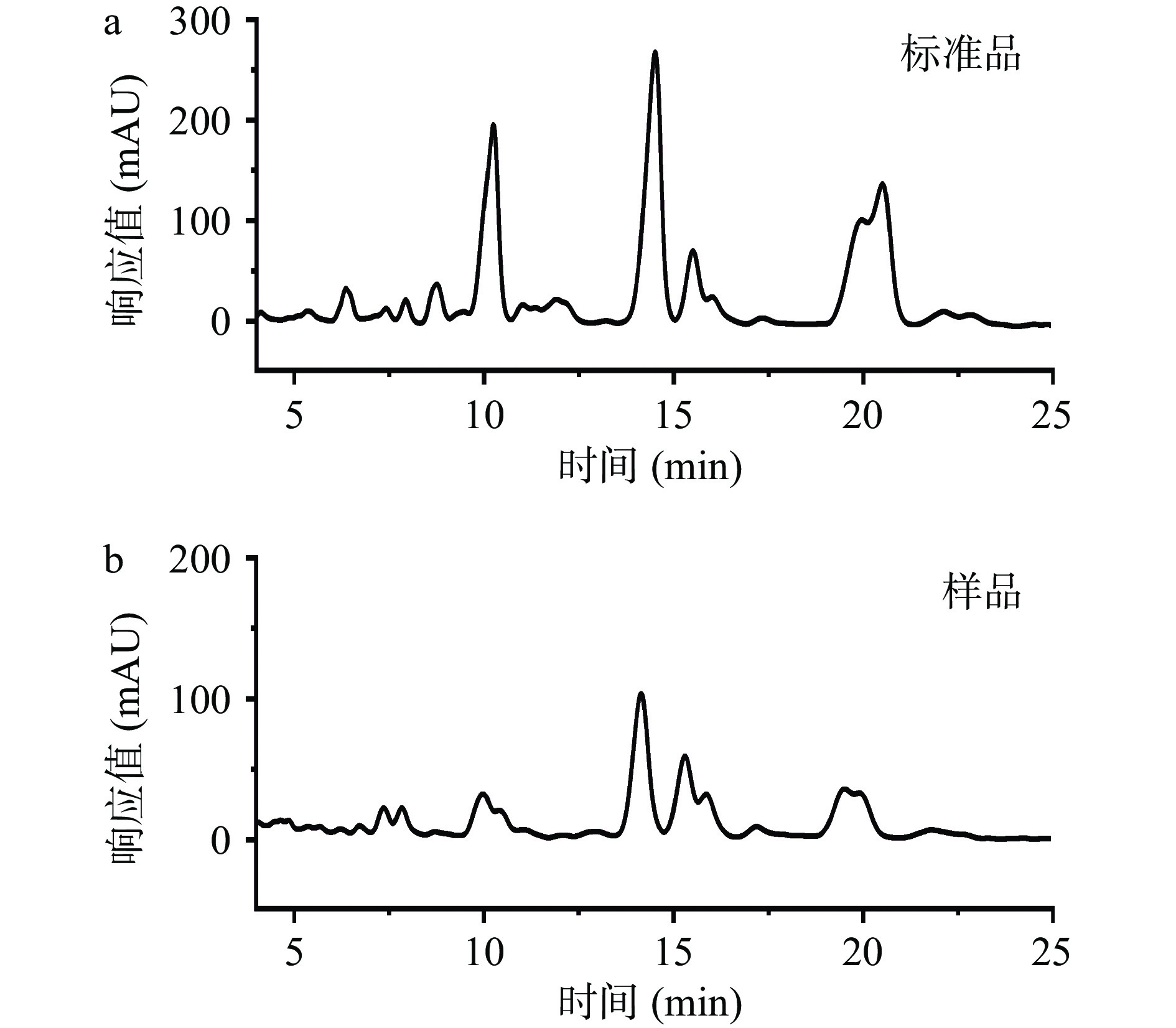
对比KC-WQ的抗菌脂肽样品和Surfactin标准品的液相图谱出峰时间(图3)发现,该菌株粗提物的保留时间在9~20 min之间。抗菌脂肽样品在9~11 min,13~16 min和19~21 min的保留时间与标准品一致,可以证实该抗菌脂肽中含有Surfactin的同系物。
表3结果显示,KC-WQ菌株的脂肽粗提物在HPLC中的保留时间范围为9.977~20.897 min。与Surfactin标准品对比,抗菌脂肽样品中同样保留时间的峰面积占据整个出峰面积的46.315%,表明该抗菌脂肽中有近50%的Surfactin成分,其余脂肽尚无商品化纯品做对照,进一步采用MALDI-TOF-MS鉴定分析。
表 3 脂肽粗提物样品HPLC保留时间及面积Table 3. HPLC retention time and area of crude lipopeptide extract sample保留时间(峰尖,min) 面积 峰面积占比(%) 1 9.977 836.250 4.275 2 10.402 299.384 1.530 3 14.149 2971.641 15.191 4 15.301 1701.197 8.697 5 15.859 841.169 4.300 6 17.189 241.511 1.235 7 19.508 1170.928 5.986 8 20.897 873.000 4.463 2.4 MALDI-TOF-MS分析结果
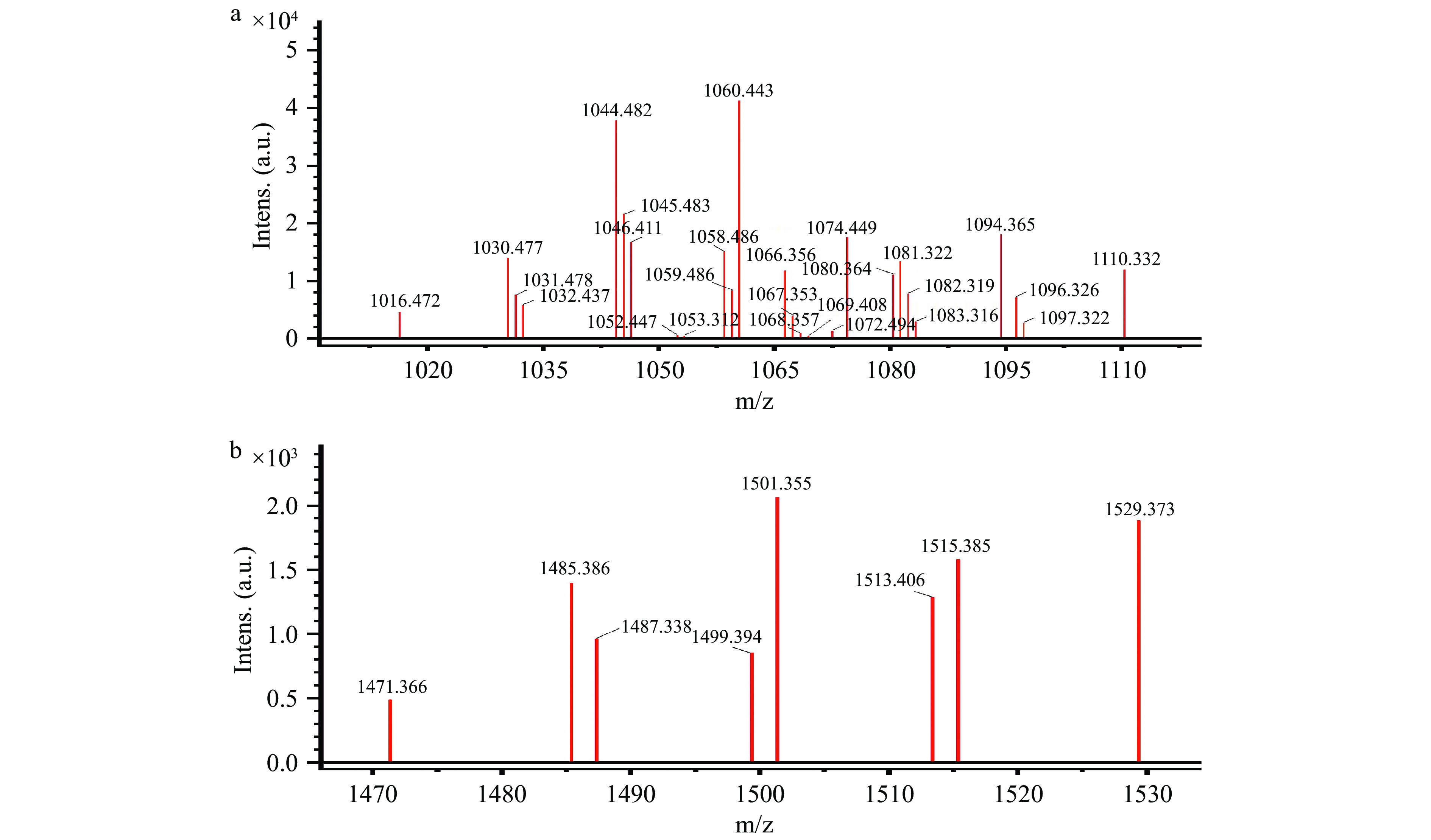
进一步采用质谱分析抗菌脂肽组成,根据黄君[24]的文献报道,采用m/z对脂肽进行分类。m/z在1030.4~1059.4的范围属于Iturin族,在994.4~1036.4属于Surfactin族(图4a),在1449.4~1491.4为Fengycin族(图4b)。由于抗菌脂肽主要由1个疏水脂肪烃链与7~10个氨基酸构成的环肽相连,其结构差异主要表现在脂肪烃链的碳原子个数[25],而脂肪烃链的长短不同,导致了每增加或减少一个碳原子,m/z相差14。本实验得到的抗菌脂肽的主要成分为C13~C16 Iturin、Iturin族中的C13~C15 Bacillomycin D、C12~C15 Surfactin以及少量的C15~C18 Fengycin A(表4)。结果证明这些粗提物的主要成分是三种抗菌脂肽的混合物,有良好的抑菌表现,同时该类抗菌脂肽已被证明具有生物安全性[26],可开发应用于食品加工环节中对有害微生物的控制、防腐保鲜等方面[27]。
表 4 MS结果分析Table 4. MS result analysisFamily m/z (M+H+) (M+Na+) (M+K+) Iturin C13~C16 1030.477 1052.447 1068.357 1044.482 1066.356 1082.319 1058.486 1080.364 1096.326 1072.494 1094.365 1110.332 C13~C15 Bacillomycin D 1031.478 1053.312 1069.408 1045.483 1067.353 1083.316 1059.486 1081.322 1097.322 Surfactin C12~C15 Surfactin − 1016.472 1032.437 − 1030.477 1046.441 − 1044.482 1060.443 − 1058.486 1074.449 Fengycin C15~C18 Fengycin A − 1471.366 1487.338 − 1485.386 1501.355 − 1499.394 1515.385 − 1513.406 1529.373 2.5 抗菌脂肽理化性质分析
2.5.1 温度对抗菌脂肽的影响
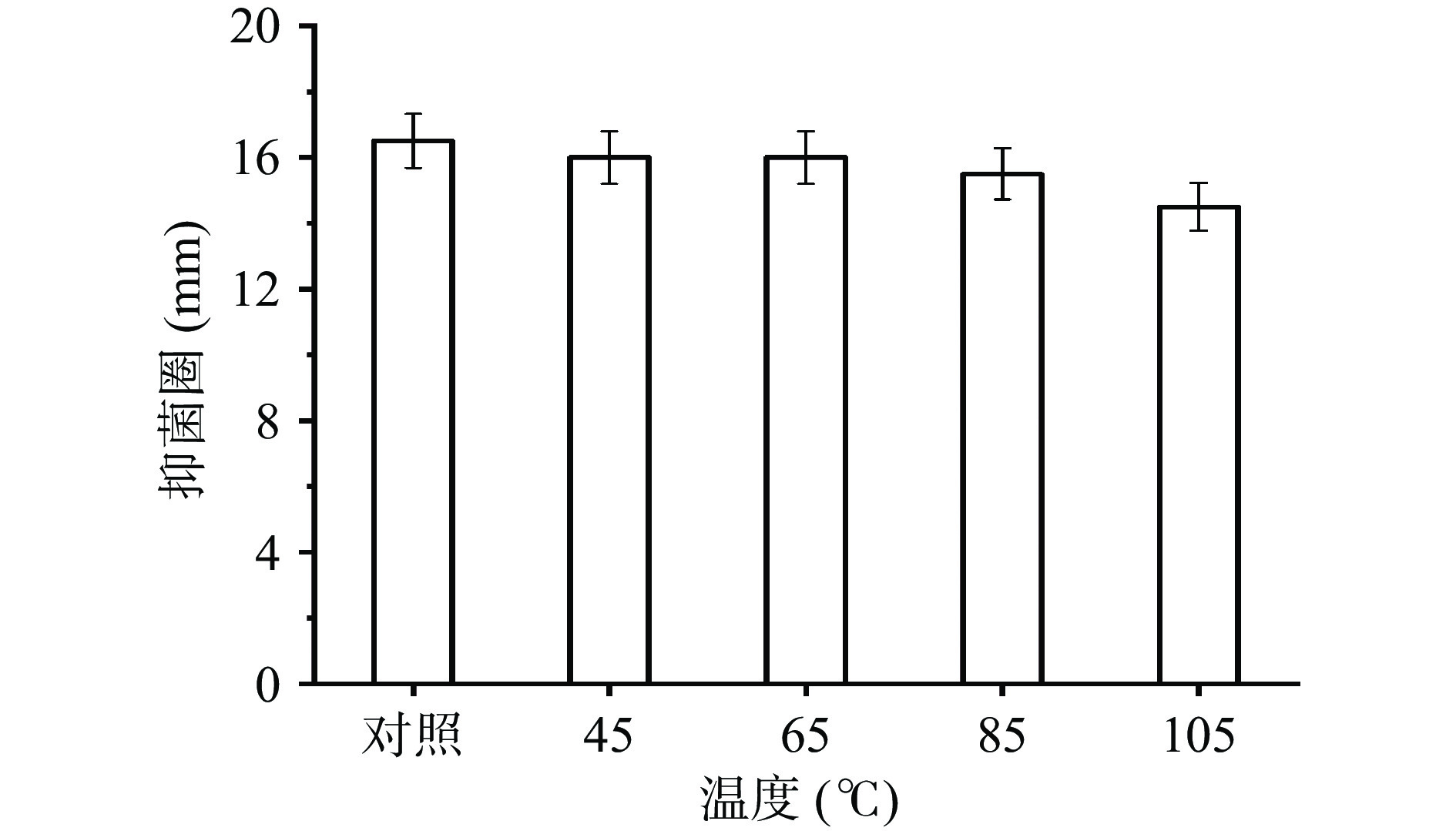
牛津杯法抑菌实验的结果发现(图5),枯草KC-WQ的脂肽粗提物经45、65、85、105 ℃处理20 min后,抑菌效果并未出现明显变化。抑菌圈直径随着温度的上升略有数值降低但不显著(P<0.05),说明该脂肽粗提物中的抑菌成分可耐高温。这些短链多肽具有热稳定性,可进行喷干等涉及高温处理的工艺[28],具有较好的加工特性。
2.5.2 最小抑菌浓度测定
由表5可知,该抗菌脂肽在较低浓度时仍对沙门氏菌有抑菌效果,最小抑菌质量浓度为0.8 mg/mL。
表 5 不同浓度的KC-WQ抗菌脂肽对沙门氏菌的抑菌效果Table 5. Inhibition of different concentrations of KC-WQ crude lipopeptide against Salmonella抗菌脂肽质量浓度(mg·mL−1) 抑菌圈直径(mm) 0.4 − 0.8 10.0±0.1 1.6 11.0±0.1 3.1 11.5±0.3 6.2 12.6±0.3 12.2 14.7±0.3 25 16.7±0.2 2.6 发酵条件优化结果
2.6.1 碳源优化结果
实验得到的脂肽粗产物及OD值如图6(a)所示。在对碳源的优化中,发现葡萄糖和淀粉以1:1,共20 g/L的浓度时抗菌脂肽粗产量实现最大,同时在600 nm波长处的吸光值也是同组实验最大值。在发酵过程中,碳源的选择直接影响到细菌的繁殖及代谢速率,在一定范围内,发酵液菌群浓度与其在600 nm波长处的吸光值成正比[29],且在吸光度最大时,抗菌脂肽产量最高。根据以上结果,可以选取葡萄糖+淀粉作为最佳碳源。
2.6.2 氮源优化结果
实验得到的粗产物质量及OD值如图6(b)所示。从结果中可以看出,添加胰蛋白胨时该菌的粗产物产量最高,并且发酵菌液在600 nm的吸光度为最高,由于氮源包含大量菌体在生长代谢过程中所需物质,不仅影响菌体繁殖生长,也会影响后期的抗菌脂肽的产量。胰蛋白胨含有丰富的氮源和氨基酸,促进菌体的生长代谢,因此可以作为KC-WQ枯草芽孢杆菌最佳氮源。
2.6.3 摇床发酵条件优化结果
摇床转速是决定发酵过程中通气量的关键因素,通气量对菌体的氧化分解作用有着显著的影响。优化结果如图7a所示。在转速达到200 r/min时,得到的粗产物产量及OD值均为最大。当转速变高或者降低时,都会导致反应产物及OD值减少,枯草芽孢杆菌属于好氧菌,适当提高转速有利于其增殖和脂肽积累,因此选用200 r/min的转速作为适宜摇床转速。
初始pH对菌体生长有显著的影响,pH过高或过低都会影响发酵速度和发酵产量。优化结果如图7b所示。当pH为5时,脂肽粗产量最低;之后随pH的升高,产量上升;当环境呈现略碱性时(pH8),产量反而下降,但仍高于pH5时的产量。因此综合考虑适宜发酵初始pH为7.0进行后续试验。
温度是影响菌体发酵的重要因素,温度过高会加快菌体的代谢反应速率,缩短生长周期,菌体提前衰老影响发酵。温度太低则会导致氧化还原速率降低,菌体生长周期变长,抗菌脂肽产量下降。优化结果如图7c所示。随着温度的升高,粗产物产量和OD值稳步提高,到达35 ℃时达到顶峰,随后下降。因此可以选取35 ℃作为发酵的适宜温度。
2.7 响应面试验
利用Design-Expert软件建立回归方程进行结果分析,以抗菌脂肽粗产量Y值作为响应值,得出多元拟合二项式模型,并对模型的显著性进行评估,最终预测出最佳发酵条件,根据预测值进行实验验证,判断模型的契合度。
利用Design-Expert软件对表6的数据进行分析设计,得出脂肽粗产量(Y)对初始pH(X1)、发酵温度(X2)和摇床转速(X3)的二次多项回归模型方程为:
表 6 响应值试验及结果Table 6. Response value test and results实验号 因素 脂肽粗产量(g/L) X1 X2 X3 1 7 35 200 1.256±0.06 2 7 37 250 1.224±0.06 3 6 35 250 1.021±0.05 4 6 37 200 0.976±0.04 5 7 35 200 1.324±0.06 6 8 37 200 0.889±0.04 7 7 37 150 1.132±0.05 8 8 35 150 1.024±0.05 9 7 35 200 1.256±0.06 10 8 33 200 0.932±0.04 11 7 35 200 1.256±0.06 12 7 35 200 1.256±0.06 13 7 33 150 1.004±0.05 14 6 35 150 0.952±0.04 15 7 33 250 1.136±0.05 16 8 35 250 1.044±0.05 17 6 33 200 0.951±0.04 Y=−40.91188+1.78756X1+2.00011X2+0.011482X3−8.447371×10−3X1X2−2.25789×10−4X1X3−10−4X2X3−0.11136X12−0.027356X22−1.44700×10−5X32
从表7得知,模型的F值为15.15,P值为0.0008,达到了显著水平,失拟项为0.0954>0.05,不显著。发酵条件X1的P<0.001,说明初始pH对发酵影响非常显著;X2的P<0.01,说明发酵温度对发酵高度显著;X3表现出不显著。模型的决定系数R2=0.9512>0.9,说明模型的线性关系显著,校正决定系数R2Adj=0.8884,说明模型与实验数据契合度较高,因此可以用模型预测发酵条件对枯草芽孢杆菌抗菌脂肽产量的影响。
表 7 二次多项回归模型方差结果Table 7. Quadratic polynomial regression model variance results方差来源 平方和 自由度 均方 F值 P 显著性 模型 0.31 9 0.034 15.15 0.0008 *** X1 0.071 1 0.071 31.68 0.0008 *** X2 0.053 1 0.053 23.84 0.0018 ** X3 3.433E-003 1 3.433E-003 1.53 0.2560 不显著 X1X2 2.712E-003 1 2.712E-003 1.21 0.3080 不显著 X1X3 1.211E-003 1 1.211E-003 0.54 0.4865 不显著 X2X3 4.000E-004 1 4.000E-004 0.18 0.6855 不显著 X12 0.20 1 0.20 87.94 <0.0001 *** X22 0.050 1 0.050 22.47 0.0021 ** X32 5.510E-003 1 5.510E-003 2.46 0.1611 不显著 残差 0.016 7 2.244E-003 失拟项 0.012 3 4.002E-003 4.33 0.0954 不显著 纯误差 3.699E-003 4 9.248E-003 总和 0.32 16 注:R2=0.9512,R2Adj=0.8884,*P<0.05,**P<0.01,*** P<0.001。 2.7.1 构建响应面分析结果
根据回归模型并利用Design-Expert软件绘制出响应面优化结果,得到了发酵温度、摇床转速、初始pH三个因素之间的3D模型图,图8a反应了摇床转速与初始pH对脂肽粗产量的交互关系,图8b反应了发酵温度与初始pH对脂肽粗产量的交互关系,图8c反应了摇床转速与发酵温度对脂肽粗产量的交互关系。经过软件进一步的结果分析,得出响应面分析结果优化后的预测发酵条件:初始pH=6.0,发酵温度为36 ℃,摇床转速为208 r/min,预测产物产量为1.311 g/L。
2.7.2 回归模型的验证
为了检验模型的准确性,对模型预测的数值进行检测实验。为便于实验的操作性,所有预测值取整数,因此取发酵温度为36 ℃,初始pH=6.0,摇床转速为208 r/min。设置三个平行组,选用优化培养基进行发酵实验,最后得到抗菌脂肽粗产量为1.236 g/L,达到了预测值的94.28%,数值较为接近预测值,说明模型预测可靠性高,可以较好地反映发酵条件各个因素对产物的影响。
3. 结论
枯草芽孢杆菌是一种天然的益生菌,分泌纯天然的抗菌脂肽,在食品、医疗等领域有着较好的开发前景。本实验以筛选到的枯草KC-WQ为研究对象,其胞外产物具有抑菌特性,对肠道类致病菌有着较好的抑菌效果;酸沉淀法获得抗菌脂肽,结合TLC、MALDI-TOF-MSL和HPLC,鉴定其主要成分为Iturin、Bacillomycin D、Surfactin和Fengycin A。该抑菌脂肽具有较好的耐热性,对沙门氏菌的最小抑菌浓度为0.8 mg/mL。最后,针对该菌株进行发酵条件优化,设计响应面和回归方程,得到最适发酵条件:初始pH6.0,发酵温度为36 ℃,摇床转速为208 r/min,预测产量为1.311 g/L,经实验验证,最后实际得到的抗菌脂肽产量为1.236 g/L。本研究获得的枯草芽孢杆菌KC-WQ,其胞外所产抗菌脂肽对Salmonella enterica subsp. enterica、Aeromonas hydrophila和Escherichia coli等常见食源性污染菌具有显著抑菌效果,理化性质稳定,在食品加工行业具备应用潜质。
-
表 1 各变量及其高低水平设计
Table 1 Variables and their high and low level design
编号 因素 −1 0 +1 X1 初始pH 6 7 8 X2 发酵温度(℃) 33 35 37 X3 摇床转速(r/min) 150 200 250 表 2 枯草芽孢杆菌KC-WQ抑菌圈直径
Table 2 Inhibition zone diameter of Bacillus subtilis KC-WQ
抑菌圈直径(mm) Ⅰ Ⅱ Ⅲ Ⅳ 沙门氏菌 0.00 11.00±1.00a 14.83±2.47b 16.50±2.18c 大肠杆菌 0.00 11.33±1.53a 12.00±2.65b 12.83±2.37c 嗜水气单胞菌 0.00 10.00±2.00a 14.40±1.04b 15.77±1.57c 注:具有显著性差异的组用不同的字母标记。 表 3 脂肽粗提物样品HPLC保留时间及面积
Table 3 HPLC retention time and area of crude lipopeptide extract sample
保留时间(峰尖,min) 面积 峰面积占比(%) 1 9.977 836.250 4.275 2 10.402 299.384 1.530 3 14.149 2971.641 15.191 4 15.301 1701.197 8.697 5 15.859 841.169 4.300 6 17.189 241.511 1.235 7 19.508 1170.928 5.986 8 20.897 873.000 4.463 表 4 MS结果分析
Table 4 MS result analysis
Family m/z (M+H+) (M+Na+) (M+K+) Iturin C13~C16 1030.477 1052.447 1068.357 1044.482 1066.356 1082.319 1058.486 1080.364 1096.326 1072.494 1094.365 1110.332 C13~C15 Bacillomycin D 1031.478 1053.312 1069.408 1045.483 1067.353 1083.316 1059.486 1081.322 1097.322 Surfactin C12~C15 Surfactin − 1016.472 1032.437 − 1030.477 1046.441 − 1044.482 1060.443 − 1058.486 1074.449 Fengycin C15~C18 Fengycin A − 1471.366 1487.338 − 1485.386 1501.355 − 1499.394 1515.385 − 1513.406 1529.373 表 5 不同浓度的KC-WQ抗菌脂肽对沙门氏菌的抑菌效果
Table 5 Inhibition of different concentrations of KC-WQ crude lipopeptide against Salmonella
抗菌脂肽质量浓度(mg·mL−1) 抑菌圈直径(mm) 0.4 − 0.8 10.0±0.1 1.6 11.0±0.1 3.1 11.5±0.3 6.2 12.6±0.3 12.2 14.7±0.3 25 16.7±0.2 表 6 响应值试验及结果
Table 6 Response value test and results
实验号 因素 脂肽粗产量(g/L) X1 X2 X3 1 7 35 200 1.256±0.06 2 7 37 250 1.224±0.06 3 6 35 250 1.021±0.05 4 6 37 200 0.976±0.04 5 7 35 200 1.324±0.06 6 8 37 200 0.889±0.04 7 7 37 150 1.132±0.05 8 8 35 150 1.024±0.05 9 7 35 200 1.256±0.06 10 8 33 200 0.932±0.04 11 7 35 200 1.256±0.06 12 7 35 200 1.256±0.06 13 7 33 150 1.004±0.05 14 6 35 150 0.952±0.04 15 7 33 250 1.136±0.05 16 8 35 250 1.044±0.05 17 6 33 200 0.951±0.04 表 7 二次多项回归模型方差结果
Table 7 Quadratic polynomial regression model variance results
方差来源 平方和 自由度 均方 F值 P 显著性 模型 0.31 9 0.034 15.15 0.0008 *** X1 0.071 1 0.071 31.68 0.0008 *** X2 0.053 1 0.053 23.84 0.0018 ** X3 3.433E-003 1 3.433E-003 1.53 0.2560 不显著 X1X2 2.712E-003 1 2.712E-003 1.21 0.3080 不显著 X1X3 1.211E-003 1 1.211E-003 0.54 0.4865 不显著 X2X3 4.000E-004 1 4.000E-004 0.18 0.6855 不显著 X12 0.20 1 0.20 87.94 <0.0001 *** X22 0.050 1 0.050 22.47 0.0021 ** X32 5.510E-003 1 5.510E-003 2.46 0.1611 不显著 残差 0.016 7 2.244E-003 失拟项 0.012 3 4.002E-003 4.33 0.0954 不显著 纯误差 3.699E-003 4 9.248E-003 总和 0.32 16 注:R2=0.9512,R2Adj=0.8884,*P<0.05,**P<0.01,*** P<0.001。 -
[1] 孙颖颖, 董鹏程, 朱立贤, 等. 食源性致病菌快速检测研究进展[J]. 食品与发酵工业,2020,46(17):264−270. [SUN Y Y, DONG P C, ZHU L X, et al. Research progress in rapid detection of foodborne pathogens[J]. Food and Fermentation Industries,2020,46(17):264−270. SUN Y Y, DONG P C, ZHU L X, et al. Research progress in rapid detection of foodborne pathogens[J]. Food and Fermentation Industries, 2020, 46(17): 264-270.
[2] 金伟伟, 贾振华, 宋水山. 芽胞杆菌产生的脂肽类抗生素的结构和应用[J]. 微生物学杂志,2017,37(3):122−127. [JIN W W, JIA Z H, SONG S S. Structure and the application of lipopeptides antibiotics from Bacillus[J]. Journal of Microbiology,2017,37(3):122−127. doi: 10.3969/j.issn.1005-7021.2017.03.020 JIN W W, JIA Z H, SONG S S. Structure and the application of lipopeptides antibiotics from Bacillus[J]. Journal of Microbiology, 2017 , 37(3): 122-127. doi: 10.3969/j.issn.1005-7021.2017.03.020
[3] RATHINAKUMAR R, WALKENHORST W F, WIMLEY W C, et al. Broad-spectrum antimicrobial eptides by rational combinatorial design and high-throughput screening the importance of interfacial activity[J]. Journal of the American Chemical Society,2009,131(22):7609−7617. doi: 10.1021/ja8093247
[4] 高晓平, 胡惠, 黄现青. Surfactin抑制乳中大肠杆菌O157活性研究[J]. 食品科学,2009,30(11):91−94. [GAO X P, HU H, HUANG X Q. Sterilization effect of Surfactin on Escherichia coli O157 in fresh milk[J]. Food Science,2009,30(11):91−94. GAO X P, HU H, HUANG X Q. Sterilization effect of Surfactin on Escherichia coli O157 in fresh milk[J]. Food Science, 2009, 30(11):91-94.
[5] MANDAL S M, BARBOSA A, FRANCO O L. Lipopeptides in microbial infection control: Scope and reality for industry[J]. Biotechnology Advances,2013,31(2):338−345. doi: 10.1016/j.biotechadv.2013.01.004
[6] HUANG E, YOUSEF A E. The lipopeptide antibiotic paenibacterin binds to the bacterial outer membrane and exerts bactericidal activity through cytoplasmic membrane damage[J]. Appl Environ Microbiol,2014,80(9):2700−2704. doi: 10.1128/AEM.03775-13
[7] SUGAWARA K, NUMATA K I, KONISHI M, et al. Empedopeptin (BMY-28117), a new depsipeptide antibiotic. II. Structure determination[J]. Journal of Antibiotics,1984,37(9):958−964. doi: 10.7164/antibiotics.37.958
[8] WASHIO K, LIM S P, ROONGSAWANG N, et al. Identification and characterization of the genes responsible for the production of the cyclic lipopeptide arthrofactin by Pseudomonas sp. MIS38[J]. Journal of the Agricultural Chemical Society of Japan,2010,74(5):992−999.
[9] SM GUÉRET, MEIER P, ROTH H J. Cyclic carbo-isosteric depsipeptides and peptides as a novel class of peptidomimetics[J]. Organic Letters,2014,16(5):1502−1505. doi: 10.1021/ol5003797
[10] KIHO T, NAKAYAMA M, YASUDA K, et al. Structure-activity relationships of globomycin analogues as antibiotics[J]. Bioorganic & Medicinal Chemistry,2004,12(2):337−361.
[11] VILELA W F D, FONSECA S G, FANTINATTI-GARBOGGINI F, et al. Production and properties of a surface-active lipopeptide produced by a new marine Brevibacterium luteolum strain[J]. Applied Biochemistry & Biotechnology,2014,174(6):2245−2256.
[12] SHARAFI H, ABDOLI M, HAJFARAJOLLAH H, et al. First report of a lipopeptide biosurfactant from thermophilic bacterium Aneurinibacillus thermoaerophilus MK01 newly isolated from municipal landfill site[J]. Applied Biochemistry & Biotechnology,2014,173(5):1236−1249.
[13] 连玲丽, 谢荔岩, 郑璐平, 等. 拮抗菌SB1的鉴定及其抗菌物质的分析[J]. 微生物学通报,2010,37(7):986−991. [LIAN L L, XIE L Y, ZHENG L P, et al. Identification of antagonistic Bacterium SB1 and analysis on its antibacterial substance[J]. Microbiology,2010,37(7):986−991. LIAN L L, XIE L Y, ZHENG L P, et al. Identification of antagonistic Bacterium SB1 and analysis on its antibacterial substance[J]. Microbiology, 2010, 37(7): 986-991.
[14] CHEN Y, X GAO, WEI Y, et al. Isolation, purification and anti-hypertensive effect of a novel angiotensin i-converting enzyme (ACE) inhibitory peptide from ruditapes philippinarum fermented with Bacillus natto[J]. Food & Function,2018,9(10):1039.
[15] 丁飞鸿, 耿云龙, 樊士德, 等. 抑制食源性致病菌脂肽的分离鉴定及生物学特性分析[J]. 食品与发酵工业,2022,48(6):195−203. [DING F H, GENG Y L, FAN S D, et al. Isolation, identifica- tion and biological characteristics analysis of lipopeptides that inhibit food-borne pathogens[J]. Food and Fermentation Industries,2022,48(6):195−203. doi: 10.13995/j.cnki.11-1802/ts.028471 DING F H, GENG Y L, FAN S D, et al. Isolation, identifica- tion and biological characteristics analysis of lipopeptides that inhib- it food-borne pathogens[J]. Food and Fermentation Industries, 2022, 48(6): 195-203. DOI: 10.13995/j.cnki.11-1802/ts.028471.
[16] VOLLENBROICH D, PAULI G, OZEL M, et al. Antimycoplasma properties and application in cell culture of surfactin, a lipopeptide antibiotic from Bacillus subtilis[J]. Appl Environ Microbiol,1997,63(1):44−49. doi: 10.1128/aem.63.1.44-49.1997
[17] 高学文, 姚仕义, HUONG Pham, 等. 基因工程菌枯草芽孢杆菌GEB3产生的脂肽类抗生素及其生物活性研究[J]. 中国农业科学,2003,36(12):1496−1501. [GAO X W, YAO S Y, HUONG Pham, et al. Lipopeptide antibiotics produced by the engineered strain Bacillus subtilis GEB3 and detection of its bioactivity[J]. Scientla Agricultura Scinica,2003,36(12):1496−1501. doi: 10.3321/j.issn:0578-1752.2003.12.012 GAO X W, YAO S Y, Huong Pham, et al. Lipopeptide antibiotics produced by the engineered strain Bacillus subtilis GEB3 and detection of its bioactivity[J]. Scientla Agricultura Scinica, 2003, 36(12): 1496-1501. doi: 10.3321/j.issn:0578-1752.2003.12.012
[18] TSUKAGOSHI N, TAMURA G, ARIMA K. A novel protoplast-bursting factor (surfactin) obtained from Bacillus subtilis IAM 1213. I. The effects of surfactin on Bacillus megaterium KM[J]. Biochimica et Biophysica Acta,1970,196(2):211−214. doi: 10.1016/0005-2736(70)90008-8
[19] 王帅, 高圣风, 高学文, 等. 枯草芽孢杆菌脂肽类抗生素发酵和提取条件[J]. 中国生物防治,2007,23(4):342−347. [WANG S, GAO S F, GAO X W, et al. Fermentation and extraction conditions of Bacillus subtilis lipopeptide antibiotics[J]. Chinese Journal of Biological Control,2007,23(4):342−347. WANG S, GAO S F, GAO X W, et al. Fermentation and extraction conditions of Bacillus subtilis lipopeptide antibiotics[J]. Chinese Journal of Biological Control, 2007, 23(4): 342-347.
[20] 喻钢, 田万红, 董思国, 等. 枯草芽孢杆菌抗菌脂肽的分离纯化及质谱检测[J]. 药物分析杂志,2014(10):56−61. [YU G, TIAN W H, DONG S G, et al. Study on purification and mass spectrometric detection of antimicrobial peptide from Bacillus subtilis[J]. Chinese Journal of Pharmaceutical Analysis,2014(10):56−61. YU G, TIAN W H, DONG S G, et al. Study on purification and mass spectrometric detection of antimicrobial peptide from Bacillus subtilis[J]. Chinese Journal of Pharmaceutical Analysis, 2014(10): 56-61
[21] 白杰, 贠建民, 祝发明, 等. 枯草芽孢杆菌菌株B3抗菌脂肽的分离纯化与鉴定[J]. 食品与发酵工业,2018,44(8):82−89. [BAI J, YUN J M, ZHU F M, et al. Isolation, purification and identification of antibacterial peptide from Bacillus subtilis strain B3[J]. Food and Fermentation Industries,2018,44(8):82−89. BAI J, YUN J M, ZHU F M, et al. Isolation, purification and identification of antibacterial peptide from Bacillus subtilis strain B3[J]. Food and Fermentation Industries, 2018, 44(8): 82-89.
[22] 曾国洪, 丛丽娜, 毕楠. 枯草芽孢杆菌诱变株产抗菌脂肽的特性[J]. 大连工业大学学报,2019,38(4):235−238. [ZENG G H, CONG L N, BI N. Characteristics of antimicrobial lipopeptides produced by Bacillus subtilis mutant strains[J]. Journal of Dalian Polytechnic University,2019,38(4):235−238. ZENG G H, CONG L N, BI N. Characteristics of antimicrobial lipopeptides produced by Bacillus subtilis mutant strains[J]. Journal of Dalian Polytechnic University, 2019, 38(4): 235-238.
[23] FU T, ISLAM M S, ALI M, et al. Two antimicrobial genes from Aegilops tauschii cosson identified by the Bacillus subtilis expression system[J]. Scientific Reports,2020,10(1):13346. doi: 10.1038/s41598-020-70314-5
[24] 黄君. 海洋枯草芽孢杆菌HS-A38产抗菌脂肽类物质发酵条件的优化[D]. 大连: 大连工业大学, 2018. HUANG J. Optimization of the fermentation conditions of Bacillus subtilis HS-A38[D]. Dalian: Dalian Polytechnic University, 2018.
[25] 金清, 肖明. 新型抗菌脂肽——表面活性素、伊枯草菌素和丰原素[J]. 微生物与感染,2018,13(1):56−64. [JIN Q, XIAO M. Novel antimicrobial peptides: Surfactin, iturin and fengycin[J]. Journal of Microbes and Infections,2018,13(1):56−64. doi: 10.3969/j.issn.1673-6184.2018.01.010 JIN Q, XIAO M. Novel antimicrobial peptides: surfactin, iturin and fengycin[J]. Journal of Microbes and Infections, 2018, 13(1): 56-64. doi: 10.3969/j.issn.1673-6184.2018.01.010
[26] CHUA B Y, ZENG W, LAU Y F, et al. Comparison of lipopeptide-based immunocontraceptive vaccines containing different lipid groups[J]. Vaccine,2007,25(1):92−101. doi: 10.1016/j.vaccine.2006.07.012
[27] 陈亮, 秦素雅, 衡军影, 等. 微生物抗菌脂肽在食品工业中的应用研究进展[J]. 河南工业大学学报:自然科学版,2018,39(5):119−126. [CHEN L, QIN S Y, HENG J Y, et al. Research and application advances of antimicrobial peptides in food industry[J]. Journal of Henan University of Technology (Natural Science Edition),2018,39(5):119−126. CHEN L, QIN S Y, HENG J Y, et al. Research and application advances of antimicrobial peptides in food industry[J]. Journal of Henan University of Technology (Natural Science Edition), 2018, 39(5): 119-126.
[28] NITSCHKE M, PASTORE G M. Production and properties of a surfactant obtained from Bacillus subtilis grown on cassava waste[J]. Bioresource Technology,2006,97(2):336−341. doi: 10.1016/j.biortech.2005.02.044
[29] 何岚, 王柳懿, 朱琪, 等. 两种绘制枯草芽孢杆菌和大肠杆菌生长曲线方法的比较[J]. 天津农业科学,2017,23(5):14−18. [HE L, WANG L Y, ZHU Q, et al. Comparison of two methods for drawing the growth curve of Bacillus subtilis and Escherichia coli[J]. Tianjin Agricultural Sciences,2017,23(5):14−18. doi: 10.3969/j.issn.1006-6500.2017.05.004 HE L, WANG L Y, ZHU Q, QIAO J Y, WANG W J. Comparison of two methods for drawing the growth curve of Bacillus subtilis and Escherichia coli[J]. Tianjin Agricultural Sciences, 2017, 23(5): 14-18. doi: 10.3969/j.issn.1006-6500.2017.05.004
-
期刊类型引用(3)
1. 贾健辉,窦博鑫,高嫚,张楚佳,刘颖,张娜. 染料木素对α-葡萄糖苷酶的抑制及分子机制. 食品工业科技. 2025(05): 63-71 .  本站查看
本站查看
2. 张楚佳,贾健辉,高嫚,王泽冉,刘颖,窦博鑫,张娜. 3种物理方法制备抗性粳米淀粉的结构与物化特性. 中国食品学报. 2025(01): 193-207 .  百度学术
百度学术
3. 高嫚,贾健辉,张楚佳,张智,刘颖,窦博鑫,张娜. 粳米重组米的制备工艺优化及性能研究. 食品工业科技. 2024(05): 169-176 .  本站查看
本站查看
其他类型引用(2)





 下载:
下载:



 下载:
下载:



