Preparation and Characterization of Multiple Composite Fluid Gel
-
摘要: 本研究以不同工艺条件下制备的复合流体凝胶为研究对象,综合考察凝胶强度、质量损失率和感官评定结果,在确定各因素的较优作用水平基础上,运用五因素四水平正交试验,确定多元复合凝胶最优制备工艺:乙酰化二淀粉磷酸酯、水解明胶和大豆油的添加量分别为6.5%、5.5%和8%,pH6.5,氯化钙浓度0.35 mol/L。基于综合评分结果,从正交组中筛选出中间组和最低组,并与最优组的各项凝胶特性指标结果进行比较。差示扫描量热结果显示,最优组持水性最好,非冻结水含量达50.33%,较中间组和最低组分别提高5.93%和12.75%;最优组最终固体残留物含量最高,达14.51%,表明其稳定性最好;最优组样品中分子作用力统一呈疏水作用力>氢键>静电作用力趋势;傅里叶红外光谱结果与分子作用力结果相互印证,均说明最优组氢键较中间组和最低组更强。综上,优化后的复合流体凝胶流变特性良好,内部结构更稳定,因此,在食品流体凝胶应用方面具有较大潜力。Abstract: The composite fluid gels prepared by different process were taken as the research object in this study. The gel strength, mass loss rate and sensory evaluation results were comprehensively investigated to determine the optimal level of each factor. On this basis, the orthogonal test of five factors and four levels was used to determine the optimal preparation process of the multiple composite gel: The addition of acetylated distarch phosphate, hydrolyzed gelatin and soybean oil were 6.5%, 5.5% and 8% respectively, pH6.5 and calcium chloride concentration 0.35 mol/L. According to the results of the comprehensive scores, the intermediate group and the lowest group were selected from the orthogonal group, and the results of each gel characteristic index of above two groups were compared with those of the optimal group. The results of differential scanning calorimetry showed that the water holding capacity of the optimal group was the best, and the content of unfrozen water was 50.33%, which was 5.93% and 12.75% higher than that of the middle group and the lowest group, respectively; the final solid residue content of the optimal group was the highest, up to 14.51%, indicating that its thermal stability was the best; the molecular forces in the optimal group showed the trend of hydrophobic force>hydrogen bond>electrostatic force; the results of Fourier transform infrared spectroscopy and molecular force confirmed each other, which showed that the hydrogen bond of the optimal group was stronger than that of the middle group and the lowest group. In summary, the optimized composite fluid gel has great potential in food fluid gel applications, which has excellent rheological properties and a more stable internal structure.
-
Keywords:
- fluid gel /
- gel characteristics /
- process optimization /
- stability /
- molecular force
-
流体凝胶(fluid gel)是指一类具有流动性、分散在非凝胶连续相(通常是水)中的胶凝颗粒悬浮液[1],具有微观结构可调控的特点,目前已作为药物或益生菌的缓释载体得到商业化应用,同时,其也作为理想的脂肪替代物,在低能量食品市场中应用潜力巨大[2]。常见的流体凝胶一般为多糖和蛋白的共混体系,向其中添加少量油脂可赋予体系更好的润滑感与稳定性。多糖-蛋白-油脂复合体系经不同程度的剪切力作用,其内部微结构发生重排,从而获得具有不同流变特性的流体凝胶[3]。
多糖、蛋白、油脂是制备流体凝胶的三大类基料组分。变性淀粉中的乙酰化二淀粉磷酸酯(acetylated distarch phosphate,ADSP)具有抗热、抗酸、抗老化等特点,与蛋白质等大分子复合时,可吸附在颗粒上形成一个厚的吸附层,且保持足够的构象自由避免聚集,从而改善体系结构和稳定性[4]。水解明胶(hydrolysate gelatin,HG)拥有蛋白水解物的多种功能特性(如抗氧化及抗菌活性等)[5]。Hu等[6]发现水解蛋白可阻止多糖链内分子结合和氢键的形成,可有效抑制淀粉多糖回生。Sunisa等[7]的研究表明水解明胶可减少蛋白质链之间的相互作用,增加网络体系的自由体积。大豆油(soybean oil,SO)为产量最大的植物油之一,在凝胶剂作用下可以发生结构化,有助于流体凝胶内部形成稳定的三维网络结构。目前,添加油脂的复合凝胶已作为脂肪替代物在奶酪方面成功应用,产品稳定性显著提高[8]。
流体凝胶自身流动性主要取决于静电和疏水相互作用,该作用可通过调节pH及离子强度来实现[9]。Lopez等[10]发现中性偏酸性条件下体系内电荷密度降低促进了链间结合,从而有利于凝胶的形成;碱性条件下,氢氧根离子对变性淀粉有增溶作用,因此体现为抑制作用。Wang等[11]发现钙离子可与多糖形成钙桥,促进凝胶的形成。此外,多糖-蛋白凝胶形成过程中常伴随静电相互作用,适当盐离子的加入能够屏蔽静电现象,以调整流体凝胶的流变特性。Basse等[12]发现离子浓度为0.5 mol/L时,对凝胶形成和凝胶弹性的促进作用远大于0.8 mol/L。因此,流体凝胶具有丰富的机械性能及流变学行为,可广泛应用于医药、食品、化工等领域。
本文采用魔芋胶、乙酰化二淀粉磷酸酯、水解明胶和大豆油为主要基料,以不同pH、氯化钙浓度等条件制备复合流体凝胶(KGM-ADSP-HG-SO,KAHS),基于正交试验确定其最优制备工艺,并对三种不同水平的复合流体凝胶自身特性进行比较分析,旨在为研发新型流体凝胶的制备工艺提供方法借鉴。
1. 材料及方法
1.1 材料与仪器
魔芋胶(食品级) 湖北强森魔芋科技有限公司;乙酰化二淀粉磷酸酯(食品级) 临沂市富兴变性淀粉厂;大豆油(食品级) 益海嘉里食品营销有限公司;无水柠檬酸钠(食品级) 北京鼎国昌盛生物科技有限责任公司;骨胶原蛋白肽(食品级,2000 Da) 包头东宝生物技术股份有限公司;分子蒸馏单甘酯 陕西晨明生物科技有限公司;磷酸、十二烷基硫酸钠(SDS)、尿素 均为分析纯,北京鼎国昌盛生物科技有限责任公司。
FA25高速分散机 上海Fluko流体机械制备有限公司;UV762紫外可见分光光度计 上海仪电分析仪器有限公司;CR21GⅡ高速离心机 日本日立公司;TA-XT Plus质构仪 英国Stable Micro System公司;Ultra Scan色差仪 美国Hunter Lab公司;MCR302流变仪 奥地利安东帕有限公司;TG209F1热重仪 德国NETISCH;Q100型差示扫描量热仪 美国TA公司;PHS-3 C pH计 上海精密科学仪器有限公司;DHG-9070型电热恒温鼓风干燥箱 上海一恒科技有限公司。
1.2 实验方法
1.2.1 多元复合流体凝胶的制备
分子蒸馏单甘酯与大豆油按质量比1:20混合,高温加热至完全溶解作为油相备用;称取各物料并将其分散于一定浓度的氯化钙溶液中,使用0.1 mol/L盐酸溶液调节pH,搅拌形成均匀水相。将油水两相混合低速剪切3 min,后于90 ℃水浴加热;待完全水合后于2000 r/min剪切20 min,静置冷却至室温后重复剪切20 min,最终制得样品,并于4 ℃冷藏保存。
1.2.2 单因素实验
采用单因素实验设计,依次考察不同基料添加量对制备流体凝胶的影响,保持pH6.5,氯化钙浓度0.2 mol/L:保持魔芋胶4%,水解明胶6%,大豆油8%不变,考察不同乙酰化二淀粉磷酸酯添加量(0、2%、4%、6%、8%、10%)对凝胶特性的影响;保持魔芋胶4%,乙酰化二淀粉磷酸酯6%,大豆油8%不变,考察不同水解明胶添加量(0、2%、4%、6%、8%、10%)对凝胶特性的影响;保持魔芋胶4%,乙酰化二淀粉磷酸酯6%,水解明胶6%不变,考察不同大豆油添加量(0、2%、4%、6%、8%、10%)对凝胶特性的影响;
保持魔芋胶4%,乙酰化二淀粉磷酸酯6%,水解明胶6%,大豆油8%,氯化钙浓度为0.2 mol/L不变,考察不同pH(3、4、5、6、7、8、9、10)对凝胶特性的影响;保持魔芋胶4%,乙酰化二淀粉磷酸酯6%,水解明胶6%,大豆油8%,pH6.5不变,考察不同氯化钙浓度(0、0.1、0.2、0.3、0.4、0.5、0.6、0.7 mol/L)对凝胶特性的影响。
1.2.3 正交试验
根据单因素实验结果,按表1设计进行正交试验。为消除不同指标间的量纲差异,同时对凝胶强度、质量损失率与感官评定指标进行离差标准化(min-max normalization,MMN),将三者标准化后的数值分别乘以各自权重系数(0.4、0.3和0.3,由学校和企业专家共同开会讨论决定)后进行加和,其和值即为综合评分(Y)。
表 1 正交试验因素与水平Table 1. Factors and level tables of orthogonal experiment水平 因素 A 乙酰化二淀粉磷酸酯添加量(%) B 水解明胶添加量(%) C 大豆油添加量(%) D pH E 氯化钙浓度(mol/L) 1 5.0 5.0 7.0 5.5 0.30 2 5.5 5.5 7.5 6 0.35 3 6.0 6.0 8.0 6.5 0.40 4 6.5 6.5 8.5 7.0 0.45 1.2.4 质构特性及凝胶强度测定
将上述流体凝胶置于直径6 cm、高度10 cm的圆柱型孔板中,样品表面均匀且高度保持一致,置于室温下平衡30 min后,使用质构仪测定。质构测定采用TPA模式,参数设定如下:探头P/0.5,测定前、中、后速度均为1 mm/s,触发力5 g,应变50%,进行两次压缩,两次压缩时间间隔为4 s,每个样品重复测定6次;凝胶强度测定选择相同模式,参数设定如下:探头:P/5S,测试前中后速度均为1 mm/s,触发力5 g,应变50%,每个样品平行测定15次。
1.2.5 感官评定
评定方法依据于学萍等[13]、潘治利等[14]的感官评定法并稍作修改,邀请15位感官评定经验丰富食品专业人员(7男8女,平均年龄23岁)对流体凝胶的挤出流畅性、组织状态、色泽和涂抹性进行综合评分,感官评分标准见表2。
表 2 感官评分标准Table 2. Sensory evaluation criteria评价指标 评价标准 评分范围(分) 能流畅连续挤出 15~20 挤出流畅性(20分) 挤出流畅性良好 8~14 挤出困难 1~7 组织状态均匀,光滑,无气泡,无塌陷 27~40 组织状态(40分) 组织状态较均匀,稍光滑,稍有气泡,稍塌陷 14~26 组织状态不均匀,粗糙,气泡很多,塌陷厉害 1~13 颜色均匀一致,表面光泽度好 15~20 色泽(20分) 颜色基本均匀一致,表面光泽度较好 8~14 颜色不均匀,表面光泽度差 1~7 易涂抹,涂层连贯均匀 15~20 涂抹性(20分) 较易涂抹,涂层稍不均匀或者不连贯 8~14 难涂抹,涂层不均匀,不连贯 1~7 1.2.6 动态流变特性
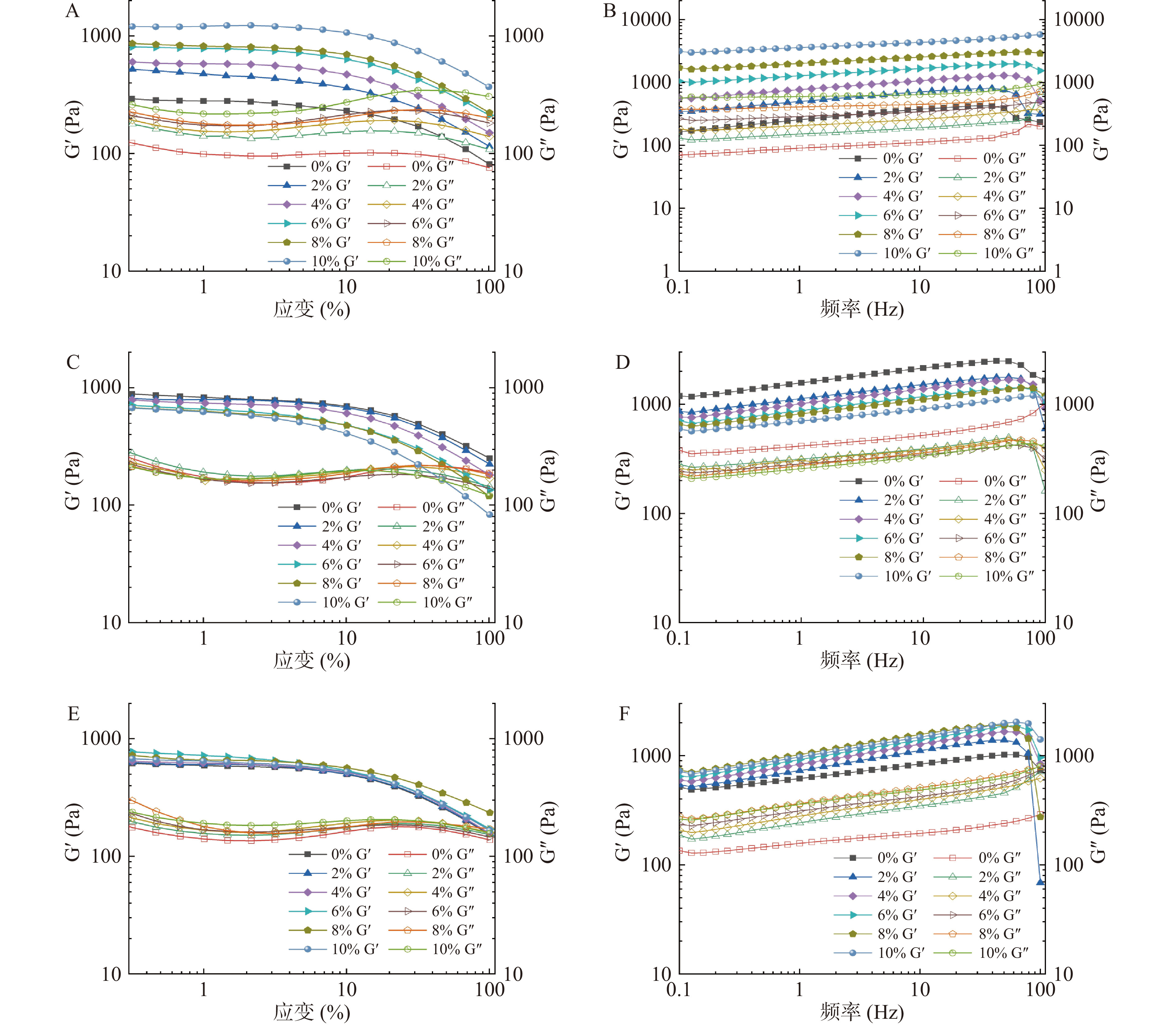
采用MCR302流变仪测量流体凝胶的剪切流变性。药匙取20 mL流体凝胶均匀分散于平板上。缓慢降低上板(直径75 mm),两个平行板间隙闭合至1 mm。动态振荡模式实验:先进行应变扫描,应变扫描范围为0.1%~100%,固定频率1 Hz,以此确定线性粘弹区。25 ℃恒温下,确定1%应变后,进行动态频率扫描,频率扫描范围为0.1~100 Hz,测定储能模量(G')和损耗模量(G'')频率函数曲线。
1.2.7 质量损失率
称取5 g流体凝胶置于离心管中,于4 ℃、10000 r/min条件下离心20 min后,弃去上清液,分别对空离心管、离心前后带凝胶的离心管进行称重,分别记其质量为m1、m2和m3,凝胶质量损失率按式(1)进行计算:
质量损失率(%)=(m2−m3)/(m2−m1)×100 (1) 1.2.8 差示扫描量热分析
称取20 mg流体凝胶,放入40 μL氧化铝坩埚底部后密封,在流速为20 mL/min氮气保护下,将坩埚置于差示扫描量热仪中进行测定,测定温度范围为−50~60 ℃,升温速率为10 ℃/min,进行差示扫描量热法(differential scanning calorimeter,DSC)分析。水分形态分析[15]:可冻结水(Wf)含量通过样品在0 ℃附近的焓变(ΔH)计算得出,见公式(2)。非冻结水含量(Wnf)由总水分含量(EWC)减去可冻结水含量(Wf)可得,见公式(3),EWC按GB 5009.3-2016《食品中水分的测定》的方法进行测定。
Wf(%)=ΔHΔH0×100 (2) Wnf(%)=EWC−Wf (3) 其中:ΔH为复合凝胶DSC测得吸热峰面积计算的单位质量焓变(J/g);ΔH0为纯水的单位质量焓变(J/g),334.00 J/g。
1.2.9 热稳定性
称取20 mg样品于热重分析仪中,采用高纯氮气为载气,气体流量为30 mL/min,以10 ℃/min的速度将样品从25 ℃加热至600 ℃,对样品进行热重(thermogravimetry,TG)和热重微分(thermogravimetric differential,DTG)测定。
1.2.10 分子相互作用力
参考金杨等[16]的方法,并加以调整。将试验样品分别与纯水、0.6 mol/L氯化钠、0.6 mol/L脲、0.6 mol/L十二烷基硫酸钠溶液以1:10(wt%)混合搅拌。室温静置平衡30 min后采用1.2.4质构测定方法,测定实验组与对照组(纯水组)之间凝胶硬度变化,通过凝胶硬度变化值表征静电作用力、氢键、疏水相互作用大小。
1.2.11 傅里叶变换红外光谱
采用傅里叶变换红外光谱(fourier transform infrared spectrometer,FTIR)对复合凝胶进行分析。分别称取2 mg冷冻干燥后的凝胶粉末与200 mg溴化钾混匀、研磨、压片进行全波段扫描。FTIR测试条件:波长4000~400 cm−1,分辨率4 cm−1,温度25 ℃,扫描32次。
1.3 数据处理
运用SPSS 22.0软件和Origin 2018软件进行数据处理和作图,采用多重比较法中的最小显著差法(least significant difference, LSD),且P<0.05判定为显著性差异。
2. 结果与分析
2.1 单因素实验结果
2.1.1 基料组分对多元复合流体凝胶质构特性的影响
物料不同添加量对复合流体凝胶质构特性的影响如表3所示。随着乙酰化二淀粉磷酸酯的增加,凝胶硬度、粘着性总体呈上升趋势,添加量最大与添加量为0%时相比,凝胶硬度和粘度增幅分别为194.70%、225.81%。由于乙酰化二淀粉磷酸酯具有磷酸酯基团,增大了淀粉膨润率使之充分吸收水分,支撑凝胶体系,从而提高凝胶的质构特性[17]。相比添加量为0时,当水解明胶添加量为10%时,凝胶硬度、粘着性、内聚性及胶着性均呈下降趋势,凝胶硬度和粘着性降幅较大,分别达25.84%、42.90%,这可能与水解明胶肽链的静电相互作用和空间排斥力不平衡有关。随着水解明胶添加量的增加,凝胶弹性变化不显著(P>0.05),表明水解明胶添加量对凝胶弹性指标影响较小。上述结果与王煜桐等[18]和Mirzapour等[19]报道的凝胶质构特性随水解明胶添加量变化的趋势一致。粘着性随大豆油的增加显著下降(P<0.05),凝胶硬度则先上升后下降。当大豆油含量为8%时,凝胶硬度达到最大值(93.49 g)。可能是大豆油与凝胶基质相互作用充当活性填充剂,减少了凝胶基质内颗粒的间隙,提高了蛋白凝胶的硬度,但高浓度大豆油(10%)会导致硬度下降,可能是由于油滴的聚集行为破坏了凝胶网络结构。Jiao等[20]研究发现添加3%鱼油,鱼糜凝胶硬度有所增加,而进一步添加则会导致凝胶硬度降低。
表 3 添加不同基料组分制得多元复合流体凝胶质构特性Table 3. Determination of the texture index of multiple composite fluid gel prepared by adding different base components基料组分 添加量(%) 硬度(g) 粘着性(g·s) 弹性 内聚性 胶着性(g) 乙酰化二淀粉磷酸酯 0 37.57±3.52e −135.54±11.79a 0.91±0.03a 0.63±0.06a 23.51±1.78d 2 39.00±1.89e −140.33±18.99a 0.89±0.02abc 0.59±0.01ab 22.89±1.09d 4 57.55±3.32d −177.35±5.94b 0.86±0.03c 0.53±0.03bc 30.78±2.41c 6 78.50±3.37c −238.36±22.43c 0.86±0.05bc 0.54±0.04bc 42.63±3.60b 8 86.23±5.61b −294.35±27.85d 0.91±0.03ab 0.50±0.02cd 43.18±4.16b 10 110.72±2.01a −441.60±12.13e 0.92±0.02a 0.46±0.04d 51.92±4.04a 水解明胶 0 65.41±2.81a −320.58±34.6d 0.91±0.04a 0.48±0.03a 48.48±2.61a 2 62.51±0.31b −250.02±6.42c 0.90±0.01a 0.45±0.02ab 42.35±1.60b 4 57.51±1.11c −220.92±14.39bc 0.90±0.02a 0.44±0.01bc 40.01±0.73b 6 56.51±1.51c −199.91±8.65ab 0.91±0.03a 0.40±0.00cd 39.75±2.34b 8 51.91±1.81d −189.35±14.69ab 0.91±0.01a 0.39±0.03d 39.59±3.36b 10 48.51±1.21e −183.05±6.58a 0.90±0.01a 0.39±0.01d 39.33±0.22b 大豆油 0 75.38±4.10b −336.58±22.97d 0.75±0.02b 0.59±0.03a 44.29±1.79a 2 87.95±6.84a −325.65±9.81cd 0.71±0.02b 0.52±0.02bc 45.51±3.30a 4 92.62±4.42a −318.1±9.96bcd 0.72±0.05b 0.51±0.01bc 46.01±1.76a 6 92.76±4.02a −296.14±26.07bc 0.72±0.05b 0.51±0.01bc 46.35±0.84a 8 93.49±1.36a −285.54±5.74b 0.71±0.02b 0.49±0.05c 42.43±3.98a 10 80.97±1.78b −246.98±22.13a 0.83±0.01a 0.55±0.03ab 43.91±2.67a 注:同列同一处理不同小写字母表示差异显著(P<0.05);表4同。 2.1.2 基料组分对多元复合流体凝胶感官评价的影响
由表4可知,随着乙酰化二淀粉磷酸酯添加量的增加,流体凝胶的挤出流畅性、组织状态和涂抹性得分均先上升后下降,可能是凝胶分子间交联作用增大,促使凝胶硬度增强(表3)。当乙酰化二淀粉磷酸酯添加量大于8%时,复合凝胶挤出困难且表面粗糙,添加量为6%时,流体凝胶组织状态最好,总体感官得分最高。增加水解明胶添加量,凝胶挤出流畅性和涂抹性增强,组织状态及感官总分先增加后减小。综合考虑,为避免水解明胶对复合凝胶破坏性过大并同时改善复合凝胶流动性,应控制其添加量约为6%。不同大豆油添加量对流体凝胶的挤出流畅性、色泽和涂抹性差异并不显著,但对组织状态评分呈显著差异。组织状态评分先上升后下降,可能是由于适量的大豆油可增强凝胶强度,但过量的大豆油会从网络孔隙中流出,导致凝胶表面析油严重,塌陷程度变大,组织状态均一性变差[21]。表3中凝胶性能变化趋势也印证了上述观点。因此,大豆油添加量为8%左右,可有效缓解大豆油析油和组织状态均一性较差的现象,且具有总体最佳感官体验。
表 4 添加不同基料组分制得多元复合流体凝胶感官评价结果(分)Table 4. Sensory evaluation results of multiple composite fluid gel prepared by adding different base components (score)基料组分 添加量(%) 挤出流畅性 组织状态 色泽 涂抹性 感官总分 乙酰化二淀粉磷酸酯 0 17.5±1.0a 20.7±2.3c 16.3±1.2a 16.8±0.8c 71.3±2.1b 2 17.3±1.4a 20.7±2.0c 17.2±1.5a 18.2±0.8a 73.3±2.4b 4 18.0±0.6a 25.7±2.0b 17.2±0.8a 17.8±1.2a 78.7±1.6b 6 12.0±0.8b 27.5±0.8a 17.5±1.0a 17.3±1.0bc 79.7±1.5a 8 12.0±2.5b 14.3±1.4d 17.3±0.8b 13.2±1.9d 56.8±4.3c 10 9.7±2.2c 9.3±2.3e 17.2±0.8c 10.8±1.9e 47.0±3.7d 水解明胶 0 17.3±1.0b 21.2±1.7c 17.3±0.5a 16.8±0.8c 72.7±3.0c 2 17.3±0.5b 22.8±1.6b 17.7±0.5a 17.3±0.8c 75.2±1.5b 4 17.7±0.5ab 24.2±0.8a 17.8±1.2a 17.7±0.8bc 77.3±1.9b 6 18.0±0.6ab 24.0±1.1a 18.0±0.6a 18.2±0.8ab 78.2±1.9a 8 18.0±0.9ab 20.2±1.5cd 17.5±1.0a 18.5±0.5ab 74.2±1.9bc 10 18.5±0.8a 18.8±0.8d 18.2±0.8a 18.7±0.5a 74.2±1.2bc 大豆油 0 18.2±0.8a 18.2±0.8c 18.2±1.2a 18.3±0.5ab 72.8±1.8c 2 18.3±0.5a 19.3±1.0c 18.5±0.8a 18.5±0.5a 74.7±2.0b 4 18.2±0.8a 21.0±1.7b 18.5±0.5a 18.0±0.6ab 75.7±2.3ab 6 18.3±0.5a 21.7±0.bab 18.2±0.8a 18.2±0.8ab 76.3±1.0ab 8 18.5±0.5a 22.8±0.8a 18.2±0.8a 17.8±0.4ab 77.3±1.0a 10 17.7±1.0a 19.3±1.0c 18.3±0.5a 17.7±0.5b 73.0±1.3c 2.1.3 基料组分对多元复合流体凝胶流变特性的影响
多元复合流体凝胶动态流变特性须在线性粘弹区内进行测定。线性粘弹区是指复合模量G'不随应变而变化的区域[22]。由应变扫描曲线(图1)可知,选取应变为1%能确保所施加的应变不会破坏凝胶网络结构。动态流变学考察了不同样品的变化趋势,储能模量G'表示形变可逆且贮存能量的弹性性质,损耗模量G''表示形变不可逆而能量损耗的粘性性质[23]。分析图1可知,各组样品G'均大于G'',即体系以弹性性能为主。G'和G''均随频率增加而增大,且呈频率依赖性,说明体系具有典型的弱凝胶特性。G'和G''随乙酰化二淀粉磷酸酯添加量增加而增大,当添加量为10%时,G'和G''达到最大值(图1B)。说明该流体凝胶在乙酰化二淀粉磷酸酯作用下,分子间网络交联程度显著增加。这与修琳等[24]研究的多糖蛋白凝胶储能与损耗模量均随淀粉增加而增加的趋势相似。随水解明胶的添加,G'和G''均呈下降趋势。水解明胶添加量为10%时,流动性最强,G'和G''则降至最低值(图1D)。张炜杰等[25]发现水解明胶的小分子链起润滑作用,减少了分子间流动时的摩擦力,宏观表现为粘度降低,流动性增加。由图1F可知,大豆油添加量为8%时,G'和G''最大;当添加量大于8%,G'和G''开始下降,可能是复合凝胶大分子间相分离,形成不同相的浓度差,导致体系结构和性质出现差异。这与凝胶质构特性变化(表3)相呼应。Wu等[26]发现复合凝胶中添加的油脂可作为活性填充剂能与基质作用,能增强储能模量及凝胶强度。三种基料物质随着频率增加,储能模量与损耗模量始终呈缓慢增加的变化趋势,说明该凝胶体系稳定性较强。由图1B可知,在频率接近100 Hz时,乙酰化二淀粉磷酸酯组的模量变化最小,说明该淀粉对体系稳定性可能有一定的促进作用。
2.1.4 pH和氯化钙浓度对多元复合流体凝胶稳定性的影响
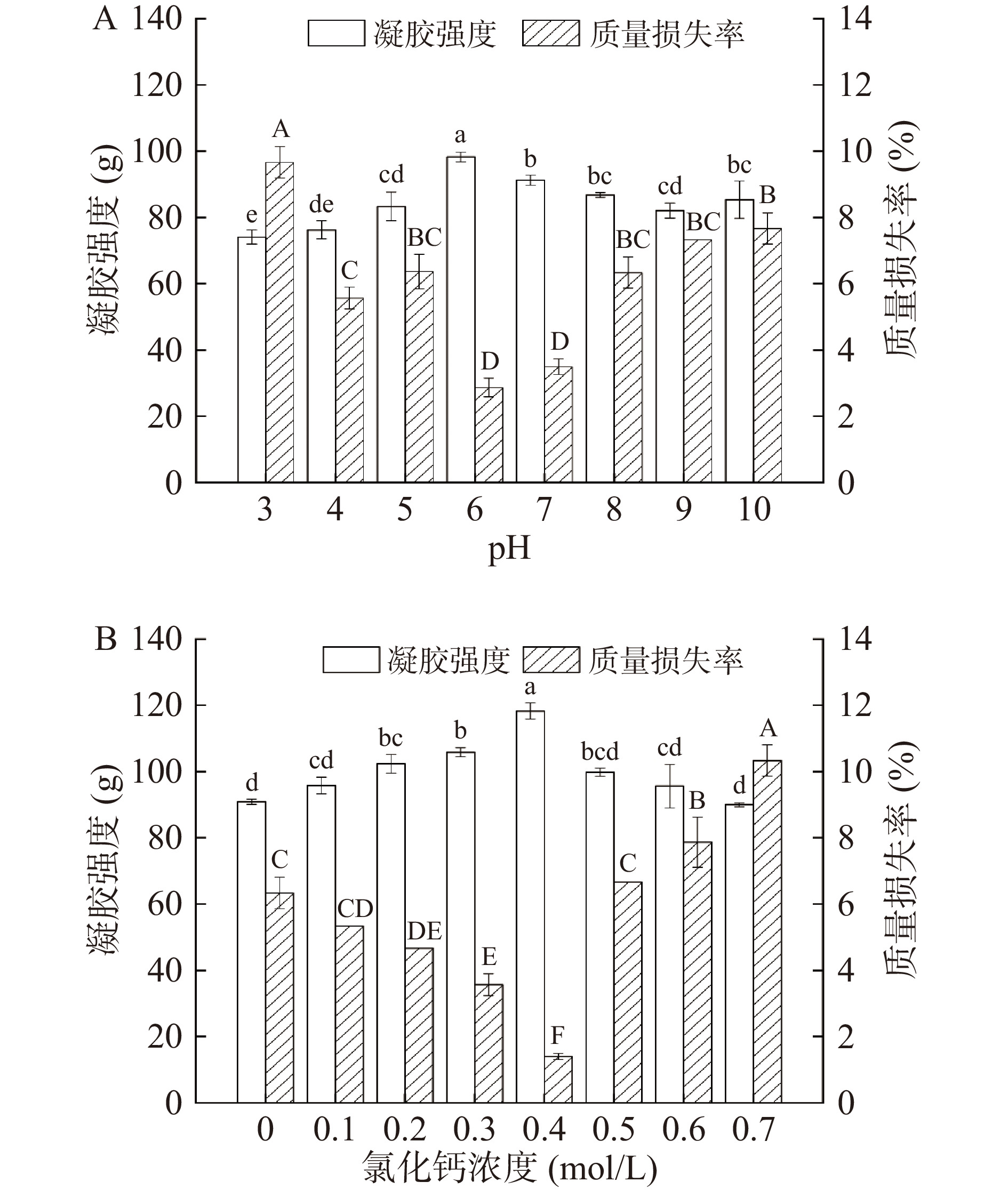
质量损失率和凝胶强度能反映凝胶稳定性及凝胶性能,可直观地评价凝胶品质和质量。凝胶质量损失率与其结构有关,凝胶强度越强结构越稳定,质量损失率越低。由图2A可知,凝胶强度随pH升高先增加后减小,当pH为6时,凝胶强度最大(98.23 g)。由于pH靠近水解凝胶等电点时,分子间静电斥力降低且氢键生成,促使凝胶网络的形成和成长;反之,当pH远离其等电点时,分子链展开,分子相互靠近较困难,凝胶强度减弱[27]。观察图2A可知,复合流体凝胶质量损失率与凝胶强度呈负相关,凝胶强度越强,质量损失率越小。质量损失主要是由于析油现象,大豆油填充于凝胶网络结构中,当凝胶三维网络结构越紧密,凝胶强度越强,对大豆油的束缚力也越强,从而降低了复合流体凝胶的质量损失率。
图2B显示,不同氯化钙浓度影响下,复合流体凝胶的凝胶强度和质量损失率均有一定的差异。随着盐浓度的增加,凝胶强度呈先上升后下降的趋势,质量损失率变化趋势与之相反。当氯化钙浓度为0.4 mol/L时,凝胶强度升至最大值(118.31 g),质量损失率降至最小值(1.4%)。Cao等[28]发现由于钙离子对多糖-蛋白凝胶中的带电物质能产生静电屏蔽效应。因此,适当添加钙离子能显著提高凝胶强度(P<0.05),但过量盐离子将中和体系的负电荷,使凝胶之间斥力减弱,形成的网络节点数也随之减少,凝胶强度降低[29]。适量钙离子可使多糖凝胶体系孔径变小、孔径数量增加,提高体系持水性和凝胶强度,但过量钙离子则导致凝胶相分离[30]。
2.2 正交试验确定最优配方工艺
根据单因素实验结果,选择乙酰化二淀粉磷酸酯、水解明胶及大豆油添加量,氯化钙浓度及pH作为考察对象,采用5因素4水平方法,以综合评分(Y)为指标,按照L16(45)正交表进行正交试验,正交试验结果见表5,方差分析结果见表6。由表5可知,复合凝胶为KAHS-5组和KAHS-14组综合评分较高,分别为0.76和0.83。经离差标准化分析可知,各因素对粘弹性流体凝胶影响程度依次为B>A>E>C>D,且D为不显著因素,理论最佳配方为A4B2C3D3E2,即乙酰化二淀粉磷酸酯6.5%、水解明胶5.5%、大豆油8%、pH6.5、氯化钙0.35 mol/L。经外部重复试验验证三次后,其综合评分高达0.98±0.01,故可将其定义为“最优组”,记为KAHS-S-H。观察表5,基于综合评分高低,从中进一步筛选出综合评分最低的KAHS-4组(为0.01),以及综合评分居中的KAHS-7组(为0.57),将其分别定义为“最低组”和“中间组”,依次记为KAHS-4-L和KAHS-7-M。本研究后续对三组不同配方复合凝胶(最低组、中间组和最优组)的热稳定性进行比较分析,并初步探讨其内在机制。
表 5 正交试验结果Table 5. The results of orthogonal test试验号 因素 指标 A 乙酰化二淀粉磷酸酯 B 水解明胶 C 大豆油 D pH E 氯化钙 凝胶强度(g) 质量损失率(%) 感官总分
(分)综合评分(Y) 1 1 1 1 1 1 73.82 5.55 77.5 0.48 2 1 2 2 2 2 80.89 4.89 79.3 0.75 3 1 3 3 3 3 71.99 5.33 74.8 0.36 4 1 4 4 4 4 62.33 6.44 73.0 0.01 5 2 1 2 3 4 81.80 4.00 77.3 0.76 6 2 2 1 4 3 77.49 4.00 76.2 0.64 7 2 3 4 1 2 79.70 5.55 77.3 0.57 8 2 4 3 2 1 78.90 5.11 76.3 0.55 9 3 1 3 4 2 76.41 4.00 74.5 0.55 10 3 2 4 3 1 75.00 5.78 77.5 0.48 11 3 3 1 2 4 69.68 4.44 75.3 0.44 12 3 4 2 1 3 65.47 5.78 72.8 0.12 13 4 1 4 2 3 71.89 5.11 76.8 0.47 14 4 2 3 1 4 88.47 4.89 78.7 0.83 15 4 3 2 4 1 78.43 4.22 76.0 0.62 16 4 4 1 3 2 79.36 3.56 75.5 0.68 K1 1.60 2.26 2.25 2.00 2.14 K2 2.52 2.70 2.25 2.21 2.54 K3 1.58 1.98 2.29 2.28 1.59 K4 2.61 1.37 1.52 1.82 2.04 R 1.03 1.33 0.76 0.46 0.96 最优水平 A4 B2 C3 D3 E2 最优配方(S) A4B2C3D3E2 表 6 基于综合评分的正交试验方差分析Table 6. The variance analysis of orthogonal test based on comprehensive score方差来源 III型平方和 自由度 均方 F 显著性 校正模型 280.001a 15 18.667 11.030 0.000* 截距 341436.658 1 341436.658 201742.511 0.000* A 93.958 3 31.319 18.505 0.000* B 78.046 3 26.015 15.371 0.000* C 54.815 3 18.272 10.796 0.000* D 8.127 3 2.709 1.601 0.209 E 45.056 3 15.019 8.874 0.000* 误差 54.158 32 1.692 总计 341770.818 48 校正的总计 334.159 47 注:*表示显著(P<0.05);a:R2=0.838(调整R2=0.762)。 2.3 不同综合评分等级的多元复合流体凝胶热稳定性分析
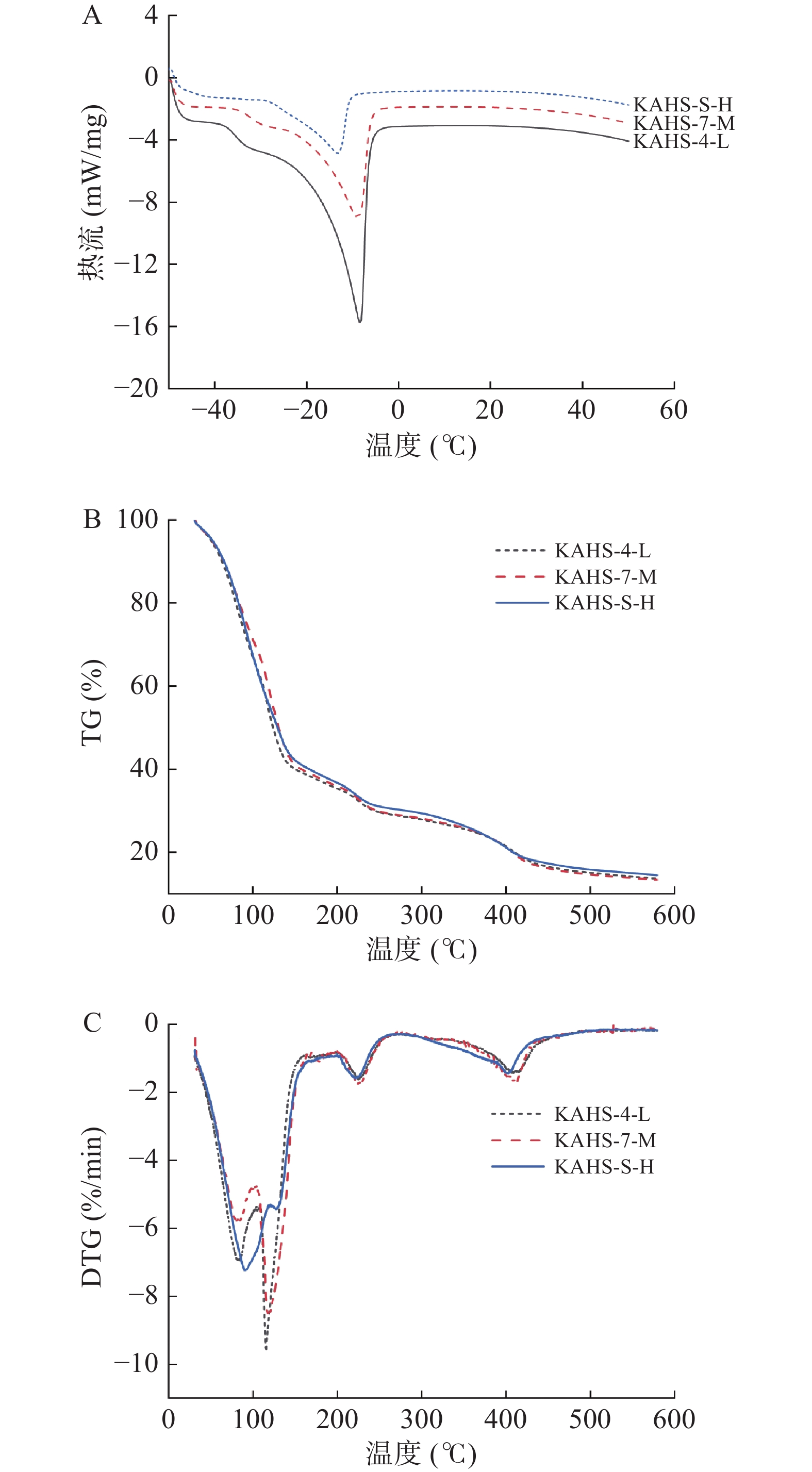
图3A为复合流体凝胶差示扫描量热图,各组凝胶样品的谱峰反映其热焓变化。复合凝胶最低组(KAHS-4-L)、中间组(KAHS-7-M)和最优组(KAHS-S-H)谱图相似,−20~0 ℃之间均有一个较宽的吸收峰,表明复合凝胶中可冻结水在升温过程中发生了焓变,故可知体系中可冻结水和非冻结水含量。通过分析焓变可知,三组复合凝胶中最优组可冻结水含量最低(8.22%),非冻结水含量最高(50.33%)。
图3B结果显示,最低组、中间组、最优组三组热解最终固体残留物分别为13.41%、13.66%、14.51%,且最优组热重曲线总体位于其他两组上方,表明最优组凝胶热稳定性最好。DTG曲线显示(图3C),三组样品均出现3个明显的失重峰,表明其热分解主要分为三阶段:第一阶段(30~200 ℃),此阶段凝胶体系开始失去自由水和中间水,由于最优组的自由水与亲水基团紧密结合,形成的非冻结结合水使结构更稳定,故第一阶段最优组失重速率小于其他两组;第二个阶段(200~300 ℃),主要失去非冻结水,体系中亲水基团的结合水脱除及凝胶侧链上的氢键受热断裂分解;最后阶段(300~600 ℃),主要是凝胶体系大分子链的分解。凝胶体系热稳定性与分子作用力有关,根据图3结果推测,最优组凝胶分子作用力可能显著强于另外两组。
由表7可知,三组复合凝胶的熔融峰起点均小于0 ℃。根据“三态水”模型可知,当复合凝胶达到溶胀平衡时,可冻结中间水含量较低,其熔融峰被自由水掩盖、叠加[31]。同时,复合凝胶吸收峰温度有所偏移,且吸收峰温度最优组<中间组<最低组,即最优组冰点温度最低。结合焓变结果可知,最优组中水分子有生成更多氢键的可能,以形成类似“笼形”的“聚集体”,增强凝胶网络与水分子之间作用力,将更多水分子禁锢在复合凝胶网络中,使不易流动的水流动性变差、冰点下降,吸热峰的峰值向低温区移动。综上分析,最优组持水能力比最低组和中间组强。
表 7 不同综合评分等级的多元复合流体凝胶水分分布状态Table 7. Moisture distribution of multiple composite fluid gels with different comprehensive scoring grades指标 KAHS-4-L KAHS-7-M KAHS-S-H θ0(℃) −16.54±0.28a −18.15±0.06b −24.27±0.57c θt(℃) −8.63±0.17a −9.00±0.28a −13.25±0.11b ∆θ(℃) 7.91±0.33c 9.15±0.29b 11.02±0.58a ∆H0(J/g) 334.00 334.00 334.00 ∆H(J/g) 46.13±1.43a 36.88±0.62b 27.46±0.85c EWC(%) 58.45±2.23a 58.55±1.56a 58.55±2.5a Wf(%) 13.81±0.43a 11.04±0.27b 8.22±0.24c Wnf(%) 44.64±2.27b 47.51±1.58ab 50.33±2.51a 注:θ0为开始熔化的温度;θt为峰值温度;同行不同字母表示各组间差异显著(P<0.05)。 2.4 不同综合评分等级的多元复合流体凝胶分子间作用力分析
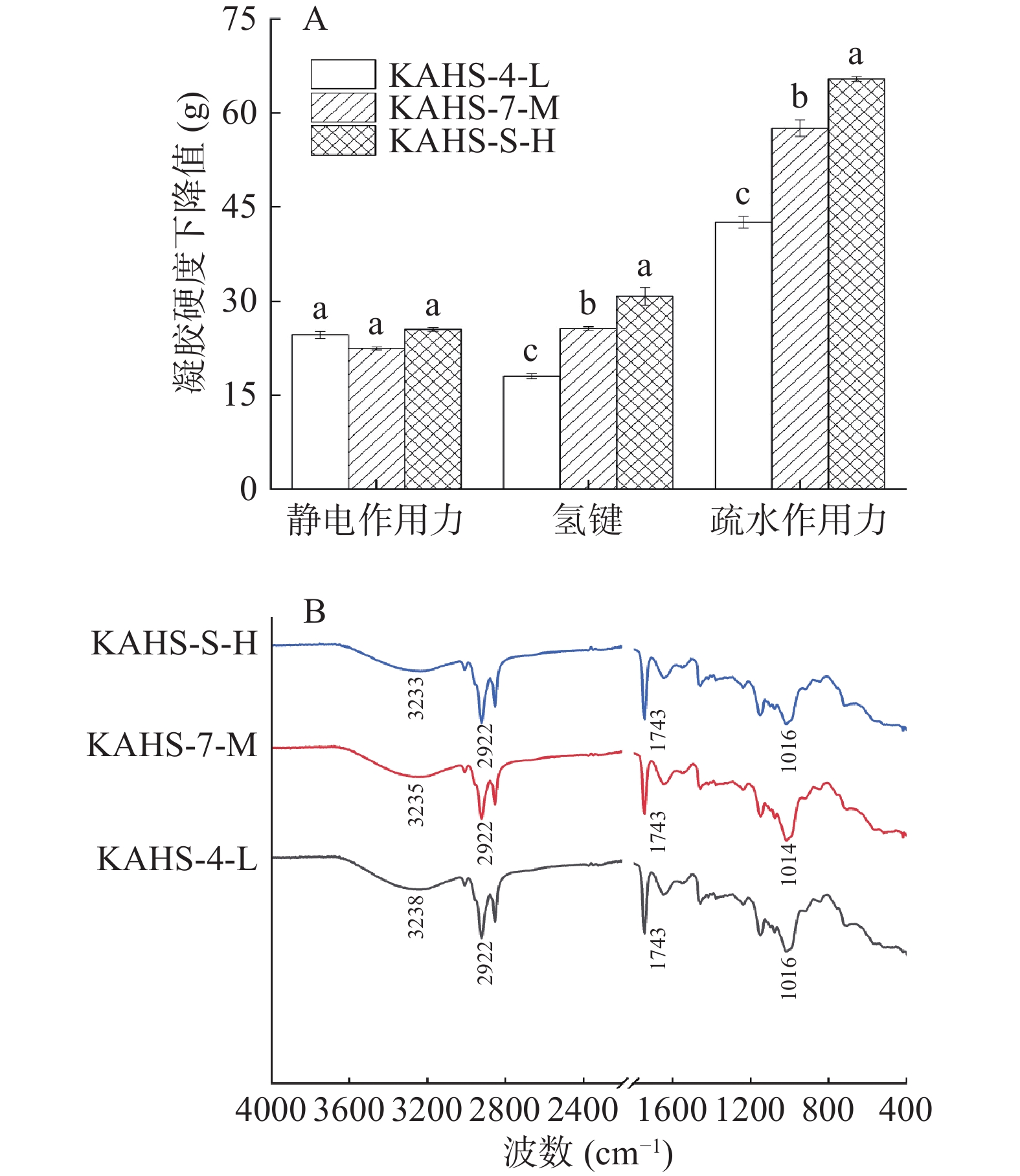
复合流体凝胶需要一定分子间作用力来维持凝胶内部结构,作用力类型可能为静电作用、氢键、疏水作用等。本研究通过添加对凝胶有不同破坏作用的试剂来确定分子间作用力类型。氯化钠主要削弱静电作用,但对氢键作用无影响;脲则破坏氢键作用,且不会削弱静电作用;SDS则破坏疏水作用。通过以上破坏力间接判断分子间作用力大小[32]。图4A反映不同试剂作用后,与对照组相比凝胶硬度的变化值来表征相互作用力大小。各组凝胶分子间作用力主要是疏水作用力,氢键和静电作用力相对较弱,说明疏水作用力是凝胶体系中维持网络结构的主要因素,且最优组疏水作用力最高。一方面,可能因为复合凝胶暴露大量疏水性氨基酸残基,显著增强了分子间疏水相互作用;另一方面,疏水作用力是维持魔芋胶三维结构的主要作用力,90 ℃热诱导后,疏水作用力提高[33]。李晓飞等[34]研究发现的温度降低会使凝胶体系疏水作用力减弱,侧面印证了此观点。同时,最优组氢键比其他两组强。综上所述,最优组分子作用力相对最强,与上述结论中最优组热稳定性较强的现象相呼应。
FTIR是用于研究分子结构的常用手段,根据光谱图中振动谱带的强度、宽度和出峰位置等信息,可从分子水平分析高聚物的构象变化。观察图4B可知,最低组、中间组、最优组三组凝胶样品具有相似的红外光谱,表明三组复合凝胶均没有生成新官能团,最低组、中间组、最优组分别在3238.48、3235.55、3233.12 cm−1附近出现较大峰,且凝胶发生红移,分子间O-H氢键伸缩振动,与分子内和分子间的氢键作用有关。O-H氢键伸缩振动向低波数方向移动,分子间键能增强[35],表明最优组氢键大于其他两组,这与分子作用力结论相互印证。
3. 结论
本研究创制了一种新型多元流体凝胶体系。随着乙酰化二淀粉磷酸酯和大豆油添加量的升高,该流体凝胶的硬度、储能模量及损耗模量呈递增趋势,表明加入乙酰化二淀粉磷酸酯和大豆油能够增强复合凝胶相互作用力和网络结构。然而,随着水解明胶添加量的升高,上述指标呈相反趋势。通过正交试验确定了复合凝胶的最优工艺配方:6.5%乙酰化二淀粉磷酸酯、5.5%水解明胶和8%大豆油,保持pH及氯化钙浓度分别为6.5、0.35 mol/L。热重及差示扫描量热结果显示,最优组复合凝胶的热稳定及持水性最佳,凝胶分子间作用力主要为疏水作用力,其次为氢键和静电作用力,且最优组复合凝胶的氢键和疏水作用力最强。傅里叶红外光谱结果同样表明,最优组复合凝胶的氢键键能高于最低组和中间组。为制备新型多元流体凝胶提供了基础研究。
-
表 1 正交试验因素与水平
Table 1 Factors and level tables of orthogonal experiment
水平 因素 A 乙酰化二淀粉磷酸酯添加量(%) B 水解明胶添加量(%) C 大豆油添加量(%) D pH E 氯化钙浓度(mol/L) 1 5.0 5.0 7.0 5.5 0.30 2 5.5 5.5 7.5 6 0.35 3 6.0 6.0 8.0 6.5 0.40 4 6.5 6.5 8.5 7.0 0.45 表 2 感官评分标准
Table 2 Sensory evaluation criteria
评价指标 评价标准 评分范围(分) 能流畅连续挤出 15~20 挤出流畅性(20分) 挤出流畅性良好 8~14 挤出困难 1~7 组织状态均匀,光滑,无气泡,无塌陷 27~40 组织状态(40分) 组织状态较均匀,稍光滑,稍有气泡,稍塌陷 14~26 组织状态不均匀,粗糙,气泡很多,塌陷厉害 1~13 颜色均匀一致,表面光泽度好 15~20 色泽(20分) 颜色基本均匀一致,表面光泽度较好 8~14 颜色不均匀,表面光泽度差 1~7 易涂抹,涂层连贯均匀 15~20 涂抹性(20分) 较易涂抹,涂层稍不均匀或者不连贯 8~14 难涂抹,涂层不均匀,不连贯 1~7 表 3 添加不同基料组分制得多元复合流体凝胶质构特性
Table 3 Determination of the texture index of multiple composite fluid gel prepared by adding different base components
基料组分 添加量(%) 硬度(g) 粘着性(g·s) 弹性 内聚性 胶着性(g) 乙酰化二淀粉磷酸酯 0 37.57±3.52e −135.54±11.79a 0.91±0.03a 0.63±0.06a 23.51±1.78d 2 39.00±1.89e −140.33±18.99a 0.89±0.02abc 0.59±0.01ab 22.89±1.09d 4 57.55±3.32d −177.35±5.94b 0.86±0.03c 0.53±0.03bc 30.78±2.41c 6 78.50±3.37c −238.36±22.43c 0.86±0.05bc 0.54±0.04bc 42.63±3.60b 8 86.23±5.61b −294.35±27.85d 0.91±0.03ab 0.50±0.02cd 43.18±4.16b 10 110.72±2.01a −441.60±12.13e 0.92±0.02a 0.46±0.04d 51.92±4.04a 水解明胶 0 65.41±2.81a −320.58±34.6d 0.91±0.04a 0.48±0.03a 48.48±2.61a 2 62.51±0.31b −250.02±6.42c 0.90±0.01a 0.45±0.02ab 42.35±1.60b 4 57.51±1.11c −220.92±14.39bc 0.90±0.02a 0.44±0.01bc 40.01±0.73b 6 56.51±1.51c −199.91±8.65ab 0.91±0.03a 0.40±0.00cd 39.75±2.34b 8 51.91±1.81d −189.35±14.69ab 0.91±0.01a 0.39±0.03d 39.59±3.36b 10 48.51±1.21e −183.05±6.58a 0.90±0.01a 0.39±0.01d 39.33±0.22b 大豆油 0 75.38±4.10b −336.58±22.97d 0.75±0.02b 0.59±0.03a 44.29±1.79a 2 87.95±6.84a −325.65±9.81cd 0.71±0.02b 0.52±0.02bc 45.51±3.30a 4 92.62±4.42a −318.1±9.96bcd 0.72±0.05b 0.51±0.01bc 46.01±1.76a 6 92.76±4.02a −296.14±26.07bc 0.72±0.05b 0.51±0.01bc 46.35±0.84a 8 93.49±1.36a −285.54±5.74b 0.71±0.02b 0.49±0.05c 42.43±3.98a 10 80.97±1.78b −246.98±22.13a 0.83±0.01a 0.55±0.03ab 43.91±2.67a 注:同列同一处理不同小写字母表示差异显著(P<0.05);表4同。 表 4 添加不同基料组分制得多元复合流体凝胶感官评价结果(分)
Table 4 Sensory evaluation results of multiple composite fluid gel prepared by adding different base components (score)
基料组分 添加量(%) 挤出流畅性 组织状态 色泽 涂抹性 感官总分 乙酰化二淀粉磷酸酯 0 17.5±1.0a 20.7±2.3c 16.3±1.2a 16.8±0.8c 71.3±2.1b 2 17.3±1.4a 20.7±2.0c 17.2±1.5a 18.2±0.8a 73.3±2.4b 4 18.0±0.6a 25.7±2.0b 17.2±0.8a 17.8±1.2a 78.7±1.6b 6 12.0±0.8b 27.5±0.8a 17.5±1.0a 17.3±1.0bc 79.7±1.5a 8 12.0±2.5b 14.3±1.4d 17.3±0.8b 13.2±1.9d 56.8±4.3c 10 9.7±2.2c 9.3±2.3e 17.2±0.8c 10.8±1.9e 47.0±3.7d 水解明胶 0 17.3±1.0b 21.2±1.7c 17.3±0.5a 16.8±0.8c 72.7±3.0c 2 17.3±0.5b 22.8±1.6b 17.7±0.5a 17.3±0.8c 75.2±1.5b 4 17.7±0.5ab 24.2±0.8a 17.8±1.2a 17.7±0.8bc 77.3±1.9b 6 18.0±0.6ab 24.0±1.1a 18.0±0.6a 18.2±0.8ab 78.2±1.9a 8 18.0±0.9ab 20.2±1.5cd 17.5±1.0a 18.5±0.5ab 74.2±1.9bc 10 18.5±0.8a 18.8±0.8d 18.2±0.8a 18.7±0.5a 74.2±1.2bc 大豆油 0 18.2±0.8a 18.2±0.8c 18.2±1.2a 18.3±0.5ab 72.8±1.8c 2 18.3±0.5a 19.3±1.0c 18.5±0.8a 18.5±0.5a 74.7±2.0b 4 18.2±0.8a 21.0±1.7b 18.5±0.5a 18.0±0.6ab 75.7±2.3ab 6 18.3±0.5a 21.7±0.bab 18.2±0.8a 18.2±0.8ab 76.3±1.0ab 8 18.5±0.5a 22.8±0.8a 18.2±0.8a 17.8±0.4ab 77.3±1.0a 10 17.7±1.0a 19.3±1.0c 18.3±0.5a 17.7±0.5b 73.0±1.3c 表 5 正交试验结果
Table 5 The results of orthogonal test
试验号 因素 指标 A 乙酰化二淀粉磷酸酯 B 水解明胶 C 大豆油 D pH E 氯化钙 凝胶强度(g) 质量损失率(%) 感官总分
(分)综合评分(Y) 1 1 1 1 1 1 73.82 5.55 77.5 0.48 2 1 2 2 2 2 80.89 4.89 79.3 0.75 3 1 3 3 3 3 71.99 5.33 74.8 0.36 4 1 4 4 4 4 62.33 6.44 73.0 0.01 5 2 1 2 3 4 81.80 4.00 77.3 0.76 6 2 2 1 4 3 77.49 4.00 76.2 0.64 7 2 3 4 1 2 79.70 5.55 77.3 0.57 8 2 4 3 2 1 78.90 5.11 76.3 0.55 9 3 1 3 4 2 76.41 4.00 74.5 0.55 10 3 2 4 3 1 75.00 5.78 77.5 0.48 11 3 3 1 2 4 69.68 4.44 75.3 0.44 12 3 4 2 1 3 65.47 5.78 72.8 0.12 13 4 1 4 2 3 71.89 5.11 76.8 0.47 14 4 2 3 1 4 88.47 4.89 78.7 0.83 15 4 3 2 4 1 78.43 4.22 76.0 0.62 16 4 4 1 3 2 79.36 3.56 75.5 0.68 K1 1.60 2.26 2.25 2.00 2.14 K2 2.52 2.70 2.25 2.21 2.54 K3 1.58 1.98 2.29 2.28 1.59 K4 2.61 1.37 1.52 1.82 2.04 R 1.03 1.33 0.76 0.46 0.96 最优水平 A4 B2 C3 D3 E2 最优配方(S) A4B2C3D3E2 表 6 基于综合评分的正交试验方差分析
Table 6 The variance analysis of orthogonal test based on comprehensive score
方差来源 III型平方和 自由度 均方 F 显著性 校正模型 280.001a 15 18.667 11.030 0.000* 截距 341436.658 1 341436.658 201742.511 0.000* A 93.958 3 31.319 18.505 0.000* B 78.046 3 26.015 15.371 0.000* C 54.815 3 18.272 10.796 0.000* D 8.127 3 2.709 1.601 0.209 E 45.056 3 15.019 8.874 0.000* 误差 54.158 32 1.692 总计 341770.818 48 校正的总计 334.159 47 注:*表示显著(P<0.05);a:R2=0.838(调整R2=0.762)。 表 7 不同综合评分等级的多元复合流体凝胶水分分布状态
Table 7 Moisture distribution of multiple composite fluid gels with different comprehensive scoring grades
指标 KAHS-4-L KAHS-7-M KAHS-S-H θ0(℃) −16.54±0.28a −18.15±0.06b −24.27±0.57c θt(℃) −8.63±0.17a −9.00±0.28a −13.25±0.11b ∆θ(℃) 7.91±0.33c 9.15±0.29b 11.02±0.58a ∆H0(J/g) 334.00 334.00 334.00 ∆H(J/g) 46.13±1.43a 36.88±0.62b 27.46±0.85c EWC(%) 58.45±2.23a 58.55±1.56a 58.55±2.5a Wf(%) 13.81±0.43a 11.04±0.27b 8.22±0.24c Wnf(%) 44.64±2.27b 47.51±1.58ab 50.33±2.51a 注:θ0为开始熔化的温度;θt为峰值温度;同行不同字母表示各组间差异显著(P<0.05)。 -
[1] FERNANDEZ F I, DOUAIRE M, NORTON I T. Rheology and tribological properties of Ca-alginate fluid gels produced by diffusion-controlled method[J]. Food Hydrocolloids,2013,32(1):115−122. doi: 10.1016/j.foodhyd.2012.12.009
[2] SMANIOTTO F, ZAFEIRI I, PROSAPIO V, et al. Understanding the encapsulation and release of small molecular weight model actives from alginate fluid gels[J]. Food Structure,2021,27(6):100179.
[3] GHEBREMEDHIN M, SEIFFERT S, VILGIS T A. Physics of agarose fluid gels: Rheological properties and microstructure[J]. Current Research in Food Science,2021,4(2):436−448.
[4] YU B, ZHENG L, CUI B, et al. The effects of acetylated distarch phosphate from tapioca starch on rheological properties and microstructure of acid-induced casein gel[J]. International Journal of Biological Macromolecules,2020,159:1132−1139. doi: 10.1016/j.ijbiomac.2020.05.049
[5] CAO W, SHI L, HAO G, et al. Effect of molecular weight on the emulsion properties of microfluidized gelatin hydrolysates[J]. Food Hydrocolloids,2021,111:106267. doi: 10.1016/j.foodhyd.2020.106267
[6] HU Y, HE C, ZHANG M, et al. Inhibition from whey protein hydrolysate on the retrogradation of gelatinized rice starch[J]. Food Hydrocolloids,2020,108:105840. doi: 10.1016/j.foodhyd.2020.105840
[7] NUANMANO S, PRODPRAN T, BENJAKUL S. Potential use of gelatin hydrolysate as plasticizer in fish myofibrillar protein film[J]. Food Hydrocolloids,2015,47:61−68. doi: 10.1016/j.foodhyd.2015.01.005
[8] TARTE R, PAULUS J S, ACEVEDO N C, et al. High-oleic and conventional soybean oil oleogels structured with rice bran wax as alternatives to pork fat in mechanically separated chicken-based bologna sausage[J]. LWT,2020,131:109659. doi: 10.1016/j.lwt.2020.109659
[9] 朱科学, 赵书凡, 朱红英, 等. 苦丁茶冬青多糖流变学特性研究[J]. 食品工业科技,2017,38(22):61−65. [ZHU K X, ZHAO S F, ZHU H Y, et al. Rheological properties of polysaccharide isolated from llex kudingcha C. J. Tseng[J]. Science and Technology of Food Industry,2017,38(22):61−65. [10] LOPEZ G, RICHTERING W. Oscillatory rheology of carboxymethyl cellulose gels: Influence of concentration and pH[J]. Carbohydrate Polymers,2021,267:118117. doi: 10.1016/j.carbpol.2021.118117
[11] WANG W, JIANG L, REN Y, et al. Gelling mechanism and interactions of polysaccharides from mesonablumes: Role of urea and calcium ions[J]. Carbohydrate Polymers,2019,212:270−276. doi: 10.1016/j.carbpol.2019.02.059
[12] BASSE B, BOSC V, SAITER J M, et al. Combined effects of ionic strength and enzymatic pre-treatment in thermal gelation of peanut proteins extracts[J]. Food Research International,2020,137:109362. doi: 10.1016/j.foodres.2020.109362
[13] 于学萍, 童群义. 乙酰化二淀粉磷酸酯对豪猪肝酱稳定性的影响研究[J]. 食品工业科技,2016,37(1):288−292. [YU X P, TONG Q Y. Effect of acetylated distarch phosphate on stability of porcupine liver sauce[J]. Science and Technology of Food Industry,2016,37(1):288−292. [14] 潘治利, 张垚, 艾志录, 等. 马铃薯淀粉糊化和凝胶特性与马铃薯粉品质的关系[J]. 食品科学,2017,38(5):197−201. [PAN Z L, ZHANG Y, AI Z L, et al. Relationship between gelatinization and gelling properties of potato starch and potato noodles[J]. Food Science,2017,38(5):197−201. doi: 10.7506/spkx1002-6630-201705032 [15] YOSHIKO I, XU X, TADASHI T, et al. Enzymatically depolymerized alginate oligomers that cause cytotoxic cytokine production in human mononuclear cells[J]. Bioscience, Biotechnology, and Biochemistry,2003,67(2):258−263. doi: 10.1271/bbb.67.258
[16] 金杨, 刘丽莎, 张小飞, 等. 凝固温度对填充豆腐凝胶特性及分子间作用力的影响[J]. 食品科学,2020,41(23):49−55. [JIN Y, LIU L S, ZHANG X F, et al. Effect of coagulation temperature on gelling properties and chemical forces of Tofu coagulated with glucono-δ-lactone[J]. Food Science,2020,41(23):49−55. doi: 10.7506/spkx1002-6630-20200602-027 [17] 吴香, 李新福, 李聪, 等. 变性淀粉对肌原纤维蛋白凝胶特性的影响[J]. 食品科学,2020,41(2):22−28. [WU X, LI X F, LI C, et al. Effect of different modified starches on gel properties of myofibrillar protein[J]. Food Science,2020,41(2):22−28. doi: 10.7506/spkx1002-6630-20190227-209 [18] 王煜桐, 马洪梅. 水解明胶对明胶凝冻强度的影响探究[J]. 明胶科学与技术,2014,34(1):43−44. [WANG Y T, MA H M. Effect of hydrolyzed gelatin on gelatin gel strength[J]. The Science and Technology of Gelatin,2014,34(1):43−44. doi: 10.3969/j.issn.1004-9657.2014.01.007 [19] MIRZAPOUR-KOUHDASHT A, MOOSAVI-NASAB M, KRISHNASWAMK K, et al. Optimization of gelatin production from barred mackerel by-products: Characterization and hydrolysis using native and commercial proteases[J]. Food Hydrocolloids,2020,108:105970. doi: 10.1016/j.foodhyd.2020.105970
[20] JIAOX D, CAO H W, FAN D M, et al. Effects of fish oil incorporation on the gelling properties of silver carp surimi gel subjected to microwave heating combined with conduction heating treatment[J]. Food Hydrocolloids,2019,94:164−173. doi: 10.1016/j.foodhyd.2019.03.017
[21] WANG X, FENG Y, FENG T, et al. Modulation effect of glycerol on plasticization and water distribution of vacuum-dried calcium alginate gel beads encapsulating peppermint oil/β-cyclodextrin complex[J]. Food Bioscience,2021,41(7):100968.
[22] 周凤娟, 许时婴, 杨瑞金, 等. 可溶性丝素蛋白的流变性质和胶凝性质[J]. 食品科学,2007,28(12):58−62. [ZHOU F J, XU S Y, YANG R J, et al. Rheological properties and gel properties of soluble silk fibroin from sikl waste[J]. Food Science,2007,28(12):58−62. doi: 10.3321/j.issn:1002-6630.2007.12.009 [23] CHEN D, FANG F, FEDERICI E, et al. Rheology, microstructure and phase behavior of potato starch-protein fibril mixed gel[J]. Carbohydr Polym,2020,239:116247. doi: 10.1016/j.carbpol.2020.116247
[24] 修琳, 张淼, 许秀颖, 等. 绿豆蛋白对荞麦淀粉糊化和流变特性的影响[J]. 食品科学,2020,41(16):57−61. [XIU L, ZHANG M, XU X Y, et al. Effect of mung bean protein on gelatinization and rheological properties of buckwheat starch[J]. Food Science,2020,41(16):57−61. doi: 10.7506/spkx1002-6630-20190630-417 [25] 张炜杰, 丁丁. 水解明胶对明胶流变性能的影响[J]. 明胶科学与技术,2014,34(3):141−146. [ZHANG W J, DING D. Effect of hydrolyzed gelatin on rheological properties of gelatin[J]. The Science and Technology of Gelatin,2014,34(3):141−146. doi: 10.3969/j.issn.1004-9657.2014.03.006 [26] WU M, XIONG Y L, CHEN J. Rheology and microstructure of myofibrillar protein–plant lipid composite gels: Effect of emulsion droplet size and membrane type[J]. Journal of Food Engineering,2011,106(4):318−324. doi: 10.1016/j.jfoodeng.2011.05.022
[27] 满泽洲, 涂宗财, 王辉, 等. 加工条件对鱼鳞明胶凝胶性能和微观结构的影响[J]. 食品科学,2013,34(23):67−71. [MAN Z Z, TU Z C, WANG H, et al. Effects of processing conditions on gel performance and microstructure of fish scale gelatin[J]. Food Science,2013,34(23):67−71. [28] CAO L, LU W, GE J, et al. Modulation of oligoguluronate on the microstructure and properties of Ca-dependent soy protein gels[J]. Carbohydr Polym,2020,250:116920. doi: 10.1016/j.carbpol.2020.116920
[29] YANG J, SHEN M, WU T, et al. Role of salt ions and molecular weights on the formation of mesona chinensis polysaccharide-chitosan polyelectrolyte complex hydrogel[J]. Food Chemistry,2020,333:127493. doi: 10.1016/j.foodchem.2020.127493
[30] 王撼辰, 丑述睿, 崔慧军, 等. 钙离子添加量对苹果果胶-苹果多酚复配物体系流变、凝胶及质构特性的影响[J]. 食品科学,2019,40(24):46−52. [WANG H C, NIU S R, CUI H J, et al. Impacts of Calcium ion addition on rheological, gel and textural properties of apple pectin-apple polyphenol compound[J]. Food Science,2019,40(24):46−52. doi: 10.7506/spkx1002-6630-20190122-275 [31] BABA T, SAKAMOTO R, SHIBUKAWA M, et al. Solute retention and the states of water in polyethylene glycol and poly (vinyl alcohol) gels[J]. Journal of Chromatography A,2004,1040(1):45−51. doi: 10.1016/j.chroma.2004.03.065
[32] 任仙娥, 李春枝, 杨锋, 等. 涡流空化改善大豆分离蛋白溶解性的分子间作用机制[J]. 食品科学,2020,41(3):93−98. [REN X E, LI C Z, YANG F, et al. Intermolecular interaction mechanism for improvement in solubility of soy protein isolate by swirling cavitation[J]. Food Science,2020,41(3):93−98. doi: 10.7506/spkx1002-6630-20190306-078 [33] CHEN J, LI J, LI B. Identification of molecular driving forces involved in the gelation of konjac glucomannan: Effect of degree of deacetylation on hydrophobic association[J]. Carbohydrate Polymers,2011,86(2):865−871. doi: 10.1016/j.carbpol.2011.05.025
[34] 李晓飞, 李培源, 李安琪, 等. 黄原胶添加对碱法诱导魔芋胶凝胶特性及凝胶机制的影响[J]. 中国农业科学,2020,53(14):2941−2955. [LI X F, LI P Y, LI A Q, et al. Effects of xanthan addition on the gel properties and gel mechanism of alkaline-induced konjac glucomannan gels[J]. Scientia Agricultura Sinica,2020,53(14):2941−2955. doi: 10.3864/j.issn.0578-1752.2020.14.017 [35] JIANG W X, QI J R, LIAO J S, et al. Acid/ethanol induced pectin gelling and its application in emulsion gel[J]. Food Hydrocolloids,2021,118(1):106774.





 下载:
下载:



 下载:
下载:



