Effect of pH and Ionic Strength on the Pickering Emulsion Stability of Bagasse Nanocellulose
-
摘要: 以甘蔗渣为原料制备纤维素纳米晶(CNCs)用于稳定Pickering乳液,考察pH和离子强度对乳液稳定性的影响。结果表明,水解得到的CNCs,长度为120 nm左右,结晶度为70%。CNCs稳定的Pickering乳液粒径,随制备条件pH的升高而减小,在pH11的条件下,由于去质子化,使得乳液相对均一;此外,CNCs稳定的Pickering乳液粒径随着盐离子浓度的增加而增大,在100 mmol/L的浓度下,由于盐离子的静电屏蔽作用致使静电斥力减小,乳液破乳,分层更加明显。实验结果表明了甘蔗渣CNCs在作为固体粒子制备Pickering乳液中具有潜力,为甘蔗渣的利用提供新的思路。
-
关键词:
- 纳米纤维素 /
- Pickering 乳液 /
- 甘蔗渣 /
- pH /
- 离子强度
Abstract: Cellulose nanocrystalline (cncs) were prepared from bagasse as raw material to stabilize the Pickering emulsion to examine the effect of pH and ionic strength on emulsion stability. The results showed that the CNCs obtained by hydrolysis had a length of about 120 nm and a crystallinity of 70%. The particle size of the Pickering emulsion stabilized by CNCs decreased with the increase of the pH value of the preparation conditions. Under the condition of pH 11, the emulsion was relatively uniform due to deprotonation. In addition, the particle size of the Pickering emulsion stabilized by CNCs increased with the concentration of salt ions. At a concentration of 100 mmol/L, the electrostatic repulsion reduced due to the electrostatic shielding effect of salt ions, the emulsion broke, and the layering became more obvious. The experimental results showed that bagasse CNCs had potential in preparing Pickering emulsion as solid particles, and would provide new ideas for the utilization of bagasse.-
Keywords:
- nanocellulose /
- Pickering emulsion /
- bagasse /
- pH /
- ionic strength
-
甘蔗是我国南方主要的糖料作物,甘蔗渣是甘蔗榨糖之后的副产物,多被废弃,甘蔗渣中含有48%左右的纤维素,利用困难,造成资源的浪费和环境的负担[1-4]。
目前纤维素的利用以制备生物乙醇、饲料、纤维素板材、水凝胶为主[5],但研究发现通过纤维素水解得到的纤维素纳米晶(CNCs)是制备皮克林(Pickering)乳液的良好壁材[6]。Pickering乳液是指利用较小尺寸粒子(纳米级或微米级颗粒)本身特性就能起到稳定乳液的一种新兴载体技术[7]。一些食品级的固体粒子麦醇溶蛋白、淀粉纳米晶体、固体脂质颗粒以及纤维素纳米晶粒子等已被证明可用来稳定Pickering乳液[8]。其中,CNCs粒子由于其可再生性、可持续性、生物可降解性和生物相容性,以及低碳排放和低密度等优良特性,成为当下很多研究工作者感兴趣的对象[9]。现已经有很多科研人员利用农林废料制备出CNCs,比如山竹果皮[10]、白果壳[11]、银杏叶[12]等,这些CNCs能够稳定Pickering乳液,但是目前有关甘蔗渣制备CNCs用于稳定Pickering乳液的研究较少,而甘蔗渣CNCs具有较高的长径比、较好的力学强度、良好的稳定性以及其来源丰富等特点,有望成为Pickering乳液稳定剂[13]。
CNCs之所以能用于稳定Pickering乳液主要在于它良好的两亲性和独特的纳米尺寸,使其能不可逆地吸附于油-水界面,并将油相包裹形成致密的单层或多层界面结构,同时结合空间位阻以阻止相邻油滴间的碰撞和聚集来稳定乳液[14]。但是,很多因素(如pH、离子强度等)会影响粒子在油-水的吸附行为。本研究以甘蔗渣CNCs用来制备Pickering乳液,考察其pH和盐离子的稳定性,探讨其作为固体粒子在Pickering乳液中的应用潜力,这对甘蔗渣的综合利用具有一定的指导意义。
1. 材料和方法
1.1 材料与仪器
甘蔗渣 榨汁后得到渣,源于广东省丰收糖业发展有限公司;大豆油 食品级,金龙鱼益海嘉里食品营销有限公司;氢氧化钠、亚氯酸钠、乙酸、无水乙醇 均为分析纯,西陇科学股份有限公司。
ATS/AMF-5型微射流高压均质机 安托思纳米技术(苏州)有限公司;Zetasizer Pro纳米粒度及ZETA电位分析仪 英国马尔文仪器有限公司;T18高速剪切机 美国IKA公司;傅里叶红外光谱仪(FTIR) 美国Nicolet 公司;上海雷磁pH计 江苏迅迪仪器科技有限公司;X-ray 衍射仪(X-ray) 德国布鲁克 AXS 有限公司;JEM-1000透射电镜 日本电子株式会社;Leica DMI6000B倒置显微镜 德国Leica公司;Thermofisher/MARS哈克流变仪 美国TA公司。
1.2 甘蔗渣纤维素的提取
参考Hu等[15]的方法对甘蔗渣进行提纯处理。将潮湿的甘蔗渣在50℃烘箱中过夜,再将其粉碎,粉碎好的甘蔗渣和7.5%亚氯酸钠按照料液比1:12(w/v)的比例混合,用冰醋酸将pH调节到3.9,在75 ℃水浴条件下搅拌加热2h,随后用滤网过滤除去亚氯酸钠溶液,用去离子水洗涤至中性,置于50 ℃烘箱中干燥过夜,再与同体积10%氢氧化钠混合,在室温搅拌10 h,过滤收集滤渣,用去离子水洗涤至中性,95%乙醇洗脱,50 ℃烘干后粉碎。
1.3 甘蔗渣CNCs的制备
参考 Mandal等[16]的方法并稍作修改。用64%的硫酸水解甘蔗渣纤维素,料液比1:20,水解温度45 ℃,水解时间30 min,反应结束后添加10倍的去离子水来终止水解,稀释后的悬浮液静置24 h,弃去上清液,下层悬浮液用离心方式洗涤(12000 r/min,20 min),直至悬浮液pH3~4,后5000 r/min离心20 min,收集上清液,呈淡蓝色胶体状,该胶体即为甘蔗渣纤维素纳米晶(CNCs),在4 ℃透析,直到中性,并冻干后备用。
1.4 CNC结构性质表征
1.4.1 CNCs形态观察
参考李霞[17]的方法,用透射电镜(TEM)观察CNCs的形态,颗粒悬浮液稀释至0.1%,随后用移液枪吸取20 μL置于洁净的铜网上,静置2 min,并用滤纸移除多余的悬浮液,吸取2 μL醋酸双氧铀(1%)进行染色,2 min后用滤纸移除多余的染色剂。染色后的样品置于40 ℃下干燥后使用TEM进行观察,操作电压为200 kV。CNCs的长度和宽度均使用软件Nano Measurer 进行统计测定。
1.4.2 傅里叶红外(FTIR)和X射线衍射(X-ray)测量
FTIR 和 X-ray 用于观察CNCs 的化学基团和结晶度的差异。参考范柳萍等[11]的方法将干燥的 CNCs 颗粒粉末和溴化钾进行压片。FTIR 的扫描波长范围 4000~400 cm−1。X-ray 测量的 2θ 范围 3°到 50°(1°/min)。纤维素结晶度根据公式(1)计算:
结晶度=(I002−Iam)×100/I002 (1) 1.4.3 颗粒粒径和电位测定
按照Yang等[12]的方法,CNCs颗粒稀释100倍,粒径和Zeta电位是用Zetasizer Pro纳米粒度及ZETA电位分析仪测量。
1.5 Pickering乳液的制备和性质分析
1.5.1 Pickering乳液的制备
按照Kasiri等[18]的方法制备乳液。将0.4%(w/v)CNCs颗粒悬浮液的pH调为5、7、9、11(固定离子强度为0)或离子强度为10、50、75、100 mmol/L(固定pH为11),按油水比3:7的比例进行混合,制备乳液。用T18高速剪切机以12000 r/min的速率处理混合体系,2 min后得到粗乳液,随后用ATS/AMF-5型微射流高压均质机进一步处理粗乳液(30 MPa,2次)得到Pickering乳液。
1.5.2 乳液的粒径和电位
参考Thunnalin等[10]的方法,乳液的粒径尺寸和粒径分布采用Zetasizer Pro纳米粒度及ZETA电位分析仪进行测定。大豆油的折射率为 1.49。乳液样品用去离子水进行分散,每个样品测量 3次。
1.5.3 乳液微观结构
按照Yang等[12]的方法,用Leica DMI6000B倒置显微镜对乳液微观结构进行观察。乳液用去离子水稀释10倍,随后吸取 20 μL的样品,仔细滴在载玻片上,轻轻盖上盖玻片进行观察。
1.5.4 乳液流变特性
按照李霞[17]方法,用Thermofisher/MARS哈克流变仪评估了乳剂的流变特性,取新鲜乳剂(5 mL)放入盘中,等待设定温度达到25 °C。当剪切速率从0.01 s−1增加到20 s−1时,记录表观黏度。
1.5.5 乳析指数
参考Huang等[19]的方法,通过监测乳液层高度在30 d时的变化来评估乳析指数(CI)。CI使用以下公式计算:CI(%)= Hs/ Ht×100
其中Hs是乳液下层清液的高度(cm),Ht是乳液的总高度(cm)。
1.6 数据处理
各组实验重复3次,采用统计学分析软件SPSS18.0 进行差异显著性分析(P<0.05),Origin 9.1 软件进行作图处理。
2. 结果与分析
2.1 CNCs的结构表征
CNCs的形态和尺寸如图1所示,在64wt% H2SO4,料液比为1:15,时间为30 min,温度45 ℃的水解条件下,得到的CNCs颗粒长度在120 nm左右,直径约为10 nm,长径比为12,形态为短棒状。此外,图中的CNCs颗粒分布不均匀,有聚集现象,这是由于纤维素分子中分布着大量的活性羟基基团,使得其分子内和分子间易形成强大的范德华力和氢键作用力,致使CNCs颗粒之间易发生聚集,金克霞[20]在研究毛竹纤维素时有类似的发现。
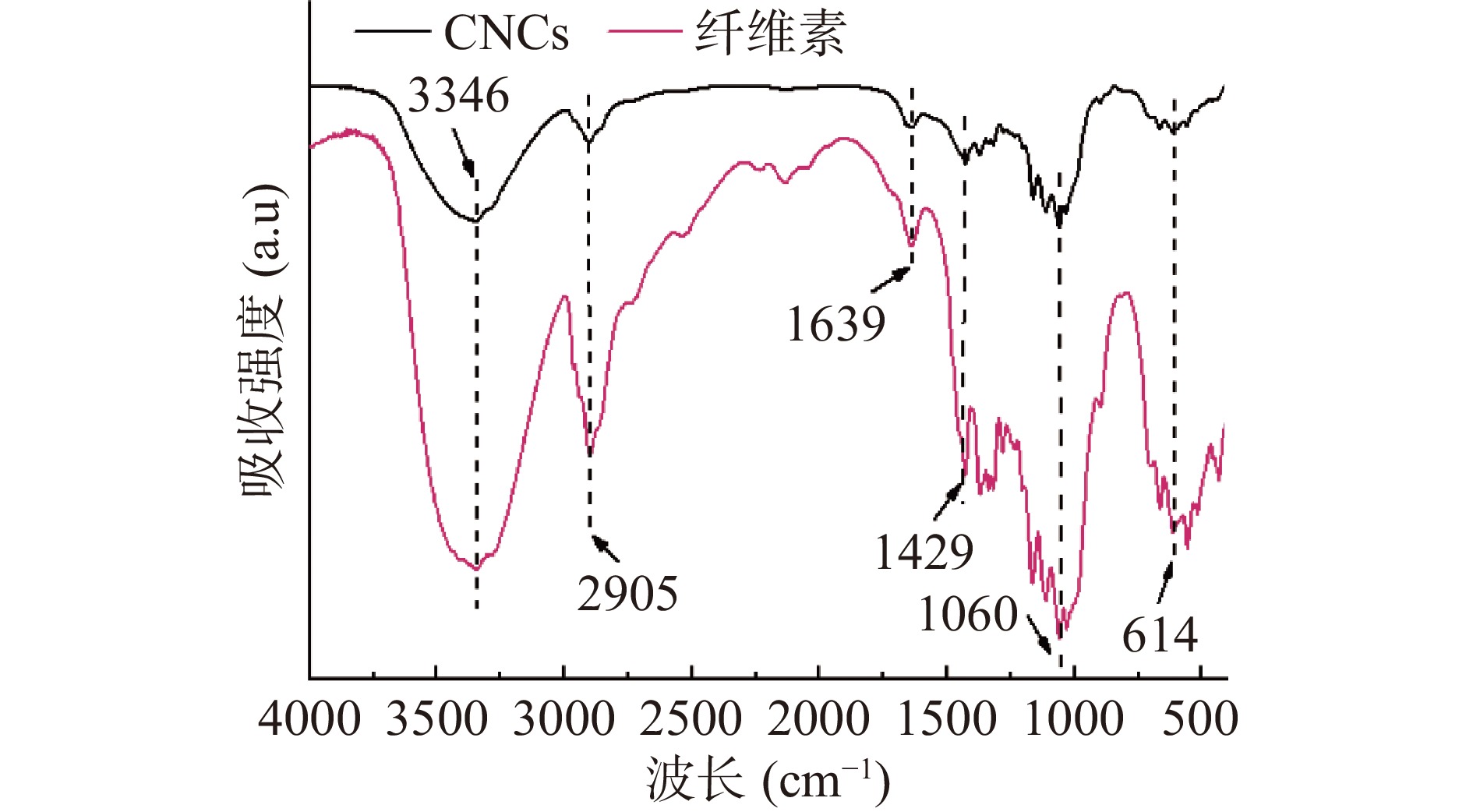
CNCs和纤维素的FTIR图谱如图2所示,在3346和1639 cm−1处有宽吸收峰,分别羟基的拉伸振动和弯曲振动,在2905 cm−1处的吸收峰是由于C-H的伸缩振动,在1639 cm−1处的吸收峰是由于C=C的伸缩,同时与吸附的水有关。1429 cm−1处的吸收峰可能是因为C-O-C的伸缩模式,在614 cm−1处向外弯曲的吸收峰,是纤维素的特征峰[21]。这个结果表明了通过酸水解制备得到CNCs仍保持天然纤维素的基本化学结构。
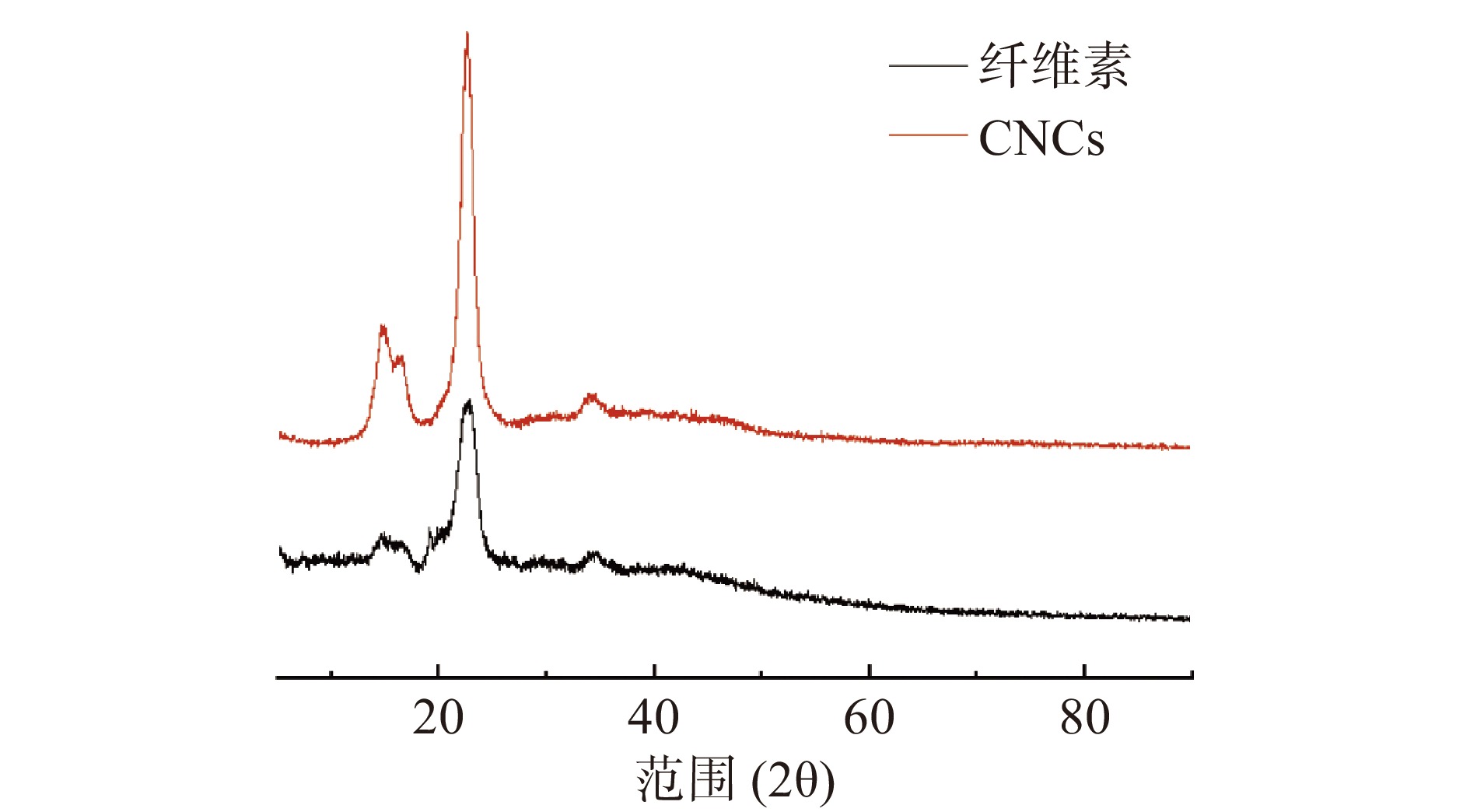
CNCs和纤维素的XRD图如图3所示,CNCs和纤维素的特征衍射峰的位置位于2θ=14.64°、16.43°、22.71°、34.2°,分别对应(
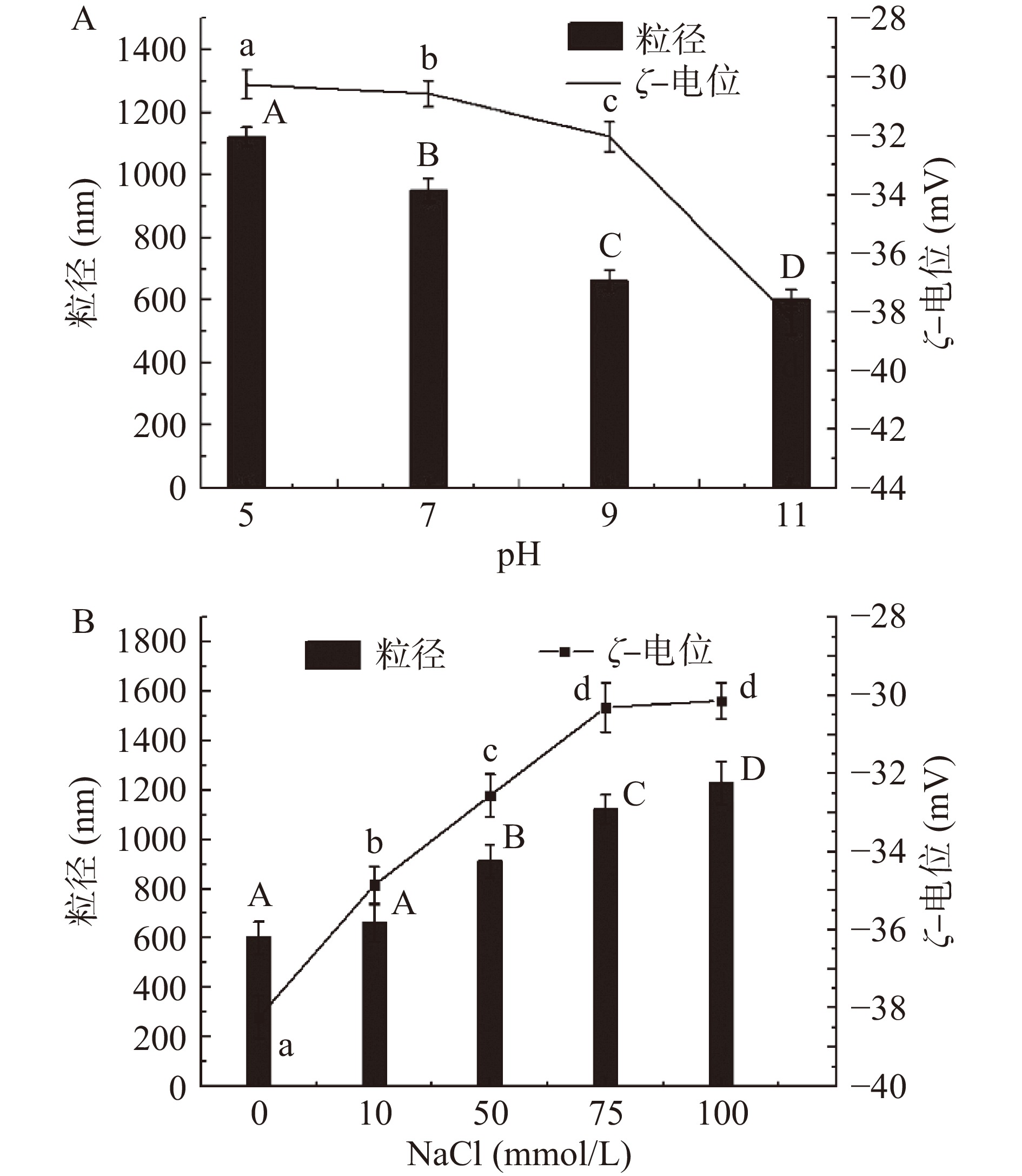
1¯10 )、(110)、(020)和(004)晶面。以上角度都属于Ⅰ型纤维素,并且是典型的纤维素晶体构型[22],但与纤维素相比,CNCs的衍射峰强度比纤维素高两倍左右,表明在水解过程中除去了非晶组分,这可能是在非晶区域中部分糖苷键断裂造成的,纤维素和CNCs的结晶度分别为32%和70%,CNCs结晶度高,因为酸水解破坏了较细的微晶区域和无序的相,使得微晶尺寸更加均一[23],Garvey等[23]在研究中也报道了类似的纤维素晶体构型。由甘蔗渣提取的CNCs颗粒在不同pH条件下的粒径和电位如图4A所示。CNCs颗粒粒径随着pH的增加而显著减小(P<0.05)。在pH7条件时,粒径为950 nm,与TEM结果差异较大,是因为CNCs颗粒非常容易聚集。随着pH从5增加到11,Zeta电位的绝对值增加了12 mV,这可能是因为用硫酸水解时,一部分残留的磺酸基团随机分布在CNCs颗粒表面,使其表面带负电荷而在分子间形成静电斥力,但由于pH的增加,在碱性条件下去质子化[24],使得Zeta电位的绝对值增加。
![]() 图 4 不同pH和离子强度条件下CNCs颗粒的粒径和电位注:A.在pH5~11条件下CNCs颗粒的粒径和电位;B.在离子强度10~100 mmol/L条件下CNCs颗粒的粒径和电位;同一指标相同类型的不同字母表示样本间显著差异(P<0.05);图5同。Figure 4. Particle size and zeta potential of the CNCs suspensions of different pH and different ionic strengths
图 4 不同pH和离子强度条件下CNCs颗粒的粒径和电位注:A.在pH5~11条件下CNCs颗粒的粒径和电位;B.在离子强度10~100 mmol/L条件下CNCs颗粒的粒径和电位;同一指标相同类型的不同字母表示样本间显著差异(P<0.05);图5同。Figure 4. Particle size and zeta potential of the CNCs suspensions of different pH and different ionic strengths由甘蔗渣提取的CNCs颗粒在不同离子强度条件下的粒径和电位如图4B所示。CNCs颗粒粒径随着离子强度的增加而显著增加(P<0.05),粒径从660 nm增加到1200 nm。与此同时,离子强度由0 mmol/L增加到100 mmol/L,Zeta电位的绝对值减少了8 mV,这可能是CNCs表面的负电荷与 Na+发生静电吸附作用,使得Zeta电位的绝对值降低,且静电斥力减小,促使纳米颗粒发生聚集。李霞[17]也在盐对油棕榈纳米纤维素颗粒悬浮液的影响中报道了,提高盐浓度会使得Zeta电位的绝对值降低。
2.2 CNCs稳定的Pickering乳液特性
2.2.1 粒径和电位分析
粒径和电位是乳液最重要的指标,是影响乳液稳定性的主要原因,并且不同大小的粒径和电位的乳液具有不同的应用价值。
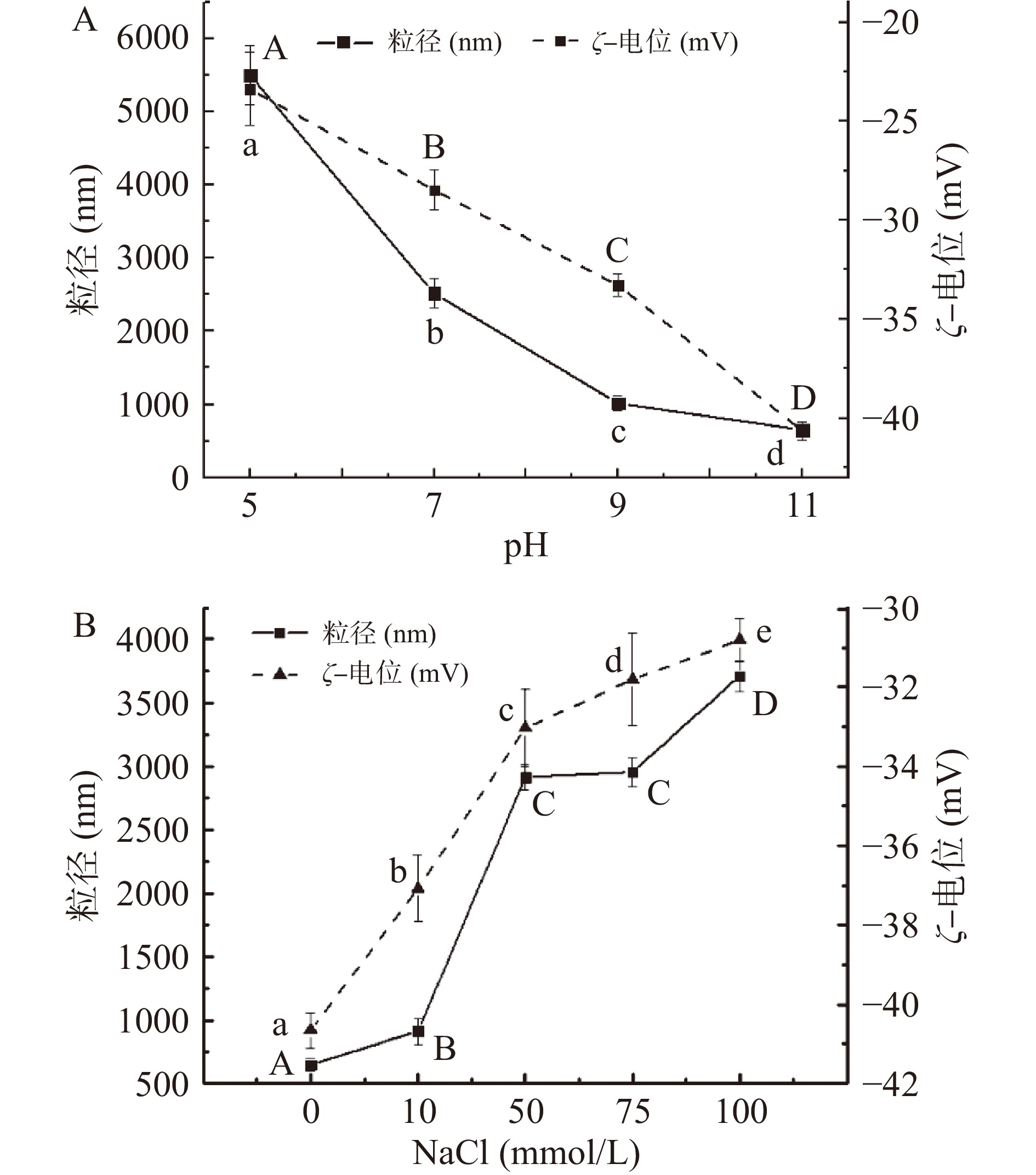
在不同的pH条件下,CNCs-Pickering乳液的粒径和电位的分布如图5A所示,乳液的粒径随着pH的增大而显著减小(P<0.05),从5507 nm减小到650 nm。Zeta电位的绝对值随着pH的增大而显著增大(P<0.05),从23.38 mV增加到40.65 mV,这与CNCs颗粒自身电位随pH的变化是一致的,可能是由于液滴表面吸附的CNCs在碱性条件下去质子化所致,Thunnalin等[10]在山竹果皮制备纤维素中也报道了在较高的pH 条件下,乳液Zeta电位的绝对值会增加。
在不同离子强度条件下,CNCs-Pickering乳液的粒径和电位的分布如图5B所示,乳液的粒径随着离子强度的增加而显著增大(P<0.05),从920 nm增加到3720 nm。Zeta电位的绝对值随着离子强度的增加而显著减小(P<0.05),减小了10 mV,这是因为NaCl对其的静电屏蔽作用,NaCl屏蔽了CNCs粒子的表面电荷,减弱了CNCs粒子与CNCs粒子之间和CNCs粒子与水之间的相互作用,促进了CNCs粒子与油的相互作用,使得粒径发生聚集而增大。何康慧[25]在用竹笋水不溶性膳食纤维制备乳液中也报道了离子强度增强会使得粒径增大,Zeta电位的绝对值会减小。
2.2.2 乳液形态观察
图6A是不同pH条件下的CNCs-Pickering乳液的微观结构。在pH5、pH7、pH9时,液滴的大小不一,并且可以观察到液滴间发生聚集形成一个大液滴,说明乳液在此条件下稳定性相对较差,但在pH11时,液滴相对较为均一,呈现小液滴状,这可能是在高pH时,液滴的净电荷量相对较多,因此液滴间的静电斥力较大,阻止了液滴融合变大[26],说明乳液粒径分布应较为均匀,而且稳定性相对较好。
图6B是不同离子强度条件下的CNCs-Pickering乳液的微观结构。在10 mmol/L时,乳液呈现小液滴状态,液滴间的空间位阻阻止了液滴聚集变大,但液滴的大小会随着离子强度的增加而逐渐变大,而此时静电屏蔽能力逐渐增强[27],静电斥力减弱,因此在100 mmol/L时,乳液液滴间发生了明显聚集,甚至破乳,出现了大油滴。
2.2.3 流变特性
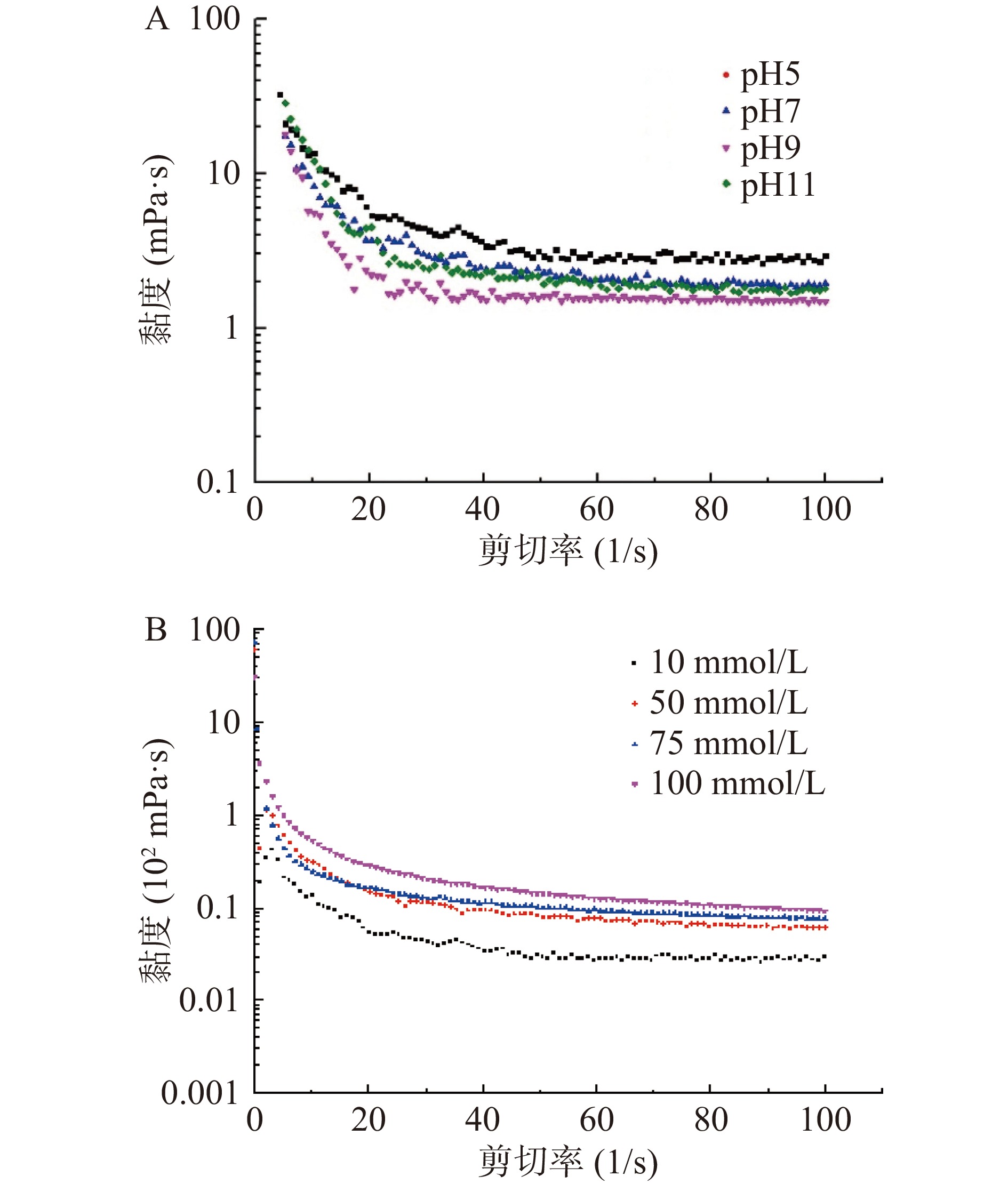
图7A是不同pH条件下的CNCs-Pickering乳液的表观黏度曲线图。乳液均表现出剪切变稀,这可能是因为在高速剪切下,乳液中的絮凝被慢慢破坏。当剪切速率<10 s−1,乳液在pH11时表观黏度最高,当剪切速率>10 s−1,乳液在pH5时黏度最大。这可能是因为在剪切速率较小时,高pH的乳液液滴间的静电斥力较大,但随着剪切速率的增大,液滴间的静电斥力被破坏,而在低pH时形成的大的液滴群会抵抗剪切速率,使得在剪切速率>10 s−1时,pH5的乳液的表观黏度最大[28]。但总体来看,在不同pH条件下的乳液黏度都较小,乳液流动性较强,相似的结果在银杏纳米纤维素中也有报道[7]。
图7B是不同离子强度条件下的CNCs-Pickering乳液的表观黏度曲线图。乳液的黏度随着盐浓度的增加而增加,在离子强度为100 mmol/L时,乳液黏度最高;在离子强度为10 mmol/L时,乳液黏度最低。Huang等[19]也报道,在一定范围内增加盐浓度可以提高Pickering乳液的表观黏度。这可能是因为NaCl屏蔽的静电屏蔽作用,使得CNCs粒子内的疏水相互作用增大,CNCs粒子在油水界面上的吸附量增加[29],Pickering乳液会产生弱絮凝现象,因此乳液黏度增加[30]。
2.2.4 乳液的乳析指数
CI值表示一段时间内,互不相溶的两种液体,其中一相以液滴状分散于另一相的能力。CNCs-Pickering乳液在不同pH的CI和外观形态如图8A和图8a所示。在pH5时,乳液分层速度最快,在第5 d达到顶峰;在pH11的条件下,乳液分层相对较慢,在第7 d时达到峰值,且CI值明显低于在pH5、pH7、pH9条件下的CI值。另外pH11时的乳液下清层比较浑浊,其他三个乳液下清层相对澄清透明。这可能是因为在较低pH时,形成了较大的液滴群,并且液滴聚集,使得乳液在最开始时分层现象最为明显。乳液随着pH的增大CI值会逐渐减小并会延迟分层,翟希川在研究细菌纤维素中也发现增大pH 会延缓乳液的分层现象[26]。
![]() 图 8 在不同pH和离子强度条件下由CNCs稳定的Pickering乳液的乳析指数和外观形态注:A.在pH5~11条件下CNCs-Pickering乳液的乳析指数,a.在pH5~11条件下CNCs-Pickering乳液的外观形态;B.在离子强度10~100 mmol/L条件下CNCs-Pickering乳液的乳析指数,b.在离子强度10~100 mmol/L条件下CNCs-Pickering乳液的外观形态。Figure 8. Creaming index and appearance morphology of the Pickering emulsion stabilized by CNCs at different pH and different ion strengths
图 8 在不同pH和离子强度条件下由CNCs稳定的Pickering乳液的乳析指数和外观形态注:A.在pH5~11条件下CNCs-Pickering乳液的乳析指数,a.在pH5~11条件下CNCs-Pickering乳液的外观形态;B.在离子强度10~100 mmol/L条件下CNCs-Pickering乳液的乳析指数,b.在离子强度10~100 mmol/L条件下CNCs-Pickering乳液的外观形态。Figure 8. Creaming index and appearance morphology of the Pickering emulsion stabilized by CNCs at different pH and different ion strengthsCNCs-Pickering乳液在不同离子强度下的CI和外观形态如图8B和图8b所示。在NaCl浓度为100 mmol/L时,乳液在1 d内就会分层,在第6 d达到顶峰。而在低NaCl条件下,乳液会在1 d分层,在第7 d达到峰值。100 mmol/L乳液的CI值高于低盐浓度的CI值,表明在100 mmol/L的条件下有最少的乳化层,这可能是因为在高盐浓度的条件下,NaCl会对纤维素粒子有较高的静电屏蔽作用,在这种作用下,液滴聚集,水、油会有较快的分层的速度。但NaCl浓度较低时,油水界面会形成网状结构,减缓乳液的分层速度。这与Yang等[12]在研究银杏纳米纤维素中的发现是相似的。
3. 结论
本文研究了以甘蔗渣CNCs作为Pickering乳液的稳定剂,探究pH和离子强度对乳液的形成和稳定性的影响。结果表明,通过水解后得到的CNCs仍然保持Ⅰ型纤维素构型,有较高的结晶度,CNCs-Pickering乳液在pH11和10 mmol/L时有最低的乳析指数、较小的粒径、较高的Zeta电位绝对值,良好的微观结构和较好的流变性能。揭示了甘蔗渣CNCs在不同pH和离子强度下的乳化性能,这对甘蔗渣副产物作为潜在乳化剂在食品、化妆品或医药领域中的应用具有重要意义。
-
图 4 不同pH和离子强度条件下CNCs颗粒的粒径和电位
注:A.在pH5~11条件下CNCs颗粒的粒径和电位;B.在离子强度10~100 mmol/L条件下CNCs颗粒的粒径和电位;同一指标相同类型的不同字母表示样本间显著差异(P<0.05);图5同。
Figure 4. Particle size and zeta potential of the CNCs suspensions of different pH and different ionic strengths
图 8 在不同pH和离子强度条件下由CNCs稳定的Pickering乳液的乳析指数和外观形态
注:A.在pH5~11条件下CNCs-Pickering乳液的乳析指数,a.在pH5~11条件下CNCs-Pickering乳液的外观形态;B.在离子强度10~100 mmol/L条件下CNCs-Pickering乳液的乳析指数,b.在离子强度10~100 mmol/L条件下CNCs-Pickering乳液的外观形态。
Figure 8. Creaming index and appearance morphology of the Pickering emulsion stabilized by CNCs at different pH and different ion strengths
-
[1] ARACELI G, ALESSANDRO G, JALEL L, et al. Industrial and crop wastes: A new source for nanocellulose biorefinery[J]. Industrial Crops & Products,2016,93:26−38.
[2] PATCHIYA P, PRASERT R, HAO X G, et al. Nanocellulose: Extraction and application[J]. Carbon Resources Conversion,2018,1(1):32−43. doi: 10.1016/j.crcon.2018.05.004
[3] 陈媛, 张欢, 余永, 等. 纤维素纳米晶稳定Pickering 乳液及其环境响应性研究进展[J]. 食品与发酵工业,2020,46(24):238−245. [CHEN Y, ZHANG H, YU Y, et al. Progress in stability of Pickering elotion and its environmental responsiveness[J]. Food and Fermentation Industry,2020,46(24):238−245. [4] 林荣珍. 甘蔗渣综合利用发展现状探讨[J]. 企业科技与发展,2020(6):62−64. [LIN R Z. Discussion on the development status of the comprehensive utilization of sugar bagasse[J]. Science and Technology and Development,2020(6):62−64. doi: 10.3969/j.issn.1674-0688.2020.11.023 [5] 芦长椿. 纤维素资源的开发及利用新进展[J]. 纺织导报,2021(3):38−40. [LU C C. New progress in the development and utilization of cellulose resources[J]. Textile Herald,2021(3):38−40. doi: 10.3969/j.issn.1003-3025.2021.03.018 [6] LI Z, WU H R, YANG M, et al. Stability mechanism of O/W Pickering emulsions stabilized with regenerated cellulose[J]. Carbohydrate Polymers,2018,181:224−233. doi: 10.1016/j.carbpol.2017.10.080
[7] LIANG E L, SANGANGTAPRIVY. S, YONG K H, et al. Recent advances of characterization techniques for the formation, physical properties and stability of Pickering emulsion[J]. Advances in Colloid and Interface Science,2020,277:102−117.
[8] 佟臻, 韦阳, 高彦祥. 基于食品级胶体颗粒稳定Pickering乳液的研究进展[J]. 食品工业科技,2019,40(4):317−324. [[TONG Z, WEI Y, GAN Z X. Progress in stabilizing Pickering emulsion based on food-grade colloidal particles[J]. Science and Technology of Food Industry,2019,40(4):317−324. [9] SUN X J, SUN X F, ZHAN H, et al. Isolation and characterization of cellulose from sugarcane bagasse[J]. Polymer Degradation and Stability,2004,84(2):331−339. doi: 10.1016/j.polymdegradstab.2004.02.008
[10] THUNNALIN W, MANOP S. Microfibrillated cellulose from mangosteen (Garcinia mangostana L.) rind: Preparation, characterization, and evaluation as an emulsion stabilizer[J]. Food Hydrocolloids,2013,32:383−394. doi: 10.1016/j.foodhyd.2013.01.023
[11] 范柳萍, 倪洋, 段慧. 白果壳纤维素纳米丝(CNFs)的制备及其在Pickering中的应用[J]. 粮油食品科技,2021,29(3):54−60. [FAN L P, NI Y, DUAN H. Preparation of ginkgo-shell cellulose nanometer filaments and its application in Pickering[J]. Grain & Oil Science and Technology,2021,29(3):54−60. [12] YANG N, LI J W, FAN L P. Production of nanocellulose with different length from ginkgo seed shells and applications for oil in water Pickering emulsions[J]. Biological Macromolecules,2020,149:617−626. doi: 10.1016/j.ijbiomac.2020.01.263
[13] LI J H, WEI X Y, WANG Q H, et al. Homogeneous isolation of nanocellulose from sugarcane bagasse by high pressure homogenization[J]. Carbohydrate Polymers,2012,90(4):1609−1613. doi: 10.1016/j.carbpol.2012.07.038
[14] WEI X Y, WANG Y H, LI J H, et al. Effects of temperature on cellulose hydrogen bonds during dissolution in ionic liquid[J]. Carbohydrate Polymers,2018,201:387−391. doi: 10.1016/j.carbpol.2018.08.031
[15] HU X Y, HU K, ZENG L L, et al. Hydrogels prepared from pineapple peel cellulose using ionic liquid and their characterization and primary sodium salicylate release study[J]. Carbohydrate Polymers,2010,82(1):62−68. doi: 10.1016/j.carbpol.2010.04.023
[16] MANDAL A, CHAKRABARTY D. Isolation of nanocellulose from waste sugarcane bagasse(SCB) and its characterization[J]. Carbohydrate Polymers,2011,86(3):1291−1299. doi: 10.1016/j.carbpol.2011.06.030
[17] 李霞. 不同结构纳米纤维素稳定 Pickering乳液的作用机制与应用研究[D]. 广州: 华南理工大学, 2019 LI X. The mechanism and application of Pickering emulsion[D]. Guangzhou: Institutes of Technology of South China, 2019.
[18] KASIRI N, FATHI M. Production of cellulose nanocrystals from pistachio shells and their application for stabilizing Pickering emulsions[J]. International Journal of Biological Macromolecules,2018,106:1023−1031. doi: 10.1016/j.ijbiomac.2017.08.112
[19] HUANG Z L, HUANG X B. Fabrication and stability of Pickering emulsions using moringa seed residue protein: Effect of pH and ionic strength[J]. International Journal of Food Science and Technology,2021,56:3484−3494. doi: 10.1111/ijfs.14975
[20] 金克霞. 毛竹纤维素纳米晶导电薄膜制备及电磁屏蔽性能研究[D]. 北京: 中国林业科学研究院, 2020 JIN K X. Preparation and electromagnetic shielding properties of bamboo cellulose nanocrystalline conductive film[D]. Beijing: Chinese Academy of Forestry Sciences, 2020.
[21] RAM B, CHA H. New spherical nanocellulose and thiol-based adsorbent for rapid and selective removal of mercuric ions[J]. Chemical Engineering Journal,2018,331:587−596. doi: 10.1016/j.cej.2017.08.128
[22] MORIANA R, VILAPIANA R. Cellulose nanocrystals from forest residues as reinforcing agents for composites: A study from macro-to nano-dimensions[J]. Carbohydrate Polymers,2016,139:139−149. doi: 10.1016/j.carbpol.2015.12.020
[23] GARVEY C J, PARKER I H. On the interpretation of X-Ray diffraction powder patterns in term of the nanostructure of cellulose I fibres[J]. Macromolecular Chemistry and Physics,2005,206(15):1568−1575. doi: 10.1002/macp.200500008
[24] LI X, LI J, GONG J, et al. Cellulose nanocrystals (CNCs) with different crystalline allomorph for oil in water Pickering emulsions[J]. Carbohydrate Polymers,2018,183:303−310. doi: 10.1016/j.carbpol.2017.12.085
[25] 何康慧. 竹笋水不溶性膳食纤维稳定Pickering乳液及其应用[D]. 武汉: 华中农业大学, 2020 HE K H. Bamboo shoot water-soluble dietary fiber stabilized Pickering emulsion and its application[D]. Wuhan: Huazhong Agricultural University, 2020.
[26] 翟希川. 细菌纤维素纳米纤维的制备及其稳定的 Pickering乳液的特性研究[D]. 西安: 陕西师范大学, 2019 ZHAI X C. Preparation of bacterial cellulose nanofibers and stable Pickering emulsion[D]. Xi’an: Shaanxi Normal University, 2019.
[27] SOUZA G, FERREIRA R, PAULA C, et al. The effect of essential oil chemical structures on Pickering emulsion stabilized with cellulose nanofibrils[J]. Journal of Molecular Liquids, 2020, 320(PB).
[28] SHIMA S. Nanocellulose for stabilization of pickering emulsions and delivery of nutraceuticals and its interfacial adsorption mechanism[J]. Food and Bioprocess Technology: An International Journal,2020,13(8):1292−1328. doi: 10.1007/s11947-020-02481-2
[29] DONG H, DING Q J, JIANG Y F, et al. Pickering emulsions stabilized by spherical cellulose nanocrystals[J]. Carbohydrate Polymers,2021,265:118101−118101. doi: 10.1016/j.carbpol.2021.118101
[30] 陆宇. 基于纳米纤维素的Pickering乳液的制备与研究[D]. 扬州: 扬州大学, 2020 LU Y. Preparation and study of Pickering emulsion based on nanoflulose[D]. Yangzhou: Yangzhou University, 2020.
-
期刊类型引用(5)
1. 袁辛锐,杨其长,王芳,林致通. 紫胡萝卜复合发酵饮料的研制及其挥发性风味物质分析. 食品工业科技. 2024(02): 201-209 .  本站查看
本站查看
2. 林彦,段涵怡,叶敬榕,杨雪,张凤英. 微波辅助热水浸提黄芩茎叶多糖的工艺优化. 饲料工业. 2024(10): 106-112 .  百度学术
百度学术
3. 黄越,黄传书,杨碧文,赵珮,刘艳,王梅,吴均,戴宏杰. 桑椹酒发酵工艺优化及其挥发性成分分析. 食品研究与开发. 2024(12): 111-119 .  百度学术
百度学术
4. 赵港国,李晓晓,张婧靖,王军燕,麻静静,甄攀,贾丽艳. 基于响应面法优化库德毕赤酵母强化发酵工艺生产清香型白酒. 中国酿造. 2024(08): 224-229 .  百度学术
百度学术
5. 崔粲,梁雨璐,黄建梅. 党参酒发酵工艺优化及成分表征. 中国现代中药. 2024(10): 1754-1764 .  百度学术
百度学术
其他类型引用(4)







 下载:
下载:



 下载:
下载:
