Properties of Polysaccharides from Polygonatum sibiricum Extracted with Deep Eutectic Solvents
-
摘要: 为研究低共熔溶剂提取条件对黄精多糖性质及体外抗氧化活性的影响,以鸡头黄精为原料,对不同条件下低共熔溶剂提取得到的黄精多糖进行相对分子量、单糖组成等基本性质和体外抗氧化活性的测定。结果显示,相比于传统水提醇沉法,采用低共熔溶剂法提取黄精多糖,70 ℃时得率为18%,提高了36%,所得多糖的相对分子量变小且半乳糖含量升高;100 ℃提取的多糖相对分子量更小,且主要成分为葡萄糖。羟基自由基与DPPH自由基清除率、总抗氧化能力测定结果均表明,采用低共熔熔剂在70 ℃条件下提取的黄精多糖体外抗氧化能力明显高于传统水提醇沉法和低共熔溶剂法在100 ℃条件下提取的黄精多糖。当浓度为3.0 mg/mL时,采用低共熔熔剂在70 ℃提取的黄精多糖总抗氧化能力为4.5 U/mL,是水提多糖的4.3倍,是100 ℃条件提取黄精多糖的7.4倍。低共熔溶剂对黄精多糖具有降低分子量、提高抗氧化性等效果,研究结果可以为低共熔溶剂在多糖提取方面的应用提供参考。Abstract: In order to understand the effect of deep eutectic solvents (DESs) extraction conditions on the properties changes and antioxidant activity in vitro of Polygonatum sibiricum polysaccharides (PSP), Polygonatum sibiricum was taken as the main raw material, and the relative molecular weight, monosaccharide composition and antioxidant activities of polysaccharides extracted with DESs were analyzed. The results showed that compared with the traditional water extraction method, the yield of polysaccharides extracted by 70 ℃ DESs was 18%, which was 36% higher than that by traditional water extraction. The molecular weight of PSP decreased and the galactose content increased; the molecular weight of HDPSP which extracted at 100 ℃ was lower, and the main component was glucose. The scavenging rates of hydroxyl free radical and DPPH free radical and the total antioxidant capacity of Polygonatum sibiricum polysaccharide showed that the antioxidant capacity of Polygonatum sibiricum polysaccharide extracted with DESs at 70 ℃ was significantly higher than that of polysaccharide extracted at 100 ℃ and water extraction. When the concentration was 3.0 mg/mL, the total antioxidant capacity of polysaccharides extracted at 70 ℃ was 4.5 U/mL, 4.3 times that of water-extracted polysaccharides, and 7.4 times that of polysaccharides extracted at 100 ℃. Deep eutectic solvent can reduce molecular weight and improve antioxidant activity of Polygonatum sibiricum polysaccharide. The results can provide reference for the application of deep eutectic solvent in polysaccharide extraction.
-
黄精为百合科植物,其根茎是中国的传统药品,味甘性平,具有补气养阴、健脾、润肺、益肾之功效;2017年成为新资源食品之一,含有多种营养成分,包括多糖、蛋白质、维生素等,生食、炖服、晒干食用均可。黄精主要分为鸡头黄精(Polygonatum sibiricum)、滇黄精(Polygonatum kingianum)和多花黄精(Polygonatum cyrtonema)。从黄精中分离出多种化合物,包括甾体皂苷类、三萜皂苷类、异黄酮类、生物碱类、木质素类、苯乙肉桂类、多糖和凝集素等[1]。黄精多糖是黄精的主要活性成分之一,具有抗氧化[2-4]、调节糖脂代谢[5-7]、调节免疫[8-9]、抗衰老[10]等活性。
低共熔溶剂(Deep eutectic solvents,DESs)是一种新型的绿色溶剂[11],呈弱酸性,有助于分解植物细胞壁中的木质素及纤维素,促进植物活性物质的溶出[12],已被成功应用于植物活性成分的萃取过程中,对天然活性成分表现出高效的提取效果[13-16]。尤其是随着温度的升高,DESs粘度降低[17],更有利于植物多糖的提取,但高温对DESs提取黄精多糖的影响机制还有待研究。
在前期研究中,本团队优化了低共熔溶剂提取黄精多糖的工艺,多糖得率大大提高。70 ℃时低共熔溶剂提取的黄精多糖得率为18%,相比于水提黄精多糖提高了36%。本实验主要研究低共熔溶剂提取的黄精多糖的性质和活性,尤其是对不同温度条件下提取的黄精多糖相对分子量、单糖组成等性质和体外抗氧化活性进行对比分析,为低共熔溶剂提取黄精多糖的应用提供理论依据。
1. 材料与方法
1.1 材料与仪器
鸡头黄精 湖北省十堰市丹江口市武当山基地;氯化胆碱 上海国药控股化学试剂有限公司;草酸 国药集团化学试剂有限公司;总抗氧化能力试剂盒 南京建成生物工程研究所;无水乙醇、浓盐酸、浓硫酸、磷酸、苯酚、葡萄糖 北京化工厂;甘露糖、鼠李糖、核糖、半乳糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、阿拉伯糖、岩藻糖 标准品,纯度≥99%,Sigma公司。
Agilent1200高效液相色谱仪(配有示差检测器和B.03.01色谱工作站) 安捷伦科技有限公司;岛津LC-20AD液相色谱仪 岛津有限公司;FD-2A冷冻干燥机 北京博医康实验仪器有限公司;TU-1810PU紫外分光光度计 北京普析通用仪器厂;TG16-WS台式离心机 长沙湘仪离心机仪器有限公司。
1.2 实验方法
1.2.1 黄精多糖的提取与制备
1.2.1.1 黄精预处理
取黄精60 ℃干燥6 h,粉碎并过60目筛。取粉末0.5 g,加入80%乙醇25 mL混匀,超声30 min,4000 r/min离心10 min,用80%乙醇洗涤沉淀2~3次,得到黄精沉淀,备用。
1.2.1.2 水提醇沉法提取黄精多糖
参考《中国药典》方法,略有改动。取黄精沉淀按1:50(g/mL)的料液比加入蒸馏水,沸水回流2 h。趁热过滤,保留滤渣备用。浓缩滤液,加入4倍体积无水乙醇,4 ℃静置12 h,离心后取沉淀冻干,得到黄精粗多糖WPSP。
1.2.1.3 DESs法提取黄精多糖
参考汪涛等[18]的实验方法,略有改动。将氯化胆碱和草酸按摩尔比1:1加热混合形成DESs,冷却后保存备用。取黄精按1:20(g/mL)料液比加入DESs,温度70 ℃条件下反应40 min,过滤后取滤液浓缩,加入4倍体积的无水乙醇,4 ℃静置12 h,离心后取沉淀冻干,得到黄精粗多糖DPSP。为研究低共熔溶剂极端提取条件对黄精多糖性质的影响,将提取温度提高至100 ℃,按前面操作得到黄精粗多糖HDPSP。
1.2.1.4 DESs法处理WPSP
取1 g WPSP按1:20(g/mL)料液比加入DESs,温度70 ℃,反应40 min,过滤后取滤液浓缩,加入4倍体积的无水乙醇,4 ℃静置12 h,离心后取沉淀冻干,得到黄精粗多糖DES-WPSP。
1.2.1.5 DESs法处理滤渣
取1.2.1.2中的滤渣1 g,采用同1.2.1.4的方法处理,得到黄精粗多糖DES-RPSP。
1.2.2 黄精多糖性质的测定
1.2.2.1 多糖含量的测定
采用苯酚硫酸法[19]。准确吸取0.1 mg/mL葡萄糖标准溶液0、0.2、0.4、0.6、0.8、1.0 mL分别置于比色试管中,加蒸馏水补至1.0 mL。各加入5%苯酚1.0 mL和浓硫酸5.0 mL,摇匀,冷却后于490 nm条件下测定其吸光值,以水作空白试验,绘制标准曲线,并求得标准线性方程为:y=8.8071x+0.0005,R2=0.9998。取1 mg/mL样品溶液1.0 mL采用上述方法测定样品吸光值后,代入标准线性方程计算多糖含量。
多糖含量(mg/mL)=样品吸光值−0.00058.8071 多糖得率(%)=多糖含量×多糖质量黄精质量×100 1.2.2.2 还原糖含量的测定
参考黄小兰等[20]的方法,绘制标准曲线,并求得标准线性方程为:y=8.8071x+0.0005,R2=0.9998。多糖样品以同样方法测还原糖含量。
1.2.2.3 多糖相对分子量的测定
参考黄奕诚等[21]的方法,略加改动。采用示差折光检测器,安捷伦水相GPC/SEC色谱柱PL aquagel-OH MIXED-M (8 μm, 300 mm×7.5 mm),流动相为水,流速为1.0 mL/min,柱温为30 ℃,1 mg/mL样品溶液过0.22 μm滤膜后进样,进样量为20 μL。以保留时间为横坐标,lgMw为纵坐标绘制标准曲线,并求得标准线性方程为:y=−1.0984x+13.66,R2=0.9925。
1.2.2.4 单糖组成的测定
参考周彦强等[22]和张璐等[23]的实验条件,略加改动。仪器为岛津LC-20AD,色谱柱为Xtimate C18(4.6 mm×200 mm,5 μm),柱温为30 ℃,流速为1.0 mL/min,检测波长为250 nm,进样量为20 μL,流动相为0.05 mol/L磷酸二氢钾溶液:乙腈=83:17。精确吸取50 μg/mL混合对照标准品溶液(甘露糖、鼠李糖、核糖、半乳糖、葡萄糖醛酸、半乳糖醛酸、葡萄糖、阿拉伯糖、岩藻糖)250 μL,加入0.6 mol/L NaOH溶液250 μL、0.4 mol/L的PMP-甲醇500 μL,70 ℃反应1 h。冷却后加入0.3 mol/L HCl 500 μL、1 mL氯仿混匀,离心后取上清,萃取3次。上清用于HPLC。样品测定方法与标准品相同。
1.2.3 多糖抗氧化活性的测定
1.2.3.1 DPPH自由基清除能力的测定
参考Wang等[24]的实验方法并略加改动。取500 μL不同浓度的WPSP、DPSP和HDPSP溶液(0.5~3.0 mg/mL),加入0.1 mg/mL DPPH乙醇溶液500 μL,混匀后黑暗中放置30 min,于517 nm处测吸光度值A1;以无水乙醇代替DPPH乙醇溶液进行实验,测定样品溶液本底的吸光度值A2;以蒸馏水代替样品进行实验,测定空白对照组的吸光度值A0。DPPH自由基的清除率为:
DPPH自由基清除率(%)=(1−A1−A2A0)×100 1.2.3.2 羟基自由基清除能力的测定
参考Ling等[25]的实验方法并略加改动。取500 μL不同浓度的WPSP、DPSP和HDPSP溶液(0.5~3.0 mg/mL),加入2 mg/mL FeSO4溶液150 μL、1% H2O2溶液500 μL、1.5 mg/mL水杨酸乙醇溶液500 μL混匀,37 ℃水浴1 h,于526 nm处测定吸光度值B1;以无水乙醇代替水杨酸乙醇溶液进行实验,测定样品溶液本底的吸光度值B2;以蒸馏水代替样品进行实验,测定空白对照组的吸光度值B0。羟基自由基清除率为:
羟基自由基消除率(%)=(1−B1−B2B0)×100 1.2.3.3 总抗氧化能力(T-AOC)的测定
参照总抗氧化能力(T-AOC)测定试剂盒中的操作方法:依次加入试剂一1 mL、0.5 mL不同浓度的WPSP、DPSP和HDPSP溶液(0.5~3.0 mg/mL)、试剂二应用液2 mL、试剂三应用液0.5 mL混匀,37 ℃水浴30 min,加入0.1 mL的试剂四混匀,静置10 min,于波长520 nm处测定各管吸光度值。以蒸馏水替代样品溶液,同样步骤加入试剂一至四,测定,为对照管吸光度值。
总抗氧化能力(U/mL)=C1−C00.01×30×4.10.5 式中:在37 ℃时每分钟每毫克多糖使反应体系的吸光度值每增加0.01时为1 U;对照管的吸光度记为C0;样品管的吸光度记为C1。
1.3 数据处理
所有试验数据使用IBM SPSS Statistics 20软件进行处理,结果均用平均值±标准差表示。
2. 结果与分析
2.1 不同方法提取黄精多糖得率的比较
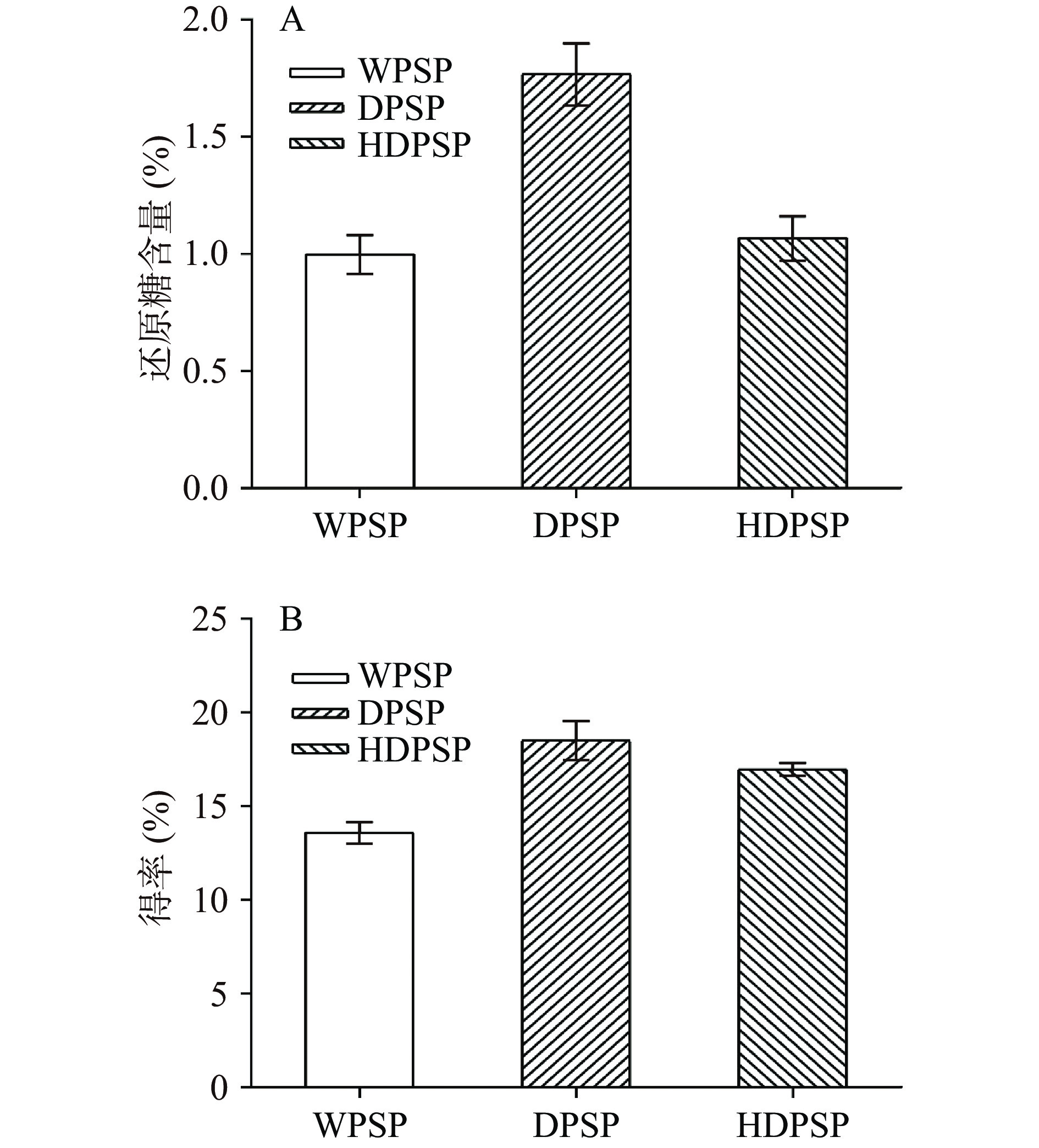
传统水提醇沉提取的多糖(WPSP)、70 ℃条件下DESs法提取的多糖(DPSP)和100 ℃条件DESs法提取的多糖(HDPSP)的得率和还原糖含量如图1所示。70 ℃低共熔溶剂法提取黄精多糖得率为18%,相较于传统水提醇沉法得率提高了36%;且DPSP的还原糖含量比WPSP提高了77%,这可能是由于低共熔溶剂对多糖分子长链具有打断作用,产生了更多的低分子量多糖或者有更多的还原性基团暴露出来,从而引起还原性末端含量升高。但是100 ℃ 条件下低共熔溶剂法提取得到的黄精多糖HDPSP得率和还原糖含量都有所降低,其机理尚不清晰。
2.2 不同方法提取黄精多糖分子量的比较
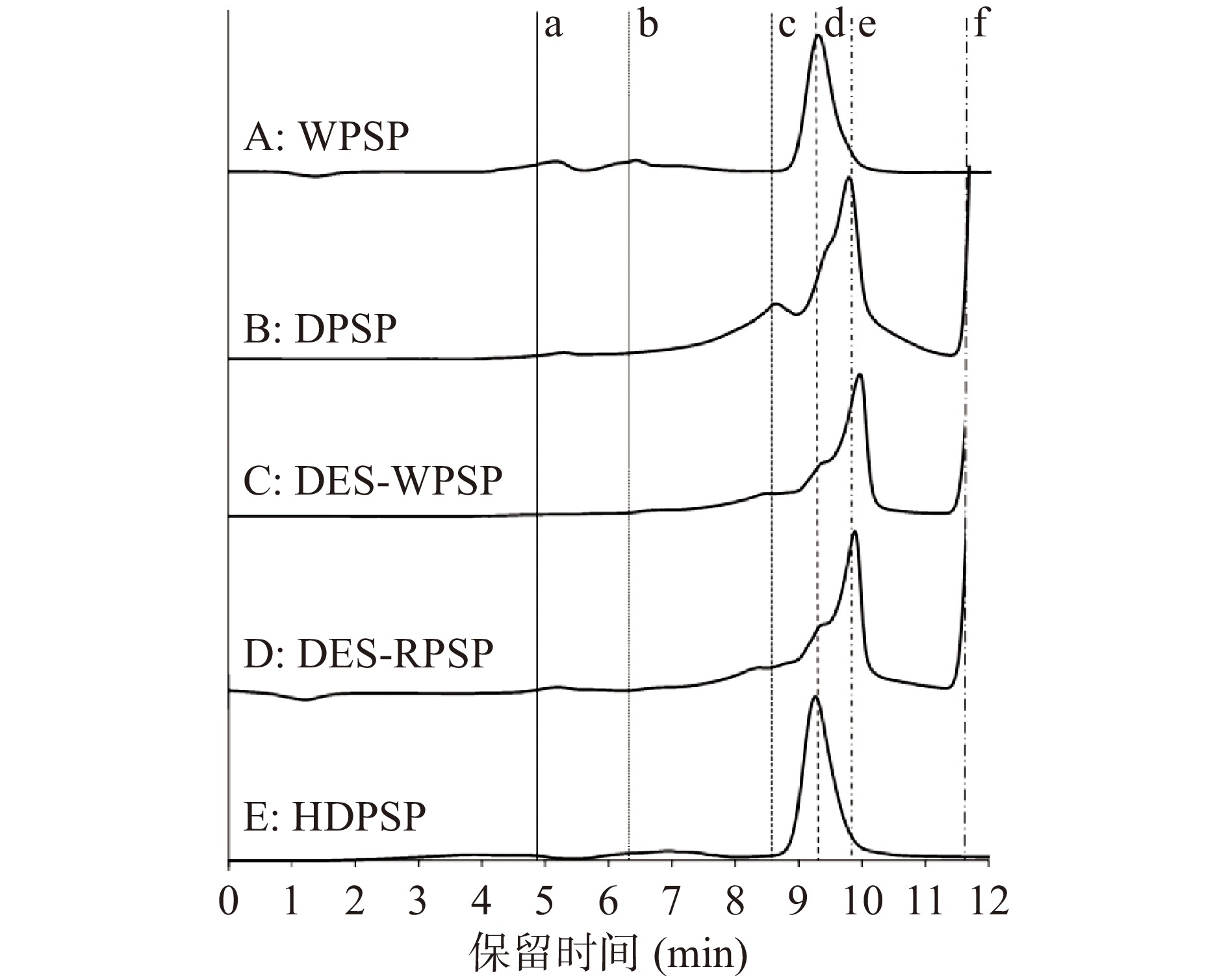
为了研究DESs对多糖的作用,在WPSP、DPSD、HDPSP之外,用DESs处理WPSP后得到了多糖DES-WPSP,用DESs处理传统水提多糖剩余的渣滓得到了多糖DES-RPSP。5种黄精多糖的GPC分子量测定保留时间-信号图如图2所示,分子量汇总结果如表1所示。通过B、C、D和A的对比,峰a、b的含量变少甚至消失,并出现新的峰c,说明DESs处理对黄精多糖具有降低分子量的作用。而且通过C、D的对比发现没有新增加的峰且峰形相似,说明DESs法可以进一步将黄精渣滓内剩余的多糖RPSP更充分地提取出来。E是多糖HDPSP的GPC分子量测定结果,可以发现分子量较为集中,分子量为4.8 kDa。
表 1 不同处理条件下黄精多糖的分子量Table 1. Molecular weight of Polygonatum sibiricum polysaccharide under different treatment conditions编号 样品 峰a(Da) 峰b(Da) 峰c(Da) 峰d(Da) A WPSP 1.0×108 4.2×106 − 4.1×103 B DPSP 1.0×108 − 8.5×103 3.9×103 C DES-WPSP − − 8.4×103 3.9×103 D DES-RPSP 1.0×108 − 8.2×103 3.9×103 E HDPSP 1.2×108 − − 4.8×103 2.3 不同方法提取黄精多糖单糖组成的比较
为了研究DESs提取对黄精多糖单糖组成的影响,本实验对WPSP、DPSP、HDPSP、DES-WPSP、DES-RPSP多糖的单糖组成进行分析比较,结果如表2。这几种多糖的单糖组成以甘露糖、葡萄糖和半乳糖为主要成分,还含有鼠李糖、葡萄糖醛酸和半乳糖醛酸等。经过DESs处理的多糖相较于水提醇沉法得到的多糖在单糖组成上差异明显。由于DES-WPSP为DESs直接降解多糖、DPSP为边提取黄精多糖边降解多糖、DES-RPSP为边提取黄精渣滓多糖边降解多糖,按照此顺序,随着体系中多糖与DESs接触面积比例的减小,甘露糖含量逐渐降低,DES-RPSP的甘露糖含量为4.04%;半乳糖含量逐渐升高,DES-RPSP的半乳糖含量为72.85%。HDPSP的单糖组成变化最为明显,除葡萄糖及其醛酸含量升高及核糖、木糖含量基本不变外,其他的单糖含量均降低,可能是因为低共熔溶剂剧烈的降解作用引起了单糖的丢失,导致这些单糖含量降低。
表 2 五种黄精多糖中单糖组分含量的比较(%)Table 2. Comparison of five kinds of PSPs’ monosaccharides components(%)含量 WPSP DES-WPSP DPSP DES-RPSP HDPSP 甘露糖 45.66 27.71 11.04 4.04 21.78 核糖 0.26 0.09 0.16 0.19 0.28 鼠李糖 1.80 3.51 3.78 3.55 0.42 葡萄糖醛酸 0.62 0.76 1.82 2.03 1.90 半乳糖醛酸 5.20 12.57 7.71 6.72 1.27 葡萄糖 26.67 19.78 10.48 10.31 64.89 半乳糖 16.09 34.15 64.57 72.85 6.62 木糖 0.17 0.09 0.10 0.12 0.19 阿拉伯糖 3.01 0.53 0.25 0.10 2.16 岩藻糖 0.54 0.82 0.08 0.11 0.48 2.4 不同方法提取黄精多糖体外抗氧化活性的比较
2.4.1 DPPH自由基清除能力
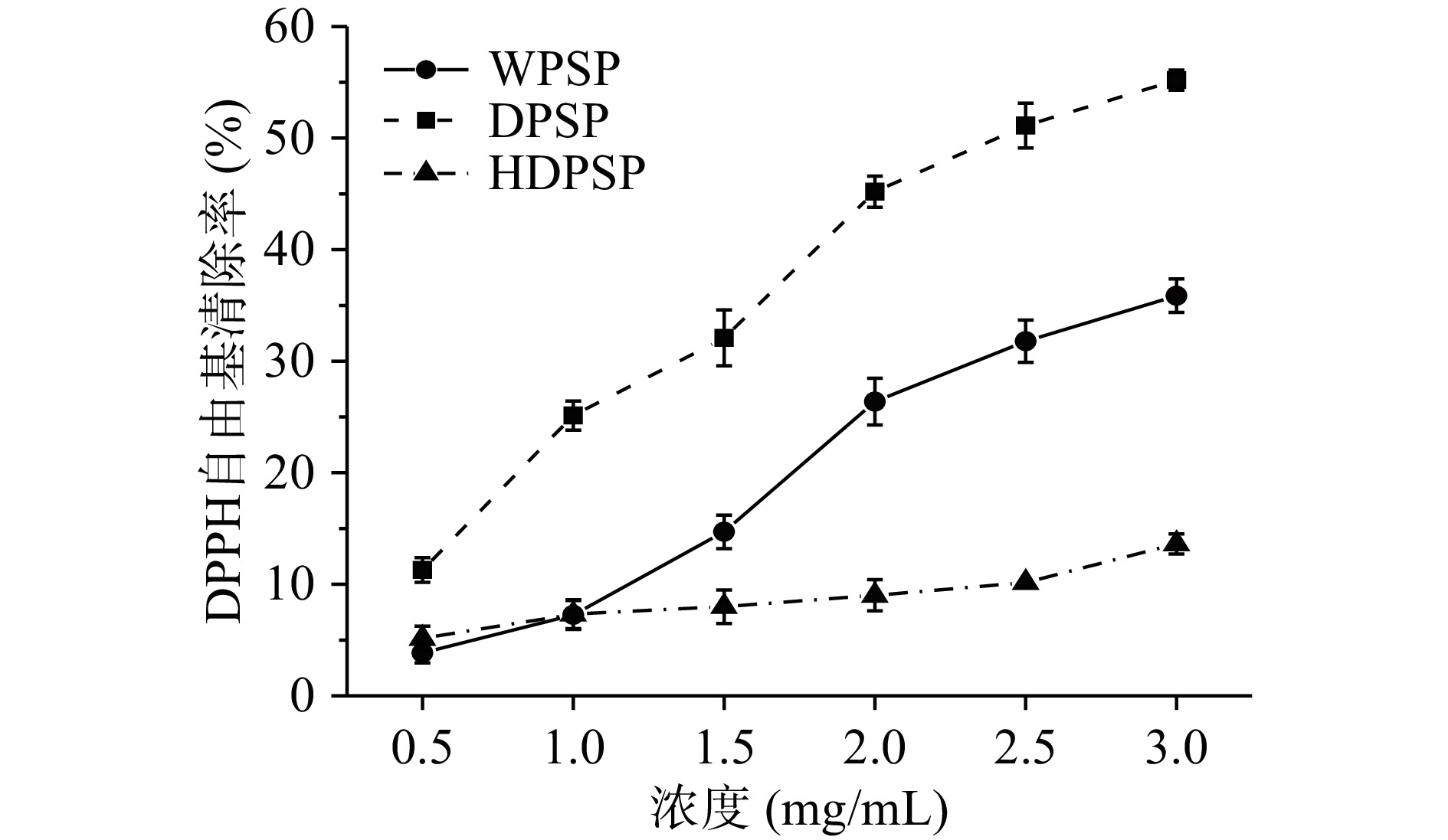
DPPH分析法是用来筛选自由基清除剂和判断抗氧化活性的常见方法,抗氧化剂的清除能力可以用DPPH自由基半数清除率(IC50值)时抗氧化剂的浓度来表示。对WPSP、DPSP、HDPSP的DPPH自由基清除能力进行测定,结果如图3。在0.5~3.0 mg/mL的范围内,DPSP和HDPSP的DPPH自由基清除率随浓度的提高而增强,且在此范围内,DPSP的清除能力都比同浓度下的WPSP和HDPSP高。WPSP、DPSP、HDPSP的半数清除率分别是3.89、2.50、15.63 mg/mL,即DPPH自由基的清除能力从高到低依次是DPSP、 WPSP、HDPSP。
2.4.2 羟自由基清除能力
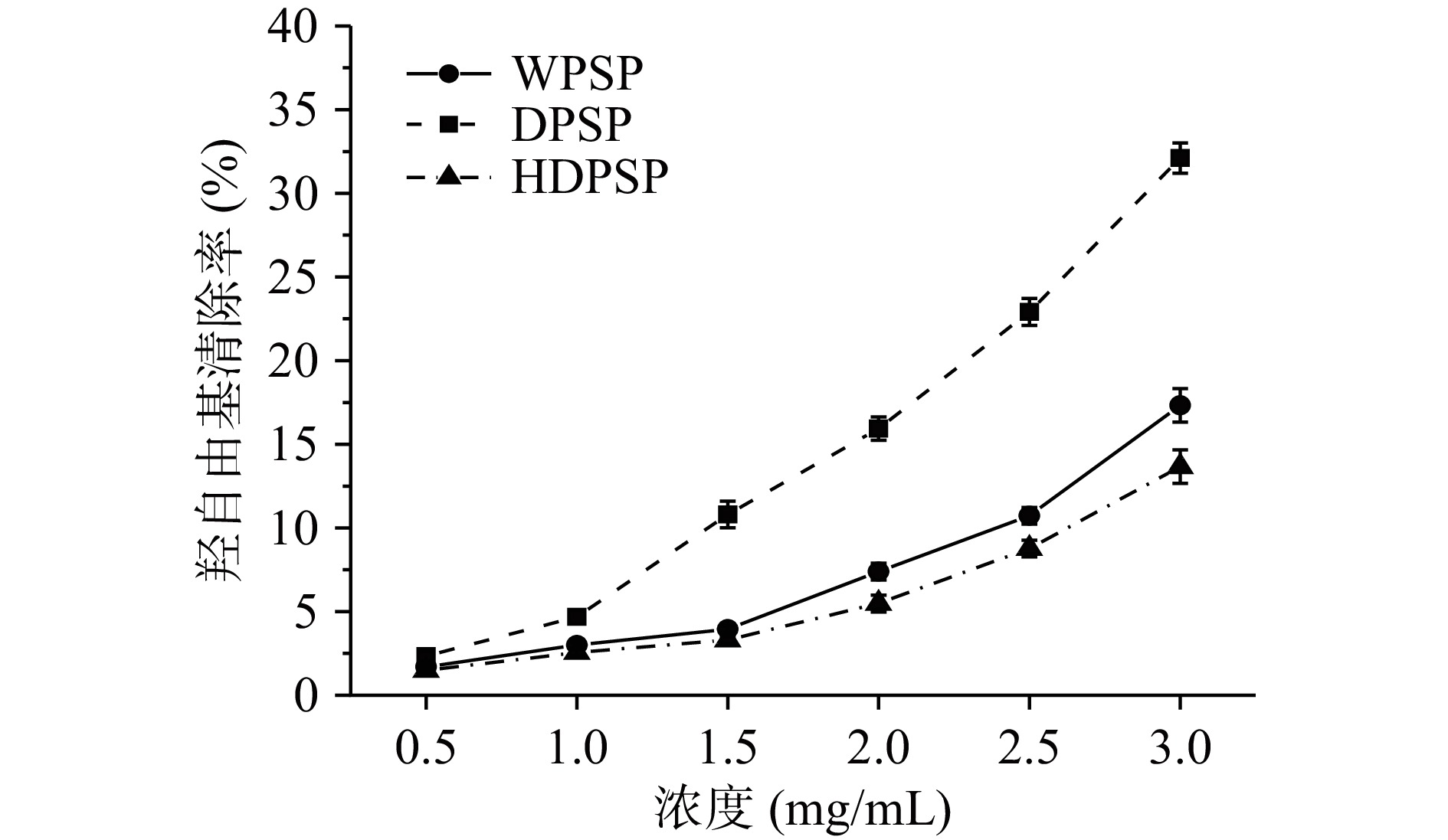
利用Fenton反应产生羟自由基,通过对比羟自由基清除率来反映抗氧化剂的抗氧化能力。三种多糖WPSP、DPSP、HDPSP对羟自由基清除能力如下图4所示。在0.5~3.0 mg/mL的浓度范围内,多糖对羟自由基清除能力随浓度的升高而增强。WPSP、DPSP、HDPSP对羟自由基半数清除率分别是8.87、4.70、11.18 mg/mL,即羟自由基清除能力从高到低依次是DPSP、WPSP、HDPSP。
2.4.3 总抗氧化能力
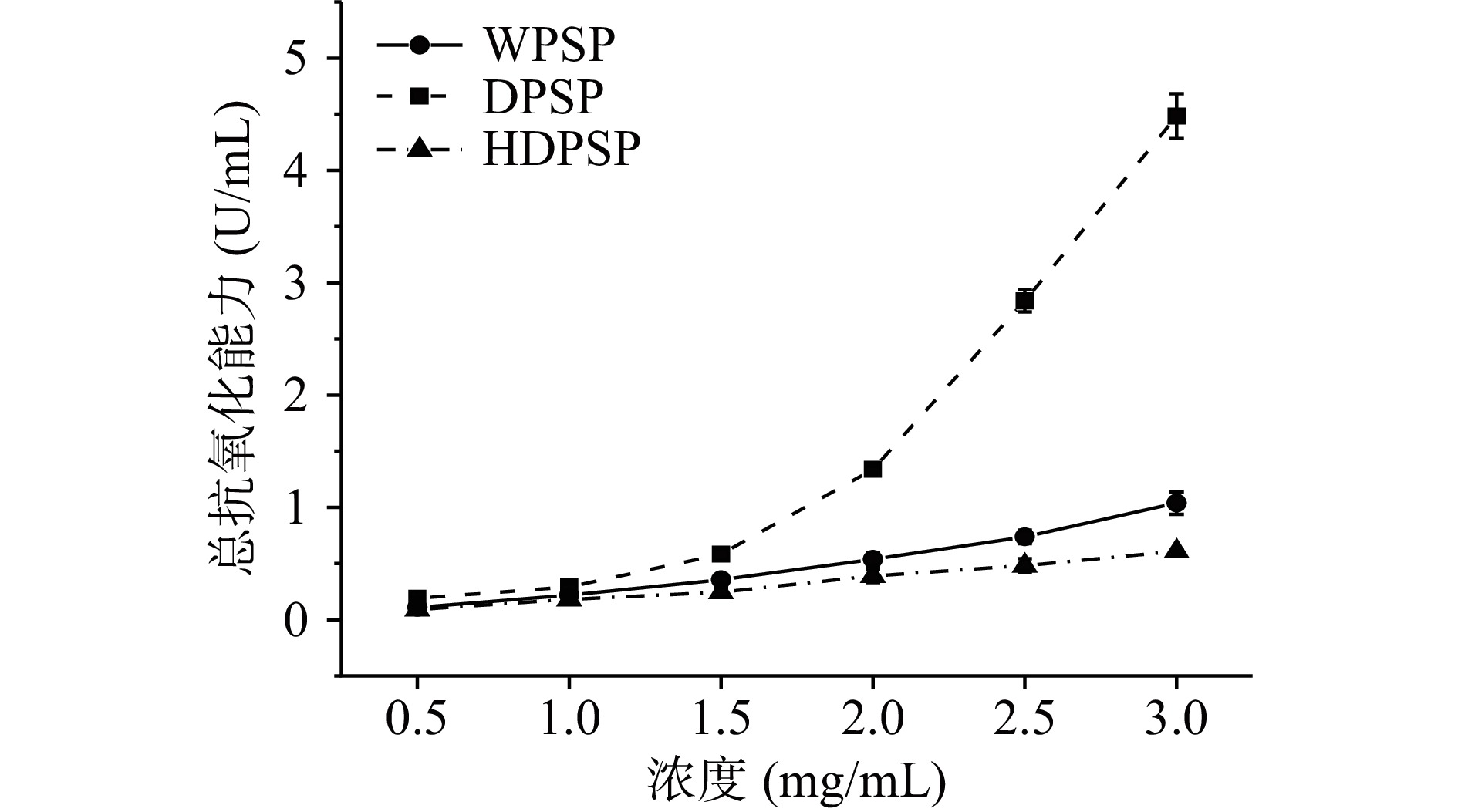
采用T-AOC法测得三种多糖WPSP、DPSP、HDPSP总抗氧化能力如下图5所示。随着多糖浓度的升高,多糖的总抗氧化能力增强。当浓度为3.0 mg/mL时,DPSP的总抗氧化能力为4.5 U/mL,是WPSP的4.3倍,是HDPSP的7.4倍。它们的总抗氧化能力的高低依次是:DPSP、WPSP、HDPSP。
3. 讨论与结论
DESs提取可以有效提高黄精多糖的得率,而且得到的多糖在分子量、单糖组成、抗氧化能力等性质方面存在差异。DESs法提取生黄精多糖得率为18%,比经典水提法提高了36%,但是其作用机理尚不清晰。张成武[26]研究发现大多数低共熔溶剂一定程度上破坏了纤维素分子内氢键,使纤维素的结晶度降低、表面变得粗糙。低共熔溶剂对木质素和纤维素的破坏,有利于DESs通过植物纤维层提取多糖,大部分多糖能通过氢键作用被提取出来。结果表明,DESs可以降低黄精多糖分子量,当温度提高至100 ℃时,大部分的多糖分子量被降低至4 kDa左右。此外,从水提取后剩余的黄精渣滓中采用DESs法再次提取,得到的多糖GPC测定结果中没有新的峰出现。DESs可以将水提得到的多糖分子打开,分子量降低,并进一步将渣滓里的残留多糖更充分地提取出来。黄精多糖分子量的降低,可能会促进机体对多糖的吸收[27-28],但还需要进一步的验证。
黄精多糖是以甘露糖、葡萄糖和半乳糖为主的多聚糖。和WPSP相比,DESs处理黄精多糖会引起单糖组成的变化,尤其是甘露糖和半乳糖的比例。具体DESs的作用机制,还需进一步纯化黄精多糖,或者采用模式寡糖为原料,探究DESs降解黄精多糖后多糖结构和组分的变化。
低共熔溶剂提取的多糖有更好的体外抗氧化活性。黄秀红等[29]根据茶多糖的特性优化茶多糖低共熔溶剂提取工艺,与经典水提醇沉法相比,茶多糖得率、DPPH自由基抗氧化能力和羟自由基抗氧化能力分别提高了20%、54%、33%。Shang等[30]的研究发现海胆多糖经低共熔溶剂处理后具有良好的体外抗氧化活性。本研究体外抗氧化试验中,DPSP具有更好的体外抗氧化活性,这可能是因为黄精多糖经DESs在70 ℃温度下打开分子链,官能团暴露增加,还原性末端含量增加。研究结果可以为低共熔溶剂在黄精多糖提取方面的应用提供科学参考,促进黄精的开发利用,提升黄精多糖的药用价值和经济价值。
-
表 1 不同处理条件下黄精多糖的分子量
Table 1 Molecular weight of Polygonatum sibiricum polysaccharide under different treatment conditions
编号 样品 峰a(Da) 峰b(Da) 峰c(Da) 峰d(Da) A WPSP 1.0×108 4.2×106 − 4.1×103 B DPSP 1.0×108 − 8.5×103 3.9×103 C DES-WPSP − − 8.4×103 3.9×103 D DES-RPSP 1.0×108 − 8.2×103 3.9×103 E HDPSP 1.2×108 − − 4.8×103 表 2 五种黄精多糖中单糖组分含量的比较(%)
Table 2 Comparison of five kinds of PSPs’ monosaccharides components(%)
含量 WPSP DES-WPSP DPSP DES-RPSP HDPSP 甘露糖 45.66 27.71 11.04 4.04 21.78 核糖 0.26 0.09 0.16 0.19 0.28 鼠李糖 1.80 3.51 3.78 3.55 0.42 葡萄糖醛酸 0.62 0.76 1.82 2.03 1.90 半乳糖醛酸 5.20 12.57 7.71 6.72 1.27 葡萄糖 26.67 19.78 10.48 10.31 64.89 半乳糖 16.09 34.15 64.57 72.85 6.62 木糖 0.17 0.09 0.10 0.12 0.19 阿拉伯糖 3.01 0.53 0.25 0.10 2.16 岩藻糖 0.54 0.82 0.08 0.11 0.48 -
[1] ZHAO P, ZHAO C, LI X, et al. The genus polygonatum: A review of ethnopharmacology, phytochemistry and pharmacology[J]. Journal of Ethnopharmacol,2018,214:274−291.
[2] 王艳, 董鹏, 金晨钟, 等. 黄精多糖组成及其抗氧化活性分析[J]. 基因组学与应用生物学,2019,38(5):2191−2199. [WANG Y, DONG P, JIN C Z, et al. Analysis on composition of Polygonatum sibiricum polysaccharide and its anti-oxidant activity[J]. Genomics and Applied Biology,2019,38(5):2191−2199. [3] 苏伟, 赵利, 刘建涛, 等. 黄精多糖抑菌及抗氧化性能研究[J]. 食品科学,2007,28(8):55−57. [SU W, ZHAO L, LIU J T, et al. Study on bacteriostasis and anti-oxidation of Polyonatic sibiricum polysacchaides[J]. Food Science,2007,28(8):55−57. doi: 10.3321/j.issn:1002-6630.2007.08.007 [4] 张静, 张艳贞, 陈文, 等. 四产地黄精中多糖含量及抗氧化活性比较[J]. 食品工业科技,2013,34(2):147−148. [ZHANG J, ZHANG Y Z, CHEN W, et al. Comparison of polysaccharide content and anti-oxidation activity in Polygonatum from four different regions[J]. Science and Technology of Food Industry,2013,34(2):147−148. [5] WANG Y, QIN S C, PEN G Q, et al. Potential ocular protection and dynamic observation of Polygonatum sibiricum polysaccharide against streptozocin-induced diabetic rats model[J]. Experimental Biology & Medicine,2016,242(1):92−101.
[6] CAI J, ZHU Y, ZUO Y, et al. Polygonatum sibiricum polysaccharide alleviates inflammatory cytokines and promotes glucose uptake in highglucose and highinsulininduced 3T3L1 adipocytes by promoting Nrf2 expression[J]. Molecular Medicine Reports,2019,20(4):3951−3958.
[7] YANG J X, WU S, HUANG X L, et al. Hypolipidemic activity and antiatherosclerotic effect of polysaccharide of Polygonatum sibiricum in rabbit model and related cellular mechanisms[J]. Evid Based Complement Alternat Med,2015,2015:391065.
[8] CHEN Z, LIU J, KONG X, et al. Characterization and immunological activities of polysaccharides from Polygonatum sibiricum[J]. Biological & Pharmaceutical Bulletin,2020,43(6):959−967.
[9] SHU G, XU D, ZHAO J, et al. Protective effect of Polygonatum sibiricum polysaccharide on cyclophosphamide-induced immunosuppression in chickens[J]. Research in Veterinary Science,2021,135:96−105.
[10] ZHENG S. Protective effect of Polygonatum sibiricum polysaccharide on D-galactose-induced aging rats model[J]. Scientific Reports,2020,10(1):2246.
[11] 李利芬, 余丽萍, 梁坚坤, 等. 低共熔溶剂提取植物活性成分的研究进展[J]. 粮食与油脂,2020,287(3):12−15. [LI L F, YU L P, LIANG J K, et al. Research progress on extraction of plamt active components by deep eutectic solvents[J]. Cereals & Oils,2020,287(3):12−15. [12] 司马国宝, 王帅, 崔莹, 等. 低共熔溶剂对木质纤维素分离及木质素提取的研究进展[J]. 现代化工,2019,39(9):26−30. [SIMA G B, WANG S, CUI Y, et al. Research progress in lignocellulose separation and lignin extraction by deep eutectic solvents[J]. Modern Chemical Industry,2019,39(9):26−30. [13] MBOUS Y P, HAYYAN M, HAYYAN A, et al. Applications of deep eutectic solvents in biotechnology and bioengineering-Promises and challenges[J]. Biotechnology Advances,2017,35(2):105−134.
[14] 都宏霞, 缪领珍, 胡梓恒, 等. 低共熔溶剂提取桂花黄酮的工艺优化[J]. 现代食品科技,2021,37(5):9. [DU H X, LIAO L Z, HU Z H, et al. Optimizing the extraction of flavonoids from Osmanthus fragrans using deep eutectic solvents[J]. Modern Food Science & Technology,2021,37(5):9. [15] 李霄, 薛成虎, 高立国, 等. 芹菜叶中芹菜素的提取工艺优化及其体外抗氧化性研究[J]. 当代化工,2017,46(7):1293−1298. [LI X, XUE C H, GAO L G, et al. Optimization of extraction process of apigenin in celery leaves and its antioxidant activity in vitro[J]. Contemporary Chemical Industry,2017,46(7):1293−1298. doi: 10.3969/j.issn.1671-0460.2017.07.005 [16] CRONIN D J, CHEN X, MOGHODDAM L, et al. Deep eutectic solvent extraction of high-purity lignin from a corn stover hydrolysate[J]. ChemSusChem,2020,13(17):4678−4690.
[17] ZHANG Q, KARINE D O V, ROYER S, et al. Deep eutectic solvents: Syntheses, properties and applications[J]. Chemical Society Reviews,2012,41(21):7108−7146.
[18] 汪涛, 周新群, 孙君社, 等. 低共熔溶剂提取黄精多糖工艺优化及抗氧化活性研究[J]. 食品科学技术学报,2020,158(6):115−124. [WANG T, ZHOU X Q, SUN J S, et al. Study on optimal process and antioxidant activity of Polygonatum sibiricum polysaccharides extracted by deep eutectic solvents[J]. Journal of Food Science and Technology,2020,158(6):115−124. [19] DUBOIS M, GILLES K A, HAMILTON J K, et al. Colorimetric method for determination of sugars and related substances[J]. Analytical Chemistry,1956,28(3):350−356.
[20] 黄小兰, 周祥德, 杨勤, 等. 不同产地地参中总糖, 可溶性多糖和还原糖含量的比较分析[J]. 中国野生植物资源,2020,39(6):23−27. [HUANG X L, ZHOU X D, YANG Q, et al. Content comparative analysis of total sugar, soluble polysaccharide and reducing sugar in Lycopus lucidus var. hirtus Regel from different habitats[J]. Chinese Wild Plant Resources,2020,39(6):23−27. [21] 黄奕诚, 陈雪香, 贺丽苹, 等. 蛹虫草多糖的纯化及其分子量的测定[J]. 现代食品科技,2012,28(8):1054−1057. [HUANG Y C, CHEN X X, HE L P, et al. Isolation, purification and molecular weight determination of polysaccharides from Cordyceps militaris[J]. Modern Food Science & Technology,2012,28(8):1054−1057. [22] 周彦强, 吴光斌, 陈发河. PMP柱前衍生化HPLC法测定黄秋葵多糖的单糖组成[J]. 食品科学,2019,40(4):276−281. [ZHOU Y Q, WU G B, CHEN F H. Analysis of monosaccharide composition of polysaccharides from okra by pre-column derivatization high performance liquid chromatography[J]. Food Science,2019,40(4):276−281. [23] 张璐,杨莹莹. 高效液相色谱法测定党参多糖的单糖组成及含量[J]. 中国食品添加剂,2021,32(12):163−169. [ZHANG L, YANG Y Y. Determination of monosaccharide composition and content of Codonopsis pilosula polysaccharide by HPLC[J]. China Food Additives,2021,32(12):163−169. [24] WANG Y F, JIA J, REN X, et al. Extraction, preliminary characterization and in vitro antioxidant activity of polysaccharides from Oudemansiella radicata mushroom[J]. International Journal of Biological Macromolecules,2018,120(B):1760−1769.
[25] LING C, HUANG G. Extraction, characterization and antioxidant activities of pumpkin polysaccharide[J]. International Journal of Biological Macromolecules,2018,118(A):770−774.
[26] 张成武. 低共熔溶剂预处理木质纤维素的研究[D]. 天津: 天津大学, 2016. ZHANG C W. Study on pretreatment of lignocellulose with low eutectic solvent[D]. Tianjin: Tianjin University, 2016.
[27] 武晓琳, 常耀光, 王静凤, 等. 不同分子量海参岩藻聚糖硫酸酯的制备及消化吸收特性的初步研究[J]. 中国海洋药物,2011,30(3):20−24. [WU X L, CHANG Y G, WANG J F, et al. Preparation of different molecular weights of sea cucumber fucoidan and study on their absorptive characteristics in rats[J]. Chinese Journal of Marine Drugs,2011,30(3):20−24. [28] WANG Y, LIU N, XUE X, et al. Purification, structural characterization and in vivo immunoregulatory activity of a novel polysaccharide from Polygonatum sibiricum[J]. International Journal of Biological Macromolecules,2020,160:688−694.
[29] 黄秀红, 刘丽辰, 阮怿航, 等. 响应面优化低共熔溶剂提取乌龙茶多糖的研究[J]. 食品研究与开发,2020,41(11):96−103. [HUANG X H, LIU L C, RUAN Y H, et al. Optimization of deep eutectic solvents extraction of polysaccharides from Oolong tea by response surface methodology[J]. Food Research and Development,2020,41(11):96−103. [30] SHANG X C, CHU D, ZHANG J X, et al. Microwave-assisted extraction, partial purification and biological activity in vitro of polysaccharides from bladder-wrack (Fucus vesiculosus) by using deep eutectic solvents[J]. Separation and Purification Technology,2020,259(1):118169.
-
期刊类型引用(3)
1. 贾健辉,窦博鑫,高嫚,张楚佳,刘颖,张娜. 染料木素对α-葡萄糖苷酶的抑制及分子机制. 食品工业科技. 2025(05): 63-71 .  本站查看
本站查看
2. 张楚佳,贾健辉,高嫚,王泽冉,刘颖,窦博鑫,张娜. 3种物理方法制备抗性粳米淀粉的结构与物化特性. 中国食品学报. 2025(01): 193-207 .  百度学术
百度学术
3. 高嫚,贾健辉,张楚佳,张智,刘颖,窦博鑫,张娜. 粳米重组米的制备工艺优化及性能研究. 食品工业科技. 2024(05): 169-176 .  本站查看
本站查看
其他类型引用(2)










 下载:
下载:
 下载:
下载:



