Purification of Proanthocyanidins from Binchuan Grape Seed and Its Effects on Proliferation of HepG2 Cells
-
摘要: 目的:研究云南大理宾川葡萄籽原花青素纯化及对肝癌HepG2细胞增殖的影响。方法:考察了上样液质量浓度、pH、流速、乙醇体积分数等对葡萄籽原花青素吸附及解析的影响,研究AB-8型大孔吸附树脂纯化云南大理宾川葡萄籽原花青素的条件。将纯化过程中乙醇梯度洗脱得到的不同极性葡萄籽原花青素作用于HepG2细胞,采用CCK8法检测不同浓度各极性葡萄籽原花青素对肝癌HepG2细胞增殖的影响。结果:AB-8树脂纯化葡萄籽原花青素的最佳工艺为上样液pH4.0,质量浓度为6.0 mg/mL,流速为1.0 BV/h,洗脱液的体积分数为30%,洗脱体积4 BV。此纯化使葡萄籽提取物中原花青素的含量从22.77%±0.32%提高至94.73%±0.6429%,回收率为80.55%±1.6499%。以10%、20%、30%、40%乙醇洗脱的葡萄籽原花青素极性部位各浓度对肝癌HepG2细胞的增殖均有抑制作用,其中未纯化部位(即提取物未经过大孔树脂纯化)给药浓度为200 μg/mL时抑制作用最为显著(P<0.001),10%乙醇组IC50为25.09 μg/mL,抑制效果良好。结论:云南大理宾川葡萄籽原花青素用AB-8型大孔树脂进行纯化,方法可行,该葡萄籽原花青素对肝癌HepG2细胞的增殖有较好抑制作用。Abstract: Objective: To study the purification of grape seed proanthocyanidins from Binchuan, Dali, Yunnan and their effects on the proliferation of HepG2 cells. Method: The effects of sample concentration, pH, flow rate, and ethanol volume fraction on the adsorption and resolution of grape seed proanthocyanidins were investigated, and the conditions for the AB-8 type macroporous adsorption resin to purify grape seed proanthocyanidins from Binchuan, Dali, Yunnan were studied. Grape seed proanthocyanidins of different polarities obtained by the ethanol gradient elution during the purification process were applied to HepG2 cells, and the effects of different concentrations of grape seed proanthocyanidins of different polarities on the proliferation of liver cancer HepG2 cells were detected by the CCK8 method. Results: The best process for AB-8 resin to purify grape seed proanthocyanidins was the pH of the sample solution 4.0, the mass concentration was 6.0 mg/mL, the flow rate was 1.0 BV/h, the volume fraction of the eluent was 30%, and the elution volume was 4 BV. This purification increased the content of proanthocyanidins in the grape seed extract from 22.77%±0.32% to 94.73%±0.6429%, with a recovery rate of 80.55%±1.6499%. The polar parts of grape seed proanthocyanidins eluted with 10%, 20%, 30% and 40% ethanol had inhibitory effects on the proliferation of liver cancer HepG2 cells, and the unpurified part (that is, the extract had not been purified by macroporous resin) that inhibitory effect was most significant when the administration concentration was 200 μg/mL (P<0.001). The IC50 of the 10% ethanol group was 25.09 μg/mL, which showed a better inhibitory effect. Conclusion: The grape seed proanthocyanidins in Binchuan, Dali, Yunnan are purified with AB-8 type macroporous resin, and the method is feasible. The grape seed proanthocyanidins have a good inhibitory effect on the proliferation of liver cancer HepG2 cells.
-
Keywords:
- grape seed /
- proanthocyanidin /
- purification /
- hepatocarcinoma HepG2 cell /
- proliferation
-
葡萄籽系葡萄科葡萄属葡萄(Vitis vinifera L.)的种子[1]。葡萄籽多酚作为葡萄籽提取物的主成分,是目前国内外公认清除自由基极为有效的天然抗氧化剂[2],其多酚主要成分为原花青素[3]。原花青素(procyanidins,PC)是由儿茶素或表儿茶素缩合而成的生物类黄酮,作为天然强有效的自由基清除剂,能有效清除·OH、O2-·、NO·、DPPH·等多种自由基,具有舒张血管、降血糖、降血脂[4-5],抑制肾、肠功能障碍、提高记忆力[6-8]及抗肥胖、美白等作用[9-11]。近年来,葡萄籽原花青素在抗肿瘤方面的研究备受关注,其对皮肤癌、口腔癌、乳腺癌、肝癌、肺癌、前列腺癌、胃癌、结肠癌、膀胱癌等均有一定的预防或治疗作用[12]。肝癌是全球第六大常见癌症,其发病率和死亡率均位于各类癌症前十位(发展中国家中发病率85%,居不同癌种第一),中国作为最大的发展中国家,肝癌发病总数占全球肝癌病人总数的50%[13],目前治疗肝癌的方法主要有手术切除、肝移植和放化疗法[14-16]。可见,以葡萄籽原花青素抑制肝癌的活性,研究意义较大,应用前景广阔。
云南大理宾川县处于干热河谷地区,得天独厚的地理环境,适宜葡萄种植栽培,拥有全国县级最大葡萄生产基地。宾川葡萄籽资源丰富,多酚类物质主要是原花青素含量高,开发价值极大。文献中报道葡萄籽原花青素对肝癌HepG2细胞作用的研究较少,本文以云南大理宾川产葡萄籽为原料,对其原花青素提取物进行纯化,考察了上样液质量浓度、pH、流速、乙醇体积分数等对原花青素吸附及解析的影响,确定最佳纯化工艺,并测定了不同极性葡萄籽原花青素对肝癌HepG2细胞增殖的影响,期望对云南大理宾川葡萄籽的开发和利用提供一定依据。
1. 材料与方法
1.1 材料与仪器
葡萄籽原花青素提取物 实验室自制;HepG2细胞株 中国科学院昆明细胞库;原花青素对照品 纯度≥95%,天津尖峰天然产物研究开发有限公司;甲醇、正丁醇、盐酸、硫酸铁铵等 均为分析纯,国药集团化学试剂有限公司;胎牛血清(四季青)、DMEM高糖培养基(Gibco)、胰酶-EDTA消化液(0.25%)(Hyclone)、PBS磷酸盐缓冲液、H-青链霉素混合液 BI公司;CCK8(日本同仁) 北方智杰方远科技有限公司;二甲基亚砜DMSO(细胞培养级) 索莱宝生物科技有限公司;食用酒精 市售。
UV759S紫外-可见分光光度计 上海精科公司;EX125DZH电子天平 奥豪斯仪器(常州)有限公司;DK-98-ΠA电热恒温水浴锅 天津市泰斯特仪器有限公司;SHZ-D Ш予华牌循环水真空泵 郑州巩义市予华仪器有限责任公司;LAB-25OSY超纯水仪 南京欧凯环境科技有限公司;SB-1100旋转蒸发仪 上海泉杰仪器有限公司;LGJ-10F真空冷冻干燥机 河南兄弟仪器设备有限公司;BSC-1600 ΠA2生物安全柜 苏州安泰空气技术有限公司;311二氧化碳培养箱 赛默飞世尔科技公司;ECLIPSE倒置显微镜 尼康;TD6台式低速离心机 湖南赫西仪器装备有限公司;INFINITE M200 PRO酶标仪 瑞士TECAN公司;YXQ-LS-50S立式电热压力蒸汽灭菌锅 上海博迅实业有限公司医疗设备厂;101-1EBS电热鼓风干燥箱 北京市永光明医疗仪器有限公司。
1.2 实验方法
1.2.1 葡萄籽原花青素提取物的制备
该部分内容为实验室前期研究确定。将干燥的葡萄籽,粉碎并过2号筛备用。采用超声醇提取法提取原花青素,料液比为1:30 g/mL;乙醇浓度50%;超声温度50 ℃;超声时间55 min;超声功率331.5 W。提取2次,提取液过滤,合并滤液,减压浓缩,2800 r/min离心5 min,取上清液冻干制成葡萄籽原花青素提取物备用。
1.2.2 原花青素含量测定
1.2.2.1 标准曲线和回归方程的建立
本实验采用盐酸-正丁醇法[17]测定原花青素标准曲线。称取25 mg(精确至0.1 mg)原花青素标准品于25 mL容量瓶中,用甲醇溶解并定容至刻度,摇匀,得原花青素标准储备液质量浓度为1.0 mg/mL。分别吸取原花青素标准储备液0.00、0.50、1.00、2.00、3.00、4.00、5.00 mL置于10 mL容量瓶中,加甲醇至刻度,摇匀,制成原花青素系列标准溶液。分别精密移取1.0 mL原花青素系列标准溶液于10 mL棕色容量瓶中,加入5%盐酸-正丁醇6.0 mL,2%硫酸铁铵溶液0.2 mL,混匀,置沸水中精确加热40 min后,立即置于冰水中冷却,冷却至室温后,用5%盐酸-正丁醇补足至容量瓶刻度线,在加热完毕15 min后,于546 nm波长处测吸光度。得到葡萄籽原花青素浓度C(mg/mL)与吸光度A的回归方程为:A=1.8937C+0.0293,R2=0.9973。结果表明,原花青素浓度在0~0.6 mg/mL范围内与546 nm处吸光值线性关系良好。
1.2.2.2 固体试样溶液的制备
称取冻干粉50 mg(精确至0.1 mg),置于50 mL容量瓶中,加入30 mL甲醇,超声处理20 min,放冷至室温后,加甲醇至刻度,摇匀,离心或放置至澄清后取上清液待测。取1 mL上清液按1.2.2.1中方法测定原花青素含量。液体试样:吸取1 mL的待测溶液,按1.2.2.1中方法测定原花青素含量。
1.2.3 AB-8树脂对葡萄籽原花青素提取物的静态吸附
1.2.3.1 大孔树脂预处理
将大孔吸附树脂浸泡在体积分数95%的乙醇中,充分溶胀,湿法装柱,用95%乙醇清洗至流出液加适量蒸馏水无白色混浊,再用蒸馏水洗至流出液无醇味,处理好的树脂备用。
1.2.3.2 静态吸附动力学特性的测定
准确称取处理好的AB-8型树脂2.0 g于150 mL锥形瓶中,加入质量浓度为10.0 mg/mL的葡萄籽原花青素提取物溶液20 mL,置于摇床中,25 ℃,160 r/min,振摇吸附6 h,每隔1 h取吸附液1 mL,用盐酸-正丁醇法测定吸光度,绘制静态吸附动力曲线。按以下公式计算吸附率:
式中:C0表示起始原花青素浓度,mg/mL;C1表示平衡时原花青素浓度,mg/mL。
1.2.3.3 考察上样液pH
取处理好的AB-8型树脂2.0 g于150 mL锥形瓶中,加入质量浓度为10.0 mg/mL的葡萄籽原花青素提取物溶液20 mL,pH分别为2.0、3.0、4.0、5.0、6.0,置于摇床中,25 ℃,160 r/min,振摇吸附6 h,取1 mL吸附液,用盐酸-正丁醇法测吸光度,计算吸附率,分析上样溶液pH对大孔树脂吸附的影响。
1.2.3.4 考察上样液质量浓度
取处理好的4份AB-8型树脂2.0 g于150 mL锥形瓶中,分别加入质量浓度为4.0、6.0、8.0、10.0 mg/mL的葡萄籽原花青素提取物溶液20 mL,pH均为4.0,置于摇床中,25 ℃,160 r/min,振摇吸附6 h,取吸附液1 mL,用盐酸-正丁醇法测定吸光度,计算吸附率,分析上样溶液质量浓度对大孔树脂吸附的影响。
1.2.4 AB-8树脂对葡萄籽原花青素提取物的动态吸附
将预处理好的树脂装入1.2 cm×50 cm的色谱柱中,装柱体积为10 mL。将葡萄籽原花青素提取液调整到最适pH上柱,对上样流速、洗脱剂体积分数等进行动态吸附与解吸实验。实验中待样液全部通过树脂柱后,用去离子水洗至流出液无色,再用不同浓度的乙醇以一定速度洗脱,收集洗脱液,减压浓缩,冷冻干燥,测定吸附率及解析率。
式中:C2表示上样液中原花青素浓度,mg/mL;C3表示洗脱液中原花青素浓度,mg/mL;V2表示上样体积,mL;V3表示洗脱液体积,mL。
1.2.4.1 考察上样流速
上样质量浓度为6.0 mg/mL,pH4.0,分别以1.0、2.0 BV/h流速上样,每10 mL为一个单位收集流出液,测定吸光度计算其对原花青素的吸附率。
1.2.4.2 考察洗脱剂体积分数
上样质量浓度为6.0 mg/mL,pH4.0,上样流速为1 BV/h,上样量为2 BV,上样结束后用4 BV体积的蒸馏水洗涤,然后分别用体积分数10%、20%、30%、40%、50%、60%、70%的乙醇各4 BV进行洗脱,将洗脱液减压浓缩、冷冻干燥,计算解析率。
1.2.5 葡萄籽原花青素回收率和纯度的测定
将葡萄籽原花青素提取液按最佳纯化工艺:上样液pH4.0,上样液的质量浓度为6.0 mg/mL,上样液的流速为1.0 BV/h,洗脱液的体积分数为30%,洗脱体积4 BV上柱洗脱,收集洗脱液,减压浓缩后冻干,计算原花青素的回收率和纯度。
式中:C2表示上样液原花青素浓度,mg/mL;C3表示洗脱液中原花青素浓度,mg/mL;V2表示上样体积,mL;V3表示洗脱液体积,mL;M表示洗脱液冻干后质量,mg。
1.2.6 CCK8法检测肝癌HepG2细胞增殖情况
1.2.6.1 供试样品制备
按1.2.4中葡萄籽原花青素提取物最佳纯化工艺,洗脱液稍有改动,以10%、20%、30%、40%乙醇溶液进行梯度洗脱,制备不同极性部位葡萄籽原花青素。具体方法:称取适量葡萄籽原花青素提取物,加水溶解,制得葡萄籽原花青素提取物水溶液(即未纯化部位)。通过AB-8大孔吸附树脂对该水溶液进行吸附,以不同浓度乙醇溶液梯度洗脱,收集各浓度洗脱液,合并相同浓度洗脱液,减压浓缩,将各浓缩液制成冻干粉,得到不同极性葡萄籽原花青素备用。
1.2.6.2 肝癌HepG2细胞的培养
从液氮罐里取出装有癌细胞的冻存管,置37 ℃水浴锅里,摇晃1 min,使之全部融化,然后将冻存液迅速转移到60 mm细胞培养皿中,加入含10%血清和1%青链霉素混合液的高糖培养基(完全培养基)5 mL,吹匀,在37 ℃、5% CO2无菌培养箱里培养,一般4 h细胞完全贴壁,48 h后传代。丢弃细胞培养废液,用PBS清洗两遍,注意动作轻柔,防止洗掉贴壁细胞,加入适量胰酶并在显微镜下观察,等到细胞开始变得圆润并且开始脱落,加入完全培养基终止消化,以1000 r/min离心5 min。丢弃上清液,加入完全培养液,吹散重悬细胞,按照1:3的比例进行传代。每2 d更换培养液一次,待细胞密度达到80%~90%时,即可用细胞开展实验。
1.2.6.3 葡萄籽原花青素提取物对肝癌HepG2细胞增殖的影响
取对数生长期的细胞,以104个细胞/孔接种至96孔板,每孔加100 μL,分为空白组、对照组、葡萄籽原花青素提取物不同浓度的各极性组,每组分别设5个复孔。空白组和对照组加完全培养液,给药组分别加25、50、100、200 μg/mL的葡萄籽原花青素提取物各极性冻干粉溶液,放入37 ℃,5% CO2培养箱孵育,48 h后吸走培养液,用PBS清洗两次,再加入含有10% CCK8的完全培养液,2 h后用酶标仪测定在450 nm处的吸光度。按照以下公式计算出存活率:
1.3 数据处理
实验平行3次,用统计软件GraphPad Prism7.0进行分析,实验数据用平均值±标准偏差(Mean±SD)表示,多组间比较采用One-way ANOVA。
2. 结果与分析
2.1 AB-8树脂静态吸附动力学特征
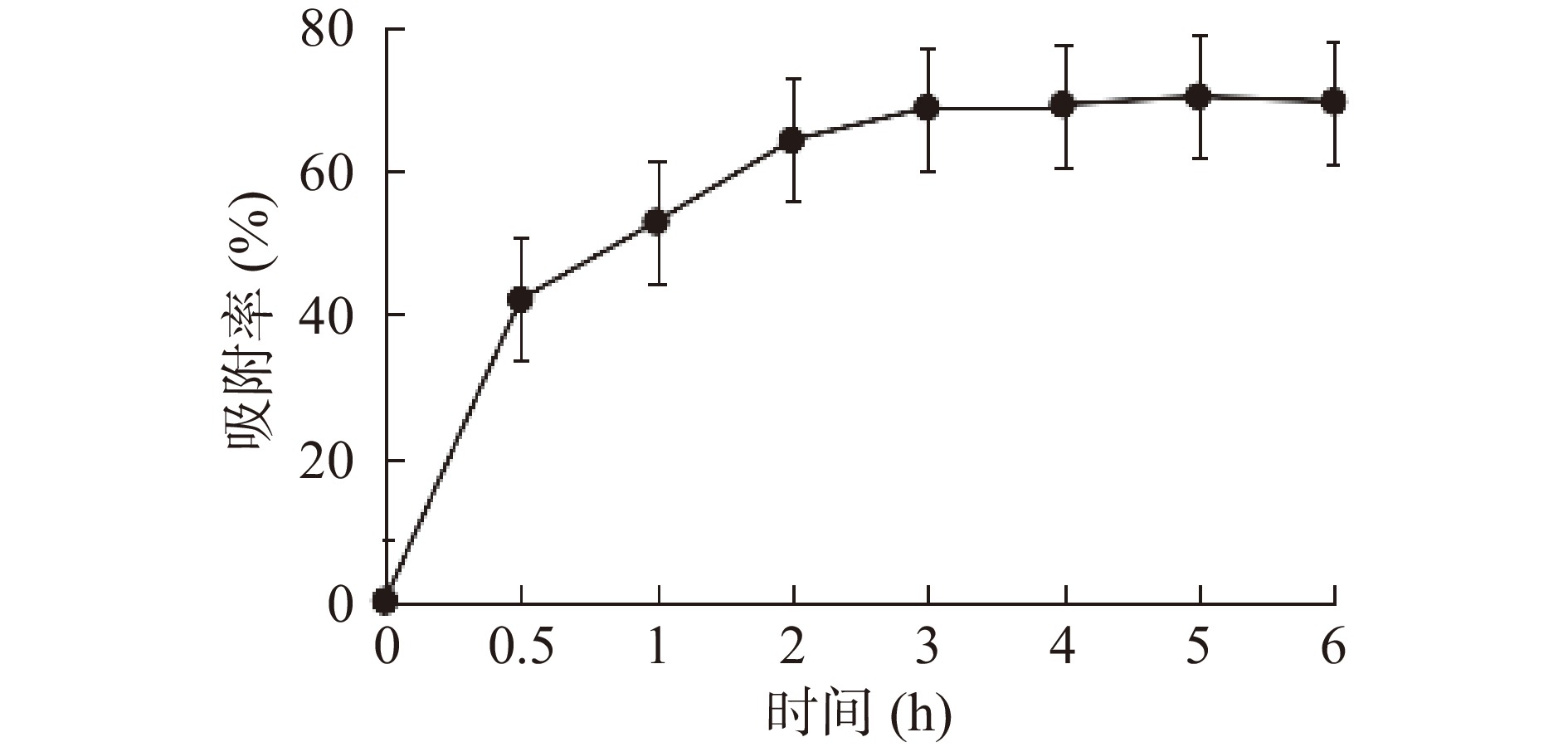
AB-8树脂静态吸附动力学曲线如图1所示。由图1可知,0.5 h内AB-8树脂对原花青素快速吸附,0.5~3 h内吸附速度变缓,3 h后吸附达到饱和,故静态吸附3 h适宜。
2.2 pH对AB-8树脂吸附葡萄籽原花青素的影响
由图2可以看出,随着pH的升高AB-8树脂对葡萄籽原花青素的吸附率呈先升高后略降低的趋势,说明一定的酸性条件有利于原花青素的吸附,其原因可能是黄酮类化合物含有酚羟基和糖苷键,当pH较小时以分子状态存在,主要依靠范德华力与树脂进行物理吸附;而在碱性条件下,以离子状态存在,吸附比较困难[18]。研究发现,pH2.0时提取溶液变得很红,pH6.0时溶液开始变成绿色,说明pH对提取物溶液中原花青素分子结构影响较大,故提取物溶液的pH应保持在适宜的范围内,当pH4.0时吸附率最高且提取物溶液颜色与未调pH前无明显差异,故最适合的pH为4.0。
2.3 上样液质量浓度对AB-8树脂吸附葡萄籽原花青素的影响
由图3可知,葡萄籽提取物浓度为6.0 mg/mL时,AB-8树脂对葡萄籽原花青素吸附率最高,此后随上样浓度的增加,吸附率逐渐降低。可能是由于上样液质量浓度增加使传质速度变慢,导致树脂周围的原花青素分子过多,使得部分原花青素未被吸附,最终导致树脂的吸附率降低。故上样质量浓度为6.0 mg/mL适宜。
2.4 上样流速对AB-8树脂吸附葡萄籽原花青素的影响
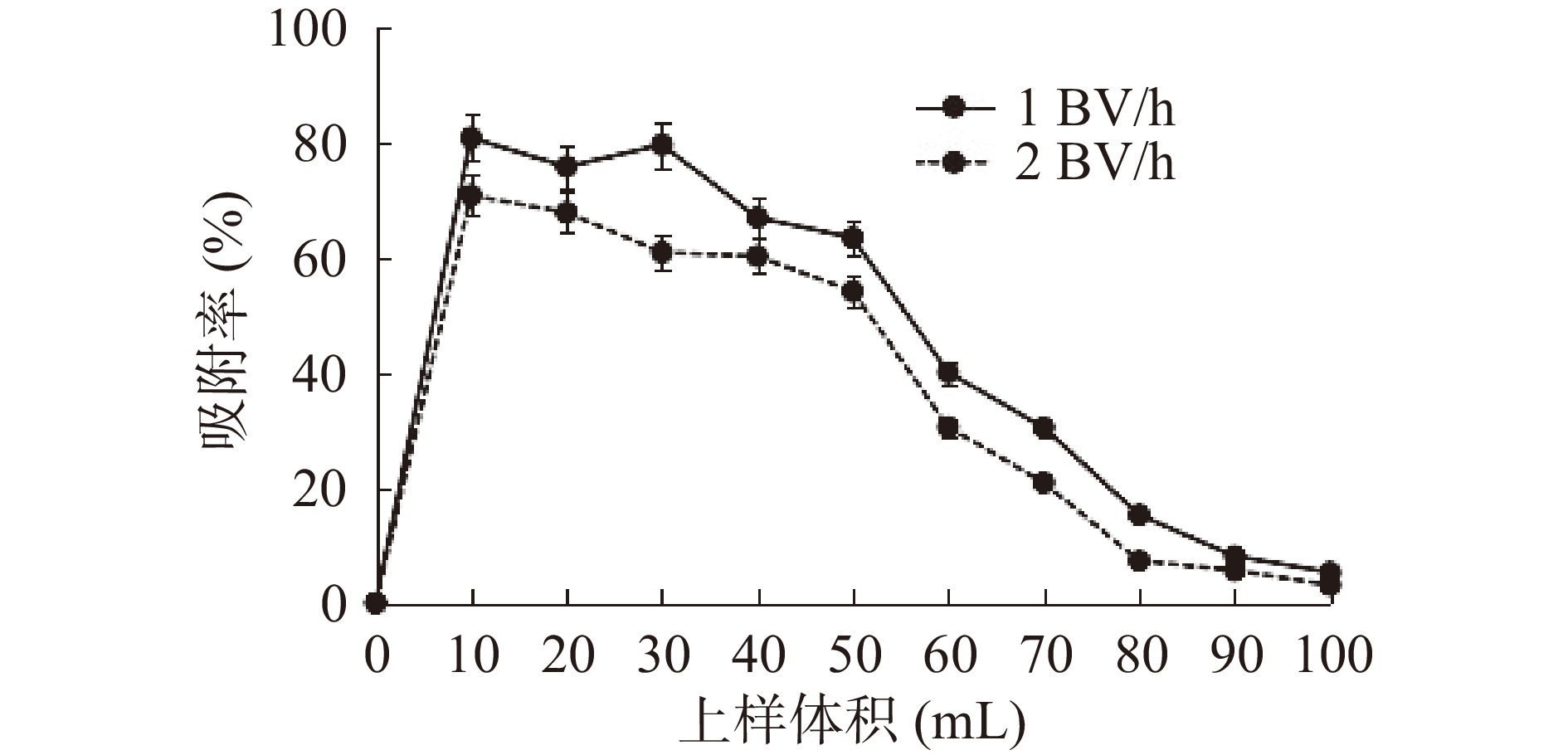
上样流速是影响大孔树脂吸附效率的关键因素,若上样速度过快,会使原花青素吸附量减少,导致花青素样品的浪费;若上样流速太慢,虽然可以使大孔树脂充分吸附原花青素,但耗时较长,影响效率[19]。由图4可以看出,随着上样流速的增大,AB-8树脂对原花青素的吸附率降低,说明高流速上样时目标成分损失大,低流速可使目标成分充分吸附于树脂。综合考虑,选择上样流速1 BV/h。
2.5 洗脱剂体积分数对洗脱的影响
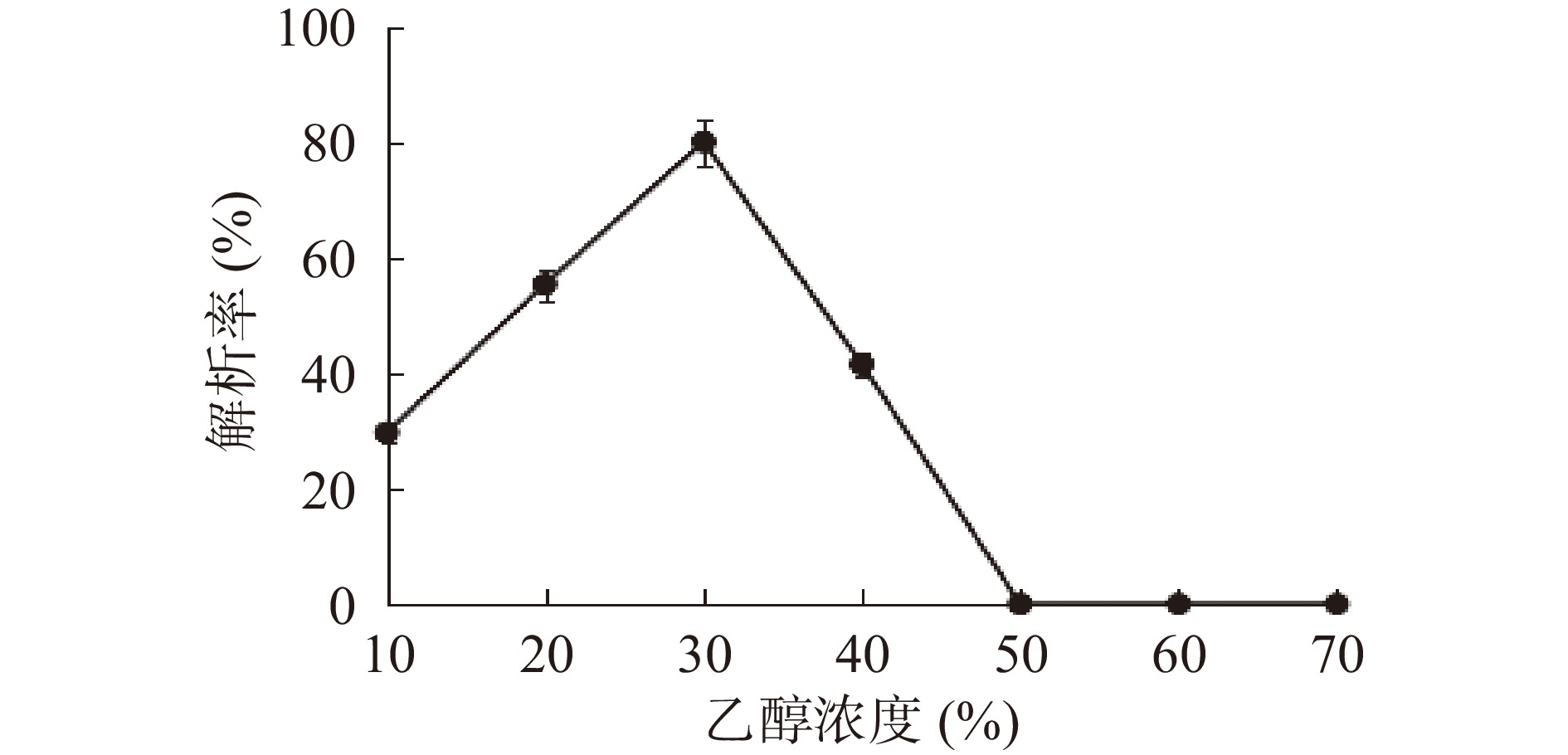
由图5可知,随着乙醇浓度的增大,解析率呈先上升后下降的趋势。乙醇浓度在10%~30%范围内,随着乙醇浓度的升高,解析率逐渐增大;当乙醇浓度为30%时,解析率最大,之后随着乙醇浓度的增大,解析率逐渐减小,乙醇浓度为50%、60%、70%时解析率为零。有研究报道,低浓度乙醇(低于40%)可洗脱原花青素的单体及低聚体(有活性部分),40%以上的乙醇可洗脱原花青素的高聚体。同时,乙醇浓度越高,解吸液杂质含量也越多,纯度越低[19]。综合考虑,选择30%乙醇作为葡萄籽原花青素的洗脱剂。
2.6 葡萄籽原花青素回收率和纯度
根据静态实验和动态时验确定吸附、解吸条件,得到最佳纯化工艺:上样液pH4.0,上样液的质量浓度为6.0 mg/mL,上样液的流速为1.0 BV/h,洗脱液的体积分数为30%,洗脱体积4 BV,并在此条件下,平行重复实验3次,计算原花青素的回收率和纯度。经计算吸附前葡萄籽提取物中原花青素纯度为22.77%±0.32%,AB-8树脂纯化后测定纯度为94.73%±0.6429%,原花青素的纯度大大提高,回收率为80.55%±1.6499%。如表1所示。
表 1 葡萄籽原花青素回收率及纯度Table 1. Extraction rate and purity of grape seed proanthocyanidins上样浓度
(mg/mL)上样体积(mL) 上样液原花青素浓度(mg/mL) 洗脱液体积(mL) 洗脱液原花青素浓度(mg/mL) 洗脱液干重(mg) 回收率
(%)纯化后纯度(%) 6 100 0.4144±0.0050 200 0.1669±0.0053 35.25±1.3629 80.55±1.6499 94.73±0.6429 2.7 不同极性葡萄籽原花青素对肝癌HepG2细胞增殖的影响
不同剂量的各极性葡萄籽原花青素对肝癌HepG2细胞作用48 h后,对其增殖产生不同的影响。数据分析显示,各极性组细胞的存活率与对照组比较均有显著变化(P<0.01或P<0.001)。由表2可知,除10%乙醇组外,其余各组细胞存活率随给药浓度的升高而降低,剂量与药效有很好的线性关系,抑制效果最明显的均为200 μg/mL。与对照组比较,不同极性葡萄籽原花青素各浓度对HepG2细胞的增殖均有抑制作用,10%乙醇组低浓度作用更明显;20%乙醇组,药物浓度为50、100 μg/mL作用基本一致,200 μg/mL抑制作用高度显著(P<0.001)。实验结果显示,葡萄籽原花青素对肝癌HepG2细胞的增殖可起到抑制作用,使其存活率降低。根据文献报道葡萄籽原花青素对多种肿瘤均有抑制作用,如可诱导人食管癌细胞ECA109凋亡[20],可抑制低氧环境下鼻咽癌CNE-2Z细胞HIF-1α表达[21],抑制骨肉瘤143B细胞[22]及MG63细胞[23]、B16黑色素瘤细胞[24]增殖,作用于结肠癌SW480和SW620细胞后,两种细胞形态均发生明显改变且细胞增殖能力下降、细胞周期改变、凋亡率升高[25];联合顺铂可促进人肺腺癌细胞A549[26]、喉癌Hep-2细胞[27]凋亡,联合吉西他滨可抑制胰腺癌PANC-1细胞增殖并促其凋亡[28],进一步提示应用葡萄籽原花青素研发抗癌新药潜力极大。
表 2 各极性组细胞的存活率及IC50值(组别 给药浓度(μg/mL) 存活率(%) IC50值(μg/mL) 对照组 100.00 −
未纯化部位组25 79.21±3.2070** 41.7000 50 39.63±0.4057*** 100 10.78±0.2576*** 200 6.48±0.1704***
10%乙醇组25 50.01±1.9450*** 25.0900 50 48.30±0.6256*** 100 55.00±1.0520*** 200 59.04±1.1360***
20%乙醇组25 68.29±5.4170*** 126.9400 50 56.63±2.6890*** 100 56.53±1.0340*** 200 37.55±0.9091***
30%乙醇组25 60.56±0.9845*** 49.9400 50 49.98±2.2180*** 100 35.22±0.4284*** 200 17.66±0.3302***
40%乙醇组25 53.94±1.6240*** 41.3700 50 48.52±1.1740*** 100 40.92±1.6560*** 200 22.48±0.1926*** 注:与对照组相比,*表示影响显著,P<0.05;**表示影响极显著,P<0.01;***表示影响高度显著,P<0.001。 3. 讨论与结论
研究发现,植物体外抗肝癌细胞生长的天然活性成分包括多糖、黄酮、萜类、酚类等化合物[29]。当前研究显示,病毒、宿主和环境因素之间的复杂相互作用最终导致肝癌的发生和发展[30]。关于葡萄籽原花青素抗癌方面的研究,文献报道较多,但未见云南大理宾川葡萄籽原花青素的相关研究。本文研究了AB-8树脂纯化云南大理宾川葡萄籽原花青素,得到最佳纯化工艺为上样液pH4.0,质量浓度6.0 mg/mL,上样液流速1.0 BV/h,洗脱液体积分数30%,洗脱体积4 BV。此纯化使葡萄籽提取物中原花青素的含量从22.77%±0.32%提高到94.73%±0.6429%,回收率为80.55%±1.6499%。纯化后的不同极性葡萄籽原花青素对肝癌HepG2细胞的生长具有不同程度的抑制作用,但其抗肝癌相关机制及相应通路的研究还未开展,后续可以深入研究。
-
表 1 葡萄籽原花青素回收率及纯度
Table 1 Extraction rate and purity of grape seed proanthocyanidins
上样浓度
(mg/mL)上样体积(mL) 上样液原花青素浓度(mg/mL) 洗脱液体积(mL) 洗脱液原花青素浓度(mg/mL) 洗脱液干重(mg) 回收率
(%)纯化后纯度(%) 6 100 0.4144±0.0050 200 0.1669±0.0053 35.25±1.3629 80.55±1.6499 94.73±0.6429 表 2 各极性组细胞的存活率及IC50值(
Table 2 Cell survival rate and IC50 value of each polarity group(
组别 给药浓度(μg/mL) 存活率(%) IC50值(μg/mL) 对照组 100.00 −
未纯化部位组25 79.21±3.2070** 41.7000 50 39.63±0.4057*** 100 10.78±0.2576*** 200 6.48±0.1704***
10%乙醇组25 50.01±1.9450*** 25.0900 50 48.30±0.6256*** 100 55.00±1.0520*** 200 59.04±1.1360***
20%乙醇组25 68.29±5.4170*** 126.9400 50 56.63±2.6890*** 100 56.53±1.0340*** 200 37.55±0.9091***
30%乙醇组25 60.56±0.9845*** 49.9400 50 49.98±2.2180*** 100 35.22±0.4284*** 200 17.66±0.3302***
40%乙醇组25 53.94±1.6240*** 41.3700 50 48.52±1.1740*** 100 40.92±1.6560*** 200 22.48±0.1926*** 注:与对照组相比,*表示影响显著,P<0.05;**表示影响极显著,P<0.01;***表示影响高度显著,P<0.001。 -
[1] 赵坤生, 时倩, 李秀昌. 葡萄籽化学成分与药理作用研究进展[J]. 泰山医学院学报,2019,40(9):718−720. [ZHAO K S, SHI Q, LI X C. Research progress on the chemical constituents and pharmacological effects of grape seeds[J]. Journal of Taishan Medical College,2019,40(9):718−720. doi: 10.3969/j.issn.1004-7115.2019.09.022 [2] BAGCHI D, BAGCHI M, STOHS S J, et al. Free radicals and grape seed proanthocyanidin extract: Importance in human health and disease prevention[J]. Toxicology,2000,148(2):187−197.
[3] QI Y, ZHANG H, WU G, et al. Mitigation effects of proanthocyanidins with different structures on acrylamide formation in chemical and fried potato crisp models[J]. Food Chemistry,2018,250:98−104. doi: 10.1016/j.foodchem.2018.01.012
[4] GJ A, MM A, PMB C, et al. Mechanisms of endothelium-dependent vasorelaxation induced by procyanidin B2 in venous bypass graft[J]. Journal of Pharmacological Sciences,2020,142(3):101−108. doi: 10.1016/j.jphs.2019.11.006
[5] 刘丹, 邓建军, 张超, 等. 原花青素防治Ⅱ型糖尿病的研究进展[J]. 食品科学,2019,40(9):302−308. [LIU D, DENG J J, ZHANG C, et al. Research progress of proanthocyanidins in the prevention and treatment of type Ⅱ diabetes[J]. Food Science,2019,40(9):302−308. doi: 10.7506/spkx1002-6630-20180131-441 [6] WANG E H, YU Z L, PING G F, et al. Grape seed procyanidin extract attenuate sodium fluoride-induced oxidative damage and apoptosis in rat kidneys[J]. Biomedical and Environmental Sciences,2020,33(6):454−457.
[7] GONZÁLEZ-QUILEN C, RODRÍGUEZ-GALLEGO E, BELTRÁN-DEBÓN R, et al. Health-promoting properties of proanthocyanidins for intestinal dysfunction[J]. Nutrients,2020,12(1):130. doi: 10.3390/nu12010130
[8] GONG X, XU L, FANG X, et al. Protective effects of grape seed procyanidin on isoflurane-induced cognitive impairment in mice[J]. Pharmaceutical Biology,2020,58(1):200−207. doi: 10.1080/13880209.2020.1730913
[9] WEI S, ZHENG Y, ZHANG M, et al. Grape seed procyanidin extract inhibits adipogenesis and stimulates lipolysis of porcine adipocytes in vitro[J]. J Anim Sci,2018,96(7):2753−2762. doi: 10.1093/jas/sky158
[10] CAO J, YU X, DENG Z, et al. Chemical compositions, antiobesity, and antioxidant effects of proanthocyanidins from lotus seed epicarp and lotus seed pot[J]. J Agric Food Chem,2018,66(51):13492−13502. doi: 10.1021/acs.jafc.8b05137
[11] VAZQUEZ-FLORES A A, MARTINEZ-GONZALEZ A I, ALVAREZ-PARRILLA E, et al. Proanthocyanidins with a low degree of polymerization are good inhibitors of digestive enzymes because of their ability to form specific interactions: A hypothesis[J]. Journal of Food Science,2018,83(10-12):2895−2902.
[12] 刘洁. 葡萄籽提取物原花青素对人膀胱癌细胞生长的抑制作用及机制研究[D]. 武汉: 华中科技大学, 2009. LIU J. Study on the inhibitory effect and mechanism of grape seed extract proanthocyanidins on the growth of human bladder cancer cells[D]. Wuhan: Huazhong University of Science and Technology, 2009.
[13] 徐春明, 庞高阳, 李婷. 花青素的生理活性研究进展[J]. 中国食品添加剂,2013(3):205−210. [XU C M, PANG G Y, LI T. Research progress on the physiological activities of anthocyanins[J]. China Food Additives,2013(3):205−210. doi: 10.3969/j.issn.1006-2513.2013.03.028 [14] TANG L, JIN X, HU X, et al. Glaucocalyxin a inhibits the growth of liver cancer focus and SMMC-7721 cells[J]. Oncol Lett,2016,11(2):1173−1178. doi: 10.3892/ol.2015.4002
[15] ZHONG J H, LI H, XIAO N, et al. Hepatic resection is safe and effective for patients with hepatocellular carcinoma and portal hypertension[J]. Plos One,2014,9(9):e108755. doi: 10.1371/journal.pone.0108755
[16] INGLE P V, SAMSUDIN S Z, CHAN P Q, et al. Development and novel therapeutics in hepatocellular carcinoma: A review[J]. Ther Clin Risk Manag,2016,12:445−455.
[17] 闫文杰, 李凯, 吕倩倩, 等. 海娇颜片中原花青素含量快速测定方法优化[J]. 食品安全质量检测学报,2020,11(3):841−846. [YAN W J, LI K, LU Q Q, et al. Optimization of rapid determination method for proanthocyanidin content in Haijiaoyan tablets[J]. Journal of Food Safety and Quality Testing,2020,11(3):841−846. [18] 宋倩, 赵声兰, 刘芳, 等. 大孔吸附树脂分离纯化核桃壳总黄酮[J]. 食品与发酵工业,2012,38(12):180−184. [SONG Q, ZHAO S L, LIU F, et al. Separation and purification of total flavonoids from walnut shell by macroporous adsorption resin[J]. Food and Fermentation Industries,2012,38(12):180−184. [19] 马小琴, 王晓敏, 周凡. 大孔吸附树脂法分离纯化葡萄籽中原花青素[J]. 食品研究与开发,2017,38(16):54−57. [MA X Q, WANG X M, ZHOU F. Separation and purification of proanthocyanidins from grape seeds by macroporous adsorption resin method[J]. Food Research and Development,2017,38(16):54−57. doi: 10.3969/j.issn.1005-6521.2017.16.012 [20] 郭方明, 李述刚, 宋关玲, 等. 葡萄籽提取物原花青素诱导人食管癌细胞ECA109凋亡[J]. 食品科学,2019,40(9):115−121. [GUO F M, LI S G, SONG G L, et al. Grape seed extract proanthocyanidins induce apoptosis in human esophageal cancer cells ECA109[J]. Food Science,2019,40(9):115−121. doi: 10.7506/spkx1002-6630-20180202-024 [21] 胡俊丽, 张月飞, 宋瑾, 等. 葡萄籽提取物对人鼻咽癌细胞HIF-1α表达的影响[J]. 广东医科大学学报,2017,35(4):356−359. [HU J L, ZHANG Y F, SONG J, et al. Effects of grape seed extract on the expression of HIF-1α in human nasopharyngeal carcinoma cells[J]. Journal of Guangdong Medical University,2017,35(4):356−359. doi: 10.3969/j.issn.1005-4057.2017.04.008 [22] 谢佳卿, 赵佳丽, 李爱芳, 等. 葡萄籽原花青素对人骨肉瘤143B细胞的作用及机制研究[J]. 中国细胞生物学学报,2017,39(12):1543−1549. [XIE J Q, ZHAO J L, LI A F, et al. Effects and mechanism of grape seed proanthocyanidins on human osteosarcoma 143B cells[J]. Chinese Journal of Cell Biology,2017,39(12):1543−1549. [23] 于长水, 徐佳元, 王春雷, 等. 葡萄籽原花青素抑制人骨肉瘤MG63细胞增殖的机制研究[J]. 中华骨与关节外科杂志,2019,12(2):141−144. [YU C S, XU J Y, WANG C L, et al. Study on the mechanism of grape seed proanthocyanidins inhibiting the proliferation of human osteosarcoma MG63 cells[J]. Chinese Journal of Bone and Joint Surgery,2019,12(2):141−144. doi: 10.3969/j.issn.2095-9958.2019.02.13 [24] 张慧瑛, 邢芙玲, 罗光宏, 等. 葡萄籽原花青素抑制小鼠B16-F0黑色素瘤细胞黑色素生成的影响[J]. 中药药理与临床,2017,33(1):63−66. [ZHANG H Y, XING F L, LUO G H, et al. Effects of grape seed proanthocyanidins on melanogenesis in B16-F0 melanoma cells of mice[J]. Pharmacology and Clinics of Chinese Materia Medica,2017,33(1):63−66. [25] 石焕焕, 吕程程, 朱运峰. 葡萄籽原花青素对结肠癌细胞抑制作用的初步研究[J]. 中国细胞生物学学报,2019,41(8):1523−1533. [SHI H H, LU C C, ZHU Y F. Preliminary study on the inhibitory effect of grape seed proanthocyanidins on colon cancer cells[J]. Chinese Journal of Cell Biology,2019,41(8):1523−1533. [26] 王海, 连燕娜, 周游, 等. 低聚葡萄籽原花青素联合顺铂对人肺腺癌细胞A549凋亡的影响[J]. 食品科学,2017,38(19):177−181. [WANG H, LIAN Y N, ZHOU Y, et al. Effects of oligomeric grape seed proanthocyanidins combined with cisplatin on apoptosis of human lung adenocarcinoma cell A549[J]. Food Science,2017,38(19):177−181. doi: 10.7506/spkx1002-6630-201719028 [27] 孙英殊, 王雪峰, 何丽霞, 等. 葡萄籽原花青素联合顺铂对喉癌细胞Hep-2生物学作用及机制研究[J]. 临床军医杂志,2017,45(2):176−179. [SUN Y S, WANG X F, HE L X, et al. Study on the biological effects and mechanism of grape seed proanthocyanidins combined with cisplatin on Hep-2 laryngeal carcinoma cells[J]. Clinical Journal of Medical Officer,2017,45(2):176−179. [28] 周世繁, 张娟. 葡萄籽原花青素联合吉西他滨对胰腺癌细胞增殖与凋亡的研究[J]. 中国临床药理学杂志,2018,34(15):1862−1864. [ZHOU S F, ZHANG J. Study of grape seed proanthocyanidin combined with gemcitabine on the proliferation and apoptosis of pancreatic cancer cells[J]. Chinese Journal of Clinical Pharmacology,2018,34(15):1862−1864. [29] 张琳, 马龙, 刘涛, 等. 琐琐葡萄提取物多糖、黄酮对肝癌细胞HepG2的增殖抑制作用[J]. 新疆医科大学学报,2009,32(5):529−532. [ZHANG L, MA L, LIU T, et al. Inhibitory effects of Suosuo grape extract polysaccharides and flavonoids on the proliferation of hepatocellular carcinoma cell HepG2[J]. Journal of Xinjiang Medical University,2009,32(5):529−532. doi: 10.3969/j.issn.1009-5551.2009.05.005 [30] 朱芳成, 毕华强, 赵毅, 等. 乙型肝炎病毒核心蛋白触发人肝癌细胞异常卟啉代谢的机制[J]. 病毒学报,2019,35(4):592−598. [ZHU F C, BI H Q, ZHAO Y, et al. The mechanism of hepatitis B virus core protein triggering abnormal porphyrin metabolism in human liver cancer cells[J]. Acta Virology,2019,35(4):592−598. -
期刊类型引用(5)
1. 王月蓉,赵广河,赵丰丽,覃云斌,陈静,张弘. 脐橙皮水溶性膳食纤维提取工艺优化及其体外益生活性评价. 广西师范大学学报(自然科学版). 2025(01): 101-109 .  百度学术
百度学术
2. 沈康,郭瑞成,徐天旭,王伟华. DEAE-52纤维素柱层析纯化处理对西梅可溶性膳食纤维的影响. 食品与发酵工业. 2024(17): 209-217 .  百度学术
百度学术
3. 卢翠文,欧萍,叶有明,何晓燕,杨东美. 微波辅助酶法提取茶酒糟中可溶性膳食纤维及其抗氧化性能研究. 饲料研究. 2024(20): 75-79 .  百度学术
百度学术
4. 池玉闽,董怡,何强,张文学,向燕,何培君,邓莎,何贵萍,贾利蓉. 油橄榄果肉和核壳中膳食纤维的功能特性分析. 现代食品科技. 2023(05): 157-163 .  百度学术
百度学术
5. 王虎玄,赵天添,王聪,张一凡,朱亚南,孙宏民. 陕北狗头红枣可溶性膳食纤维提取工艺优化及其理化特性与抗氧化活性研究. 陕西科技大学学报. 2022(05): 54-62+99 .  百度学术
百度学术
其他类型引用(2)











 下载:
下载:




 下载:
下载:



