Development of a Ratiometric Fluorescence Sensor for Ascorbic Acid Based on Oxidase-mimicking Activity of CoOOH Nanoflake
-
摘要: 研究建立一种基于羟基氧化钴纳米片(CoOOH)类氧化酶活性的比率荧光传感器,可快速、灵敏、准确地测定抗坏血酸(Ascorbic acid,AA)。在氢氧化钠溶液中,以氯化钴为原料、次氯酸钠为氧化剂,在超声条件下制备具有类氧化酶活性的CoOOH纳米片,并采用透射电子显微镜(TEM)、紫外可见吸收光谱(UV-vis)、X射线衍射(XRD)和傅里叶红外光谱(FT-IR),对所合成的材料表面形貌、光吸收特性、结晶度以及表面基团进行表征,并通过对照试验对所合成的CoOOH纳米片构建比率荧光传感器的可行性进行验证。以检测体系中CoOOH纳米片浓度及孵育时间为单因素,优化检测AA的最佳条件,并建立相应的标准曲线。结果表明,CoOOH纳米片呈典型的纳米级六边形片状,其他表征结果也与以往报道的相符。CoOOH纳米片最佳工作浓度为39.1 μmol/L,最佳孵育时间为25 min。在最优条件下,428 nm处的荧光强度(F428)与568 nm处荧光强度(F568)比值F428/F568与AA浓度在0.5~10.0 μmol/L范围内呈现良好的线性关系,线性方程为y=0.79416x+0.37917(R2=0.9965),检测限303 nmol/L(RSN=3)。将其应用于果汁饮料样品检测,回收率在88.0%~115.9%之间,且检测结果与国家标准方法的检测结果相符。以上结果表明该传感器对检测AA有较好的选择性和准确度,为AA的快速检测提供一种新思路。Abstract: This work aimed at developing a ratiometric fluorescence sensor for sensitive and accurate detection of ascorbic acid (AA) based on oxidase-mimicking activity of CoOOH nanoflake. CoOOH nanoflake with oxidase-like activity was prepared by using CoCl2 as precursor, NaClO as oxidant through a sonication method. The as-synthesized CoOOH nanoflake was characterized by transmission electron microscopy (TEM), UV–vis absorption, X-ray diffraction (XRD), and Fourier transform infrared (FT-IR) spectra. Control experiments were used to demonstrate the feasibility for constructing the radiometric fluorescent sensor using the as-synthesized CoOOH nanoflake. Single-factor experiments were conducted to optimized the optimal concentration of CoOOH nanoflake and incubation time for AA detection. The results showed that the as-synthesized CoOOH nanoflakes exhibited typical hexagonal plate shape, and other characterization results also were consistent with those in previous works. The optimal concentration of CoOOH nanoflake was 39.1 μmol/L, and the optimal incubation time was 25 min. Under the optimal conditions, it was found that F428/F568 linearly correlated with AA concentration from 0.5 to 10.0 μmol/L with correlation coefficients of 0.9965. The regression equation was y=0.79416x+0.37917 (R2=0.9965) with a limit of detection of 303 nmol/L (RSN=3). The recoveries from fruit juice beverage samples spiked with varying concentrations of AA were in the range of 88.0%~115.9%, and analytical results of the sensor were correlated well with those of national standard method of China. These results indicated that the ratiometric fluorescent sensor had excellent selectivity and accuracy for AA detection, creating a new avenue for rapid detection of AA.
-
Keywords:
- ascorbic acid (AA) /
- CoOOH nanoflake /
- ratiometric fluorescence sensor
-
抗坏血酸(Ascorbic acid,AA),又名维生素C,是人体必不可少的微量营养素之一,在许多生化过程中起着关键作用[1]。人体内不能自行合成AA,必须从水果、蔬菜和维生素C片等外来基质摄取。机体缺乏AA将导致多种疾病的发生,例如免疫力低下、坏血病、心脏及脾脏损伤等;相反如果摄入过多可能会破坏维生素B12,导致贫血,儿童易患骨病[2]。因此,AA的测定对于疾病诊断及食品安全具有重要意义。
当前用于AA的分析比技术主要包括比色法[3–5]、荧光分析法[6–8]、电化学分析法[9–11]以及高效液相色谱法[12–14]等。其中,荧光分析法由于其灵敏度高、操作简便、成本低等优势被广泛采用。尤其是近些年纳米材料的快速发展,将纳米材料构建无酶、无标记的荧光传感器用于AA的检测引起了研究者们的广泛兴趣。作为新兴的二维金属氧化物,羟基氧化钴纳米片(CoOOH)在300~700 nm具有广而强的吸收峰,是一种优良的荧光猝灭剂,同时具有类氧化酶活性可与常见的氧化酶底物作用。AA可以还原降解CoOOH纳米片为Co2+使其失去上述两种特性,基于此,当前已有多种基于CoOOH检测AA的荧光传感器报道。例如,Lv等[15]通过在荧光石墨碳氮纳米片表面原位生长CoOOH,CoOOH作为荧光能量受体与石墨碳氮之间产生荧光共振能量转移,使石墨碳氮纳米片的荧光猝灭;而当AA存在时,AA可还原降解CoOOH使石墨碳氮的荧光恢复。将该探针用于细胞提取液AA检测,检测限为0.14 μmol/L。Li等[16]利用CoOOH具有类氧化酶活性,可将对苯二胺(p-Phenylenediamine,p-PD)转化为红棕色的氧化态对苯二胺(p-Phenylenediamine oxidized,p-PDox),而p-PDox可以使碳点的荧光猝灭。当AA浓度不断提高,CoOOH逐渐被还原降解失去类氧化酶活性,p-PDox生成受到抑制,碳点的荧光逐渐增强,该方法对AA的检测限到达0.09 μmol/L。然而,上述两种传感器都是基于单一荧光信号测定的“开-关”或“关-开”策略,假阴性、假阳性风险高,易受其他还原性小分子如多巴胺(Dopamine,DA)、半胱氨酸(Cysteine,Cys)、谷胱甘肽(Glutathione,GSH)的干扰,特异性有待提高。
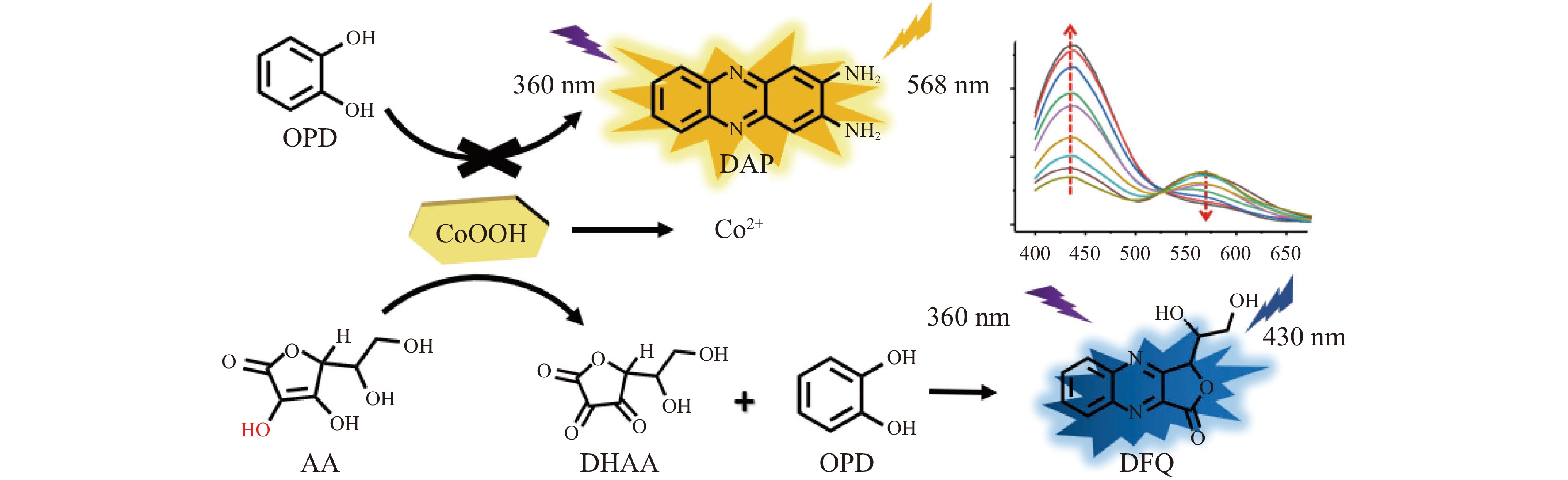
比率型荧光传感器通过记录两个不同发射带荧光强度的比值变化,可以显著地削弱样品、设备等外界条件的影响,从而提高结果的准确性和可靠性[17-18]。而目前基于CoOOH纳米片检测AA的比率荧光传感器未见报道。鉴于此,本文以CoCl2为原料制备CoOOH纳米片,利用CoOOH纳米片具有氧化物酶活性,能将邻苯二胺(o-Phenylenediamine,OPD)转化为荧光物质2,3-二氨基吩嗪(2,3-Diaminophenazine,DAP);而AA可以使CoOOH纳米片还原为Co2+失去类氧化酶活性,抑制DAP的形成;与此同时,AA被氧化为脱氢抗坏血酸(Dehydroascorbic acid,DHAA)遇到剩余的OPD发生缩合反应生成具有荧光的喹喔啉(Quinoxaline,DFQ)。当AA浓度变化时,体系中DAP与DFQ的荧光信号强度F568与F428呈相反变化趋势,从而可利用比率荧光信号(F428/F568)实现对AA更为准确与灵敏地测定(图1所示)。基于上述原理,本文开发了一种可快速、灵敏、选择性检测果汁样品中AA含量的比率荧光传感器,对检测体系中的CoOOH纳米片浓度及孵育时间进行优化,并对传感器的抗干扰性能、准确度以及可靠性进行评价。
1. 材料与方法
1.1 材料与仪器
无水氯化钴(CoCl2)、次氯酸钠(NaClO)、抗坏血酸(AA)、六合水三氯化铁(FeCl3·6H2O) 上海阿拉丁化学有限公司;邻苯二胺(OPD) 上海易恩化学技术有限公司;氢氧化钠 天津市大茂化学试剂厂;盐酸多巴胺 上海麦克林生化科技有限公司;所有试剂均为分析纯;葡萄汁饮料、蜜桃汁饮料、苹果汁饮料等样品 均购于华南农业大学校内或周边超市。
MS 3 basic漩涡混匀振荡器 德国IKA;SpectraMax i3x多功能微孔板检测平台 美国Molecular Devices公司;Evolution 300紫外可见分光光度计 德国Thermo Fisher Scientific公司;Tecnai 12高分辨透射电子显微镜 荷兰FEI;FE28-Standard pH酸度计 德国梅特勒—托利多仪器有限公司。
1.2 实验方法
1.2.1 CoOOH纳米片的制备与表征
1.2.1.1 CoOOH纳米片制备
参照文献[19]报道的方法合成,具体步骤如下:称取129.84 mg的氯化钴溶于100 mL超纯水,得到10.0 mol/L溶液A。称取0.4 g氢氧化钠溶于10 mL超纯水,得到1.0 mol/L溶液B。用超纯水稀释次氯酸钠溶液,得到0.9 mol/L溶液C。将50 mL溶液A和1.5 mL溶液B混合加入离心管中超声反应5 min,将反应后的溶液在4000 r/min条件下离心20 min,弃去上清液;再将沉淀重新分散在50 mL超纯水中,向其加入2.5 mL的溶液C后超声反应20 min,产生棕褐色沉淀,在12000 r/min条件下离心10 min,弃去上清液;用乙醇和超纯水分别洗涤3次。将得到的CoOOH纳米片重新分散到50 mL超纯水得10 mmol/L的CoOOH纳米片溶液备用。
1.2.1.2 透射电镜(TEM)表征
取10 μL CoOOH溶液滴于镀有碳膜的铜网(300目)表面,室温干燥后,于FEI透射电子显微镜下进行表征。
1.2.1.3 紫外-可见光谱测试(UV-Vis)
使用美国Thermo Fisher Scientific公司的Evolution 300紫外-可见分光光度计进行吸光度的测量,测试使用的石英池的光径为1 cm,测试温度为25 ℃。
1.2.1.4 X射线衍射测试(XRD)
将CoOOH溶液冻干后的粉末用研钵研细,称量100 mg样品于X射线粉末衍射仪下进行表征。
1.2.1.5 红外光谱测试(FT-IR)
使用德国Bruker公司的VERTEX 70型傅立叶变换红外光谱仪对样品进行测试(波数范围:0~4000 cm−1)。
1.2.2 比率荧光传感器可行验证
首先,将等体积1 mmol/L的CoOOH纳米片溶液与1 mmol/L的AA混合,比较混合前后CoOOH纳米片溶液的紫外吸收光谱,以验证AA对CoOOH纳米片的还原降解作用。其次,将50 μL的CoOOH纳米片(100 μmol/L),50 μL OPD溶液(5 mmol/L)与50 μL醋酸缓冲溶液(0.2 mol/L,pH4.8),并在360 nm激发下对混合溶液的荧光发射光谱进行扫描,以验证CoOOH纳米片将OPD转化为荧光物质DAP的能力。随后,将50 μL的CoOOH纳米片(100 μmol/L),50 μL OPD溶液(5 mmol/L)与50 μL含50 μmol/L AA的醋酸缓冲溶液(0.2 mol/L,pH4.8)混合,并在360 nm激发下对混合溶液的荧光发射光谱进行扫描,验证AA引发比率荧光响应的能力。
1.2.3 比率荧光传感器的检测条件优化
对传感体系中CoOOH纳米片的量、反应时间进行优化,以达到传感器最佳检测性能。对CoOOH纳米片备用液(10 mmol/L)进行倍比稀释。取不同浓度的CoOOH纳米片稀释液50 μL加入96孔酶标板中,再依次加入50 μL AA(10 μmol/L)、50 μL OPD(5 mmol/L),在37 ℃下温育一段时间后,测定体系的比率荧光值F428/F568的变化,同时用等体积的醋酸盐缓冲液(0.2 mol/L,pH4.8)代替AA作为空白对照。按照式1计算单位AA浓度(10 μmol/L)变化下比率荧光值增长率,探讨实验最佳的CoOOH纳米片浓度。在最佳CoOOH纳米片浓度下,其他条件同上,每镉5 min测定体系比率荧光值,并按式1计算比率荧光值增长率,选取增长率趋于稳定的时间点确定最佳反应时间。
(1) 式中,I0和I1分别代表空白组与存在AA时体系的比率荧光值(F428/F568)。
1.2.4 比率荧光传感器的选择性
考察水果、蔬菜和蔬果汁等实际样品中可能存在的干扰物质,如常见还原性物质、氨基酸和金属离子对检测体系的影响。用醋酸盐缓冲液(pH4.8)配制AA标准溶液(100 μmol/L)和干扰物质溶液:甘氨酸(Glycine,Gly)、盐酸多巴胺(DA)、葡萄糖(GLU)、尿酸(UA)、L-半胱氨酸(Cys)的浓度为200 μmol/L;K+、Na+、Cu2+、Co2+、Ca2+、Al3+、Fe3+的浓度为1 mmol/L。在同等实验条件下,向各干扰物质和AA中依次加入CoOOH纳米片和OPD进行反应并测定体系比率荧光值F428/F568。同时,用该传感器分别测试在100 μmol/L DA、Glu、Cys、UA存在下对100 μmol/L的AA的响应情况。
1.2.5 抗坏血酸的检测
取50 μL终浓度为39.1 μmol/L(备用液稀释256倍)的CoOOH纳米片溶液加入到50 μL浓度为0.0、0.5、1.0、2.0、4.0、6.0、8.0、10.0 μmol/L的AA标准溶液中,再向其中加入50 μL浓度为5 mmol/L的OPD溶液,于37 ℃中温育25 min后用多功能酶标仪的荧光分析模块进行荧光光谱的检测。选取360 nm的激发波长,扫描荧光发射光谱,通过计算体系中两荧光强度的比值F428/F568并以其为纵坐标值,AA浓度为横坐标值构建定量检测AA的标准曲线。
1.2.6 样品处理与加标回收试验
选取葡萄汁、蜜桃汁作为检验样品。参考已报道的文献[6]进行预处理:分别量取各种果汁试样30 mL于50 mL的塑料离心管中,12000 r/min条件下离心10 min,用0.22 μm孔径滤膜对上清液进行过滤。参考果汁中AA的含量,用醋酸盐缓冲液稀释使终浓度在方法检测线性范围,测定果汁中初始AA含量。再通过标准加入法,向样品分别添加1.0、2.0、5.0 μmol/L三个水平的AA,再用该传感器进行测定,计算加标回收率的公式如式(2)所示:
(2) 式中,K0、K1、K2分别代表的是空白测定值、加标量、加标试样测定值。
1.2.7 实际样品检测与仪器确证
随机选取市售果汁饮料5个样品分别用该传感器与食品中AA国家标准检测方法中的荧光法(食品中抗坏血酸的测定GB 5009.86-2016)对其AA含量进行测定,将两种方法的结果进行对比以验证传感器检测实际样品的可靠性。
1.3 数据处理
所有实验数据采用Excel 2016软件进行整理,使用Origin 2017进行分析作图。
2. 结果与分析
2.1 CoOOH纳米片的表征
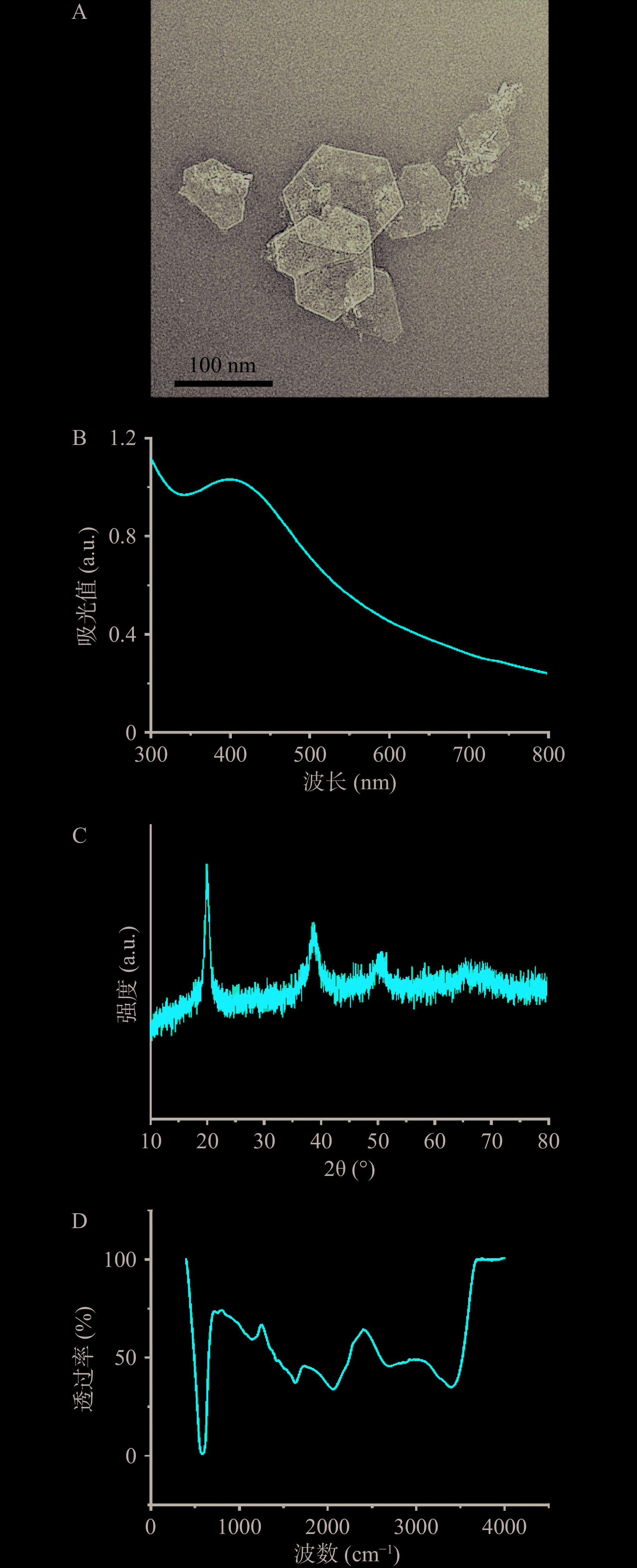
CoOOH纳米片的TEM图如图2A所示,所合成的CoOOH纳米片呈现典型的纳米级六边形片状[19]。紫外可见光谱图(图2B)显示,CoOOH纳米片溶液在300~700 nm范围内有较强的吸收带,并在400 nm左右有特征吸收峰。对CoOOH纳米片冻干粉进行XRD测试,结果如图2C所示,根据标准的JCPDS卡(No.07-0169),图中20.0°、39.2°与50.6°的三个峰分别对应着(003)、(012)、(018)晶面[19],表明合成的CoOOH纳米片具有较高的结晶度;CoOOH纳米片的FT-IR图(图2D)在579 cm−1处有一个强烈的吸收峰是CoOOH特征吸收峰,为Co-O2−与周围氧化物相互作用的峰[20]。上述表征结果表明,CoOOH纳米片合成成功。
2.2 比率荧光传感器可行性验证
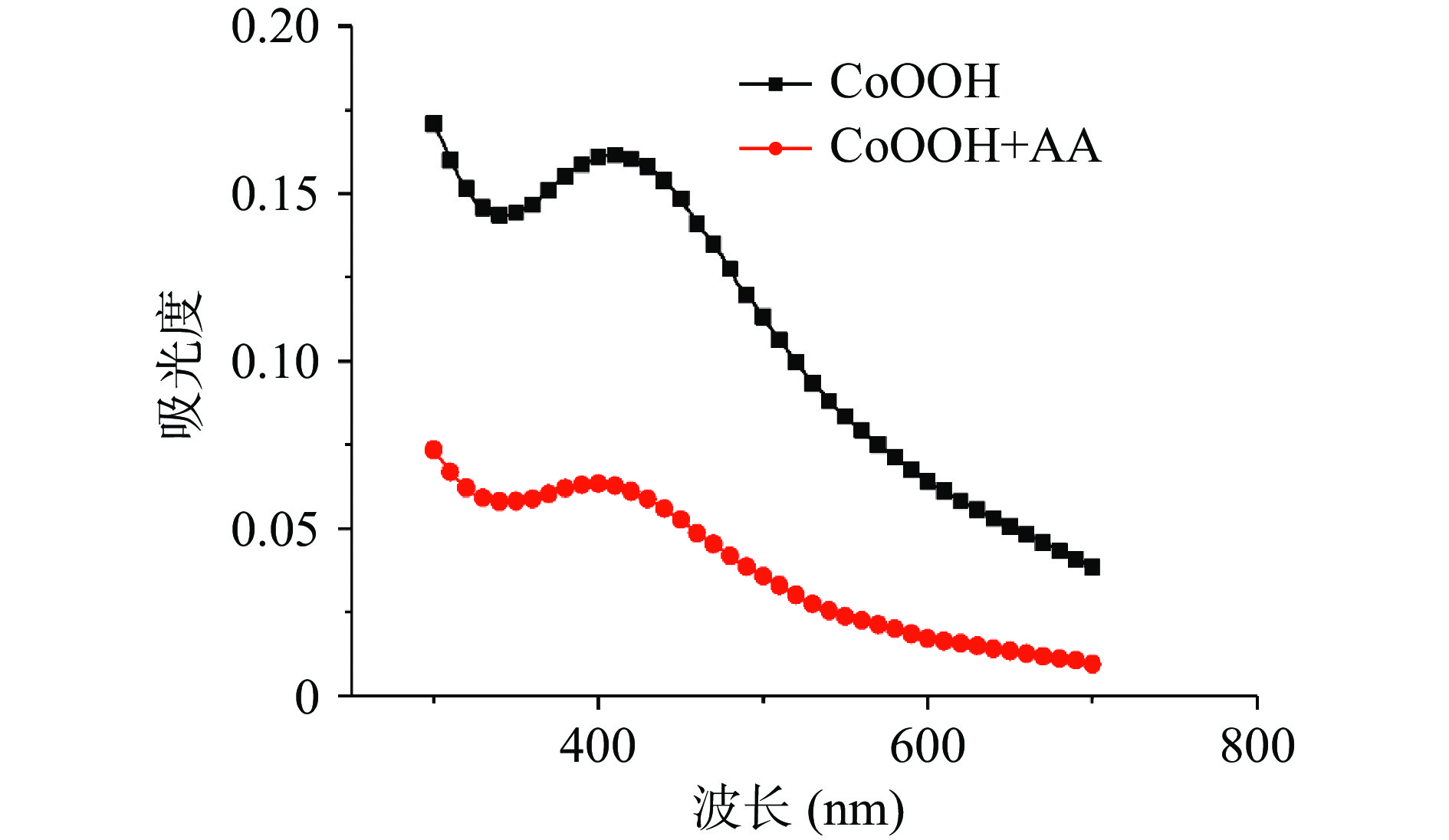
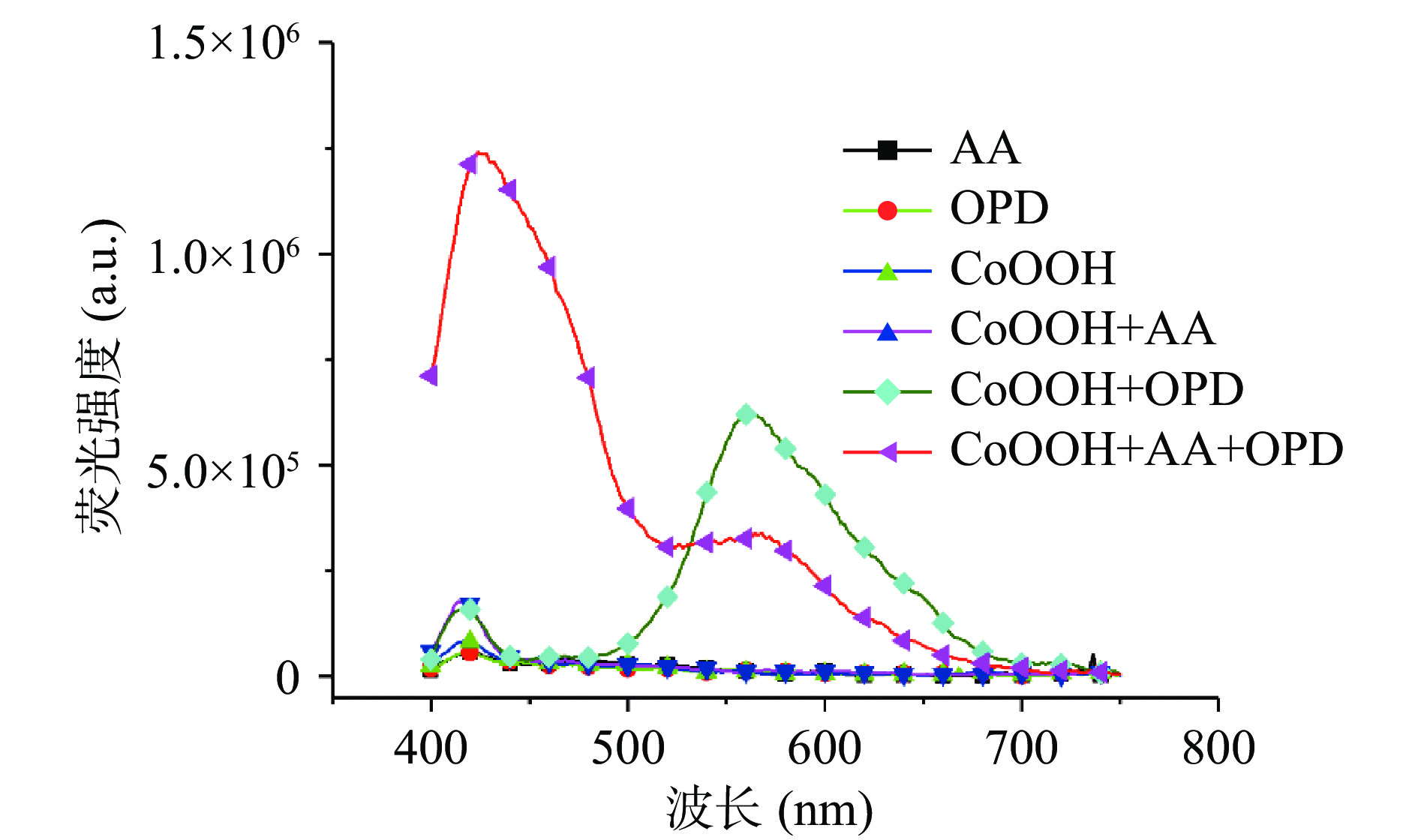
为了探究该比率荧光传感器的可行性,对CoOOH纳米片、AA和OPD之间相互作用的结果进行考察。从图3中可以看到,当AA存在时,CoOOH纳米片在400 nm处的特征吸收峰强度显著下降,这是由于AA可以使CoOOH纳米片还原降解为Co2+,与以往文献报道相符[15-16,20]。单独对AA、OPD、CoOOH纳米片或是CoOOH纳米片与AA混合溶液的荧光光谱进行扫描,均未检测出明显的荧光发射峰,而将CoOOH纳米片与OPD混合,温育5 min后,在568 nm处检测到明显一个荧光发射峰(图4),这与OPD的氧化产物DAP的发射波长相符,证明CoOOH纳米片具有类氧化酶特性[21]。当将CoOOH纳米片与OPD及AA混匀,温育一段时间后,进行荧光光谱扫描。可以观察到试样在568 nm处的荧光强度明显下降,同时在428 nm处检测到一个新的荧光发射峰,这与DHAA和OPD缩合反应生产的典型荧光物质喹喔啉(DFQ)的荧光发射峰波长相符[22]。根据反应CoOOH+AA+2H+→Co2++DHAA+2H2O可知[23],CoOOH纳米片被还原降解为Co2+,AA被氧化成DHAA。因此,将AA、与过量的CoOOH纳米片与OPD混合,AA先与CoOOH纳米片反应生成DHAA,再与OPD反应生成DFQ,残余的CoOOH纳米片将OPD转化为DAP;而随着加入AA浓度增加,CoOOH纳米片被降解的越多,从而导致DAP的生成量减少,相对应的568 nm处荧光强度减弱;同时,DHAA生成量上升,另一荧光产物DFQ增加,428 nm处的荧光强度增强,由此可形成AA浓度依赖的比率荧光响应。上述结果表明该比率荧光传感器原理上是可行的。
2.3 比率荧光传感器的优化
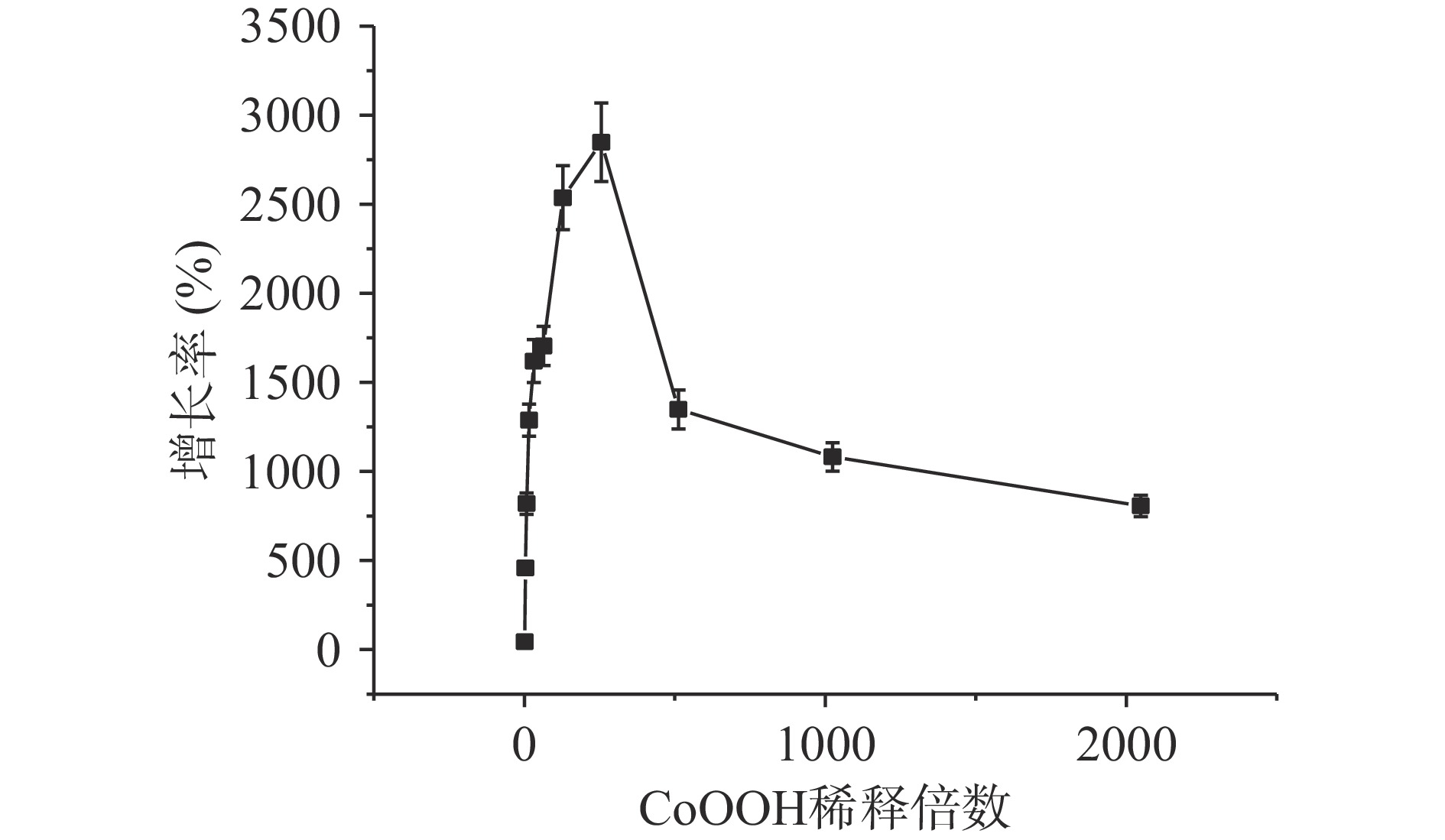
由图5可知,当CoOOH纳米片的稀释倍数小于256倍时,增长率随CoOOH纳米片稀释倍数的增加而增加;当CoOOH纳米片的稀释256倍时,增长率达到了最大值2850%;当CoOOH纳米片的稀释倍数大于256倍时,增长率随CoOOH纳米片稀释倍数的增加而减少。这是由于CoOOH纳米片具有一定的荧光猝灭能力[20,23],CoOOH纳米片浓度过高,AA虽然能够充分反应完转化为DFQ,但是DFQ的荧光会被过多的CoOOH纳米片所猝灭,导致F428上升并不会很明显,所以F428/F568增长率不会最高。而如果CoOOH纳米片浓度太低,AA不能充分反应完转化为DFQ,亦不能到达最高比率荧光信号增长率。因此,选择浓度为39.1 μmol/L的CoOOH纳米片用于AA检测。
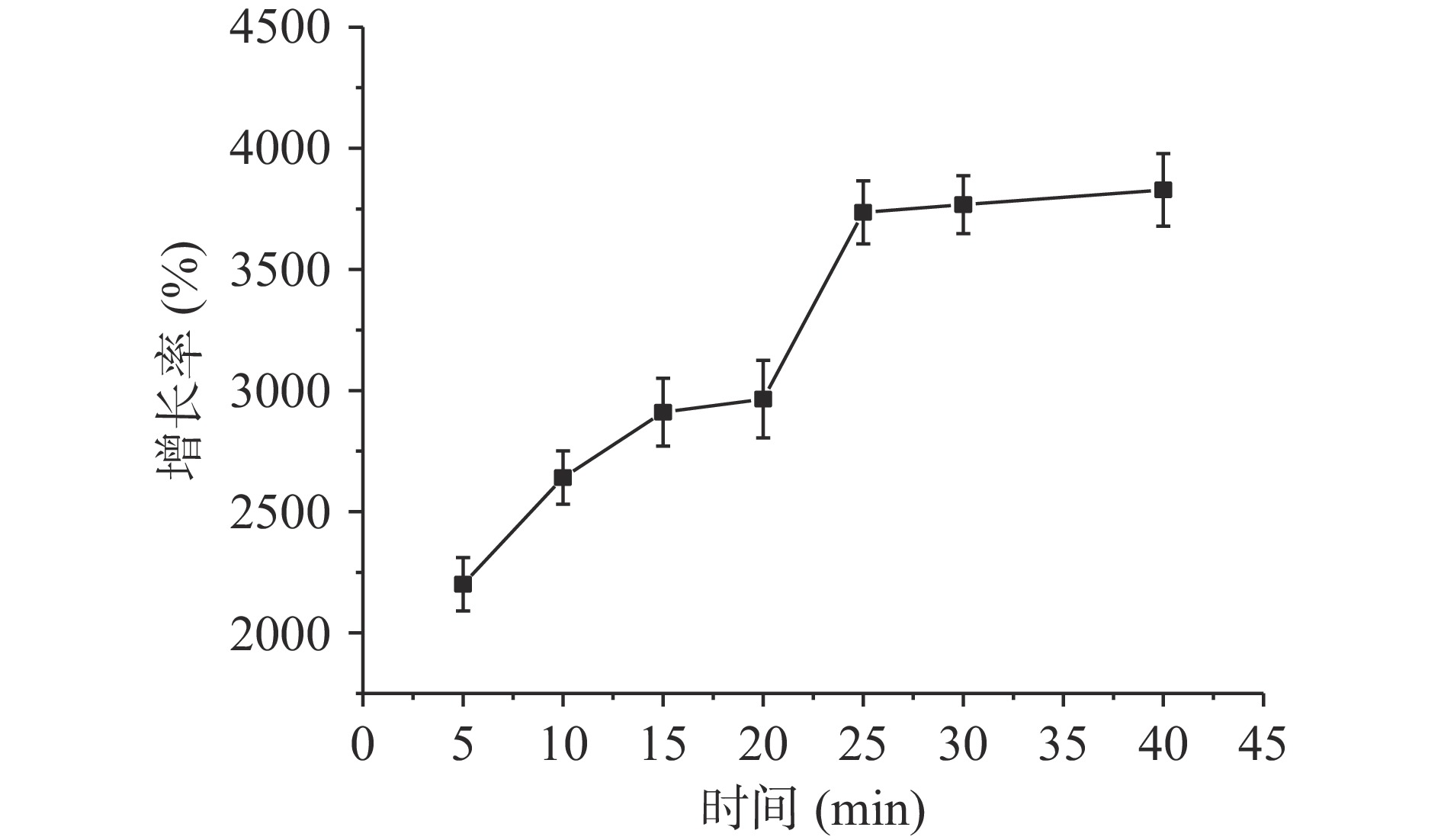
对传感体系的反应时间进行优化,由图6可知,当反应时间小于25 min,体系的比率荧光值增长率随时间的增加而增加;当反应超过25 min后,增长率减缓,说明此时体系中反应物基本上已经反应完毕,故取25 min作为体系反应时间。
2.4 比率荧光传感器对AA的选择性
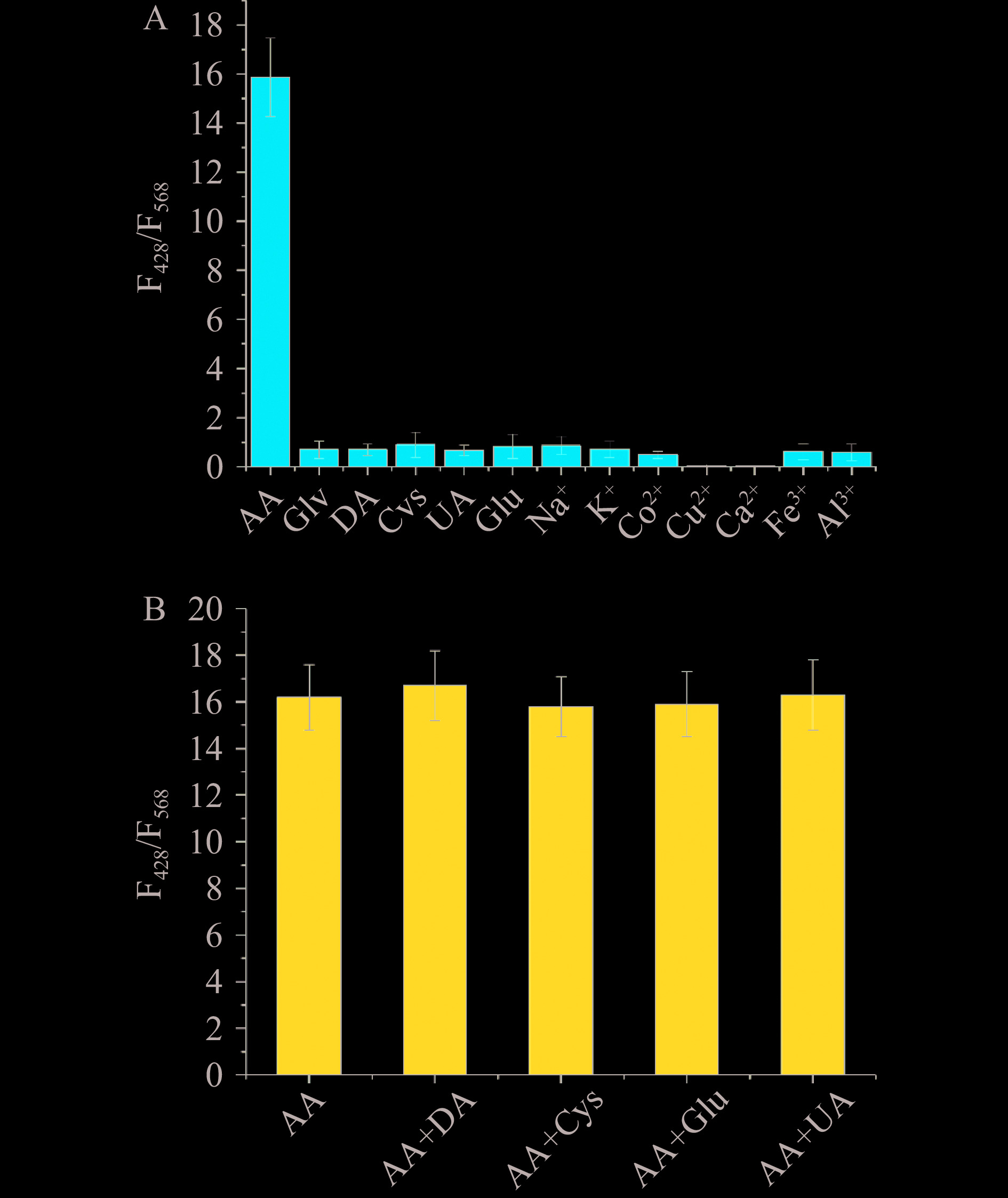
选择性是确保传感器准确、可靠的前提。如图7A所示该传感器对100 μmol/L的AA产生明显的响应信号,比率荧光值F428/F568达到15.9,而对于浓度为200 μmol/L葡萄糖(Glu)、尿酸(UA)、甘氨酸(Gly)、多巴胺(DA)、半胱氨酸(Cys),以及浓度为1 mmol/L的常见金属离子,如Na+、Ka+、Cu2+等,该传感器的响应很弱,F428/F568均小于0.9,表明该传感器对AA具有强的选择性。这可归因于CoOOH纳米片是一种对AA选择性好的识别材料;AA的烯二醇基团可以还原CoOOH纳米片降解为Co2+。虽然DA、Cys、UA、Glu等也具有还原性,但是与CoOOH纳米片氧化还原反应的活性相对慢很多[23],即使这些还原物质在短时间内可以少量还原CoOOH纳米片,对568 nm处的荧光强度F568略有影响,但是其氧化产物不会像DHAA那样与OPD反应,F428的强度不受影响。因此,该比率荧光传感器与同样利用AA还原降解CoOOH纳米片,基于单一荧光信号测定的“开-关”或“关-开”荧光传感器相比[15-16],对这些同样具有还原性的小分子具有更强抗干扰能力。如图7B所示,即使存在相当浓度这些还原物质(100 μmol/L),该比率荧光传感体系对AA的响应无显著性差别。
2.5 标准曲线与检出限
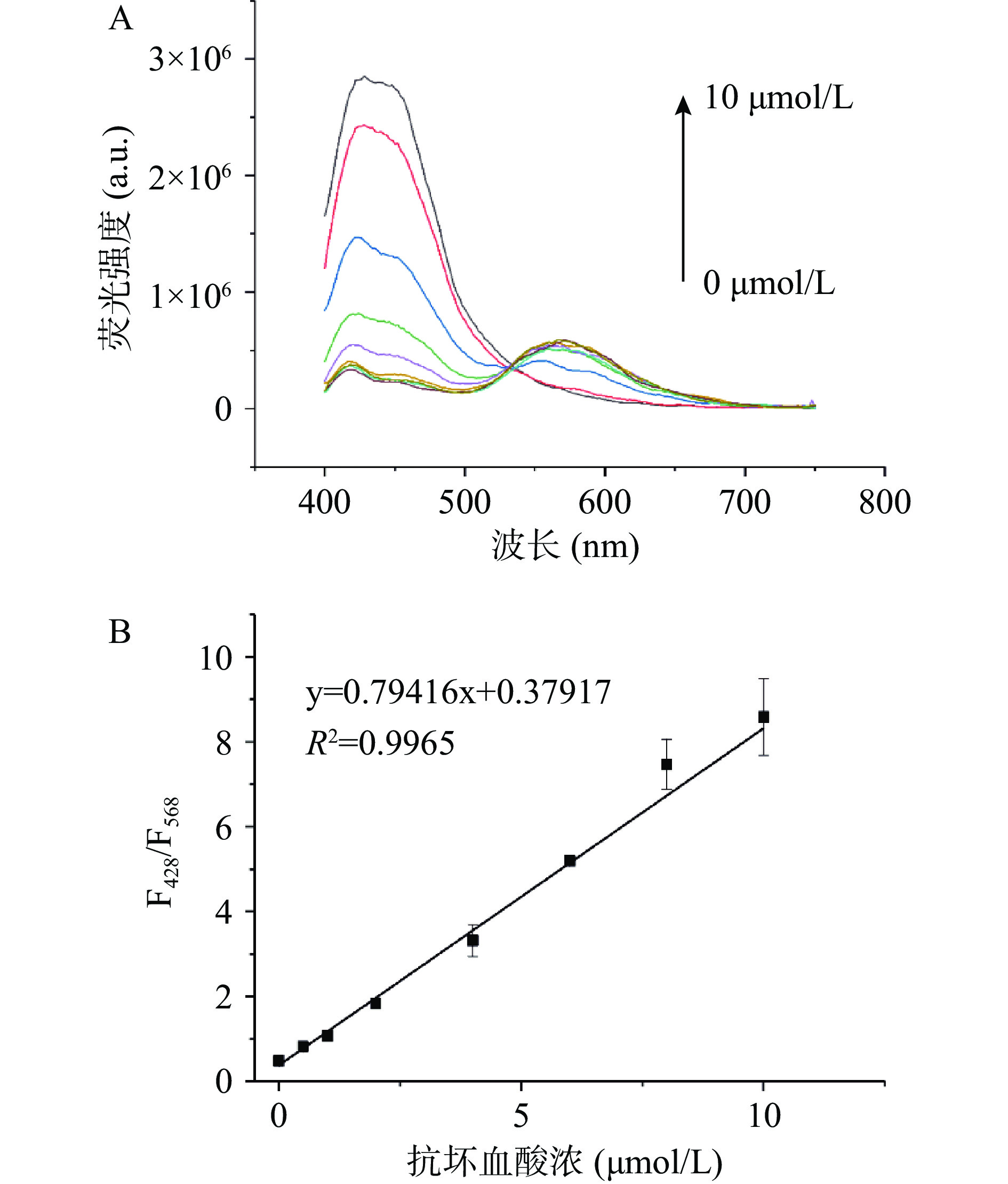
在最佳实验条件下,通过荧光光谱记录了AA在0~10 μmol/L浓度范围内,引起的体系荧光强度的变化。根据检测结果,建立了F428/F568与AA浓度的标准曲线。结果如图8所示,可以看出随着AA浓度的増加,428 nm处的荧光强度逐渐上升,568 nm处的荧光强度逐渐下降(图8A),体系比率荧光值F428/F568相应上升,且与AA浓度在0.5~10.0 μmol/L范围内的AA有着良好的线性关系(图8B),线性回归方程式为:y=0.79416x+0.37917(其中y表示比率荧光值F428/F568,x表示AA的浓度),定量限为500 nmol/L(S/N=10),检测限达到303 nmol/L(S/N=3)。与前期报道的一些检测AA的比色或荧光分析方法相比,该方法具相当的甚至更高的检测灵敏度(表1所示)。
2.6 加标回收试验与实际样品中AA的检测
为了验证该传感器的准确性,本研究选取了市售的葡萄汁、蜜桃汁,进行加标回收试验。将前处理得到的果汁饮料稀释液分别分成四份,分别向其添加0.0、1.0、2.0、5.0 μmol/L的AA,用所建立的比率荧光传感器进行检测。添加回收结果显示该传感器对两种果汁中AA的测定,回收率在88.0%~115.9%之间(表2所示),表明本研究所建立的比率荧光传感器具有较好的准确性。同时,为验证所建立传感器检测实际样品的可靠性,采用国家标准方法(GB-5009.86-2016)中的荧光法对传感器的检测结果进行验证。如表3所示,该比率荧光传感器对随机选取的市售果汁饮料中AA的检测结果与国家标准方法所得结果具有较好的一致性,表明该传感器用于AA检测可靠性强,可用于实际样品中AA的测定。
表 2 果汁样品中抗坏血酸的检测结果与加标回收率(n=3)Table 2. Recoveries of AA from different fruit juice samples by the proposed sensor (n=3)样品名称 检测量(μmol/L) 加标浓度(μmol/L) 实测量(μmol/L) 回收率(%) 蜜桃汁饮料 0.91 1.0 1.81 90.3 2.0 3.00 104.6 5.0 5.68 95.5 葡萄汁饮料 1.33 1.0 2.21 88.0 2.0 3.64 115.9 5.0 6.62 105.9 表 3 实际样品中抗坏血酸的检测Table 3. Determination of ascorbic acid in real samples样品 比率荧光传感器
(μmol/L)荧光法(GB 5009.86-2016)
(μmol/L)橙汁饮料 447 433 葡萄汁饮料 104 108 蜜桃汁饮料 143 137 桑葚汁饮料 87.6 89.8 柠檬汁饮料 442 427 3. 结论
本研究构建了一种基于CoOOH纳米片氧化酶活性测定AA的比率荧光传感器。以氯化钴为原料制备了一种具有类氧化酶活性的CoOOH纳米片。以检测体系CoOOH纳米片浓度及孵育时间为单因素,优化得到检测AA的最佳条件为CoOOH纳米片最佳工作浓度为39.1 μmol/L,最佳孵育时间为25 min。在最优条件下该传感器对0.5~10 μmol/L的AA具有线性响应,定量限与检测限分别为500与303 nmol/L。选择性试验结果表明,常见金属离子及具有还原性的干扰物对该传感器没有显著影响,说明该传感器具有好的选择性及抗干扰能力。用于果汁饮料样品中AA的测定,回收率在88.0%~115.9%,且检测结果与国际标准方法的检测结果具有较好的一致性,表明该传感器用于实际样品检测具有好的准确性与可靠性。总之,本研究所构建的比率荧光传感器具有成本低廉、操作简便、灵敏度高、选择性好等优点,为快速、准确测定AA提供新的可能。
-
表 1 不同AA测定方法检测性能比较
Table 1 Comparison of the performance of different AA probing strategy
表 2 果汁样品中抗坏血酸的检测结果与加标回收率(n=3)
Table 2 Recoveries of AA from different fruit juice samples by the proposed sensor (n=3)
样品名称 检测量(μmol/L) 加标浓度(μmol/L) 实测量(μmol/L) 回收率(%) 蜜桃汁饮料 0.91 1.0 1.81 90.3 2.0 3.00 104.6 5.0 5.68 95.5 葡萄汁饮料 1.33 1.0 2.21 88.0 2.0 3.64 115.9 5.0 6.62 105.9 表 3 实际样品中抗坏血酸的检测
Table 3 Determination of ascorbic acid in real samples
样品 比率荧光传感器
(μmol/L)荧光法(GB 5009.86-2016)
(μmol/L)橙汁饮料 447 433 葡萄汁饮料 104 108 蜜桃汁饮料 143 137 桑葚汁饮料 87.6 89.8 柠檬汁饮料 442 427 -
[1] WANG C, PAN C, WEI Z, et al. Bionanosensor based on N-doped graphene quantum dots coupled with CoOOH nanosheets and their application for in vivo analysis of ascorbic acid[J]. Analytica Chimica Acta,2020,1100:191−199. doi: 10.1016/j.aca.2019.11.008
[2] YANG J, MA Q, HUANG F, et al. A New Fluorimetric method for the determination of ascorbic acid[J]. Analytical Letters,1998,31(15):2757−2766. doi: 10.1080/00032719808005341
[3] CHEN H, LIU Y, LI H, et al. Non-oxidation reduction strategy for highly selective detection of ascorbic acid with dual-ratio fluorescence and colorimetric signals[J]. Sensors and Actuators, 2019, 281: 983−988.
[4] ZHANG Y, ZHAI J L, LI F L, et al. Green synthesis of gold nanoparticles and their application in colorimetric detection of vitamin C[J]. Chinese Journal of Analytical Chemistry,2020,48:1041−1049.
[5] ZHUO S J, FANG J, LI M, et al. Manganese (II)-doped carbon dots as effective oxidase mimics for sensitive colorimetric determination of ascorbic acid[J]. Microchimica Acta,2019,186(12):1−8.
[6] LIU J J, CHEN Y L, WANG W F, et al. "Switch-On" fluorescent sensing of ascorbic acid in food samples based on carbon quantum dots-MnO2 probe[J]. Journal of Agricultural and Food Chemistry,2016,64:371−380. doi: 10.1021/acs.jafc.5b05726
[7] NA W, Li N, SU X. Enzymatic growth of single-layer MnO2 nanosheets in situ: Application to detect alkaline phosphatase and ascorbic acid in the presence of sulfanilic acid functionalized graphene quantum dots[J]. Sensors and Actuators B-Chemical,2018,274:172−179. doi: 10.1016/j.snb.2018.07.116
[8] LIU J J, CHEN Z T, TANG D S, et al. Graphene quantum dots-based fluorescent probe for turn-on sensing ascorbic acid[J]. Sensors Actuators B Chemical,2015,212:214−219. doi: 10.1016/j.snb.2015.02.019
[9] BERGOI I, ARNAU P R, DMITRY B, et al. Electrochemical detection of ascorbic acid in artificial sweat using a flexible alginate/CuO-modified electrode[J]. Microchimica Acta,2020,187(9):3231−223.
[10] CHARLTON H, BONGIWE S, ERIC G, et al. Simultaneous detection of paracetamol, ascorbic acid, and caffeine using a bismuth-silver nanosensor[J]. Electroanalysis,2020,32(12):3098−3107. doi: 10.1002/elan.202060389
[11] 纪文亮, 张美宁, 毛兰群. 鼠脑中维生素C活体电化学分析研究进展[J]. 分析化学,2019,47(10):1559−1571. [JI W L, ZHANG M N, MAO L Q, et al. Recent advances on in vivo electrochemical analysis of vitamin C in rat brain[J]. Chinese Journal of Analytical Chemistry,2019,47(10):1559−1571. [12] ATTILA S, SZENDE V, ISTVÁN K, et al. Quantification of plasma and leukocyte vitamin C by high performance liquid chromatography with mass spectrometric detection[J]. Journal of Analytical Chemistry,2020,75(9):1168−1176. doi: 10.1134/S1061934820090038
[13] 赵伟曼, 吕慧娟, 杨伟汉, 等. 高效液相色谱法测定可溶微针贴片中维生素C的含量[J]. 山西医科大学学报, 2019, 50(5): 632−635 ZHAO W M, LYU H J, YANG W H, et al. Determination of vitamin C in dissolving microneedles by high performance liquid chromatography[J] Journal of Shanxi Medical University, 2019, 50(5): 632−635.
[14] 李玉彩, 李响明, 周永妍, 等. RP-HPLC测定含银杏叶提取物的注射液中维生素C的含量[J]. 中国现代中药, 2019, 21(3): 380−382,389 LI Y C, LI X M, ZHOU Y Y, et al. Determination of vitamin C in injection containing ginkgo leaves extract by RP-HPLC[J] Modern Chinese Medicine, 2019, 21(3): 380−382,389.
[15] LV Y, JIANG C, HU K, et al. In-situ growth of cobalt oxyhydroxide on graphitic-phase C3N4 nanosheets for fluorescence turn-on detection and imaging of ascorbic acid in living cells[J]. Microchimica Acta,2019,186(6):360. doi: 10.1007/s00604-019-3487-5
[16] LI N, ZHONG Y Q, LIU S G, et al. Smartphone assisted colorimetric and fluorescent triple-channel signal sensor for ascorbic acid assay based on oxidase-like CoOOH nanoflakes[J]. Spectrochimica Acta Part a-Molecular and Biomolecular Spectroscopy,2020:238.
[17] LUO L, SONG Y, ZHU C, et al. Fluorescent silicon nanoparticles-based ratiometric fluorescence immunoassay for sensitive detection of ethyl carbamate in red wine[J]. Sensors and Actuators B-Chemical,2018,255:2742−9. doi: 10.1016/j.snb.2017.09.088
[18] ARAFEH B, FOROUGH G, SAMIRA A, et al. Ratiometric fluorescent nanoprobes for visual detection: Design principles and recent advances - A review[J]. Analytica Chimica Acta,2019,1079:30−58. doi: 10.1016/j.aca.2019.06.035
[19] WEN S H, ZHONG X L, WU Y D, et al. Colorimetric assay conversion to highly sensitive electrochemical assay for bimodal detection of arsenate based on cobalt oxyhydroxide nanozyme via arsenate absorption[J]. Analytical Chemistry,2019,91(10):6487−97. doi: 10.1021/acs.analchem.8b05121
[20] LI H, JIN R, KONG D, et al. Switchable fluorescence immunoassay using gold nanoclusters anchored cobalt oxyhydroxide composite for sensitive detection of imidacloprid[J]. Sensors and Actuators B-Chemical,2019,283:207−14. doi: 10.1016/j.snb.2018.12.026
[21] LIU S G, HAN L, LI N, et al. A fluorescence and colorimetric dual-mode assay of alkaline phosphatase activity via destroying oxidase-like CoOOH nanoflakes[J]. Journal of Materials Chemistry B,2018,6(18):2843−50. doi: 10.1039/C7TB03275G
[22] CHUNG H K, INGLE J D. Fluorimetric kinetic method for the determination of total ascorbic acid with o-phenylenediamine[J]. Analytica Chimica Acta,1991,243:89−95. doi: 10.1016/S0003-2670(00)82544-1
[23] LI L, WANG C, LIU K, et al. Hexagonal cobalt oxyhydroxide-carbon dots hybridized surface: highly sensitive fluorescence turn-on probe for monitoring of ascorbic acid in rat brain following brain ischemia[J]. Analytical Chemistry,2015,87(6):3404−11. doi: 10.1021/ac5046609
[24] TAN H, MA C, GAO L, et al. Metal–Organic framework-derived copper nanoparticle@carbon nanocomposites as peroxidase mimics for colorimetric sensing of ascorbic acid[J]. Chemistry–A European Journal,2014,20(49):16377−16383. doi: 10.1002/chem.201404960
[25] DARABDHARA G, SHARMA B, DAS M R, et al. Cu-Ag bimetallic nanoparticles on reduced graphene oxide nanosheets as peroxidase mimic for glucose and ascorbic acid detection[J]. Sensors and Actuators B: Chemical,2017,238:842−851. doi: 10.1016/j.snb.2016.07.106
[26] GAO C, ZHU H, CHEN J, et al. Facile synthesis of enzyme functional metal-organic framework for colorimetric detecting H2O2 and ascorbic acid[J]. Chinese Chemical Letters,2017,28(5):1006−1012. doi: 10.1016/j.cclet.2017.02.011
[27] ZHU J, ZHAO Z, LI J, et al. Fluorescent detection of ascorbic acid based on the emission wavelength shift of CdTe quantum dots[J]. Journal of Luminescence,2017,192:47−55. doi: 10.1016/j.jlumin.2017.06.015
[28] WANG X, LONG C, JIANG Z, et al. In situ synthesis of fluorescent copper nanoclusters for rapid detection of ascorbic acid in biological samples[J]. Analytical Methods,2019,11(36):4580−4585. doi: 10.1039/C9AY01627A
[29] YAN X, He L, ZHOU C, et al. Fluorescent detection of ascorbic acid using glutathione stabilized Au nanoclusters[J]. Chemical Physics,2019,522:211−213. doi: 10.1016/j.chemphys.2019.03.008
[30] MA X, LIN S, DANG Y, et al. Carbon dots as an “on-off-on” fluorescent probe for detection of Cu (II) ion, ascorbic acid, and acid phosphatase[J]. Analytical and Bioanalytical Chemistry,2019,411(25SI):6645−6653.
[31] LIU X, TIAN M, LI C, et al. Polyvinylpyrrolidone-stabilized Pt nanoclusters as robust oxidase mimics for selective detection of ascorbic acid[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects,2021,625:126985. doi: 10.1016/j.colsurfa.2021.126985
-
期刊类型引用(5)
1. 王月蓉,赵广河,赵丰丽,覃云斌,陈静,张弘. 脐橙皮水溶性膳食纤维提取工艺优化及其体外益生活性评价. 广西师范大学学报(自然科学版). 2025(01): 101-109 .  百度学术
百度学术
2. 沈康,郭瑞成,徐天旭,王伟华. DEAE-52纤维素柱层析纯化处理对西梅可溶性膳食纤维的影响. 食品与发酵工业. 2024(17): 209-217 .  百度学术
百度学术
3. 卢翠文,欧萍,叶有明,何晓燕,杨东美. 微波辅助酶法提取茶酒糟中可溶性膳食纤维及其抗氧化性能研究. 饲料研究. 2024(20): 75-79 .  百度学术
百度学术
4. 池玉闽,董怡,何强,张文学,向燕,何培君,邓莎,何贵萍,贾利蓉. 油橄榄果肉和核壳中膳食纤维的功能特性分析. 现代食品科技. 2023(05): 157-163 .  百度学术
百度学术
5. 王虎玄,赵天添,王聪,张一凡,朱亚南,孙宏民. 陕北狗头红枣可溶性膳食纤维提取工艺优化及其理化特性与抗氧化活性研究. 陕西科技大学学报. 2022(05): 54-62+99 .  百度学术
百度学术
其他类型引用(2)





 下载:
下载:


 下载:
下载:



