Protective Effects of British Red Kidney Bean Antioxidant Peptide Components on H2O2 Induced Oxidative Stress Damage in PC12 Cells
-
摘要: 为了探究英国红芸豆抗氧化肽组分的抗氧化作用,采用超滤、葡聚糖凝胶G-15层析技术对碱性蛋白酶酶解英国红芸豆抗氧化蛋白质制备的抗氧化产物进行分级,研究抗氧化活性较高的组分对H2O2损伤的PC12细胞的影响。结果表明:抗氧化肽组分BRKBAPC-2能缓解H2O2对PC12造成的细胞生长抑制作用,随着肽浓度的提高,细胞内活性氧(ROS)水平,丙二醛(MDA)含量及乳酸脱氢酶(LDH)胞外活力均有所降低,超氧化物歧化酶(SOD)、过氧化氢酶(CAT)活力以及还原型谷胱甘肽(GSH)含量均具有所提高,尤其BRKBAPC-2浓度为200 μg/mL时,ROS水平为32.53%,MDA含量为0.96 nmol/μg prot,LDH胞外活力为202.12 U/L,与模型组相比,均极显著降低(P<0.01);SOD活力为(555.48±3.64)U/mg prot,CAT活力为(14.77±1.30)U/mL,GSH含量为(140.88±8.19)μmol/g prot,与模型组相比,均极显著提高(P<0.01),此外,其可抑制线粒体膜电位的降低,改善细胞周期的阻滞情况,阻止细胞凋亡关键酶Caspase-3和Caspase-9的激活。可见,抗氧化肽组分BRKBAPC-2对H2O2引起的PC12细胞氧化损伤具有一定的保护作用。Abstract: In order to explore the antioxidant effect of the British red kidney bean antioxidant peptide components, ultrafiltration and dextran gel G-15 chromatography technology were used to classify the antioxidant products prepared by alkaline protease enzymatic hydrolysis of the British red kidney bean antioxidant protein, and the effect of components with higher antioxidant activity on PC12 cells damaged by H2O2 was studied. The results showed that the antioxidant peptide component BRKBAPC-2 could alleviate the cell growth inhibitory effect of H2O2 on PC12. With the increasing of peptide concentration, the level of intracellular reactive oxygen species (ROS) levels, malondialdehyde (MDA) content and lactate dehydrogenase (LDH) extracellular activity were all reduced, the activity of superoxide dismutase (SOD), catalase (CAT) and the content of reduced glutathione (GSH) were all increased, especially when the concentration of BRKBAPC-2 was 200 μg/mL, ROS level was 32.53%, MDA content was 0.96 nmol/μg prot, LDH extracellular activity was 202.12 U/L, compared with the model group, they were significantly reduced (P<0.01). SOD activity was (555.48±3.64) U/mg prot, CAT activity was (14.77±1.30) U/mL, and GSH content was (140.88±8.19) μmol/g prot, compared with the model group, they were significantly improved (P<0.01). In addition, the BRKBAPC-2 with 200 μg/mL could inhibite the decrease of mitochondrial membrane potential, improve cell cycle resistance, prevent the activation of the key enzymes Caspase-3 and Caspase-9 of cell apoptosis. It could be seen that the antioxidant peptide component BRKBAPC-2 had a certain protective effect on the oxidative damage of PC12 cells caused by H2O2.
-
芸豆是世界上种植面积仅次于大豆的食用豆类作物,在我国东北、华北、西北和西南的高寒、冷凉地区均有种植[1]。英国红芸豆粒色紫红,蛋白质含量约为22%左右,含有人体所需的8种必需氨基酸,是营养价值较高的植物蛋白源[2]。
氧化应激是指机体在受到刺激时,体内自由基增加或机体抗氧化能力减弱,导致氧化-抗氧化系统失衡[3],从而积累过多的活性(ROS),如过氧化氢(H2O2)、超氧阴离子和羟自由基[4]。ROS会损伤核酸、蛋白质和脂质等生物大分子[5],导致动脉粥样硬化[6]、阿尔兹海默症[7]、糖尿病[8]、炎症[9]以及衰老[10]的发生。
生物活性肽因具有较强的生物活性和很高的生物安全性而成为国内外的研究热点。抗氧化肽是指具有抗氧化功能的生物活性肽,由于具有分子量小、生物活性高、抗原性低、易吸收等特点而被广泛研究[11-12]。大量研究表明,食源性蛋白酶解物如小麦胚芽水解物、乳清蛋白酶解物、蛋清源活性肽以及核桃水解肽等通过体外细胞试验探究了其抗氧化作用机制[13-16]。
团队在前期研究了英国红芸豆抗氧化肽组分在体外的抗氧化活性[17],本研究拟将英国红芸豆抗氧化肽组分进行超滤、葡聚糖凝胶G-15层析分离纯化,将活性较高的组分作用于PC12细胞,探究英国红芸豆抗氧化肽组分对H2O2诱导PC12细胞氧化应激损伤的保护作用,以期进一步阐明英国红芸豆抗氧化肽的抗氧化作用机制,为英国红芸豆抗氧化肽在食品保健及医药领域的应用提供理论依据。
1. 材料与方法
1.1 材料与仪器
英国红芸豆 黑龙江八一农垦大学国家杂粮工程技术研究中心提供;英国红芸豆抗氧化肽组分(British red kidney bean antioxidant peptide components,BRKBAPC) 制备方法见参考文献[17];PC12细胞 上海制备生物科技有限公司;过氧化氢 分析纯,国药集团化学试剂有限公司;VC 超纯级,Bomeibio公司;DMEM高糖液体培养基、磷酸盐缓冲液(PBS) Biosharp公司;青/链霉素、四唑盐(MTT)、线粒体膜电位检测试剂盒(JC-1) Solarbio公司;胎牛血清(FBS)、胰蛋白酶消化液 美国Gibco公司;二甲基亚砜(DMSO) 美国Sigma公司;活性氧(ROS)测定试剂盒、BCA蛋白质浓度测定试剂盒、丙二醛(MDA)测定试剂盒、乳酸脱氢酶(LDH)测定试剂盒、超氧化物歧化酶(SOD)活性测定试剂盒、过氧化氢酶(CAT)活性测定试剂盒、还原型谷胱甘肽(GSH)测定试剂盒 南京建成生物工程研究所;Caspase-3活性检测试剂盒、Caspase-9活性检测试剂盒、细胞周期与细胞凋亡检测试剂盒 碧云天生物技术研究所。
CBS-170 CO2培养箱 德国Binder公司; XDS-1系列倒置生物显微镜 重庆重光实业有限公司;Cf72-8YW酶联免疫检测仪 珀金埃尔默仪器有限公司;FACS Calibvr型流式细胞仪 美国贝克曼公司;2J1-0013紫外可见分光光度计 日本HITACHI公司。
1.2 实验方法
1.2.1 英国红芸豆抗氧化肽组分的分级分离
按照参考文献[17]的方法制备抗氧化肽组分并对其进行超滤分级,在前期研究中,发现小于1 kDa的组分抗氧化活性最强。本研究采用Sephadex G-15柱层析对小于1 kDa的抗氧化肽组分进一步分离,凝胶柱规格1 cm×40 cm,上样量2 mL,质量浓度0.1 g/mL,以蒸馏水为流动相,流速1 mL/min,洗脱5 h,在220 nm波长下检测出峰情况,收集不同出峰时间的组分,冷冻干燥备用。采用Collection Microsoft软件进行数据分析,计算峰面积。
1.2.2 PC12细胞培养及分组
将PC12细胞接种于含10%的胎牛血清、1%的青/链霉素的DMEM完全培养基中,置于37 ℃、5% CO2的饱和湿度恒温培养箱中培养,待细胞数量达到80%~90%后,吸去培养液,用pH为7.4的PBS冲洗两次,加入1 mL胰蛋白酶消化1 min,进行传代培养。将状态良好的对数生长期PC12细胞接种于培养板中,并对其进行分组。空白组(只加入DMEM完全培养基)、模型组(加入等量的DMEM完全培养基24 h后,加入H2O2溶液刺激4 h)、样品组(加入低剂量、中剂量、高剂量的英国红芸豆抗氧化肽组分干预24 h后,加入H2O2溶液刺激4 h)、阳性对照组(加入VC干预24 h后,加入H2O2溶液刺激4 h)。
1.2.3 H2O2诱导PC12细胞氧化应激损伤模型的建立
将对数生长期生长状态良好的PC12细胞按照1.0×105 个/mL接种于96孔培养板中,每孔200 μL,置于37 ℃、5% CO2的培养箱中培养24 h,按照1.2.2中空白组和模型组(H2O2终浓度分别为125、250、500、1000、2000、4000 μmol/L)处理细胞后,每孔加入MTT(终浓度为5 mg/mL),继续孵育4 h,小心吸出上清培养液,每孔加入150 μL DMSO,充分震荡10 min。以490 nm为试验波长,630 nm为参比波长,用酶标仪测定吸光值,计算细胞存活率。
(1) 1.2.4 抗氧化肽组分及VC浓度对H2O2诱导PC12细胞损伤作用的影响
细胞培养同1.2.3,按照1.2.2中空白组、模型组、样品组以及阳性对照组(抗氧化肽组分终浓度和VC终浓度都为5、10、25、50、100、200、250、500、1000 μg/mL)处理细胞后,按1.2.3方法测定并计算细胞存活率。
1.2.5 利用MTT法分析抗氧化肽组分对PC12细胞的毒性
细胞培养同1.2.3并按照1.2.2中空白组、(低、中、高剂量)样品组处理细胞(样品组不用加入H2O2溶液刺激细胞)后,按1.2.3方法测定并计算细胞存活率。
1.2.6 抗氧化肽组分对H2O2诱导PC12细胞的氧化因子以及抗氧化水平的影响
细胞培养同1.2.3,并按照1.2.2中细胞分组处理细胞后,小心吸出100 μL上清培养液,加入新的96孔板中,按照试剂盒说明书测定氧化因子LDH活力。
细胞培养同1.2.3,但接种于6孔板中,并按照1.2.2中细胞分组处理细胞后,1000 r/min离心10 min收集细胞后,按照氧化因子ROS测定试剂盒说明书,加入终浓度为10 μmol/L的DCFH-DA荧光探针室温孵育30 min,经流式细胞仪分析,采用Cyexpert 1.2软件进行数据分析。
细胞培养及细胞分组处理同上,1000 r/min离心10 min收集细胞后,用细胞超声破碎仪以功率300 W,冰水浴条件下破碎细胞,制备细胞匀浆待测。按试剂盒说明书测定氧化因子MDA、抗氧化物GSH含量以及抗氧化酶SOD、CAT活力并用BCA蛋白质浓度测定试剂盒测定蛋白浓度。
1.2.7 抗氧化肽组分对H2O2诱导PC12细胞内线粒体膜电位、细胞周期、Caspase-3及Caspase-9活力的影响
细胞培养同1.2.6,按照1.2.2中细胞分组处理细胞后,1000 r/min离心10 min收集细胞后。按线粒体膜电位检测试剂盒说明书以及细胞周期与细胞凋亡检测试剂盒说明书,经流式细胞仪分析,采用Cyexpert 1.2软件进行数据分析;按试剂盒说明书检测Caspase-3及Caspase-9活力,并用BCA蛋白质浓度测定试剂盒测定蛋白浓度。
1.3 数据处理
所有细胞试验做3次独立重复试验,采用SPSS 20.0统计软件进行统计学分析。试验数据以均数±标准差(
2. 结果与分析
2.1 Sephadex G-15层析分离英国红芸豆抗氧化肽
英国红芸豆抗氧化肽组分经Sephadex G-15层析分离结果见图1。
由图1可知,分子量小于1 kDa的抗氧化肽组分经Sephadex G-15层析被分出2个组分,分别为BRKBAPC-1和BRKBAPC-2,采用Collection Microsoft软件对峰面积进行计算,峰面积分别为932.65、1440.33。
2.2 H2O2诱导PC12细胞氧化应激损伤模型的建立
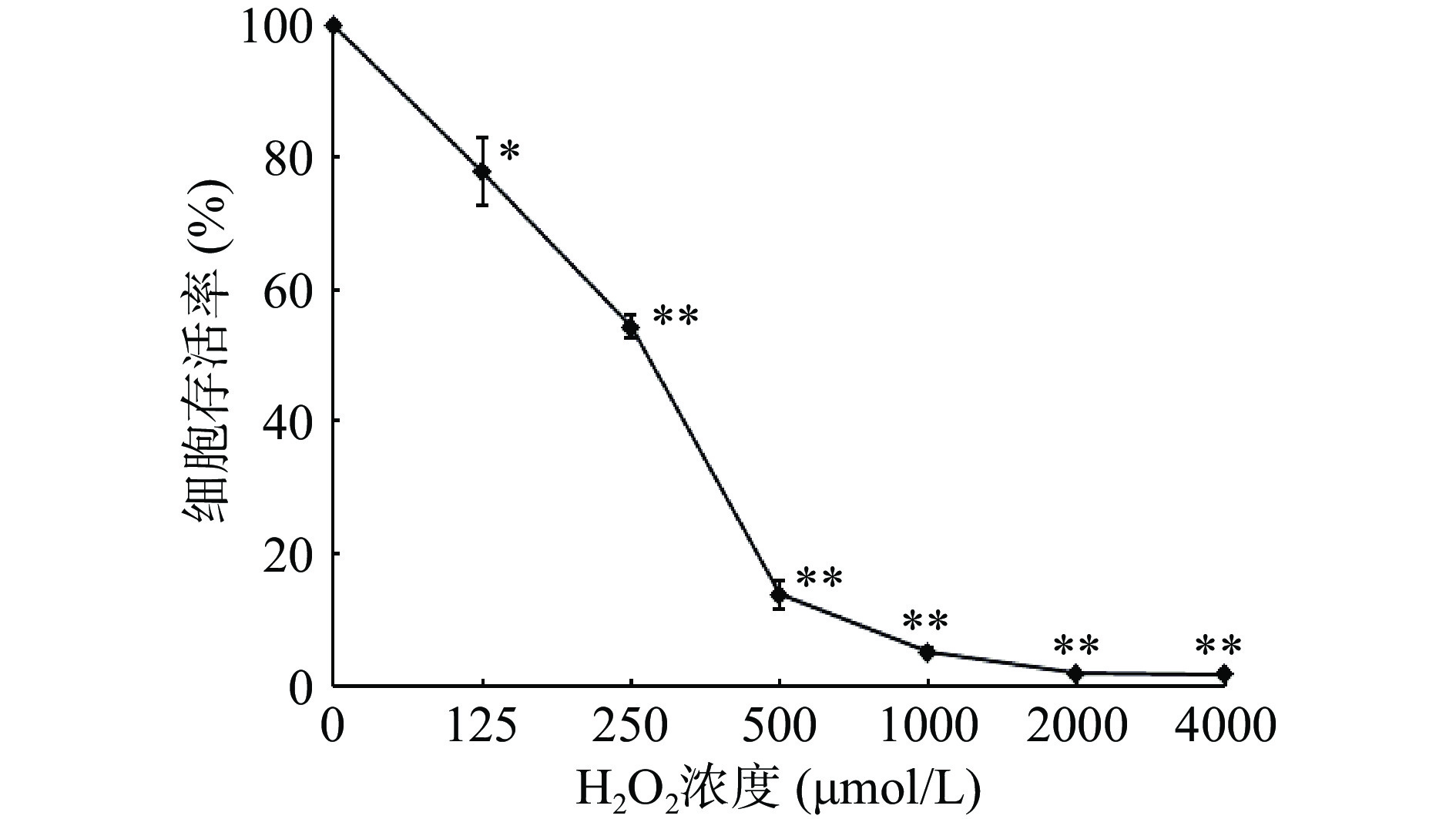
MTT法是一种广泛应用于检测细胞增殖的方法[18]。H2O2作为ROS的主要成分之一,会引起氧化应激并导致细胞凋亡或坏死[19]。4 h H2O2处理对PC12细胞的氧化损伤情况见图2。由图2可以看出,H2O2对PC12细胞的损伤呈剂量依赖性关系。与空白组相比,PC12细胞经125、250、500、1000、2000、4000 μmol/L的H2O2作用4 h后,细胞存活率分别降至77.81%、54.33%、13.83%、5.13%、1.94%以及1.77%。因此,在后续的试验中,选择250 μmol/L的H2O2作为最佳半数致死浓度,建立氧化损伤的PC12细胞模型。
2.3 抗氧化肽组分及VC对H2O2诱导PC12细胞的保护作用
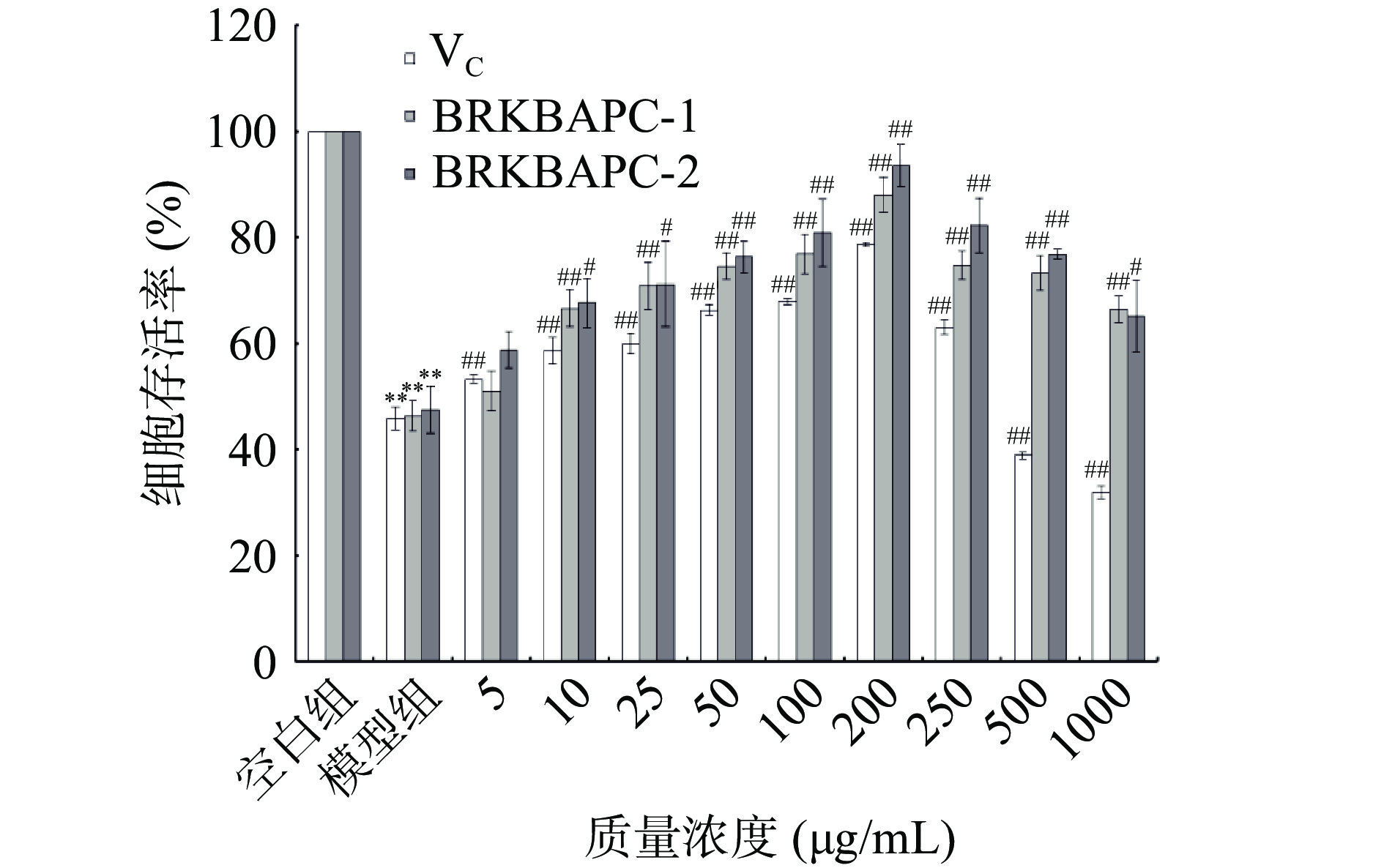
为了确定后续试验中BRKBAPC-1、BRKBAPC-2的低、中、高剂量的作用浓度以及阳性对照组VC最佳作用浓度,通过MTT试验,研究了不同浓度的BRKBAPC-1、BRKBAPC-2对H2O2氧化损伤PC12细胞的作用,结果见图3。
![]() 图 2 H2O2的不同浓度对PC12细胞存活率的影响注:* 表示与空白组相比,P<0.05;**表示P<0.01;图4同。Figure 2. Effects of different concentrations of H2O2 on viability of PC12 cells
图 2 H2O2的不同浓度对PC12细胞存活率的影响注:* 表示与空白组相比,P<0.05;**表示P<0.01;图4同。Figure 2. Effects of different concentrations of H2O2 on viability of PC12 cells与空白组相比,模型组存活率极显著降低(P<0.01),在5~200 μg/mL范围内,细胞存活率均与BRKBAPC-1、BRKBAPC-2以及VC浓度呈剂量依赖性关系,且在200 μg/mL时作用效果最好。并且,BRKBAPC-2相比BRKBAPC-1具有更强的保护作用。因此,选择50(低剂量)、100(中剂量)、200 μg/mL(高剂量)作为BRKBAPC-2后续试验的浓度梯度以及200 μg/mL作为VC后续试验的浓度,进一步研究英国红芸豆抗氧化肽组分BRKBAPC-2对H2O2诱导PC12细胞氧化应激损伤的保护作用。
2.4 抗氧化肽组分对PC12细胞的毒性
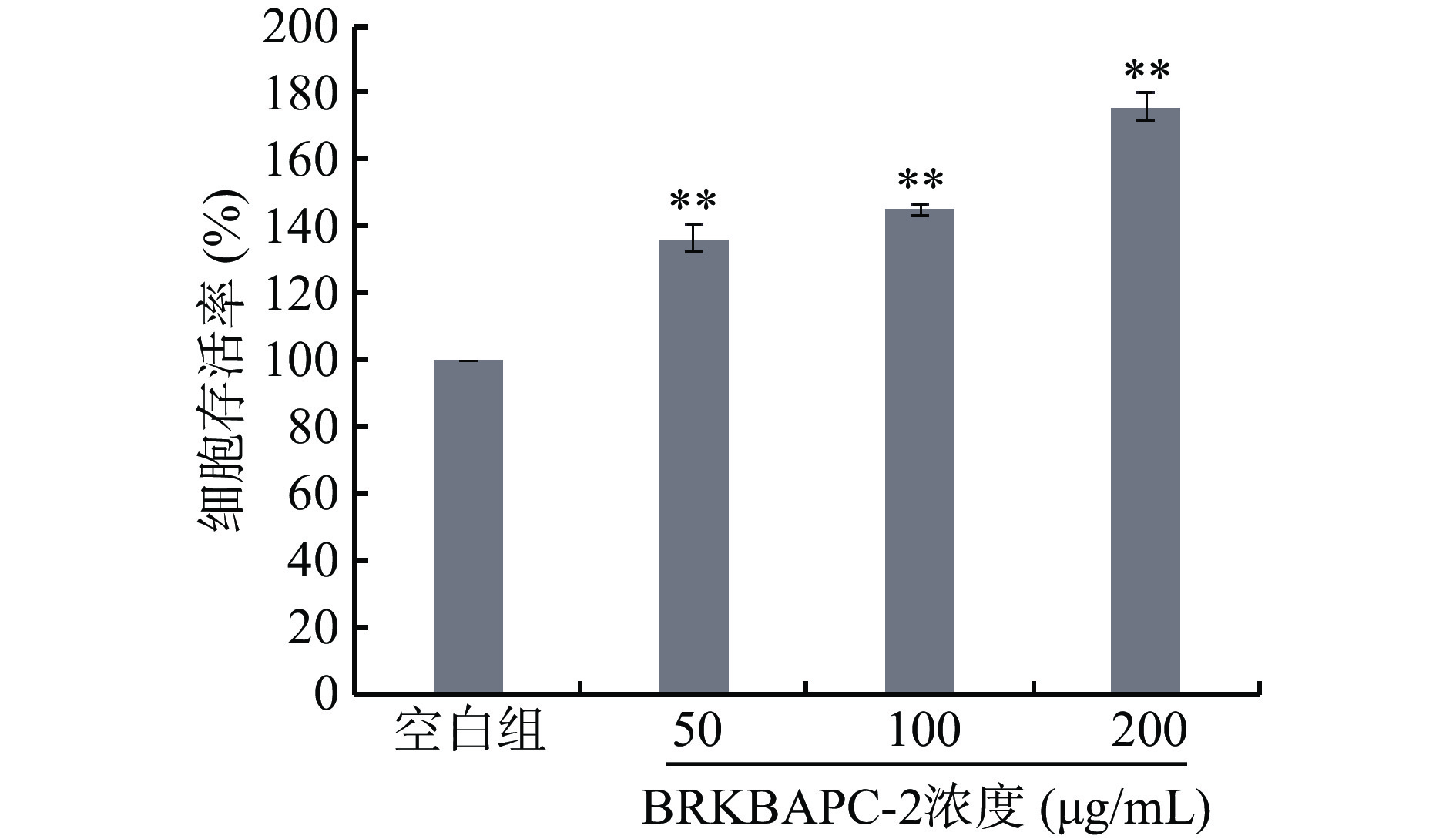
BRKBAPC-2对PC12细胞毒性作用结果见图4。由图4可知,与空白组相比,BRKBAPC-2的浓度为50、100、200 μg/mL时,对细胞无毒性作用,且对细胞有促进生长的作用,PC12细胞存活率极显著增加(P<0.01)。这与Amiot等[20]报道牛奶酶解物可以提高人角质化细胞的存活率6.1%~51.9%,以及刁静静等[21]研究发现不同级分绿豆肽能够增加巨噬细胞存活率的结果趋势一致。
2.5 抗氧化肽组分对H2O2诱导PC12细胞胞外LDH活力的影响
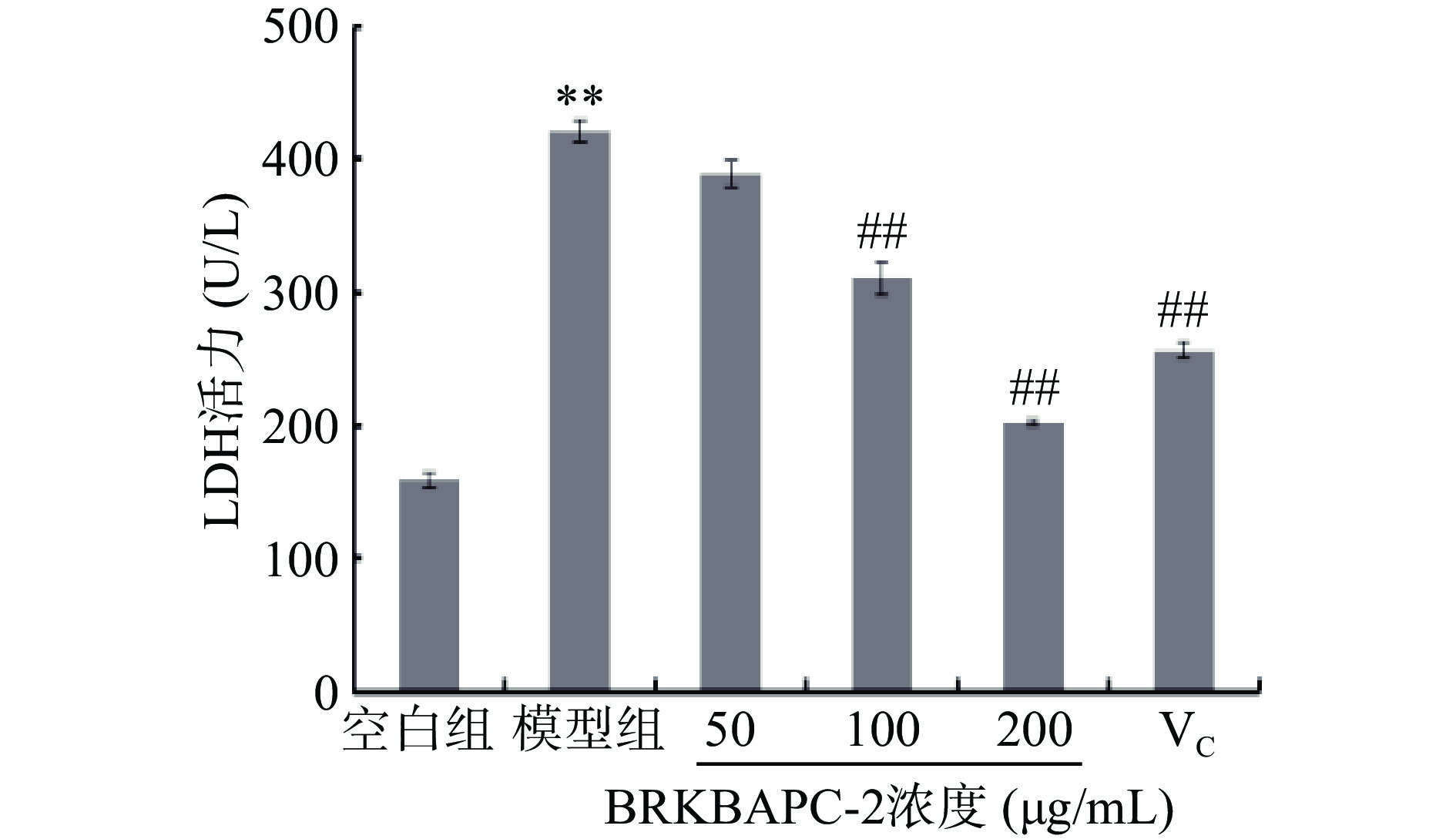
LDH是一种稳定的细胞质酶,当细胞膜受损时会释放到细胞培养液中[22]。因此,通过检测培养液中LDH的活力,可以判断细胞膜受损的情况,进一步反映细胞损伤情况。
如图5所示,与空白组相比,模型组PC12细胞经H2O2处理后,LDH的活力达到420.11 U/L,表明PC12细胞膜的完整性受到破坏,导致LDH释放到细胞培养液中。而受H2O2刺激的PC12细胞经50、100、200 μg/mL BRKBAPC-2预处理后,LDH的活力分别降低为388.89、310.05、202.12 U/L,可见BRKBAPC-2可以极显著改善H2O2对PC12细胞膜的损伤(P<0.01),且高剂量组效果优于200 μg/mL VC组。张燕等[15]研究蛋清源抗氧化肽对HEK293细胞氧化应激损伤的抑制作用中,发现H2O2处理组LDH活力显著高于正常组,而蛋清源抗氧化肽样品组中活力显著低于H2O2处理组,证明了蛋清源抗氧化肽可以维持细胞膜完整性,降低氧化损伤细胞胞外LDH释放量,本项研究结果与上述结果相似,即BRKBAPC-2能降低PC12细胞胞外LDH活力。
2.6 抗氧化肽组分对H2O2诱导PC12细胞内ROS生成的影响
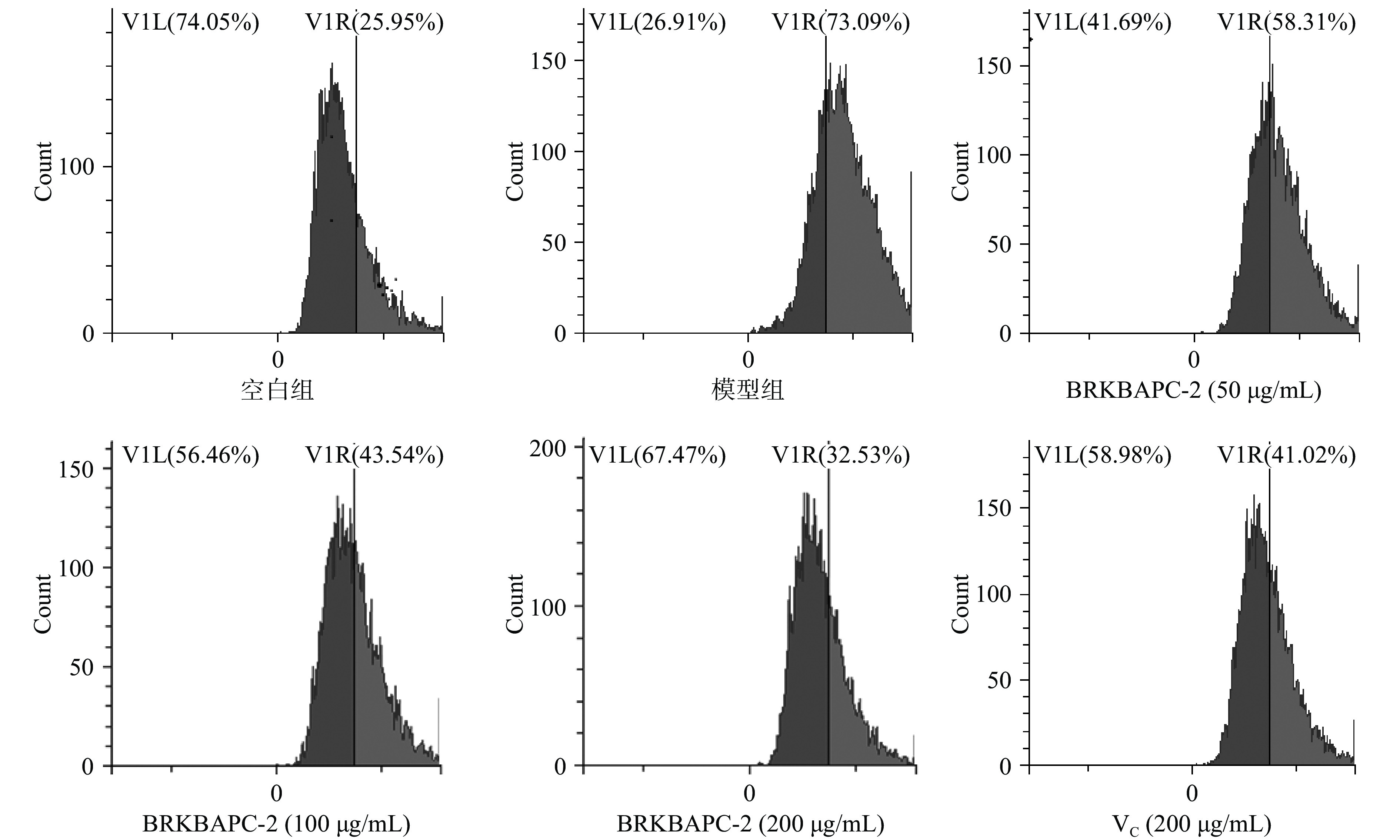
在正常生理条件下,机体会产生微量的ROS,其主要来源是机体氧化代谢产生的性质活泼的含氧化合物,如过氧化氢、超氧阴离子和羟自由基。而当机体受到有害刺激时,体内活性氧自由基产生过多,氧化-抗氧化平衡受到破坏,就会导致组织损伤。因此,细胞内ROS的含量是反映细胞氧化损伤程度的一个重要标志[3-4]。目前,检测细胞内ROS最常用便捷的方法是DCFH-DA荧光探针法,常以正常细胞作为内参,以发生荧光信号强度改变的细胞数占总细胞数的比值表征细胞内的ROS水平,右侧往左偏移量越大代表荧光强度越高,百分比占比越高代表ROS水平越高[23]。
如图6可知,经H2O2刺激的PC12细胞内ROS含量约为空白组的2.81倍,说明H2O2处理可促进细胞内ROS的产生。而受H2O2刺激的PC12细胞经50、100、200 μg/mL BRKBAPC-2预处理后,细胞内ROS水平分别降低为58.31%、43.54%、32.53%,可见,BRKBAPC-2可以抑制H2O2诱导PC12胞内ROS含量的升高,从而发挥其抗氧化应激的功能,降低ROS对细胞和机体引发的氧化损伤。这与马萍等[23]发现紫花芸豆肽能缓解H2O2对PC12细胞造成的细胞氧化损伤,减少胞内ROS的水平的研究结果一致。
2.7 抗氧化肽组分对H2O2诱导PC12细胞的MDA的影响
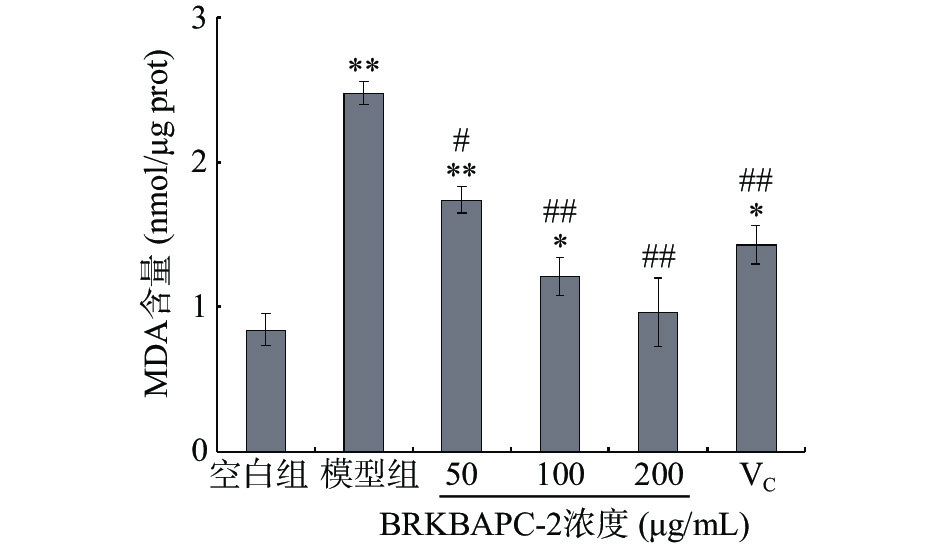
MDA是脂质过氧化物的分解产物,评价脂质过氧化的重要指标,可间接地反映细胞损伤的程度[24]。
如图7所示,与空白组相比,模型组的PC12细胞经H2O2刺激后,细胞内MDA含量显著(P<0.05)升高至2.48 nmol/μg prot,说明H2O2促进了细胞的脂质过氧化反应,且MDA含量越高,细胞损伤越严重。而受H2O2刺激的PC12细胞经50、100、200 μg/mL BRKBAPC-2预处理,与模型组相比,细胞内MDA含量明显降低,分别为1.74、1.21、0.96 nmol/μg prot(P<0.05),且中、高剂量组优于VC组,表明BRKBAPC-2能显著降低细胞的MDA水平,对细胞的脂质过氧化反应有改善作用。此项研究结果与Shen等[25]从培养的冬虫夏草菌丝体中分离出的多糖通过降低MDA水平来保护PC12细胞免受H2O2诱导的伤害的报道相符。
2.8 抗氧化肽组分对H2O2诱导PC12细胞内抗氧化酶及抗氧化物的影响
超氧化物歧化酶(SOD)是抗氧化酶,可清除超氧阴离子,其活性高低可间接反映组织自由基的含量和细胞受损程度[26]。过氧化氢酶(CAT)是一种广泛存在于生物组织中的氧化还原酶,能够催化H2O2分解为H2O和O2,具有清除H2O2的作用。还原型谷胱甘肽(GSH)是机体内最重要的非酶性抗氧化物,具有清除自由基、解毒、促进铁质吸收等作用,是衡量机体抗氧化能力的重要标志[27]。
由表1可知,与空白组相比,模型组CAT、SOD的活力和GSH的含量均极显著下降(P<0.01);与模型组相比,经过100、200 μg/mL BRKBAPC-2预处理后CAT、SOD的活力和GSH的含量均极显著提高(P<0.01)。由此表明,BRKBAPC-2能够增加PC12细胞中CAT、SOD的活力和GSH的含量。王丹丹等[27]在研究松花粉提取物、葡萄籽提取物以及竹叶黄酮对H2O2诱导PC12细胞氧化损伤的保护作用时发现,三种提取物能够提高CAT、SOD的活力以及提高GSH的含量,从而来发挥抗氧化作用,其试验结果与本次试验表1中得出的结果一致。
表 1 BRKBAPC-2对PC12细胞CAT、SOD、GSH的影响(mean±SD)Table 1. Effects of BRKBAPC-2 on CAT, SOD and GSH in H2O2-induced PC12 cells (mean±SD)组别 CAT(U/mL) SOD(U/mg prot) GSH(μmol/g prot) 空白组 17.62±3.00 617.55±19.19 150.24±2.73 模型组 3.21±0.39** 427.52±9.88** 90.74±1.58** BRKBAPC-2(50 μg/mL) 5.10±0.27# 477.20±18.74 108.66±4.41# BRKBAPC-2(100 μg/mL) 9.17±0.82## 513.83±6.19## 126.07±2.96## BRKBAPC-2(200 μg/mL) 14.77±1.30## 555.48±3.64## 140.88±8.19## VC(200 μg/mL) 12.06±1.30## 533.61±20.42## 113.55±1.49## 2.9 抗氧化肽组分对H2O2诱导PC12细胞内线粒体膜电位的影响
线粒体膜电位(MMP)的水平代表线粒体的膜完整性,线粒体膜电位的下降是细胞凋亡的重要指标[28]。使用JC-1通过流式细胞仪检测PC12细胞MMP变化的影响如图8所示。
由图8可知,与空白组比,模型组线粒体膜电位降低了21.59%。而经H2O2刺激的PC12细胞经50、100、200 μg/mL BRKBAPC-2以及200 μg/mL VC预处理后,与模型组相比,细胞内线粒体膜电位(MMP)的水平明显升高至75.67%、80.39%、87.99%、83.92%。可见,BRKBAPC-2能够在一定程度上抑制线粒体膜电位的降低,从而对氧化损伤的PC12细胞具有一定的保护作用。这与Zhu等[13]发现小麦胚芽分离蛋白水解物抑制了线粒体膜电位的降低的试验结果相同。
2.10 抗氧化肽组分对H2O2诱导PC12细胞周期的影响
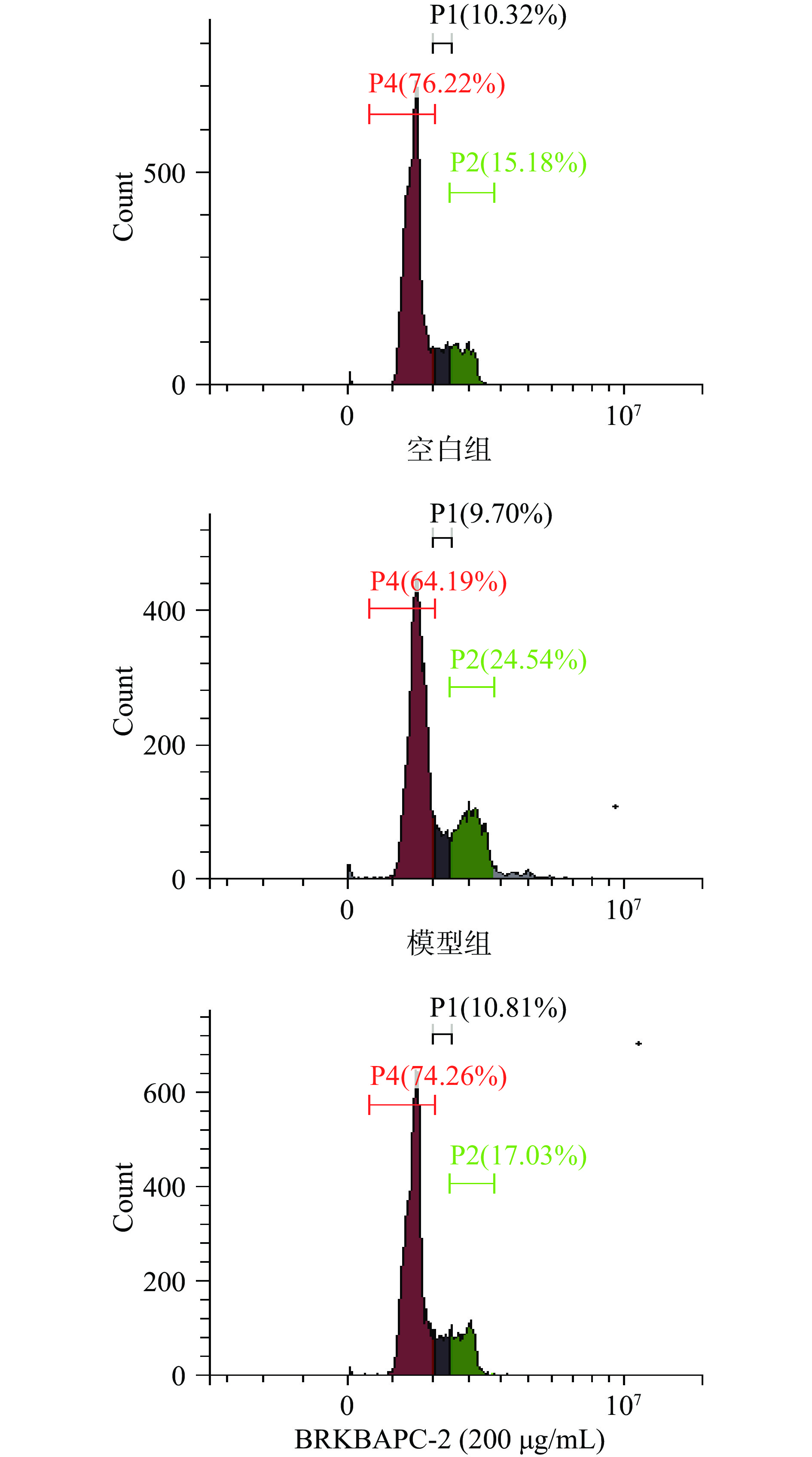
细胞周期可分为G0/G1期、S期以及G2/M期,其中,G0/G1期为DNA合成前期,S期为DNA复制期,而G2/M期主要为细胞分裂期,细胞周期阻滞是控制细胞增殖和诱导细胞凋亡的重要调控机制之一[29]。
如图9,与空白组相比,模型组PC12细胞G0/G1期下降至64.19%,G2/M期的比例增加至24.54%。而经200 μg/mL BRKBAPC-2预处理后,G2/M期比例下降为17.03%,说明PC12细胞经H2O2处理,会使其细胞阻滞在G2/M期,而BRKBAPC-2可改善H2O2对PC12细胞周期的阻滞情况。
2.11 抗氧化肽组分对H2O2诱导PC12细胞内Caspase-3及Caspase-9活力的影响
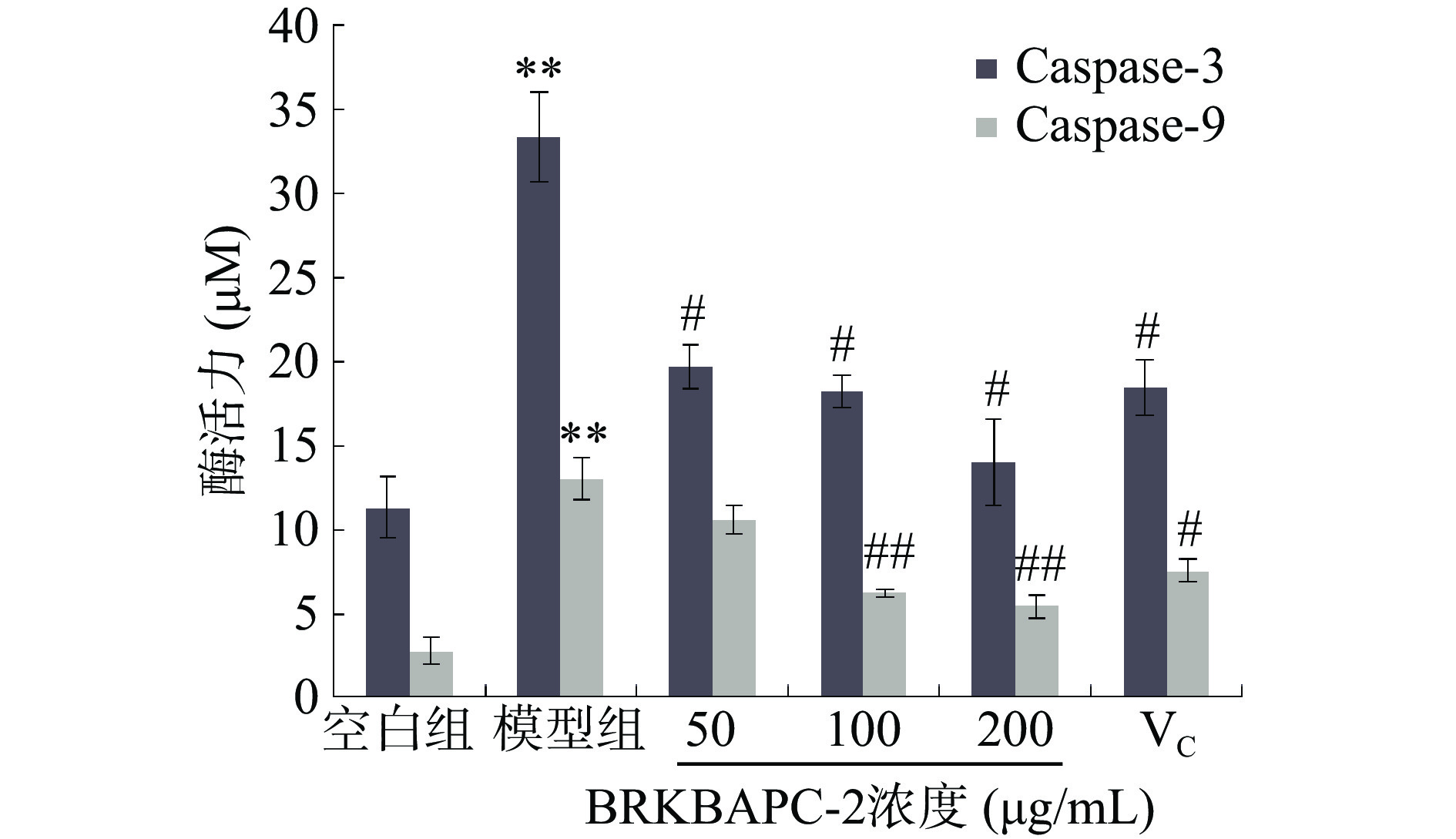
Caspase(Cysteine-requiring Aspartate Protease)是一个在细胞凋亡过程中起重要作用的蛋白酶家族,Caspase-3是细胞凋亡过程中的一个关键酶,Caspase-9是细胞凋亡信号转导过程中比较重要的一个Caspase。线粒体释放细胞色素C以后,Caspase-9可以和细胞色素C等形成复合物,同时被激活。激活的Caspase-9可以激活细胞凋亡的最关键酶Caspase-3,从而促进后续的细胞凋亡信号[30]。
由图10可知,细胞在H2O2损伤及BRKBAPC-2、VC保护下,各组Caspase-3和Caspase-9分别呈现不同的活性水平。与空白组相比,模型组细胞的Caspase-3和Caspase-9活性分别极显著提高(P<0.01)22.03%、10.31%。而经过50、100、200 μg/mL BRKBAPC-2和200 μg/mL VC预处理后,Caspase-3和Caspase-9活性显著降低(P<0.05),说明BRKBAPC-2在一定程度上抑制了由细胞色素C的释放引起的凋亡酶Caspase-3和Caspase-9的激活,防止了细胞凋亡的进一步发生。BRKBAPC-2抑制H2O2诱导Caspase-3和Caspase-9激活可能与降低细胞内ROS、稳定细胞线粒体膜电位有关。
3. 结论
综上所述,经过BRKBAPC-2处理,氧化损伤的PC12细胞内,抗氧化酶活力增强,抗氧化物含量增加,有害物质MDA的积累减少,线粒体膜电位的稳定性被恢复,细胞周期的阻滞得到了改善,抑制了细胞凋亡关键酶Caspase-3和Caspase-9的激活。因此,BRKBAPC-2的预处理能够保护氧化损伤的PC12细胞,具有一定的抗氧化作用,初步探讨了细胞内抗氧化肽的抗氧化机制,为英国红芸豆抗氧化肽在食品保健及医药领域的应用提供理论依据。但这种抗氧化保护作用的具体分子生物学机制及其在体内的抗氧化机制还有待进一步的深入研究。
-
图 2 H2O2的不同浓度对PC12细胞存活率的影响
注:* 表示与空白组相比,P<0.05;**表示P<0.01;图4同。
Figure 2. Effects of different concentrations of H2O2 on viability of PC12 cells
表 1 BRKBAPC-2对PC12细胞CAT、SOD、GSH的影响(mean±SD)
Table 1 Effects of BRKBAPC-2 on CAT, SOD and GSH in H2O2-induced PC12 cells (mean±SD)
组别 CAT(U/mL) SOD(U/mg prot) GSH(μmol/g prot) 空白组 17.62±3.00 617.55±19.19 150.24±2.73 模型组 3.21±0.39** 427.52±9.88** 90.74±1.58** BRKBAPC-2(50 μg/mL) 5.10±0.27# 477.20±18.74 108.66±4.41# BRKBAPC-2(100 μg/mL) 9.17±0.82## 513.83±6.19## 126.07±2.96## BRKBAPC-2(200 μg/mL) 14.77±1.30## 555.48±3.64## 140.88±8.19## VC(200 μg/mL) 12.06±1.30## 533.61±20.42## 113.55±1.49## -
[1] 梁珊. 芸豆蛋白的提取及理化功能特性研究[D]. 西安: 西北农林科技大学, 2015. LIANG Shan. Study on the extraction of kidney bean protein and its physical and chemical properties[D]. Xi'an: North West Agriculture and Forestry University, 2015.
[2] 韩晶, 郑文彬, 崔素萍, 等. 黑龙江芸豆主栽品种营养价值的评价[J]. 食品科技,2016,41(3):99−104. [HAN Jing, ZHENG Wenbin, CUI Suping, et al. Evaluation of protein nutritional value of main kidney bean in Heilongjiang province[J]. Journal of Food Technology,2016,41(3):99−104. [3] PISOSCHI A M, POP A. The role of antioxidants in the chemistry of oxidative stress: A review[J]. European Journal of Medicinal Chemistry,2015,97:55−74. doi: 10.1016/j.ejmech.2015.04.040
[4] 李兴太, 纪莹. 线粒体氧化应激与天然抗氧化剂研究进展[J]. 食品科学,2015,36(7):288−297. [LI Xingtai, JI Ying. Recent advances in mitochondrial oxidative stress and natural antioxidants[J]. Journal of Food Science,2015,36(7):288−297. [5] 申迎宾. 四种谷物多酚抗氧化、降血脂作用评价研究[D]. 无锡: 江南大学, 2016. SHEN Yingbin. Evaluation of the anti-oxidation and hypolipidemic effects of four kinds of grain polyphenols [D]. Wuxi: Jiangnan University, 2016.
[6] 李扬雪. MiR-210在过氧化氢诱导大鼠心肌细胞氧化应激损伤中的作用及其机制研究[D]. 长春: 吉林大学, 2016. LI Yangxue. The role and mechanism of MiR-210 in the oxidative stress injury of rat cardiac cells induced by hydrogen peroxide [D]. Changchun: Jilin University, 2016.
[7] 陈思, 董培良. 阿尔兹海默症与氧化应激反应的关系及抗氧化药物的研究进展[J]. 中国现代医药杂志,2016,18(11):98−100. [CHEN Si, DONG Peiling. The relationship between Alzheimer’s disease and oxidative stress and the research progress of antioxidant drugs[J]. Chinese Journal of Modern Medicine,2016,18(11):98−100. doi: 10.3969/j.issn.1672-9463.2016.11.031 [8] POLCE S A, BURKE C, FRANCA L M, et al. Ellagic acid alleviates hepatic oxidative stress and insulin resistance in diabetic female rats[J]. Nutrients,2018,10(5):531−537. doi: 10.3390/nu10050531
[9] TAHIR A, HAROON B, HYUN K T, et al. Melatonin attenuates D-galactose-induced memory impairment, neuroinflammation and neurodegeneration via RAGE/NF-κB/JNK signaling pathway in aging mouse model[J]. Journal of Pineal Research,2015,58(1):71−85. doi: 10.1111/jpi.12194
[10] JANINA S, BINEET P, PETTERI I. Telomere length, sibling competition and development of antioxidant defense in wild house mice[J]. Mechanisms of Ageing and Development,2017,169:45−52. doi: 10.1016/j.mad.2017.10.002
[11] 唐宁, 庄红. 玉米抗氧化肽Leu-Pro-Phe 抗氧化稳定性研究[J]. 中国食品学报,2015,15(2):49−55. [TANG Ning, ZHUANG Hong. Study on the antioxidant stability of corn antioxidant peptide Leu-Pro-Phe[J]. Journal of Chinese Institute of Food Science and Technology,2015,15(2):49−55. doi: 10.16429/j.1009-7848.2015.02.008 [12] 张晖, 唐文婷, 王立, 等. 抗氧化肽的构效关系研究进展[J]. 食品与生物技术学报,2013,32(7):7−13. [ZHANG Hui, TANG Wenting, WANG Li, et al. Research progress on the structure-activity relationship of antioxidant peptides[J]. Journal of Food and Biotechnology,2013,32(7):7−13. doi: 10.3969/j.issn.1673-1689.2013.07.001 [13] ZHU Kexue, GUO Xu, GUO Xiaona, et al. Protective effects of wheat germ protein isolate hydrolysates (WGPIH) against hydrogen peroxide-induced oxidative stress in PC12 cells[J]. Food Research International,2013,53(1):297−303. doi: 10.1016/j.foodres.2013.05.007
[14] 凌玉芳. 乳清蛋白酶解物对过氧化氢诱导的氧化损伤的保护作用[D]. 无锡: 江南大学, 2011. LING Yufang. Protective effect of whey protein hydrolysate on hydrogen peroxide-induced oxidative damage [D]. Wuxi: Jiangnan University, 2011.
[15] 张燕, 陈志飞, 赵颂宁, 等. 蛋清源抗氧化肽对HEK293细胞氧化应激损伤的抑制作用及机制[J]. 中国食品学报,2019,19(10):11−22. [ZHANG Yan, CHEN Zhifei, ZHAO Songning, et al. Inhibitory effect and mechanism of egg white-derived antioxidant peptides on oxidative stress damage of HEK293 cells[J]. Journal of Chinese Institute of Food Science and Technology,2019,19(10):11−22. doi: 10.16429/j.1009-7848.2019.10.002 [16] 郭勇, 秦汉雄, 魏贞, 等. 长白山核桃源五肽对过氧化氢诱导PC12细胞氧化损伤的保护作用及机理[J]. 食品科学,2019,40(13):143−149. [GUO Yong, QIN Hanxiong, WEI Zhen, et al. Protective effect and mechanism of Changbai hickory pentapeptide on hydrogen peroxide-induced oxidative damage in PC12 cells[J]. Journal of Food Science,2019,40(13):143−149. doi: 10.7506/spkx1002-6630-20180529-414 [17] 韩晶. 黑龙江芸豆主栽品种蛋白质营养价值分析及抗氧化活性肽的研究[D]. 大庆: 黑龙江八一农垦大学, 2016. HAN Jing. Analysis of protein nutritional value of main cultivated kidney bean varieties in Heilongjiang and study on antioxidant peptides [D]. Daqing: Heilongjiang Bayi Agricultural University, 2016.
[18] LI Yan, ZHANG Wenting, CHEN Chun, et al. Inotodiol protects PC12 cells against injury induced by oxygen and glucose deprivation/restoration through inhibiting oxidative stress and apoptosis[J]. Journal of Applied Biomedicine,2018,16(2):126−132. doi: 10.1016/j.jab.2017.11.004
[19] LIU Jingbo, CHEN Zhifei, HE Jing, et al. Anti-oxidative and anti-apoptosis effects of egg white peptide, Trp-Asn-Trp-Ala-Asp, against H2O2-induced oxidative stress in human embryonic kidney 293 cells[J]. Food & Function,2014,5(12):3179−3188. doi: 10.1039/c4fo00665h
[20] AMIOT J, GERMAIN L, TURGEON S, et al. Peptides from milk protein hydrolysates to improve the growth of human keratinocytes in culture[J]. International Dairy Journal,2004,14(7):619−626. doi: 10.1016/j.idairyj.2003.11.007
[21] 刁静静, 迟治平, 刘妍兵, 等. 不同级分绿豆肽免疫活性的分析[J]. 食品科学,2020,41(1):133−138. [DIAO Jingjing, CHI Zhiping, LIU Yanbing, et al. Analysis of immunological activity of different fractions of mung bean peptides[J]. Journal of Food Science,2020,41(1):133−138. [22] HONG Hao, LIU Guoqing. Protection against hydrogen peroxide-induced cytotoxicity in PC12 cells by scutellarin[J]. Life Sciences,2004,74(24):2959−2973. doi: 10.1016/j.lfs.2003.09.074
[23] 马萍, 程天赋, 郭增旺, 等. 紫花芸豆肽修复H2O2对HepG2细胞的氧化应激损伤[J]. 食品科学,2020,41(1):175−182. [MA Ping, CHEN Tianfu, GUO Zengwang, et al. Purple kidney bean peptide repairs H2O2 oxidative stress damage to HepG2 cells[J]. Journal of Food Science,2020,41(1):175−182. [24] 丁红军. 芝麻抗氧化肽的分离纯化与生物活性研究[D]. 西安: 陕西师范大学, 2008. DING Hongjun. Separation, purification and biological activity of sesame antioxidant peptides [D]. Xi'an: Shaanxi Normal University, 2008.
[25] SHEN Wenbin, SONG Dan, WU Jianyong, et al. Protective effect of a polysaccharide isolated from a cultivated cordyceps mycelia on hydrogen peroxide-induced oxidative damage in PC12 cells[J]. Phytotherapy Research,2011,25(5):675−680. doi: 10.1002/ptr.3320
[26] AOSHIMA H, HIRATA S, AYABE S. Antioxidative and anti-hydrogen peroxide activities of various herbal teas[J]. Food Chemistry,2007,103(2):617−622. doi: 10.1016/j.foodchem.2006.08.032
[27] 王丹丹. 三种植物提取物对H2O2诱导PC12细胞氧化损伤的保护作用研究[D]. 济南: 山东师范大学, 2016. WANG Dandan. Study on protective effect of three plant extracts on H2O2 induced oxidative damage in PC12 cells [D]. Ji'nan: Shandong Normal University, 2016.
[28] WANG H, YANG J H, HSIEH S C, et al. Allyl sulfides inhibit cell growth of skin cancer cells through induction of DNA damage mediated G2/M arrest and apoptosis[J]. Journal of Agricultural and Food Chemistry,2010,58(11):7096−7103. doi: 10.1021/jf100613x
[29] ROMANOV V, WHYARD T C, WALTZER W C, et al. Aristolochic acid-induced apoptosis and G2 cell cycle arrest depends on ROS generation and MAP kinases activation[J]. Archives of Toxicology,2015,89(1):47−56. doi: 10.1007/s00204-014-1249-z
[30] 刘萍, 丛国正, 独军政, 等. 细胞凋亡信号传导通路的研究进展[J]. 湖北农业科学,2010(3):715−717. [LIU Ping, CONG Zhengguo, DU Junzheng, et al. Research progress of apoptosis signal transduction pathway[J]. Journal of Hubei Agricultural Sciences,2010(3):715−717. doi: 10.3969/j.issn.0439-8114.2010.03.063 -
期刊类型引用(0)
其他类型引用(1)








 下载:
下载:

 下载:
下载:
