Establishment and Application of A Method for Detecting the Cyanogenic Glycoside in Sweet Cassava Root and Its Products
-
摘要: 生氰糖苷含量的高低对评估食用木薯块根及其制品的食用安全性及其重要。以木薯块根和木薯粉为试材,本研究建立了亚麻苦苷和百脉根苷2种生氰糖苷(Cyanogenic Glycosides,CNGs)的快速提取和高效液相色谱-蒸发光散射(HPLC-ELSD)检测的方法,分析了不同品种木薯块根、木薯粉及其制品中CNGs含量变化。结果表明,食用木薯块根及木薯粉中CNGs提取最佳的硫酸溶液浓度分别为0.025和0.100 mol/L;HPLC-ELSD检测方法可有效分离亚麻苦苷和百脉根苷,其浓度在4.1~820.0 mg/L和2.5~250.0 mg/L范围内线性相关性较好,相关系数(r)分别达到了0.9996和0.9993,检测限(LOD)分别为2.1和0.5 mg/kg,定量限(LOQ)分别为8.2和2.0 mg/kg;该方法重复性和样品稳定性的标准偏差(RSD)都低于5.0%;木薯块根和木薯粉中2种CNGs的平均加标回收率分别在89.3%~96.3%和107.5%~114.9%之间,重复间RSD小于3.4%。样品验证结果表明:不同的木薯品种CNGs含量差异较大;种植8~9个月的木薯制备木薯粉CNGs含量较低;蒸煮加工方式可有效清除木薯食品中CNGs。本方法操作简单、稳定性较好、准确度高,在食用木薯块根及其制品中CNGs的分析与评价等研究方面具有较强的应用前景。Abstract: The contents of cyanogenic glycosides (Cyanogenic Glycosides, CNGs) are very important to evaluate the safety of sweet cassava roots and their products. Using cassava roots and cassava products as test materials in this study, a method for rapid extraction and high performance liquid chromatography-evaporative light scattering (HPLC-ELSD) detection of two kinds of cyanogenic glycosides was established. The content of CNGs in different varieties of cassava roots, cassava flour, and their products were analyzed. The results showed that the optimal extraction concentrations of sulfuric acid solution for these two GNSs from cassava roots and flour were 0.025 and 0.100 mol/L, respectively. The HPLC-ELSD method was effective in the separation of linamarin and lotaustralin. The linear correlation was good in the range of 4.1 to 820.0 mg/L and 2.5 to 250.0 mg/L, which correlation coefficients (r) reached 0.9996 and 0.9993 respectively. The LOD was 2.1 and 0.5 mg/L, and the LOQ was 8.2 and 2.0 mg/kg, respectively. The relative standard deviation (RSD) of repeatability and sample stability are both less than 5.0%. The average recovery rates of two CNGs in cassava roots and cassava products were between 89.3%~96.3% and 107.5%~114.9%, respectively. And the RSD of the repeatability of the recovery was less than 3.4%. The results of sample verification showed that the content of CNGs in different cassava varieties were quite different, The content of CNGs was lower in cassava flour which was prepared from cassava grown for 8~9 months, and the cooking method could effectively remove CNGs in cassava food. This method was simple, stable and accurate, and had a strong application prospect in the analysis and evaluation of CNGs in sweet cassava roots and their products.
-
Keywords:
- sweet cassava root /
- cassava flour /
- cassava product /
- cyanogenic glycosides /
- HPLC-ELSD
-
木薯(Manihot esculenta Crantz,Cassava)为大戟科木薯属多年生植物,与甘薯、马铃薯并称世界三大薯类作物,是目前淀粉和生物能源生产的重要原料,也是全球约10亿人口的主要粮食。木薯中存在亚麻苦苷(Linamarin)和百脉根苷(Lotaustralin)2种生氰糖苷(Cyanogenic Glycosides,CNGs)[1],在蒸煮或加工过程中,亚麻苦苷酶会降解部分CNGs产生不稳定的丙酮氰醇,进而产生的氢氰酸(HCN)和醛、酮等小分子化合物,少部分CNGs会稳定的存在于木薯食品中,若加工后食品中CNGs残留量较高,摄入人体内后,在β-葡糖糖苷酶的作用下会分解成HCN,容易引起呼吸中枢及血管运动中枢麻痹,甚至导致死亡[2]。在非洲和南美地区,长期食用CNGs高含量的木薯食品,会引发热带神经性共济失调症(TAN),在儿童和生育期妇女中还可能引发永久性下肢瘫痪症(konzo)[1,3-5]。食用木薯块根及其制品中CNGs的存在,给木薯“食用化”带来不可忽视的安全隐患。因此,对其CNGs的准确定量是评价其安全性的重要方式。
研究者在探索CNGs检测方法的过程中发现,木薯块根和木薯食品在高水分条件下,由于细胞结构破坏或自身降解酶的存在,使得以HCN含量表示氰化物的测量结果偏低[4, 6-8]。由此认为,稳定高效的提取方法是对氰化物准确定量的前提。随着色谱检测技术的发展,高效液相色谱分别配备示差检测器(RI)[9-10]或蒸发光检测器(ELSD)[11],UPLC-MS/MS[12-13]都可直接对CNGs的含量进行定量分析。但其也有各自的不足之处,如RI的灵敏度较低,重复性较差,目前已较少应用,如 Sornyotha等[10]利用其纯化木薯块根中亚麻苦苷,亚麻苦苷回收率可达到91.5%以上,但其分离效果较差,需要进行薄层层析去除杂质以达到样品的基线分离;UHPLC-MS/MS虽然灵敏度高,重复性好,能对多种CNGs同时定性定量分析,但样品需要进行脱脂或固相萃取等前处理,仪器设备昂贵成本较高,对于方法的普及难度较大[12];蒸发光散射检测器(ELSD)作为一种新型的通用型检测器,与液相色谱结合实现了重复性好、灵敏度高等优势,在木薯、亚麻籽、苦杏仁等作物单一的CNGs的检测中已广泛应用[10-11,14]。如邹良平等[11]通过甲醇溶液提取木薯叶片中亚麻苦苷,评价了不同木薯品种中亚麻苦苷含量的差异,但并未对方法的回收率进行验证;周新城等[15]在其基础上,用预热的80%甲醇提取木薯中2种CNGs,但甲醇有毒,提取过程中试管易爆管,对操作人员安全难以保证,也会影响提取效果。前人研究结果证明,稳定高效的提取方法是CNGs准确定量的前提。
因此,本研究以食用木薯块根及其制品为实验材料,期望通过优化CNGs提取方法,建立HPLC-ELSD同时测定木薯块根及其制品中2种CNGs的定量分析方法,以期为木薯及其制品中氰化物的安全评估提供检测依据。
1. 材料与方法
1.1 材料与仪器
‘华南9号’(SC9)、‘华南12号’(SC12)、‘华南6068’(SC6068)木薯新鲜块根 2019年采收于国家木薯种质资源圃;亚麻苦苷(Linamarin, LI)、百脉根苷(Lotaustralin, LO)标准样品 加拿大TRC公司(纯度≥99.0%);甲醇、乙腈 色谱纯,美国Sigma公司;浓硫酸、甲酸等 分析纯,国药集团化学试剂有限公司。
采用Agilent1260型液相色谱系统:配备G1311C四元泵、G1329B自动进样器、G4260B蒸发光检测器和G1316A柱温箱 美国安捷伦科技有限公司;Atlantic C18色谱柱(4.6 mm×150 mm,5 μm) 美国Waters公司;Elix3+Synergy 超纯水系统 美国Millipore公司;BSA124S万分之一天平 美国Sartorius公司;PT1200E手提式组织匀浆机 瑞士KINEMATICA公司。
1.2 实验方法
1.2.1 木薯块根的预处理及其食品制备
1.2.1.1 木薯新鲜块根的处理
SC9、SC12和SC6068不同木薯品种块根收获后,用自来水清洗、沥干表面水分,除去外表皮,分别把块根的韧皮部(肉质皮层)和木质部(块根实质)切成1 cm左右的颗粒,液氮速冻,保存于−40 ℃冰箱待用。
1.2.1.2 木薯粉的制备
2019年3月下旬种植的SC9、SC12和SC6068木薯品种,分别在木薯种植后块根膨大期(6~7个月)、膨大期(7~8个月)、稳定期(8~9个月)和后熟期(9个月以上)四个时期采收新鲜块根,参照张振文等[16]方法,剥去木薯新鲜块根韧皮部,切丝、烘干、粉碎并过80目钢筛,制备成木薯粉,常温保存备用。
1.2.1.3 木薯粉食品的制备
利用1.2.1.2中制备好的 SC9品种木薯粉,参照《木薯及其食品加工技术》中的加工流程制备木薯饼干、木薯蛋糕、木薯面条、木薯馒头和木薯年糕[17],随机取100.0 g制备好的木薯食品,放置于−20 ℃冰箱待用。
1.2.2 木薯新鲜块根中CNGs的提取
称取冻存的木薯新鲜块根组织20.0 g,用匀浆机快速粉碎后,加入液氮,准确称取冷冻的木薯新鲜块根粉末1.00 g放入50 mL离心管中,按1:30的比例加入预冷(4~8 ℃)的0.025 mol/L硫酸溶液,在4 ℃条件下转速10000 r/min离心10 min,收集上清液。取1 mL上清液用0.22 μm PTFE水系微孔滤膜过滤,用于高效液相色谱分析。每个样品设置3个重复。
1.2.3 木薯粉及其食品中CNGs的提取
准确称取0.200 g的木薯粉粉末和用匀浆机快速粉碎的木薯食品粉末,加入预冷(4~8 ℃)的0.100 mol/L硫酸溶液1.5 mL,在4 ℃条件下转速10000 r/min 离心10 min,收集上清液。取1 mL上清液用0.22 μm PTFE水系微孔滤膜过滤,用于高效液相色谱分析。每个样品设置3个重复。
1.2.4 ELSD检测参数优化
根据仪器性能、流动相的种类和比例,参照文献[18-19]方法,首先,设定氮气气流速度为1.6 L/min,用100 mg/L亚麻苦苷和百脉根苷混合标准溶液进样,在80~100 ℃范围内改变漂移管温度,观察基线水平和2种CNGs的峰面积变化,确定ELSD最佳的偏移管温度;然后,固定优化的漂移管温度,观察1.6~2.4 L/min范围内氮气流速2种CNGs的峰面积变化,确定流动相挥发较好的最佳气流速度;最后,设定1~9不同的检测增益因子,观察2种CNGs的峰面积变化和基线水平,确定同时检测2种CNGs的最佳增益因子。
1.2.5 木薯中CNGs的检测
参照文献[9,12]方法并进行修改,利用液相色谱仪和1.2.4确定的ELSD检测参数分析样品中CNGs。色谱条件如下:Waters Atlantic C18色谱柱(4.6 mm×150 mm,5 μm),柱温25 ℃,采用二元梯度洗脱,流动相A为含0.1%甲酸(V/V)的80%乙腈/水(V/V),B为0.1%(V/V)甲酸水溶液。起始时A为10%,B为90%,到15 min时,A和B都为50%;18 min时,A为100%,保持2 min;到22 min时A变化为10%,B%为90%;平衡柱子5 min,进下一个样。流速0.6 mL/min;漂移管温度95 ℃,雾化温度80 ℃,气流速度:2.0 L/min;增益为3;进样量10 μL。
以外标法计算试样中2种CNGs的含量。LI或LO含量(mg/kg)=CV/1000M。其中:C-标准曲线查得LI或LO的浓度,mg/L;V-样品的提取液总体积,L;M-样品质量,kg。
1.2.6 标准溶液的配制
分别精确称取4.10和2.50 g的亚麻苦苷和百脉根苷,用色谱甲醇溶液溶解,配制成浓度为4100和2500 mg/L的标准储备液,置于−20 ℃冰箱中保存备用。用0.025 mol/L的硫酸溶液稀释亚麻苦苷和百脉根苷两种标准储备液,分别配置成4.1~820.0 mg/L和2.5~250.0 mg/L的5个梯度标准溶液,置于4~8 ℃冰箱中保存待用,用于方法线性关系的考察。
1.3 数据处理
每组实验重复三次,数据格式为平均值±标准误。采用Microsoft Excel2013进行数据分析和制图,采用SPSS22.0统计软件进行显著性分析。
2. 结果与分析
2.1 木薯样品中CNGs提取条件的优化
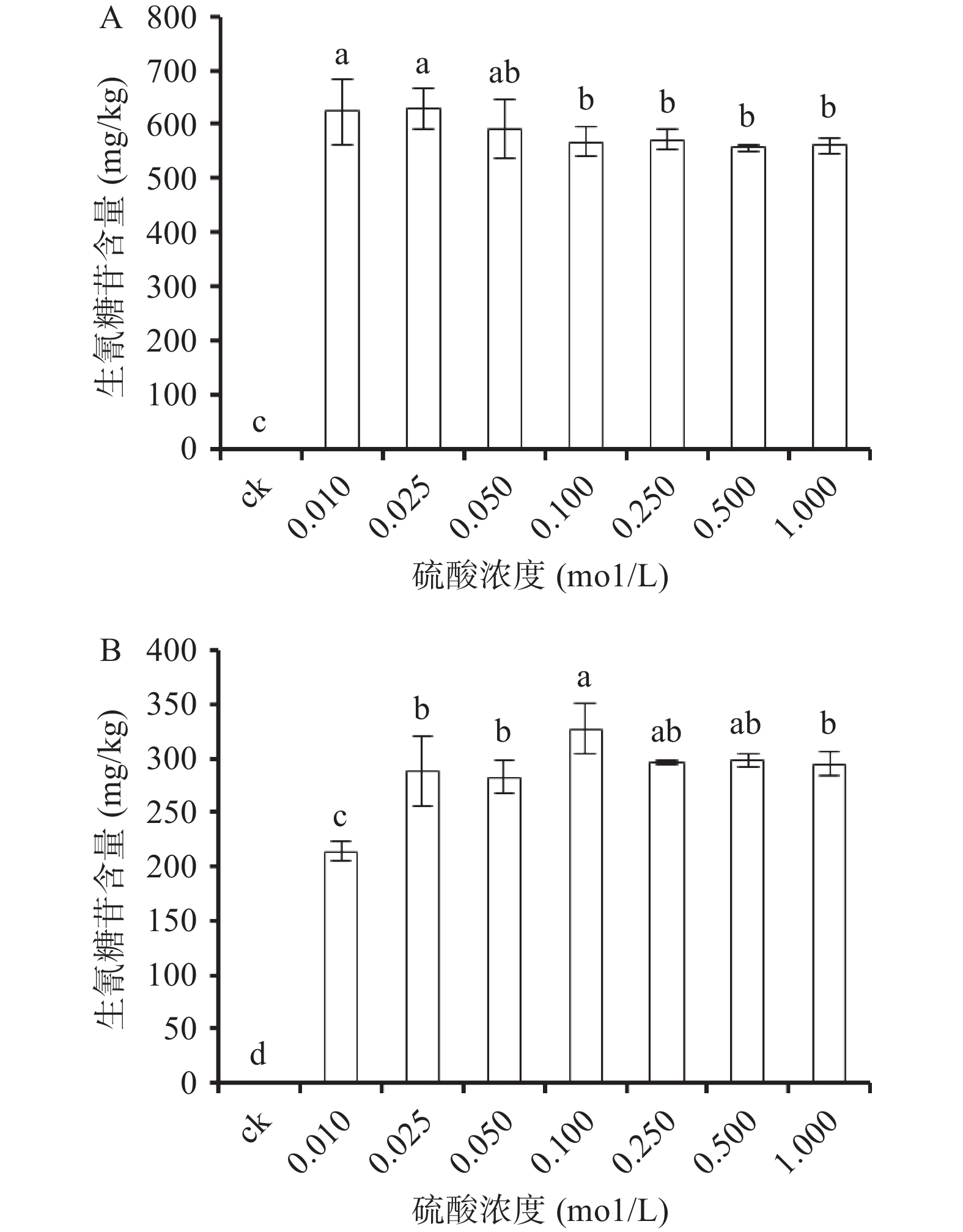
Bradbury等[20]研究结果表明,低浓度的HCl溶液可抑制亚麻苦苷酶活性,并且不同浓度的盐酸对酶活性的抑制效果差异显著。Sornyotha等[10]评价了不同种类的酸和不同酸浓度提取木薯块根中亚麻苦苷提效果差异,认为采用0.25 mol/L硫酸溶液可有效提取木薯中亚麻仁苦苷的含量,提取率可达97%以上。而本实验对不同浓度硫酸溶液提取CNGs效果比较发现:当硫酸浓度为0.010~0.050 mol/L时,木薯新鲜块根中CNGs含量升高,但未达到显著差异,并在提取溶液硫酸浓度为0.025 mol/L时,CNGs达到了最高含量630.07 mg/g(图1A),随后开始下降。木薯粉中CNGs含量随着硫酸浓度的升高呈现先升后降的趋势,当提取溶液硫酸浓度为0.100 mol/L时,CNGs达到了最高含量327.24 mg/g(图1B)。证明不同硫酸溶液浓度适合不同的样品形态中CNGs的提取,如0.025 mol/L硫酸溶液适合木薯新鲜块根样品CNGs的提取(图2A),而0.100 mol/L硫酸溶液适合木薯粉样品CNGs的提取,并且纯水提取样品(ck)中CNGs未检测到(图1B)。由此证明,样品在水湿润的条件下可以激活降解CNGs的相关酶,这验证了Bradbury等[20]的研究结果,并推测不同样品中降解CNGs的酶活性不同,需要不同浓度的硫酸以抑制其活性,而具体的抑制效率,需要进一步的实验证明。因此,为了保证样品中CNGs的稳定和有效提取,后续实验分别选择0.025和0.100 mol/L的硫酸溶液提取木薯新鲜块根和木薯粉及食品中的CNGs。
2.2 ELSD检测参数优化条件的确定
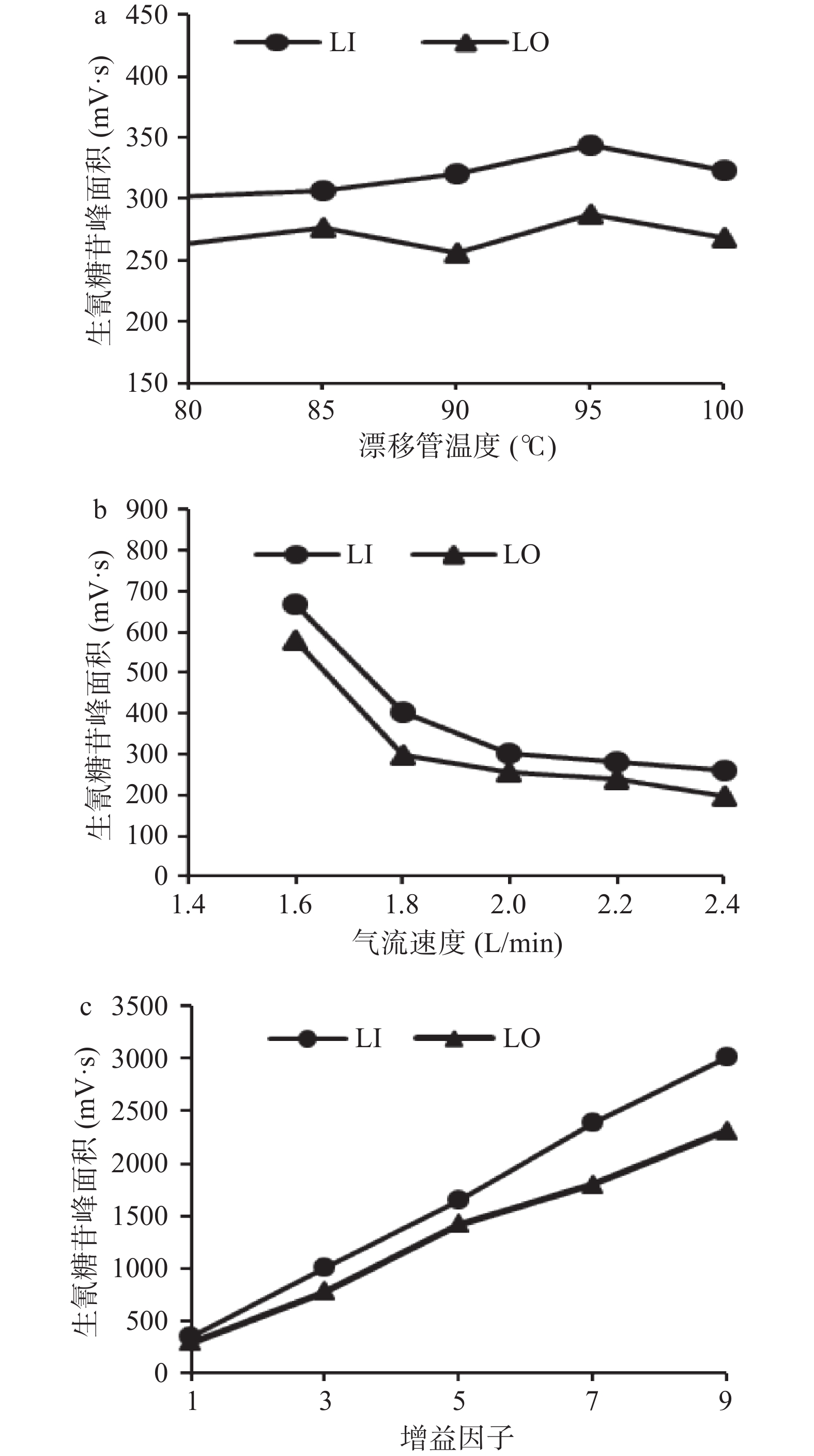
根据漂移管温度、气流速度和增益因子优化,结果显示:在80~100 ℃范围内改变漂移管温度,峰面积呈先升高后降低的趋势,基线都较平稳,当漂移管温度为95 ℃时,流动相基本挥发,峰面积最高(图2a),确定漂移管温度为95 ℃;通过1.6~2.4 L/min氮气流速范围,观察2种CNGs的峰面积变化发现,峰面积在1.6~1.8 L/min气流速度时快速下降,在2.0~2.5 L/min气流时峰面积变化不明显,并且基线噪音小(图2b)。因此,为节约载气,气流速度选择2.0 L/min。同时,因样品中亚麻苦苷和百脉根苷的含量差异较大,调整不同的增益因子,峰面积随着增益因子的增加而增加,但是基线噪音也开始增大,在增益为3时,样品峰峰形较好,并能同时检测2种CNGs(图2c)。因此,ELSD参数选择漂移管温度为95 ℃,氮气气流速度为2.0 L/min,增益因子为3,采集样品中的CNGs。
2.3 木薯样品中CNGs的检测
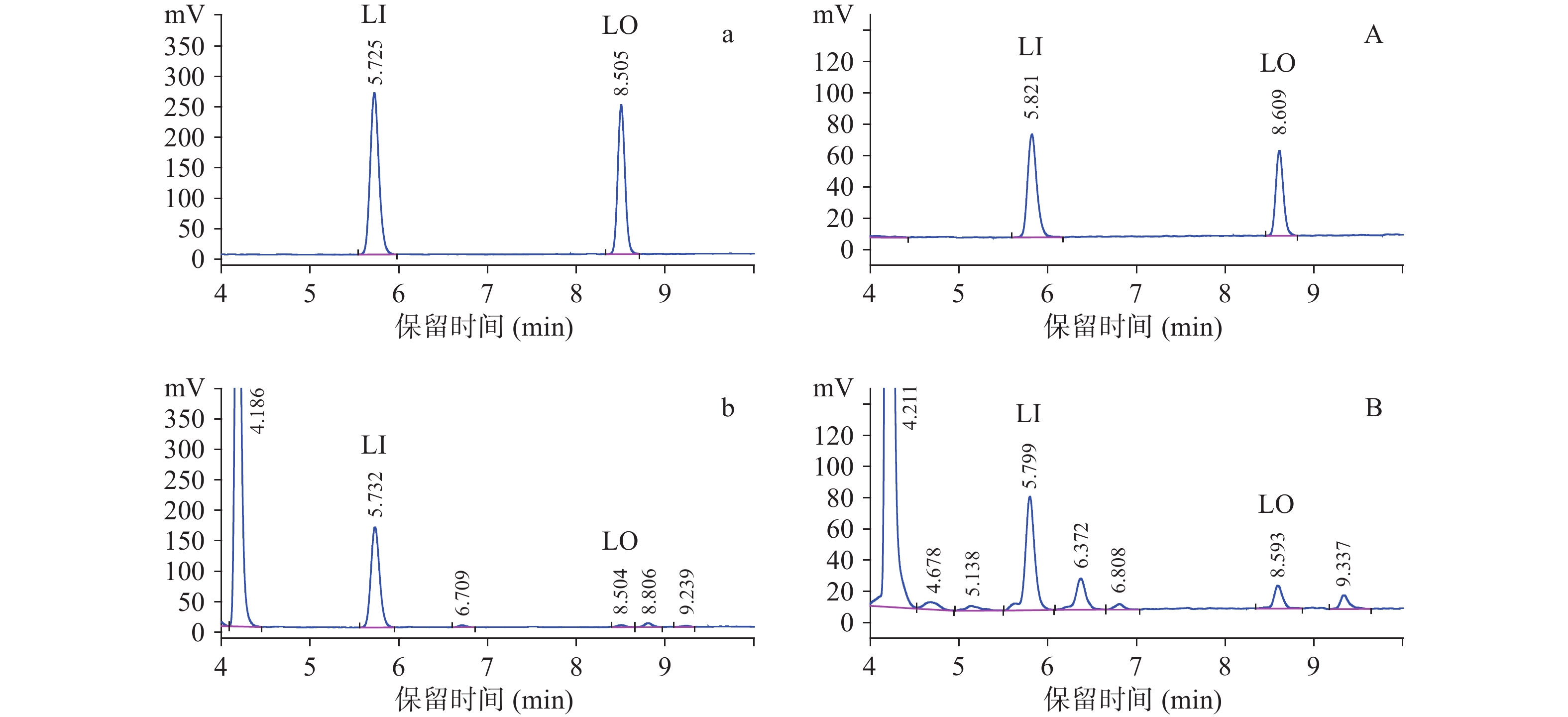
以优化的ELSD参数为检测条件,对标准品和样品中的亚麻苦苷和百脉根苷进行分析,结果显示:标准品中2种CNGs在保留时间分别为5.8和8.6 min左右(图3a、3A),样品(木薯肉质皮层和木薯粉)中保留时间分别为5.8和8.6 min左右(图3b、3B),保留时间基本一致。标准样品和样品中峰形较好,无拖尾现象。
2.4 HPLC-ELSD检测方法的验证
2.4.1 线性关系、检出限考察
在1.2.5的色谱条件下,依次进样10 μL,根据仪器性能和参照文献[21]方法,以CNGs标准样品浓度的自然对数(lgX)与ELSD测得的峰面积的自然对数(lgY)进行线性回归分析,两者间存在着良好的线性关系,亚麻苦苷和百脉根苷的线性相关性(r)达到了0.9996和0.9993(表1)。并分别以3倍和10倍信噪比确定两种CNGs检出限和定量限,亚麻苦苷和百脉根苷的检出限分别为2.1和0.5 mg/kg,定量限分别为8.2和2.0 mg/kg。
表 1 2种CNGs的线性范围、相关性、检出限和定量限Table 1. Linear range, correlation, detection limit and quantification limit of the two CNGs生氰糖苷 线性范围
(mg/L)回归方程 相关系数
(r)检出限(mg/kg) 定量限
(mg/kg)亚麻苦苷 4.1~820.0 lgY=1.4456(lgX)−0.5363 0.9996 2.1 8.2 百脉根苷 2.5~250.0 lgY=1.4494(lgX)−0.3571 0.9993 0.5 2.0 2.4.2 仪器精密度试验
以任意样品连续进样4次,每次进样体积为10 μL,按照1.2.4色谱条件进行分离检测,计算峰面积RSD,考察仪器的精密度。如表2所示,亚麻苦苷的峰面积分别为1372.0、1372.3、1368.9、1371.1 mV·s,RSD为0.1%,百脉根苷的峰面积分别为314.9、291.8、300.9、301.9 mV·s,RSD为3.1%,证明仪器精密度较好。
表 2 仪器精密度试验Table 2. The test of instrument precision生氰糖苷 1 2 3 4 平均 RSD(%) 亚麻苦苷峰面积(mV·s) 1372.0 1372.3 1368.9 1371.1 1371.1 0.1 百脉根苷峰面积(mV·s) 314.9 291.8 300.9 301.9 302.4 3.1 2.4.3 样品稳定性试验
取任意一样品溶液,如表3所示,每隔4 h进样1次测定峰面积,进样后放置于4~8 ℃冰箱,计算24 h内样品中亚麻苦苷和百脉根苷的含量变化,其亚麻苦苷含量分别为1192.7、1218.4、1241.1、1194.1、1272.1、1328.1 mg/kg,百脉根苷含量分别为300.9、280.4、291.2、303.1、273.5、298.2 mg/kg,亚麻苦苷和百脉根苷的含量变化的RSD分别为4.7%、4.6%,表明样品在24 h内稳定性较好。
表 3 样品稳定性试验Table 3. The test of sample stability生氰糖苷(mg/kg) 1 2 3 4 5 6 平均 RSD(%) 亚麻苦苷含量 1192.7 1218.4 1241.1 1194.1 1272.1 1328.1 1241.1 4.7 百脉根苷含量 300.9 280.4 291.2 303.1 273.5 298.2 291.2 4.6 2.4.4 回收率试验
取木薯肉质块根和木薯粉样品分别12份,每份样品0.2000 g,分别取9个样品加入不同的提取溶液,再分别按表4中加入量的浓度加入3个浓度梯度的亚麻苦苷和百脉根苷标准混合溶液;另外,以3份样品不加入亚麻苦苷和百脉根苷标准样品作为对照检测本底量。所有样品按照提取和检测流程进行回收率试验,每梯度设置3个重复。以回收率=(测得量−加入量)/加入量计算回收率。样品回收率结果见表4所示:木薯块根样品中亚麻苦苷回收率在91.5%~96.3%之间,重复间RSD为2.6%,百脉根苷回收率在89.3%~95.4%之间,RSD为3.1%;木薯粉亚麻苦苷回收率在107.5%~114.9%之间,RSD为3.4%,百脉根苷回收率在108.6%~114.4%之间,重复间RSD为2.6%。样品中亚麻苦苷和百脉根苷加标回收率较好,方法准确度较高,可用于实际样品的测定。
表 4 方法的回收率Table 4. Recovery test for the method生氰糖苷 样品 本底量(mg/kg) 加入量
(mg/kg)测得量
(mg/kg)回收率
(%)平均回收率
(%)RSD
(%)亚麻苦苷 木薯肉质块根 14.7±0.9 27.3 41.0±2.1 96.3±3.5 93.7 2.6 54.7 64.2±0.9 91.5±1.3 109.3 116.6±4.1 93.2±4.6 木薯粉 59.7±1.2 54.7 118.5±1.1 107.5±2.0 111.7 3.4 109.3 188.6±7.9 114.9±4.9 164.0 253.2±12.4 112.8±7.5 百脉根苷 木薯肉质块根 5.5±0.3 16.7 20.7±0.7 91.0±4.0 91.9 3.1 33.3 35.3±0.3 89.3±1.0 66.7 69.2±0.1 95.4±1.7 木薯粉 7.0±0.4 16.7 18.3±1.6 108.6±5.6 111.3 2.6 33.3 36.9±2.0 110.8±4.2 66.7 75.3±6.0 114.4±6.3 注:数据格式为平均值±标准误。 2.5 样品验证
2.5.1 不同品种木薯块根中CNGs含量测定
研究表明[22],木薯中CNGs主要以亚麻苦苷和百脉根苷两种形式存在,分别占体内总量的95%~97%和3%~5%,不同的组织之间差异较大。通过样品考察发现:木薯肉质皮层亚麻苦苷和百脉根苷含量分别在407.9~2221.1、100.6~222.5 mg/kg之间;肉质块根亚麻苦苷和百脉根苷含量分别在106.5~713.8、0~46.6 mg/kg之间。3个木薯品种的块根中CNGs同样以亚麻苦苷为主,百脉根苷少量或检测不到,并且块根肉质皮层的CNGs含量远远高于肉质块根(表5)。同时,不同品种木薯块根CNGs的含量差异较大,亚麻苦苷高的木薯品种,百脉根苷含量同样也高,这可能与不同品种中亚麻苦苷酶活性有关。验证结果证明,建立的HPLC-ELSD方法可用于分析不同木薯品种中亚麻苦苷和百脉根苷。
表 5 不同木薯品种肉质皮层和肉质块根中CNGs含量Table 5. Cyanogenic glycosides contents in sweet cassava root cortex and root flesh of different varieties样品 品种 亚麻苦苷(mg/kg,FW) 百脉根苷(mg/kg,FW) 块根肉质皮层 SC9 2221.1± 151.8 214.2 ±12.7 SC12 972.8 ±28.5 222.5 ±14.2 SC6068 407.9 ±14.5 100.6 ±4.6 肉质块根 SC9 556.7 ±32.4 26.7 ±2.0 SC12 713.8 ±48.3 44.6 ±0.6 SC6068 106.5 ±6.7 ND 注:“ND”表示未检测到;表6同。 2.5.2 不同采收时期木薯粉中CNGs含量测定
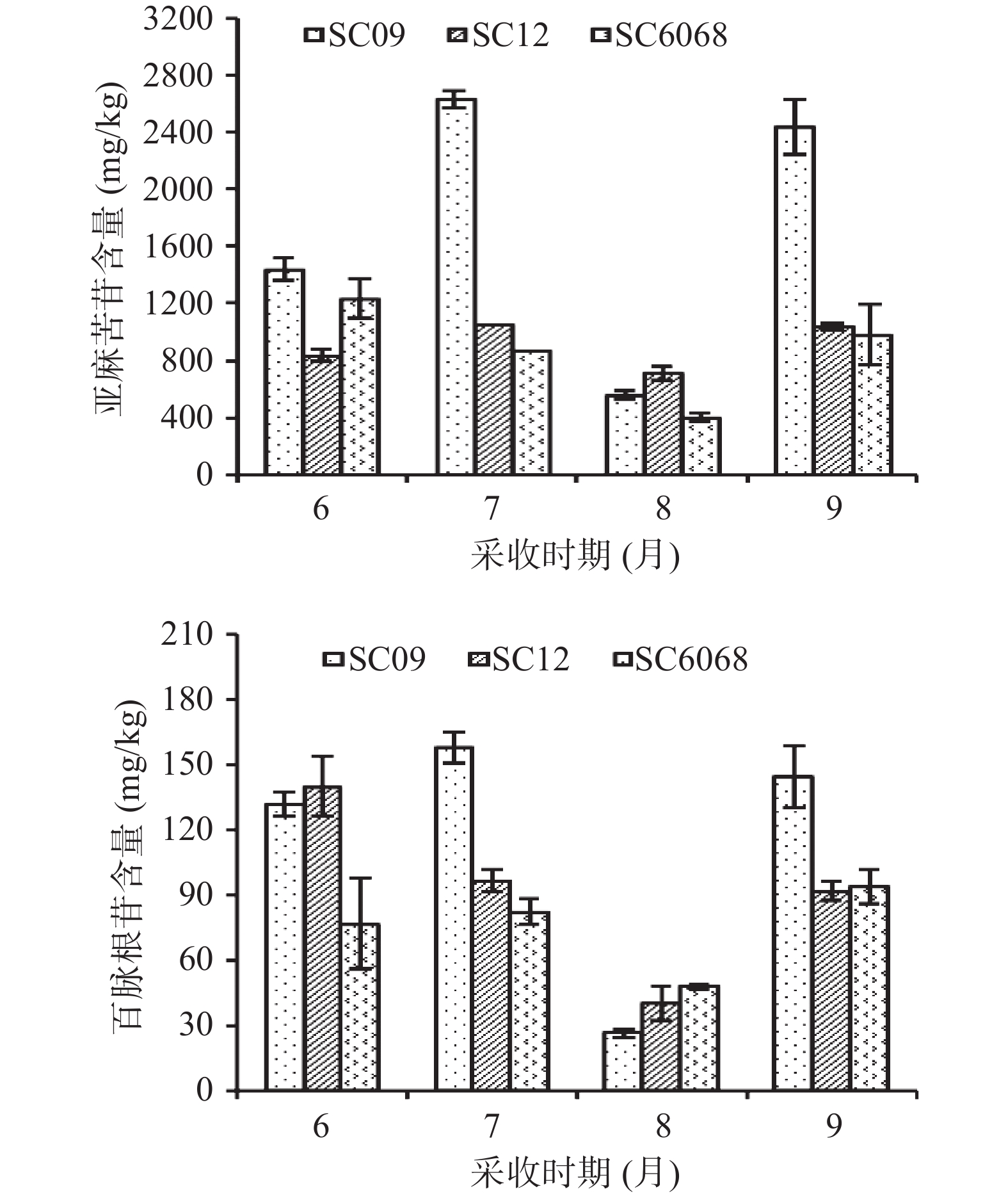
韩和悦[23]研究表明,木薯中CNGs含量受品种和采收时期的影响较大,木薯在进入成熟稳定期后,其CNGs含量相对较低,不同品种CNGs含量随采收时间的时空变化趋势也基本一致。由图4可知,木薯粉中主要的CNGs为亚麻苦苷,含量是百脉根苷的10倍左右。考察的3个品种不同采收时期制备的木薯粉中2种CNGs变化规律基本一致,种植6~8个月的木薯制备的木薯粉中2种CNGs含量都先升高再降低;在种植8个月时CNGs的含量为最低;在种植9个月以后,其CNGs的含量再次升高。形成这一趋势的原因可能是木薯种植8个月后,块根已充分膨大,各项代谢处于稳定状态,CNGs酶的活性也较低;而木薯块根进入后熟阶段后(9个月以上),木薯种植区气温开始下降,叶片开始脱落,块根生长处于稳定状态,CNGs稳定积累以抵御逆境[2,24]。SC9品种制备的木薯粉各个采收时期的CNGs含量相对较高,这与韩和悦的研究结果不同,这可能是由于不同的种植环境气候差异所致。样品验证结果发现,CNGs含量高的品种,相同的加工工艺制备木薯粉,其CNGs含量也较高(表6、图4)。因此,分析不同品种和不同采收时期木薯粉中CNGs含量变化,可作为提供木薯粉制作原料采收时期选择的依据。
表 6 木薯制品中CNGs含量及加工过程对产品的CNGS清除率Table 6. Content of CNGS in cassava products and the removal rate of CNGS in processed products样品名称 亚麻苦苷
(mg/kg,DW)百脉根苷
(mg/kg,DW)CNGs清除率
(%)木薯粉 450.8±29.6 96.6±5.2 0 木薯饼干 199.2±12.7 ND 63.6 木薯蛋糕 151.8±9.7 ND 72.3 木薯面条 99.5±5.6 ND 81.8 木薯馒头 ND ND 100.0 木薯年糕 ND ND 100.0 2.5.3 木薯粉食品中CNGs含量测定
实验分析了木薯粉加工为不同食品后CNGs含量变化。分析发现,木薯粉中存在2种CNGs,亚麻苦苷和百脉根苷含量分别为450.8、96.6 mg/kg;木薯粉加工的食品中仅检测到亚麻苦苷,木薯饼干、木薯面条和木薯蛋糕中亚麻苦苷含量分别为199.2、151.8和99.5 mg/kg。并以木薯食品中CNGs清除率=(木薯粉CNGs总含量-木薯粉加工后CNGs总含量)/木薯粉CNGs总含量,分析了加工对木薯食品中CNGs清除率的影响,木薯饼干、蛋糕、面条、馒头和年糕在加工过程中CNGs清除率分别为63.6%、72.3%、81.8%、100.0%和100.0%(表6)。有研究表明,通过剥去块根肉质皮层,浸泡、晾晒、蒸煮、烘干、油炸等方式[4,25-28],可以有效地清除食品中大部分氰化物,特别是木薯食品加工和食用过程中,剥去块根肉质皮层可有效降低氰化物含量[26]。但不同的加工方式,其氰化物的清除率不同[29]。研究者认为,降低木薯及其制品中HCN含量需要从选择好的品种,适时采收,充分加工,遵循良好生产操作规范出发[30]。本实验结果也显示,木薯粉在制作不同的食品过程中,不同的加工方式CNGs降解程度不同,证明选择合适的加工方式,可以有效清除木薯食品中的CNGs。
3. 结论
实验通过提取液硫酸浓度的优化,确定了食用木薯块根及木薯粉中CNGs提取的最佳提取浓度分别为0.025和0.100 mol/L,该提取方法简单、安全、重复性好,可应用于木薯块根及其制品中CNGs快速提取;通过色谱检测参数的优化,建立了一种同时分析木薯块根及其制品中亚麻苦苷和百脉根苷的HPLC-ELSD检测方法,该方法重复性和稳定性较好,可应于木薯中CNGs种类和含量差异分析。样品分析结果证明,木薯品种、生长期和加工方式对木薯新鲜块根及其制品中CNGs含量的都有影响。该方法的建立,有助于育种工作者利用CNGs的含量对资源的分类、选择和利用;有助于加工研究者根据品种、采收时期CNGs的含量差异,选择合适加工工艺以降低其食品中CNGs含量,并为后期木薯食品的开发和食用安全评价提供理论参考。
-
表 1 2种CNGs的线性范围、相关性、检出限和定量限
Table 1 Linear range, correlation, detection limit and quantification limit of the two CNGs
生氰糖苷 线性范围
(mg/L)回归方程 相关系数
(r)检出限(mg/kg) 定量限
(mg/kg)亚麻苦苷 4.1~820.0 lgY=1.4456(lgX)−0.5363 0.9996 2.1 8.2 百脉根苷 2.5~250.0 lgY=1.4494(lgX)−0.3571 0.9993 0.5 2.0 表 2 仪器精密度试验
Table 2 The test of instrument precision
生氰糖苷 1 2 3 4 平均 RSD(%) 亚麻苦苷峰面积(mV·s) 1372.0 1372.3 1368.9 1371.1 1371.1 0.1 百脉根苷峰面积(mV·s) 314.9 291.8 300.9 301.9 302.4 3.1 表 3 样品稳定性试验
Table 3 The test of sample stability
生氰糖苷(mg/kg) 1 2 3 4 5 6 平均 RSD(%) 亚麻苦苷含量 1192.7 1218.4 1241.1 1194.1 1272.1 1328.1 1241.1 4.7 百脉根苷含量 300.9 280.4 291.2 303.1 273.5 298.2 291.2 4.6 表 4 方法的回收率
Table 4 Recovery test for the method
生氰糖苷 样品 本底量(mg/kg) 加入量
(mg/kg)测得量
(mg/kg)回收率
(%)平均回收率
(%)RSD
(%)亚麻苦苷 木薯肉质块根 14.7±0.9 27.3 41.0±2.1 96.3±3.5 93.7 2.6 54.7 64.2±0.9 91.5±1.3 109.3 116.6±4.1 93.2±4.6 木薯粉 59.7±1.2 54.7 118.5±1.1 107.5±2.0 111.7 3.4 109.3 188.6±7.9 114.9±4.9 164.0 253.2±12.4 112.8±7.5 百脉根苷 木薯肉质块根 5.5±0.3 16.7 20.7±0.7 91.0±4.0 91.9 3.1 33.3 35.3±0.3 89.3±1.0 66.7 69.2±0.1 95.4±1.7 木薯粉 7.0±0.4 16.7 18.3±1.6 108.6±5.6 111.3 2.6 33.3 36.9±2.0 110.8±4.2 66.7 75.3±6.0 114.4±6.3 注:数据格式为平均值±标准误。 表 5 不同木薯品种肉质皮层和肉质块根中CNGs含量
Table 5 Cyanogenic glycosides contents in sweet cassava root cortex and root flesh of different varieties
样品 品种 亚麻苦苷(mg/kg,FW) 百脉根苷(mg/kg,FW) 块根肉质皮层 SC9 2221.1± 151.8 214.2 ±12.7 SC12 972.8 ±28.5 222.5 ±14.2 SC6068 407.9 ±14.5 100.6 ±4.6 肉质块根 SC9 556.7 ±32.4 26.7 ±2.0 SC12 713.8 ±48.3 44.6 ±0.6 SC6068 106.5 ±6.7 ND 注:“ND”表示未检测到;表6同。 表 6 木薯制品中CNGs含量及加工过程对产品的CNGS清除率
Table 6 Content of CNGS in cassava products and the removal rate of CNGS in processed products
样品名称 亚麻苦苷
(mg/kg,DW)百脉根苷
(mg/kg,DW)CNGs清除率
(%)木薯粉 450.8±29.6 96.6±5.2 0 木薯饼干 199.2±12.7 ND 63.6 木薯蛋糕 151.8±9.7 ND 72.3 木薯面条 99.5±5.6 ND 81.8 木薯馒头 ND ND 100.0 木薯年糕 ND ND 100.0 -
[1] BANEA-MAYAMBU J P, TYLLESKAR T, GITEBO N, et al. Geographical and seasonal association between linamarin and cyanide exposure from cassava and the upper motor neurone disease konzo in former Zaire[J]. Tropical Medicine & International Health,1997,2(12):1143−51.
[2] CRESSEY P, REEVE J. Metabolism of cyanogenic glycosides: A review[J]. Food and Chenical Toxicology,2019,125(3):225−232.
[3] OLUWOLE O S A, ONABOLU A O, LINK H, et al. Persistence of tropical ataxic neuropathy in a Nigerian community[J]. Journal of Neurology, Neurosurgery & Psychiatry,2000,69(1):96−101.
[4] BRADBURY J H, DENTON I C. Rapid wetting method to reduce cyanogen content of cassava flour[J]. Food Chemistry,2010,121(2):591−594. doi: 10.1016/j.foodchem.2009.12.053
[5] KASSA R M, KASENSA N L, MONTERROSO V H, et al. On the biomarkers and mechanisms of konzo, a distinct upper motor neuron disease associated with food (cassava) cyanogenic exposure[J]. Food and Chemical Toxicoligy,2011,49(3):571−578. doi: 10.1016/j.fct.2010.05.080
[6] BRADBURY J H, DENTON I C. Simple method to reduce the cyanogen content of gari made from cassava[J]. Food Chemistry,2010,123(3):840−845. doi: 10.1016/j.foodchem.2010.05.020
[7] 张烨, 王珂, 刘石生. 外源β-葡萄糖苷酶处理结合异烟酸-吡唑啉酮分光光度法测定橡胶籽中氰化物含量[J]. 食品科学,2017,38(14):290−296. [ZHANG Y, WANG K, LIU S S. Spectrophotometric determination of cyanide content in rubber seeds using isonicotinic acid-pyrazolone after exogenous β-glucosidase pretreatment[J]. Food Science,2017,38(14):290−296. doi: 10.7506/spkx1002-6630-201714045 [8] BRADBURY M G, GAN S V E, BRADBURY J H. Picrate paper kits for determination of total cyanogens in cassava roots and all forms of cyanogens in cassava products[J]. Journal of the Science of Food and Agriculture,1999,79(4):593−610. doi: 10.1002/(SICI)1097-0010(19990315)79:4<593::AID-JSFA222>3.0.CO;2-2
[9] STOCHMAL A, OLESZEK W. Determination of c yanogenic glucosides in white clover (Trfolium repens L.) by high performance liquid chromatography[J]. Phytochemical Analysis,1994,5(5):271−272. doi: 10.1002/pca.2800050511
[10] SORNYOTHA S, KYU K L, RATANAKHANOKCHAI K. Purification and detection of linamarin from cassava root cortex by high performance liquid chromatography[J]. Food Chemistry,2007,104(4):1750−1754. doi: 10.1016/j.foodchem.2006.10.071
[11] 邹良平, 起登凤, 李玖慧, 等. 高效液相色谱-蒸发光检测法测定木薯生氰糖苷的含量[J]. 中国农学通报,2014,30(24):47−51. [ZOU L P, QI D F, LI J H, et al. Using high performance liquid chromatography (HPLC)-evaporative light detector assay for content determination of cyanogenic glucosides in cassava[J]. Chinese Agricultural Science Bulletin,2014,30(24):47−51. doi: 10.11924/j.issn.1000-6850.2014-0070 [12] ZHONG Y, XU T, CHEN Q, et al. Development and validation of eight cyanogenic glucosides via ultra-highperformance liquid chromatography-tandem mass spectrometry in agri food[J]. Food Chemistry,2020,331(30):1−7.
[13] MUZASHVILI T, MONIUSZKO-SZAJWAJ B, PECIO L, et al. Ultraperformance liquid chromatography tandem mass spectrometry determination of cyanogenic glucosides in trifolium species[J]. Journal of Agricultural and Food Chenistry,2014,62(8):1777−1782. doi: 10.1021/jf4056659
[14] 刘易, 陈佳, 朱颖洁, 等. 基于表面增强拉曼光谱和顶空-气相色谱/氮磷检测技术的生氰糖苷类中成药中游离态氰化物含量测定[J]. 药物分析杂志,2018,38(7):1202−1209. [LIU Y, CHEN J, ZHU Y J, et al. Determination of free cyanide in Chinese patent medicines of cyanogenic glycosides based on surface-enhanced Raman spectroscopy and headspace/ gas chromatography-nitrogen and phosphorus detection techniques[J]. Chin J Pharm Anal,2018,38(7):1202−1209. [15] 周新成, 陈新, 卢诚, 等. 木薯叶片和块根中氰苷的快速提取[J]. 现代农业科技,2020(24):214−216, 220. [ZHOU X C, CHEN X, LU C, et al. Quick extraction of cyanogenic glycoside from cassava leaves and storage roots[J]. Modern Agricultural Technology,2020(24):214−216, 220. doi: 10.3969/j.issn.1007-5739.2020.24.085 [16] 张振文, 林立铭, 徐缓, 等. 细度对食用木薯粉理化品质和消化特性的影响[J]. 中国粮油学报,2020,35(8):56−61. [ZHANG Z W, LIN L M, XU H, et al. Effects of physic-chemical traits and digestion characteristics on sweet cassava flour with different size[J]. Journal of the Chinses cereals and Oils Association,2020,35(8):56−61. doi: 10.3969/j.issn.1003-0174.2020.08.010 [17] 张振文, 李开绵. 木薯及其食品加工技术[M]. 北京. 中国农业出版社, 2019: 65−105. ZHANG Z W, LI K M. Cassava and its food processing technology [M]. Beijing: China Agriculture Press, 2019: 65−105.
[18] 冯埃生, 邹汉法, 汪海林, 等. 影响高效液相色谱/挥发激光散射检测器检测性能基本因素的考察[J]. 药物分析杂志,1996,16(6):54−57. [FENG A S, ZOU H F, WANG H L, et al. Investigation of the basic factors affecting the detection performance of high performance liquid chromatography/volatile laser scattering detector[J]. Chinese Journal of Pharmaceutical Analysis,1996,16(6):54−57. [19] 王巧娥, 丁明玉. 蒸发光散射检测技术研究进展[J]. 分析测试学报,2006,25(6):126−132. [WANG Qiaoe, DING Mingyu. Progress on evaporative light-scattering detection[J]. Journal of Instrumental Analysis,2006,25(6):126−132. doi: 10.3969/j.issn.1004-4957.2006.06.036 [20] BRADBURY J H. Development of a sensitive picrate method to determine total cyanide and acetone cyanohydrin contents of gari from cassava[J]. Food Chemistry,2009,113(4):1329−1333. doi: 10.1016/j.foodchem.2008.08.081
[21] 王琴飞, 蔡坤, 林立铭, 等. 木薯茎杆基质比例对3种食用菌海藻糖含量的影响[J]. 食品科学,2016,37(18):102−106. [WANG Q F, CAI K, LIN L M, et al. Effect of cassava stalk substrate ratio on trehalose content in three cultivated edible fungi[J]. Food Science,2016,37(18):102−106. doi: 10.7506/spkx1002-6630-201618017 [22] NAMBISAN B, SUNDARESAN S. Distribution of linamarin and its metabolizing enzymes in cassava tissues[J]. Journal of the Science of Food & Agriculture,1994,66(4):503−507.
[23] 韩和悦. 11个食用木薯品种的品质研究与评价[D]. 广州: 仲恺农业工程学院, 2017. HAN H Y. Research and evaluation of 11 edible cassava breed’ quality[D]. Guangzhou: Zhongkai University of Agriculture and Engineering, 2017.
[24] 黄洁, 周建国. 木薯间套作与高效利用技术[M]. 海口: 海南出版社, 2015: 35. HUANG J, ZHOU J G. Intercropping and high benefit utilization of cassava[M]. Haikou: Hainan Publishing House, 2015, 35.
[25] 田静, 朱琳, 董朝霞, 等. 处理方法对木薯块根氢氰酸含量和营养成分的影响[J]. 草地学报,2017,25(4):875−879. [TIAN J, ZHU L, DONG Z X, et al. Effects of treatment methods on the hydrocyanic acid content and nutrient composition of cassava roots[J]. Acta Agrestia Sinica,2017,25(4):875−879. [26] 刘畅, 陈宇, 刘石生. 不同处理方法对木薯中氰化物残留的影响[J]. 食品科技,2014,39(12):190−193. [LIU C, CHEN Y, LIU S S. Different processing methods on the effect of cyanide residue in the cassava[J]. Food Science and Technology,2014,39(12):190−193. [27] BRADBURY J H, DENTON I C. Mild methods of processing cassava leaves to remove cyanogens and conserve key nutrients[J]. Food Chemistry,2011,127(4):1755−1759. doi: 10.1016/j.foodchem.2011.02.053
[28] NAMBISAN, B. Strategies for elimination of cyanogens from cassava for reducing toxicity and improving food safety[J]. Food and Chemical Toxicology,2011,49(3):690−693. doi: 10.1016/j.fct.2010.10.035
[29] 熊丽娜, 陆柏益. 农产品中生氰糖苷安全性及减控技术研究进展[J]. 中国食品学报,2014,14(2):208−216. [XIONG L N, LU B Y. Security and removal methods of cyanogenic glycoside in agricultural products[J]. Journal of Chinese Institute of Food Science and Technology,2014,14(2):208−216. [30] 钟永恒, 陆柏益, 李开绵. 木薯质量安全、营养品质与加工利用新进展[J]. 中国食品学报,2019,19(6):284−292. [ZHONG Y H, LU B Y, LI K M. Research advances on the safety, nutrition and processing of cassava[J]. Journal of Chinese Institute of Food Science and Technology,2019,19(6):284−292.





 下载:
下载:
 下载:
下载:
