Effects of Conjugated Linoleic Acid on Lipid Accumulation and Intestinal Microbiota in Obese Rats Induced by High-fat Diet
-
摘要: 目的:以高脂饲料诱导建立肥胖大鼠模型,探讨共轭亚油酸(CLA)干预对肥胖大鼠脂质蓄积和肠道菌群的影响。方法:将40只SPF级雄性SD大鼠按体重随机分为四组,每组10只,除对照组(ND组)以普通饲料喂养外,其余组均以高脂饲料喂养。其中ND组灌胃花生油1 g/kg;高脂模型组(HD组)灌胃花生油1 g/kg;高脂共轭亚油酸低剂量组(LC组)灌胃0.2%共轭亚油酸1 g/kg;高脂共轭亚油酸高剂量组(HC组)灌胃2%共轭亚油酸1 g/kg,干预9周。于实验末采集大鼠粪便后提取粪便中细菌DNA后进行16S rDNA测序,之后麻醉采血后处死,取肝脏、肾周脂肪和睾周脂肪组织,于−80 ℃保存。结果:HD组大鼠体重、内脏脂肪、血清和肝脏甘油三酯和总胆固醇显著高于ND组(P<0.05),高剂量共轭亚油酸干预可显著降低大鼠体重、血清甘油三酯和总胆固醇及肝脏总胆固醇(P<0.05);高脂饲料诱导可使大鼠肠道菌群属水平中Eubacterium_coprostanoligenes_group(真杆菌属)、Psychrobacter(嗜冷杆菌属)、Corynebacterium_1(棒状杆菌_1)、Staphylococcus(葡萄球菌属)的相对丰度增加;高剂量CLA干预可改变肥胖大鼠的肠道菌群的组成,如在属水平上显著增加了Bifidobacterium(双歧杆菌属)、Butyrivibrio(丁酸弧菌属)、Ruminococcaceae_UCG-014(瘤胃球菌科_UCG-014)等的相对丰度(P<0.05),减少了Staphylococcus(葡萄球菌属)、Corynebacterium_1(棒状杆菌_1)等的相对丰度(P<0.05)。结论:共轭亚油酸可降低高脂饲料诱导肥胖大鼠的体重和脂质蓄积,其作用可能与调节大鼠肠道菌群组成有关。Abstract: Objective: To investigate the effects of conjugated linoleic acid (CLA) on lipid accumulation and intestinal microbiota in obese rats. Methods: Forty SPF male SD rats were randomly divided into four groups according to body weight, 10 rats in each group. The ND group was fed with ordinary diet, and the other groups were fed with high-fat diet. Among them, the ND group was intragastrically administered with peanut oil 1 g/kg, the model group (HD group) was intragastrically administered with peanut oil 1 g/kg, the low-dose group (LC group) was intragastrically administered with 0.2% conjugated linoleic acid 1 g/kg, and the high-dose group (HC group) was intragastrically administered with 2% conjugated linoleic acid 1 g/kg for 9 weeks of intervention. Bacterial DNA was extracted from feces of mice after collection of feces at the end of the experiment followed by 16S rDNA sequencing, after which blood was collected and sacrificed under anesthesia, and organ and visceral fat were taken and stored at −80 ℃. Results: The body weight, visceral fat, serum and liver triglycerides and total cholesterol of rats in the HD group were significantly higher than those in the ND group (P<0.05), and high-dose CLA intervention could significantly reduce the body weight, serum triglycerides, total cholesterol and liver total cholesterol of rats (P<0.05). High-fat diet could increase the relative abundance of Eubacterium_coprostanoligenes_group, Psychrobacter, Corynebacterium_1 and Staphylococcus in the intestinal microbiota level of rats. High-dose CLA could change the composition of intestinal microbiota in obese rats, such as significantly increasing the relative abundance of Bifidobacterium, Butyrivibrio and Ruminococcaceae_UCG-014 at the genus level (P<0.05) and reducing the relative abundance of Staphylococcus and Corynebacterium_1 (P<0.05). Conclusion: Conjugated linoleic acid could reduce body weight and lipid accumulation of obese rats induced by high fat diet, which might be related to the regulation of intestinal microbiotal diversity.
-
Keywords:
- conjugated linoleic acid /
- obesity /
- intestinal microbiota /
- lipid
-
肥胖是一种由多因素引起的慢性代谢性疾病,其会引起一系列健康问题。随着人们生活方式的改变,能量摄入和消耗不平衡引起肥胖患病率急剧上升。流行病学调查显示中国成年人肥胖的患病率为14%,其中男性的患病率为14%,女性为14.1%;腹部肥胖患病率为35.1%,男性患病率为30.7%,女性为32.4%[1]。全球范围内,目前有13亿人超重或肥胖[2],肥胖已经成为重要的全球公共卫生问题。
近年来,多项研究表明肠道菌群紊乱与肥胖等代谢性疾病发生发展密切相关[3-5],肠道菌群在肥胖中的作用引起人们广泛关注。共轭亚油酸(Conjugated linoleic acid,CLA)是亚油酸的同分异构体,是具有共轭不饱和双键的亚油酸位置异构体和几何异构体混合物的总称[6]。其中cis9、trans11-CLA和trans10、cis12-CLA是两种主要异构体[7]。CLA的主要天然食品来源是反刍动物的肉类和乳制品[8]。有研究表明,共轭亚油酸可以在改善肥胖和脂代谢等方面发挥有益作用[9-12],但其对于肥胖的具体机制和对健康的影响还有待进一步讨论。此外,CLA还可通过增强肠道免疫力,发挥调节肠道稳态的作用[13]。另有文献报道,肠道沙门氏菌中的跨膜组氨酸激酶受体PhoQ可作为长链不饱和脂肪酸(如CLA)的受体,而该受体对于沙门氏菌在肠道中的定植起到至关重要的作用[14],因此推测CLA可通过竞争受体进而影响沙门氏菌等有害菌在肠道的定植。另外一项研究发现接种产CLA的干酪乳酸菌可以预防沙门氏菌引起的肠道紊乱[15]。因此,CLA可以在一定程度上影响肠道菌群构成,但是目前尚未见有关CLA对高脂饲料喂养大鼠脂质蓄积的预防作用以及与肠道菌群关系的研究报道。本研究通过采用脂肪供能比为45%的高脂饲料诱导建立大鼠肥胖模型,采用预防性给予CLA灌胃的方式,观察其对肥胖大鼠脂质蓄积及肠道菌群构成的影响,从而为CLA通过影响肠道菌群进而起到预防肥胖的作用机制提供线索。
1. 材料与方法
1.1 材料与仪器
雄性SPF级SD大鼠 40只,6周龄,体重150 g左右,福建医科大学动物中心(福建福州,动物许可号:SCXK(闽)2016-0002);共轭亚油酸 其中c9、t11-CLA占38.6%,t10、c12-CLA占37.8%,其余异构体占4.5%,棕榈酸占4.0%,硬脂酸占2.5%,油酸占9.7%,亚油酸占1.9%,酸值196.9,购自青岛澳海生物有限公司;总胆固醇测试盒、甘油三酯测试盒 南京建成生物工程研究所;45%棕榈油高脂饲料 南通特洛菲饲料科技有限公司(饲料代码:TP0861A),饲料配方:普通饲料49%,酪蛋白17%,糖10%,棕榈油20%,纤维素1%,维生素和矿物质4%,饲料能量4.3 kcal/g,总能量占比中蛋白质为22%,脂肪为45%,碳水化合物为33%。
Satorius BS 224S电子天平 赛多利斯科学仪器有限公司;XB160M-SCS电子天平 瑞士Precisa公司;Z323K型台式冷冻高速离心机 德国HERMLE公司;TG16-WS台式高速离心机 湖南湘仪实验室仪器开发有限公司;其林贝尔XW-80A旋涡混合器 上海巴玖实业有限公司;Multisakn go酶标仪 美国赛默飞世尔科技有限公司。
1.2 实验方法
1.2.1 动物分组及处理
将40只SPF级雄性SD大鼠按体重随机分为四组,每组10只,除对照组(ND组)以普通饲料喂养外,其余组均以高脂饲料喂养。其中ND组和高脂模型组(HD组)均灌胃花生油1 g/kg;高脂共轭亚油酸低剂量组(LC组)和高脂共轭亚油酸高剂量组(HC组)分别灌胃以花生油稀释的0.2%和2%共轭亚油酸1 g/kg BW,共干预9周。实验期间各组大鼠自由摄食和饮水,符合福建医科大学实验动物伦理委员会要求。
1.2.2 血清和肝脏生化指标测定
实验末,将各组大鼠禁食12 h后,使用干冰麻醉大鼠后心脏采血,血液样本室温静置1 h后,3000 r/min,离心10 min,取血清样本待测;将大鼠处死后,剖检采集肝脏组织、肾周脂肪和睾周脂肪组织,并用电子天平测定脂肪重量;取肝脏组织样本,加入无水乙醇制备10%的肝匀浆,冰水浴条件下进行组织匀浆,2500 r/min,离心10 min,取上清液待测,按照试剂盒说明书分别测定血清和肝脏样本中的TC和TAG,计算各指标含量。
1.2.3 粪便微生物提取及16S rDNA测序
实验末无菌采集大鼠粪便,于−80 ℃保存。采集的粪便样本委托上海百趣生物医学科技有限公司进行粪便微生物16S rDNA测序。测序过程如下:提取样品总DNA后,用细菌16S rRNA (V3+V4)区域引物(5'-ACTCCTACGGGAGGCAGCA-3'和5'-GGACTACHVGGGTWTCTAAT-3')进行PCR扩增,扩增条件为95 ℃预变性5 min,15个循环(95 ℃变性1 min,50 ℃退火1 min,72 ℃延伸1 min),最后72 ℃延伸7 min。获取PCR产物后,用1.8%的琼脂糖凝胶回收PCR产物,然后对其产物进行纯化,纯化步骤如下:样品与磁珠按照1:1混匀后进行磁珠筛选片段,35 μL洗脱。向PCR产物中加入50 μL的磁珠,混匀室温5 min后,置于磁力架上5 min,去上清;加入200 μL的80%乙醇清洗磁珠,室温30 s后弃上清,重复此步骤一次;置磁力架上干燥3 min,用37 μL双蒸水重悬磁珠,室温孵育2 min,置于磁力架上2 min,吸取35 μL上清至新的PCR管中。电泳结束后,用ImageJ软件定量。根据Illumina HiSeq 2500进行测序得到的原始图像数据文件,经碱基识别分析转化为原始测序序列,结果以FASTQ文件格式存储,其中包含测序序列的序列信息以及其对应的测序质量信息用于后续数据分析。
1.3 数据处理
采用IBM SPSS 20.0软件对数据进行统计分析,结果以
2. 结果与分析
2.1 CLA干预对大鼠体重的影响
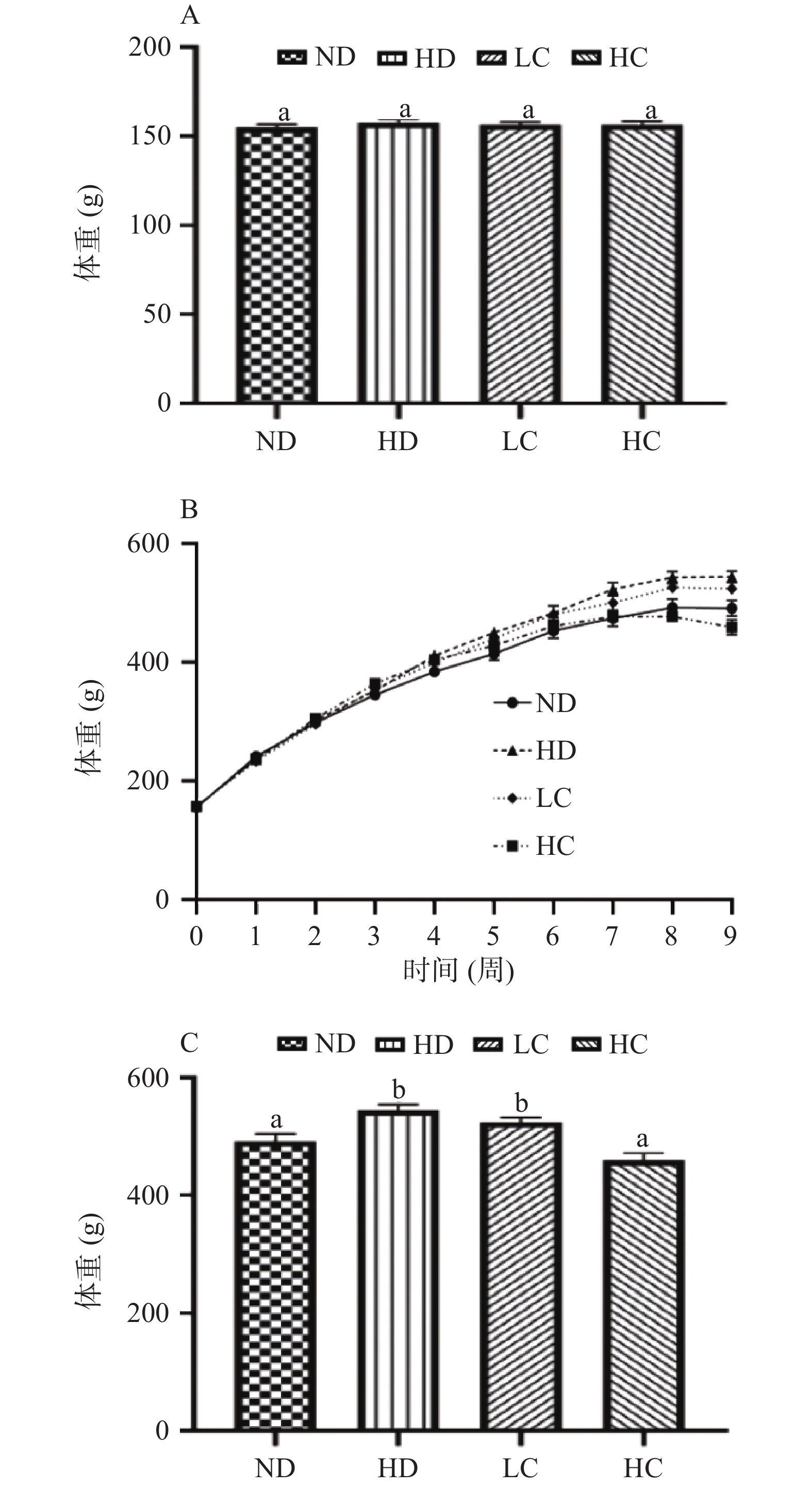
如图1A所示,4组大鼠的初始体重无显著性差异(P>0.05)。图2B显示了各组的体重变化趋势,可以看出干预期间大鼠体重逐渐增加,而HC组在干预第8周开始体重出现下降趋势。干预9周后,与ND组比较,HD组大鼠体重显著增加(P<0.05)。与HD组相比,HC组大鼠体重显著降低(P<0.05),而LC组体重并无显著性差异(P>0.05)。结果表明预防性给予高剂量CLA可抑制高脂饲料喂养大鼠体重增长。
2.2 CLA对SD大鼠内脏脂肪重量及血生化指标的影响
由表1可见,与ND组相比,高脂饲料诱导可显著升高大鼠肾周脂肪、睾周脂肪重量,升高血清TC和TAG水平,证实高脂模型组造模成功。与HD组相比,低剂量CLA干预对大鼠肾周脂肪、睾周脂肪重量、血清TAG、肝脏TC和肝脏TAG无显著影响(P>0.05),但能降低血清TC水平(P<0.05);高剂量CLA干预可显著降低大鼠肾周及睾周脂肪重量,降低血清TC、TAG和肝脏TC水平(P<0.05),但对肝脏TAG水平无显著影响(P>0.05)。以上结果表明高剂量CLA可预防高脂饲料喂养引起的大鼠内脏脂肪含量增加。此外,CLA干预后大鼠血清TC、TAG和肝脏TC水平明显降低,说明CLA同时可预防大鼠血清TAG和TC的蓄积,该结果与其他研究的人群和动物研究结果相近[12,16-19]。
表 1 干预9周后各组大鼠内脏脂肪重量及生化指标Table 1. Visceral fat and blood lipid levels of SD rats in each group after 9 weeks of intervention分组 ND组 HD组 LC组 HC组 肾周脂肪重量(g) 6.97±0.89a 13.49±0.67c 11.83±0.74bc 10.39±1.21b 睾周脂肪重量(g) 6.59±0.67a 11.86±0.77c 10.71±0.76bc 8.84±0.41b 血清TC(mmol/L) 4.34±0.44a 6.34±0.31b 4.78±0.40a 3.77±0.23a 血清TAG(mmol/L) 2.41±0.19a 2.95±0.08b 2.60±0.19ab 2.13±0.13a 肝脏TC(mmol/L) 4.57±0.14a 7.19±0.57c 6.34±0.10bc 6.21±0.23b 肝脏TAG(mmol/L) 8.43±0.82a 12.34±0.60b 12.01±0.6b 12.88±1.04b 注:以上数据以±SEM的形式表示,不同字母表示组间差异有统计学意义,P<0.05;表2同。 2.3 CLA对肠道菌群多样性及结构的作用
2.3.1 肠道菌群的α和β多样性分析
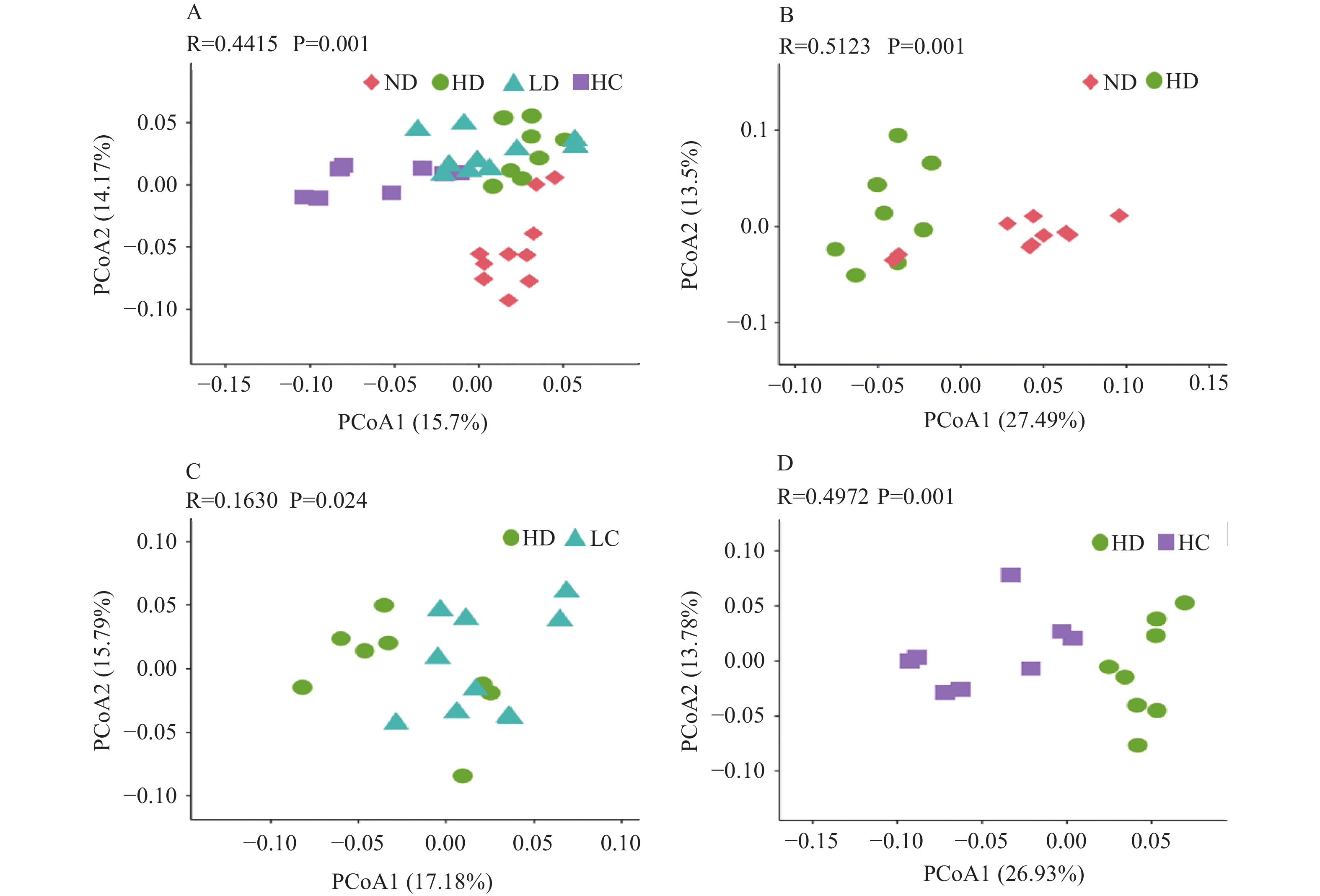
α多样性反映的是单个样品物种丰度及物种多样性,Chao1和Ace指数是用于衡量物种丰富度的指标,Chao1和Ace指数越大,说明物种的丰富度越高。Shannon和Simpson指数用于衡量物种多样性,Shannon指数和Simpson指数值越大,说明物种多样性越高。由表2可见,Ace指数分析显示,高剂量CLA的菌群多样性指数与高脂模型组比较显著降低(P<0.05),而低剂量CLA的菌群多样性指数与对照组无显著性差异(P>0.05);Chao 1指数分析显示,高剂量CLA的菌群多样性与高脂模型组比较显著降低(P<0.05),而与对照组的菌群多样性无显著性差异(P>0.05);Shannon指数和Simpson指数显示了各组的肠道菌群多样性无显著性差异(P>0.05),说明高脂饲料和CLA对肠道菌群的多样性无明显影响。β多样性反映了不同组之间的丰度差异,如图2所示,四组间β多样性的差异具有统计学意义(P<0.05),高脂模型组和对照组的肠道菌群组成有显著性差异(P<0.05),高脂模型组和高剂量CLA组的肠道菌群组成的差异具有统计学意义(P<0.05),说明高脂模型组和对照组的肠道菌群组成有明显差异,且CLA可以明显改变受到高脂饲料影响的肠道菌群组成。
表 2 肠道菌群的α多样性分析Table 2. Alpha diversity analysis of intestinal microbiota分组 ND组 HD组 LC组 HC组 Ace指数 790.260±6.757b 796.479±5.416b 800.021±6.385b 759.443±10.712a Chao 1指数 795.571±7.396ab 806.056±7.771b 810.629±5.593b 773.603±12.038a Shannon指数 0.967±0.003a 0.967±0.007a 0.962±0.004a 0.965±0.008a Simpson指数 6.621±0.071a 6.666±0.218a 6.556±0.121a 6.593±0.101a 2.3.2 肠道菌群组成差异分析
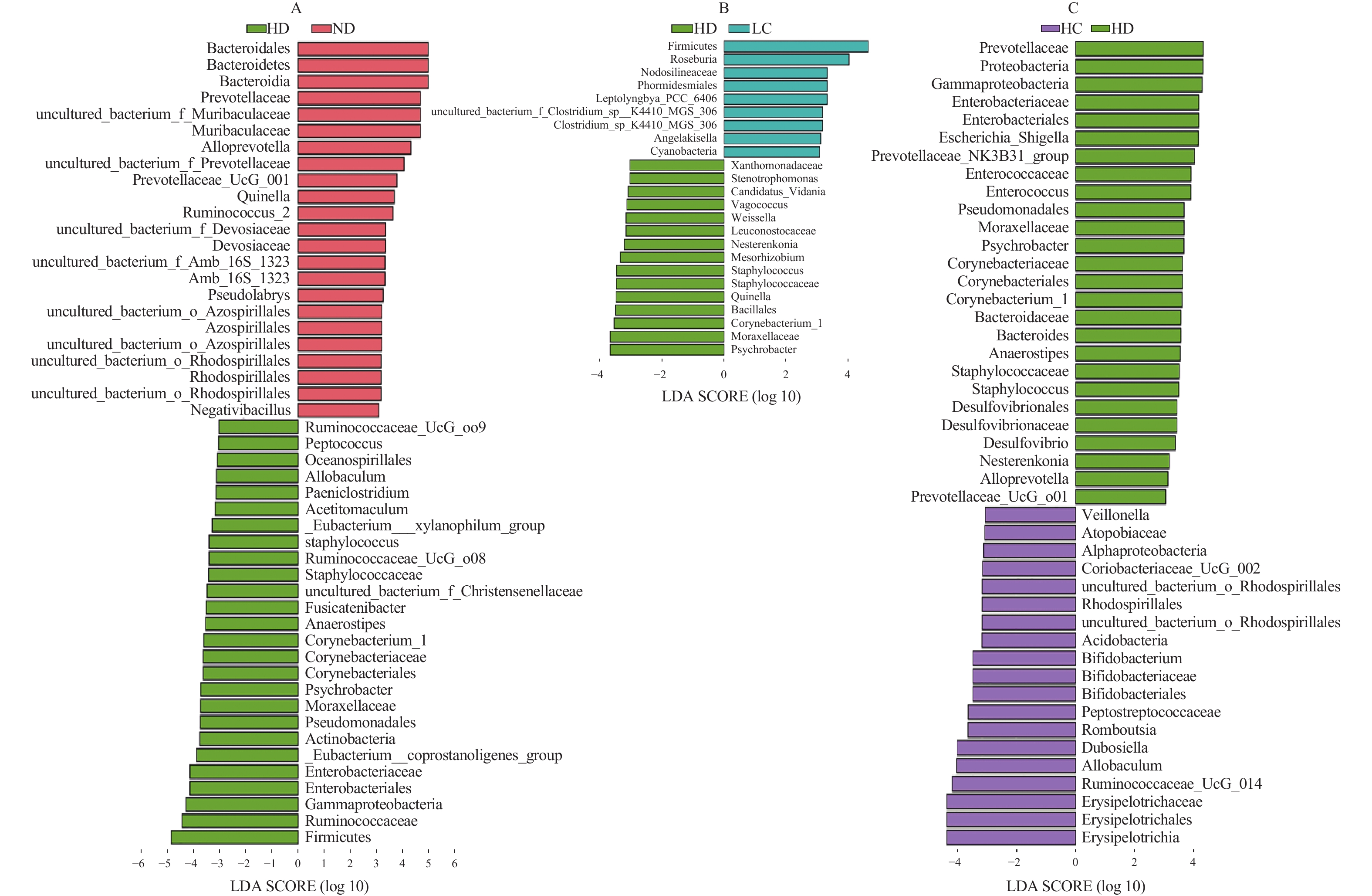
为进一步分析四组肠道菌群组成差异,采用LEfSe分析进行两两比较,ND与HD组相比,在属水平上,ND组的主要菌群为Alloprevotella(拟普雷沃菌属)、Prevotellaceae_UCG_001(普雷沃氏菌科_UCG-001)、Ruminococcus_2(瘤胃球菌属_2),HD组主要菌群为Eubacterium_coprostanoligenes_group
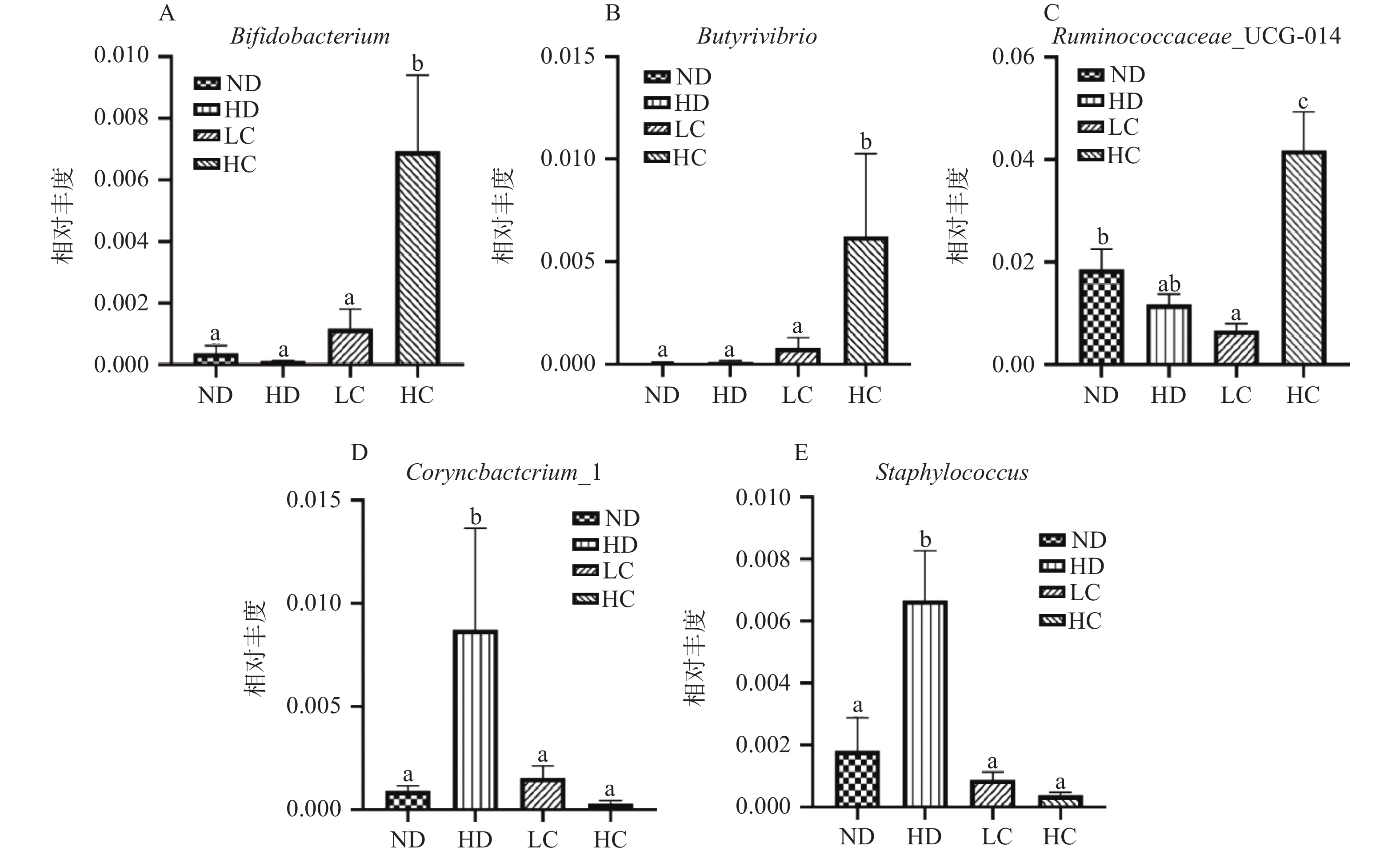
(真杆菌属)、Psychrobacter(嗜冷杆菌属)、Corynebacterium_1(棒状杆菌属_1)、Staphylococcus(葡萄球菌属)(图3A);LC与HD组相比,在属水平上,LC组的主要菌群为Roseburia(罗氏菌属)、Leptolyngbya_PCC_6406(瘦鞘丝藻属_PCC_6406)、uncultured_bacterium_f_Clostridium_sp__K4410_MGS_306(未分类的梭菌属),HD组的主要菌群为Psychrobacter(嗜冷杆菌属)、Corynebacterium_1(棒状杆菌属_1)、Staphylococcus(葡萄球菌属)(图3B);HC与HD组相比,在属水平上,HC组的主要菌群为Ruminococcaceae_UCG_014(瘤胃球菌科_UCG_014)、Romboutsia(罗姆布茨菌属)、Bifidobacterium(双歧杆菌属),HD组的主要菌群为Escherichia_shigella(大肠志贺氏杆菌属)、Enterococcus(肠球菌属)、Corynebacterium_1(棒状杆菌属_1)、Staphylococcus(葡萄球菌属)(图3C)。 为研究HC组与肥胖相关的菌群,进一步作如图4所示的属水平关键肠道菌群相对丰度,结果显示,在属水平上,HC组显著升高了Bifidobacterium(双歧杆菌属)、Butyrivibrio(丁酸弧菌属)、Ruminococcaceae_UCG_014(瘤胃球菌科_UCG_014)等的相对丰度(P<0.05),显著降低了Corynebacterium_1(棒状杆菌属_1)、Staphylococcus(葡萄球菌属)等的相对丰度。其中,Bifidobacterium(双歧杆菌属)、Butyrivibrio(丁酸弧菌属)、Ruminococcaceae_UCG_014(瘤胃球菌科_UCG_014)是与短链脂肪酸(short-chain fatty acids,SCFA)生成有关的菌群。Agnieszka等[20]研究发现肥胖患者中,Bifidobacterium(双歧杆菌属)丰度显著低于健康个体,并与高密度脂蛋白浓度呈正相关。其可通过产生SCFA,维持糖脂平衡,减少肥胖的发生发展[21]。Ruminococcaceae_UCG_014(瘤胃球菌科_UCG_014)和Butyrivibrio(丁酸弧菌属)在缓解肥胖发生发展同样发挥着重要的作用。Ruminococcaceae_UCG_014(瘤胃球菌科_UCG_014)是瘤胃球菌属家族的一员,据报道该菌是SCFA的产生菌[22],具有缓解高脂饮食诱导肥胖的作用[23]。Butyrivibrio(丁酸弧菌属)则是丁酸的产生菌[24],丁酸可以有效缓解肥胖[25]。以上结果表明,高剂量CLA可以显著逆转由于高脂饲料导致的肠道菌群紊乱,增加短链脂肪酸产生菌属的相对丰度。
2.3.3 菌群相对丰度与肥胖相关指标的相关性分析
将四组体重、内脏脂肪重量和生化指标与菌门和菌属数据作Spearman相关性分析,如图5所示,在门水平上,Bacteroidetes(拟杆菌门)与血清TAG呈显著正相关(P<0.05),Epsilonbacteraeota与体重和睾周脂肪呈极显著负相关(P<0.01),Rokubacteria(棒状杆菌门)与肾周脂肪和睾周脂肪呈显著负相关(P<0.05),Tenericutes(软壁菌门)与血清TC呈显著正相关(P<0.05),Firmicutes(厚壁菌门)与血清TAG呈显著负相关(P<0.05);在属水平上,Corynebacterium_1(棒状杆菌属_1)与体重呈显著正相关(P<0.05),与血清TC呈显著正相关(P<0.01),而Bifidobacterium(双歧杆菌属)与血清TAG呈显著负相关(P<0.01),其他菌群与相关指标的相关性无显著性差异(P>0.05)。因此,Corynebacterium _1
(棒状杆菌属_1)可能与肥胖的发生发展和血脂异常有关,而Bifidobacterium(双歧杆菌属)能够改善高脂饮食诱导的血脂异常。 3. 讨论与结论
在本研究中,高剂量CLA干预可显著降低高脂饲料喂养的大鼠体重和内脏脂肪重量(P<0.05),说明CLA可预防高脂饲料诱导的体重和脂肪的增长。同时,CLA干预后大鼠血清TC、TAG及肝脏TC降低,说明CLA可预防体内的甘油三酯和胆固醇的蓄积。此外,肠道菌群的结果显示高剂量CLA可逆转由高脂饲料导致的肠道菌群紊乱,主要表现在显著增加产生短链脂肪酸的菌属Bifidobacterium(双歧杆菌属)、Butyrivibrio(丁酸弧菌属)、Ruminococcaceae_UCG-014(瘤胃球菌科_UCG-014)的相对丰度,这些菌群在维持肠腔厌氧环境中有关键作用[26]。
此外,本研究还发现血清TAG和Bifidobacterium(双歧杆菌属)相对丰度呈极显著负相关(P<0.01)。Chaplin A等[27]的研究表明CLA干预未逆转高脂饲料导致的Bifidobacterium(双歧杆菌属)的降低。而本研究显示CLA能够显著升高Bifidobacterium(双歧杆菌属)的相对丰度,可能是由于该研究采用的是C57BL/6小鼠每日灌胃6 mg/d干预54 d,与本研究的动物品系、干预剂量和干预时间不同所致。Ruminococcaceae_UCG-014(瘤胃球菌科_UCG-014)和Butyrivibrio(丁酸弧菌)在缓解肥胖发生发展同样发挥着重要的作用。本研究显示对照组和高脂模型组组Butyrivibrio(丁酸弧菌)的相对丰度非常低,而CLA干预后随着剂量的升高其相对丰度越来越高,提示Butyrivibrio(丁酸弧菌)可能是CLA干预的特征菌群。以上可知,在高剂量CLA干预下,肠道中某些与SCFA产生的专性厌氧菌明显增加,这可能是CLA发挥抑制肥胖和调节血糖的生理基础之一。此外,兼性厌氧菌相对丰度的显著增加是肠道菌群失调的重要特征之一[26],本研究发现在CLA干预后兼性厌氧菌的相对丰度明显降低,其中由于高脂饮食诱导的Staphylococcus(葡萄球菌属)、Corynebacterium_1(棒状杆菌属_1)等相对丰度的显著增加可以被高剂量的CLA干预逆转。据报道,低氧环境利于专性厌氧菌生长,它们可降解纤维生成SCFA,进而促进宿主健康[28]。另有研究发现,SCFA刺激PPAR-γ信号传导,驱动结肠上皮细胞的能量代谢向β-氧化转化,抑制肠道上皮细胞氧合作用,维持肠腔厌氧环境,形成不利于兼性厌氧菌生长的肠腔微环境[29],进而维持肠道屏障,避免脂多糖、鞭毛蛋白等有害菌群代谢产物入血循环,抑制全身炎症发生,这对机体糖脂稳态至关重要[30]。因此,高剂量CLA干预后兼性厌氧菌减少可能与SCFA产生相关的肠道菌群明显增加有关。
综上所述,CLA能够显著降低体重、内脏脂肪并且改善高脂饲料导致的甘油三酯和胆固醇蓄积,可能与CLA重塑肠道菌群有关。经过高剂量CLA干预后,肠道菌群中专性厌氧菌和兼性厌氧菌的相对丰度发生显著的变化,同时与SCFA产生有关的菌群在高剂量的CLA干预后显著增加,这可能是CLA发挥抑制肥胖和降低脂质蓄积的重要生理基础。同时,本研究存在一定的局限性,尚未检测粪便中的菌群代谢物,后续实验将进一步采用肠道菌群测序与代谢组学技术以明确CLA调节肥胖相关的菌群代谢物。
-
表 1 干预9周后各组大鼠内脏脂肪重量及生化指标
Table 1 Visceral fat and blood lipid levels of SD rats in each group after 9 weeks of intervention
分组 ND组 HD组 LC组 HC组 肾周脂肪重量(g) 6.97±0.89a 13.49±0.67c 11.83±0.74bc 10.39±1.21b 睾周脂肪重量(g) 6.59±0.67a 11.86±0.77c 10.71±0.76bc 8.84±0.41b 血清TC(mmol/L) 4.34±0.44a 6.34±0.31b 4.78±0.40a 3.77±0.23a 血清TAG(mmol/L) 2.41±0.19a 2.95±0.08b 2.60±0.19ab 2.13±0.13a 肝脏TC(mmol/L) 4.57±0.14a 7.19±0.57c 6.34±0.10bc 6.21±0.23b 肝脏TAG(mmol/L) 8.43±0.82a 12.34±0.60b 12.01±0.6b 12.88±1.04b 注:以上数据以±SEM的形式表示,不同字母表示组间差异有统计学意义,P<0.05;表2同。 表 2 肠道菌群的α多样性分析
Table 2 Alpha diversity analysis of intestinal microbiota
分组 ND组 HD组 LC组 HC组 Ace指数 790.260±6.757b 796.479±5.416b 800.021±6.385b 759.443±10.712a Chao 1指数 795.571±7.396ab 806.056±7.771b 810.629±5.593b 773.603±12.038a Shannon指数 0.967±0.003a 0.967±0.007a 0.962±0.004a 0.965±0.008a Simpson指数 6.621±0.071a 6.666±0.218a 6.556±0.121a 6.593±0.101a -
[1] ZHANG X, ZHANG M, ZHAO Z, et al. Geographic variation in prevalence of adult obesity in china: Results from the 2013-2014 national chronic disease and risk factor surveillance[J]. Annals of Internal Medicine,2020,172(4):291−293. doi: 10.7326/M19-0477
[2] ABARCA GÓMEZ L, ABDEEN Z A, HAMID Z A, et al. Worldwide trends in body-mass index, underweight, overweight, and obesity from 1975 to 2016: A pooled analysis of 2416 population-based measurement studies in 128·9 million children, adolescents, and adults[J]. Lancet,2017,390(10113):2627−2642. doi: 10.1016/S0140-6736(17)32129-3
[3] CANFORA E E, MEEX R C R, VENEMA K, et al. Gut microbial metabolites in obesity, NAFLD and T2DM[J]. Nature Reviews Endocrinology,2019,15(5):261−273. doi: 10.1038/s41574-019-0156-z
[4] LI R, HUANG X, LIANG X, et al. Integrated omics analysis reveals the alteration of gut microbe-metabolites in obese adults[J]. Briefings in Bioinformatics,2020:bbaa165.
[5] KOOTTE R S, LEVIN E, SALOJARVI J, et al. Improvement of insulin sensitivity after lean donor feces in metabolic syndrome is driven by baseline intestinal microbiota composition[J]. Cell Metabolism,2017,26(4):611−619. doi: 10.1016/j.cmet.2017.09.008
[6] TRICON S, BURDGE G C, WILLIAMS C M, et al. The effects of conjugated linoleic acid on human health-related outcomes[J]. Proceedings of the Nutrition Society,2005,64(2):171−182. doi: 10.1079/PNS2005418
[7] LAWSON R E, MOSS A R, GIVENS D I. The role of dairy products in supplying conjugated linoleic acid to man’s diet: A review[J]. Nutrition Research Reviews,2001,14(1):153−172. doi: 10.1079/095442201108729178
[8] SCHMID A, COLLOMB M, SIEBER R, et al. Conjugated linoleic acid in meat and meat products: A review[J]. Meat Science,2006,73(1):29−41. doi: 10.1016/j.meatsci.2005.10.010
[9] BASAK S, DUTTAROY A K. Conjugated linoleic acid and its beneficial effects in obesity, cardiovascular disease, and cancer[J]. Nutrients,2020,12(7):1913. doi: 10.3390/nu12071913
[10] CHURRUCA I, FERNANDEZ QUINTELA A, PORTILLO M P. Conjugated linoleic acid isomers: Differences in metabolism and biological effects[J]. Biofactors,2009,35(1):105−111. doi: 10.1002/biof.13
[11] BLANKSON H, STAKKESTAD J A, FAGERTUN H, et al. Conjugated linoleic acid reduces body fat mass in overweight and obese humans[J]. Journal of Nutrition,2000,130(12):2943−2948. doi: 10.1093/jn/130.12.2943
[12] GAULLIER J M, HALSE J, HOYE K, et al. Supplementation with conjugated linoleic acid for 24 months is well tolerated by and reduces body fat mass in healthy, overweight humans[J]. Journal of Nutrition,2005,135(4):778−784. doi: 10.1093/jn/135.4.778
[13] MOREIRA T G, HORTA L S, GOMES-SANTOS A C, et al. CLA-supplemented diet accelerates experimental colorectal cancer by inducing TGF-β-producing macrophages and T cells[J]. Mucosal Immunology,2019,12(1):188−199. doi: 10.1038/s41385-018-0090-8
[14] CARABAJAL M A, VIARENGO G, YIM L, et al. PhoQ is an unsaturated fatty acid receptor that fine-tunes Salmonella pathogenic traits[J]. Science Signaling,2020,13(628):eaaz3334. doi: 10.1126/scisignal.aaz3334
[15] PENG M, TABASHSUM Z, PATEL P, et al. Prevention of enteric bacterial infections and modulation of gut microbiota with conjugated linoleic acids producing Lactobacillus in mice[J]. Gut Microbes,2020,11(3):433−452. doi: 10.1080/19490976.2019.1638724
[16] MARTIN GONZALEZ M Z, PALACIOS H, RODRIGUEZ M A, et al. Beneficial effects of a low-dose of conjugated linoleic acid on body weight gain and other cardiometabolic risk factors in cafeteria diet-fed rats[J]. Nutrients,2020,12(2):408. doi: 10.3390/nu12020408
[17] 夏珺, 郑明月, 李灵杰, 等. 共轭亚油酸改善肥胖糖尿病小鼠的糖脂代谢[J]. 南方医科大学学报,2019,39(6):740−746. [XIA J, ZHENG M Y, LI L J, et al. Conjugated linoleic acid improves glucose and lipid metabolism in diabetic mice[J]. Journal of Southern Medical University,2019,39(6):740−746. [18] LASO N, BRUGUE E, VIDAL J, et al. Effects of milk supplementation with conjugated linoleic acid (isomers cis-9, trans-11 and trans-10, cis-12) on body composition and metabolic syndrome components[J]. British Journal of Nutrition,2007,98(4):860−867.
[19] GARIBAY NIETO N, QUEIPO GARCIA G, ALVAREZ F, et al. Effects of conjugated linoleic acid and metformin on insulin sensitivity in obese children: Randomized clinical trial[J]. Journal of Clinical Endocrinology & Metabolism,2017,102(1):132−140.
[20] SROKA OLEKSIAK A, MŁODZIŃSKA A, BULANDA M, et al. Metagenomic analysis of duodenal microbiota reveals a potential biomarker of dysbiosis in the course of obesity and type 2 diabetes: A pilot study[J]. J Clin Med,2020,9(2):369. doi: 10.3390/jcm9020369
[21] CANI P D. Microbiota and metabolites in metabolic diseases[J]. Nature Reviews Endocrinology,2019,15(2):69−70. doi: 10.1038/s41574-018-0143-9
[22] TIAN B, ZHAO J, ZHANG M, et al. Lycium ruthenicum anthocyanins attenuate high-fat diet-nduced colonic barrier dysfunction and inflammation in mice by modulating the gut microbiota[J]. Molecular Nutrition & Food Research,2021,65(8):2000745.
[23] ZHAO L, ZHANG Q, MA W, et al. A combination of quercetin and resveratrol reduces obesity in high-fat diet-fed rats by modulation of gut microbiota[J]. Food & Function,2017,8(12):4644−4656.
[24] FOMENKY B E, DO D N, TALBOT G, et al. Direct-fed microbial supplementation influences the bacteria community composition of the gastrointestinal tract of pre- and post-weaned calves[J]. Scientific Reports,2018,8(1):14147. doi: 10.1038/s41598-018-32375-5
[25] LIU H, WANG J, HE T, et al. Butyrate: A double-edged sword for health?[J]. Advances in Nutrition,2018,9(1):21−29. doi: 10.1093/advances/nmx009
[26] KRISS M, HAZLETON K Z, NUSBACHER N M, et al. Low diversity gut microbiota dysbiosis: Drivers, functional implications and recovery[J]. Current Opinion in Microbiology,2018,44:34−40. doi: 10.1016/j.mib.2018.07.003
[27] CHAPLIN A, PARRA P, SERRA F, et al. Conjugated linoleic acid supplementation under a high-fat diet modulates stomach protein expression and intestinal microbiota in adult mice[J]. PLOS One,2015,10(4):e0125091. doi: 10.1371/journal.pone.0125091
[28] LITVAK Y, BYNDLOSS M X, BAUMLER A J. Colonocyte metabolism shapes the gut microbiota[J]. Science,2018,362(6418):eaat9076. doi: 10.1126/science.aat9076
[29] BYNDLOSS M X, OLSAN E E, RIVERA CHAVEZ F, et al. Microbiota-activated ppar-gamma signaling inhibits dysbiotic enterobacteriaceae expansion[J]. Science,2017,357(6351):570−575. doi: 10.1126/science.aam9949
[30] HERSOUG L G, MØLLER P, LOFT S. Role of microbiota-derived lipopolysaccharide in adipose tissue inflammation, adipocyte size and pyroptosis during obesity[J]. Nutrition Research Reviews,2018,31(2):153−163. doi: 10.1017/S0954422417000269
-
期刊类型引用(1)
1. 刀梅,宫树森,韦祖粉,王青芬,杨自云,吴田. 诱导剂对海巴戟莨菪亭累积的影响. 西北农林科技大学学报(自然科学版). 2024(08): 133-142 .  百度学术
百度学术
其他类型引用(0)






 下载:
下载:

 下载:
下载:



