Improvement Effect of the EPS Produced by Long Shelf-life Yogurt Culture on DSS-Induced Enteritis
-
摘要: 为探究常温酸奶发酵剂发酵过程中分泌的胞外多糖(EPS)对小鼠结肠炎的缓解作用,本研究在常温酸奶发酵剂A和发酵剂B分别发酵后的常温酸奶中提取纯化胞外多糖,测定其分子特性、结构形貌和单糖组成,同时通过葡聚糖硫酸钠(DSS)诱导小鼠结肠炎,分析了两种胞外多糖对小鼠体重、结肠组织病理学、小鼠炎症因子、髓过氧化物酶(MPO)和紧密连接蛋白(ZO-1、Occludin)表达量的影响。结果表明,EPS-A和EPS-B在分子形貌和单糖组成上均有明显差异。EPS-A结构略疏松,由盐酸氨基半乳糖、半乳糖和葡萄糖3种单糖构成,其摩尔比为0.345:0.21:0.435;EPS-B结构致密,由盐酸氨基半乳糖、盐酸氨基葡萄糖、半乳糖和葡萄糖4种单糖构成,其摩尔比为0.421:0.05:0.207:0.322。各胞外多糖治疗组均能够恢复炎症性肠病(IBD)小鼠体重,但是均不能显著降低疾病活动指数(DAI)评分;EPS-A高剂量组结肠形态接近空白对照组,两者的结肠长度和结肠系数没有显著性差异(P>0.05);结合不同治疗组中炎症因子TNF-α、IL-1β、IL-10表达量,EPS-A高剂量组对炎症因子的反应效果最好,和药物治疗组的反应效果无显著性差异(P>0.05);EPS-A胞外多糖高剂量组和低剂量组同药物治疗组的ZO-1和Occludin蛋白的表达量显著性提高(P<0.05),EPS-B高剂量组ZO-1蛋白的表达量相较于模型组也有显著性提高(P<0.05),但是效果不如EPS-A组;不同胞外多糖治疗组在降低MPO活性方面均没有显著改善(P>0.05)。综合以上结果可知EPS-A能够显著改善小鼠肠炎情况,其效果优于EPS-B。Abstract: In order to study the relieving effect of extracellular polysaccharides (EPS-A,EPS-B) which were extracted and purified from long shelf-life yogurt fermented by long shelf-life yogurt culture A and culture B, their molecular characteristics, structural morphology and monosaccharide composition were determined, and the mouse weight, influence of colon histopathology, the expression of inflammatory factors, the content of myeloperoxidase (MPO) and tight junction proteins (ZO-1, Occludin) in mice were also analyzed through constructing an animal model of colonic inflammation in mice by dextran sulfate sodium (DSS). The results showed that there were significantly differences on the molecular morphology and monosaccharide compositions between EPS-A and EPS-B. The EPS-A was slightly loose in structure, composed of three monosaccharides (galactosamine hydrochloride, galactose and glucose) with a molar ratio of 0.345:0.21:0.435. The structure of EPS-B was compact and it composed of four monosaccharides (galactosamine hydrochloride, glucosamine hydrochloride, galactose and glucose) with a molar ratio of 0.421:0.05:0.207:0.322. The weight of IBD mice was recovered in all the exopolysaccharide treatment groups, but there was no significant decrease in the disease activity index (DAI) score. The colon morphology of the high dose group of EPS-A was close to that of the blank control group, and there was no significant difference in colon length and colon coefficient between the two groups (P>0.05), the same below). Combined with the expression of inflammatory factor (TNF-α, IL-1β, IL-10) in different treatment groups, the high dose group of EPS-A had the best response to those inflammatory factors, and there was no significant difference between it and the drug treatment group (P>0.05). The expression of ZO-1 and occludin protein in the high-dose and low-dose groups of EPS-A was significantly improved and same as the drug treatment group (P<0.05). The expression of ZO-1 protein in the high-dose group of EPS-B was also significantly higher than that in the model group, but the effect was not as good as that in the EPS-A group (P<0.05). There was no significant improvement in reducing MPO activity in different extracellular polysaccharide treatment groups compared with the model group (P>0.05). In summary, it could be seen that EPS-A can significantly improve the enteritis of mice, and its effect was better than that of EPS-B.
-
Keywords:
- long shelt-life yogurt /
- EPS /
- IBD /
- inflammatory factor /
- intestinal repair
-
炎症性肠病(IBD)是慢性易复发的肠道疾病。近些年IBD的发病率不断上升,频繁腹痛、血性腹泻、便秘、乏力是本病的主要症状,不仅严重影响患者的正常工作和生活,而且增加了长期复发患者继发感染和结肠癌的风险[1]。尽管IBD病因不明,但合理的假设是与个体遗传、肠道上皮细胞完整性受损、肠道菌群激活了遗传易感宿主的异常和过度活跃的免疫反应相关[2]。
大量研究表明,多糖类益生元能够降低髓过氧化物酶(MPO)活性,减少氧化应激反应,保护IBD患者的结肠组织[3]。而乳酸菌EPS作为潜在的益生元,可通过TLR2和NF-κB信号通路调节宿主炎症反应来抑制疾病,从而有效促进 T 细胞的增殖以具有缓解IBD的功效[4-5]。EPS是许多乳酸菌产生的重要代谢产物[6],研究报道保加利亚乳杆菌、嗜热链球菌、嗜酸乳杆菌、植物乳杆菌、鼠李糖乳杆菌、干酪乳球菌和乳酸乳球菌在代谢过程中都可以产生EPS[7]。但不同种乳酸菌所产EPS的功能机理存在一定的差异性,植物乳杆菌 YW11所产EPS显著改善肠炎小鼠的体重降低和肠炎损伤情况,并且能够减少促炎因子(TNF-α、IL-1β、IFN-γ、IL-6、IL-12和IL-18)的产生,增强抗炎因子IL-10的产生,减轻IBD症状[8];而植物乳杆菌NCU116所产EPS则促进STAT3和紧密连接蛋白启动子结合,使上皮屏障功能和紧密连接蛋白的表达量增加,调节肠道上皮屏障功能,从而抑制肠道炎症[9]。
商业化常温酸奶发酵剂一般包含保加利亚乳杆菌和嗜热链球菌,但不同品牌的常温酸奶所选用的保加利亚乳杆菌和嗜热链球菌型号不同,因此推测在常温酸奶的发酵过程中,不同菌株代谢产生的EPS在结构和功能方面也可能存在差异。目前对于商业化常温酸奶发酵剂所含菌株分泌的EPS特性还鲜有研究。因此,本研究以伊利集团提供的商业化常温酸奶发酵剂为研究对象,研究其发酵过程中分泌的EPS的分子形貌和单糖组成及对DSS诱导的慢性肠炎的改善作用,从而更加深入的了解常温酸奶所产胞外多糖的特性和其益生作用。
1. 材料与方法
1.1 材料与仪器
常温酸奶发酵剂A(保加利亚乳杆菌+嗜热链球菌)、常温酸奶发酵剂B(保加利亚乳杆菌+嗜热链球菌) 内蒙古伊利实业集团股份有限公司提供;SPF级雄性Balb/c小鼠(6周龄) 北京维通利华试验动物技术有限公司,实验动物生产许可证号:SCXK(京)2016-0006;16种单糖标品(果糖、葡萄糖、岩藻糖、鼠李糖、盐酸氨基半乳糖、阿拉伯糖、盐酸氨基葡萄糖、半乳糖、N-乙酰-D氨基葡萄糖、木糖、甘露糖、果糖、核糖、古罗马糖醛酸、半乳糖醛酸、葡萄糖醛酸、甘露糖醛酸)和4',6-二脒基-2-苯基吲哚(DAPI)染色剂 美国Sigma公司;DEAE-Sepharose FF填料 英国Waterman公司;Sepharose CL-6B填料 Amersham Bioscience 公司;三氯乙酸(TCA)、三氟乙酸(TFA)、无水乙醇、氯化钠、柳氮磺吡啶、苯酚、溴化钾、硼氢化钠、醋酸酐、伊红、苏木精、二甲苯、石蜡等分析纯试剂和含0.5% Tween-20的pH7.6 Tris-HCl缓冲液(TBST)、磷酸盐缓冲液(PBS) 北京索莱宝科技有限公司;葡聚糖硫酸钠(DSS) 美国MP公司;酶联免疫试剂盒和髓过氧化物酶(MPO)试剂盒 上海酶联生物科技有限公司;聚偏氟乙烯(PVDF)转印膜和ECL化学发光试剂盒 美国Millipore公司;Anti-GAPDH antibody、Anti-NFκB p65 antibody、ZO-1和Occludin蛋白相关试剂盒 英国Abcam公司;Rabbit Anti-Phospho-NFκB p65 (Ser468) antibody、Rabbit Anti-IKB alpha antibody、Rabbit Anti-phospho-IKB alpha (Tyr42) antibody、生物素标记的山羊抗兔Ig、辣根酶标记链霉卵白素 北京博奥森生物技术有限公司。
Nicolet-170型傅里叶红外光谱仪(FT-IR) 美国Nicolet公司;7890A型气相色谱仪(GC) 美国Agilent公司;HWS12型恒温水浴锅 上海一恒科学技术有限公司;BX53F型荧光显微镜 赛默飞世尔有限公司;MLS-3750型高压蒸汽灭菌锅 日本Sanyo公司;Beta1-8 LDplus型真空冷冻干燥机 德国Christ公司;TGL-16M型台式高速冷冻离心机 上海卢湘仪离心机仪器有限公司。
1.2 实验方法
1.2.1 胞外多糖的提取纯化及分析
1.2.1.1 胞外多糖的提取
参考常温酸奶的制作工艺[10],利用常温酸奶发酵剂A和B分别制备常温酸奶,然后在常温酸奶中加入TCA溶液,搅拌后10000 r/min离心45 min,去除沉淀。上清加入无水乙醇静置12 h后,12000 r/min离心45 min,取离心后的沉淀溶解于蒸馏水,后装入分子截流量为8000~14000 Da的透析袋中透析48 h,冷冻干燥得到粗多糖。
1.2.1.2 胞外多糖的纯化
将粗制多糖溶于蒸馏水中配制成10 mg/mL的多糖溶液,首先用DEAE-Sepharose Fast Flow离子交换柱(2.6 cm×40 cm)纯化,利用蒸馏水和NaCl溶液进行梯度洗脱。将再次透析干燥后的多糖样品再溶于0.9%(w/v)NaCl缓冲液,配制成20 mg/mL的EPS溶液,然后用同浓度NaCl溶液作为洗脱液,经过Sepharose CL-6B凝胶柱进行层析纯化,然后收集进行冷冻干燥[11]。
1.2.1.3 扫描电镜(SEM)观察多糖分子形貌
称取5 mg冻干后的胞外多糖样品,固定于云母片表面,洗耳球吹去未固定粉末,喷金30 s,将制好的样品放置样品室中进行扫描电镜观察,并进行拍照。
1.2.1.4 红外光谱(FT-IR)分析
称取2 mg纯化后的EPS样本和200 mg干燥溴化钾粉末,研磨制备样品颗粒。利用傅里叶变换红外光谱仪在4000~400 cm−1范围内测定,分辨率为4 cm−1 。
1.2.1.5 热重- 差示扫描量热(TG-DSC)分析
将5 mg EPS样品放入Al2O3 坩埚。实验在20~600 ℃的温度范围内以10 ℃/min的线性加热速率进行。根据重量损失和相对于温度的热流曲线,得到TG-DSC热图[12]。
1.2.1.6 胞外多糖的单糖组成分析
称取5 mg纯化的EPS样品与2 mL浓度为2 mol/L的TFA在120 ℃下水解3 h。水解后,通过减压蒸发除去样品中的水和TFA,然后将甲醇加入干燥的样品中,减压蒸发,重复五次,去除残留的TFA,用30 mg硼氢化钠还原样品,加入1 mL醋酸酐,乙酰化的样品利用气相色谱仪进行分析[13]。16种单糖标品(果糖、葡萄糖、岩藻糖、鼠李糖、盐酸氨基半乳糖、阿拉伯糖、盐酸氨基葡萄糖、半乳糖、N-乙酰-D氨基葡萄糖、木糖、甘露糖、果糖、核糖、古罗马糖醛酸、半乳糖醛酸、葡萄糖醛酸、甘露糖醛酸)采用相同的方法进行分析,但无需水解。
1.2.2 胞外多糖对DSS诱导肠炎的改善作用
1.2.2.1 构建IBD动物模型
本实验采用SPF级雄性BALB/c小鼠,动物实验遵守中国动物实验管理规定进行。小鼠被关在保持恒温的(22~24 ℃)有木屑的塑料笼子里,光照/黑暗循环时间为12 h,保证小鼠自由进食和饮水。在此条件下饲养小鼠,适应生长7 d后进行实验。自适应喂养7 d后,将BALB/c小鼠(n=56)随机分为7组,每组8只,具体分组见表1。在实验期间,除空白对照组外,其余实验组连续14 d给予3.5% DSS(w/v)饮用水,诱导小鼠产生急性IBD模型,每天早上更换新制的DSS溶液。在连续14 d饮用DSS溶液造模成功后,各治疗组于上午8:00~10:00灌胃EPS或者注射相应治疗药物,1次/d,连续7 d。空白对照组和模型组给予等量生理盐水。灌胃量为10 mL/kg 体重。28 d后小鼠麻醉处死,在无菌操作下立即取出肠道及内容物冷冻保存。动物实验严格遵守实验动物福利伦理与保护相关规定,随时接受实验动物伦理委员会的监督与检查。
表 1 动物实验分组Table 1. Animal experiment group组别 适应饲养 造模 干预7 d 灌胃物 剂量 空白对照组(C) 适应7 d 自由饮食14 d 生理盐水 10 mL/kg 模型组(M) 适应7 d DSS 14 d 生理盐水 10 mL/kg 阳性对照组(P) 适应7 d DSS 14 d 柳氮磺吡啶 0.45 g/kg EPS高剂量(EPS-AH) 适应7 d DSS 14 d EPS高 50 mg/kg*1 EPS低剂量(EPS-AL) 适应7 d DSS 14 d EPS低 3.5 mg/kg*2 EPS高剂量(EPS-BH) 适应7 d DSS 14 d EPS高 50 mg/kg EPS低剂量(EPS-BL) 适应7 d DSS 14 d EPS低 3.5 mg/kg 注:*1来源:根据之前研究其他来源的胞外多糖对DSS诱导肠炎的改善作用中所做的不同胞外多糖的补给量梯度确定的。*2来源:胞外多糖低剂量根据两个常温酸奶发酵剂发酵的酸奶中的胞外多糖含量分别为EPS-A 0.424 g/L、EPS-B 0.367 g/L,成年人按照每天服用0.5 L计算,平均体重为60 kg,综合两个胞外多糖的产量数据,确定胞外多糖低剂量为3.5 mg/kg。 1.2.2.2 疾病活动指数DAI评估
于诱导及治疗期间,每天观察小鼠体重变化情况,同时记录粪便性状,便血情况,按照表2所述标准进行评分,DAI=(体重下降分值+粪便性状分值+便血情况分值)/3。
1.2.2.3 结肠组织病理学分析
将结肠在4%多聚甲醛溶液中固定24 h后取出,依次经过脱水、浸蜡、包埋、切片、捞片和烤片,脱蜡复水等步骤处理后,进行苏木精-伊红(HE)染色5 min,最后在光学显微镜下观察结肠组织结构。结肠组织学损伤标准评分按照表3进行[15]。
表 3 HE切片组织学评分Table 3. Histological score评分 描述 病变范围 0 正常结肠形态结构,无上皮破坏,隐窝缺失 1 病变范围占所有检查视野1%~25% 2 病变范围占所有检查视野26%~50% 3 病变范围占所有检查视野51%~75% 4 病变范围占所有检查视野75%~100% 病变深度 0 无炎症细胞浸润 1 炎症细胞浸润局限于黏膜层 2 炎症细胞浸润至黏膜下层 3 炎症细胞浸润突破黏膜下层,到达肌层 4 炎症细胞浸润结肠全层 1.2.2.4 结肠系数与结肠长度测定
动物实验结束后处死小鼠,取出无盲肠的结肠,称取其质量及小鼠体重,并计算结肠系数:结肠系数=结肠重量/小鼠体重。拍摄结肠整体形态照片,用游标卡尺测量结肠长度。
1.2.2.5 细胞炎症因子含量测定
取约1 cm的小鼠结肠组织以1:9的比例加入9倍预冷的无菌PBS溶液置于玻璃研磨器中研磨成匀浆后,12000 r/min在4 ℃离心20 min,收集上清于−20 ℃保存,以检测免疫相关细胞炎症因子。根据酶联免疫试剂盒说明书测定小鼠结肠中细胞因子TNF-α、IL-1β和IL-10的含量。
1.2.2.6 髓过氧化物酶(MPO)含量测定
准确称取结肠组织重量,根据MPO试剂盒进行测定。
1.2.2.7 紧密连接蛋白表达量测定
石蜡包埋结肠组织后切片,二甲苯脱蜡,梯度酒精浸泡水化。使用pH6.0柠檬酸缓冲液进行抗原修复,磷酸盐缓冲液(PBS)清洗三次,每 2 min,而后在室温下用5%的BSA封闭1 h。滴加 100 μL 稀释一抗,一抗稀释浓度为ZO-1(1:400)、Occludin(1:200),暗处4 ℃孵育过夜。每个切片用PBS溶液洗涤三次,加入稀释后的Alexa Fluor 594标记山羊抗兔IgG,室温下避光孵育1 h。随后,再次使用PBS溶液洗涤切片,封片剂中加入DAPI,混匀,封片剂加到载玻片上,盖上盖玻片,室温下避光放置至少10 min[16]。封片、观察,使用image-Pro6.0 对400×图片进行光密度值分析。
1.3 数据处理与分析
数据以平均值±标准误表示,采用SPSS和origin软件进行处理。P<0.05表示差异具有统计学意义。
2. 结果与分析
2.1 胞外多糖结构分析及单糖组成
2.1.1 胞外多糖的分离纯化
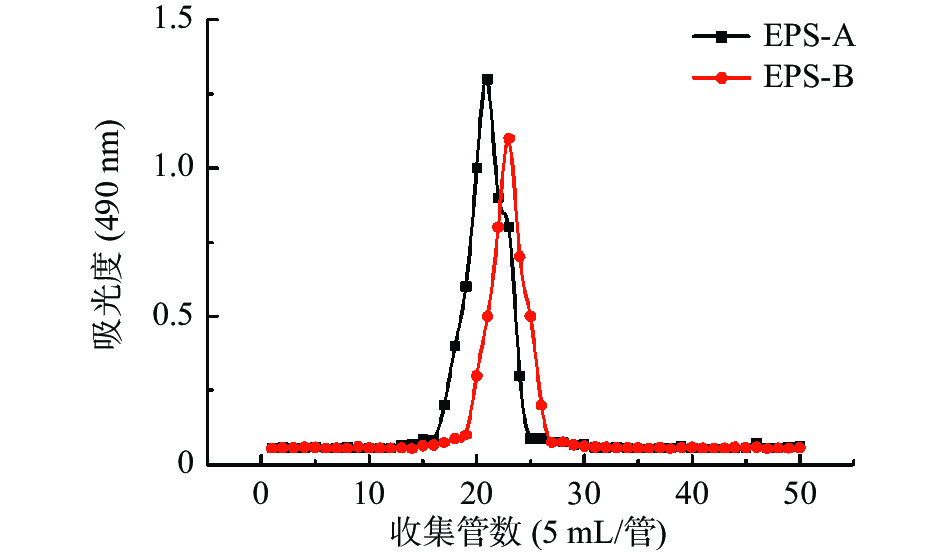
利用发酵剂A和发酵剂B分别发酵后得到的常温酸奶经脱蛋白和乙醇沉淀后制得粗胞外多糖,产量分别为424和367 mg/L。粗胞外多糖再依次经过DEAE-Sepharose Fast Flow 离子交换柱和Sepharose CL-6B凝胶柱进行凝胶渗透层析纯化,得到纯化的胞外多糖单峰,发酵剂A和发酵剂B所产纯化的胞外多糖分别命名为EPS-A和EPS-B,然后进行进一步的分析。(图1)
2.1.2 分子形貌观察
EPS-A和EPS-B扫描电镜照片如图2所示,胞外多糖均表现出相对稳定的三维立体结构,疏松多孔,多为片状与丝状结构重叠呈现纤维网状结构。这些结构分布不规则,糖链互相缠绕,与片层堆积成立体结构。其中EPS-A胞外多糖结构略疏松,管状结构较少;EPS-B胞外多糖的结构分布致密,纤维结构较粗,表面分散着许多大小不同的球状小块,结构分布不规则。乳酸菌胞外多糖的这种高度分支且多孔结构有利于与水形成聚合物,在食品中起到提升产品粘度、增加食品稳定性质和提高持水力等作用,有效地改善了食品的物理特性及感官品质[17]。
2.1.3 红外光谱(FT-IR)分析
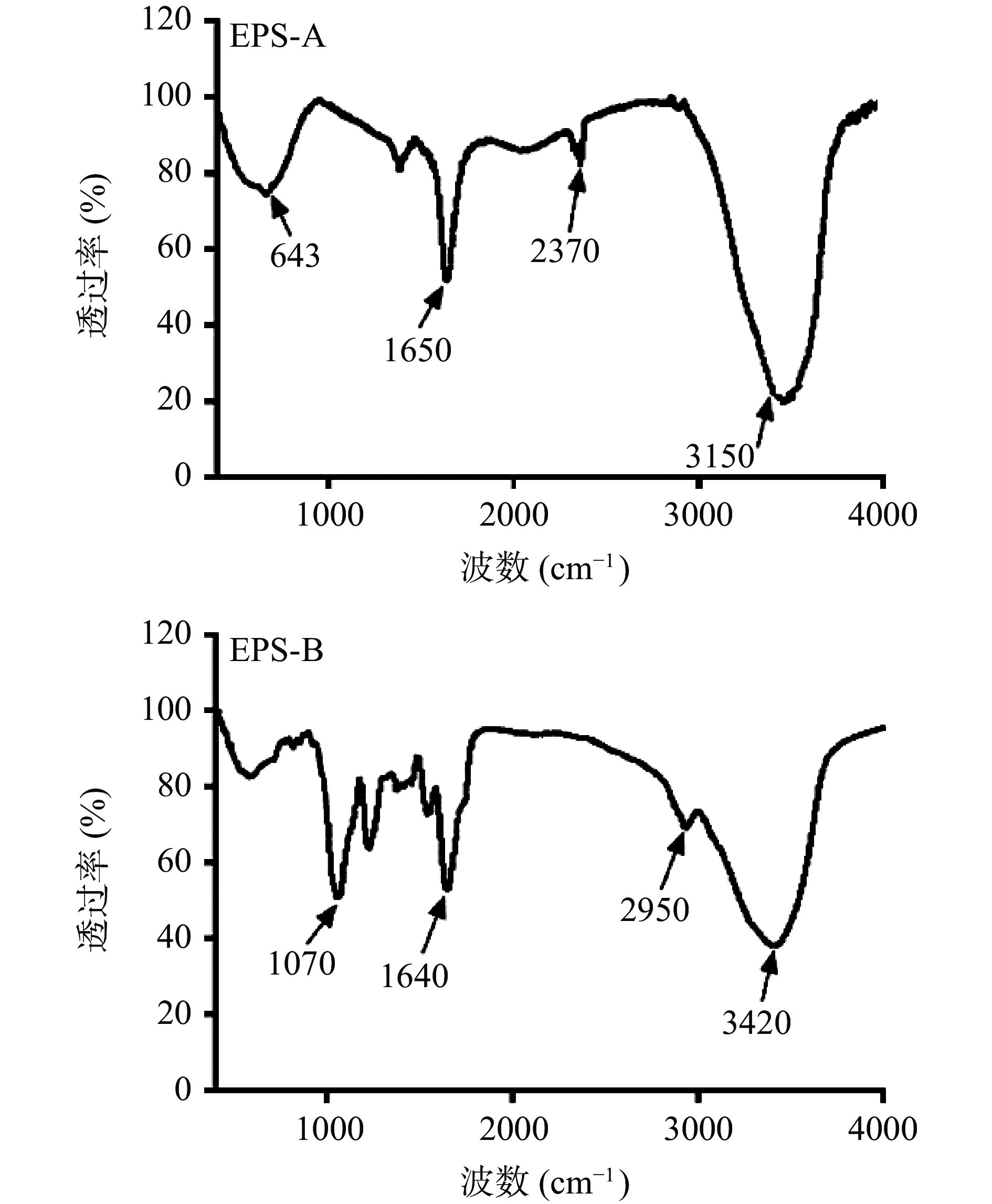
如图3所示,EPS-A的FT-IR吸收光谱在4000~400 cm−1范围内呈现出多种多糖的典型吸收峰。在3150 cm−1处有一个宽而强烈的拉伸峰,表明存在大量的羟基(O-H),证实该化合物是多糖[18]。在1650 cm−1处的吸收是由于C=O键和羧基的伸缩振动[19]。EPS-B的FT-IR吸收光谱在4000~400 cm−1范围内呈现出多种多糖的典型吸收峰。在3420 cm−1处有一个宽而强烈的拉伸峰,表明存在大量的羟基(O-H),证实该化合物是多糖[20]。在2950 cm−1处的另一个弱峰是由C-H伸缩振动引起的[21]。在1640 cm−1处的吸收是由于C=O键和羧基的伸缩振动。在1000~1200 cm−1处的C-O-C和C-O-H的广泛延伸,以及在1070 cm−1处的最强吸收带进一步证实了该聚合物是多糖[22]。
2.1.4 热重-差示扫描量热(TG-DSC)分析
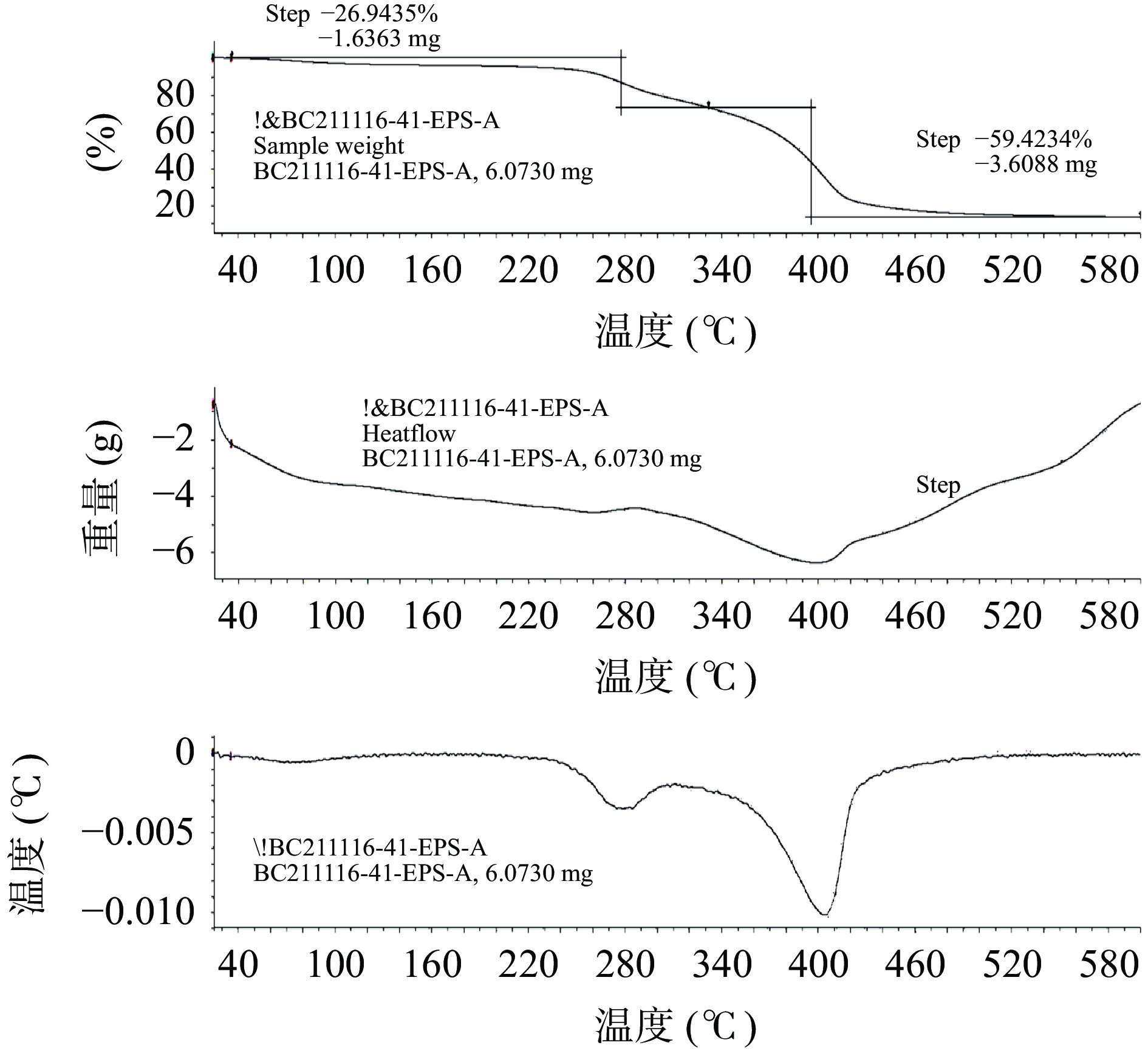
从图4~图5热重曲线中可以看出,EPS-A胞外多糖样品在20~270 ℃之间均有第一次明显的质量损失,这是由于胞外多糖中的自由水、结合水及其中的易挥发物质损失造成的。在330 ℃时,由于胞外多糖的自身降解,样品出现了第二次明显的质量损失,胞外多糖的降解温度Td为330 ℃左右,具有较高的热稳定性。EPS-B样品的加热过程可以分为两个阶段。在第一步中,初步失重约为7.688%,主要是由于EPS样品在温度从20℃上升到280℃期间的水分损失。这表明EPS中有大量的羧基[12],这增加了第一相的降解,因为羧基与更多的水分子结合[23]。在第二步中,样品在400℃左右的失重量增加,达到50.96%,达到一个平台。高温加热会导致EPS环结构中的C-C和C-O键断裂,导致CO、CO2和H2O的释放[24]。EPS在285℃左右开始降解,对应于最快的失重温度。这表明EPS具有很高的热稳定性。EPS-A和EPS-B胞外多糖的热重曲线均符合胞外多糖热分解特性。
2.1.5 单糖组成分析
结果如图6所示,EPS-A胞外多糖的单糖组成为盐酸氨基半乳糖(GalN):半乳糖(Gla):葡萄糖(Glc),其组成比例为0.345:0.21:0.435;EPS-B胞外多糖的单糖组成为盐酸氨基半乳糖(GalN):盐酸氨基葡萄糖(GlcN):半乳糖(Gla):葡萄糖(Glc),其组成比例为0.421:0.05:0.207:0.322。这2种胞外多糖均为杂多糖,组成单糖中均含有盐酸氨基半乳糖、葡萄糖和半乳糖,EPS-B胞外多糖还额外含有盐酸氨基葡萄糖,由此可见,不同的乳酸菌胞外多糖的单糖种类及组成比例不同。
2.2 胞外多糖对DSS诱导肠炎的改善作用
根据曹明泽等[25]造模方法判断本研究结果。本研究中模型组的体重、结肠系数、血清TNF-α、结肠组织髓过氧化物酶(MPO)等指标和对照组在P<0.05时有显著性差异,即可认为造模成功。
2.2.1 胞外多糖对小鼠生长性能的影
在图7(a)中可以看出空白对照组小鼠体重随时间的增加而逐渐增长,DAI值趋近于0;模型组和其他治疗组在DSS诱导期间体重增长缓慢,到12 d时开始有下降趋势,EPS-B胞外多糖低剂量组体重下降最为明显,同时在图7(b)中该组DAI评分略高于模型组,推测胞外多糖EPS-B低剂量组在治疗初期对于慢性肠炎没有改善作用,甚至还会导致更严重的炎症反应。治疗2 d后(第16 d),除EPS-B低剂量组外,其他各胞外多糖治疗组体重下降情况较模型组逐渐改善,体重恢复效果和药物治疗组相同,但是其他各胞外多糖治疗组的DAI评分仍然接近模型组,和药物治疗组存在显著差异(P<0.05)。
2.2.2 结肠情况与组织病理学分析
图8中,从小鼠结肠形态来看,光镜下空白对照组小鼠结肠黏膜结构完整,腺体排列整齐,可见大量杯状细胞,黏膜固有层及下层未见明显的免疫细胞浸润,无炎症;模型组小鼠结肠黏膜结构破坏,隐窝缺失,上皮细胞脱落,黏膜及黏膜下层大量中性粒细胞及淋巴细胞浸润。不同治疗组对结肠炎症的改善程度排序由强到弱依次为:药物治疗组>EPS-AH>EPS-BH>EPS-AL>EPS-BL,其中药物治疗组和EPS-A胞外多糖高剂量组的结肠形态均接近空白对照组,两者的结肠系数和结肠长度均无显著性差异(P>0.05),但是EPS-A胞外多糖高剂量的病变评分和药物治疗组存在显著差异,前者的病变评分显著高于后者(P<0.05)。
2.2.3 细胞炎症因子含量测定
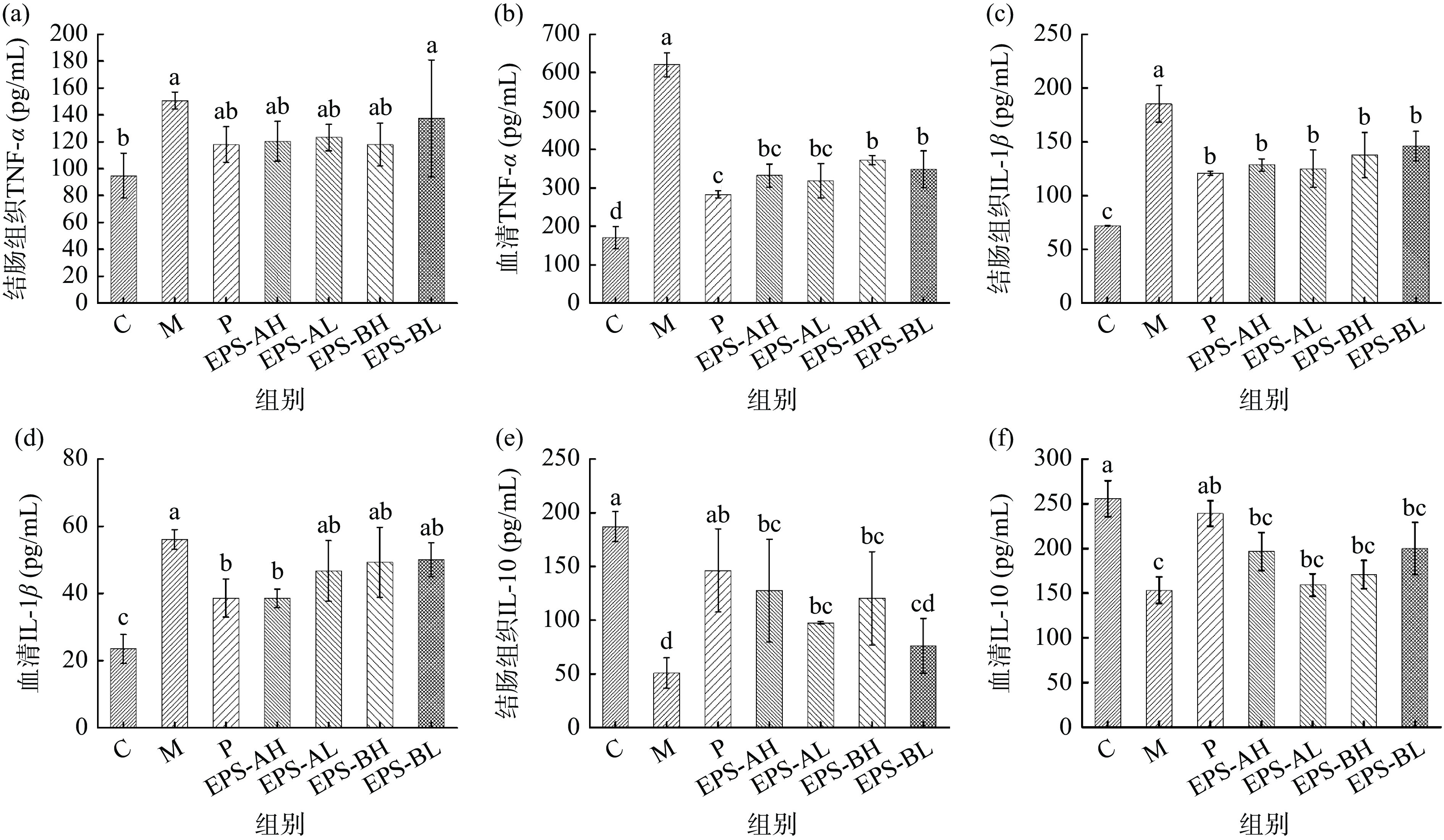
由巨噬细胞产生的TNF-α和IL-1β是典型的促炎因子,能够促进内皮细胞粘附分子的表达,帮助中性粒细胞迁移,增加巨噬细胞的吞噬能力诱导其释放炎症介质进而引起炎症[26]。IL-10是一种抗炎细胞因子,主要由单核细胞产生,可抑制巨噬细胞和Th1T细胞合成促炎因子(IL-1β和TNF-α)[27]。研究表明,若机体缺乏IL-10,小鼠会自发地形成肠炎[28]。
图9结果表明,与空白组相比,模型组中抗炎因子的水平显著升高(P<0.05),促炎因子的水平显著降低(P<0.05),表明模型组小鼠的免疫功能异常,有明显的炎症反应。所有治疗组结肠组织中的TNF-α含量均没有显著下降(P>0.05),但血清中的TNF-α含量呈显著性下降(P<0.05),同时EPS-A的高剂量组和低剂量组的TNF-α含量均和药物组的含量无显著性差异(P>0.05),Popivanova等研究发现抑制TNF-α的表达能够缓解DSS诱导的小鼠结肠炎症状[29];所有治疗组的结肠组织IL-1β含量都显著低于模型组(P<0.05),EPS-A高剂量组的血清IL-1β含量同药物治疗组含量无显著性差异(P>0.05),较模型组均有显著下降(P<0.05),Tummala等[30]发现AOM/DSS诱导的结肠肿瘤中IL-1β含量显著升高,说明IL-1β含量是DSS诱导的结肠炎症的标志物之一;EPS-A高剂量组和低剂量组、EPS-B高剂量组结肠组织中的IL-10含量显著高于模型组(P<0.05),但是低于药物治疗组。综合不同治疗组中TNF-α、IL-1β、IL-10含量,可以看出各胞外多糖治疗组中EPS-A高剂量组对炎症因子的反应效果最好,和药物治疗组的反应效果无显著性差异(P>0.05)。
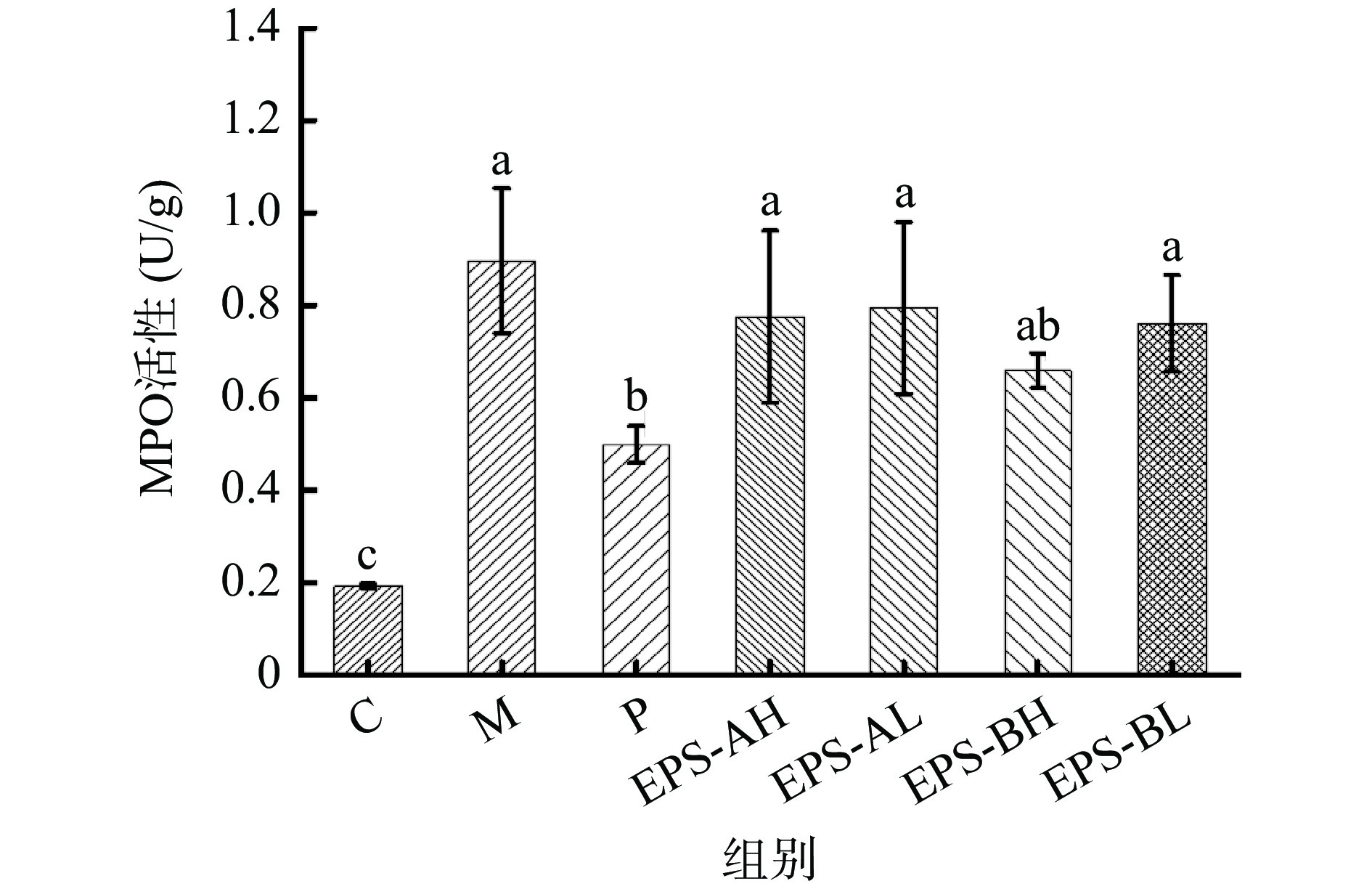
2.2.4 髓过氧化物酶(MPO)含量测定
MPO活性的增高可以反映中性粒细胞在某一组织中的增高,间接反映炎症的存在,可以作为判断机体炎症指数[31]。MPO的活性越强,代表机体的炎症水平越严重。不同治疗组的EPS对肠炎小鼠MPO活性的影响结果见图10:模型组经DSS诱导后的肠炎小鼠结肠组织MPO活性显著增加(P<0.05),药物治疗组可以显著降低MPO活性(P<0.05),但给予不同种类和不同剂量的EPS干预后,仅仅略微降低了结肠中的MPO活性,降低效果均不显著(P>0.05)。
2.2.5 EPS对小鼠肠道屏障的影响
肠道黏膜的丧失被认为是产生肠炎的重要原因[32]。杯状细胞和肠上皮细胞分泌的粘蛋白是肠黏膜力学屏障的重要组成部分[33]。ZO-1和Occludin是重要的肠道屏障紧密连接蛋白,可间接反映肠屏障损害程度;其表达程度越高,屏障修复和抵御外界损伤能力越强[34]。图11(a)和图11(b)中模型组ZO-1和Occludin蛋白表达量显著性减少(P<0.05),相比于模型组,EPS-A胞外多糖高剂量组和低剂量组同药物治疗组ZO-1和Occludin蛋白的表达量显著性提高(P<0.05),EPS-B高剂量组ZO-1蛋白的表达量相较于模型组也有显著性提高(P<0.05),但是效果不如EPS-A高剂量组和低剂量组。空白组小鼠结肠ZO-1和Occludin蛋白表达显著(P<0.05),在管腔上皮细胞、隐窝上皮细胞及上皮细胞连接处顶端均可观察到表达。在图11(c)和图11(d)中与模型组相比,给予不同治疗后,ZO-1和Occludin蛋白表达均有所增强,其表达多位于管腔上皮细胞、隐窝上皮细胞、上皮细胞连接处顶端及少部分胞浆,尤其是药物组和EPS-A高剂量组可在上述细胞位置观察到明显ZO-1和Occludin蛋白表达。
3. 结论
本研究中两种商业化常温酸奶发酵剂产的胞外多糖EPS-A和EPS-B展现出不同的分子形貌和单糖组成,在研究不同胞外多糖对DSS诱导小鼠IBD肠炎的影响实验中,发现EPS-A和EPS-B均能够缓解肠炎,其中EPS-A对肠炎的治疗效果最为显著,小鼠摄入50 mg/kg EPS-A 7 d后缓解肠炎的效果和药物治疗组相同。研究发现多糖的免疫活性和多糖中的单糖组分存在相关性[35],刘袆帆等[36]通过对比33种具有免疫活性的石斛多糖,确定了具有免疫活性的多糖包含7种单糖,分别为葡萄糖、甘露糖、鼠李糖、阿拉伯糖、半乳糖、木糖和葡萄糖醛酸,其中葡萄糖、半乳糖和甘露糖的影响最为显著,葡萄糖是对抗氧化性影响最大的单糖。Kang等[37]的研究证明由葡萄糖、甘露糖和半乳糖组成的副干酪乳杆菌KB28的EPS可以抑制小鼠巨噬细胞中TNF-α等细胞因子的表达。EPS-A中葡萄糖的比例为45.5%,葡萄糖和半乳糖之和的比例为64.5%;EPS-B中上述比例分别为32.2%和52.9%,均低于EPS-A。因此,可以推测EPS-A中更多的葡萄糖和半乳糖是EPS-A对IBD肠炎改善效果优于EPS-B的原因,从而也证明常温酸奶发酵剂A制备的常温酸奶同样具有抗炎活性。
-
表 1 动物实验分组
Table 1 Animal experiment group
组别 适应饲养 造模 干预7 d 灌胃物 剂量 空白对照组(C) 适应7 d 自由饮食14 d 生理盐水 10 mL/kg 模型组(M) 适应7 d DSS 14 d 生理盐水 10 mL/kg 阳性对照组(P) 适应7 d DSS 14 d 柳氮磺吡啶 0.45 g/kg EPS高剂量(EPS-AH) 适应7 d DSS 14 d EPS高 50 mg/kg*1 EPS低剂量(EPS-AL) 适应7 d DSS 14 d EPS低 3.5 mg/kg*2 EPS高剂量(EPS-BH) 适应7 d DSS 14 d EPS高 50 mg/kg EPS低剂量(EPS-BL) 适应7 d DSS 14 d EPS低 3.5 mg/kg 注:*1来源:根据之前研究其他来源的胞外多糖对DSS诱导肠炎的改善作用中所做的不同胞外多糖的补给量梯度确定的。*2来源:胞外多糖低剂量根据两个常温酸奶发酵剂发酵的酸奶中的胞外多糖含量分别为EPS-A 0.424 g/L、EPS-B 0.367 g/L,成年人按照每天服用0.5 L计算,平均体重为60 kg,综合两个胞外多糖的产量数据,确定胞外多糖低剂量为3.5 mg/kg。 计分 体重下降(%) 粪便性状 便血情况 0 0 正常 阴性 1 1~5 形成粪便但易粘附 弱阳性 2 6~10 半成型软粪便 阳性 3 11~15 粪浆状,但不粘附于肛门 强阳性 4 >15 腹泻,粘附肛门 肉眼可见血便 表 3 HE切片组织学评分
Table 3 Histological score
评分 描述 病变范围 0 正常结肠形态结构,无上皮破坏,隐窝缺失 1 病变范围占所有检查视野1%~25% 2 病变范围占所有检查视野26%~50% 3 病变范围占所有检查视野51%~75% 4 病变范围占所有检查视野75%~100% 病变深度 0 无炎症细胞浸润 1 炎症细胞浸润局限于黏膜层 2 炎症细胞浸润至黏膜下层 3 炎症细胞浸润突破黏膜下层,到达肌层 4 炎症细胞浸润结肠全层 -
[1] SULTAN S, EL-MOWAFY M, ELGAML A, et al. Metabolic influences of gut microbiota dysbiosis on inflammatory bowel disease[J]. Front Physiol,2021,12:715506. doi: 10.3389/fphys.2021.715506
[2] JEONG D Y, KIM S, SON M J, et al. Induction and maintenance treatment of inflammatory bowel disease: A comprehensive review[J]. Autoimmun Rev,2019,18(5):439−454. doi: 10.1016/j.autrev.2019.03.002
[3] 陈国伟, 邱春红, 田灵敏, 等. 食源性天然产物中多糖干预炎症性肠病的研究进展[J]. 食品科学,2019,40(13):281−287. [CHEN G W, QIU C H, TIAN L M, et al. Recent progress in food-derived natural polysaccharideintervention in inflammatory bowel disease[J]. Food Science,2019,40(13):281−287. doi: 10.7506/spkx1002-6630-20180619-371 CHEN G W, QIU C H, TIAN L M, et al. Recent progress in food-derived natural polysaccharideintervention in inflammatory bowel disease[J]. Food Science, 2019, 40(13): 281-287. doi: 10.7506/spkx1002-6630-20180619-371
[4] ROUND J L, LEE S M, LI J, et al. The toll-like receptor 2 pathway establishes colonization by a commensal of the human microbiota[J]. Science,2011,332(6032):974−977. doi: 10.1126/science.1206095
[5] HAYASHI A, SATO T, KAMADA N, et al. A single strain of Clostridium butyricum induces intestinal IL-10- producing macrophages to suppress acute experimental colitis in mice[J]. Cell Host Microbe,2013,13(6):711−722. doi: 10.1016/j.chom.2013.05.013
[6] 胡丹丹. 植物乳杆菌LP17-1对小鼠结肠炎缓解作用的研究及其胞外多糖分离提取[D]. 长沙: 中南林业科技大学, 2021 HU D D. Study on the alleviating effect of Lactobacillus plantarum LP17-1 on colitis in miceand the isolation and extraction of extracellular[D]. Changsha: Central South University of Forestry and Technology, 2021.
[7] JIANG Y, YANG Z. A functional and genetic overview of exopolysaccharides produced by Lactobacillus plantarum[J]. Journal of Functional Foods,2018,47:229−240. doi: 10.1016/j.jff.2018.05.060
[8] MIN Z, XIAONA H, AZIZ T, et al. Exopolysaccharides from Lactobacillus plantarum YW11 improve immune response and ameliorate inflammatory bowel disease symptoms[J]. Acta Biochim Pol,2020,67(4):485−493.
[9] ZHOU X, QI W, HONG T, et al. Exopolysaccharides from Lactobacillus plantarum NCU116 regulate intestinal barrier function via STAT3 signaling pathway[J]. J Agric Food Chem,2018,66(37):9719−9727. doi: 10.1021/acs.jafc.8b03340
[10] 伍素芳. 常温饮用型酸奶生产工艺的优化[J]. 饮料工业,2020,23(6):62−66. [WU S F. Optimization ofproduction process for long life drinking yoghurt[J]. Beverage Industry,2020,23(6):62−66. WU S F. Optimization ofproduction process for long life drinking yoghurt[J]. Beverage Industry, 2020, 23(6): 62-66.
[11] WANG J, ZHAO X, TIAN Z, et al. Characterization of an exopolysaccharide produced by Lactobacillus plantarum YW11 isolated from Tibet Kefir[J]. Carbohydr Polym,2015,125:16−25. doi: 10.1016/j.carbpol.2015.03.003
[12] WANG Y, LI C, LIU P, et al. Physical characterization of exopolysaccharide produced by Lactobacillus plantarum KF5 isolated from Tibet Kefir[J]. Carbohydrate Polymers,2010,82(3):895−903. doi: 10.1016/j.carbpol.2010.06.013
[13] LI W, JI J, CHEN X, et al. Structural elucidation and antioxidant activities of exopolysaccharides from Lactobacillus helveticus MB2-1[J]. Carbohydr Polym,2014,102:351−359. doi: 10.1016/j.carbpol.2013.11.053
[14] 吴淑娟, 王新军, 张武胜, 等. 石榴汁对DSS诱导的小鼠溃疡性结肠炎的作用[J/OL]. 食品科学: 1−13[2023-04-26]. http://kns.cnki.net/kcms/detail/11.2206.TS.20220915.1817.022.html. WU S J, WANG X J, ZHANG W S, et al. Effects of pomegranate juice on DSS-induced ulcerative colitis inmice[J/OL]. Food Science, 2022: [2023-04-26]. http://kns.cnki.net/kcms/detail/11.2206.TS.20220915.1817.022.html.
[15] JANG Y J, KIM W K, HAN D H, et al. Lactobacillus fermentum species ameliorate dextran sulfate sodium-induced colitis by regulating the immune response and altering gut microbiota[J]. Gut Microbes,2019,10(6):696−711. doi: 10.1080/19490976.2019.1589281
[16] 许良中, 杨文涛. 免疫组织化学反应结果的判断标准[J]. 中国癌症杂志, 1996, 6(4): 229-231 XU LZ, YANG W T. Judgment criteria of immunohistochemical reaction results[J].China Oncology, 1996, 6(4): 229-231.
[17] ALE E C, PEREZLINDO M J, PAVON Y, et al. Technological, rheological and sensory characterizations of a yogurt containing an exopolysaccharide extract from Lactobacillus fermentum Lf2, a new food additive[J]. Food Res Int,2016,90:259−267. doi: 10.1016/j.foodres.2016.10.045
[18] LI C, LI W, CHEN X, et al. Microbiological, physicochemical and rheological properties of fermented soymilk produced with exopolysaccharide (EPS) producing lactic acid bacteria strains[J]. LWT-Food Science and Technology,2014,57(2):477−485. doi: 10.1016/j.lwt.2014.02.025
[19] SHUHONG Y, MEIPING Z, HONG Y, et al. Biosorption of Cu2+, Pb2+ and Cr6+ by a novel exopolysaccharide fromArthrobacter ps-5[J]. Carbohydr Polym,2014,101:50−56. doi: 10.1016/j.carbpol.2013.09.021
[20] DU R, YU L, YU N, et al. Characterization of exopolysaccharide produced by Levilactobacillus brevis HDE-9 and evaluation of its potential use in dairy products[J]. Int J Biol Macromol,2022,217:303−311. doi: 10.1016/j.ijbiomac.2022.07.057
[21] KAVITA K, MISHRA A, JHA B. Extracellular polymeric substances from two biofilm forming Vibrio species: Characterization and applications[J]. Carbohydr Polym,2013,94(2):882−888. doi: 10.1016/j.carbpol.2013.02.010
[22] SHINGEL K I. Determination of structural peculiarities of dexran, pullulan and γ-irradiated pullulan by Fourier-transform IR spectroscopy[J]. Carbohydrate Research,2002,337(16):1445−1451. doi: 10.1016/S0008-6215(02)00209-4
[23] İSPIRLI H, SAGDIC O, YıLMAZ M T, et al. Physicochemical characterisation of an α-glucan from Lactobacillus reuteri E81 as a potential exopolysaccharide suitable for food applications[J]. Process Biochemistry,2019,79:91−96. doi: 10.1016/j.procbio.2018.12.015
[24] MIAO M, MA Y, HUANG C, et al. homopolysaccharide from Lactobacillus reuteri SK24.003[J]. Carbohydr Polym,2015,131:377−383. doi: 10.1016/j.carbpol.2015.05.066
[25] 曹明泽, 王旭荣, 王磊, 等. 小鼠溃疡性结肠炎模型的建立与评价[J]. 中国畜牧兽医,2016,43(1):171−175. [[CAO M Z, WANG X R, WANG L, et al. Physicochemical properties of a water soluble extracellular[J]. China Animal Husbandry & Veterinary Medicine,2016,43(1):171−175. [CAO M Z, WANG X R, WANG L, et al. Physicochemical properties of a water soluble extracellular [J]. ChinaAnimal Husbandry &Veterinary Medicine, 2016, 43(1): 171-175.
[26] ZHANG Z, LI S, CAO H, et al. The protective role of phloretin against dextran sulfate sodium-induced ulcerative colitis in mice[J]. Food Funct,2019,10(1):422−431. doi: 10.1039/C8FO01699B
[27] LI B, ALLI R, VOGEL P, et al. IL-10 modulates DSS-induced colitis through a macrophage-ROS-NO axis[J]. Mucosal Immunol,2014,7(4):869−878. doi: 10.1038/mi.2013.103
[28] SOUFLI I, TOUMI R, RAFA H, et al. Overview of cytokines and nitric oxide involvement in immuno- pathogenesis of inflammatory bowel diseases[J]. World J Gastrointest Pharmacol Ther,2016,7(3):353−360. doi: 10.4292/wjgpt.v7.i3.353
[29] POPIVANOVA B K, KITAMURA K, WU Y, et al. Blocking TNF-alpha in mice reduces colorectal carcinogenesis associated with chronic colitis[J]. J Clin Invest,2008,118(2):560−570.
[30] TUMMALA P, ROOKE M, DAHLSTROM J E, et al. Glutathione transferase omega 1 confers protection against azoxymethane-induced colorectal tumourformation[J]. Carcinogenesis,2021,42(6):853−863.
[31] 李玥, 钱家鸣. 双歧杆菌对葡聚糖硫酸钠(DSS)诱导的小鼠结肠炎肠道黏膜的保护作用及其对NF-κB的影响[J]. 现代消化及介入诊疗,2010,15(3):131−135. [LI Y, QIAN J M. The probiotics, bifidobacterium, ameliorates dextran sulfate sodium induced colitis in mice[J]. Modern Digestion & Intervention,2010,15(3):131−135. LI Y, QIAN J M. The probiotics, bifidobacterium, ameliorates dextran sulfate sodium induced colitis in mice[J]. Modern Digestion & Intervention, 2010, 15(3): 131-135.
[32] EOM T, KIM Y S, CHOI C H, et al. Current understanding of microbiota- and dietary-therapies for treating inflammatory bowel disease[J]. J Microbiol,2018,56(3):189−198. doi: 10.1007/s12275-018-8049-8
[33] ARIKE L, HOLMEN-LARSSON J, HANSSON G C. Intestinal Muc2 mucin O-glycosylation is affected by microbiota and regulated by differential expression of glycosyltranferases[J]. Glycobiology,2017,27(4):318−328.
[34] 徐婧, 徐豪明, 周有连, 等. 抗生素清肠对丁酸梭菌保护肠炎小鼠肠黏膜屏障的影响及初步机制研究[J]. 现代消化及介入诊疗,2021,26(2):208−213,221. [XU J, XU H M, ZHOU Y L, et al. Effect ofantibiotic cocktail on the intestinal mucosal barrier of mice with colitis protected by Clostridium butyricum[J]. Modern Digestion & Intervention,2021,26(2):208−213,221. XU J, XU H M, ZHOU Y L, et al. Effect ofantibiotic cocktail on the intestinal mucosal barrier of mice with colitis protected by Clostridium butyricum[J]Modern Digestion & Intervention, 2021, 26(2): 208-213+221.
[35] FERREIRA S S, PASSOS C P, MADUREIRA P, et al. Structure-function relationships of immunostimulatory polysaccharides: A review[J]. Carbohydrate Polymers,2015,132:378−396. doi: 10.1016/j.carbpol.2015.05.079
[36] 刘袆帆, 郭烁璇, 林映妤, 等. 石斛多糖的构效关系研究进展[J]. 现代食品科技,2021,37(1):308−338. [LIUH F, GUO S X, LIN Y S, et al. The relationship between the structure and function of dendrobium polysaccharides: A review[J]. Modern Food Science and Technology,2021,37(1):308−338. LIUH F, GUO S X, LIN Y S, et al. The relationship between the structure and function of dendrobium polysaccharides: A review[J]. Modern Food Science and Technology, 2021, 37(1): 308-338.
[37] KANG H, CHOI H S, KIM J E, et al. Exopolysaccharide-overproducing Lactobacillus paracasei KB28 induces cytokines in mouse peritoneal macrophages via modulation of NF-kappabeta and MAPKs[J]. J Microbiol Biotechnol,2011,21(11):1174−1178. doi: 10.4014/jmb.1105.05026
-
期刊类型引用(1)
1. 徐畅,刘天一,刘文佳,张俐敏,莫继先. 微生物胞外多糖的来源、生物合成及功能研究进展. 生物技术进展. 2024(03): 368-376 .  百度学术
百度学术
其他类型引用(1)





 下载:
下载:






 下载:
下载:



