Enzymatic Preparation of Phenolic Acid-Pectin and Its Antioxidant and Antibacterial Activities
-
摘要: 本研究旨在探索酶促接枝改性对果胶结构和功能性质的影响,为开发具有生物活性的新型食品包装材料提供科学依据。以脂肪酶为催化剂,分别将对羟基苯甲酸和没食子酸接枝到果胶分子上。采用1H NMR、FTIR和XPS等分析技术对改性果胶的结构进行表征,并评估其抗氧化和抗菌活性。结果表明,对羟基苯甲酸修饰果胶(Hb-Pe)和没食子酸修饰果胶(Ga-Pe)的接枝率分别达到21.8%和22.9%。同时,与未改性果胶相比,Ga-Pe表现出显著(P<0.05)提高的DPPH自由基清除能力(69.6%)和β-胡萝卜素漂白抑制能力(65.5%),而对羟基苯甲酸改性果胶Hb-Pe的抗氧化活性提升有限,两项指标仅分别为5.54%和28.6%。此外,两种改性果胶对大肠杆菌和金黄色葡萄球菌的抑菌圈直径分别为15.7、13.3 mm (Hb-Pe)和16.6、12.6 mm(Ga-Pe),均显著(P<0.05)高于未改性果胶的抑菌效果。本研究证实了酶促接枝改性能够有效提升果胶的生物活性,为延长食品保质期提供了新的思路。Abstract: This study explored the impact of enzymatic grafting modification on the structure and functional properties of pectin, aiming to provide a scientific foundation for the development of novel food packaging materials with bioactive properties. Using lipase as a catalyst, p-hydroxybenzoic acid and gallic acid were grafted onto pectin molecules. The structure of the modified pectin was characterized using 1H NMR, FTIR, and XPS analytical techniques, and its antioxidant and antibacterial activities were evaluated. The results showed that the grafting rates of p-hydroxybenzoic acid-modified pectin (Hb-Pe) and gallic acid-modified pectin (Ga-Pe) reached 21.8% and 22.9%, respectively. Notably, compared to unmodified pectin, Ga-Pe exhibited significantly (P<0.05) enhanced DPPH free radical scavenging capacity (69.6%) and β-carotene bleaching inhibition capacity (65.5%), while the improvement in antioxidant activity of Hb-Pe was limited, with the two indicators being only 5.54% and 28.6%, respectively. Furthermore, the inhibition zone diameters of the two modified pectins against Escherichia coli and Staphylococcus aureus were 15.7, 13.3 mm (Hb-Pe) and 16.6, 12.6 mm (Ga-Pe), respectively, which were significantly (P<0.05) higher than those of unmodified pectin. This study confirms that enzymatic grafting modification can effectively enhance the bioactivity of pectin, providing a new approach for extending the shelf life of food products.
-
Keywords:
- pectin /
- p-hydroxybenzoic acid /
- gallic acid /
- lipase /
- antioxidant /
- antibacterial
-
果胶是一类存在于各种植物细胞中,由α-1,4糖苷键连接的几种双半乳糖醛酸组成的复杂植物多糖,具有增稠特性、稳定特性、胶凝特性和乳化稳定等性质,可广泛应用于食品加工、生物医药和保健品领域[1−3]。除此之外,果胶在食品包装领域广受关注。它不仅能够提高食品的质感和稳定性,还能通过形成凝胶网络,减缓食品中水分的流失,从而延长食品的保质期。然而,尽管果胶在食品保鲜中展现出了一定的应用优势,其本身并不具备抗氧化和抑菌活性,这两者恰恰是延长食品保质期中至关重要的因素[4−7]。在食品储存和保鲜过程中,氧化反应可能引起脂质的变质,损害食品的质量和感官属性。同时,微生物的生长与繁殖是导致食品腐败的直接原因[8−10]。由于果胶及其基于果胶的复合膜自身缺乏针对这两个关键问题的应对能力,因此其在食品保鲜领域的应用受到了一定限制。
酚酸类化合物,因其独特的化学结构和生物活性,被广泛研究和应用于食品保鲜领域。这些化合物含有一个或多个酚羟基,这些酚羟基赋予了酚酸出色的抗氧化和抑菌特性,从而在食品保存中发挥重要作用[11]。对羟基苯甲酸因其结构简单、来源广泛和抗氧化能力强被广泛研究,没食子酸则因含有多个酚羟基,具有更强的抗氧化和抑菌效果,是最常用于鱼肉保鲜的酚酸[12−14]。通过将酚酸接枝到果胶分子上,不仅可以保留果胶的原有优点,还能赋予其抗氧化和抑菌的功能,有效克服了果胶在食品保鲜应用中的局限性[2,15]。
本研究通过一种温和高效的方法,即通过脂肪酶作为催化剂,实现酚酸对果胶的分子修饰。通过探讨改性果胶的结构变化,并评估其在抗氧化与抑菌方面的潜在应用价值。本研究将为食品包装材料领域提供一种新的视角,特别是在开发具有生物活性、能够有效延长食品保质期和提高食品安全性的新型材料方面。
1. 材料与方法
1.1 材料与仪器
果胶、没食子酸、对羟基苯甲酸、1,1-二苯基-2-苦肼基(DPPH)、β-胡萝卜素 上海麦克林生化科技有限公司;脂肪酶(≥5000 U/g) 上海阿拉丁试剂有限公司;无水乙醇、四氢呋喃、二氯甲烷 西陇化工股份有限公司;大肠杆菌(Escherichia coli,E. coli)、金黄色葡萄球菌(Staphylococcus aureus,S. aureus) 中国微生物菌种收藏管理中心;Luria–Bertani(LB)液体培养基、LB琼脂培养基、液体培养基、真菌培养基、营养琼脂 北京陆桥技术有限公司;本文所用试剂均为分析纯。
NICOLET IS 10傅里叶红外光谱仪(Fourier Infrared Spectrometer,FTIR)、EscaLab 250Xi X射线光电子能谱仪(X-ray photoelectron spectrometer,XPS) 美国赛默飞世尔有限责任公司;BRUKER 600M核磁共振仪(Nuclear Magnetic Resonance Spectrometer,NMR) 德国布鲁克有限责任公司;T9紫外可见光谱仪(Ultraviolet visible spectrophotometer,UV-Vis) 北京普析通用仪器有限责任公司。
1.2 实验方法
1.2.1 酚酸修饰果胶的制备
将5.10 g的没食子酸溶解于300 mL的四氢呋喃中。随后,将10 g天然果胶(编号为Na-Pe)溶解于300 mL的去离子水中,并加入1 g的脂肪酶。接着,将上述两种溶液混合,并于60 ℃下反应24 h。反应完成后,通过旋转蒸发去除混合溶液中的四氢呋喃。接着,将样品在7000~14000 Da的透析袋中透析96 h,以除去多余的没食子酸。最后,通过冷冻干燥去除样品中的水分,得到没食子酸接枝的果胶,将其编号为Ga-Pe[16−18]。采用同样的方法制备对羟基苯甲酸接枝果胶,编号为Hb-Pe。
1.2.2 接枝率的测定
本研究采用分光光度法测定改性果胶的酚酸接枝率。首先配制1%(w/v)的改性果胶溶液,并稀释至合适倍数以确保在测定时能够观察到明显的吸收峰,此时改性果胶浓度记为C1。使用紫外-可见分光光度计在记录样品在最大吸收波长处的吸光度(Ga-Pe为263 nm,Hb-Pe为251 nm),每个样品进行3次重复测定,取平均值用于计算。同时,配制一系列已知浓度的没食子酸和对羟基苯甲酸标准溶液,分别测定其在263和251 nm处吸光度,建立浓度与吸光度的标准曲线(对羟基苯甲酸:y=98.816x−0.116,R2=0.9999;没食子酸:y=51.743x+0.0109,R2=0.9998)。将改性果胶样品的吸光度代入相应的标准曲线,计算出改性果胶中酚酸浓度(记为C2)。然后根据以下公式计算接枝率:
接枝率(%)=C2C1×100 (1) 其中:C1为酚酸浓度;C2为改性果胶浓度。
1.2.3 结构表征
1H NMR分析:样品溶解在DMSO-d6中,并在室温下采集1H NMR谱图,操作为频率600 MHZ,化学位移以ppm表示,并参照残留溶剂峰进行校正。
FTIR分析:样品以KBr压片法制备,通过FTIR对改性前后果胶的官能团进行表征,扫描范围为4000~400 cm−1,扫描次数32次,采样波长设置为4 cm−1。
XPS分析:样品直接涂布在XPS样品支架上,应用C1s(284.80 eV)能标进行电荷校正,并使用Al Kα射线(HV=1486.6 eV)作为X射线源,分析C1s的高分辨谱。
1.2.4 DPPH自由基清除率
使用无水乙醇配制DPPH溶液,并将其稀释至最大吸收波长处的吸光度接近0.8。然后取4 mL配制好的DPPH溶液添加到10 mL离心管中,向其DPPH溶液中滴加60 μL配制好的浓度为1 mg/L的果胶溶液。另需做一组空白以无水乙醇代替样品,并置于在黑暗环境中静置30 min,其在528 nm处吸光度。DPPH自由基清除率按照以下公式计算[19]:
DPPH自由基清除率(%)=A0−A1A0×100 (2) 其中:A0为参照样的吸光度,A1为样品的吸光度。
1.2.5 β-胡萝卜素漂白抑制率
首先,将10 mL含有β-胡萝卜素(1 mg/mL)的二氯甲烷溶液置于梨形瓶中,再加入400 μL亚油酸、4 mL吐温80和100 mL蒸馏水。在40 ℃条件下旋转蒸发减压去除氯仿,混合形成乳化液。取10 mL乳化液,并将其用水定容至100 mL,制备成乳化稀释液。取5 mL乳化稀释液放入7 mL离心管中,向其加入60 μL浓度为1 mg/L的果胶溶液。混匀后测定其在470 nm处吸光度。将所有试管置于50 ℃恒温水浴中。在120 min后测定改性前后果胶溶液在470 nm波长下反应终点的吸光度。空白样品不包含所测样品,使用无水乙醇代替。β-胡萝卜素漂白的抑制率用下式进行计算[20]:
β-胡萝卜素漂白抑制率(%)=(1−A0hsample−A2hsampleA0hcontrol−A2hcontrol)×100 (3) 其中:A0hcontrol和A2hcontrol分别表示空白样在加热前后的吸光度(470 nm);A0hsample和A2hsample分别表示花色苷样品在加热前后的吸光度(470 nm)。
1.2.6 抑菌活性的测定
本研究采用抑菌圈法评估天然果胶和改性果胶对大肠杆菌和金黄色葡萄球菌的抑菌活性[18]。首先,将冷冻保存的菌株分别接种于LB培养基(大肠杆菌)和营养肉汤培养基(金黄色葡萄球菌)中,在37 ℃和200 r/min条件下振荡培养18 h,获得活化菌液。然后,将一定量活化菌液加入50 ℃左右的平板培养基中,使培养基中的活菌浓度达到106~107 CFU/mL,混匀后倒入无菌平板使其凝固。用无菌打孔器在平板表面打4~5个孔,并在孔中加入60 μL的5%果胶溶液。将平板置于4 ℃条件下,使果胶溶液充分扩散到培养基中,然后转移至37 ℃培养箱中培养24 h。培养结束后,测量形成的抑菌圈直径,以评估样品对测试菌株的抑菌活性,抑菌圈直径越大,表示抑菌活性越强。
1.3 数据处理
所有实验均进行三次重复,结果以平均值±标准差表示。使用SPSS 22.0统计软件对数据进行统计分析。组间差异比较采用单因素方差分析(one-way ANOVA),显著性水平设定为P<0.05。
2. 结果与分析
2.1 果胶1H NMR与接枝率分析
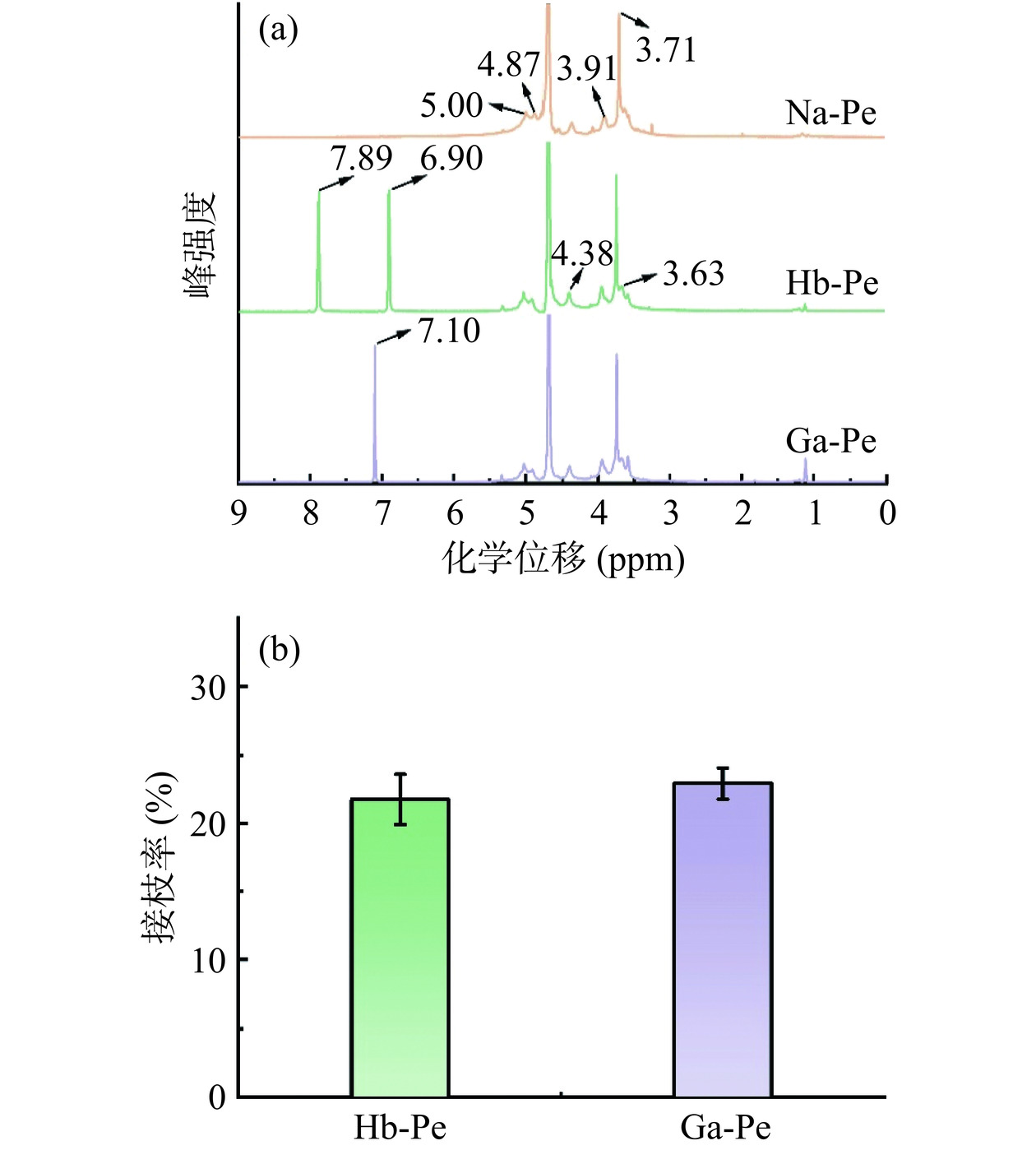
图1为天然果胶和改性果胶的1H NMR光谱和接枝率。由图1(a)可以看出,天然果胶(Na-Pe)在6.00~3.00 ppm范围内有6个特征峰,其中位于3.63 ppm处的特征峰是由果胶分子中甲酯基上的氢核造成的,其他5个特征峰(分别位于5.00、4.87、4.38、3.91和3.71 ppm)反映了半乳糖醛酸和半乳糖醛酸甲酯糖环上的5组氢核[17]。另外,与Na-Pe的光谱相比,可以在Hb-Pe光谱上观察到两个新的特征峰,分别位于7.89和6.90 ppm,这分别对应了对羟基苯甲酸苯环上的两组对称的氢核。同时可以在Ga-Pe光谱上观察到位于7.10 ppm处的特征峰,这对应了没食子酸苯环上的1组对称的氢核[17]。以上现象表明,对羟基苯甲酸和没食子酸均成功接枝于果胶分子上。
通过分光光度法测定了天然果胶和改性果胶的接枝率,其结果如图1(b)所示。由图1(b)可以看出,Hb-Pe和Ga-Pe接枝率分别达到21.8%和22.9%,两者之间没有显著性差异(P>0.05)。
2.2 果胶FTIR分析
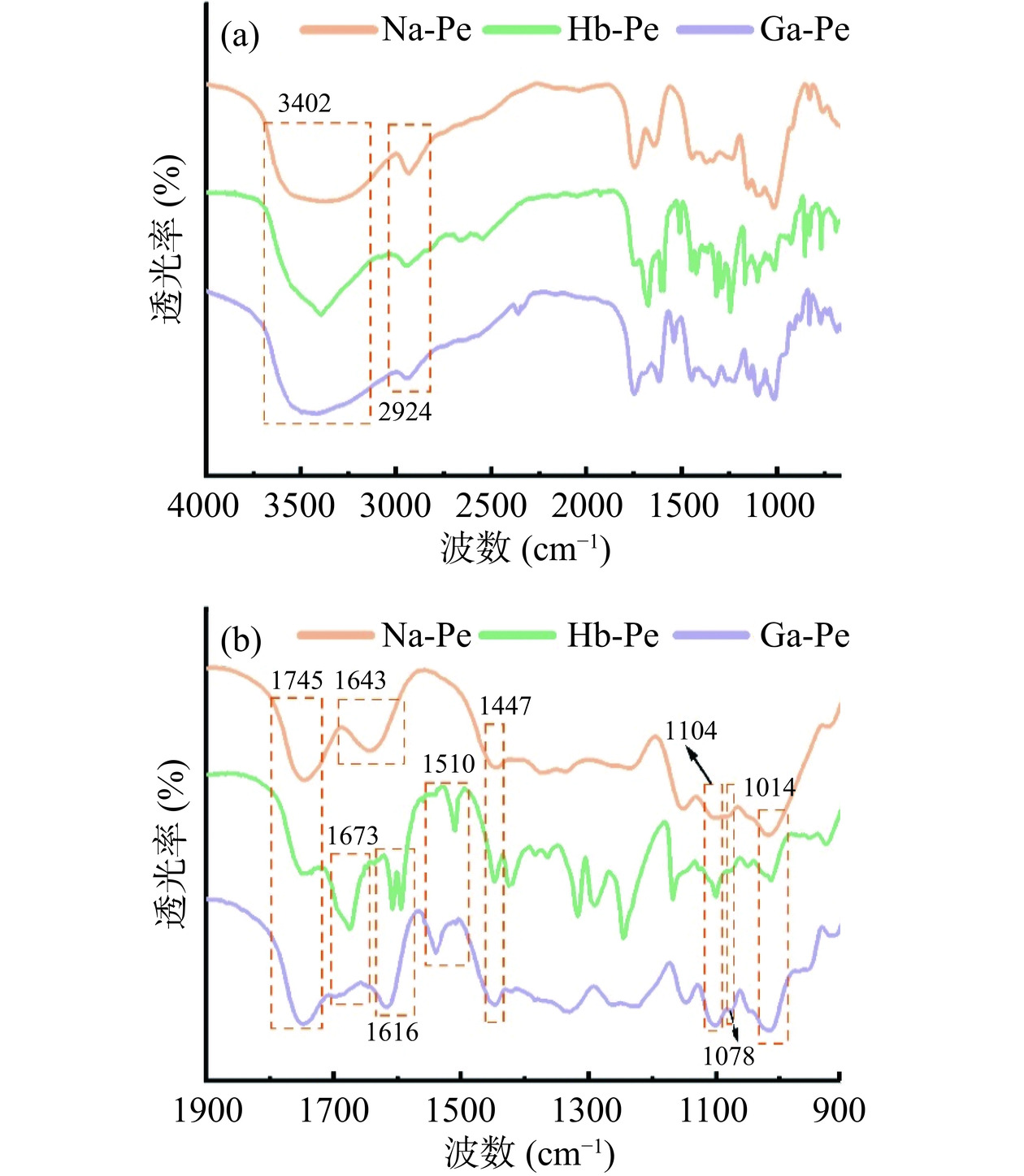
采用FTIR对天然果胶改性前后的官能团进行表征,结果如图2所示。在图2(a)中,位于3402 cm−1处的吸收峰是由于-OH、氢键的伸缩振动造成的,2924 cm−1处的吸收峰为C-H伸缩振动区内的典型峰值,主要来源为果胶的甲氧基。在果胶酰化改性后,其吸收峰相对强度有所减弱,表明酰化后果胶中甲氧基数量减少[21−23]。
图2(b)中,Na-Pe光谱中1745和1673 cm−1处的两个峰是天然果胶的特征吸收峰,分别是由半乳糖醛酸中的羧基和半乳糖醛酸甲酯中C=O的伸缩振动所引起,1447 cm−1处的吸收峰则是由羧基中C-OH的伸缩振动造成的。另外,位于1104、1078和1014 cm−1处的吸收峰是果胶分子中半乳糖醛酸糖环的骨架振动造成的。经酚酸接枝后,可以在1510 cm−1观察到一个新的吸收峰,该峰是由酚酸分子上苯环的骨架振动引起的[24]。除此之外,天然果胶位于1643 cm−1处的吸收峰被1673和1616 cm−1处的两个吸收峰覆盖,这是酚酸的羧基以及新形成的酯基造成的。以上结果表明,在脂肪酶的催化作用下,对羟基苯甲酸和没食子酸均通过其分子上的羟基与果胶分子的羧基发生酯化反应,从而实现共价接枝[25−27]。
2.3 果胶XPS分析
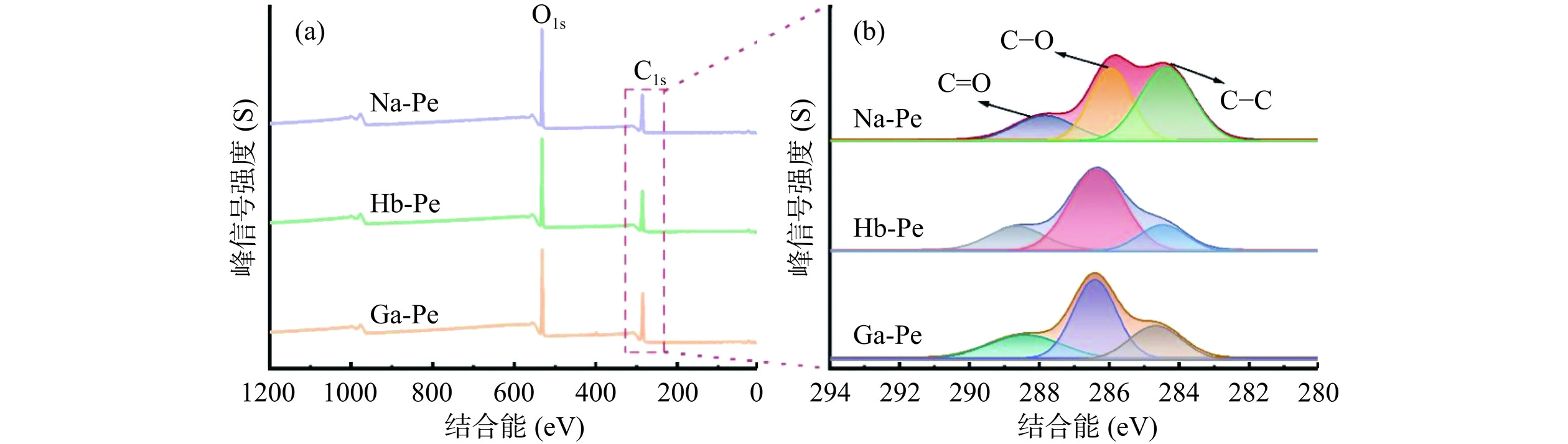
为了进一步验证FTIR分析中的结论,通过XPS对天然果胶和改性果胶中元素的结合能进行表征,其结果如图3所示。由图3(a)可以看出,C元素和O元素为天然果胶和改性果胶中最主要的元素。对C1s峰进行精细扫描,并分峰拟合,结果如图3(b)所示。可以看出,C1s峰由三个子峰组成,分别对应了果胶中C=O、C-O和C-C。另外,从图中还可以观察到,接枝两种酚酸后,C-C对应的子峰相对峰面积明显降低。显而易见,这是由于酚酸的共价接枝,进而影响了C的结合能。该结果进一步验证了FTIR的结论。
2.4 抗氧化活性分析
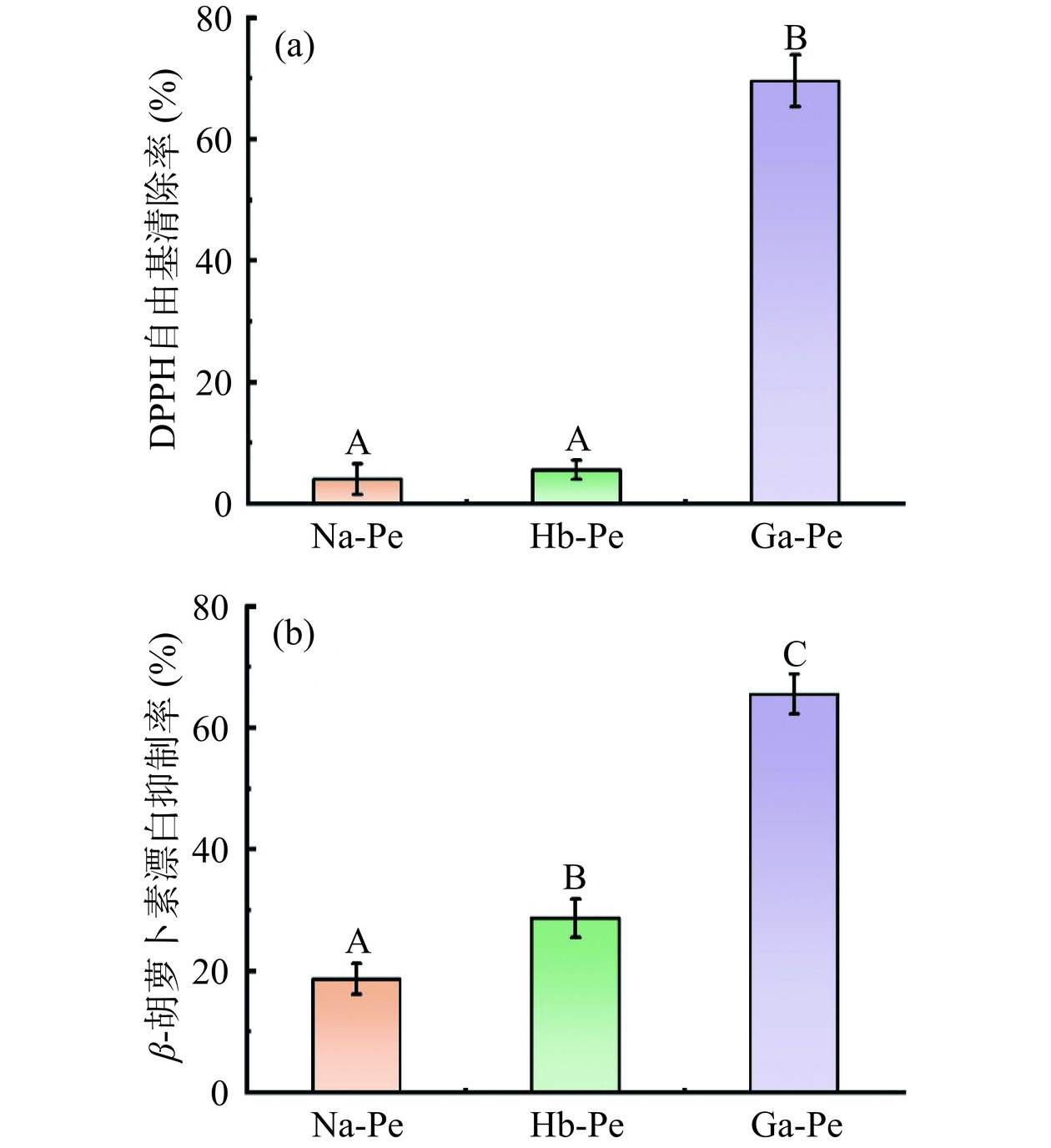
大多数酚酸具备优良的抗氧化活性,这主要得益于其分子结构中的酚羟基。酚羟基是良好的电子供体,并与氧自由基稳定结合,进而发挥抗氧化功能。然而,将酚酸通过共价连接与果胶分子结合时,可能会对酚羟基的结构完整性造成影响,进一步可能影响其原有的抗氧化活性。因此,通过DPPH自由基清除率和β-胡萝卜素漂白抑制率评价了天然果胶和改性果胶的抗氧化活性,结果如图4所示。由图4(a)可以看出,Na-Pe和Hb-Pe的DPPH自由基清除率分别为4.52%和5.54%,两者没有显著性差异(P>0.05),而Ga-Pe的DPPH自由基清除率高达69.6%。这可能是由于对羟基苯甲酸仅有一个酚羟基,其与果胶分子上的羧基形成酯基,从而失去了提供电子的能力。与此相比,没食子酸分子上具有三个酚羟基,即便损失了一个酚羟基,其接枝复合物仍然能保持优异的抗氧化活性[28]。
另外,由图4(b)可以看出,Hb-Pe和Ga-Pe的β-胡萝卜素漂白抑制率分别为28.6%和65.5%,与DPPH自由基清除率中的结果略有不同,二者均显著(P<0.05)高于Na-Pe。这可能是由于改性果胶在两种实验中的抗氧化机理不同造成的。在DPPH自由基清除实验中,改性果胶通过提供电子从而清除自由基。而在β-胡萝卜素漂白实验中,油酸在加热过程中发生链式反应,生成的自由基进攻β-胡萝卜素,并造成漂白现象。对羟基苯甲酸的引入提高了果胶的亲脂性,使其更容易吸附在油酸表面,从而阻碍了链式反应的发生,并抑制了β-胡萝卜素的漂白进程[17]。相较而言,Ga-Pe还能够进一步清除油酸产生的自由基,从而切断链式反应的发生,因此其能够最大程度抑制β-胡萝卜素的漂白现象[20,29]。
2.5 天然和改性果胶抗菌活性对比
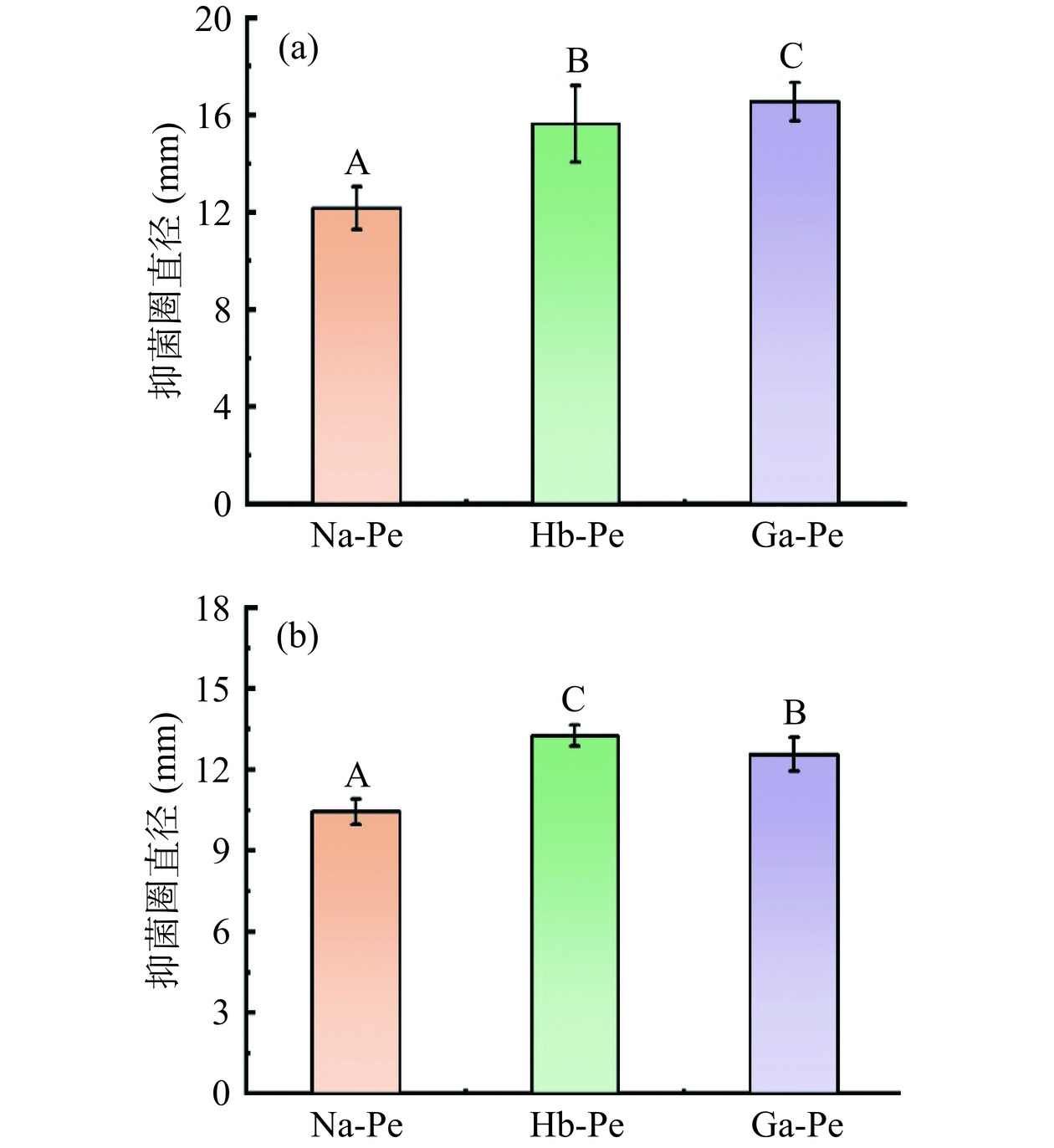
除了抗氧化活性,抑菌活性是酚酸的另一个重要特性。通过抑菌圈法测定了果胶在改性前后对大肠杆菌和金黄色葡萄球菌的抑制作用,结果如图5所示。由图5可以看出,无论是对革兰氏阴性菌(大肠杆菌)还是革兰氏阳性菌(金黄色葡萄球菌),对羟基苯甲酸和没食子酸的接枝均能显著提高果胶的抑菌活性。具体来说,Hb-Pe和Ga-Pe在对大肠杆菌的抑制作用上没有出现显著性差别,但Hb-Pe对金黄色葡萄球菌的抑制作用显著(P<0.05)高于Ga-Pe。改性果胶的抗菌机制可能与酚酸能够抑制细菌细胞膜形成、破坏细菌细胞壁通透性等原因有关[30],虽然改性果胶的抑菌机理有待进一步探索,但与天然果胶相比,其优异的抑菌活性可大大拓展其在食品包装和保鲜方面的应用。
3. 结论
本研究采用酶促接枝改性技术,成功地将对羟基苯甲酸和没食子酸接枝到果胶分子上,并通过1H NMR、FTIR和XPS等分析手段对改性果胶的结构进行了详细表征。抗氧化和抗菌活性测试结果表明,改性果胶,特别是没食子酸改性果胶(Ga-Pe),展现出显著增强的抗氧化能力和抑菌活性。本研究首次将酚酸类化合物与果胶进行酶促接枝改性,避免了传统化学法存在的催化剂残留和环境污染等问题。同时,本研究系统探究了接枝改性对果胶结构和功能性质的影响,加深了对酚酸类化合物与果胶相互作用机制的理解。本研究结果证实了酶促接枝改性在制备功能化果胶方面的可行性和有效性,为开发新型生物活性食品包装材料提供了重要的理论依据和实践指导。这些发现有望推动果胶基食品包装材料的应用,提高食品安全性和延长货架期,具有广阔的应用前景。
-
-
[1] CIRIMINNA R, FIDALGO A, SCURRIA A, et al. Pectin:New science and forthcoming applications of the most valued hydrocolloid[J]. Food Hydrocolloids,2022,127:107483. doi: 10.1016/j.foodhyd.2022.107483
[2] 张璇, 赵文, 高哲, 等. 果胶与多酚相互作用机制及其对食品加工特性影响的研究进展[J]. 食品工业科技,2024,45(1):378−386. [ZHANG X, ZHAO W, GAO Z, et al. Research progress on the interaction mechanism of pectin and polyphenol and their effect on food processing characteristics[J]. Science and Technology of Food Industry,2024,45(1):378−386.] ZHANG X, ZHAO W, GAO Z, et al. Research progress on the interaction mechanism of pectin and polyphenol and their effect on food processing characteristics[J]. Science and Technology of Food Industry, 2024, 45(1): 378−386.
[3] 陈怡君, 王晓慧, 陈艳萍, 等. 响应面法优化超声波-微波协同辅助酸法提取猕猴桃皮果胶工艺及果胶理化性质分析[J]. 食品与发酵工业,2022,48(13):238−246. [CHEN Y J, WANG X H, CHEN Y P, et al. Optimization of ultrasound-microwave assisted acid extraction of pectin from kiwifruit peel by response surface method and the analysis of physicochemical properties of pectin[J]. Food and Fermentation Industries,2022,48(13):238−246.] CHEN Y J, WANG X H, CHEN Y P, et al. Optimization of ultrasound-microwave assisted acid extraction of pectin from kiwifruit peel by response surface method and the analysis of physicochemical properties of pectin[J]. Food and Fermentation Industries, 2022, 48(13): 238−246.
[4] THIVYA P, BHOSALE Y K, ANANDAKUMAR S, et al. Development of active packaging film from sodium alginate/carboxymethyl cellulose containing shallot waste extracts for anti-browning of fresh-cut produce[J]. International Journal of Biological Macromolecules,2021,188:790−799. doi: 10.1016/j.ijbiomac.2021.08.039
[5] SGANZERLA W G, DA ROSA C G, DA SILVA A P G, et al. Application in situ of biodegradable films produced with starch, citric pectin and functionalized with feijoa (Acca sellowiana (Berg) Burret) extracts:An effective proposal for food conservation[J]. International Journal of Biological Macromolecules,2021,189:544−553. doi: 10.1016/j.ijbiomac.2021.08.146
[6] HUANG B Q, ZHANG Z G, DING N S, et al. Preparation of acylated chitosan with caffeic acid in non-enzymatic and enzymatic systems:Characterization and application in pork preservation[J]. International Journal of Biological Macromolecules,2022,194:246−253. doi: 10.1016/j.ijbiomac.2021.11.193
[7] HUANG B Q, ZHANG Z G, DING N S, et al. Investigation of the pectin grafting with gallic acid and propyl gallate and their antioxidant activities, antibacterial activities and fresh keeping performance[J]. International Journal of Biological Macromolecules,2021,190:343−350. doi: 10.1016/j.ijbiomac.2021.08.219
[8] FLÓREZ M, GUERRA-RODRÍGUEZ E, CAZÓN P, et al. Chitosan for food packaging:Recent advances in active and intelligent films[J]. Food Hydrocolloids,2022,124:107328. doi: 10.1016/j.foodhyd.2021.107328
[9] RINCÓN E, ESPINOSA E, GARCÍA-DOMÍNGUEZ M T, et al. Bioactive pectic polysaccharides from bay tree pruning waste:Sequential subcritical water extraction and application in active food packaging[J]. Carbohydrate Polymers,2021,272:118477. doi: 10.1016/j.carbpol.2021.118477
[10] ZHOU Z C, HAN P, BAI S Q, et al. Caffeic acid-grafted-chitosan/polylactic acid film packaging enhances the postharvest quality of Agaricus bisporus by regulating membrane lipid metabolism[J]. Food Research International,2022,158:111557. doi: 10.1016/j.foodres.2022.111557
[11] SANTOS L P, MORAIS D R, SOUZA N E, et al. Phenolic compounds and fatty acids in different parts of Vitis labrusca and V. vinifera grapes[J]. Food Research International,2011,44(5):1414−1418. doi: 10.1016/j.foodres.2011.02.022
[12] FU L L, XIAO Q, RU Y, et al. Bio-based active packaging:Gallic acid modified agarose coatings in grass carp (Ctenopharyngodon idellus) preservation[J]. International Journal of Biological Macromolecules,2024,255:128196. doi: 10.1016/j.ijbiomac.2023.128196
[13] ZHANG L L, WANG W B, YUE X Y, et al. Gallic acid as a copigment enhance anthocyanin stabilities and color characteristics in blueberry juice[J]. Journal of Food Science and Technology Mysore,2020,57(4):1405−1414. doi: 10.1007/s13197-019-04175-w
[14] HUANG J Y, HU Z H, HU L P, et al. Pectin-based active packaging:A critical review on preparation, physical properties and novel application in food preservation[J]. Trends in Food Science & Technology,2021,118:167−178.
[15] 杨鹄隽, 左锋, 王坤, 等. 基于自由基介导的酚酸-柑橘果胶接枝共聚物制备及其理化特性[J]. 食品科学,2022,43(24):60−66. [YANG H J, ZUO F, WANG K, et al. Preparation and physicochemical properties of phenolic acid-citrus pectin graft copolymers mediated by free radicals[J]. Food Science,2022,43(24):60−66.] doi: 10.7506/spkx1002-6630-20220301-018 YANG H J, ZUO F, WANG K, et al. Preparation and physicochemical properties of phenolic acid-citrus pectin graft copolymers mediated by free radicals[J]. Food Science, 2022, 43(24): 60−66. doi: 10.7506/spkx1002-6630-20220301-018
[16] LIU J N, ZHUANG Y H, HU Y H, et al. Improving the color stability and antioxidation activity of blueberry anthocyanins by enzymatic acylation with p-coumaric acid and caffeic acid[J]. LWT-Food Science and Technology,2020,130:109673. doi: 10.1016/j.lwt.2020.109673
[17] ZHANG G G, ZHENG C M, HUANG B Q, et al. Preparation of acylated pectin with gallic acid through enzymatic method and their emulsifying properties, antioxidation activities and antibacterial activities[J]. International Journal of Biological Macromolecules,2020,165:198−204. doi: 10.1016/j.ijbiomac.2020.09.195
[18] LIU J N, WANG T L, HUANG B Q, et al. Pectin modified with phenolic acids:Evaluation of their emulsification properties, antioxidation activities, and antibacterial activities[J]. International Journal of Biological Macromolecules,2021,174:485−493. doi: 10.1016/j.ijbiomac.2021.01.190
[19] LIU J, N CHEN B Q, HU Q Y, et al. Pectin grafted with resorcinol and 4-hexylresorcinol:Preparation, characterization and application in meat preservation[J]. International Journal of Biological Macromolecules,2023,237:124212. doi: 10.1016/j.ijbiomac.2023.124212
[20] YANG W, KORTESNIEMI M, YANG B, et al. Enzymatic acylation of anthocyanins isolated from alpine bearberry (Arctostaphylos alpina) and lipophilic properties, thermostability, and antioxidant capacity of the derivatives[J]. Journal of Agricultural and Food Chemistry,2018,66(11):2909−2916. doi: 10.1021/acs.jafc.7b05924
[21] PAN J, XU H, DABBOUR M, et al. Effect of pectin concentration on emulsifying properties of black soldier fly (Hermetia illucens) larvae albumin modified by pH-shifting and ultrasonication[J]. International Journal of Biological Macromolecules,2024,257:128779. doi: 10.1016/j.ijbiomac.2023.128779
[22] 刘敏, 罗国柳, 覃小丽, 等. 果胶酯化度对酪蛋白-果胶相互作用及其复合物性能的影响[J]. 食品与发酵工业,2023,49(24):80−87. [LIU M, LUO G L, QIN X L, et al. Interaction and properties of the noncovalent of casein-pectin complexes:Effect of esterified degree of pectin[J]. Food and Fermentation Industries,2023,49(24):80−87.] LIU M, LUO G L, QIN X L, et al. Interaction and properties of the noncovalent of casein-pectin complexes: Effect of esterified degree of pectin[J]. Food and Fermentation Industries, 2023, 49(24): 80−87.
[23] ZHENG C M, ZHANG Z G, DING N S, et al. Synthesis of amidated pectin with amino acid using ultra-low temperature enzymatic method and its evaluation of fat mimic characteristics[J]. Food Hydrocolloids,2022,125:107454. doi: 10.1016/j.foodhyd.2021.107454
[24] LI R X, FAN H K, LI B W, et al. Comparison on emulsifying and emulgelling properties of low methoxyl pectin with varied degree of methoxylation from different de-esterification methods[J]. International Journal of Biological Macromolecules,2024,263:130432. doi: 10.1016/j.ijbiomac.2024.130432
[25] WANG P K, FEI P, ZHOU C X, et al. Stearic acid esterified pectin:Preparation, characterization, and application in edible hydrophobic pectin/chitosan composite films[J]. International Journal of Biological Macromolecules,2021,186:528−534. doi: 10.1016/j.ijbiomac.2021.06.030
[26] CAI J, ZENG F S, ZHENG S Y, et al. Preparation of lipid-soluble bilberry anthocyanins through acylation with cinnamic acids and their antioxidation activities[J]. Journal of Agricultural and Food Chemistry,2020,68(28):7467−7473. doi: 10.1021/acs.jafc.0c01912
[27] WANG P K, FEI P, ZHOU C X, et al. Preparation of acylated pectins with phenolic acids through lipase-catalyzed reaction and evaluation of their preservation performance[J]. LWT-Food Science and Technology,2021,147:111615. doi: 10.1016/j.lwt.2021.111615
[28] IBEOGU I H, BAKO H K, YAR M S, et al. Gelatin-serum plasma film incorporated with curcumin for improvement of antioxidant and antibacterial properties for fresh pork packaging application[J]. Food Hydrocolloids,2024,149:109617. doi: 10.1016/j.foodhyd.2023.109617
[29] YANG W, KORTESNIEMI M, MA X, et al. Enzymatic acylation of blackcurrant (Ribes nigrum) anthocyanins and evaluation of lipophilic properties and antioxidant capacity of derivatives[J]. Food Chemistry,2019,281:189−196. doi: 10.1016/j.foodchem.2018.12.111
[30] XIANG Z D, GUAN H D, ZHAO X, et al. Dietary gallic acid as an antioxidant:A review of its food industry applications, health benefits, bioavailability, nano-delivery systems, and drug interactions[J]. Food Research International,2024,180:114068. doi: 10.1016/j.foodres.2024.114068
-
期刊类型引用(5)
1. 尚学钰,美合日班,苏玲,王琦. 黑木耳可溶性膳食纤维功能特性和降脂活性研究. 食品工业科技. 2025(02): 112-121 .  本站查看
本站查看
2. 张潇予,王丹妮,柴欣,于卉娟,崔英,王跃飞. 补骨脂的质量特征解析及其在减毒工艺中的应用. 中草药. 2024(08): 2784-2791 .  百度学术
百度学术
3. 马力亚,李梅梅,黄玉卓,舒劲. 四神丸治疗溃疡性结肠炎的研究概况. 中医药临床杂志. 2024(05): 987-994 .  百度学术
百度学术
4. 徐波,陈天天,杜薛平,张海峰,陈伟,黄凯健,董大勇. 益肾化痰祛瘀方治疗绝经后骨质疏松症(肾虚血瘀型)的效果及对氧化应激的影响. 中医药学报. 2024(09): 60-63 .  百度学术
百度学术
5. 钟婉滢,苗建银,叶灏铎,马凤,胡一晨. 藜麦蛋白肽的酶解制备及体外降血脂与降尿酸活性研究. 食品工业科技. 2023(23): 156-166 .  本站查看
本站查看
其他类型引用(1)





 下载:
下载:
 下载:
下载:



