Determination of Five Alkaloids in Vinegar Corydalis yanhusuo by Quantitative Analysis of Multi-components by Single Marker Method
-
摘要: 目的:以延胡索乙素为内参物,建立一测多评法(QAMS)用于测定醋延胡索中5种生物碱类成分的含量。方法:采用高效液相色谱法,以乙腈-水(含0.1%磷酸, pH6.0)为流动相,梯度洗脱,根据各成分含量与色谱峰面积之间的关系,计算原阿片碱、盐酸巴马汀、盐酸小檗碱及延胡索甲素与延胡索乙素的相对校正因子(RCF),进行方法学考察,测定5种生物碱成分含量,并采用外标法(ESM)测定含量,比较两种方法含量测定结果的差异,验证QAMS的准确性和可行性。结果:原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索甲素的相对于延胡索乙素的RCF分别为0.405、1.868、1.571、1.049;5种生物碱类成分在一定范围内线性关系良好,精密度、重复性和稳定性符合要求,平均回收率在98.38%~101.28%之间;10批不同产地延胡索经醋制后的炮制品,采用QAMS与ESM所测定5种生物碱的含量无显著差异。结论:所建立的QAMS法可用于醋延胡索中5种生物碱类成分的定量分析,结果准确、方法可行,该方法可为含生物碱类成分、多指标质量控制的中药材及炮制品的质量评价提供参考。Abstract: Objective: Setting tetrahydropalmatine as an internal reference, to establish a quantitative analysis of multi-components by single marker (QAMS) method for the determination of five alkaloids contents in vinegar Corydalis yanhusuo. Method: HPLC was employed using gradient elution with a mobile phase consisting of acetonitrile-water (containing 0.1% phosphoric acid, pH6.0). The methodological investigation was conduct to estalish a proper method. According to the relationship between the content and the chromatographic peak area of each component, calculated the relative correction factors (RCF) of protopine, palmatine hydrochloride, berberine hydrochloride and corydaline to tetrahydropalmatine. And then, the contents of five alkaloid components were determined in the various samples. Meanwhile, external standard method (ESM) was used to determine the contents. The variation in the results obtained from QAMS and RCF was statistically analyzed to confirm the precision and practicability of QAMS. Results: The linear relationship between the five alkaloids was good in a certain linear range, and the precision, stability, and repeatability met the required standards. The average recovery ranged from 98.38% to 101.28%. The RCF values of protopine, palmatine hydrochloride, berberine hydrochloride, and corydaline to tetrahydropalmatine were 0.405, 1.868, 1.571, and 1.049, respectively. There was no significant difference in the content of the five alkaloids measured by QAMS and ESM in 10 batches of processed Corydalis yanhusuo from different regions after vinegar processing. Conclusion: The developed QAMS method in this study could be effectively used for the quantitative analysis of five alkaloid components in vinegar Corydalis yanhusuo. The results were highly accurate and the method was considered feasible. This method could be served as a valuable reference for the quality evaluation of raw and processed products of TCM, containing alkaloids or multi-indicator components.
-
延胡索又名元胡,具有悠久的食用和药用历史,其粉末加入红糖水中可缓解腹痛[1],加入三七大蒜糊中可缓解癌痛[2]。根据“醋注肝经,且资住痛”理论,延胡索醋制后归肝经作用增强,因此多采用其醋制品来发挥镇痛作用[3]。生物碱类化合物是一类重要的天然产物,是(醋)延胡索发挥活性的主要成分[4−5],主要包括原小檗碱类(叔胺类延胡索甲素、延胡索乙素和季胺类盐酸小檗碱、盐酸巴马汀)、原阿片类(原阿片碱)等生物碱类成分[6],其中原阿片碱,具有镇痛、抗炎、抗癌等作用[7−8];延胡索甲素、延胡索乙素同为延胡索行血镇痛的主要活性成分,具有镇痛、镇静、保护胃肠道等作用[9−10],盐酸巴马汀具有抗炎、抗菌、抗溃疡等作用[11−12],盐酸小檗碱具有抑菌、降糖、保护神经系统等作用[13−14]。上述5种生物碱为其发挥活性的主要物质基础[15],因此将原阿片碱、盐酸小檗碱、盐酸巴马汀、延胡索乙素以及延胡索甲素选为指标成分进行含量测定。
目前对醋延胡索的质量控制中,一般仅针对延胡索乙素,难以全面控制其质量,也有采用色谱法测定醋延胡索中多种生物碱类成分含量的报道[16−17],但面临指标性成分选择困难,对照品价格昂贵的问题。一测多评法(quantitative analysis of multi-componentsby single marker,QAMS)是利用有效成分间存在的内在函数关系,在相应的线性范围内,在仅测定一个成分(内参物)的基础上,实现对多种成分同步检测的方法[18],该方法通过建立内参物与待测成分之间的相对校正因子(relative correction factory,RCF),作为计算多种待测成分含量的依据,解决单一指标成分控制质量不够全面,多指标成分控制质量对照品价格昂贵、难以获得全部的问题,已广泛应用于斑花黄堇、钩藤、苦参等含有多种生物碱成分的中药材的质量评价中[19−23]。
虽有采用一测多评法测定延胡索中多种生物碱含量的报道[24−25],但关于一测多评方法应用于醋延胡索的研究较少。因此本研究采用统一的醋制法对不同产地延胡索按相关标准进行炮制,旨在避免因炮制方法不同而导致的中药材质量差异,随后通过梯度洗脱HPLC色谱技术,选取价廉易得的延胡索乙素为内参物,拟合延胡索乙素与各生物碱类成分的相对校正因子,通过只测定延胡索乙素的含量,实现对醋延胡索中原阿片碱、盐酸小檗碱、盐酸巴马汀及延胡索甲素延胡索含量的同步,减少了对照品的使用数量,降低了检测成本,为醋延胡索中生物碱类成分的含量测定提供了新思路。
1. 材料与方法
1.1 材料与仪器
延胡索 10批不同产地样品,信息来源见表1,经鉴定均为罂粟科紫堇属植物延胡索(Corydalis yanhusuo W.T.Wang)的干燥块茎;氨水(分析纯) 天津市科密欧化学试剂有限公司;米醋 广东李锦记食品有限公司;乙腈(色谱纯) 北京Dimka公司;磷酸(分析纯) 天津市光复精细化工研究所;甲醇(分析纯) 天津大茂化学试剂厂;超纯水;原阿片碱(批号:110853-201805,纯度:99.6%)、延胡索甲素(批号:110720-202019,纯度:99.5%)、盐酸巴马汀(批号:110732-201913,纯度:85.7%)、延胡索乙素(批号:110726-202020,纯度:99.3%)、盐酸小檗碱(批号:110713-202015,纯度:85.9%) 中国食品药品检定研究院。
表 1 延胡索样品来源信息Table 1. Source information of Corydalis yanhusuo samples样品编号 产地 批号 S1 河南唐河 210606 S2 河南信阳 Z2001008 S3 陕西汉中 C808210701 S4 陕西宝鸡 20220101 S5 浙江金华 211001 S6 浙江东阳 20221001 S7 安徽亳州 21120101 S8 广西玉林 211009 S9 湖北武汉 210202 S10 河北承德 200912 日立Chromaster液相色谱仪(配有5410型检测器、5310型柱温箱、5210型自动进样器、5110二元梯度洗脱泵) 日本HITACHI公司;VGT-1990QTD型超声波清洗器 苏州江东精密仪器限公司;RE-52A型旋转蒸发仪 上海亚荣生化仪器厂;JJ124BF型天平 上海精胜科学仪器有限公司;YB-2500A粉碎机 永康式速峰工贸有限公司;DF型真空干燥箱 上海力辰邦西仪器科技有限公司。
1.2 实验方法
1.2.1 对照品溶液的制备
分别精密称取原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索乙素、延胡索甲素对照品适量,加甲醇溶解制成浓度为96.00 μg/mL原阿片碱、24.00 μg/mL盐酸巴马汀、62.50 μg/mL盐酸小檗碱、120.50 μg/mL延胡索乙素与100.50 μg/mL延胡索甲素的混合对照品储备溶液。取1 mL上述混合对照品储备溶液于5 mL容量瓶中,加甲醇定容,制成含19.20 μg/mL原阿片碱、4.80 μg/mL盐酸巴马汀、12.50 μg/mL盐酸小檗碱、24.10 μg/mL延胡索乙素与20.10 μg/mL延胡索甲素的混合对照品溶液。
1.2.2 醋延胡索样品的制备
将10批延胡索样品,按《中国药典》2020年版[26]醋灸法炮制:取净延胡索薄片,称重,取20 g延胡索药材,用4 g米醋拌匀,置于密闭容器中,加盖闷润,待醋被吸进后,翻炒至表面颜色略为加深,取出、置于真空干燥箱中,干燥后用中药粉碎机粉碎,即得。
1.2.3 供试品溶液的制备
取“1.2.2”项下醋延胡索粉末(过三号筛)0.5 g,精密称定,置于圆底烧瓶中,精密加入浓氨试液-甲醇(1:20)混合溶液50 mL,称重,60 ℃回流提取1 h,冷却,再称重,用浓氨试液-甲醇(1:20)补足减失的重量,摇匀,过滤,精密量取续滤液25 mL,旋转蒸发仪蒸干,加甲醇溶解残渣,并转移到5 mL量瓶中,加入甲醇定容,摇匀,0.45 μm微孔滤膜过滤,取续滤液,即得[27]。
1.2.4 液相色谱条件
Diamonsil C18 色谱柱(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸水溶液(三乙胺调至pH6.0,B);梯度洗脱(0~15 min,22% A;15~35 min,22%~80% A;35~50 min,80% A);检测波长为280 nm;流速为1.0 mL/min;柱温为30 ℃;进样量为10 μL;理论塔板数按延胡索乙素计不低于3000;分离度>1.5.
1.2.5 QAMS方法学考察
1.2.5.1 线性关系、检出限和定量限
精密取“1.2.1”项下混合对照品储备溶液,精确取0.25、0.5、1、2、4 mL的混和对照品溶液液,分别置于5 mL容量瓶中,加甲醇定容,按“1.2.4”项下色谱条件进样测定,以不同对照品溶液浓度(C)为横坐标,峰面积(A)为纵坐标进行回归,计算回归方程。取“1.2.1”项下混合对照品溶液,逐级稀释,按“1.2.2”项下色谱条件测定,计算信噪比(S/N),以S/N=3时对应的待分析物浓度为检出限,S/N=10时对应的待分析物浓度为定量限。
1.2.5.2 相对校正因子
采用多点校正法[28],精密取混合对照品溶液,按“1.2.4”项下色谱条件分别进样1、2、5、8、10、20 μL。记录各成分色谱峰峰面积,以延胡索乙素为内参物(S),按下列公式计算各成分的相对校正因子(fi/s):
fi/s=Ai×CsAs×Ci 式中:fi/s表示相对校正因子;AS表示内参物的峰面积,mAU·min;CS表示内参物的浓度,μg/mL;Ai表示待测成分的峰面积,mAU·min;Ci表示待测成分的浓度,μg/mL。
1.2.5.3 待测组分色谱峰定位
利用相对保留时间法[29]ri/s=ti/ts(ti:待测成分的保留时间,min;ts:内参物的保留时间,min;ri/s为二者的比值即相对保留时间)。对不同仪器和色谱柱、不同体积流量、不同柱温的待测组分色谱峰进行定位;根据保留时间计算公式,已知内参物延胡索乙素的保留时间,根据对原阿片碱、盐酸小檗碱、盐酸巴马汀、延胡索甲素的相对保留时间以及各生物碱的峰型进行定位。
1.2.5.4 精密度、重复性、重复性和平均回收率
精确移取“1.2.1”项下混合对照品溶液1份,进样测定,连续进样6次,进行精密度试验;精密称定醋延胡索样品(S1)1份,按“1.2.3”项下方法制备6份供试品溶液,进样测定,记录5种生物碱的峰面积并计算RSD值,进行重复性试验;精密称定醋延胡索样品(S1)1份,按“1.2.3”项下方法制备供试品溶液,分别于0、2、4、8、12、24 h进样测定,记录5种生物碱的峰面积并计算RSD值,进行稳定性试验;精密称定醋延胡索样品(S1)9份,每份0.25 g,分别精密加入相当于供试品中待测成分含量的80%、100%、120%的混合对照品溶液,按“1.2.3”项下方法制备供试品溶液,进样测定,进行加样回收率试验。
1.2.5.5 耐用性和系统适用性
精密取混合对照品溶液10 μL,按“1.2.4”项下色谱条件进样,考察不同实验室的两套液相色谱Hitachi Chromaster、Hitachi ELITE LaChrom系统及三种不同色谱柱Promosil C18(250 mm×4.6 mm,5 μm)、Agilent C18(250 mm×4.6 mm,5 μm)、Diamonsil C18(250 mm×4.6 mm,5 μm),不同体积流量(0.8、1.0、1.2 mL/min)、不同柱温(25、30、35 ℃)对相对校正因子的影响。
1.2.6 生物碱含量测定
分别取经炮制的10批醋延胡索药材,按“1.2.3”项下方法制备供试品溶液、“1.2.4”项下色谱条件进样测定,每份测定三次,分别采用外标法[30](external standard method,ESM)Cx=Cr×Ax/Ar(Cx为样品浓度,μg/mL;Cr为对照浓度,μg/mL;Ax为样品峰面积,mAU·min;Ar为对照峰面积,mAU·min)和建立的QAMS测定醋延胡索样品中原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索乙素、延胡索甲素5种生物碱的含量。
1.3 数据处理
利用Microsoft Excel 2019软件进行数据汇总和分析,应用IBM SPSS Statistics 27.0软件进行t检验分析。
2. 结果与分析
2.1 QAMS方法学考察结果
2.1.1 线性关系
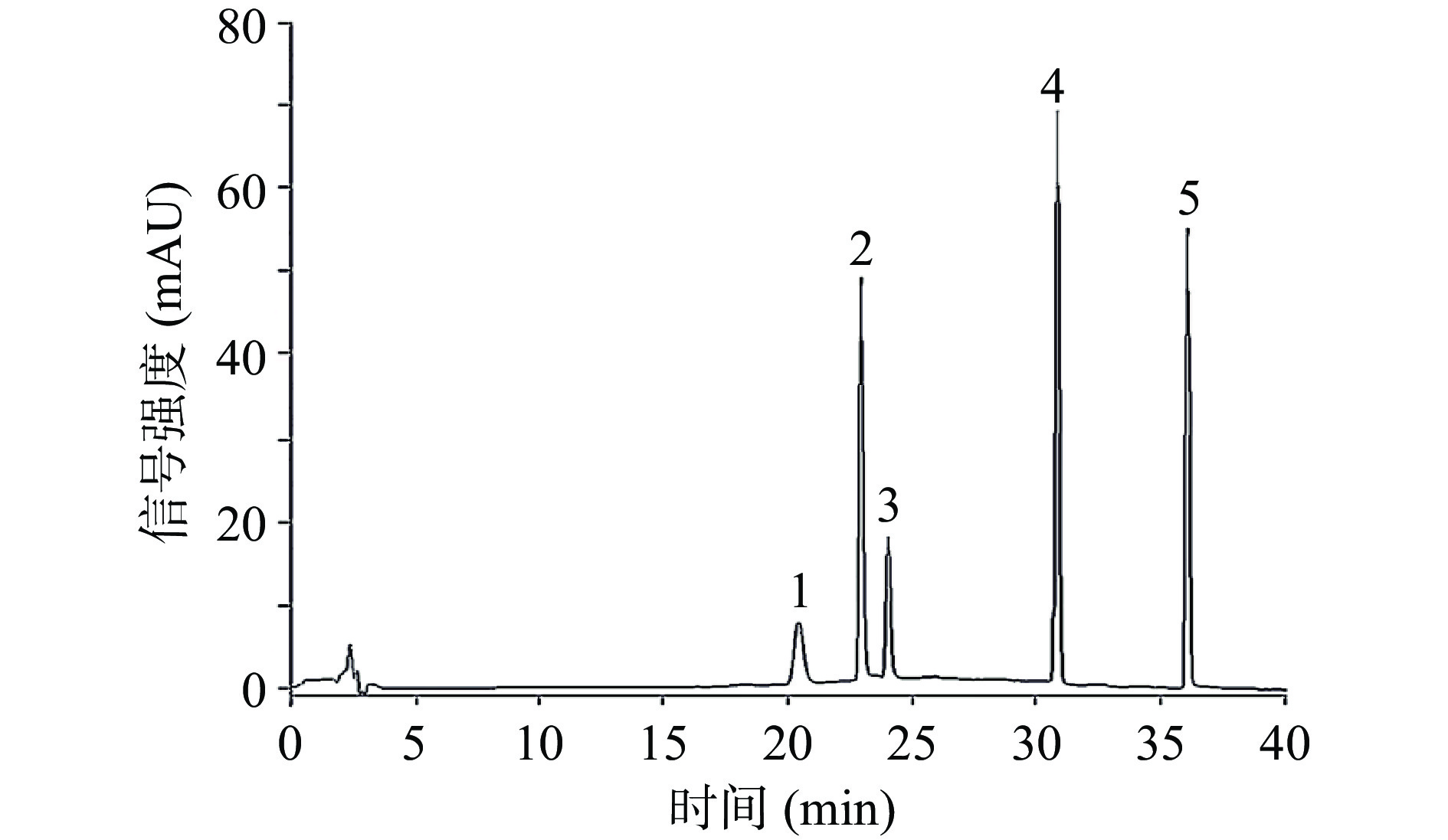
记录5种生物碱混合对照品色谱图如图1。以不同对照品溶液浓度(C)为横坐标,峰面积(A)为纵坐标进行回归分析,结果见表2。结果表明,这5种生物碱在线性范围内与峰面积线性关系良好,相关系数r>0.9992。以S/N=3时计算得出检出限为0.036~0.089 μg/mL,S/N=10时计算得出定量限为0.127~0.314 μg/mL。
表 2 对照品的线性关系、检出限与定量限Table 2. Linear relationships, LODs and LOQs of reference substance生物碱 回归方程 线性范围
(μg/mL)r 检出限
(μg/mL)定量限
(μg/mL)原阿片碱 y=6176.1x+9964.4 3.84~76.80 0.9996 0.063 0.211 盐酸小檗碱 y=24608x+8570.6 0.96~19.20 0.9999 0.089 0.314 盐酸巴马汀 y=28475x+30653 2.50~50.00 0.9995 0.036 0.127 延胡索乙素 y=14864x+38433 4.82~96.40 0.9993 0.081 0.303 延胡索甲素 y=15476x+36195 4.01~80.20 0.9992 0.067 0.228 2.1.2 相对校正因子
按“1.2.5.2”项下进行试验,以延胡索乙素为内参物,计算原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索甲素相对校正因子,取相对校正因子的平均值为定量用的fi/s,结果见表3,可知,原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索甲素相对于延胡索乙素的fi/s分别为1.71、1.91、2.63、0.75,RSD值<3%。
表 3 醋延胡索中4个成分的相对校正因子Table 3. Relative correction factors of four components in vinegar Corydalis yanhusuo进样量(μL) fa/s fb/s fc/s fd/s 1 0.415 1.905 1.639 1.041 2 0.405 1.906 1.596 1.043 5 0.406 1.850 1.551 1.056 8 0.408 1.847 1.568 1.048 10 0.398 1.815 1.522 1.062 20 0.396 1.865 1.549 1.045 平均值 0.405 1.865 1.571 1.049 RSD% 1.71 1.91 2.63 0.78 注:s为延胡索乙素,a~d为原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索甲素;表4、表6同。 2.1.3 待测组分色谱峰定位
按“1.2.5.3”项下进行试验,计算原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索甲素相对于延胡索乙素的相对保留时间ri/s和ri/s的RSD,结果见表4,可知不同仪器与色谱柱、不同体积流量、不同柱温的RSD值均<3%,对相对保留值影响较小,表明相对保留时间法可用于待测组分色谱峰的定位。
表 4 不同因素对相对保留时间的影响Table 4. Effects of different factors on relative retention times因素 ra/s rb/s rc/s rd/s 仪器与
色谱柱Hitachi
ChromasterPromosil C18 0.645 0.734 0.753 1.122 Agilent C18 0.651 0.750 0.774 1.136 Diamonsil C18 0.648 0.760 0.778 1.112 Hitachi ELITE
LaChromPromosil C18 0.653 0.761 0.790 1.125 Agilent C18 0.671 0.754 0.778 1.126 Diamonsil C18 0.628 0.740 0.768 1.133 平均值 0.649 0.750 0.774 1.126 RSD(%) 2.14 1.45 1.60 0.76 流速 0.8 mL/min 0.648 0.752 0.764 1.125 1.0 mL/min 0.653 0.754 0.772 1.128 1.2 mL/min 0.667 0.740 0.780 1.119 平均值 0.656 0.749 0.772 1.124 RSD% 1.50 1.01 1.04 0.41 柱温 25 ℃ 0.653 0.754 0.769 1.129 30 ℃ 0.658 0.748 0.775 1.126 35 ℃ 0.655 0.752 0.781 1.123 平均值 0.655 0.751 0.775 1.126 RSD(%) 0.38 0.40 0.77 0.27 2.1.4 精密度、稳定性、重复性和回收率
按“1.2.5.4”项下进行试验,5种生物碱的精密度、重复性、稳定性及加样回收率考察结果见表5,精密度、重复性、稳定性RSD均小于2%,平均回收率在98.38%~101.28%之间,RSD值均小于2%,表明该方法精密度、重复性、稳定性及回收率良好。
表 5 5种生物碱的精密度、稳定性重复性和回收率Table 5. Precision, stability, repeatability and recovery of five alkaloids生物碱 精密度 重复性 稳定性 回收率 RSD(%) RSD(%) RSD(%) 平均回收率
(%)RSD
(%)原阿片碱 0.92 0.66 1.08 98.38 1.52 盐酸小檗碱 0.90 0.86 1.29 101.28 1.37 盐酸巴马汀 0.58 1.02 0.73 98.32 1.46 延胡索乙素 0.89 1.44 0.68 99.28 0.87 延胡索甲素 0.82 1.32 0.89 98.36 0.86 2.1.5 耐用性和系统适用性
按“1.2.5.5”项下进行试验、按“1.2.5.2”项下方法计算原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索甲素相对于延胡索乙素的校正因子fi/s和fi/s的RSD值,结果见表6,可知不同仪器与色谱柱、不同流速及柱温对醋延胡索中各生物碱类成分的fi/s的RSD值均<3%,表明色谱柱、仪器的更换、流速及柱温的微小变化对fi/s无显著影响。
表 6 不同因素对相对校正因子的影响Table 6. Effects of different factors on relative correction factors因素 fa/s fb/s fc/s fd/s 仪器与
色谱柱Hitachi
ChromasterPromosil C18 0.415 1.905 1.639 1.045 Agilent C18 0.419 1.983 1.674 1.037 Diamonsil C18 0.416 1.932 1.565 1.032 Hitachi ELITE
LaChromPromosil C18 0.409 1.915 1.565 1.044 Agilent C18 0.401 1.860 1.568 1.054 Diamonsil C18 0.404 1.873 1.473 1.032 平均值 0.411 1.911 1.581 1.041 RSD(%) 1.75 1.90 1.55 0.83 流速 0.8 mL/min 0.409 1.806 1.541 1.047 1.0 mL/min 0.408 1.828 1.573 1.044 1.2 mL/min 0.405 1.896 1.581 1.043 平均值 0.407 1.843 1.565 1.045 RSD% 0.51 2.55 1.35 0.20 柱温 25 ℃ 0.415 1.921 1.605 1.048 30 ℃ 0.408 1.928 1.573 1.038 35 ℃ 0.420 1.926 1.592 1.032 平均值 0.414 1.925 1.590 1.039 RSD(%) 1.45 0.19 1.01 0.78 2.2 生物碱含量测定
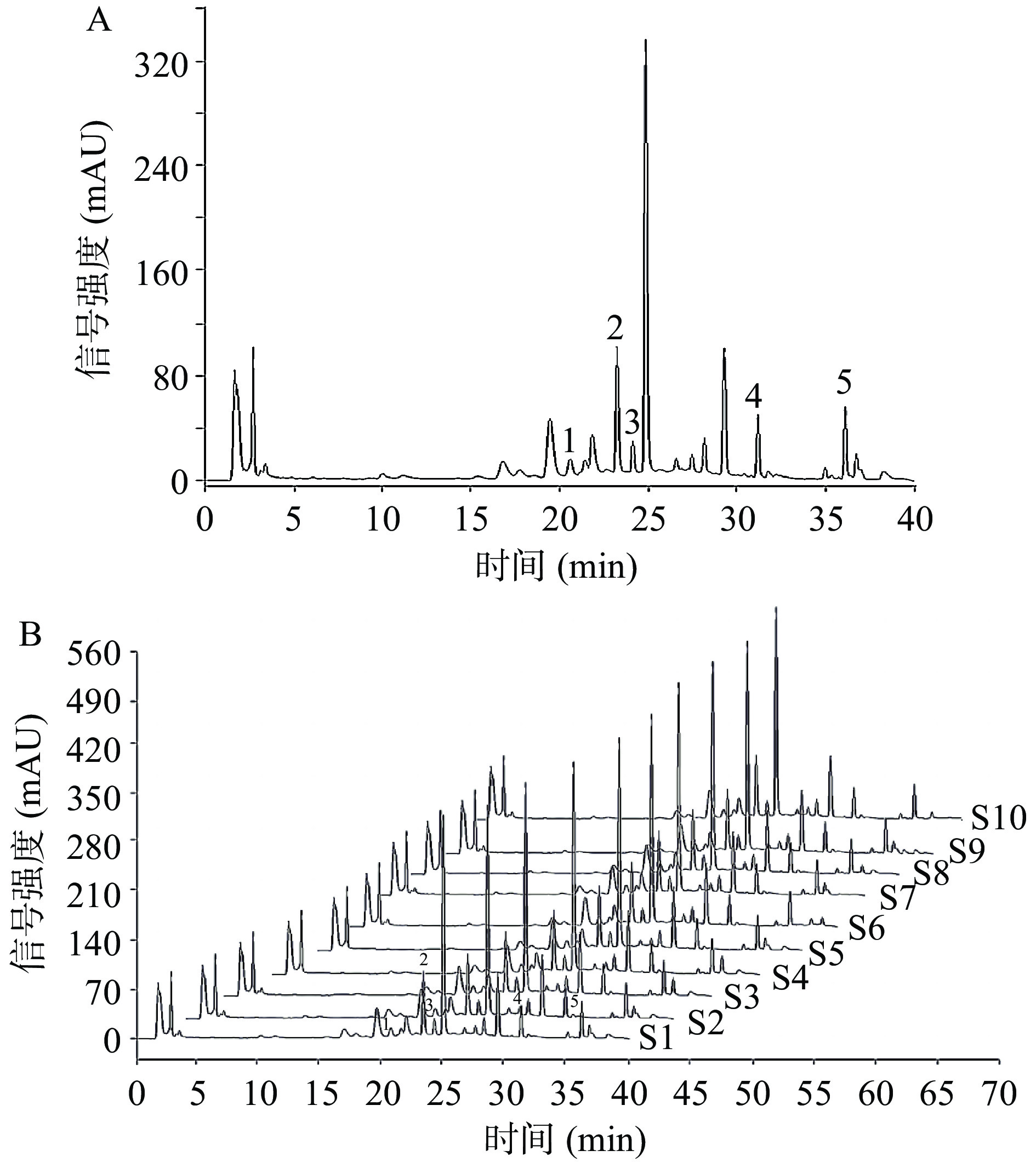
按“1.2.6”项下进行试验,记录时色谱图(S1、图2A),分别采用ESM与建立的QAMS测定醋延胡索样品中原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索乙素、延胡索甲素5种生物碱的含量,10批样品的HPLC见图2B,含量测定平均值结果见表7,采用SPSS软件t检验对含量测定结果进行分析比较,结果原阿片碱、盐酸巴马汀、盐酸小檗碱和延胡索甲素的ESM值和QAMS值两组方法的P>0.05,故原阿片碱、盐酸巴马汀、盐酸小檗碱和延胡索甲素的ESM值和QAMS值间无显著差异(P>0.05),表明建立的QAMS法准确可行。
表 7 醋延胡索中5种生物碱含量测定结果(mg/g)Table 7. Determination results of five alkaloids in vinegar Corydalis yanhusuo (mg/g)样品编号 延胡索乙素 原阿片碱 盐酸巴马汀 ESM QAMS ESM QAMS S1 0.6236±0.014 0.4736±0.017 0.4768±0.017 0.4407±0.011 0.4357±0.011 S2 0.3044±0.015 0.4307±0.008 0.4336±0.008 0.3093±0.006 0.3058±0.006 S3 0.5259±0.022 0.4193±0.009 0.4221±0.009 0.1696±0.009 0.1677±0.009 S4 0.3002±0.016 0.3986±0.007 0.4013±0.007 0.1991±0.010 0.1968±0.010 S5 0.8812±0.017 0.7471±0.036 0.7522±0.037 0.4519±0.016 0.4468±0.015 S6 0.7854±0.044 0.4780±0.023 0.4812±0.023 0.5284±0.018 0.5225±0.018 S7 0.7284±0.014 0.4736±0.041 0.4768±0.041 0.4407±0.017 0.4357±0.017 S8 0.5281±0.031 0.3641±0.004 0.3665±0.004 0.4499±0.021 0.4448±0.021 S9 0.5960±0.030 0.3199±0.051 0.3220±0.051 0.4334±0.073 0.4285±0.072 S10 0.4230±0.044 0.4285±0.022 0.4314±0.022 0.4318±0.010 0.4270±0.010 P 0.953 0.934 样品编号 盐酸小檗碱 延胡索甲素 ESM QAMS ESM QAMS S1 0.1907±0.014 0.1903±0.014 0.4777±0.018 0.4808±0.018 S2 0.1483±0.017 0.1481±0.017 0.3635±0.020 0.3659±0.021 S3 0.0909±0.003 0.0907±0.003 0.5344±0.012 0.5379±0.012 S4 0.1053±0.029 0.1051±0.029 0.4257±0.082 0.4286±0.083 S5 0.2036±0.038 0.2032±0.038 0.6272±0.011 0.6314±0.011 S6 0.2600±0.025 0.2596±0.025 0.6328±0.027 0.6370±0.027 S7 0.1907±0.028 0.1903±0.028 0.4777±0.014 0.4808±0.014 S8 0.2069±0.025 0.2066±0.025 0.4810±0.017 0.4842±0.017 S9 0.1663±0.022 0.1659±0.022 0.4816±0.020 0.4849±0.021 S10 0.1484±0.013 0.1481±0.013 0.3155±0.018 0.3176±0.018 P 0.989 0.944 3. 结论
本实验建立一测多评法(QAMS)用于测定醋延胡索中5种生物碱类成分的含量,考察了精密度、重复性、稳定性以及回收率,经考察精密度、重复性及稳定性的RSD值小于2%,平均回收率98.38%~101.28%之间,均符合要求。同时考察了不同仪器和不同色谱柱、不同体积流量、不同柱温下各成分间的相对校正因子及相对保留时间的变化,RSD值均小于3%,表明该方法具有良好的适应性且在不同的因素下均能行准确定位。本实验还对ESM法测得不同产地醋延胡索中的原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索乙素、延胡索甲素进行含量测定,ESM含量测定值和QAMS计算值利用SPSS软件进行t检验,结果表明2种方法含量测定的结果经t检验后无显著差异(P>0.05),说明建立的QAMS法结果准确、方法可行。采用QAMS法测定醋延胡索中各生物碱成分含量能极大地减少对照品使用数量,节约成本,增加检测便利性,因此该方法可应用于醋延胡索的含量测定,期待为醋延胡索的制剂加工、质量评价与临床应用提供依据。
-
表 1 延胡索样品来源信息
Table 1 Source information of Corydalis yanhusuo samples
样品编号 产地 批号 S1 河南唐河 210606 S2 河南信阳 Z2001008 S3 陕西汉中 C808210701 S4 陕西宝鸡 20220101 S5 浙江金华 211001 S6 浙江东阳 20221001 S7 安徽亳州 21120101 S8 广西玉林 211009 S9 湖北武汉 210202 S10 河北承德 200912 表 2 对照品的线性关系、检出限与定量限
Table 2 Linear relationships, LODs and LOQs of reference substance
生物碱 回归方程 线性范围
(μg/mL)r 检出限
(μg/mL)定量限
(μg/mL)原阿片碱 y=6176.1x+9964.4 3.84~76.80 0.9996 0.063 0.211 盐酸小檗碱 y=24608x+8570.6 0.96~19.20 0.9999 0.089 0.314 盐酸巴马汀 y=28475x+30653 2.50~50.00 0.9995 0.036 0.127 延胡索乙素 y=14864x+38433 4.82~96.40 0.9993 0.081 0.303 延胡索甲素 y=15476x+36195 4.01~80.20 0.9992 0.067 0.228 表 3 醋延胡索中4个成分的相对校正因子
Table 3 Relative correction factors of four components in vinegar Corydalis yanhusuo
进样量(μL) fa/s fb/s fc/s fd/s 1 0.415 1.905 1.639 1.041 2 0.405 1.906 1.596 1.043 5 0.406 1.850 1.551 1.056 8 0.408 1.847 1.568 1.048 10 0.398 1.815 1.522 1.062 20 0.396 1.865 1.549 1.045 平均值 0.405 1.865 1.571 1.049 RSD% 1.71 1.91 2.63 0.78 注:s为延胡索乙素,a~d为原阿片碱、盐酸巴马汀、盐酸小檗碱、延胡索甲素;表4、表6同。 表 4 不同因素对相对保留时间的影响
Table 4 Effects of different factors on relative retention times
因素 ra/s rb/s rc/s rd/s 仪器与
色谱柱Hitachi
ChromasterPromosil C18 0.645 0.734 0.753 1.122 Agilent C18 0.651 0.750 0.774 1.136 Diamonsil C18 0.648 0.760 0.778 1.112 Hitachi ELITE
LaChromPromosil C18 0.653 0.761 0.790 1.125 Agilent C18 0.671 0.754 0.778 1.126 Diamonsil C18 0.628 0.740 0.768 1.133 平均值 0.649 0.750 0.774 1.126 RSD(%) 2.14 1.45 1.60 0.76 流速 0.8 mL/min 0.648 0.752 0.764 1.125 1.0 mL/min 0.653 0.754 0.772 1.128 1.2 mL/min 0.667 0.740 0.780 1.119 平均值 0.656 0.749 0.772 1.124 RSD% 1.50 1.01 1.04 0.41 柱温 25 ℃ 0.653 0.754 0.769 1.129 30 ℃ 0.658 0.748 0.775 1.126 35 ℃ 0.655 0.752 0.781 1.123 平均值 0.655 0.751 0.775 1.126 RSD(%) 0.38 0.40 0.77 0.27 表 5 5种生物碱的精密度、稳定性重复性和回收率
Table 5 Precision, stability, repeatability and recovery of five alkaloids
生物碱 精密度 重复性 稳定性 回收率 RSD(%) RSD(%) RSD(%) 平均回收率
(%)RSD
(%)原阿片碱 0.92 0.66 1.08 98.38 1.52 盐酸小檗碱 0.90 0.86 1.29 101.28 1.37 盐酸巴马汀 0.58 1.02 0.73 98.32 1.46 延胡索乙素 0.89 1.44 0.68 99.28 0.87 延胡索甲素 0.82 1.32 0.89 98.36 0.86 表 6 不同因素对相对校正因子的影响
Table 6 Effects of different factors on relative correction factors
因素 fa/s fb/s fc/s fd/s 仪器与
色谱柱Hitachi
ChromasterPromosil C18 0.415 1.905 1.639 1.045 Agilent C18 0.419 1.983 1.674 1.037 Diamonsil C18 0.416 1.932 1.565 1.032 Hitachi ELITE
LaChromPromosil C18 0.409 1.915 1.565 1.044 Agilent C18 0.401 1.860 1.568 1.054 Diamonsil C18 0.404 1.873 1.473 1.032 平均值 0.411 1.911 1.581 1.041 RSD(%) 1.75 1.90 1.55 0.83 流速 0.8 mL/min 0.409 1.806 1.541 1.047 1.0 mL/min 0.408 1.828 1.573 1.044 1.2 mL/min 0.405 1.896 1.581 1.043 平均值 0.407 1.843 1.565 1.045 RSD% 0.51 2.55 1.35 0.20 柱温 25 ℃ 0.415 1.921 1.605 1.048 30 ℃ 0.408 1.928 1.573 1.038 35 ℃ 0.420 1.926 1.592 1.032 平均值 0.414 1.925 1.590 1.039 RSD(%) 1.45 0.19 1.01 0.78 表 7 醋延胡索中5种生物碱含量测定结果(mg/g)
Table 7 Determination results of five alkaloids in vinegar Corydalis yanhusuo (mg/g)
样品编号 延胡索乙素 原阿片碱 盐酸巴马汀 ESM QAMS ESM QAMS S1 0.6236±0.014 0.4736±0.017 0.4768±0.017 0.4407±0.011 0.4357±0.011 S2 0.3044±0.015 0.4307±0.008 0.4336±0.008 0.3093±0.006 0.3058±0.006 S3 0.5259±0.022 0.4193±0.009 0.4221±0.009 0.1696±0.009 0.1677±0.009 S4 0.3002±0.016 0.3986±0.007 0.4013±0.007 0.1991±0.010 0.1968±0.010 S5 0.8812±0.017 0.7471±0.036 0.7522±0.037 0.4519±0.016 0.4468±0.015 S6 0.7854±0.044 0.4780±0.023 0.4812±0.023 0.5284±0.018 0.5225±0.018 S7 0.7284±0.014 0.4736±0.041 0.4768±0.041 0.4407±0.017 0.4357±0.017 S8 0.5281±0.031 0.3641±0.004 0.3665±0.004 0.4499±0.021 0.4448±0.021 S9 0.5960±0.030 0.3199±0.051 0.3220±0.051 0.4334±0.073 0.4285±0.072 S10 0.4230±0.044 0.4285±0.022 0.4314±0.022 0.4318±0.010 0.4270±0.010 P 0.953 0.934 样品编号 盐酸小檗碱 延胡索甲素 ESM QAMS ESM QAMS S1 0.1907±0.014 0.1903±0.014 0.4777±0.018 0.4808±0.018 S2 0.1483±0.017 0.1481±0.017 0.3635±0.020 0.3659±0.021 S3 0.0909±0.003 0.0907±0.003 0.5344±0.012 0.5379±0.012 S4 0.1053±0.029 0.1051±0.029 0.4257±0.082 0.4286±0.083 S5 0.2036±0.038 0.2032±0.038 0.6272±0.011 0.6314±0.011 S6 0.2600±0.025 0.2596±0.025 0.6328±0.027 0.6370±0.027 S7 0.1907±0.028 0.1903±0.028 0.4777±0.014 0.4808±0.014 S8 0.2069±0.025 0.2066±0.025 0.4810±0.017 0.4842±0.017 S9 0.1663±0.022 0.1659±0.022 0.4816±0.020 0.4849±0.021 S10 0.1484±0.013 0.1481±0.013 0.3155±0.018 0.3176±0.018 P 0.989 0.944 -
[1] 赵国禄. 饮食调养治疗痛经[J]. 东方食疗与保健,2007(6):50−51 ZHAO G L. Treatment of dysmenorrhea by dietary recuperation[J]. Oriental Diet Therapy and Health Care,2007(6):50−51.
[2] 黄衍强, 袁栋. 癌痛食疗有良方[J]. 祝您健康,2006(3):33 HUANG Y Q, YUAN D. Food therapy for cancer pain[J]. For Your Health,2006(3):33.
[3] WU L Y, YANG Y, MAO Z J, et al. Processing and compatibility of Corydalis yanhusuo:Phytochemistry, pharmacology, pharmacokinetics, and safety[J]. Evidence-based Complementary and Alternative Medicine,2021,2021(31):1271953−1271961.
[4] 冯自立, 赵正栋, 刘建欣. 延胡索化学成分及药理活性研究进展[J]. 天然产物研究与开发,2018,30(11):2000−2008 FENG Z L, ZHAO Z D, LIU J X. Research progress on chemical components and pharmacological effects of Corydalis yanhusuo[J]. Natural Product Research and Development,2018,30(11):2000−2008.
[5] TIAN B, TIAN M, HUANG S M. Advances in phytochemical and modern pharmacologica research of Rhizoma Corydalis [J]. Pharmary Biology,2020,58(1):265−275. doi: 10.1080/13880209.2020.1741651
[6] 张铁军, 许浚, 韩彦琪, 等. 中药质量标志物(Q-marker)研究:延胡索质量评价及质量标准研究[J]. 中草药,2016,47(9):1458−1467 ZHANG T J, XU J, HAN Y Q, et al. Quality markers research on Chinese materia medica:Quality evaluation and quality standards of Corydalis rhizoma[J]. Chinese Traditional and Herbal Drugs,2016,47(9):1458−1467.
[7] WANG L H, LING B K, YANG C, et al. Identification and quantification, metabolism and pharmacokinetics, pharmacological qctivities, and botanical preparations of protopine:A review[J]. Molecules (Basel, Switzerland),2021,27(1):215. doi: 10.3390/molecules27010215
[8] YUAN H L, ZHAO Y L, QIN X J, et al. Diverse isoquinolines with anti-inflammatory and analgesic bioactivities from Hypecoum erectum[J]. Journal of Ethnopharmacology,2021,270:113811. doi: 10.1016/j.jep.2021.113811
[9] JIANG W N, JING X, LI M, et al. Corydaline and l-tetrahydropalmatine attenuate morphine-induced conditioned place preference and the changes in dopamine D2 and GluA1 AMPA receptor expression in rats[J]. European Journal of Pharmacology,2020,884:173397. doi: 10.1016/j.ejphar.2020.173397
[10] LEE T H, SON M, KIM S Y. Effects of corydaline from Corydalis tuber on gastric motor function in an animal model[J]. Biological & Pharmaceutical Bulletin,2010,33(6):958−962.
[11] 曾超, 莫婷婷, 陆梅元, 等. 黄连抗胃溃疡炎症的作用机制及其活性成分的实验研究[J]. 时珍国医国药,2020,31(7):1559−1562 doi: 10.3969/j.issn.1008-0805.2020.07.007 ZENG C, MO T T, LU M Y, et al. Experimental study on the mechanism of action of Coptis chinensis Franch against gastric ulcer inflammation and its active components[J]. Lishizhen Medicine and Materia Medica Research,2020,31(7):1559−1562. doi: 10.3969/j.issn.1008-0805.2020.07.007
[12] 帅丽华, 姜登钊, 刘怀, 等. 黄连成分与阿米卡星联合用药对多重耐药大肠埃希菌的体外活性研究[J]. 天津医药,2016,44(10):1259−1262 SHUAI L H, JIANG D Z, L H, et al. In vitro activity of amikacin combined with the ingredient of coptis chinensis against multiple drug resistance of Escherichia coli[J]. Tianjin Medical Journal,2016,44(10):1259−1262.
[13] 陈美琳, 李芝奇, 范琦琦, 等. 小檗碱药理作用及其相关作用机制研究进展[J]. 中草药,2022,53(18):5861−5872 CHEN M L, LI Z Q, FAN Q Q, et al. Research progress on pharmacological action and related mechanism of berberine[J]. Chinese Traditional and Herbal Drugs,2022,53(18):5861−5872.
[14] XIAO C W, LIU Y, WEI Q, et al. Inhibitory effects of berberine hydrochloride on trichophyton mentagrophytes and the underlying mechanisms[J]. Molecules,2019,24(4):742. doi: 10.3390/molecules24040742
[15] 赵丽沙, 董宇, 王娜妮, 等. 醋延胡索饮片及其颗粒剂的谱-效关系[J]. 中国临床药学杂志,2018,27(6):391−396 ZHAO L S, DONG Y, WANG N N, et al. Study on spectrum-effect relationship of Corydalis pieces and granules[J]. Chinese Jouranl of Clinical Pharmacy,2018,27(6), 391−396.
[16] WU F, WU M M, ZHONG C C, et al. Simultaneous qualitative and quantitative analysis of eight alkaloids in Corydalis decumbentis rhizoma (Xiatianwu) and Corydalis rhizoma ( Yanhusuo) by high-performance liquid chromatography and high-resolution mass spectrometry combined with chemometric methods[J]. Journal Separation Science,2022,45(15):2833−2844. doi: 10.1002/jssc.202200259
[17] 曹瑶, 李凯, 原军宁, 等. 延胡索不同生长时期和不同部位中8种生物碱含量动态比较[J]. 中药材,2021,44(1):41−46 CAO Y, LI K, YUAN J N, et al. Dynamic comparison of eight alkaloids content in different growth stages and different parts of Corydalis yanhusuo[J]. Journal of Chinese Medicinal Materials,2021,44(1):41−46.
[18] 王智民, 钱忠直, 张启伟, 等. 一测多评法建立的技术指南[J]. 中国中药杂志,2011,36(6):657−658 WANG Z M, QIAN Z Z, ZHANG Q W, et al. Technical guidelines for the establishment of quantitative analysis of multi-components by single marker[J]. China Journal of Chinese Materia,2011,36(6):657−658.
[19] 杜清, 陈志, 吴江, 等. 一测多评法同时测定斑花黄堇药材中4种生物碱成分[J]. 中草药,2021,52(19):6038−6044 DU Q, CHEN Z, WU J, et al. Simultaneous determination of four alkaloids in different original Corydalis conspersa by QAMS[J]. Chinese Traditional and Herbal Drugs,2021,52(19):6038−6044.
[20] 梁颖欣, 朱旦, 黄舒婷, 等. 一测多评法测定钩藤中7种生物碱类成分的含量[J]. 中药材,2019,42(8):1820−1823 LIANG Y X, ZHU D, HUANG S T, et al. Content determination of seven alkaloids in Uncaria rhynchophylla by QAMS[J]. Journal of Chinese Medicinal Materials,2019,42(8):1820−1823.
[21] 陈静, 王淑美, 孟江, 等. 一测多评法测定苦参中5种生物碱的含量[J]. 中国中药杂志,2013,38(9):1406−1410 CHEN J, WANG S M, MENG J, et al. Determination of five alkaloids in Sophora flavescens with quantitative analysis of multi-components by single marker[J]. China Journal of Chinese Materia Medica,2013,38(9):1406−1410.
[22] 徐鑫梅, 武鑫玥, 易欢, 等. 一测多评法测定藏药小檗皮中6种成分的含量[J]. 中国新药杂志,2020,29(24):2852−2858 XU X M, WU X Y, YI H, et al. Determination of 6 components in Tibetan medicine Berberis cortex with quantitative analysis of multi-components by single marker[J]. Chinese Journal of New Drugs,2020,29(24):2852−2858.
[23] 袁汉文, 吕梦颖, 罗江溢, 等. 基于特征图谱和一测多评法的黄柏质量控制研究[J]. 中草药,2022,53(17):5491−5496 YUAN H W, LÜ M Y, LUO J Y, et al. Quality control of Phellodendri chinensis cortex based on HPLC characteristic fingerprint and single standard to determine multi-components method[J]. Chinese Traditional and Herbal Drugs,2022,53(17):5491−5496.
[24] 任慧, 崔小敏, 胡静, 等. 一测多评法对金铃子散中来源于延胡索的5个生物碱成分含量的同时测定[J]. 西部中医药,2022,35(11):73−77 REN H, CUI X M, HU J, et al. Simultaneous determination of five alkaloids from Corydalis rhizomain jinlingzi powder by QAMS[J]. Western Journal of Traditional Chinese Medicine,2022,35(11):73−77.
[25] 刘瑞洁, 张雪, 叶晓霞, 等. 一测多评法测定元胡止痛系列制剂中5种成分的含量[J]. 中国医药工业杂志,2019,50(11):1318−1323 LIU R J, ZHANG X, YE X X, et al. Simultaneous determination of five components in Yuanhu zhitong series preparations by QAMS[J]. Chinese Journal of Pharmaceuticals,2019,50(11):1318−1323.
[26] 国家药典委员会. 中华人民共和国药典2020年版(四部)[S]. 北京:中国医药科技出版社, 2020:31 Chinese pharmacopoeia commission. Pharmacopoeia of the People's Republic of China 2020 (part IV)[S]. Beijing:China Medical Science Press, 2020:31.
[27] 国家药典委员会. 中华人民共和国药典2020年版(一部)[S]. 北京:中国医药科技出版社, 2020:145 Chinese pharmacopoeia commission. Pharmacopoeia of the People's Republic of China 2020 (part I)[S]. Beijing:China Medical Science Press, 2020:145.
[28] ZHANGY, LI Q, FENG Y, et al. Simultaneous determination of eight chemical components in angelicae sinensis radix and its herbal products by QAMS[J]. Journal of Analytical Methods in Chemistry, 2021.
[29] ZHANG J H, CHEN L X, QIU J N, et al. Simultaneous determination of six chromones in saposhnikoviae radix via quantitative analysis of multi-components by single marker[J]. Journal of Analytical Methods in Chemistry,2020,2020(22):1−13.
[30] DONG X , ZHENG F , LIU X, et al. Simultaneous quantitative analysis of Q-Marker with one single reference in Glycyrrhiza uralensis Fisch[J]. Journal of Chromatographic Science, 2020, 58(6):511−519.
-
期刊类型引用(1)
1. 刘梦文,沈静,阿依努尔·白克热,贺诗茹,肖辉,徐维盛. 一测多评法同时测定桑叶中9种绿原酸类和黄酮类成分. 食品工业科技. 2024(15): 295-303 .  本站查看
本站查看
其他类型引用(0)





 下载:
下载:
 下载:
下载:



