Analysis of the Effect of Drying Methods on Volatile Components of Toona sinensis Based on GC-IMS and GC-MS Combined with Chemometrics
-
摘要: 为研究干燥方式对香椿挥发性风味物质的影响,利用气相色谱-离子迁移谱技术(gaschromatography-ion mobility spectrometry,GC-IMS)和气相色谱-质谱联用技术(gas chromatography-mass spectrometry,GC-MS)、相对香气活性值(relative odor activity value,ROAV)对真空冷冻干燥、热泵干燥、热风干燥、微波真空干燥的香椿样品进行挥发性成分分析,并进一步结合化学计量方法主成分分析(principal component analysis,PCA)和偏最小二乘判别分析(partial least squares-discriminant analysis,PLS-DA),探究样品间挥发性成分的差异性。结果表明,通过GC-IMS检测到78个峰,鉴定出59种化合物。通过GC-MS鉴定出94种挥发性化合物,主要挥发性成分是硫化物、烯烃类和醛类。经过干燥后总挥发性化合物的含量显著降低。通过ROAV法确定了(E,Z)-二-1-丙烯基二硫化物、2-巯基-3,4-二甲基-2,3-二氢噻吩、正己醛、2-己烯醛、丁香酚等为香椿样品中关键香气化合物。PCA和PLS-DA结果表明,不同干燥方式的样品与新鲜样品有明显的分离,彼此之间也有明显的区别。鲜样和真空冷冻干燥样品为一组,其他3个干燥香椿样品为一组。根据变量投影重要性(variable importance in projection,VIP)得分共筛选出10种(VIP>1)标志挥发性化合物。干燥方式对香椿风味特性影响显著,真空冷冻干燥组与鲜样最为接近,考虑实际应用热泵干燥为香椿最适宜的脱水方式。本研究为热加工过程中风味品质控制提供一定的理论参考。
-
关键词:
- 香椿 /
- 干燥方式 /
- 气相色谱-离子迁移谱(GC-IMS) /
- 气相色谱-质谱联用技术(GC-MS) /
- 挥发性化合物
Abstract: To investigate the effect of drying methods on the volatile flavor substances of Toona sinensis, the volatile components of vacuum freeze-dried, heat pump-dried, hot air-dried, and microwave vacuum-dried Toona sinensis samples were analyzed by gas chromatography-ion mobility spectrometry (GC-IMS) and gas chromatography-mass spectrometry (GC-MS) coupled with relative odor activity values, and the differences of volatile components among samples were further explored by combining the stoichiometric principal component analysis and partial least square discriminant analysis. The results showed that 78 peaks were detected and 59 compounds were identified by GC-IMS. 94 kinds of volatile compounds were identified by GC-MS, and the main volatile components were sulfides, olefins and aldehydes. The content of total volatile compounds was significantly reduced after drying. The key aroma compounds in Toona sinensis samples were identified by ROAV method, such as (E,Z)-di-1-propenyldisulfide, 2-mercapto-3,4-dimethyl-2,3-dihydrothiophene, hexanal, 2-hexenal and eugenol. The PCA and PLS-DA results showed that the samples with different drying methods were not only clearly separated from the raw samples, but also significantly different from each other. The raw samples and vacuum freeze-dried samples were grouped, and the other three dried Toona sinensis samples were grouped. According to the variable importance in projection score, a total of 10 (VIP>1) labeled volatile compounds were selected. The drying method had significant effect on the flavor characteristics of Toona sinensis, and the vacuum freeze-dried group was the closest to the raw sample, while heat pump-drying was the most suitable dehydration method for Toona sinensis, considering the practical application. This study provides some theoretical references for flavor quality control in the thermal processing process. -
香椿(Toona sinensis (A. Juss.) Roem),又名香椿头、椿树,起源于中国,已有两千多年的栽培历史,分布于亚洲地区[1−2]。由于其独特的风味和较高的营养价值,香椿嫩芽是中国最受欢迎的木本蔬菜之一[3]。近年来,香椿芽已出口到许多不同的国家,如俄罗斯、韩国、日本和马来西亚[4]。香椿芽均价35元/kg,冬季温室栽培的新鲜香椿芽价格可高达100~200元/kg[5],其重要经济价值引起了人们的广泛关注。但香椿芽不能像其他蔬菜一样全年生产供应。一般来说,每年3月开始可以采摘香椿嫩芽食用,出芽两周左右,若不及时采收,就会发生纤维化、木质化,香气淡化甚至消失,不再适宜食用[6]。此外,新鲜香椿嫩芽含水量达85%~90%,极易腐败变质,风味散失,严重影响其商品价值,已成为困扰产业发展的瓶颈和亟待解决的关键问题。
干燥可以使果蔬重量减轻、体积缩小、食用方便、利于运输和长期保藏。香椿属于热敏性物料,干燥过程对其品质影响较大,故干燥是其加工的关键操作之一。常用的干燥方法有热风干燥、微波干燥、热泵干燥、真空冷冻干燥、红外干燥等。热风干燥是以热空气为传热介质,热交换的同时不断带走物料表面水分,具有操作简便、生产效率高、成本低廉等优势,但干燥时间较长。微波真空干燥技术是在真空条件下利用微波能进行物料干燥的组合干燥技术,微波穿透力强,使物料内、外同时升温形成整体加热,具有高效、低温、易控及环保等特点,但由于微波场的空间不均匀性导致其加热不均匀。热泵干燥是利用热泵从低温热源吸收热量的原理,因具有节能、高效、智能环保、有效地保持脱水蔬菜的品质等优势得到广泛应用[7−8]。真空冷冻干燥是将物料冻结到共晶点温度以下,在低压状态下通过升华除去物料中水分的一种干燥方法,能极大地保留原有的活性物质、色泽、风味、形态,但是干燥时间长、能耗大、设备较贵[7]。目前,关于香椿干燥的研究集中在干燥特性、干燥模型[9],不同干燥方式下的营养品质如维生素C、蛋白质、叶绿素,抗氧化活性,物理特性如复水性能、微观结构等方面[10−11]。风味是决定干燥食品可接受性的重要品质属性,挥发性风味物质的种类和含量受干燥加工方法影响较大。干燥过程中由于复杂的物理、化学变化导致一些挥发性组分损失或新组分生成,影响干制品风味品质[12]。Zhai等[13]通过气相色谱-嗅闻测定和气相色谱-质谱法对太阳能干燥香椿和真空干燥香椿进行分析,鉴定出了64种香气活性化合物,其中2-异丙基-3-甲氧基吡嗪、丁香酚和β-紫罗兰酮是影响两种干燥香椿总香气的重要香气物质。然而,目前关于不同干燥方式处理对香椿整体香气的影响尚未有系统研究。
挥发性香气化合物最常用的分析技术是气相色谱-质谱联用技术,已广泛应用于挥发性有机化合物的分离、鉴定和定量,具有高灵敏度和良好的重现性[14]。当与多元分析如PCA、PLS-DA相结合时,GC-MS可进一步用于不同样本的分类和鉴别,以及不同样本中潜在生物标志物的识别[15]。然而,将这两种技术联合应用于香椿挥发性香气特征(或潜在生物标志物)的鉴别,目前还很少有系统的研究。GC-IMS作为一种新型气相分离检测技术,兼具GC的高分离能力和IMS的高分辨、高灵敏度,另外样品几乎不需要任何前处理,在药物检测、食品风味分析和环境保护方面[16−18],已有广泛应用。
基于此,采用热风干燥、微波真空干燥、热泵干燥、真空冷冻干燥等技术对香椿进行干燥处理;同时采用GC-MS、GC-IMS及ROAV等检测分析技术,结合PCA、PLS-DA等化学计量学方法,对香椿风味化合物分析,研究不同干燥方式对香椿风味化合物的影响规律,旨在探究香椿芽较合理有效的干燥方式,减少干燥过程中风味物质损失,为采取有效技术手段对香椿加工过程进行风味调控、达到保香增香的目地提供基础理论依据,推进香椿产业向更深更广发展。
1. 材料与方法
1.1 材料与仪器
香椿 品种为红油香椿,于2022年4月3日采自河南省农业科学院现代农业研究开发基地香椿园,陆地头茬,选取新鲜、健壮、长度15 cm左右的香椿嫩芽,运至实验室,储存于4 ℃备用,测定其含水量质量分数为84.14%(WB,湿基);正构烷烃(C7~C30)、2-甲基-3-庚酮 标准品,Sigma-Aldrich;正酮C4~C9(标准品)、氯化钠(分析纯) 国药化学试剂北京有限公司;甲醇、二氯甲烷 色谱级,德国默克公司;液氮 郑州博越商贸股份有限公司。
BGZ-146型电热鼓风干燥箱 上海博迅医疗生物仪器股份有限公司;KL-2D-6KW型微波真空干燥设备 广州市凯棱工业用微波设备有限公司;VFD-2000A型真空冷冻干燥机 上海比朗仪器制造有限公司;AGHD-015ELC型空气能热泵烘干机 国信机械制造有限公司;8890A-5977B型气相色谱-质谱联用仪(GC-MS)、HP-5MS石英毛细管色谱(30 m×0.25 μm×0.25 μm)、50/30 μm二乙烯基苯/碳分子筛/聚二甲基硅氧烷(divinylbenzene/carboxen/polydimethylsiloxane,DVB/CAR/PDMS)固相微萃取头 美国安捷伦公司;FlavourSpec气相色谱离子迁移谱联用仪 德国G.A.S公司。
1.2 实验方法
1.2.1 干燥方法
香椿分为五组,每组500 g,第一组,新鲜香椿未经干燥处理(RAW),用液氮冷冻新鲜的香椿芽,用磨粉机粉碎,过60目筛,然后装在食品级聚乙烯塑料储存袋中,在−80 ℃下保存待用。在参阅相关方法[9−10,19]的基础上,经过预试验,确定香椿最终的干燥工艺条件,按表1的工艺和参数设置进行干燥处理,干燥至水分含量5%以下结束实验(图1)。将干燥后的样品粉碎,过60目筛,在−80 ℃冰箱保存直到分析。
表 1 4种干燥方式的工艺条件和参数Table 1. Process conditions and parameters of four drying methods干燥方式 干燥参数 干燥时间 真空冷冻干燥(VFD) 将香椿嫩芽均匀平铺放在真空冷冻干燥机的托盘中,冷冻干燥机参数:预冻温度设置为−50 ℃,预冻时间为
30 min,真空度为0.01 kPa,预冻完成后打开真空泵和真空计,当真空度低于50 Pa时,打开隔板控温,智能冷冻
干燥机自动升华干燥和解析干燥。35 h 热泵干燥(HPD) 将香椿嫩芽均匀放在铺纱布的筛网上,然后放入空气能热泵烘干机中,设定干燥温度为45 ℃,湿度为10%,进行干燥。 10 h 热风干燥(HAD) 将香椿嫩芽均匀放在电热鼓风干燥箱中,设定温度为55 ℃,进行干燥。 7 h 微波真空干燥(MVD) 将香椿嫩芽均匀放入微波真空干燥机的托盘中,设置功率为3000 W,真空度−40 kPa条件下进行干燥。 15 min 1.2.2 气相色谱-离子迁移色谱(GC-IMS)分析
参考张乐等[20]的方法,精确称取0.500 g香椿样品于20 mL顶空瓶中,40 ℃加热孵化10 min,孵化转速250 r/min;顶空进样针温度80 ℃;进样体积200 μL,不分流模式;载气:高纯氮气(纯度≥99.999%)。GC条件:色谱柱为MXT-5柱(15 m×0.53 mm,0.53 μm);色谱柱温度60 ℃;载气:高纯氮气(纯度≥99.999%);载气流速程序:初始2.0 mL/min,保持2 min,在2~10 min线性增至5.0 mL/min,在10~20 min线性增至50.0 mL/min,在20~30 min线性增至100.0 mL/min。IMS条件:离子源为氘(6.5 keV);正离子模式;漂移管长度9.8 cm;管内线性电压500 V/cm;漂移管温度45 ℃;漂移气流速150 mL/min(氮气纯度≥99.999%)。
使用正酮C4~C9作为外标计算挥发性化合物的保留指数(retention index,RI),采用GC-IMS Library Search软件内置的2014NIST数据库和IMS数据库对挥发性成分定性分析。
1.2.3 气相色谱-质谱(GC-MS)分析
1.2.3.1 GC-MS测定方法
参照Zhang等[21]方法采用固相微萃取对香椿挥发性成分进行提取和定量。精确称1.000 g样品和0.2 g NaCl置于20 mL顶空瓶中,加入5 μL 2-甲基-3-庚酮内标(浓度为248 mg/L甲醇溶液),同时密封小瓶。将小瓶置于恒温水浴中40 ℃下平衡15 min,然后插入萃取头萃取30 min后取出,于GC-MS进样口解吸5 min,同时开始采集保留时间和色谱峰强度等相关数据。
GC条件为:载气为氦气(纯度99.99%),恒定流速为1.0 mL/min。前进样温度250 ℃,溶剂延迟3 min。程序升温:初始温度40 ℃,保持3 min,以2 ℃/min的速度上升到70 ℃,保持2 min,以5 ℃/min的速度上升到150 ℃,保持2 min;以8 ℃/min的速率升至230 ℃,保持5 min。MS条件:传输线温度230 ℃,电离方式为电子电离(EI),离子阱温度230 ℃,扫描方式为全扫描,范围m/z 43~800。
1.2.3.2 香气化合物的定性与定量分析
采用NIST14数据库以及保留指数(retention index,RI)对香椿中挥发性化合物进行鉴定。保留指数:在相同GC-MS检测条件下对正构烷烃标准品(C7~C30)分析,根据各正构烷烃的保留时间计算相应的保留指数,计算如公式(1)所示:
RI=100×(n+tx−tntn+1−tn) (1) 式中:tx是化合物x的保留时间;tn和tn+1分别是碳原子数为n和n+1的正构烷烃保留时间(tn<tx<tn+1)。
以2-甲基-3-庚酮为内标,根据各化合物峰面积与内标进行比较来计算每种VOC的浓度,计算如公式(2)所示:
C=Ax×C0×VA0×m (2) 式中:C是未知化合物含量,µg/g;Ax是未知化合物的峰面积,mAu·s;A0是内标物峰面积mAu·s;C0是加入内标物的质量浓度,µg/µL;V是内标物的体积,µL;m是样品质量,g。
1.2.3.3 ROAV计算
化合物浓度与阈值(水中)的比值即为ROAV值,ROAV>1时,该香气化合物对香椿香气的贡献和影响较大,ROAV<1,该化合物对总体香气无实质性贡献。计算如公式(3)所示:
ROAVi=CiOTi (3) 式中:Ci为任一组分的质量浓度μg/kg;OTi为任一组分在水中的香气阈值μg/kg。
1.3 数据处理
采用SPSS 27软件对实验数据进行方差分析(P<0.05)。GC-IMS分析结果采用仪器自带的LAV(Laboratory Analytical Viewer)软件的Gallery插件程序构建挥发性成分的指纹图谱;Dynamic PCA plug-ins插件程序作PCA分析;GC-MS分析结果在MetaboAnalyst网站上进行PLS-DA;使用Origin 8.5软件进行绘图。
2. 结果与分析
2.1 香椿挥发性有机化合物GC-IMS分析
利用GC-IMS内置数据库对5个香椿样品中的挥发性化合物进行分析,共检测到78个峰,其中鉴定出了59个化合物,如表2所示。部分化合物浓度高会产生二聚体、三聚体,与单体具有相似的保留时间,不同的漂移时间[22](其中二聚体、三聚体也作为一个物质列于表中)包括12个醛类、13个醇类、7个酮类、1个含硫类和7个酸类、4个烯类、9个酯类以及主要由呋喃和吡嗪组成的6个其他类等59个化合物。
表 2 香椿样品中挥发性有机物的GC-IMS鉴定结果Table 2. Identification of volatile organic compounds in T. sinensis samples by GC-IMS序号 中文名称 英文名称 CAS 分子式 分子量 保留指数 保留时间(s) 迁移时间(ms) 1 正丙醇 1-Propanol 71-23-8 C3H8O 60.1 547.2 106.890 1.114 2 2-甲基丙醇-D 2-Methylpropanol-D 78-83-1 C4H10O 74.1 640.9 154.350 1.363 3 2-甲基丙醇-M 2-Methylpropanol-M 78-83-1 C4H10O 74.1 641.9 154.875 1.172 4 1-丁醇 1-Butanol 71-36-3 C4H10O 74.1 655 162.540 1.181 5 3-甲基-2-丁醇 3-Bethyl-2-butanol 598-75-4 C5H12O 88.1 695.4 190.365 1.232 6 1,2-丙二醇 1,2-Propanediol 57-55-6 C3H8O2 76.1 737.9 227.745 1.27 7 3-甲基-3-丁烯醇 3-Methyl-3-butenol 763-32-6 C5H10O 86.1 759.6 248.220 1.296 8 2-乙基己醇 2-Ethylhexanol 104-76-7 C8H18O 130.2 1042.7 698.985 1.42 9 α-苯乙醇 α-Phenylethanol 98-85-1 C8H10O 122.2 1055 726.495 1.558 10 呋喃醇 Furaneol 3658-77-3 C6H8O3 128.1 1055.6 727.755 1.206 11 (-)-龙脑醇 (-)-Borneol 464-45-9 C10H18O 154.3 1153.6 947.100 1.212 12 苯乙醇 Benzeneethanol 1960/12/8 C8H10O 122.2 1155.4 950.985 1.648 13 龙脑醇 Borneol 507-70-0 C10H18O 154.3 1166.8 976.605 1.218 14 二丙基硫醚 Dipropyl sulfide 111-47-7 C6H14S 118.2 873.1 359.310 1.161 15 丁醛-D Butanal-D 123-72-8 C4H8O 72.1 580.9 123.585 1.283 16 丁醛-M Butanal-M 123-72-8 C4H8O 72.1 581.1 123.690 1.115 17 2-甲基丁醛 2-Methylbutanal 96-17-3 C5H10O 86.1 670.7 172.410 1.398 18 戊醛-M Pentanal-M 110-62-3 C5H10O 86.1 699.9 193.935 1.19 19 乙缩醛 Acetal 105-57-7 C6H14O2 118.2 725.8 216.510 1.039 20 (E)-2-戊烯醛-D (E)-2-Pentenal-D 1576-87-0 C5H8O 84.1 750.3 239.40 1.351 21 (E)-2-戊烯醛-M (E)-2-Pentenal-M 1576-87-0 C5H8O 84.1 764.1 252.420 1.105 22 己醛 Hexanal 66-25-1 C6H12O 100.2 824.8 307.335 1.563 23 庚醛 Heptanal 111-71-7 C7H14O 114.2 949.5 490.875 1.337 24 5-甲基糠醛-D 5-Methylfurfural-D 620-02-0 C6H6O2 110.1 964.2 522.480 1.476 25 5-甲基糠醛-M 5-Methylfurfural-M 620-02-0 C6H6O2 110.1 972.7 541.170 1.123 26 (E)-2-壬烯醛 (E)-2-Nonenal 18829-56-6 C9H16O 140.2 1155.9 952.245 1.42 27 乙酸-M Acetic acid-M 64-19-7 C2H4O2 60.1 590.3 128.205 1.042 28 乙酸-D Acetic acid-D 64-19-7 C2H4O2 60.1 596.4 131.250 1.151 29 丙酸-M Propanoic acid-M 153474-35-2 C3H6O2 74.1 656.8 163.590 1.264 30 丙酸-D Propionic acid-D 153474-35-2 C3H6O2 74.1 699.4 193.515 1.273 31 丁酸 Butanoic acid 107-92-6 C4H8O2 88.1 811.7 295.365 1.366 32 异戊酸 Isovaleric acid 503-74-2 C5H10O2 102.1 872.1 357.945 1.499 33 己酸 Hexanoic acid 142-62-1 C6H12O2 116.2 989.8 579.600 1.295 34 丁酮-M Butanone-M 78-93-3 C4H8O 72.1 606.6 136.290 1.246 35 丁酮-D Butanone-D 78-93-3 C4H8O 72.1 613 139.545 1.062 36 羟基丙酮 Hydroxyacetone 116-09-6 C3H6O2 74.1 631.5 149.205 1.234 37 2,3-戊二酮 2,3-Pentanedione 600-14-6 C5H8O2 100.1 688.3 184.800 1.311 38 3-戊酮 3-Pentanone 96-22-0 C5H10O 86.1 690.2 186.270 1.346 39 3-羟基-2-丁酮-D 3-Hydroxy-2-butanone-D 513-86-0 C4H8O2 88.1 729.1 219.555 1.332 40 3-羟基-2-丁酮M 3-Hydroxy-2-butanone-M 513-86-0 C4H8O2 88.1 733.1 223.230 1.061 41 乙酸乙酯-D Ethyl acetate-D 141-78-6 C4H8O2 88.1 616.7 141.435 1.334 42 乙酸丙酯-M Propyl acetate-M 109-60-4 C5H10O2 102.1 714.9 206.745 1.478 43 2-甲基丙酸乙酯 Ethyl-2-methylpropanoate 97-62-1 C6H12O2 116.2 734.1 224.175 1.198 44 γ-丁内酯 γ-Butyrolactone 96-48-0 C4H6O2 86.1 925.7 442.995 1.304 45 水杨酸甲酯 Methyl salicylate 119-36-8 C8H8O3 152.1 1201.3 1053.675 1.197 46 乙酸丙酯-T Propyl acetate-T 109-60-4 C5H10O2 102.1 715.3 207.060 1.166 47 乙酸乙酯-M Ethyl acetate-M 141-78-6 C4H8O2 88.1 623.4 144.900 1.097 48 乙酸丙酯-D Propyl acetate-D 109-60-4 C5H10O2 102.1 678.1 177.450 1.164 49 乙酸异丙酯 Isopropyl acetate 108-21-4 C5H10O2 102.1 665.5 169.050 1.167 50 苯乙烯 Styrene 100-42-5 C8H8 104.2 898 394.695 1.518 51 α-水芹烯 α-Phellandrene 99-83-2 C10H16 136.2 989.1 578.130 1.219 52 柠檬烯 Limonene 138-86-3 C10H16 136.2 1030.6 671.790 1.219 53 β-罗勒烯 β-Ocimene 13877-91-3 C10H16 136.2 1045.8 705.810 1.219 54 戊烷-D Pentanal-D 110-62-3 C5H10O 86.1 500.9 191.520 1.422 55 3-丁烯腈 3-Butenenitrile 109-75-1 C4H5N 67.1 631.7 149.310 1.127 56 2,5-二甲基呋喃 2,5-Dimethylfuran 625-86-5 C6H8O 96.1 699.1 193.305 1.356 57 2-乙酰吡嗪 2-Acetylpyrazine 22047-25-2 C6H6N2O 122.1 1022.1 652.680 1.148 58 2-乙基呋喃 2-Ethylfuran 3208-16-0 C6H8O 96.1 725.7 216.405 1.299 59 2,4-二氯苯酚 2,4-Dichlorophenol 120-83-2 C6H4Cl2O 163.0 1154.7 949.410 1.181 2.2 香椿挥发性有机化合物GC-IMS指纹图谱分析
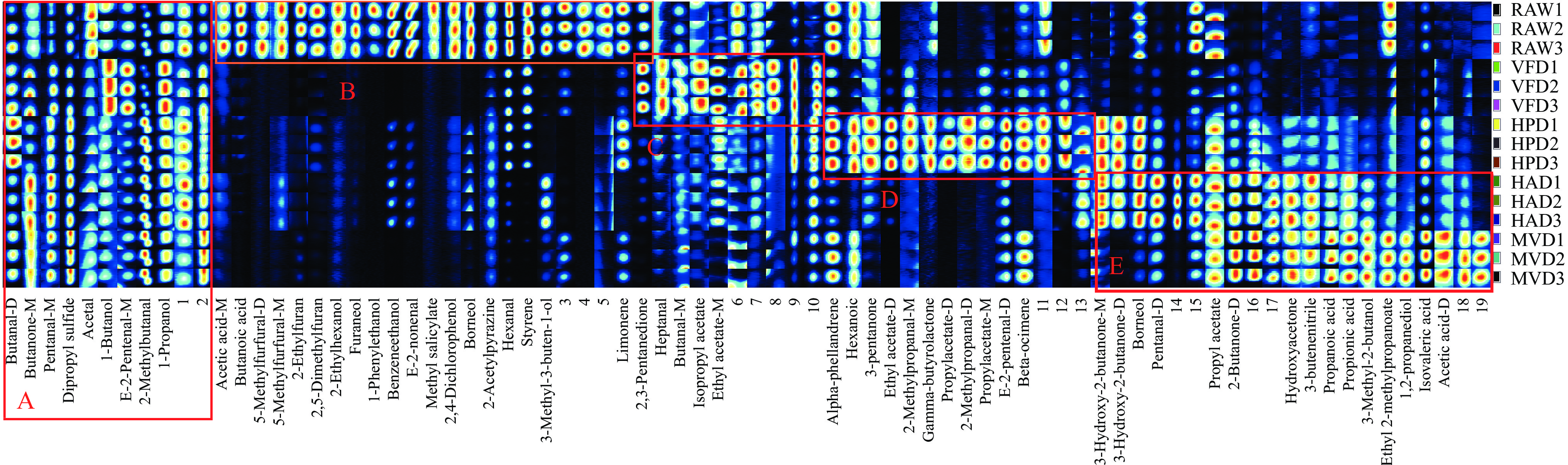
为更直观且定量地比较不同干燥方式下香椿样品中的挥发性成分差异,采用GalleryPlot插件生成香椿挥发性化合物的指纹图谱,如图2所示。斑点越亮表示化合物的浓度越高,未确定性的物质以阿拉伯数字编号。A框为所有样品共有挥发性物质的特征峰区域,有11种化合物,其中定性9种,主要为醛类化合物,包括丁醛-D、戊醛-M、乙缩醛、(E)-2-戊烯醛-M、2-甲基丁醛,含硫化合物二丙基硫醚,以及丁酮-M、正丙醇等。醛类化合物挥发性强,浓度高且阈值较低,呈现脂香、果香、叶香、清香等[21],是香椿中重要的风味成分。B框为鲜样中信号强度高于干燥处理组的物质,主要为醛类、醇类和其他类,如5-甲基糠醛、己醛、2-乙基己醇、苯乙醇、龙脑醇、呋喃醇、2-乙基呋喃、2,5-二甲基呋喃、2-乙酰吡嗪等物质。C框为真空冷冻干燥样品信号强度显著高于其他地区的物质,如乙酸异丙酯、乙酸乙酯、庚醛、丁醛等。D框为热泵干燥样品信号强度较高的物质有α-水芹烯、β-罗勒烯、3-戊酮、乙酸乙酯、乙酸丙酯、γ-丁内酯等。E框为热风和微波真空干燥样品信号强度较高的物质有3-羟基-2-丁酮-M/D、2-丁酮-D、丙酸-M/D、戊醛-D、异戊酸、乙酸-D、乙酸丙酯-M、2-甲基丙酸乙酯等物质。
2.3 香椿GC-IMS挥发性成分主成分分析(PCA)
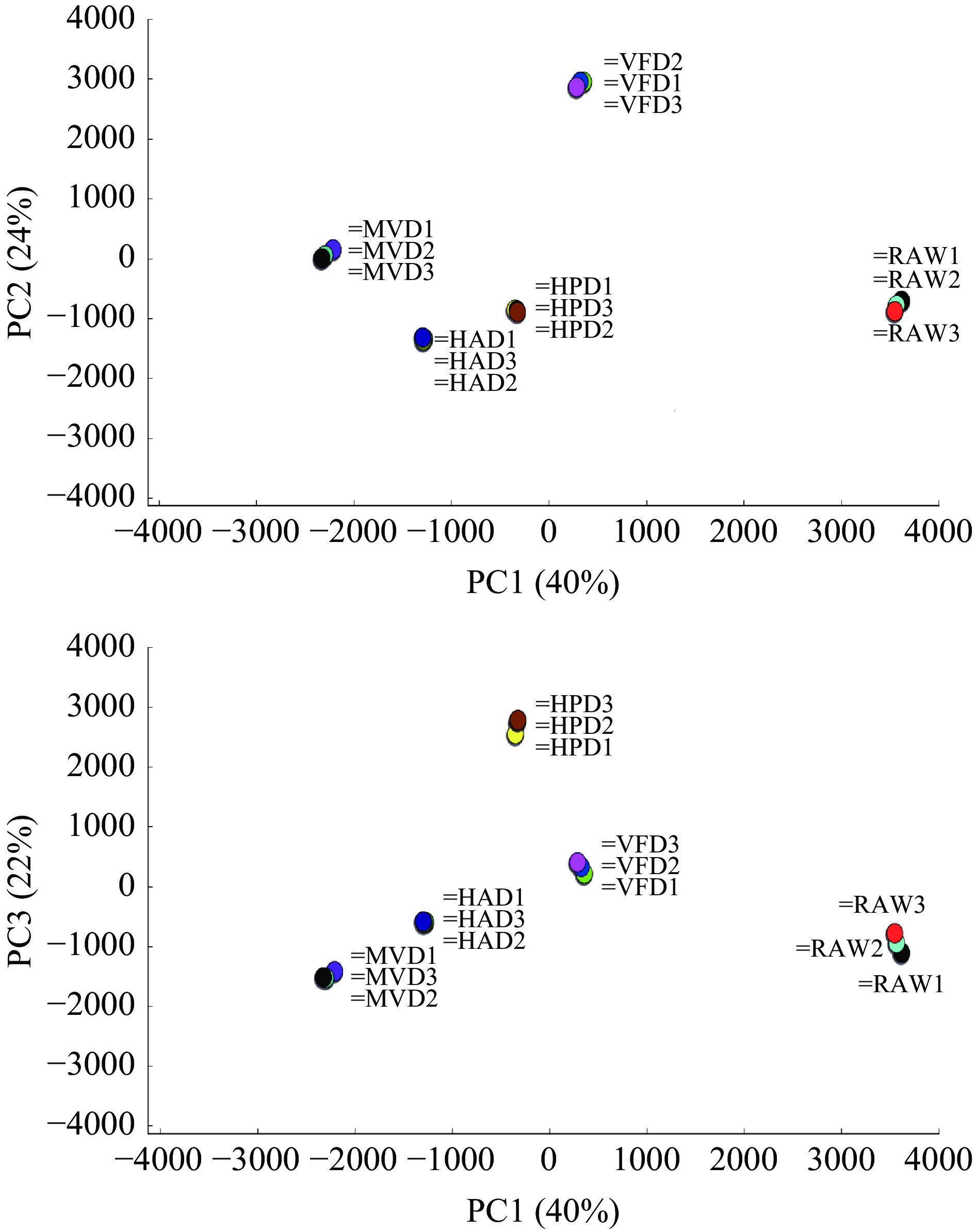
PCA是一种多变量数据分析工具,用于分析带有定量变量的多维数据集[23]。可以直观地显示样品之间的差异,样本的距离越大,说明差异越明显。使用Dynamic PCA插件对不同干燥处理的香椿挥发性物质(信号峰体积)进行PCA和数据可视化处理,如图3所示。PC1、PC2、PC3的方差贡献率分别为40%、24%和22%,各样品间均有一定的距离,根据PC1分值可以很好地把5个香椿样品分为2组,鲜样和真空冷冻干燥样品为一组,表明它们的挥发性化合物比较相似,其他3个干燥香椿样品为一组。
2.4 香椿挥发性成分GC-MS分析
不同干燥方式香椿挥发性物质的GC-MS结果见表3,在鲜样和经过热风干燥、微波真空干燥、热泵干燥、真空冷冻干燥的香椿中共鉴定出94种挥发性化合物,主要为C链介于C6~C18之间的化合物。
表 3 不同干燥方式下香椿香气成分GC-MS分析结果Table 3. GC-MS analysis results of volatile compounds of T. sinensis under different drying methods保留时间
(min)化合物 分子式 LRI RAW VFD HPD HAD MVD 定性方法 含硫 1.464 二甲基硫醚 C2H6S − − 0.213±0 0.564±0.038 0.576±0.04 MS,RI 2.841 甲基-环硫乙烷 C3H6S 681/606 0.227±0.086 1.918±0.971 1.979±0.076 0.801±0.086 0.696±0.091 MS 5.440 2,3-二氢-5-甲基-噻吩 C5H8S 791 0.173±0.072 − − − − MS 10.571 2,5-二甲基-噻吩 C6H8S 904/905 9.541±0.893 0.888±0.068 0.908±0.018 0.857±0.064 0.163±0.011 MS,RI 11.412 1,1'-硫代双-1-丙烯 C6H10S 917/904 0.136±0.021 − − − − MS,RI 13.562 1-(乙硫基)-2-甲基-1-丙烯 C6H12S 952 0.061±0 − 0.042±0.012 0.098±0.023 0.058±0.006 MS 16.493 顺式-2-乙基-3-甲基噻吩 C7H14S 998 0.108±0.08 − − − − MS 24.419 (E,Z)-二-1-丙烯基二硫化物 C6H10S2 1116/1124 12.468±1.222 0.459±0.098 0.411±0.059 1.19±0.047 0.129±0.058 MS,RI 24.776 3,4-二甲基-噻吩 C6H8S 904/908 5.969±0.821 0.398±0.036 0.428±0.033 0.634±0.046 0.086±0.052 MS,RI 26.296 (Z)丙-1-烯-1-基-丙二酸酯 C6H10S2 1162/1159 1.09±0.045 − − − − MS,RI 26.713 2-巯基-3,4-二甲基-2,3-二氢噻吩 C6H10S2 1172/1149 10.733±1.127 0.437±0.082 0.4±0.096 0.972±0.083 0.143±0.064 MS,RI 27.29 3,4-二甲基噻吩-2-硫醇 C6H8S2 1184/1193 0.718±0.103 − 0.03±0.001 − − MS,RI 27.418 1-(2-噻吩基)-1-丁酮 C8H10OS 1187 0.549±0.083 − − − − MS 32.591 (E,E)-二-1-丙烯基三硫化物 C6H10S3 1341/1348 1.615±0.336 − − − − MS,RI 39.948 1-(1-(丙-1-烯-1-基硫代)丙基)-2-
丙基二硫化物C9H18S3 1599/1592 0.249±0.129 − − − − MS,RI 41.512 (E)-1-丙烯基3,4-二甲基-2-
噻吩基二硫化物C9H12S3 1671/1671 0.48±0.034 − − − − MS,RI 43.016 薄荷硫化物 C15H24S 1749/1743 − 0.13±0.046 0.118±0.041 0.05±0.001 − MS,RI 醇类 4.871 (Z)-2-戊烯-1-醇 C5H10O 769/769 0.058±0.011 0.233±0.071 0.024±0.008 − − MS,RI 8.193 (Z)-3-己烯-1-醇 C6H12O 852/851 − 0.373±0.069 0.021±0.004 − − MS,RI 23.468 芳樟醇 C10H18O 1100/1099 − 0.072±0.033 − − − MS,RI 41.028 τ-杜松醇 C15H26O 1648/1649 − − 0.04±0.009 − − MS,RI 醛类 2.45 3-甲基丁醛 C5H10O 647/646 − − − 0.363±0.059 0.279±0.027 MS,RI 2.569 2-甲基丁醛 C5H10O 657/656 − − − 0.233±0.039 0.181±0.008 MS,RI 4.030 2-甲基-2-丁烯醛 C5H8O 734/737 − − 0.083±0.011 0.046±0.011 0.096±0.009 MS,RI 5.729 正己醛 C6H12O 801/800 4.918±0.308 1.611±0.041 0.224±0.049 0.06±0.008 − MS,RI 7.938 2-己烯醛 C6H10O 849/848 5.811±0.291 3.54±0.197 0.332±0.072 0.041±0.009 − MS,RI 13.817 苯甲醛 C7H6O 956/956 0.144±0.073 0.068±0 0.029±0 0.056±0.011 − MS,RI 19.492 苯乙醛 C8H8O 1042/1042 − − 0.033±0.005 0.057±0.013 − MS,RI 23.731 壬醛 C9H18O 1106/1105 0.107±0.014 0.101±0.044 0.04±0.01 0.035±0.004 − MS,RI 28.7 β-环柠檬醛 C10H16O 1220/1220 0.181±0 − − − − MS,RI 29.236 间苯二甲醛 C8H6O2 1236 0.122±0.031 − − − − MS 42.633 (Z,E)-2,6-金合欢醛 C15H24O 1727/1727 0.117±0.013 − − − − MS,RI 酮类 27.673 壬-3,5-二烯-2-酮 C9H14O 1193 0.197±0.075 − − − − MS 34.384 cis-茉莉酮 C11H16O 1400/1400 0.151±0.044 − − − − MS,RI 烯类 12.143 α-蒎烯 C10H16 929/928 0.693±0.059 0.094±0.022 0.074±0.035 − 0.073±0.024 MS,RI 18.319 D-柠檬烯 C10H16 1025 0.093±0 − − − − MS 32.609 δ-榄香烯 C15H24 1339/1339 − − 0.175±0.043 n.d. 0.137±0.024 MS,RI 33.492 (+)-环苜蓿烯 C15H24 1370/1368 0.1±0.01 − − − − MS,RI 33.602 依兰烯 C15H24 1374/1374 0.213±0 0.059±0 0.085±0.026 0.05±0.012 0.073±0.007 MS,RI 33.730 古巴烯 C15H24 1378/1378 − 0.078±0.048 0.219±0.05 0.288±0.035 0.464±0.112 MS,RI 33.730 α-荜澄茄油烯 C15H24 1378/1380 0.983±0.082 0.082±0 0.111±0.028 0.153±0.015 0.107±0.019 MS,RI 33.866 β-人参烯 C15H24 1383/1383 0.25±0.02 − − − − MS,RI 34.002 β-波旁烯 C15H24 1387/1386 0.26±0.02 − 0.036±0.013 − − MS,RI 34.205 (-)-β-榄香烯 C15H24 1394/1394 0.077±0.001 0.103±0 0.141±0.037 0.291±0.045 0.507±0.019 MS,RI 34.630 (Z)-β-石竹烯 C15H24 1409/1408 5.218±0.034 − 0.064±0.004 0.129±0.016 0.091±0.005 MS,RI 34.970 反式石竹烯 C15H24 1422/1418 1.734±0.794 0.496±0. 031 1.51±0.035 1.733±0.201 1.465±0.316 MS,RI 35.200 β-古尔均烯 C15H24 1431/1430 − − 0.098±0.008 0.085±0.01 0.106±0.011 MS,RI 35.378 α-香柠檬素 C15H24 1437/1438 − − − 0.059±0.005 0.074±0.006 MS,RI 35.471 α-愈创木烯 C15H24 1441/1439 0.524±0.012 0.061±0 0.183±0.068 0.162±0.023 − MS,RI 35.599 瓜亚-6,9-二烯 C15H24 1445/1450 0.65±0.082 − 0.124±0.035 0.157±0.021 0.102±0.018 MS,RI 35.676 迪纳-3,5-二烯 C15H24 1448/1458 − − − − 0.052±0.006 MS,RI 35.760 α-榄香烯 C15H24 1451/1469 0.66±0.041 − − − 0.179±0 MS,RI 35.829 表地带烯 C15H24 1476/1495 − − 0.129±0.038 − − MS,RI 35.888 葎草烯 C15H24 1456/1456 1.272±0.192 0.129±0.092 0.386±0.081 0.402±0.061 0.497±0.019 MS,RI 36.074 香橙烯 C15H24 1463/1440 0.224±0.018 0.09±0 0.096±0.028 0.168±0.023 0.132±0.025 MS,RI 36.083 带状烯 C15H24 1463 − 0.082±0 0.118±0.025 0.105±0.009 0.212±0.044 MS 36.329 桉叶三烯 C15H22 1472/1477 0.105±0 − − − − MS,RI 36.457 香附子烯 C15H24 1477/1415 0.207±0.007 − − − − MS,RI 36.483 (-)-g-杜松烯 C15H24 1519/1485 − 0.271±0.164 0.97±0.048 0.647±0.008 1.102±0.083 MS,RI 36.533 γ-姜黄烯 C15H24 1480/1479 0.229±0.023 − − − − MS,RI 36.644 大根香叶烯 C15H24 1484/1480 − 0.102±0.031 0.523±0.094 0.399±0.063 0.788±0.062 MS,RI 36.652 α-姜黄烯 C15H22 1484/1484 0.141±0.004 − − − − MS,RI 36.797 β-蛇床烯 C15H24 1490/1489 0.99±0.06 0.42±0.022 1.099±0.19 1.041±0.153 1.335±0.077 MS,RI 37.051 γ-芹子烯 C15H24 1499/1509 0.897±0.096 0.55±0.011 1.377±0.032 1.369±0.021 1.858±0.024 MS,RI 37.366 α-金合欢烯 C15H24 1510/1509 − 0.177±0.05 0.69±0.016 0.816±0.012 1.364±0.089 MS,RI 37.502 β-姜黄烯 C15H24 1515/1512 0.115±0.014 − 0.052±0.012 0.075±0.011 0.068±0.009 MS,RI 37.612 γ-杜松烯 C15H24 1519/1513 0.12±0.013 0.134±0.073 0.546±0.087 0.306±0.051 0.642±0.069 MS,RI 37.731 (-)-α-人参烯 C15H24 1523/1527 − 0.066±0 0.101±0.019 0.104±0.017 0.138±0.018 MS,RI 37.892 菖蒲烯 C15H22 1528/1529 0.426±0.019 0.483±0.024 − − − MS,RI 37.893 d-杜松烯 C15H24 1528/1528 − − 1.346±0.032 0.944±0.109 1.694±0.078 MS,RI 38.182 荜澄茄油烯 C15H24 1538/1537 − 0.067±0.019 0.117±0.021 0.104±0.013 0.183±0.027 MS,RI 38.284 异喇叭烯 C15H24 1446/1373 − − 0.079±0.013 0.068±0.013 − MS,RI 38.343 α-杜松烯 C15H24 1544/1544 − 0.085±0.037 0.328±0.047 0.185±0.03 0.378±0.043 MS,RI 38.351 β-马榄烯 C15H24 1494/1414 0.094±0.021 0.069±0.019 0.242±0.041 0.08±0.014 0.16±0.009 MS,RI 38.513 α-白菖考烯 C15H20 1550/1542 0.227±0.052 0.32±0.042 0.62±0.015 0.5±0.053 0.599±0.079 MS,RI 38.938 大根香叶烯 C15H24 1565/1562 − − 0.088±0.027 0.089±0.015 0.072±0.009 MS,RI 39.107 β-白菖考烯 C15H20 1570/1563 0.053±0 − 0.083±0.021 0.039±0.006 0.053±0.007 MS,RI 40.493 α-卡拉曼烯 C15H22 1624/1512 − − 0.054±0.015 − − MS,RI 40.611 9-甲基S-八氢菲 C15H20 1629 − 0.064±0.025 0.107±0.035 0.091±0.007 0.103±0.012 MS 41.342 (+)-戊烯 C15H24 1663/1500 − 0.049±0 0.084±0.002 − 0.053±0.005 MS,RI 41.758 卡达烯 C15H18 1682/1679 0.218±0.019 0.123±0.041 0.098±0.003 0.143±0.015 0.163±0.006 MS,RI 43.695 1,4-二甲基-7-(1-甲基乙基)-
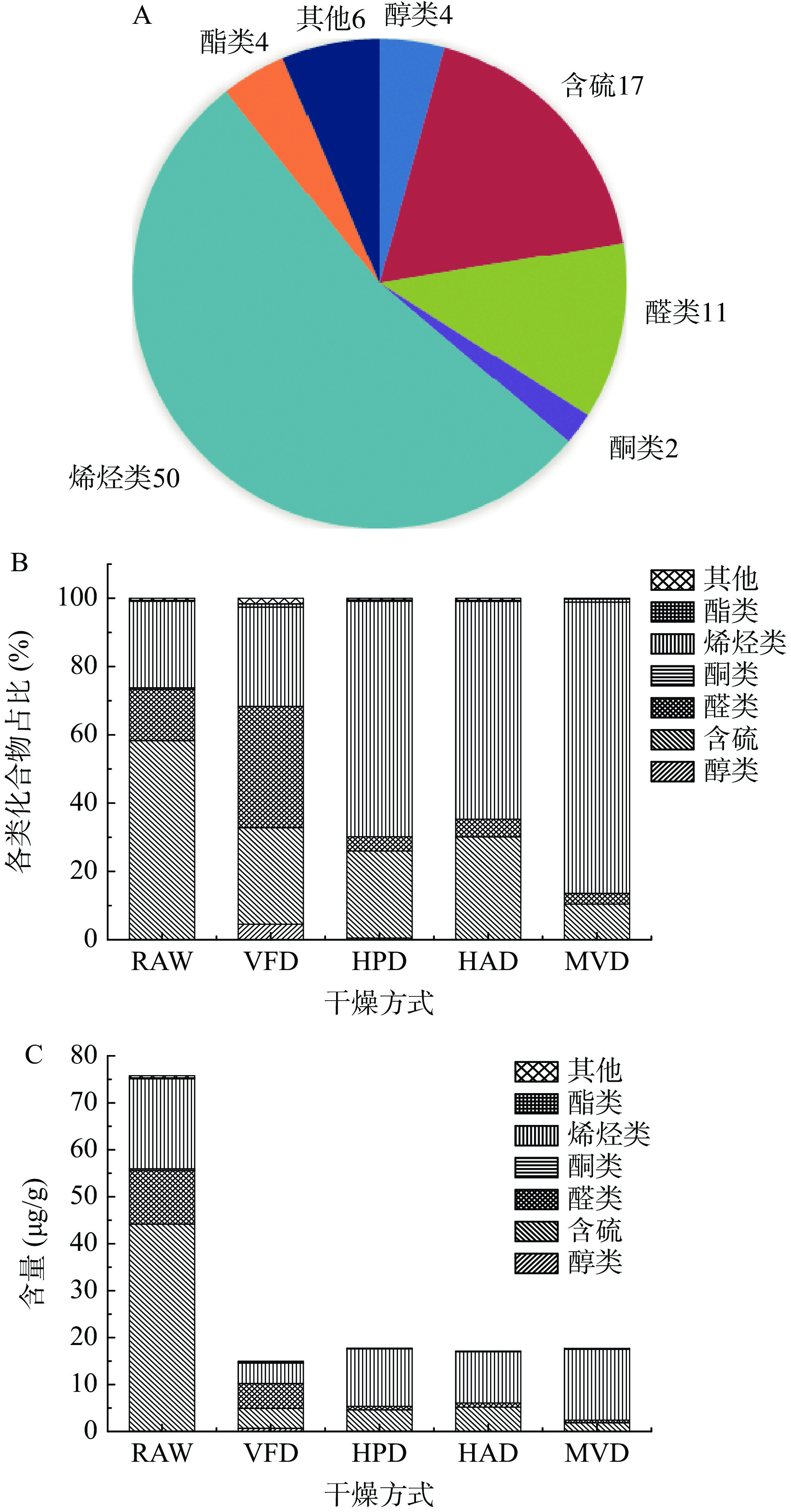
甘菊环烃C15H18 1786/1790 0.175±0.048 0.05±0 0.073±0.033 0.033±0.004 0.035±0.009 MS,RI 44.987 8,9-脱氢-环异龙胆烯 C15H22 1867 − − − 0.02±0.001 − MS 45.972 9,10-脱氢-异长叶烯 C15H22 1934 2.231±0.29 0.044±0.015 − 0.098±0.02 0.048±0 MS 酯类 44.655 (2E,6E)-乙酸金合欢酯 C17H28O2 1846/1844 0.241±0.03 0.05±0.015 0.049±0.014 0.057±0.006 0.047±0.007 MS,RI 45.097 邻苯二甲酸己-3-基异丁酯 C18H26O4 1874 − 0.032±0.024 − − 0.059±0.026 MS 45.896 棕榈酸甲酯 C17H34O2 1929/1928 − − 0.024±0.006 − − MS,RI 46.456 邻苯二甲酸二丁酯 C16H22O4 1969/1969 − 0.061±0 − − 0.055±0.032 MS,RI 其他 4.259 2-甲基呋喃 C5H6O 745/599 0.149±0.075 − − 0.032±0.009 − MS,RI 13.171 3-乙基-1H吡咯 C6H9N 945 − − − − 0.04±0.005 MS 22.227 2,6-二乙基-吡嗪 C8H12N2 1090/1078 − − 0.04±0.001 − − MS,RI 25.336 苄基腈 C8H7N 1141/1141 0.158±0.009 0.063±0 − − − MS,RI 31.445 十三烷 C13H28 1300 − 0.047±0.021 − − − MS 33.186 丁香酚 C10H12O2 1359/1359 0.14±0.005 0.138±0.005 0.051±0.009 0.072±0.005 − MS,RI 注:−表示未检测到该物质;MS表示NIST14谱库定性;RI表示计算保留指数与文献保留指数对比定性。 挥发性化合物可分为7个化学类别(图4A),包括50种烯烃类、17种含硫类、11种醛类、4种醇类、4种酯类、2种酮类,还有一个由呋喃、吡嗪、酚类等组成的6种其他物质。很明显,烯烃类和硫化物是所有检测到的挥发性化合物中的两个主要成分。由图4B可以看出鲜样和各干燥方式下均为烯烃类、含硫类、醛类含量占比较高。与鲜样相比干燥后含硫类化合物占比明显降低,其中经微波真空干燥的样品保留率最低。烯烃类化合物则在干燥后样品占比升高,其中微波真空干燥样品升高最为明显,真空冷冻干燥则升高不明显。经过干燥处理后总挥发性化合物的含量明显降低(图4C),可能是干燥过程中发生了复杂的物理、化学变化所导致,如部分水溶性物质和低沸点物质在干燥过程随着水分的蒸发发生损失以及美拉德反应、氨基酸分解、脂肪氧化、不同分子之间相互作用、大分子的降解反应等化学反应有关[24]。比较挥发性化合物含量,可以看出几种热干燥(热泵干燥、热风干燥、微波真空干燥)的挥发性化合物含量无明显差异。
研究表明含硫类化合物是香椿主要的特征香气成分[13,25−26]。鲜样中含硫化合物占比为58.21%,经过真空冷冻干燥、热泵干燥、热风干燥、微波真空干燥后含硫类化合物占比分别为30.12%、28.26%、25.51%、10.45%,经过干燥处理后表现出明显的损失(图4B)。含硫化合物的损失是由于其热稳定性差,在较高温度下发生转化或聚合。据报道,双-(1-丙烯)二硫化物可以在85 ℃重排成2-巯基-3,4-二甲基-2,3-二氢噻吩,然后进一步降解为3,4-二甲基噻吩或3,4-二甲基-2-噻吩基二硫化物[27]。鉴定出来的含硫化合物主要有3,4-二甲基-噻吩、2,5-二甲基-噻吩、2-巯基-3,4-二甲基-2,3-二氢噻吩、(E,Z)-二-1-丙烯基二硫化物、顺式-2-乙基-3-甲基噻吩、(E,E)-二-1-丙烯基三硫化物、3,4-二甲基噻吩-2-硫醇、甲基-环硫乙烷等。研究发现,香椿风味前体物质γ-谷氨酰-丙烯基-半胱氨酸、γ-谷氨酰-丙烯基-巯代甘氨酸等通过酶促反应,生成谷氨酸和丙烯基硫醇、氨和乙醛酸的中间物;丙烯基硫醇在一定条件下转化为二丙烯基二硫醚,形成香椿特征风味物质[28−29]。
烯烃类化合物是香椿挥发性成分中种类最多的物质(在鲜样和经真空冷冻干燥、热泵干燥、热风干燥、微波真空干燥后分别含有30、27、37、34、36种),除鲜样和真空冷冻干燥组外,烯烃类含量占比均最高。新鲜香椿组占比为25.31%,真空冷冻干燥组29.06%,而其他3种干燥处理组含量占比均达到60%以上,说明经过干燥处理后明显升高。香椿样品中烯烃类化合物主要为含有C15的倍半萜烯化合物,包括α-蒎烯、依兰烯、β-榄香烯、反式石竹烯、α-愈创木烯、古巴烯、(-)-异丁香烯、香橙烯、β-蛇床烯、β-马榄烯、α-白菖考烯、γ-杜松烯等。研究表明,萜烯类大多具有酯香、花香、水果香、甜香等比较柔和的气味,可以起到调和硫化物刺激味的作用[30]。另外有报道,植物抗病性可能与烯类化合物的存在有关,这也正是香椿在生长过程中极少发生病害的可能原因。
醛类化合物在所有香椿样品中含量占比均排第三,鉴定和定量出来的醛类物质主要有己醛、2-己烯醛、苯甲醛、壬醛以及β-环柠檬醛等。经过干燥后,除真空冷冻干燥组外,其他样品中醛物质的含量明显降低,分别比新鲜香椿下降了72.24%、65.50%、79.17%。醛类物质一般是由脂质水解形成游离脂肪酸,然后脂肪酸经热分解形成氢过氧化物,进一步反应形成[31]。己醛是亚油酸在过氧化氢裂解酶体系中过氧化的常见二次产物。研究表明,n-6多不饱和脂肪酸在37 ℃加热可以产生己醛,常作为脂质过氧化的量度。2-己烯醛是在氧气存在下由亚麻酸异构化而成,是植物叶片气味的主要成分,同时2-己烯醛可以通过植物叶片中的乙醇脱氢酶转化为(E)-2-己烯-1-醇。己醛具有青草味、腥味,苯甲醛具有令人愉快的坚果香气,壬醛有鱼腥味,β-环柠檬醛具有柠檬型清香气味[32−34]。这些均可能对香椿总体风味起加和作用。
其余挥发性化合物(醇、酯、酮等化合物)在干燥过程中的也发生了明显变化,可能是热加工过程中转化,与其他化合物反应或浸出到介质中的综合结果。研究表明食品物料在干燥过程中挥发性风味物质保留与干燥速率、干燥时间、干燥温度等存在密切关系,挥发物在干燥层网络组织结构中扩散系数越小、干燥时间越短、干燥温度越低、真空条件下暴露时间越短,越有利于挥发性风味物质保留[12]。由于箱式热风干燥在密闭环境下湿热作用时间较长,更易发生水解、异构、裂解等化学反应,使挥发性成分含量低。微波真空干燥过程中产生瞬时高温,使一些长链化合物和对温度敏感的化合物降解,从样品中逸出。研究表明,冷冻干燥的低温条件可能会导致酶活性下降以及代谢途径下调或破坏,从而导致挥发性化合物显着下降。此外,挥发性成分在真空条件下更容易因升华而损失[35]。
2.5 ROAV分析及关键香气化合物
挥发性风味化合物的含量并不代表其对风味的贡献,评价其贡献还需要与每个挥发性成分的香气阈值相结合。ROAV是挥发性化合物质量浓度与其香气阈值的比值,用来评估挥发性化合物对样品香气的贡献。一般认为,ROAV值越大,说明该成分对样品整体风味的贡献越大,ROAV≥1的挥发性化合物对整体香气的贡献较大,ROAV>10的挥发性化合物则被确定为重要香气成分[36],0.1≤ROAV<1的成分对样品的整体风味有重要修饰作用。为了获得关于不同香气物质对香椿样品整体香气的贡献的信息,通过查阅有关书籍[37−38]和文献[21,39]找到以下25种挥发性物质的香气阈值,计算了香气活性值,结果如表4所示。筛选出20种ROAV>1的化合物,其中鲜样、真空冷冻干燥、热泵干燥、热风干燥、微波真空干燥样品分别筛选ROAV>1的有14、9、9、12、7种。鲜样中(E,Z)-二-1-丙烯基二硫化物(3666998)、2-巯基-3,4-二甲基-2,3-二氢噻吩(275209)的ROAV最高;其次是正己醛(491)、2-己烯醛(193)、α-蒎烯(115)、β-环柠檬醛(60)、丁香酚(56)。真空冷冻干燥组最高的是(E,Z)-二-1-丙烯基二硫化物(134901)、2-巯基-3,4-二甲基-2,3-二氢噻吩(11206)、正己醛(161)、芳樟醇(123)、2-己烯醛(117)、丁香酚(55)。热泵干燥组ROAV最高的是(E,Z)-二-1-丙烯基二硫化物(120901)、2-巯基-3,4-二甲基-2,3-二氢噻吩(10248)、二甲基硫醚(708)、正己醛(22)、丁香酚(20)、壬醛(14)、α-蒎烯(12)、2-己烯醛(11)。热风干燥组ROAV最高的是(E,Z)-二-1-丙烯基二硫化物(349878)、2-巯基-3,4-二甲基-2,3-二氢噻吩(24923)、二甲基硫醚(1880)、丁香酚(29)、正己醛(6)、苯乙醛(14)、壬醛(12)。微波真空干燥组ROAV最高的是(E,Z)-二-1-丙烯基二硫化物(37848)、2-巯基-3,4-二甲基-2,3-二氢噻吩(3656)、二甲基硫醚(1920)、α-蒎烯(12)。
表 4 香椿中挥发性化合物的ROAVTable 4. ROAV of volatile compounds in T. sinensis序号 化合物 英文名称 阈值
(μg/kg)[21,37−39]风味描述 ROAV RAW VFD HPD HAD MVD 1 二甲基硫醚 Dimethyl sulfide 0.3 硫磺、洋葱、甜玉米、蔬菜味 − − 708.66 1880.27 1920.41 2 2,5-二甲基-噻吩 Thiophene,2,5-dimethyl- 3000 坚果味、硫磺味 3.18 0.30 0.30 0.29 <0.1 3 (E,Z)-二-1-丙烯基
二硫醚(E,Z)-Di-1-propenyldisulfide 0.0034 烤洋葱味 3666998.10 134901.72 120901.08 349878.92 37848.36 4 3,4-二甲基-噻吩 Thiophene,3,4-dimethyl- 5000 烤洋葱味 1.19 <0.1 <0.1 0.13 <0.1 5 2-巯基-3,4-二甲基-
2,3-二氢噻吩2-Mercapto-3,4-dimethyl-2,3-
dihydrothiophene0.039 硫磺,葱味,甜椒味 275209.05 11206.29 10248.30 24923.60 3656.47 6 (Z)-2-戊烯-1-醇 (Z)-2-Penten-1-ol 720 <0.1 <0.1 <0.1 − − 7 叶醇 (Z)-3-Hexen-1-ol 100 新鲜的青草味、植物油味 − 3.73 0.21 − − 8 芳樟醇 Linalool 0.58 柑橘香味、玫瑰花香 − 123.75 − − − 9 3-甲基丁醛 3-Methyl-butanal 1.1 巧克力味、桃子味、脂肪香 − − − 329.09 252.73 10 2-甲基丁醛 2-Methyl-butanal 1 咖啡坚果味、麦芽香、
脂肪香− − − 232.80 180.40 11 2-甲基-2-丁烯醛 2-Methyl-2-butenal 500 − − <0.1 <0.1 <0.1 12 正己醛 Hexanal 10 新鲜的青草香、果香 491.84 161.05 22.40 6.00 − 13 2-己烯醛 2-Hexenal 30 甜杏仁味、苹果梅子果香 193.70 117.98 11.05 1.37 − 14 苯甲醛 Benzaldehyde 350 强烈的苦杏仁味 0.41 0.19 <0.1 0.16 − 15 苯乙醛 Benzeneacetaldehyde 4 风信子甜花香、苜蓿蜜香 − − 8.16 14.31 − 16 壬醛 Nonanal 2.8 新鲜鸢尾草味、
柑橘皮脂肪香38.37 36.04 14.41 12.36 − 17 β-环柠檬醛 β-Cyclocitral 3 药草味、烟草味、红果味 60.18 − − − − 18 α-蒎烯 α-Pinene 6 樟脑清凉味、松木香 115.54 15.72 12.26 − 12.19 19 D-柠檬烯 D-Limonene 34 柑橘类甜香 2.72 − − − − 20 (Z)-β-石竹烯 (Z)-β-Caryophyllene 1200 木质及辛辣的香味 4.35 − <0.1 0.11 <0.1 21 反式石竹烯 Caryophyllene 1540 木头味、丁香香料味 1.13 0.32 0.98 1.13 0.95 22 葎草烯 Humulene 390 木香 3.26 0.33 0.99 1.03 1.27 23 香橙烯 Aromandendrene 340 木香 0.66 0.27 0.28 0.50 0.39 24 2-甲基呋喃 2-Methyl-furan 3500 淡的丙酮味、巧克力味 <0.1 − − <0.1 − 25 丁香酚 Eugenol 2.5 辛辣味、丁香味、木头味 55.84 55.14 20.23 28.81 − 注:−表示未检测到该物质;风味描述来自网站http://www.thegoodscentscompany.com/search2.html。 通过对新鲜香椿和干燥组的比较发现五组样品中ROAV最高的均为(E,Z)-二-1-丙烯基二硫醚和2-巯基-3,4-二甲基-2,3-二氢噻吩,并且新鲜组ROAV明显高于热处理组。正己醛、2-己烯醛、丁香酚在除微波真空干燥组外四个样品中ROAV值次之,对香椿香气具有重要贡献。芳樟醇是真空冷冻干燥组重要的化合物。本研究结果与前人的研究认为2-巯基-3,4-二甲基-2,3-二氢噻吩和二-1-丙烯基硫化物是新鲜香椿总体香气特征的重要化合物[25];丁香酚和β-紫罗兰酮是影响干燥香椿总香气的重要香气物质的结果相似[13]。
2.6 香椿样品中挥发性化合物的PLS-DA分析
PLS-DA与PCA均是通过降维将复杂数据直观化,但是PLS-DA为有监督的分析,属于模型的方法。可将高维数据可视化、判别分析和代谢变化有关的潜在代谢物。使用交叉验证评价模型的性能指标,R2为模型的拟合能力,Q2为对模型预测能力的估计,以大于0.5为宜,越接近1越好。以定性定量的94个化合物为x变量,以不同处理的香椿为y变量,进行PLS-DA建立相关模型,模型的判别效果如图5B所示,R2=0.86758,Q2=0.60925,说明该模型稳定性较好,未出现过拟合现象,具有较好的预测能力,图5A所示第1组为鲜样的样点(第4象限),第2组为真空冷冻干燥的样点(主要为第2象限),第3组为热泵干燥、热风干燥、微波真空干燥的样点(集中在第3象限)。
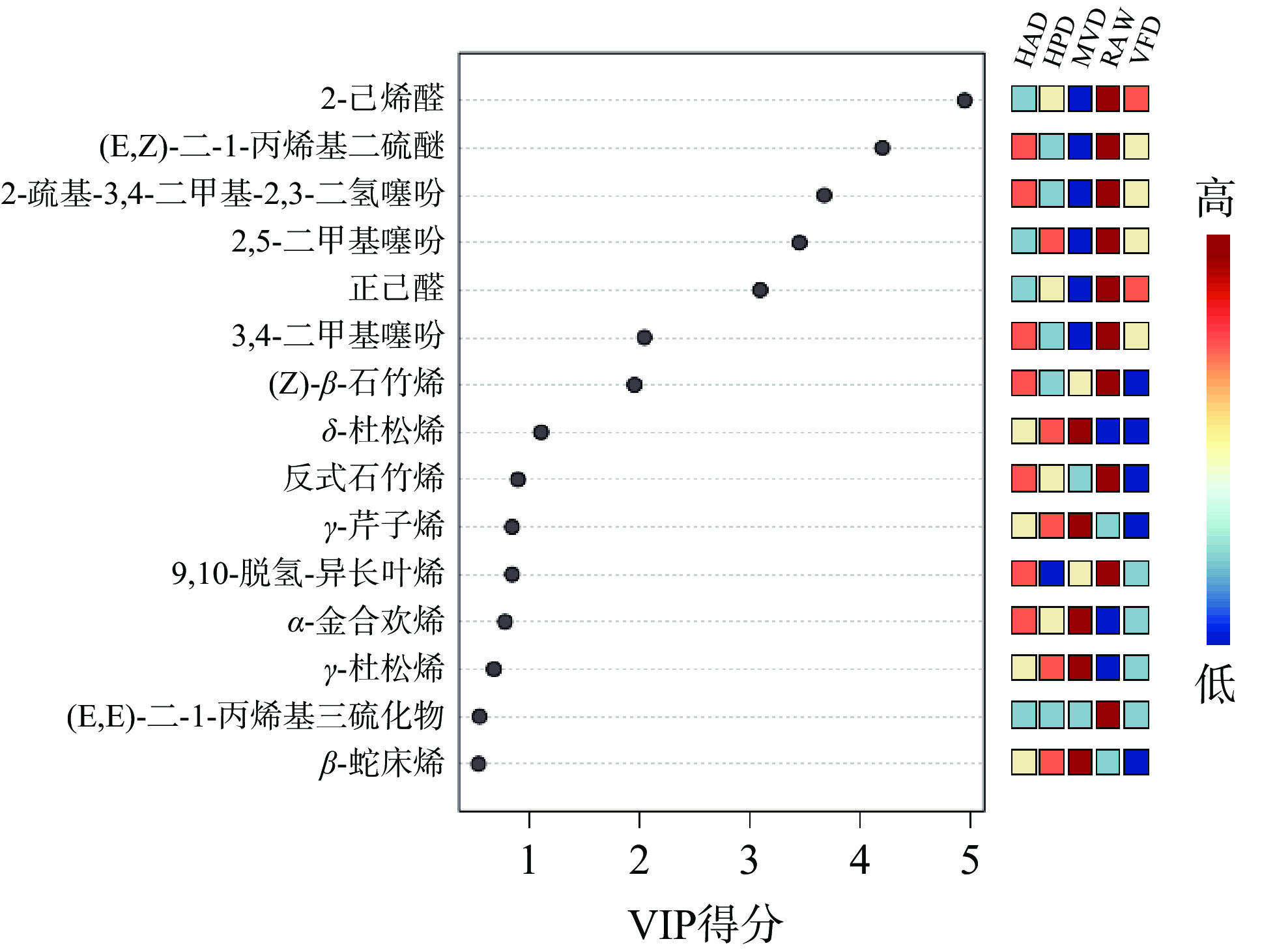
为了进一步表征不同干燥方式香椿样品挥发性化合物之间的差异,计算和检验了PLS-DA模型的VIP得分,采用“大于1”的标准,筛选出10种(VIP>1)标志性有机化合物如图6所示,其中VIP值大于4的2-己烯醛和(E,Z)-二-1-丙烯基二硫醚是最重要的区别因素,2-巯基-3,4-二甲基-2,3-二氢噻吩、2,5-二甲基噻吩、正己醛、3,4-二甲基噻吩等化合物VIP值大于2贡献也比较大,(Z)-β-石竹烯、δ-杜松烯等VIP值均大于1,为比较重要的化合物。2-己烯醛含量最高的为鲜样,其次是冷冻干燥和热泵干燥;(E,Z)-二-1-丙烯基二硫化物含量最高的是鲜样;δ-杜松烯和γ-芹子烯在微波真空干燥组含量最高。
3. 结论
采用GC-IMS、GC-MS结合化学计量学方法,对不同干燥方式下香椿的挥发性风物质进行了分析。采用GC-IMS在5组香椿样品中鉴定出59种化合物,鲜样中信号强度显著高于其他组的物质,主要为醛类、醇类以及其他类物质。通过GC-MS鉴定出94种挥发性化合物,香椿样品中的主要挥发性成分是硫化物、烯烃类和醛类。经过干燥后总挥发性化合物和特征香气成分硫化合物的含量都显著降低,在真空冷冻干燥、热泵干燥样品特征含硫化合物保留率相对较高。烯烃类化合物是香椿挥发性成分中种类最多的物质,且经过干燥处理后占比显著升高。通过ROAV法确定了(E,Z)-二-1-丙烯基二硫化物、2-巯基-3,4-二甲基-2,3-二氢噻吩、正己醛、2-己烯醛、丁香酚等为香椿样品中关键香气化合物。PCA和PLS-DA结果表明,不同干燥处理的样品与新鲜样品有明显的分离,彼此之间也有明显的区别,真空冷冻干燥样品与鲜样分为一组,与鲜样最为相似,其次为热泵干燥。但真空冷冻干燥时间长、能耗大、不利于工业化生产,结合实际应用热泵干燥为香椿最适合的脱水方式。根据VIP得分共筛选出10种(VIP>1)标志挥发性化合物可作为不同干燥方式下主要的差异物质。
GC-MS检测的主要是碳链在C8~C20之间的分子量大且含量较高的挥发性成分,而GC-IMS检测出的大多为C4~C10之间的小分子、挥发性强且含量低的挥发性成分。GC-MS和GC-IMS两种技术相结合扩大了香椿样品中挥发性成分的检测范围,在香椿风味分析中具有明显的优势。干燥方式对香椿风味特性影响显著,本研究为香椿热加工过程中风味变化规律和品质控制提供一定的理论基础和技术支撑。
-
表 1 4种干燥方式的工艺条件和参数
Table 1 Process conditions and parameters of four drying methods
干燥方式 干燥参数 干燥时间 真空冷冻干燥(VFD) 将香椿嫩芽均匀平铺放在真空冷冻干燥机的托盘中,冷冻干燥机参数:预冻温度设置为−50 ℃,预冻时间为
30 min,真空度为0.01 kPa,预冻完成后打开真空泵和真空计,当真空度低于50 Pa时,打开隔板控温,智能冷冻
干燥机自动升华干燥和解析干燥。35 h 热泵干燥(HPD) 将香椿嫩芽均匀放在铺纱布的筛网上,然后放入空气能热泵烘干机中,设定干燥温度为45 ℃,湿度为10%,进行干燥。 10 h 热风干燥(HAD) 将香椿嫩芽均匀放在电热鼓风干燥箱中,设定温度为55 ℃,进行干燥。 7 h 微波真空干燥(MVD) 将香椿嫩芽均匀放入微波真空干燥机的托盘中,设置功率为3000 W,真空度−40 kPa条件下进行干燥。 15 min 表 2 香椿样品中挥发性有机物的GC-IMS鉴定结果
Table 2 Identification of volatile organic compounds in T. sinensis samples by GC-IMS
序号 中文名称 英文名称 CAS 分子式 分子量 保留指数 保留时间(s) 迁移时间(ms) 1 正丙醇 1-Propanol 71-23-8 C3H8O 60.1 547.2 106.890 1.114 2 2-甲基丙醇-D 2-Methylpropanol-D 78-83-1 C4H10O 74.1 640.9 154.350 1.363 3 2-甲基丙醇-M 2-Methylpropanol-M 78-83-1 C4H10O 74.1 641.9 154.875 1.172 4 1-丁醇 1-Butanol 71-36-3 C4H10O 74.1 655 162.540 1.181 5 3-甲基-2-丁醇 3-Bethyl-2-butanol 598-75-4 C5H12O 88.1 695.4 190.365 1.232 6 1,2-丙二醇 1,2-Propanediol 57-55-6 C3H8O2 76.1 737.9 227.745 1.27 7 3-甲基-3-丁烯醇 3-Methyl-3-butenol 763-32-6 C5H10O 86.1 759.6 248.220 1.296 8 2-乙基己醇 2-Ethylhexanol 104-76-7 C8H18O 130.2 1042.7 698.985 1.42 9 α-苯乙醇 α-Phenylethanol 98-85-1 C8H10O 122.2 1055 726.495 1.558 10 呋喃醇 Furaneol 3658-77-3 C6H8O3 128.1 1055.6 727.755 1.206 11 (-)-龙脑醇 (-)-Borneol 464-45-9 C10H18O 154.3 1153.6 947.100 1.212 12 苯乙醇 Benzeneethanol 1960/12/8 C8H10O 122.2 1155.4 950.985 1.648 13 龙脑醇 Borneol 507-70-0 C10H18O 154.3 1166.8 976.605 1.218 14 二丙基硫醚 Dipropyl sulfide 111-47-7 C6H14S 118.2 873.1 359.310 1.161 15 丁醛-D Butanal-D 123-72-8 C4H8O 72.1 580.9 123.585 1.283 16 丁醛-M Butanal-M 123-72-8 C4H8O 72.1 581.1 123.690 1.115 17 2-甲基丁醛 2-Methylbutanal 96-17-3 C5H10O 86.1 670.7 172.410 1.398 18 戊醛-M Pentanal-M 110-62-3 C5H10O 86.1 699.9 193.935 1.19 19 乙缩醛 Acetal 105-57-7 C6H14O2 118.2 725.8 216.510 1.039 20 (E)-2-戊烯醛-D (E)-2-Pentenal-D 1576-87-0 C5H8O 84.1 750.3 239.40 1.351 21 (E)-2-戊烯醛-M (E)-2-Pentenal-M 1576-87-0 C5H8O 84.1 764.1 252.420 1.105 22 己醛 Hexanal 66-25-1 C6H12O 100.2 824.8 307.335 1.563 23 庚醛 Heptanal 111-71-7 C7H14O 114.2 949.5 490.875 1.337 24 5-甲基糠醛-D 5-Methylfurfural-D 620-02-0 C6H6O2 110.1 964.2 522.480 1.476 25 5-甲基糠醛-M 5-Methylfurfural-M 620-02-0 C6H6O2 110.1 972.7 541.170 1.123 26 (E)-2-壬烯醛 (E)-2-Nonenal 18829-56-6 C9H16O 140.2 1155.9 952.245 1.42 27 乙酸-M Acetic acid-M 64-19-7 C2H4O2 60.1 590.3 128.205 1.042 28 乙酸-D Acetic acid-D 64-19-7 C2H4O2 60.1 596.4 131.250 1.151 29 丙酸-M Propanoic acid-M 153474-35-2 C3H6O2 74.1 656.8 163.590 1.264 30 丙酸-D Propionic acid-D 153474-35-2 C3H6O2 74.1 699.4 193.515 1.273 31 丁酸 Butanoic acid 107-92-6 C4H8O2 88.1 811.7 295.365 1.366 32 异戊酸 Isovaleric acid 503-74-2 C5H10O2 102.1 872.1 357.945 1.499 33 己酸 Hexanoic acid 142-62-1 C6H12O2 116.2 989.8 579.600 1.295 34 丁酮-M Butanone-M 78-93-3 C4H8O 72.1 606.6 136.290 1.246 35 丁酮-D Butanone-D 78-93-3 C4H8O 72.1 613 139.545 1.062 36 羟基丙酮 Hydroxyacetone 116-09-6 C3H6O2 74.1 631.5 149.205 1.234 37 2,3-戊二酮 2,3-Pentanedione 600-14-6 C5H8O2 100.1 688.3 184.800 1.311 38 3-戊酮 3-Pentanone 96-22-0 C5H10O 86.1 690.2 186.270 1.346 39 3-羟基-2-丁酮-D 3-Hydroxy-2-butanone-D 513-86-0 C4H8O2 88.1 729.1 219.555 1.332 40 3-羟基-2-丁酮M 3-Hydroxy-2-butanone-M 513-86-0 C4H8O2 88.1 733.1 223.230 1.061 41 乙酸乙酯-D Ethyl acetate-D 141-78-6 C4H8O2 88.1 616.7 141.435 1.334 42 乙酸丙酯-M Propyl acetate-M 109-60-4 C5H10O2 102.1 714.9 206.745 1.478 43 2-甲基丙酸乙酯 Ethyl-2-methylpropanoate 97-62-1 C6H12O2 116.2 734.1 224.175 1.198 44 γ-丁内酯 γ-Butyrolactone 96-48-0 C4H6O2 86.1 925.7 442.995 1.304 45 水杨酸甲酯 Methyl salicylate 119-36-8 C8H8O3 152.1 1201.3 1053.675 1.197 46 乙酸丙酯-T Propyl acetate-T 109-60-4 C5H10O2 102.1 715.3 207.060 1.166 47 乙酸乙酯-M Ethyl acetate-M 141-78-6 C4H8O2 88.1 623.4 144.900 1.097 48 乙酸丙酯-D Propyl acetate-D 109-60-4 C5H10O2 102.1 678.1 177.450 1.164 49 乙酸异丙酯 Isopropyl acetate 108-21-4 C5H10O2 102.1 665.5 169.050 1.167 50 苯乙烯 Styrene 100-42-5 C8H8 104.2 898 394.695 1.518 51 α-水芹烯 α-Phellandrene 99-83-2 C10H16 136.2 989.1 578.130 1.219 52 柠檬烯 Limonene 138-86-3 C10H16 136.2 1030.6 671.790 1.219 53 β-罗勒烯 β-Ocimene 13877-91-3 C10H16 136.2 1045.8 705.810 1.219 54 戊烷-D Pentanal-D 110-62-3 C5H10O 86.1 500.9 191.520 1.422 55 3-丁烯腈 3-Butenenitrile 109-75-1 C4H5N 67.1 631.7 149.310 1.127 56 2,5-二甲基呋喃 2,5-Dimethylfuran 625-86-5 C6H8O 96.1 699.1 193.305 1.356 57 2-乙酰吡嗪 2-Acetylpyrazine 22047-25-2 C6H6N2O 122.1 1022.1 652.680 1.148 58 2-乙基呋喃 2-Ethylfuran 3208-16-0 C6H8O 96.1 725.7 216.405 1.299 59 2,4-二氯苯酚 2,4-Dichlorophenol 120-83-2 C6H4Cl2O 163.0 1154.7 949.410 1.181 表 3 不同干燥方式下香椿香气成分GC-MS分析结果
Table 3 GC-MS analysis results of volatile compounds of T. sinensis under different drying methods
保留时间
(min)化合物 分子式 LRI RAW VFD HPD HAD MVD 定性方法 含硫 1.464 二甲基硫醚 C2H6S − − 0.213±0 0.564±0.038 0.576±0.04 MS,RI 2.841 甲基-环硫乙烷 C3H6S 681/606 0.227±0.086 1.918±0.971 1.979±0.076 0.801±0.086 0.696±0.091 MS 5.440 2,3-二氢-5-甲基-噻吩 C5H8S 791 0.173±0.072 − − − − MS 10.571 2,5-二甲基-噻吩 C6H8S 904/905 9.541±0.893 0.888±0.068 0.908±0.018 0.857±0.064 0.163±0.011 MS,RI 11.412 1,1'-硫代双-1-丙烯 C6H10S 917/904 0.136±0.021 − − − − MS,RI 13.562 1-(乙硫基)-2-甲基-1-丙烯 C6H12S 952 0.061±0 − 0.042±0.012 0.098±0.023 0.058±0.006 MS 16.493 顺式-2-乙基-3-甲基噻吩 C7H14S 998 0.108±0.08 − − − − MS 24.419 (E,Z)-二-1-丙烯基二硫化物 C6H10S2 1116/1124 12.468±1.222 0.459±0.098 0.411±0.059 1.19±0.047 0.129±0.058 MS,RI 24.776 3,4-二甲基-噻吩 C6H8S 904/908 5.969±0.821 0.398±0.036 0.428±0.033 0.634±0.046 0.086±0.052 MS,RI 26.296 (Z)丙-1-烯-1-基-丙二酸酯 C6H10S2 1162/1159 1.09±0.045 − − − − MS,RI 26.713 2-巯基-3,4-二甲基-2,3-二氢噻吩 C6H10S2 1172/1149 10.733±1.127 0.437±0.082 0.4±0.096 0.972±0.083 0.143±0.064 MS,RI 27.29 3,4-二甲基噻吩-2-硫醇 C6H8S2 1184/1193 0.718±0.103 − 0.03±0.001 − − MS,RI 27.418 1-(2-噻吩基)-1-丁酮 C8H10OS 1187 0.549±0.083 − − − − MS 32.591 (E,E)-二-1-丙烯基三硫化物 C6H10S3 1341/1348 1.615±0.336 − − − − MS,RI 39.948 1-(1-(丙-1-烯-1-基硫代)丙基)-2-
丙基二硫化物C9H18S3 1599/1592 0.249±0.129 − − − − MS,RI 41.512 (E)-1-丙烯基3,4-二甲基-2-
噻吩基二硫化物C9H12S3 1671/1671 0.48±0.034 − − − − MS,RI 43.016 薄荷硫化物 C15H24S 1749/1743 − 0.13±0.046 0.118±0.041 0.05±0.001 − MS,RI 醇类 4.871 (Z)-2-戊烯-1-醇 C5H10O 769/769 0.058±0.011 0.233±0.071 0.024±0.008 − − MS,RI 8.193 (Z)-3-己烯-1-醇 C6H12O 852/851 − 0.373±0.069 0.021±0.004 − − MS,RI 23.468 芳樟醇 C10H18O 1100/1099 − 0.072±0.033 − − − MS,RI 41.028 τ-杜松醇 C15H26O 1648/1649 − − 0.04±0.009 − − MS,RI 醛类 2.45 3-甲基丁醛 C5H10O 647/646 − − − 0.363±0.059 0.279±0.027 MS,RI 2.569 2-甲基丁醛 C5H10O 657/656 − − − 0.233±0.039 0.181±0.008 MS,RI 4.030 2-甲基-2-丁烯醛 C5H8O 734/737 − − 0.083±0.011 0.046±0.011 0.096±0.009 MS,RI 5.729 正己醛 C6H12O 801/800 4.918±0.308 1.611±0.041 0.224±0.049 0.06±0.008 − MS,RI 7.938 2-己烯醛 C6H10O 849/848 5.811±0.291 3.54±0.197 0.332±0.072 0.041±0.009 − MS,RI 13.817 苯甲醛 C7H6O 956/956 0.144±0.073 0.068±0 0.029±0 0.056±0.011 − MS,RI 19.492 苯乙醛 C8H8O 1042/1042 − − 0.033±0.005 0.057±0.013 − MS,RI 23.731 壬醛 C9H18O 1106/1105 0.107±0.014 0.101±0.044 0.04±0.01 0.035±0.004 − MS,RI 28.7 β-环柠檬醛 C10H16O 1220/1220 0.181±0 − − − − MS,RI 29.236 间苯二甲醛 C8H6O2 1236 0.122±0.031 − − − − MS 42.633 (Z,E)-2,6-金合欢醛 C15H24O 1727/1727 0.117±0.013 − − − − MS,RI 酮类 27.673 壬-3,5-二烯-2-酮 C9H14O 1193 0.197±0.075 − − − − MS 34.384 cis-茉莉酮 C11H16O 1400/1400 0.151±0.044 − − − − MS,RI 烯类 12.143 α-蒎烯 C10H16 929/928 0.693±0.059 0.094±0.022 0.074±0.035 − 0.073±0.024 MS,RI 18.319 D-柠檬烯 C10H16 1025 0.093±0 − − − − MS 32.609 δ-榄香烯 C15H24 1339/1339 − − 0.175±0.043 n.d. 0.137±0.024 MS,RI 33.492 (+)-环苜蓿烯 C15H24 1370/1368 0.1±0.01 − − − − MS,RI 33.602 依兰烯 C15H24 1374/1374 0.213±0 0.059±0 0.085±0.026 0.05±0.012 0.073±0.007 MS,RI 33.730 古巴烯 C15H24 1378/1378 − 0.078±0.048 0.219±0.05 0.288±0.035 0.464±0.112 MS,RI 33.730 α-荜澄茄油烯 C15H24 1378/1380 0.983±0.082 0.082±0 0.111±0.028 0.153±0.015 0.107±0.019 MS,RI 33.866 β-人参烯 C15H24 1383/1383 0.25±0.02 − − − − MS,RI 34.002 β-波旁烯 C15H24 1387/1386 0.26±0.02 − 0.036±0.013 − − MS,RI 34.205 (-)-β-榄香烯 C15H24 1394/1394 0.077±0.001 0.103±0 0.141±0.037 0.291±0.045 0.507±0.019 MS,RI 34.630 (Z)-β-石竹烯 C15H24 1409/1408 5.218±0.034 − 0.064±0.004 0.129±0.016 0.091±0.005 MS,RI 34.970 反式石竹烯 C15H24 1422/1418 1.734±0.794 0.496±0. 031 1.51±0.035 1.733±0.201 1.465±0.316 MS,RI 35.200 β-古尔均烯 C15H24 1431/1430 − − 0.098±0.008 0.085±0.01 0.106±0.011 MS,RI 35.378 α-香柠檬素 C15H24 1437/1438 − − − 0.059±0.005 0.074±0.006 MS,RI 35.471 α-愈创木烯 C15H24 1441/1439 0.524±0.012 0.061±0 0.183±0.068 0.162±0.023 − MS,RI 35.599 瓜亚-6,9-二烯 C15H24 1445/1450 0.65±0.082 − 0.124±0.035 0.157±0.021 0.102±0.018 MS,RI 35.676 迪纳-3,5-二烯 C15H24 1448/1458 − − − − 0.052±0.006 MS,RI 35.760 α-榄香烯 C15H24 1451/1469 0.66±0.041 − − − 0.179±0 MS,RI 35.829 表地带烯 C15H24 1476/1495 − − 0.129±0.038 − − MS,RI 35.888 葎草烯 C15H24 1456/1456 1.272±0.192 0.129±0.092 0.386±0.081 0.402±0.061 0.497±0.019 MS,RI 36.074 香橙烯 C15H24 1463/1440 0.224±0.018 0.09±0 0.096±0.028 0.168±0.023 0.132±0.025 MS,RI 36.083 带状烯 C15H24 1463 − 0.082±0 0.118±0.025 0.105±0.009 0.212±0.044 MS 36.329 桉叶三烯 C15H22 1472/1477 0.105±0 − − − − MS,RI 36.457 香附子烯 C15H24 1477/1415 0.207±0.007 − − − − MS,RI 36.483 (-)-g-杜松烯 C15H24 1519/1485 − 0.271±0.164 0.97±0.048 0.647±0.008 1.102±0.083 MS,RI 36.533 γ-姜黄烯 C15H24 1480/1479 0.229±0.023 − − − − MS,RI 36.644 大根香叶烯 C15H24 1484/1480 − 0.102±0.031 0.523±0.094 0.399±0.063 0.788±0.062 MS,RI 36.652 α-姜黄烯 C15H22 1484/1484 0.141±0.004 − − − − MS,RI 36.797 β-蛇床烯 C15H24 1490/1489 0.99±0.06 0.42±0.022 1.099±0.19 1.041±0.153 1.335±0.077 MS,RI 37.051 γ-芹子烯 C15H24 1499/1509 0.897±0.096 0.55±0.011 1.377±0.032 1.369±0.021 1.858±0.024 MS,RI 37.366 α-金合欢烯 C15H24 1510/1509 − 0.177±0.05 0.69±0.016 0.816±0.012 1.364±0.089 MS,RI 37.502 β-姜黄烯 C15H24 1515/1512 0.115±0.014 − 0.052±0.012 0.075±0.011 0.068±0.009 MS,RI 37.612 γ-杜松烯 C15H24 1519/1513 0.12±0.013 0.134±0.073 0.546±0.087 0.306±0.051 0.642±0.069 MS,RI 37.731 (-)-α-人参烯 C15H24 1523/1527 − 0.066±0 0.101±0.019 0.104±0.017 0.138±0.018 MS,RI 37.892 菖蒲烯 C15H22 1528/1529 0.426±0.019 0.483±0.024 − − − MS,RI 37.893 d-杜松烯 C15H24 1528/1528 − − 1.346±0.032 0.944±0.109 1.694±0.078 MS,RI 38.182 荜澄茄油烯 C15H24 1538/1537 − 0.067±0.019 0.117±0.021 0.104±0.013 0.183±0.027 MS,RI 38.284 异喇叭烯 C15H24 1446/1373 − − 0.079±0.013 0.068±0.013 − MS,RI 38.343 α-杜松烯 C15H24 1544/1544 − 0.085±0.037 0.328±0.047 0.185±0.03 0.378±0.043 MS,RI 38.351 β-马榄烯 C15H24 1494/1414 0.094±0.021 0.069±0.019 0.242±0.041 0.08±0.014 0.16±0.009 MS,RI 38.513 α-白菖考烯 C15H20 1550/1542 0.227±0.052 0.32±0.042 0.62±0.015 0.5±0.053 0.599±0.079 MS,RI 38.938 大根香叶烯 C15H24 1565/1562 − − 0.088±0.027 0.089±0.015 0.072±0.009 MS,RI 39.107 β-白菖考烯 C15H20 1570/1563 0.053±0 − 0.083±0.021 0.039±0.006 0.053±0.007 MS,RI 40.493 α-卡拉曼烯 C15H22 1624/1512 − − 0.054±0.015 − − MS,RI 40.611 9-甲基S-八氢菲 C15H20 1629 − 0.064±0.025 0.107±0.035 0.091±0.007 0.103±0.012 MS 41.342 (+)-戊烯 C15H24 1663/1500 − 0.049±0 0.084±0.002 − 0.053±0.005 MS,RI 41.758 卡达烯 C15H18 1682/1679 0.218±0.019 0.123±0.041 0.098±0.003 0.143±0.015 0.163±0.006 MS,RI 43.695 1,4-二甲基-7-(1-甲基乙基)-
甘菊环烃C15H18 1786/1790 0.175±0.048 0.05±0 0.073±0.033 0.033±0.004 0.035±0.009 MS,RI 44.987 8,9-脱氢-环异龙胆烯 C15H22 1867 − − − 0.02±0.001 − MS 45.972 9,10-脱氢-异长叶烯 C15H22 1934 2.231±0.29 0.044±0.015 − 0.098±0.02 0.048±0 MS 酯类 44.655 (2E,6E)-乙酸金合欢酯 C17H28O2 1846/1844 0.241±0.03 0.05±0.015 0.049±0.014 0.057±0.006 0.047±0.007 MS,RI 45.097 邻苯二甲酸己-3-基异丁酯 C18H26O4 1874 − 0.032±0.024 − − 0.059±0.026 MS 45.896 棕榈酸甲酯 C17H34O2 1929/1928 − − 0.024±0.006 − − MS,RI 46.456 邻苯二甲酸二丁酯 C16H22O4 1969/1969 − 0.061±0 − − 0.055±0.032 MS,RI 其他 4.259 2-甲基呋喃 C5H6O 745/599 0.149±0.075 − − 0.032±0.009 − MS,RI 13.171 3-乙基-1H吡咯 C6H9N 945 − − − − 0.04±0.005 MS 22.227 2,6-二乙基-吡嗪 C8H12N2 1090/1078 − − 0.04±0.001 − − MS,RI 25.336 苄基腈 C8H7N 1141/1141 0.158±0.009 0.063±0 − − − MS,RI 31.445 十三烷 C13H28 1300 − 0.047±0.021 − − − MS 33.186 丁香酚 C10H12O2 1359/1359 0.14±0.005 0.138±0.005 0.051±0.009 0.072±0.005 − MS,RI 注:−表示未检测到该物质;MS表示NIST14谱库定性;RI表示计算保留指数与文献保留指数对比定性。 表 4 香椿中挥发性化合物的ROAV
Table 4 ROAV of volatile compounds in T. sinensis
序号 化合物 英文名称 阈值
(μg/kg)[21,37−39]风味描述 ROAV RAW VFD HPD HAD MVD 1 二甲基硫醚 Dimethyl sulfide 0.3 硫磺、洋葱、甜玉米、蔬菜味 − − 708.66 1880.27 1920.41 2 2,5-二甲基-噻吩 Thiophene,2,5-dimethyl- 3000 坚果味、硫磺味 3.18 0.30 0.30 0.29 <0.1 3 (E,Z)-二-1-丙烯基
二硫醚(E,Z)-Di-1-propenyldisulfide 0.0034 烤洋葱味 3666998.10 134901.72 120901.08 349878.92 37848.36 4 3,4-二甲基-噻吩 Thiophene,3,4-dimethyl- 5000 烤洋葱味 1.19 <0.1 <0.1 0.13 <0.1 5 2-巯基-3,4-二甲基-
2,3-二氢噻吩2-Mercapto-3,4-dimethyl-2,3-
dihydrothiophene0.039 硫磺,葱味,甜椒味 275209.05 11206.29 10248.30 24923.60 3656.47 6 (Z)-2-戊烯-1-醇 (Z)-2-Penten-1-ol 720 <0.1 <0.1 <0.1 − − 7 叶醇 (Z)-3-Hexen-1-ol 100 新鲜的青草味、植物油味 − 3.73 0.21 − − 8 芳樟醇 Linalool 0.58 柑橘香味、玫瑰花香 − 123.75 − − − 9 3-甲基丁醛 3-Methyl-butanal 1.1 巧克力味、桃子味、脂肪香 − − − 329.09 252.73 10 2-甲基丁醛 2-Methyl-butanal 1 咖啡坚果味、麦芽香、
脂肪香− − − 232.80 180.40 11 2-甲基-2-丁烯醛 2-Methyl-2-butenal 500 − − <0.1 <0.1 <0.1 12 正己醛 Hexanal 10 新鲜的青草香、果香 491.84 161.05 22.40 6.00 − 13 2-己烯醛 2-Hexenal 30 甜杏仁味、苹果梅子果香 193.70 117.98 11.05 1.37 − 14 苯甲醛 Benzaldehyde 350 强烈的苦杏仁味 0.41 0.19 <0.1 0.16 − 15 苯乙醛 Benzeneacetaldehyde 4 风信子甜花香、苜蓿蜜香 − − 8.16 14.31 − 16 壬醛 Nonanal 2.8 新鲜鸢尾草味、
柑橘皮脂肪香38.37 36.04 14.41 12.36 − 17 β-环柠檬醛 β-Cyclocitral 3 药草味、烟草味、红果味 60.18 − − − − 18 α-蒎烯 α-Pinene 6 樟脑清凉味、松木香 115.54 15.72 12.26 − 12.19 19 D-柠檬烯 D-Limonene 34 柑橘类甜香 2.72 − − − − 20 (Z)-β-石竹烯 (Z)-β-Caryophyllene 1200 木质及辛辣的香味 4.35 − <0.1 0.11 <0.1 21 反式石竹烯 Caryophyllene 1540 木头味、丁香香料味 1.13 0.32 0.98 1.13 0.95 22 葎草烯 Humulene 390 木香 3.26 0.33 0.99 1.03 1.27 23 香橙烯 Aromandendrene 340 木香 0.66 0.27 0.28 0.50 0.39 24 2-甲基呋喃 2-Methyl-furan 3500 淡的丙酮味、巧克力味 <0.1 − − <0.1 − 25 丁香酚 Eugenol 2.5 辛辣味、丁香味、木头味 55.84 55.14 20.23 28.81 − 注:−表示未检测到该物质;风味描述来自网站http://www.thegoodscentscompany.com/search2.html。 -
[1] PENG W, LIU Y J, HU M B, et al. Toona sinensis:A comprehensive review on its traditional usages, phytochemisty, pharmacology and toxicology[J]. Revista Brasilra de Farmacognosia,2018,29(1):111−124.
[2] 张乐, 史冠莹, 蒋鹏飞, 等. 香椿干燥特性及其特征香气化合物热降解动力学[J]. 现代食品科技,2023,39(8):257−263. [ZHANG L, SHI G Y, JIANG P F, et al. Drying characteristics of Toona sinensis and thermal degradation kinetics of key aroma compounds of Toona sinensis[J]. Modern Food Science and Technology,2023,39(8):257−263.] ZHANG L, SHI G Y, JIANG P F, et al. Drying characteristics of Toona sinensis and thermal degradation kinetics of key aroma compounds of Toona sinensis[J]. Modern Food Science and Technology, 2023, 39(8): 257−263.
[3] 王赵改, 杨慧. 香椿产业的现状及发展趋势[J]. 农产品加工,2013(7):8−10. [WANG Z G, YANG H. The current situation and development trend of the Toona sinensis industry[J]. Farm Products Processing,2013(7):8−10.] WANG Z G, YANG H. The current situation and development trend of the Toona sinensis industry[J]. Farm Products Processing, 2013(7): 8−10.
[4] JIANG X X, ZHANG B B, LE M H, et al. Analysis of nutrient composition and antioxidant characteristics in the tender shoots of Chinese toon picked under different conditions[J]. LWT-Food Science & Technology,2019,109:137−144.
[5] 食品商务网[EB/OL]. https://price.21food.cn. [6] DING S S, SU P F, WANG D C, et al. Blue and red light proportion affects growth, nutritional composition, antioxidant properties and volatile compounds of Toona sinensis sprout[J]. LWT-Food Science & Technology,2023,173:114400.
[7] 夏亚男, 侯丽娟, 齐晓茹, 等. 食品干燥技术与设备研究进展[J]. 食品研究与开发,2016(4):204−208. [XIA Y N, HOU L J, QI X R, et al. Research progress of food drying technology and equipment[J]. Food Research and Development,2016(4):204−208.] doi: 10.3969/j.issn.1005-6521.2016.04.050 XIA Y N, HOU L J, QI X R, et al. Research progress of food drying technology and equipment[J]. Food Research and Development, 2016(4): 204−208. doi: 10.3969/j.issn.1005-6521.2016.04.050
[8] 王益强. 热泵干燥技术在脱水蔬菜加工中的应用[J]. 现代制造技术与装备,2016(9):114−115. [WANG Y Q. Application of heat pump drying technology in the processing of dehydrated vegetables[J]. Modern Manufacturing Technology and Equipment,2016(9):114−115.] doi: 10.3969/j.issn.1673-5587.2016.09.062 WANG Y Q. Application of heat pump drying technology in the processing of dehydrated vegetables[J]. Modern Manufacturing Technology and Equipment, 2016(9): 114−115. doi: 10.3969/j.issn.1673-5587.2016.09.062
[9] 任广跃, 刘军雷, 刘文超, 等. 香椿芽热泵式冷风干燥模型及干燥品质[J]. 食品科学,2016,37(23):13−19. [REN G Y, LIU J L, LIU W C, et al. Drying modelling and quality of Toona sinensis subjected to heat pumpcold air drying[J]. Food Science,2016,37(23):13−19.] doi: 10.7506/spkx1002-6630-201623003 REN G Y, LIU J L, LIU W C, et al. Drying modelling and quality of Toona sinensis subjected to heat pumpcold air drying[J]. Food Science, 2016, 37(23): 13−19. doi: 10.7506/spkx1002-6630-201623003
[10] 刘艳红, 熊张平, 季春艳, 等. 干燥方式对太和香椿芽品质的影响[J]. 食品与机械,2020,36(9):201−206. [LIU Y H, XIONG Z P, JI C Y, et al. Eeffect of three drying methods on the quality of Taihe Toona sinensis bud[J]. Food & Machinery,2020,36(9):201−206.] LIU Y H, XIONG Z P, JI C Y, et al. Eeffect of three drying methods on the quality of Taihe Toona sinensis bud[J]. Food & Machinery, 2020, 36(9): 201−206.
[11] 高海生, 刘秀凤, 罗彩霞, 等. 两种干燥方法对香椿芽干品品质的影响[J]. 核农学报,2013,27(8):1184−1188. [GAO H S LIU X F, LUO C X, et al. Impacts on the quality of toon sprouts dry goods by two drying methods[J]. Journal of Nuclear Agricultural Sciences,2013,27(8):1184−1188.] GAO H S LIU X F, LUO C X, et al. Impacts on the quality of toon sprouts dry goods by two drying methods[J]. Journal of Nuclear Agricultural Sciences, 2013, 27(8): 1184−1188.
[12] 谢焕雄, 胡志超, 王海鸥, 等. 真空冷冻干燥对柠檬挥发性风味化合物保留的影响[J]. 农业工程学报,2018,34(22):282−290. [XIE H X, HU Z C, WANG H O, et al. Effect of vacuum freeze-drying methods on retention of volatile flavor compounds of lemon[J]. Transactions of the Chinese Society of Agricultural Engineering,2018,34(22):282−290.] doi: 10.11975/j.issn.1002-6819.2018.22.035 XIE H X, HU Z C, WANG H O, et al. Effect of vacuum freeze-drying methods on retention of volatile flavor compounds of lemon[J]. Transactions of the Chinese Society of Agricultural Engineering, 2018, 34(22): 282−290. doi: 10.11975/j.issn.1002-6819.2018.22.035
[13] ZHAI X T, GRANVOGL M. Characterization of the key aroma compounds in two differently dried Toona sinensis (A. Juss.) Roem. By means of the molecular sensory science concept[J]. Journal of Agricultural and Food Chemistry,2019,67(35):9885−9894. doi: 10.1021/acs.jafc.8b06656
[14] CHENG H, CHEN J, CHEN S, et al. Characterization of aroma-active volatiles in three Chinese bayberry (Myrica rubra) cultivars using GC-MS-olfactometry and an electronic nose combined with principal component analysis[J]. Food Research International,2015,72:8−15. doi: 10.1016/j.foodres.2015.03.006
[15] FENG X, WANG H, WANG Z, et al. Discrimination and characterization of the volatile organic compounds in eight kinds of huajiao with geographical indication of China using electronic nose, HS-GC-IMS and HS-SPME-GC-MS[J]. Food Chemistry,2022,375:131671. doi: 10.1016/j.foodchem.2021.131671
[16] YANG Y, WANG B, FU Y, et al. HS-GC-IMS with PCA to analyze volatile flavor compounds across different production stages of fermented soybean whey tofu[J]. Food Chemistry,2021,346(4):128880.
[17] GAO L L, ZHANG L H, LIU J, et al. Analysis of the volatile flavor compounds of pomegranate seeds at different processing temperatures by GC-IMS[J]. Molecules,2023,28(6):2717. doi: 10.3390/molecules28062717
[18] ALLAFCHIAN A R, MAJIDIAN Z, IELBEIGI V. A novel method for the determination of three volatile organic compounds in exhaled breath by solid-phase microextraction-ion mobility spectrometry[J]. Analytical and Bioanalytical Chemistry,2016,408(3):839−847. doi: 10.1007/s00216-015-9170-8
[19] 孟克迪, 张国治, 王赵改, 等. 基于GC-IMS联用技术分析不同干燥方式对香椿挥发性成分的影响[J]. 轻工学报,2023,38(3):25−34. [MENG K D, ZHANG G Z, WANG Z G, et al. Effect of different drying methods on the volatile components of Toona sinensis on GC-IMS[J]. Journal of Light Industry,2023,38(3):25−34.] doi: 10.12187/2023.03.004 MENG K D, ZHANG G Z, WANG Z G, et al. Effect of different drying methods on the volatile components of Toona sinensis on GC-IMS[J]. Journal of Light Industry, 2023, 38(3): 25−34. doi: 10.12187/2023.03.004
[20] 张乐, 张雅, 史冠莹, 等. GC-IMS结合化学计量学分析8 个产区香椿挥发性成分差异[J]. 食品科学,2022,43(22):301−308. [ZHANG L, ZHANG Y, SHI G Y, et al. Differences in volatile organic compounds of Toona sinensis from eight production regions analyzed by gas chromatography-ion mobility spectrometry combined with chemometrics[J]. Food Science,2022,43(22):301−308.] doi: 10.7506/spkx1002-6630-20220121-214 ZHANG L, ZHANG Y, SHI G Y, et al. Differences in volatile organic compounds of Toona sinensis from eight production regions analyzed by gas chromatography-ion mobility spectrometry combined with chemometrics[J]. Food Science, 2022, 43(22): 301−308. doi: 10.7506/spkx1002-6630-20220121-214
[21] ZHANG L, WANG Z, SHI G, et al. Effects of different thermal processing methods on nutrients and flavor of Toona sinensis[J]. Journal of Food Processing and Preservation,2022,46(7):16691.
[22] LI M Q, YANG R W, ZHANG H, et al. Development of a flavor fingerprint by HS-GC-IMS with PCA for volatile compounds of Tricholoma matsutake Singer[J]. Food Chemistry,2019,290:32−39. doi: 10.1016/j.foodchem.2019.03.124
[23] CHEN J H, TAO L N, ZHANG T, et al. Effect of four types of thermal processing methods on the aroma profiles of acidity regulator treated tilapia muscles using E-nose, HS-SPME-GC-MS, and HSGC-IMS[J]. LWT-Food Science and Technology,2021,147:111585. doi: 10.1016/j.lwt.2021.111585
[24] GUO Y, CHEN D, DONG Y F, et al. Characteristic volatiles fingerprints and changes of volatile compounds in fresh and dried Tricholoma matsutake Singer by HS-GC IMS and HS-SPME-GC-MS[J]. Journal of Chromatography B,2018,1099:46−55.
[25] LIU C J, ZHANG J, ZHOU Z K, et al. Analysis of volatile compounds and identification of characteristic aroma components of Toona sinensis (A. Juss.) Roem. using GC-MS and GC-O[J]. Food and Nutrition Sciences,2013,4(3):305−314. doi: 10.4236/fns.2013.43041
[26] YANG W X, CADWALLADER K R, LIU Y P, et al. Characterization of typical potent odorants in raw and cooked Toona sinensis (A. Juss.) M. Roem. by instrumental-sensory analysis techniques[J]. Food Chemistry,2019,282(1):153−163.
[27] BLOCK E, BAYER T, NAGANATHAN S, et al. Allium chemistry:Synthesis and sigmatropic rearrangements of alk(en)yl 1-propenyl disulfide S-oxides from cutonion and garlic[J]. Journal of the American Chemical Society,1996,118(12):2799−2810. doi: 10.1021/ja953444h
[28] LI J X, EIDMAN K, GAN X W, et al. Identification of (S, S)-γ-Glutamyl-(cis-S-1-propenyl) thioglycine, a naturally occurring norcysteine derivative, from the Chinese vegetable Toona sinensis[J]. Journal of Agricultural and Food Chemistry,2013,61(31):7470−7476. doi: 10.1021/jf401946d
[29] 贾建颖. 香椿γ-谷氨酰胺转肽酶的分离纯化及酶学特性研究[D]. 天津:天津科技大学, 2016. [JIA J Y. Purification and characterisation of a flavor-related enzyme, γ-glutamyl-transpeptidase, fromToona sinensis leaves[D]. Tianjin:Tianjin University of Science and Technology, 2016.] JIA J Y. Purification and characterisation of a flavor-related enzyme, γ-glutamyl-transpeptidase, from Toona sinensis leaves[D]. Tianjin: Tianjin University of Science and Technology, 2016.
[30] 史冠莹, 王晓敏, 赵守涣, 等. 不同产地香椿嫩芽主要营养成分、活性物质及挥发性成分分析[J]. 食品工业科技,2019,40(3):207−215,223. [SHI G Y, WANG X M, ZHAO S H, et al. Analysis of main nutrients, active ingredients and volatile components of Toona sinensis buds from different regions[J]. Science and Technology of Food Industry,2019,40(3):207−215,223.] SHI G Y, WANG X M, ZHAO S H, et al. Analysis of main nutrients, active ingredients and volatile components of Toona sinensis buds from different regions[J]. Science and Technology of Food Industry, 2019, 40(3): 207−215,223.
[31] GREENBERG M J. Characterization of poultry by-product meal flavor volatiles[J]. Journal of Agricultural and Food Chemistry,1981,29(4):831−834. doi: 10.1021/jf00106a038
[32] 胡梓妍, 刘伟, 何双, 等. 基于HS-SPME-GC-MS法分析3 种金橘的香气挥发性成分[J]. 食品科学,2021,42(16):176−184. [HU Z Y, LIU W, HE S, et al. Analysis of volatile components in three varieties of kumquat by headspace solid phase microextraction-gas chromatography-mass spectrometry[J]. Food Science,2021,42(16):176−184.] doi: 10.7506/spkx1002-6630-20200821-290 HU Z Y, LIU W, HE S, et al. Analysis of volatile components in three varieties of kumquat by headspace solid phase microextraction-gas chromatography-mass spectrometry[J]. Food Science, 2021, 42(16): 176−184. doi: 10.7506/spkx1002-6630-20200821-290
[33] 肖作兵, 李静, 牛云蔚, 等. GC-O/AEDA法结合OAV及香气重组试验鉴定玫瑰精油中特征香气化合物[J]. 中国食品学报,2018,18(4):319−324. [XIAO Z B, LI J, NIU Y W, et al. Characterization of the key odorants in rose oil by gas chromatography-olfactometry/aroma extract dilution analysis (AEDA), aroma recombination[J]. Journal of Chinese Institute of Food Science and Technology,2018,18(4):319−324.] XIAO Z B, LI J, NIU Y W, et al. Characterization of the key odorants in rose oil by gas chromatography-olfactometry/aroma extract dilution analysis (AEDA), aroma recombination[J]. Journal of Chinese Institute of Food Science and Technology, 2018, 18(4): 319−324.
[34] 王晓敏, 史冠莹, 王赵改, 等. 不同产地香椿抗氧化活性及挥发性成分的差异分析[J]. 现代食品科技,2020,36(7):271−281. [WANG X M, SHI G Y, WANG Z G, et al. Differences in the antioxidant activities and volatile components of Toona sinensis from different regions[J]. Modern Food Science and Technology,2020,36(7):271−281.] WANG X M, SHI G Y, WANG Z G, et al. Differences in the antioxidant activities and volatile components of Toona sinensis from different regions[J]. Modern Food Science and Technology, 2020, 36(7): 271−281.
[35] YU D X, GUO S, WANG J M, et al. Comparison of different drying methods on the volatile components of ginger (Zingiber officinale Roscoe) by HS-GC-MS coupled with fast GC E-nose[J]. Foods,2022,11:1611. doi: 10.3390/foods11111611
[36] GUO X, SCHWAB W, HO C T, et al. Characterization of the aroma profiles of oolong tea made from three tea cultivars by both GC-MS and GC-IMS[J]. Food Chemistry,2022,376:131933. doi: 10.1016/j.foodchem.2021.131933
[37] 里奥范海默特. 化合物嗅觉阈值汇编[M]. 李智宇, 王凯, 冒德寿, 等, 译. 第二版. 北京:科学出版社, 2018. [VAN GEMERT, L. J. Compilations of odor threshold values (second enlarged and revised edition)[M]. LI Z Y, WANG K, MAO D S, et al. (tanslation). Beijing:The Science Publishing Company, 2018.] VAN GEMERT, L. J. Compilations of odor threshold values (second enlarged and revised edition)[M]. LI Z Y, WANG K, MAO D S, et al. (tanslation). Beijing: The Science Publishing Company, 2018.
[38] 孙宝国, 陈海涛. 食用调香术(第三版)[M]. 北京:化学工业出版社, 2017. [SUN B G, CHEN H T. The technology of food flavoring[M]. Beijing:Chemical Industry Publishing House, 2017.] SUN B G, CHEN H T. The technology of food flavoring[M]. Beijing: Chemical Industry Publishing House, 2017.
[39] ZHAI X T, GRANVOGL M. Key odor-active compounds in raw green and red Toona sinensis (A. Juss.) Roem. and their changes during blanching[J]. Journal of Agricultural and Food Chemistry,2020,68(27):7169−7183. doi: 10.1021/acs.jafc.0c02012
-
期刊类型引用(7)
1. 王琳,李安林,熊双丽,熊得全,唐丹. 红外烤制和微波烤制猪肉品质的对比分析. 食品工业科技. 2024(08): 57-66 .  本站查看
本站查看
2. 王宇临,胡代花,王丹妮,杨旭,孔凡舒,陈小华,陈旺,冯自立. 食用菌不同部位风味物质差异及其对食品风味影响研究进展. 中国调味品. 2024(09): 200-207 .  百度学术
百度学术
3. 邓雅元,华蓉,孙达锋,游金坤,王娟,杨璐敏,代秋琼,曹燕妮. 食用菌风味成分及其检测方法研究. 中国食用菌. 2024(06): 97-103 .  百度学术
百度学术
4. 张扬,集贤,谷旭东,赵茹,张琴,朱志强. 气相色谱-离子迁移谱技术(GC-IMS)在食用菌领域的应用前景分析. 中国食用菌. 2023(06): 1-5+10 .  百度学术
百度学术
5. 何奎,贠建民,毕阳,王睿,毛永强,武淑娟. 纳米膜包装真姬菇贮藏期间挥发性风味成分变化分析. 食品科学. 2021(20): 160-166 .  百度学术
百度学术
6. 曹佳兴,许柠,汪丽萍,张国治. 挤压膨化温度对麸皮回填法制备的全麦挂面风味成分的影响. 河南工业大学学报(自然科学版). 2021(06): 71-79+133 .  百度学术
百度学术
7. 李星仪,张悦,谢永康,于贤龙,朱广飞,高振江,肖红伟,刘嫣红. 热风干燥过程相对湿度对香菇品质的影响. 农业工程学报. 2020(24): 281-291 .  百度学术
百度学术
其他类型引用(3)





 下载:
下载:


 下载:
下载:



