Antioxidative Stress and Anti-aging Effects of Lithocarpus litseifolius folium Based on Caenorhabditis elegans Model
-
摘要: 本研究对木姜叶柯提取物(Lithocarpus litseifolius folium extract,LLFE)的主要成分进行分析,以秀丽隐杆线虫(Caenorhabditis elegans,C. elegans)为模型,评价木姜叶柯(Lithocarpus litseifolius folium)对线虫的抗氧化应激和抗衰老作用,并探讨可能的作用机制。结果表明:木姜叶柯提取物中含总酚52.84±1.45 mg/g,总黄酮380.74±15.12 mg/g,总糖470.36±5.84 mg/g,二氢查尔酮类化合物含量约为6.00%,其中根皮苷含量为52.76±0.71 mg/g,根皮素1.64±0.06 mg/g,三叶苷4.88±0.01 mg/g;LLFE(0.25、1.25 mg/mL)也可以显著延长线虫在氧化应激和热应激条件下的平均寿命(P<0.05),增强自身的抗逆性;后以H2O2诱导的线虫氧化损伤为模型,发现与模型组相比,LLFE(0.05、0.25、1.25 mg/mL)可以显著提升线虫的平均寿命(P<0.05);当LLFE浓度为1.25 mg/mL时,线虫体内总超氧化物歧化酶活提升了39.85%(P<0.05)、过氧化氢酶活提升了39.21%(P<0.05),谷胱甘肽过氧化物酶活提升了66.95%(P<0.001);丙二醛和活性氧的积累量也分别减少66.05%(P<0.001)和49.69%(P<0.001)。表明LLFE有良好的抗氧化效果,进而延缓衰老的进程。Abstract: In this study, the main components of the extract of (Lithocarpus litseifolius folium extract, LLFE) were analyzed,and the anti-oxidative stress and anti-aging effects of LLFE on C.elegans were evaluated using Caenorhabditis elegans (C.elegans) as a model to explore the possible mechanisms of action.The results showed that LLFE contained 52.84±1.45 mg/g of total phenols, 380.74±15.12 mg/g of total flavonoids, 470.36±5.84 mg/g of total sugars and about 6.00% of dihydrochalcone compounds, with phloridzin 52.76±0.71 mg/g, phloretin 1.64±0.06 mg/g and trilobatin 4.88±0.01 mg/g. LLFE (0.25, 1.25 mg/mL) also significantly extended the mean lifespan of C.elegans under oxidative and heat stress conditions (P<0.05) and enhanced their own resistance to stress. After using H2O2-induced oxidative damage in C.elegans as a model, it was found that LLFE (0.05, 0.25 and 1.25 mg/mL) significantly increased the mean lifespan of C.elegans compared with the model group (P<0.05). When the LLFE concentration was 1.25 mg/mL, the total superoxide dismutase activity in C.elegans increased by 39.85% (P<0.05), catalase activity by 39.21%(P<0.05) and glutathione peroxidase activity by 66.95% (P<0.001). The accumulation of malondialdehyde and reactive oxygen species was also reduced by 66.05% (P<0.001) and 49.69% (P<0.001), respectively. This indicates that LLFE has good antioxidant effect, and then delay the process of aging.
-
衰老是一种自发的生物过程,生物体内各组织器官的结构与功能均随年龄增加而不可逆转地衰退[1],这一恶化也成为如糖尿病、心脑血管疾病、神经退行性疾病的主要危险因素[2]。经典的“自由基致衰老学说”被广泛认为是衰老的主要机制。过量的氧自由基干扰正常的代谢信号通路,引发功能蛋白的变性和脂质的过氧化,最终导致细胞结构的破坏,致使机体衰老和死亡[3]。抗氧化剂是延缓衰老的一种重要物质,植物源的天然抗氧化剂成为当前研究的热点,利用天然抗氧化剂研发抗氧化功能性食品和保健品具有重要的现实意义。
木姜叶柯是壳斗科柯属植物,在民间常作为保健凉茶食用,具有清热解毒、降压等功效。2017年,木姜叶柯被批准为新食品原料[4]。现代药理研究表明,木姜叶柯含有多种生物活性物,如二氢查尔酮类化合物,具有抗癌、抗过敏、降脂、降血糖等功效[5-9]。木姜叶柯的体外抗氧化能力已被证实,据报道,Sun等[10]以芦丁和维生素C作为阳性对照,测定了木姜叶柯中根皮苷、三叶苷和根皮素的抗氧化活性,结果显示三种化合物的抗氧化能力均高于芦丁和VC,表明木姜叶柯具有很好的体外抗氧化活性。然而,目前对于木姜叶柯的抗氧化研究多以体外化学法评价为主,而且缺乏抗氧化性和抗衰老的体内评价系统研究。为了揭示木姜叶柯的抗氧化活性成分和抗衰老功效,本研究拟从新鲜木姜叶柯中提取二氢查尔酮并对其种类和含量进行分析,并以秀丽隐杆线虫为模型,评价木姜叶柯对于线虫的抗氧化及延缓寿命作用,分析并探讨其可能的机制,期望为开发木姜叶柯抗衰老功能性食品提供相关的理论依据。
1. 材料与方法
1.1 材料与仪器
木姜叶柯(2021年12月采摘) 由江西省上饶市林业局提供;野生型秀丽隐杆线虫(C.elegans Bristol N2)、尿嘧啶合成缺陷型大肠杆菌(Escherichia coli)OP50 购自上海南方模式生物科技股份有限公司。没食子酸、福林酚试剂、碳酸钠、亚硝酸钠、芦丁、乙醇、硝酸铝、氢氧化钠、浓硫酸、苯酚 国药集团化学试剂有限公司;葡萄糖 江苏强盛功能化学股份有限公司;根皮苷标准品(HPLC≥98%) 上海源叶生物科技有限公司;根皮素标准品(HPLC>98%) 梯希爱化成工业发展有限公司;三叶苷标准品(HPLC=98%) 成都普瑞法科技开发有限公司;BCA蛋白试剂盒、超氧化物歧化酶(Superoxide Dismutase, SOD)、过氧化氢酶(Catalase, CAT)、活性氧(Reactive oxygen species,ROS)、谷胱甘肽过氧化物酶(Glutathione peroxidase,GSH-Px)、丙二醛(malondialdehyde,MDA)试剂盒 南京建成生物技术公司。
e2695高效液相色谱 美国Waters公司;Spectra Max 190酶标仪 美国Molecular Devices公司;SW-CJ超净工作台 无锡易纯净化设备有限公司;TS600DC立式双层摇床 上海天呈实验仪器制造有限公司;LRH-150恒温恒湿培养箱 上海一恒科学仪器有限公司;奥林巴斯SZ680体视显微镜 日本Olympus公司。
1.2 实验方法
1.2.1 木姜叶柯成分的提取
参考罗颖等[11]的方法并略作修改,取木姜叶柯,用水清除其表面杂质放入真空冷冻干燥机中干燥、粉碎、过80目筛。取粉末50 g,加入1 L体积分数为60%的乙醇溶液,于40 ℃,300 W、50 kHz条件下超声105 min,10000 r/min离心20 min,取上清液,在40 ℃条件下减压旋转蒸发,将浓缩液放入真空冷冻干燥机中干燥48 h,得到木姜叶柯提取物(Lithocarpus litseifolius folium extract,LLFE)冻干粉。取LLFE冻干粉,用水溶解,配制成1 mg/mL溶液,用于后述实验。
1.2.2 LLFE中活性成分的测定
1.2.2.1 总酚含量的测定
采用福林酚比色法[12]进行测定,以没食子酸为标准品,根据回归方程y=0.0218x−0.0553(x为没食子酸的浓度,单位μg/mL,y为吸光度,R2=0.9993),计算总酚含量。
1.2.2.2 总黄酮含量的测定
采用硝酸铝-亚硝酸钠显色法[13]进行测定,以芦丁为标准品,根据回归方程y=1.0362x+0.0746(x为芦丁的浓度,单位mg/mL,y为吸光度,R2=0.9989),计算总黄酮含量。
1.2.2.3 总糖含量的测定
采用苯酚-硫酸比色法[14]测定总糖含量,以葡萄糖为标准品,根据回归方程为y=5.7481x+0.0099(x为葡萄糖的浓度,单位mg/mL,y为吸光度,R2=0.9978),计算总糖含量。
1.2.2.4 根皮素、根皮苷和三叶苷含量的测定
参考Huang等[15]的方法并略作修改,称取一定质量的标准品,并溶解在40%甲醇中得到根皮苷(100 μg/mL)、三叶苷(10 μg/mL)及根皮素(1 μg/mL)的标准品储备液。取1.2.1的LLFE冻干粉10 mg,用40%的甲醇溶解,配制成1 mg/mL溶液,过0.22 μm滤膜,用于高效液相色谱检测。色谱条件:色谱柱为XBbridge®C18(4.6 mm×250 mm,5 μm),流动相组成为A:0.01%甲酸水溶液,B:乙腈;检测波长:285 nm;流速:1 mL/min;柱温:40 ℃;进样量:10 μL;梯度洗脱程序:0~17 min:30%~40%B;17~25 min:40%~30%B。
1.2.3 线虫的培养
取300 μL E.coli OP50菌液至线虫生长培养基(Nematode Growth Medium,NGM)平板上,均匀涂布,37 ℃培养12 h后,切割培养有线虫的培养基,将培养基倒置于上述平板上,放入20 ℃培养箱中培养。
NGM培养基配方:氯化钠3 g,蛋白胨2.5 g,琼脂粉17 g,加入975 mL蒸馏水,121 ℃灭菌30 min,待培养基降温至60 ℃,加入胆固醇乙醇溶液1 mL(5 mg/mL)、硫酸镁1 mL(1 mol/L)、氯化钙1 mL(1 mol/L)和1 mol/L磷酸钾缓冲液25 mL(pH6.0)。
1.2.4 线虫的同期化
参考Meng等[16]的方法并略作修改,取处于产卵期的秀丽隐杆线虫培养皿,加入5 mL M9缓冲液冲洗,并将其转移至离心管中,2000 r/min离心1 min,弃上清液,反复冲洗2~3次。去上清液后加入1~2 mL裂解液,涡旋5 min,加入5 mL M9缓冲液终止裂解,2000 r/min离心1 min,去除上清液,保留底部沉淀,沉淀继续用M9缓冲液冲洗2~3次。将含有线虫虫卵的M9缓冲液滴于涂有新鲜E.coli OP50菌液的NGM平板上,置于20 ℃培养,即可得到同期化线虫。M9缓冲液配方:磷酸氢二钠6 g/L,磷酸二氢钾3 g/L,氯化钠5 g/L,七水硫酸镁0.25 g/L。
1.2.5 线虫的毒性实验
参考Hu等[17]的方法并略作修改,使LLFE溶液的最终浓度为0.01、0.05、0.25、1.25、6.25、10 mg/mL,以M9缓冲液为参比对照,20 ℃下,将同期化线虫转移至含有不同浓度LLFE的24孔板中,每孔10条线虫,记录每小时的活虫数,计算24 h后线虫的存活率,每个浓度重复3次。
1.2.6 线虫的压力应激实验
1.2.6.1 线虫氧化应激实验
参考Liu等[18]的方法,并略作修改。将同期化的L4期线虫转移至NGM给药板中(LLFE终浓度为0.05、0.25、1.25 mg/mL),其中对照组仅含E.coli OP50菌液。每组30条线虫,20 ℃给药培养48 h后,将各组线虫转移至24孔板中,记为氧化应激实验的第0 h,其中孔内含终浓度为5 mmol/L H2O2,每隔0.5 h观察线虫存活及死亡数目并记录,直至线虫全部死亡。
1.2.6.2 线虫热应激实验
参考Liu等[18]的方法,并略作修改。线虫热应激实验分组同1.2.6.1,将给药处理后的线虫置于37 ℃恒温培养箱中,每隔2 h记录线虫存活及死亡数目,直到线虫全部死亡,实验重复3次。
1.2.7 LLFE对急性氧化应激条件下线虫的影响
1.2.7.1 实验分组及处理
将NGM培养基分为3组:正常NGM(空白对照组),含H2O2的NGM(模型组)、含H2O2及LLFE溶液(浓度分别为0.05、0.25、1.25 mg/mL)的NGM给药组。所有培养基配制时需加入五氟尿嘧啶(5-Fluorouracil),其终浓度为25 μg/mL,且H2O2的终浓度均为2 mmol/L。每个平板约含500条同期化处理的L4期线虫,并置于20 ℃培养箱中培养,以待后续实验。
1.2.7.2 线虫的寿命实验
参考Rathor等[19]的方法并略作修改,线虫分组同1.2.7.1所述,将同期化的L4期线虫(虫龄4 d)转移至上述3组NGM板中。每个平板含40条线虫,置于20 ℃恒温培养箱中培养,记为寿命试验的第0 d。每间隔24 h记录线虫的存活、死亡、删失数目,直至线虫全部死亡(死亡及删失标准:刺激或轻微触碰线虫均无反应,即为死亡;线虫钻入培养基中、丢失、爬壁、生殖道外翻均不计入统计数据,即为删失)。
1.2.7.3 线虫匀浆液的制备
参照Li等[20]的方法并略作修改,线虫分组处理同1.2.7.1所述,待线虫给药处理4 d后,将3组NGM培养基上的线虫用M9缓冲液冲洗下来,置于15 mL离心管中,4 ℃,4000 r/min离心5 min,去除上清液,冲洗2~3次,加入1 mL M9缓冲液重悬线虫,并于冰浴条件下超声破碎2 min。超声条件如下:超声功率400 W,4 ℃,超声2 s,间隔2 s。于4 ℃,12000 r/min离心10 min,得到组织匀浆上清液,取上清液立即进行蛋白浓度测定及酶活分析。实验重复3次。
1.2.7.4 线虫体内活性氧(ROS)含量的测定
参考王高坚等[21]的方法,线虫分组处理同1.2.7.1所述。将各组线虫转移至96孔板中,每孔5条。孔内预先加入200 μL M9缓冲液,每孔加入终浓度25 μmol/L的活性氧荧光探针(2',7'-Dichlorodihydrofluorescein diacetate,DCFH-DA)溶液,37 ℃避光反应,采用多功能酶标仪于激发波长485 nm,发射波长530 nm处测定荧光值。每间隔20 min检测1次,共反应3 h,每次读数前振荡。实验重复3次。
1.2.7.5 酶活及代谢产物含量的测定
对于组织匀浆上清液,按照南京建成试剂盒说明书测定蛋白浓度、SOD、CAT、GSH-Px的酶活力水平及MDA含量。实验重复3次。
1.3 数据统计与分析
所有数据均以平均值±标准偏差表示,统计分析选用GraphPad Prism 8软件。采用Duncan,s检验进行多组间显著性分析,P<0.05认为有统计学显著性意义。
2. 结果与分析
2.1 LLFE活性成分测定
LLFE冻干粉中总酚、总黄酮及总糖含量见表1,可以看出,LLFE冻干粉总酚含量为52.84±1.45 mg/g,总黄酮的含量为380.74±15.12 mg/g,总糖的含量为470.36±5.84 mg/g。
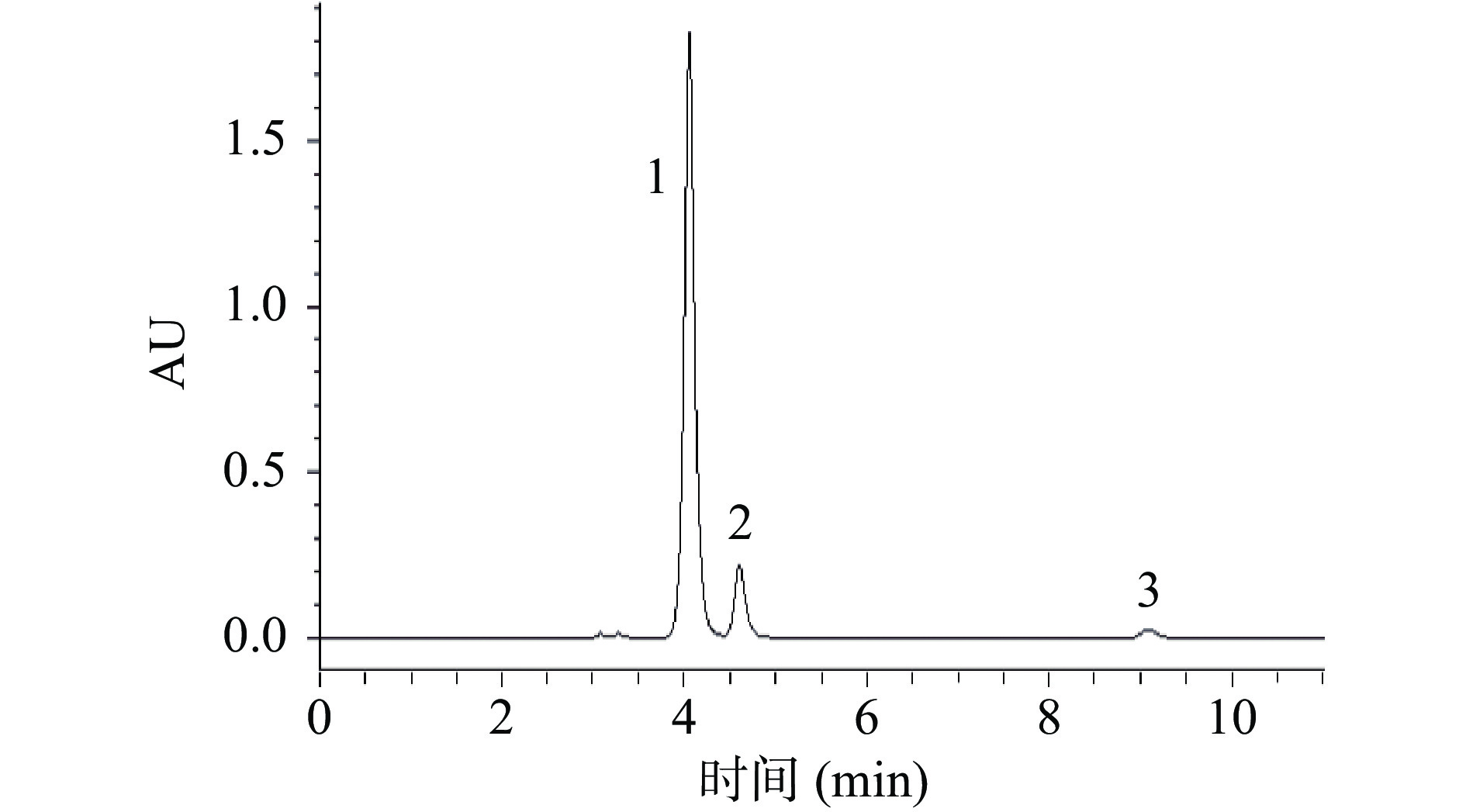
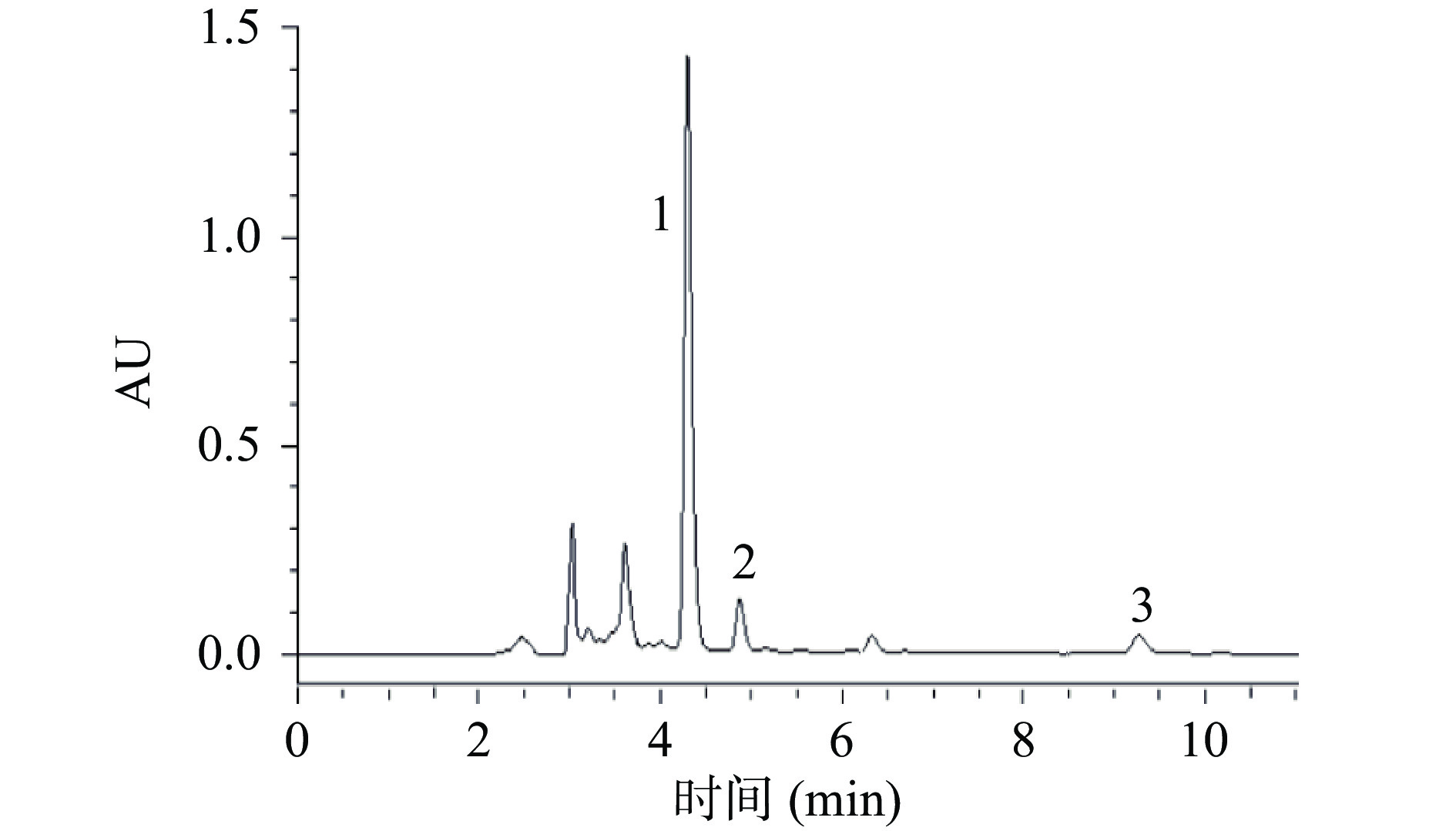
表 1 LLFE中总酚、黄酮、总糖含量Table 1. Contents of total phenols, flavonoids and total sugars in the extract of LLFE成分 含量(mg/g) 总酚 52.84±1.45 总黄酮 380.74±15.12 总糖 470.36±5.84 采用HPLC法对LLFE中的二氢查尔酮进行定量分析,从图1、图2可以看出二氢查尔酮中的根皮苷、三叶苷和根皮素能很好地分离,从表2可以看出1 g LLFE冻干粉中根皮苷、根皮素、三叶苷的含量分别为52.76±0.71、1.64±0.06、4.88±0.01 mg/g。王钰等[22]研究表明,木姜叶柯在整个生命周期中,有效成分会发生转化,其中4~8月采摘的木姜叶柯中,根皮苷的含量逐渐增加(0.74%~6.26%),三叶苷含量逐渐降低(17.14%~0.20%)、根皮素的含量逐渐降低至0(0.42%~0.00%)。赵艳敏等[23]研究表明,天然根皮苷主要来源于苹果,叶子中平均含量达16.31 mg/g,而苹果皮中根皮苷含量大约为825 μg/g[24]。相比之下,木姜叶柯含有极其丰富的根皮苷,具有成为开发根皮苷提取物的资源优势。
表 2 LLFE中总二氢查尔酮种类及含量Table 2. Dihydrochalcone species and content in extract of LLFE二氢查尔酮种类 保留时间(min) 含量(mg/g) 根皮苷 4.27 52.76±0.71 根皮素 4.84 1.64±0.06 三叶苷 9.19 4.88±0.01 2.2 毒性实验
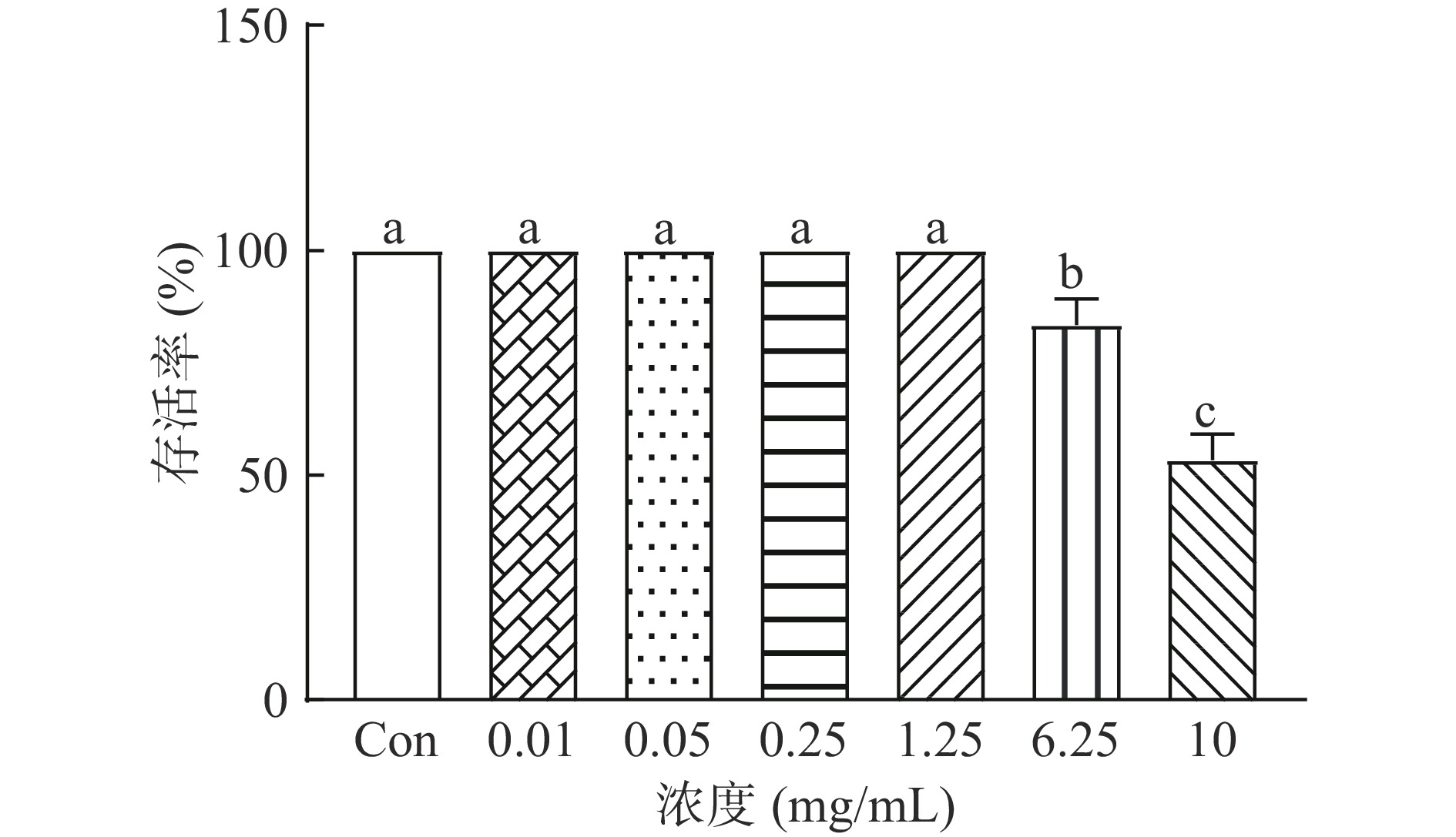
LLFE溶液的毒性实验结果如图3所示,相较于空白对照组,LLFE溶液的浓度为0.01、0.05、0.25和1.25 mg/mL时,对秀丽隐杆线虫存活率无显著影响。因此,在之后的实验中,所用的培养基中LLFE的终浓度为0.05、0.25和1.25 mg/mL。
2.3 线虫的压力应激实验
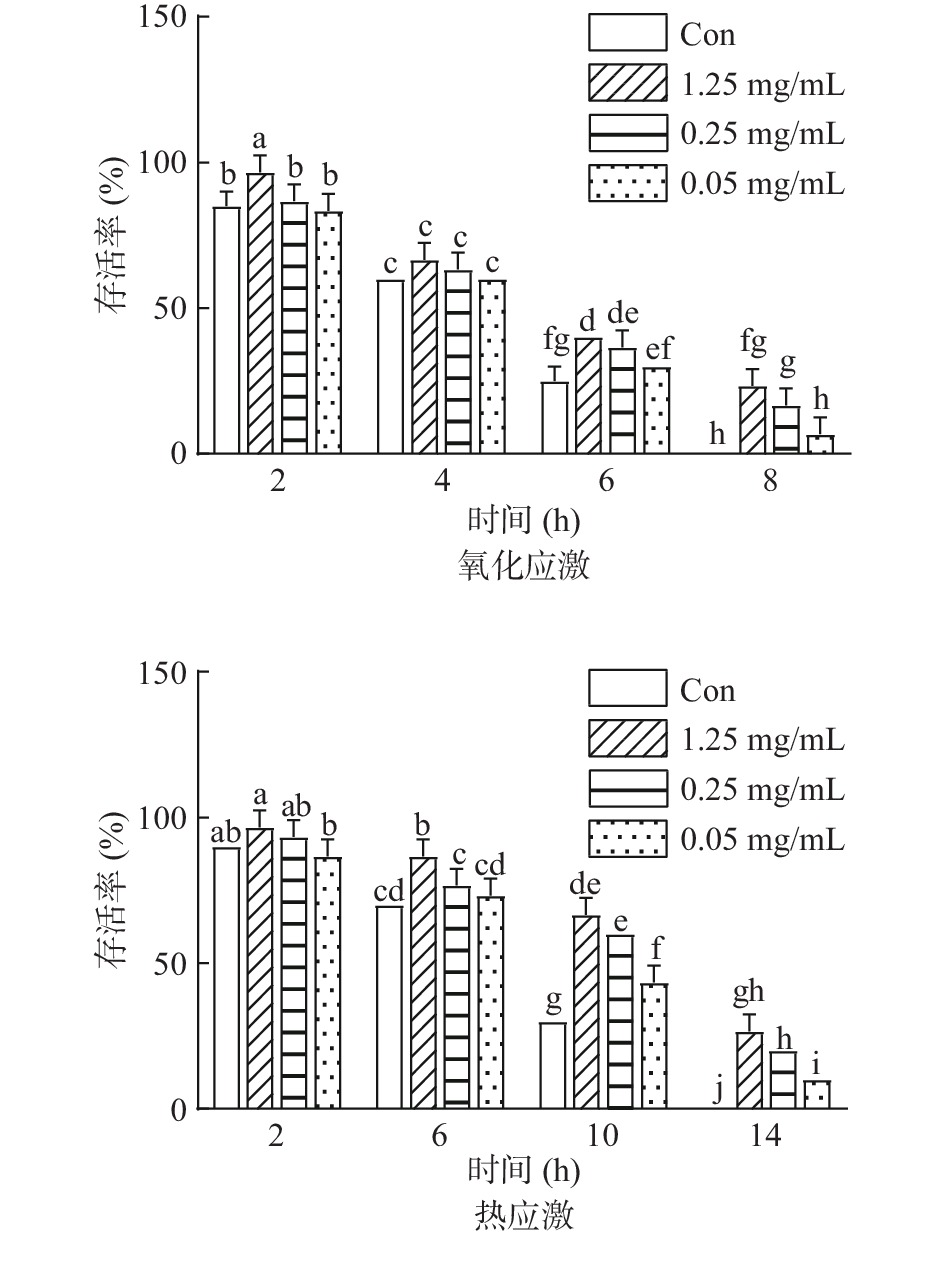
正常代谢条件下,线虫体内ROS含量处于动态平衡状态,当机体受到外界压力刺激时,会造成氧化还原系统的失衡,产生过多的活性氧等自由基,诱导细胞或组织损伤,进而导致机体死亡[25];线虫抵抗压力应激能力与其寿命密切相关[26-27]。为了进一步评价木姜叶柯提取液的抗逆性,测定了线虫对氧化应激和热应激的抗性。图4、表3结果显示,在氧化应激实验中,空白对照组线虫于8 h全部死亡,此时,0.05、0.25、1.25 mg/mL LLFE组线虫存活率分别为6.67%、16.67%和23.33%(P<0.05);在热应激实验中,空白对照组线虫于14 h全部死亡,0.25、1.25 mg/mL给药组,线虫的平均寿命分别提高至10.87±0.36、11.53±0.99 h,具有统计学意义(P<0.05)。以上结果表明LLFE可以增强线虫在不良环境下的抵抗压力应激的能力,延缓线虫的衰老。据报道,总酚及总黄酮是植物组织中广泛存在的次生代谢物,具有优良的抗氧化和自由基清除能力[28]。线虫在氧化应激条件下抗逆性的增强可能与LLFE中大量的酚类及黄酮类化合物有关,这些活性物质可以保持线虫细胞核形态的完整性,维持线粒体生物合成等生理功能,从而提高线虫在不良环境下的存活率。
表 3 压力应激下LLFE对线虫平均寿命的影响Table 3. Effect of LLFE on the mean lifespan of C. elegans under stress组别 平均寿命(h) 氧化应激 热应激 Con 4.63±0.36a 8.53±0.88b 0.05 mg/mL 4.78±0.35bc 9.47±0.72b 0.25 mg/mL 5.25±0.26ab 10.87±0.36a 1.25 mg/mL 5.57±0.40a 11.53±0.99a 注:Con为空白对照组,不同英文字母表示各剂量组之间存在显著性差异(P<0.05),相同字母表示各剂量组之间不存在显著性差异(P>0.05)。 2.4 LLFE对急性氧化应激下线虫的影响
2.4.1 LLFE对线虫寿命的影响
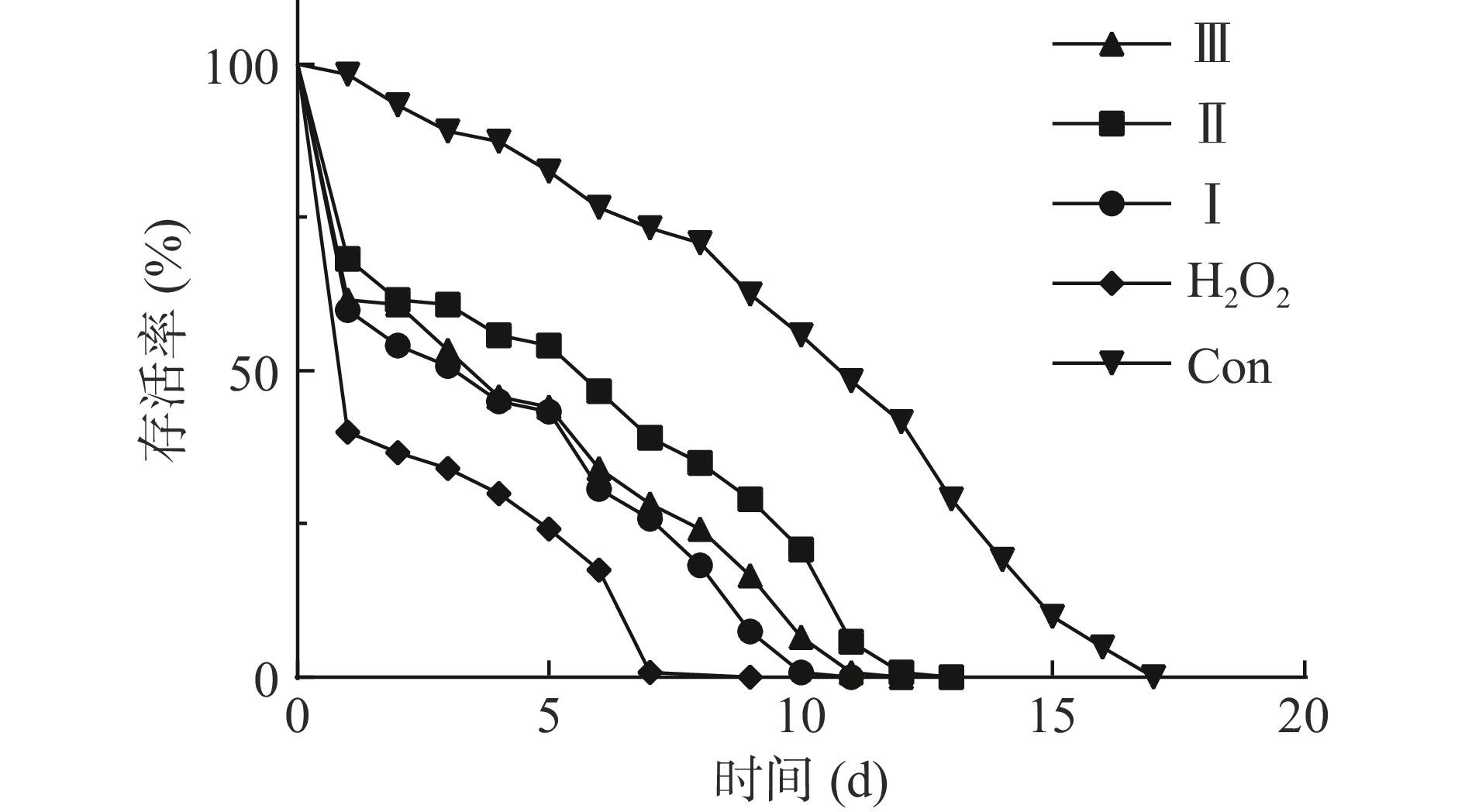
衰老时机体细胞内部环境稳态渐趋下降,大量活性氧累积会严重破坏细胞结构,影响细胞的生物分子功能,因此评估活性氧自由基对于寿命和衰老的影响具有十分重要的意义[29]。过氧化氢作为细胞内最常见的活性氧,会引起细胞膜脂质过氧化,从而产生氧化损伤,本文利用过氧化氢诱导建立秀丽隐杆线虫的氧化损伤模型,研究LLFE对线虫氧化应激的反应,从图5、表4可以看出经过氧化氢(不给药)处理后,线虫平均寿命比空白对照组缩短了72.76%,相较于模型组,不同浓度LLFE(0.05、0.25、1.25 mg/mL)给药处理后,线虫的生存曲线均右移,线虫的最大寿命分别延长至10.33±0.47、12.33±0.47和11.33±0.47 d,平均寿命也有了显著的提升(P<0.05)。Liu等[18]研究表明香菇多糖抗逆性增强归因于线虫DAF-16和SKN-1的表达,从而延长线虫寿命和保护线虫免受氧化应激的影响,Li等[30]研究表明三叶苷的抗氧化应激活性依赖于线虫体内DAF-16和SKN-1信号通路的选择性激活,从而调节包括衰老和寿命在内的各种生理功能。因此,推测LLFE的延缓衰老和抗氧化应激能力的增强可能与DAF-16的激活有关。
表 4 急性氧化应激下LLFE对线虫寿命的影响Table 4. The effect of LLFE on the lifespan of C.elegans under acute oxidative stress组别 平均寿命(d) 最大寿命(d) Con组 10.43±0.1a 17a Ⅰ 4.37±0.07d 10.33±0.47c Ⅱ 5.78±0.07b 12.33±0.47b Ⅲ 4.77±0.05c 11.33±0.47bc H2O2组 2.84±0.04e 7.67±0.94d 注:Con:空白对照组;Ⅰ:H2O2+0.05 mg/mL LLFE;Ⅱ:H2O2+0.25 mg/mL LLFE;Ⅲ:H2O2+1.25 mg/mL LLFE;H2O2组:模型组;不同英文字母表示各剂量组之间存在显著性差异(P<0.05),相同字母表示各剂量组之间不存在显著性差异(P>0.05)。图6同。 2.4.2 LLFE对线虫体内ROS的影响
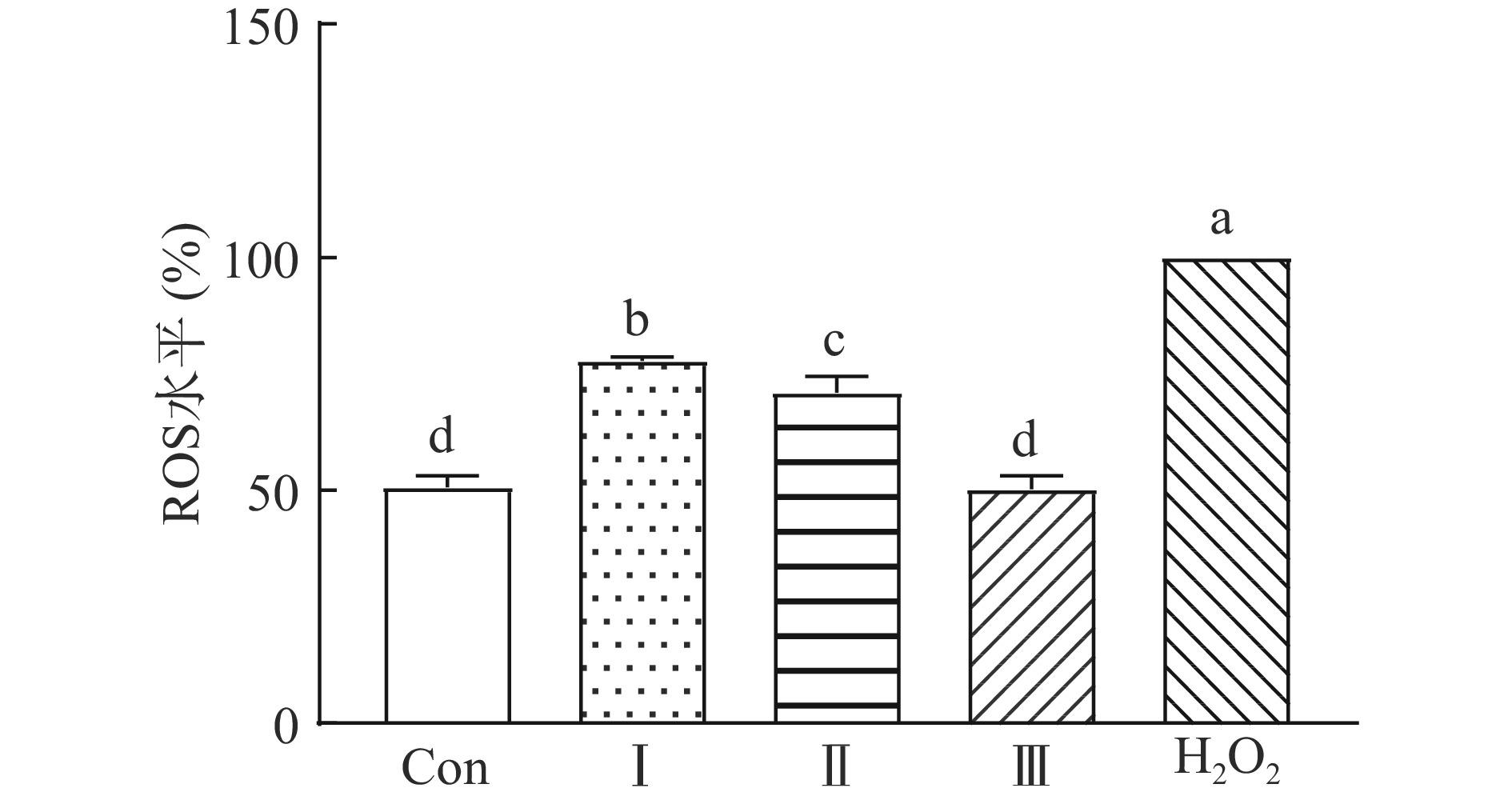
衰老是多重因素共同作用的结果,但多数研究表明与衰老相关的大多疾病都与体内ROS水平的异常升高有关[31]。过量的ROS异常堆积,产生细胞毒性是缩短线虫寿命的重要原因[32-34]。在本研究利用H2O2诱导秀丽隐杆线虫,机体通过酶系统与非酶系统产生氧自由基,致线虫体内ROS含量增加,从图6可以看出,模型组与空白对照组差异显著,表明造模成功。相较于模型组,不同浓度LLFE(0.05、0.25、1.25 mg/mL)处理后的给药组可以显著降低DCFH-DA的荧光强度(P<0.05),三种浓度下分别减少了22.29%、29.14%和49.69%。综上可知LLFE可以降低线虫在氧化应激条件下ROS的水平,而较低的ROS水平可能对延长秀丽隐杆线虫寿命及增强抗氧化应激能力有积极的作用。
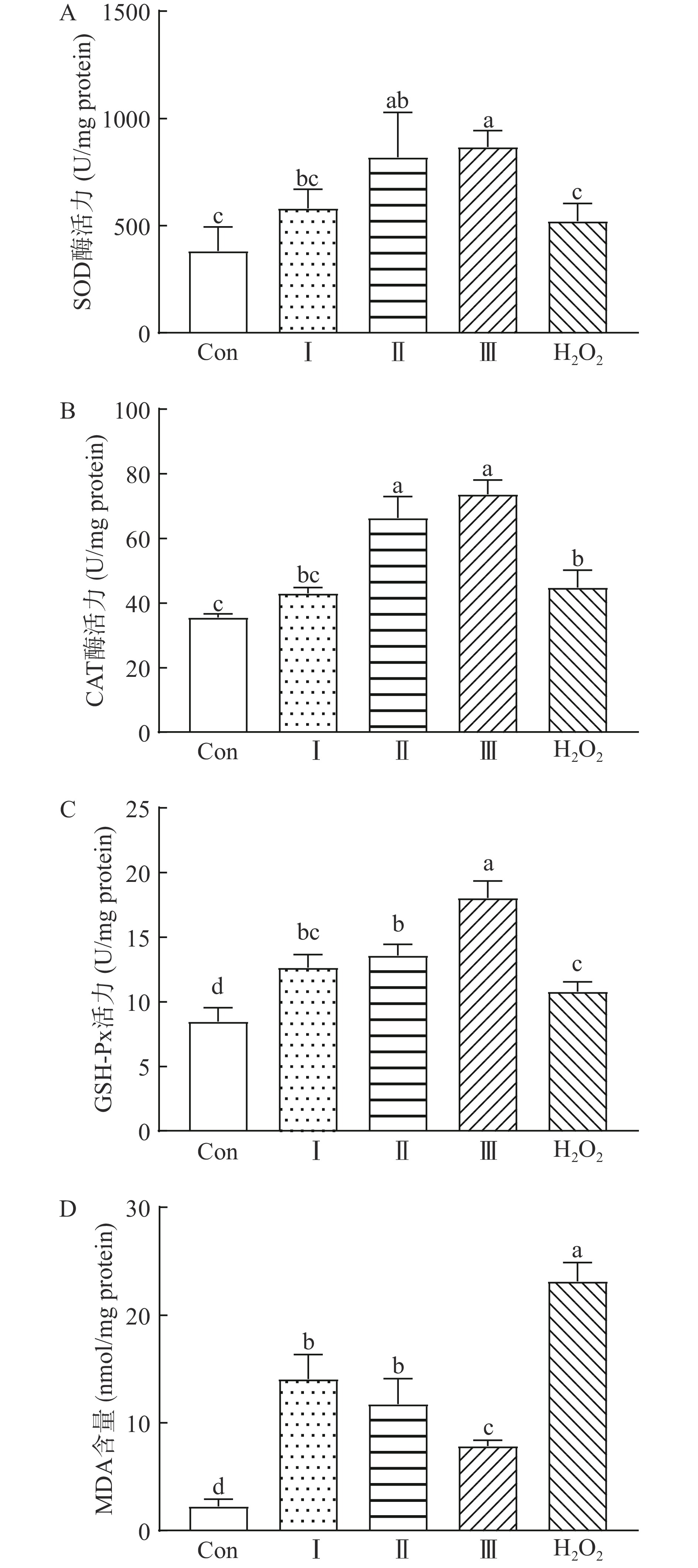
2.4.3 LLFE对线虫体内抗氧化酶系及丙二醛含量的影响
超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GSH-Px)及MDA含量对于维持生物体内平衡十分重要,是评价抗氧化能力的重要指标。由图7A-C可知模型组比空白对照组酶活性高,原因可能是H2O2易穿透细胞膜,胞外H2O2含量的提高促使胞内H2O2含量升高而导致应激反应增强[35],这是线虫的一种自我保护机制,通过提高抗氧化酶的活性来清除体内过多的自由基。谭翠等[36]研究表明当线虫受到H2O2氧化应激损伤时,其模型组SOD和CAT活性均高于空白对照组,与本实验结果基本一致。LLFE溶液的浓度与抗酶活性之间也存在剂量-反应关系,其中,较模型组,浓度为0.05、0.25 mg/mL的LLFE溶液分别将线虫体内SOD活性提高了10.27%、36.42%;当LLFE浓度为1.25 mg/mL时SOD活性最高,SOD活性提高了39.85%(P<0.05);浓度为0.25、1.25 mg/mL的LLFE溶液也分别显著地将CAT活性提高了32.60%、39.21%(P<0.05),显著地将GSH-Px活性提高了25.73%(P<0.05)、66.95%(P<0.001)。黄酮类化合物是LLFE的主要活性成分之一,具有极强的抗氧化性,可以通过提高线虫体内SOD酶活来清除线虫体内过多的自由基,使得H2O2在CAT的作用下分解成氧和水而减轻线虫的氧化损伤[37-39];GSH-Px活性的提高也可以催化H2O2以及许多有机过氧化物,产生水或有机醇,以减弱活性氧对线虫的损害[40]。由图7D可知浓度为0.25、1.25 mg/mL的LLFE溶液可以显著降低线虫体内MDA含量,相比于模型组分别下降了49.19%、66.05%(P<0.05),说明在急性氧化应激条件下,LLFE可以降低线虫脂质过氧化程度。马娜等[41]测定了根皮苷对高血脂症仓鼠体内抗氧化酶和脂质过氧化产物丙二醛的影响,结果表明根皮苷能明显降低MDA的含量,提高SOD和CAT的活性。
基于以上研究结果,可以得出木姜叶柯中丰富的总酚、总黄酮和二氢查尔酮物质,可以通过提高机体抗氧化酶SOD、CAT、GPx活力,有效地降低MDA含量,起到了抗氧化和抗衰老的作用。
3. 结论
木姜叶柯中含有丰富的酚类、黄酮类化合物和二氢查尔酮等抗氧化活性成分。以秀丽隐杆线虫为模型,采用H2O2诱导的氧化损伤线虫模型,探究木姜叶柯的抗氧化及抗衰老功效,结果表明木姜叶柯有效延长了线虫的寿命;压力应激实验表明,LLFE干预线虫后,对H2O2及热应激损伤都有一定的保护作用;较模型组,浓度为1.25 mg/mL的LLFE溶液将线虫体内SOD活性提高了39.85%,CAT活性提高了39.21%(P<0.05),并显著地将GSH-Px活性提高了66.95%(P<0.001)。另外,浓度为1.25 mg/mL的LLFE溶液显著降低线虫体内MDA含量,相比于模型组下降了66.05%(P<0.05),DCFH-DA的荧光强度也降低了49.69%(P<0.05)。LLFE的干预减轻了H2O2对线虫的氧化损伤,从而增强了线虫的抗逆性。基于线虫的体内实验结果证实了木姜叶柯的抗氧化、抗衰老特性,其抗氧化机制可能与提升生物体内抗氧化酶活有关,木姜叶柯有望成为一种天然抗氧化剂和功能性食品。揭示木姜叶柯在氧化应激环境中保护线虫的具体机制,阐明其潜在的分子靶点还需要进一步研究。
-
表 1 LLFE中总酚、黄酮、总糖含量
Table 1 Contents of total phenols, flavonoids and total sugars in the extract of LLFE
成分 含量(mg/g) 总酚 52.84±1.45 总黄酮 380.74±15.12 总糖 470.36±5.84 表 2 LLFE中总二氢查尔酮种类及含量
Table 2 Dihydrochalcone species and content in extract of LLFE
二氢查尔酮种类 保留时间(min) 含量(mg/g) 根皮苷 4.27 52.76±0.71 根皮素 4.84 1.64±0.06 三叶苷 9.19 4.88±0.01 表 3 压力应激下LLFE对线虫平均寿命的影响
Table 3 Effect of LLFE on the mean lifespan of C. elegans under stress
组别 平均寿命(h) 氧化应激 热应激 Con 4.63±0.36a 8.53±0.88b 0.05 mg/mL 4.78±0.35bc 9.47±0.72b 0.25 mg/mL 5.25±0.26ab 10.87±0.36a 1.25 mg/mL 5.57±0.40a 11.53±0.99a 注:Con为空白对照组,不同英文字母表示各剂量组之间存在显著性差异(P<0.05),相同字母表示各剂量组之间不存在显著性差异(P>0.05)。 表 4 急性氧化应激下LLFE对线虫寿命的影响
Table 4 The effect of LLFE on the lifespan of C.elegans under acute oxidative stress
组别 平均寿命(d) 最大寿命(d) Con组 10.43±0.1a 17a Ⅰ 4.37±0.07d 10.33±0.47c Ⅱ 5.78±0.07b 12.33±0.47b Ⅲ 4.77±0.05c 11.33±0.47bc H2O2组 2.84±0.04e 7.67±0.94d 注:Con:空白对照组;Ⅰ:H2O2+0.05 mg/mL LLFE;Ⅱ:H2O2+0.25 mg/mL LLFE;Ⅲ:H2O2+1.25 mg/mL LLFE;H2O2组:模型组;不同英文字母表示各剂量组之间存在显著性差异(P<0.05),相同字母表示各剂量组之间不存在显著性差异(P>0.05)。图6同。 -
[1] 孙晓康, 张艳艳, 张晓元, 等. 衰老机制及抗衰老治疗的研究进展[J]. 食品与药品,2022,24(1):74−80. [SUN X K, ZHANG Y Y, ZHANG X Y, et al. Research progress of aging mechanism and anti-aging treatment[J]. Food and Drugs,2022,24(1):74−80. SUN X K, ZHANG Y Y, ZHANG X Y, et al. Research progress of aging mechanism and anti-aging treatment[J]. Food and Drugs, 2022, 24(1): 74-80.
[2] LÓPEZ-OTÍN C, BLASCO M A, PARTRIDGE L, et al. The hallmarks of aging[J]. Cell,2013,153(6):1194−1217. doi: 10.1016/j.cell.2013.05.039
[3] 杨善岚, 吴磊, 涂嘉欣, 等. 自由基致衰老的研究进展[J]. 中华疾病控制杂志,2022,26(5):589−594. [YANG S L, WU L, TU J X, et al. Advances in the study of free radicals in aging[J]. Chinese Journal of Disease Control,2022,26(5):589−594. doi: 10.16462/j.cnki.zhjbkz.2022.05.017 YANG S L, WU L, TU J X, et al. Advances in the study of free radicals in aging[J]. Chinese Journal of Disease Control, 2022, 26(5): 589-594. doi: 10.16462/j.cnki.zhjbkz.2022.05.017
[4] SHANG A, LIU H Y, LUO M, et al. Sweet tea (Lithocarpus polystachyus Rehd. ) as a new natural source of bioactive dihydrochalcones with multiple health benefits[J]. Critical Reviews in Food Science and Nutrition,2020:1−18.
[5] LI S, ZENG J, WU Q, et al. Antioxidant and hepatoprotective effects of Lithocarpus polystachyus against carbon tetrachloride-induced injuries in rat[J]. Bangladesh Journal of Pharmacology,2013,8(4):420−427.
[6] MIN J, LI X, HUANG K, et al. Phloretin induces apoptosis of non-small cell lung carcinoma A549 cells via JNK1/2 and p38 MAPK pathways[J]. Oncology Reports,2015,34(6):2871−2879. doi: 10.3892/or.2015.4325
[7] ZHANG W, CHEN S, FU H, et al. Hypoglycemic and hypolipidemic activities of phlorizin from Lithocarpus polystachyus Rehd in diabetes rats[J]. Food Science & Nutrition,2021,9(4):1989−1996.
[8] LU M, KONG Q, XU X, et al. Evaluation of apoptotic and growth inhibitory activity of phloretin in BGC823 gastric cancer cell[J]. Tropical Journal of Pharmaceutical Research,2015,14(1):27−31. doi: 10.4314/tjpr.v14i1.5
[9] HOU S, CHEN S, HUANG S, et al. The hypoglycemic activity of Lithocarpus polystachyus Rehd leaves in the experimental hyperglycemic rats[J]. Journal of Ethnopharmacology,2011,138(1):142−149. doi: 10.1016/j.jep.2011.08.067
[10] SUN Y S, LI W, LIU Z B. Preparative isolation, quantification and antioxidant activity of dihydrochalcones from sweet tea (Lithocarpus polystachyus Rehd. )[J]. Journal of Chromatography B,2015,1002:372−378. doi: 10.1016/j.jchromb.2015.08.045
[11] 罗颖, 黄帅, 杨雪彬, 等. 木姜叶柯老叶根皮苷的抗氧化及抑菌活性研究[J]. 中国食品添加剂,2021,32(2):51−57. [LUO Y, HUANG S, YANG X B, et al. Study on the antioxidant and antibacterial activities of the phloridzin of the old leaves of Lithocarpus polystachyus Rehd[J]. China Food Additives,2021,32(2):51−57. LUO Y, HUANG S, YANG X B, et al. Study on the antioxidant and antibacterial activities of the phloridzin of the old leaves of Lithocarpus polystachyus Rehd[J]. China Food Additives, 2021, 32(2): 51-57.
[12] 范昊安, 薛淑龙, 王高坚, 等. 紫苏叶酵素发酵过程中代谢产物与抗氧化活性研究[J]. 中国酿造,2019,38(9):148−154. [FAN H A, XUE S L, WANG G J, et al. Study on metabolites and antioxidant activity of perilla leaf enzymes during fermentation[J]. China Brewing,2019,38(9):148−154. FAN H A, XUE S L, WANG G J, et al. Study on metabolites and antioxidant activity of perilla leaf enzymes during fermentation[J]. China Brewing, 2019, 38(9): 148-154.
[13] 杨小慧, 石光波, 拜晓彬, 等. 文冠果落果黄酮成分分析及抑菌性评价[J]. 食品科学,2018,39(10):53−58. [YANG X H, SHI G B, BAI X B, et al. Analysis of flavonoid composition and evaluation of antibacterial properties of deciduous fruits of Ficus wenge[J]. Food Science,2018,39(10):53−58. YANG X H, SHI G B, BAI X B, et al. Analysis of flavonoid composition and evaluation of antibacterial properties of deciduous fruits of Ficus wenge[J]. Food Science, 2018, 39(10): 53-58.
[14] 金瑾, 刘延奇, 秦令祥. 蒸汽爆破辅助提取莼菜多糖及苯酚-硫酸法测定其多糖含量的研究[J]. 粮食与油脂,2022,35(5):116−120. [JIN J, LIU Y Q, QIN L X. Steam blast-assisted extraction of polysaccharides fromUlva lactuca and determination of its polysaccharide content by phenol-sulfuric acid method[J]. Grain and Oil,2022,35(5):116−120. JIN J, LIU Y Q, QIN L X. Steam blast-assisted extraction of polysaccharides from Ulva lactuca and determination of its polysaccharide content by phenol-sulfuric acid method[J]. Grain and Oil, 2022, 35(5): 116-120.
[15] HUANG W, ZHANG C, GU Z, et al. Effect of microbial fermentation on the sensory characteristics and chemical compositions of Chinese sweet tea (Lithocarpus litseifolius (Hance) Chun)[J]. Food Bioscience,2022,46:101567. doi: 10.1016/j.fbio.2022.101567
[16] MENG F, LI J, WANG W, et al. Gengnianchun, a traditional Chinese medicine, enhances oxidative stress resistance and lifespan in Caenorhabditis elegans by modulating daf-16/FOXO[J]. Evidence-Based Complementary and Alternative Medicine, 2017, 2017.
[17] HU Q, LIU Z, GUO Y, et al. Antioxidant capacity of flavonoids from Folium Artemisiae argyi and the molecular mechanism in Caenorhabditis elegans[J]. Journal of Ethnopharmacology,2021,279:114398. doi: 10.1016/j.jep.2021.114398
[18] LIU H, WANG Y, ZHANG W, et al. Lentinan extends lifespan and increases oxidative stress resistance through DAF-16 and SKN-1 pathways in Caenorhabditis elegans[J]. International Journal of Biological Macromolecules,2022,202:286−295. doi: 10.1016/j.ijbiomac.2022.01.071
[19] RATHOR L, PANT A, NAGAR A, et al. Trachyspermum ammi L. (Carom) oil induces alterations in SOD-3, GST-4 expression and prolongs lifespan in Caenorhabditis elegans[J]. Proceedings of the National Academy of Sciences, India Section B:Biological Sciences,2017,87(4):1355−1362. doi: 10.1007/s40011-016-0710-6
[20] LI Y, CHU Q, LIU Y, et al. Radix Tetrastigma flavonoid ameliorates inflammation and prolongs the lifespan of Caenorhabditis elegans through JNK, p38 and Nrf2 pathways[J]. Free Radical Research,2019,53(5):562−573. doi: 10.1080/10715762.2019.1613534
[21] 王高坚, 王珍珍, 李嘉嘉, 等. 蓝莓酵素的体外抗氧化及对秀丽隐杆线虫的氧化应激保护作用[J]. 食品工业科技,2021,42(15):343−350. [WANG G J, WANG Z Z, LI J J, et al. In vitro antioxidant and protective effects of blueberry enzymes against oxidative stress in Caenorhabditis elegans[J]. Food Industry Science and Technology,2021,42(15):343−350. WANG G J, WANG Z Z, LI J J, et al. In vitro antioxidant and protective effects of blueberry enzymes against oxidative stress in Caenorhabditis elegans[J]. Food Industry Science and Technology, 2021, 42(15): 343-350.
[22] 王钰, 王磊, 张东星, 等. 高效液相色谱法测定木姜叶柯中根皮苷、三叶苷和根皮素的含量[J]. 天津科技,2019,46(7):66−68,70. [WANG Y, WANG L, ZHANG D Xngxing, et al. Determination of phloridzin, trilobatin and phloretin in Lithocarpus litseifolius folium by high performance liquid chromatography[J]. Tianjin Science and Technology,2019,46(7):66−68,70. doi: 10.3969/j.issn.1006-8945.2019.07.023 WANG Y, WANG L, ZHANG D Xngxing, et al. Determination of phloridzin, trilobatin and phloretin in Lithocarpus litseifolius folium by high performance liquid chromatography[J]. Tianjin Science and Technology, 2019, 46(7): 66-68, 70. doi: 10.3969/j.issn.1006-8945.2019.07.023
[23] 赵艳敏, 王皎, 宋光明, 等. 苹果树枝和叶中根皮苷及根皮素含量变化研究[J]. 食品研究与开发,2013,34(7):95−98. [ZHAO Y M, WANG J, SONG G M, et al. Study on the variation of root phloridzin and phloretin content in branches and leaves of apple trees[J]. Food Research and Development,2013,34(7):95−98. ZHAO Y M, WANG J, SONG G M, et al. Study on the variation of root phloridzin and phloretin content in branches and leaves of apple trees[J]. Food Research and Development, 2013, 34(07): 95-98.
[24] GUTIERREZ B L, ZHONG G Y, BROWN S K. Increased phloridzin content associated with russeting in apple (Malus domestica (Suckow) Borkh. ) fruit[J]. Genetic Resources and Crop Evolution,2018,65(8):2135−2149. doi: 10.1007/s10722-018-0679-5
[25] 迟东泽, 何源, 刘芳芳, 等. 鹿鞭醇提物对秀丽隐杆线虫衰老的影响[J]. 食品工业科技,2021,42(10):327−335. [CHI D Z, HE Y, LIU F F, et al. Effect of alcoholic extract of deer whip on senescence of Caenorhabditis elegans[J]. Food Industry Science and Technology,2021,42(10):327−335. CHI D Z, HE Y, LIU F F, et al. Effect of alcoholic extract of deer whip on senescence of Caenorhabditis elegans[J]. Food Industry Science and Technology, 2021, 42(10): 327-335.
[26] OLIVEIRA B F, NOGUEIRA-MACHADO J A, CHAVES M M. The role of oxidative stress in the aging process[J]. The Scientific World Journal,2010,10:1121−1128. doi: 10.1100/tsw.2010.94
[27] CAÑUELO A, GILBERT-LÓPEZ B, PACHECO-LIÑÁN P, et al. Tyrosol, a main phenol present in extra virgin olive oil, increases lifespan and stress resistance in Caenorhabditis elegans[J]. Mechanisms of Ageing and Development,2012,133(8):563−574. doi: 10.1016/j.mad.2012.07.004
[28] 仵菲, 蒲云峰, 雷晓钰, 等. 库尔勒香梨果实发育过程中酚类物质及抗氧化活性研究[J]. 果树学报,2022,39(4):574−583. [WU F, PU Y F, LEI X Y, et al. Phenolic substances and antioxidant activity in fruit development of Kulle balsam pear[J]. Journal of Fruit Trees,2022,39(4):574−583. doi: 10.13925/j.cnki.gsxb.20210320 WU F, PU Y F, LEI X Y, et al. Phenolic substances and antioxidant activity in fruit development of Kulle balsam pear[J]. Journal of Fruit Trees, 2022, 39(4): 574-583. doi: 10.13925/j.cnki.gsxb.20210320
[29] 王猛, 关思宇, 于杰, 等. 褐藻多糖的体外抗氧化活性及其延长秀丽隐杆线虫的寿命[J]. 现代食品科技,2022,38(4):1−9. [WANG M, GUAN S Y, YU J, et al. In vitro antioxidant activity of brown algae polysaccharides and their prolongation of life span in Caenorhabditis elegans[J]. Modern Food Science and Technology,2022,38(4):1−9. WANG M, GUAN S Y, YU J, et al. In vitro antioxidant activity of brown algae polysaccharides and their prolongation of life span in Caenorhabditis elegans[J]. Modern Food Science and Technology, 2022, 38(4): 1-9.
[30] LI N, LI X, SHI Y L, et al. Trilobatin, a component from Lithocarpus polystachyrus Rehd., increases longevity in C. elegans through activating SKN1/SIRT3/DAF16 signaling pathway[J]. Frontiers in Pharmacology,2021,12:655045. doi: 10.3389/fphar.2021.655045
[31] LIU Z, REN Z, ZHANG J, et al. Role of ROS and nutritional antioxidants in human diseases[J]. Frontiers in physiology,2018,9:477. doi: 10.3389/fphys.2018.00477
[32] FINKEL T, HOLBROOK N J. Oxidants, oxidative stress and the biology of ageing[J]. nature,2000,408(6809):239−247. doi: 10.1038/35041687
[33] 付敏, 张旭光, 杨柳, 等. 虾青素调控ROS介导的自噬延长秀丽隐杆线虫寿命作用[J]. 食品工业科技,2022,43(4):373−378. [FU M, ZHANG X G, YANG L, et al. Astaxanthin regulates ROS-mediated autophagy to extend the lifespan of Caenorhabditis elegans[J]. Food Industry Science and Technology,2022,43(4):373−378. FU M, ZHANG X G, YANG L, et al. Astaxanthin regulates ROS-mediated autophagy to extend the lifespan of Caenorhabditis elegans[J]. Food Industry Science and Technology, 2022, 43(4): 373-378.
[34] LOU Z R, LI P, HAN K L. Fluorescent probes for mitochondrial reactive oxygen species in biological systems[J]. Acta Physico-Chimica Sinica,2017,33(8):1573−1588.
[35] 刘星雨, 曹素芳, 朱秋轶, 等. 牛乳源促睡眠肽的体外抗氧化活性评价及对秀丽隐杆线虫的体内抗氧化作用[J]. 食品科学,2022,43(5):151−157. [LIU X Y, CAO S F, ZHU Q Y, et al. Evaluation ofin vitro antioxidant activity of bovine milk-derived sleep-promoting peptides and in vivo antioxidant effects on Caenorhabditis elegans[J]. Food Science,2022,43(5):151−157. doi: 10.7506/spkx1002-6630-20201211-121 LIU X Y, CAO S F, ZHU Q Y, et al. Evaluation of in vitro antioxidant activity of bovine milk-derived sleep-promoting peptides and in vivo antioxidant effects on Caenorhabditis elegans[J]. Food Science, 2022, 43(5): 151-157. doi: 10.7506/spkx1002-6630-20201211-121
[36] 谭翠. 发酵大麦β-葡聚糖的抗氧化作用研究[D]. 镇江: 江苏大学, 2021. TAN C. Study on the antioxidant effect of fermented barley β-glucan [D]. Zhenjiang: Jiangsu University, 2021.
[37] 黄少杰, 陈宏著, 钟淳菲, 等. 铁皮石斛叶多糖对秀丽隐杆线虫体内抗衰老作用[J]. 食品科学,2022,43(21):203−208. [HUANG S J, CHEN H Z, ZHONG C F, et al. Anti-aging effect of Dendrobium ferruginum leaf polysaccharide on Caenorhabditis elegans in vivo[J]. Food Science,2022,43(21):203−208. HUANG S J, CHEN H Z, ZHONG C F, et al. Anti-aging effect of Dendrobium ferruginum leaf polysaccharide on Caenorhabditis elegans in vivo[J]. Food Science, 2022,43(21):203-208.
[38] ZHAO W, MA Z, LIU S, et al. Transcriptome profiling reveals potential genes and pathways supporting Ananas comosus L. Merr’s high temperature stress tolerance[J]. Tropical Plant Biology,2021,14(2):132−142. doi: 10.1007/s12042-021-09287-2
[39] 阎芙洁. 桑葚花色苷对糖代谢的调控作用及其机制研究[D]. 杭州: 浙江大学, 2018. YAN F J. Study on the regulatory role of mulberry anthocyanin on glucose metabolism and its mechanism[D]. Hangzhou: Zhejiang University, 2018.
[40] AHLUWALIA R, LO H E, POLINO H, et al. Effect of increasing hydrogen peroxide concentrations on head oscillations of Caenorhabditis elegans[J]. The Expedition, 2015, 5.
[41] 马娜, 申婷婷, 吕晓玲, 等. 黑米对高脂膳食饲喂雄性小鼠抗氧化相关基因的调控[J]. 中国食品添加剂,2014(8):55−60. [MA N, SHEN T T, LÜ X L, et al. Modulation of antioxidant-related genes by black rice in high-fat diet-fed male mice[J]. China Food Additives,2014(8):55−60. MA N, SHEN T T, LÜ X L, et al. Modulation of antioxidant-related genes by black rice in high-fat diet-fed male mice[J]. China Food Additives, 2014(8): 55-60.
-
期刊类型引用(5)
1. 张惠琪,陈晓,金雪玲,黎晶晶,袁娟丽,高金燕,陈红兵,武涌. 发芽粟米活性肽减轻铜诱导秀丽隐杆线虫氧化损伤及其分子机制. 食品工业科技. 2025(01): 384-393 .  本站查看
本站查看
2. 陈思羽,李晓,杜文珍,耿月华,刘刚,谢宁. 丝状真菌Podospora anserina中光敏色素基因的鉴定及功能分析. 微生物学报. 2024(02): 443-460 .  百度学术
百度学术
3. 刘鸿基,曾琛悦,曾霞,黄钰婷,谢炜城,罗丹琪,马鸿雁,汤丹. 甜茶木姜叶柯及其主要活性成分三叶苷药理作用研究进展. 广东药科大学学报. 2024(03): 129-135 .  百度学术
百度学术
4. 赖玉萍,陈颖仪,魏婉娉,安苗青,邹泽斌,杜冰,黎攀. 美藤果叶醇提物对延缓秀丽隐杆线虫衰老的影响. 食品工业科技. 2023(21): 402-411 .  本站查看
本站查看
5. 张余威,赵文俊,李伟杰,杜冰,黎攀. 灭活芽孢杆菌DU-106对秀丽隐杆线虫的抗衰老作用. 食品科学. 2023(23): 134-141 .  百度学术
百度学术
其他类型引用(3)





 下载:
下载:
 下载:
下载:



