Anti-aging Effect and Mechanism of Ethanol Extract of Clinacanthus nutans on Caenorhabditis elegans
-
摘要: 目的:以秀丽隐杆线虫为模式生物,探究忧遁草乙醇提取物(Clinacanthus nutans ethanol extract,CNEE)对线虫的抗衰老作用及作用机制。方法:通过寿命、产卵、运动等实验检测忧遁草乙醇提取物对线虫抗衰老的作用;通过急性氧化应激、抗氧化酶活力测定、活性氧(ROS)测定、实时荧光定量PCR等实验初步探究忧遁草乙醇提取物的抗氧化能力及延缓衰老的作用机制。结果:忧遁草乙醇提取物在100 μg/mL时能延长N2野生型线虫寿命(P<0.001),对其运动能力也有促进作用(P<0.001),同时对产卵能力没有毒性影响(P>0.05);该提取物还可以提高线虫在急性氧化应激条件下的寿命(P<0.05)及过氧化氢酶的活力(P<0.01),并有效降低体内ROS的堆积情况(P<0.05),上调daf-16(P<0.01)及下游ctl-1(P<0.001)基因的表达水平。但在daf-16突变株线虫中,没有观察到正常条件或急性氧化应激条件下延寿的作用,也没有提高过氧化氢酶的活力、降低ROS水平、提高daf-16和ctl-1表达水平的情况(P>0.05)。结论:忧遁草乙醇提取物可以提高秀丽隐杆线虫抗衰老的能力,其作用机制可能与daf-16的氧化应激调控有关。Abstract: Objective: To assess the anti-aging effect and mechanism underlying the effects of ethanol extract from Clinacanthus nutans (CNEE) using Caenorhabditis elegans as the model organism. Methods: The anti-aging effects of ethanol extract from Clinacanthus nutans on nematodes were detected by experiments to assay longevity, oviposition, and exercise. The antioxidant capacity of the ethanolic extracts from Clinacanthus nutans and their mechanisms of action in delaying aging were investigated by assessing the acute oxidative stress, determining the antioxidant enzyme activity, and determining the reactive oxygen species (ROS) levels along with real-time fluorescence quantitative PCR experiments. Results: The ethanol extract from Clinacanthus nutans at 100 μg/mL could prolong the life span of N2 wild type nematode (P<0.001), promote the ability to exercise (P<0.001), and exerted no toxic effects on oviposition (P>0.05). The extract also increased nematode longevity (P<0.05) and catalase activity (P<0.01) under acute oxidative stress conditions, and effectively reduced the accumulation of ROS in vivo (P<0.05) along with upregulating the levels of daf-16 (P<0.01) and downstream ctl-1 (P<0.001) gene expressions. However, in daf-16 mutant nematodes, effects on life extension under normal conditions or acute oxidative stress were not observed, nor was there an increase in catalase activity, a decrease in ROS levels, or an increase in daf-16 and ctl-1 levels (P>0.05). Conclusion: The ethanol extract from Clinacanthus nutans enhanced the ability of nematodes to resist aging and the underlying mechanism of action may be related to the regulation of oxidative stress by daf-16.
-
Keywords:
- Clinacanthus nutans ethanol extract /
- Caenorhabditis elegans /
- anti-aging /
- antioxidant /
- daf-16
-
衰老是生物随着时间的推移,对环境的生理及心理适应能力逐渐降低,渐进性趋向死亡的现象[1]。已有研究表明,衰老能够显著提高机体的患病率[2],如冠心病、糖尿病、阿尔茨海默综合征等。目前,与衰老有关的学说有:线粒体学说、自由基学说、端粒学说、饮食限制学说等[3-4]。其中,自由基学说认为,过量的自由基可使细胞内多种物质发生氧化损伤,甚至损害蛋白质、核酸等大分子物质,影响细胞、组织、器官等的正常功能,从而导致机体出现衰老。因此,提高人体抗氧化能力对延缓衰老具有重要作用。
忧遁草(Clinacanthus nutans),又名鳄嘴花、接骨草、沙巴蛇草等,为爵床科鳄嘴花属植物,属药食同源,是海南著名的黎药之一。该药全株或叶片入药,性凉,味甘、微苦,入肝、肾经,具有清热利湿、利尿消肿、活血散瘀、消炎解酒、防癌抗癌等作用。该药最早用来治疗肾脏疾病,后因治愈淋巴癌末期患者而受到世人关注。现代药理学研究表明[5-6]:忧遁草中羽扇醇、白桦脂醇、五环三萜化合物、Beta谷甾醇和类黄酮含量极高,这些成分大多具有抗氧化[7-8]的作用。段佳辉[5]研究发现忧遁草乙醇提取物(CNEE)和水提取物均能有效清除DPPH和ABTS+自由基,且乙醇提取物抗氧化活性强于水提物,能有效减轻酒精和四氯化碳诱导的急性肝损伤,起到保肝、护肝的作用。忧遁草的抗氧化研究大多采用大、小鼠及细胞等进行实验,至今尚未发现以秀丽隐杆线虫(C. elegans)为模式生物来研究忧遁草乙醇提取物的抗氧化衰老作用的相关报道。
C. elegans的基因与人类基因同源性达60%~80%,且具有生命周期短、身体透明易于观察、饲养成本低、容易获取大量同期化样本、对人体无害等特点,因此成为国际上公认的研究衰老机制的首选模式生物[9-13]。C. elegans中的胰岛素信号通路(Insulin-like growth factor 1,IGF-1)是目前研究得较为深入的、调控氧化衰老的信号通路[2, 14-15],该通路上的daf-16基因是一种寿命调控因子,与人类FOXO家族蛋白同源,对IGF-1的调控具有重要作用。López-garcía等[16]研究富含植物甾醇的水果饮料,发现该饮料可有效延长C. elegans寿命,并提高其抗氧化能力,其机制与daf-16基因的调控有关。Maria等[17]发现草莓甲醇提取物对C. elegans的延寿、抗氧化作用与daf-16的表达有关。因此,本研究以N2野生型线虫及敲除daf-16基因的突变株线虫为动物模型,探究CNEE可能的抗衰老作用及作用机制是否与daf-16基因的调控有关,为海南道地黎药——忧遁草的进一步开发与利用提供参考。
1. 材料与方法
1.1 材料与仪器
N2野生型线虫、daf-16突变株线虫和大肠杆菌(Escherichia. coli OP50, OP50) 昆明植物研究所罗怀容教授课题组;忧遁草 五指山万家宝科技有限公司;5-氟尿嘧啶(5-Fudr)和琼脂粉 Sigma-Aldrich公司;RNA提取试剂盒 普洛麦格(北京)生物技术有限公司;逆转录及定量PCR试剂盒 YEASEN公司;过氧化氢酶试剂盒 南京建成生物工程研究所;BCA蛋白定量测定试剂盒 Biosharp公司;蛋白胨、胆固醇 海口映月生物科技有限公司;MgSO4、CaCl2 Biosharp公司。
LDZF-50L-II立式高压蒸汽灭菌器 上海申安医疗器械厂;HZQ-F160A恒温振荡器 上海一恒科学仪器有限公司;PTX-FA210S电子天平 福州华志科学仪器有限公司;LHS-250HC-1恒温恒湿箱 海南光威科技有限公司;SCILOGEX台式高速微量冷冻离心机 美国塞洛捷克公司;CLT55R大容量低速台式冷冻离心机 湖南湘仪公司;KZ-III-FP组织研磨仪 武汉赛尔维生物科技有限公司;Motic显微镜(S219030537) 北京普瑞赛司仪器有限公司。
1.2 实验方法
1.2.1 忧遁草乙醇提取物的制备
将80 g忧遁草干品粉碎,过40目筛,粉末用70%乙醇溶液(料液比为1:30 g/mL)在80 ℃下回流提取两次,每次2 h,合并滤液,旋转浓缩,浓缩液烘干得到38.55 g浸膏,浸膏4 ℃冷藏保存[18]。
1.2.2 固体培养基(NGM)的制备
称取2.4 g NaCl、2 g蛋白胨、14 g琼脂粉加入800 mL 蒸馏水中溶解混匀,121 ℃高压蒸汽灭菌25 min,待温度降至60 ℃以下,加入1 mol/L MgSO4、1 mol/L CaCl2、5 mg/mL胆固醇各800 μL,再加入20 mL K2HPO4/KH2PO4。
1.2.3 实验组和空白对照组NGM的处理
用OP50菌液(OD600=0.6)和CNEE浸膏配制不同浓度的药物,20 μg/mL(低剂量组,LD)、50 μg/mL(中剂量组,MD)、100 μg/mL(高剂量组,HD)CNEE+OP50,加入到NGM培养基中。空白对照组(BC)加入与实验组药物等体积的OP50菌液。
1.2.4 C. elegans的同期化
用M9(M9 buffer,M9)溶液将产卵期线虫(称取NaCl 4.0 g,KH2PO4 2.4 g,NaHPO4·12H2O 12.1 g加入至800 mL 蒸馏水中溶解混匀,121 ℃高压蒸汽灭菌25 min,待温度降至60 ℃以下,加入1 mol/L MgSO4 800 μL)从NGM培养基上冲洗下来,转至15 mL无菌离心管内,定容至10 mL。向管中加入5 mL裂解液(5 mol/L NaOH和5 mol/L NaClO按1:2配制,现配现用),上下颠倒混匀约6~8 min,3000 r/min离心1 min,弃上清收集沉淀。沉淀用M9溶液反复清洗2~3次,最终的沉淀加入10 mL M9溶液轻柔混匀,平放于20 ℃恒温恒湿箱中孵育16~20 h,3800 r/min离心10 min,弃上清,用移液枪轻柔吸取管底部孵育出的L1期线虫,转移至NGM培养基中培养24 h,即可得到同期化的L4期成虫[19]。
1.2.5 衰老指标的检测
1.2.5.1 寿命实验
先进行N2野生型线虫的寿命实验。N2线虫分为BC、LD、MD、HD组,共4组。随机挑取同期化L4期线虫至各组培养基中,此时记做实验第1 d,20只/板,3板/组,每组共60只,于20 ℃培养。每隔2 d在同一时间将线虫转移至新的同浓度NGM培养基中,观察线虫的存活情况。线虫死亡及剔除标准:铂金铲触碰线虫头部观察30 s,无反应即判定死亡;意外死亡、逃逸、囊袋虫、生殖孔凸起、内部孵育则剔除[19]。研究发现,当药物浓度为100 μg/mL时,N2线虫的寿命发生显著变化,因此后续的实验均在该浓度下进行。daf-16线虫分为BC和HD组,实验方法同N2线虫的寿命实验。
1.2.5.2 产卵实验
将同期化的L4期N2线虫随机挑取至BC和HD组中,1只/板,10板/组,此时记作产卵实验第1 d,每隔24 h将线虫转移至新的同浓度NGM培养基中,直到所有线虫均不产卵。含有子代的NGM培养基于20 ℃培养,3 d后统计培养基中线虫数目,计数应在子代线虫进入生殖期之前进行。记录线虫每天的产卵量及一生的总产卵量[11]。
1.2.5.3 运动实验
同期化的L4期N2线虫随机挑取至BC和HD组中,此时记作实验第1 d,30±2只/板,1板/组,观察期为10 d。观测第1、3、5、7、9 d同一时间段未转板前线虫的头部摆动频率和身体弯曲频率,每组随机挑取线虫观察,每组检测线虫数目不少于15只。头部摆动频率:头部从一个方向摆向另一方向后,再摆动回来为一次头部摆动,记录1 min线虫头部的摆动频率;身体弯曲频率:线虫向身体所在直线的方向做一个波长的运动为一次身体弯曲,记录20 s身体弯曲的频率[20]。
1.2.6 抗氧化指标的检测
1.2.6.1 急性氧化应激实验
N2和daf-16线虫各分为BC和HD组中,共计4组。随机挑取同期化的L4期线虫至各组培养基中,30只/板,1板/组,20 ℃培养3 d。将各组线虫转移至含有3%过氧化氢(H2O2)的新板中,20 ℃培养,每隔30 min观察线虫存活情况,直至所有线虫死亡。死亡及剔除方法与寿命实验相同[21]。
1.2.6.2 活性氧自由基(reactive oxygen species,ROS)测定
线虫分组情况同1.2.6.1。随机挑取同期化的L4期线虫至各组培养基中,400只/板,1板/组,20 ℃培养4 d。用M9溶液冲洗各组线虫分装于1.5 mL Ep管中,清洗2~3次。按照ROS试剂盒的操作要求对每管线虫进行荧光染色(染液:PBS和DCFH-DA探针按1000:2配制,现配现用),37 ℃培养3 h,3000 r/min离心1 min,去上清,再清洗2~3次,以去除染液。最后,将线虫制成标本,在倒置荧光显微镜下观察、拍照[22]。
1.2.6.3 抗氧化酶活力测定
线虫分组情况同1.2.6.1。随机挑取同期化的L4期线虫至各组培养基中,400只/板,1板/组,20 ℃培养4 d。用M9溶液冲洗各组线虫分装于1.5 mL Ep管中,清洗2~3次。用组织研磨仪研磨(选择植物叶片程序),随后3000 r/min离心10 min,吸取上清,按照过氧化氢酶(Catalase,CAT)试剂盒的操作要求检测CAT的活力。
1.2.7 实时荧光定量 PCR(qRT-PCR)
线虫分组情况同1.2.6.1。随机挑取同期化的L4期线虫至各组培养基中,1000只/板,1板/组,20 ℃培养5 d。收集各HD组和BC组线虫,利用RNA提取试剂盒提取线虫的总RNA,并进行逆转录,于−80 ℃保存。使用SYBR Green PCR Master Mix和q225系统进行qRT-PCR实验[19],内参基因为act-1,定量方法为:2−△△CT,引物列表如下(表1)。
表 1 秀丽隐杆线虫qRT-qPCR引物序列Table 1. qRT-PCR primer sequence of Caenorhabditis elegans基因 上游引物(5'-3') 下游引物(5'-3') act-1 GCTGGACGTGATCTTACTGATTACC GTAGCAGAGCTTCTCCTTGATGTC daf-16 CGGGTGCCTATGGAAACT TTGGAAGAGCCGATGAAG ctl-1 CGGATACCGTACTCGTGATGAT CCAAACAGCCACCCAAATCA 1.3 数据处理
以上实验均重复至少3次,数据采用SPSS 25.0 统计软件进行分析,两组间比较采用独立样本T检验。使用GraphPad Prism 8.0进行数据处理,寿命实验和急性氧化应激实验采用Kaplan-Meier生存分析法处理。采用Image J图像软件分析荧光图片,实验结果以均数±标准差(
¯X ±SD )表示,*P<0.05、**P<0.01、***P<0.001均为差异有统计学意义。2. 结果与分析
2.1 CNEE对线虫衰老相关指标的影响
2.1.1 CNEE对线虫寿命的影响
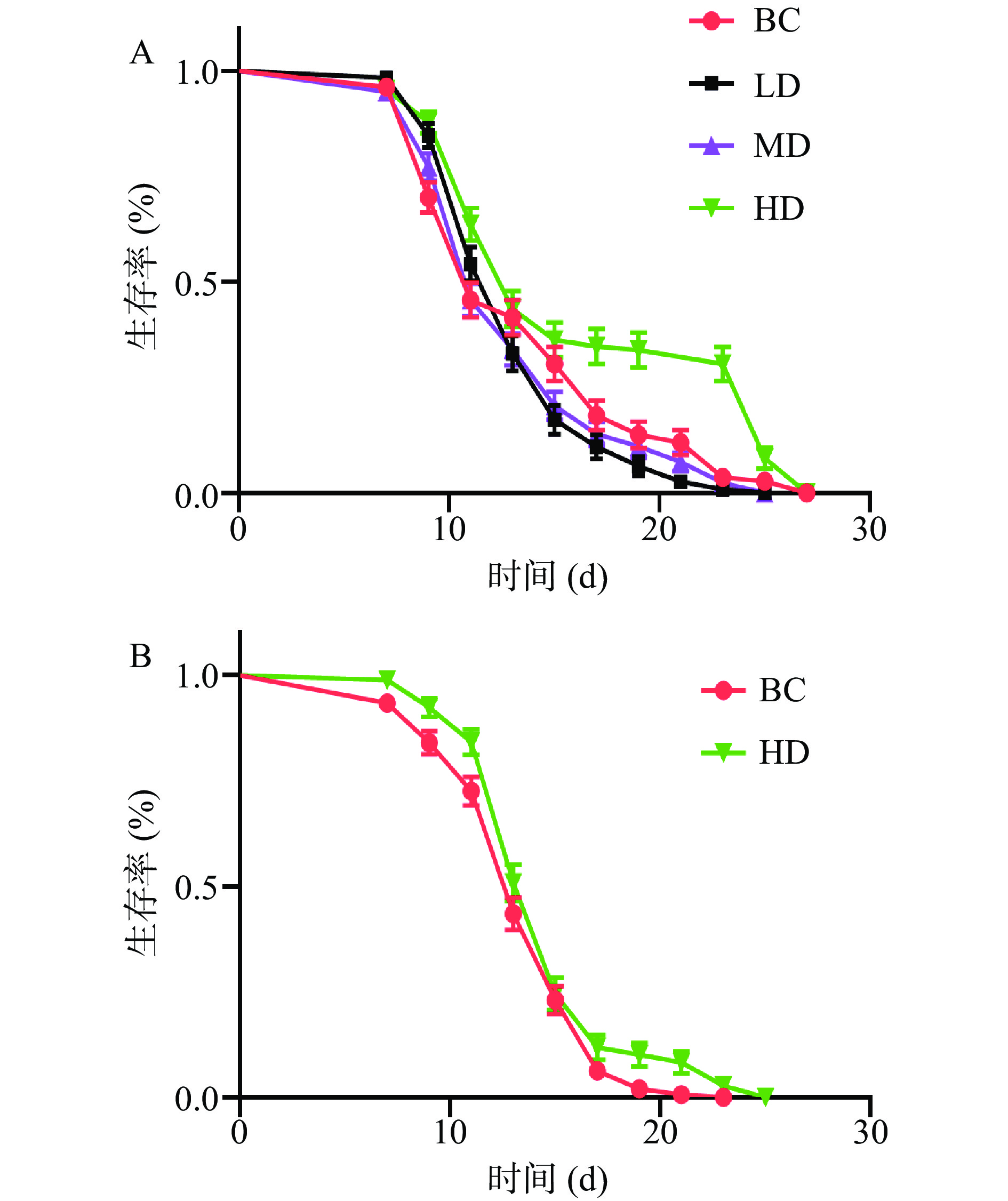
反映衰老最直接的指标是寿命的长短。不同浓度CNEE对N2野生型线虫生命周期的影响结果如图1(A)和表2所示,与BC组相比,实验组在20和50 μg/mL浓度时寿命延长不显著(P>0.05),而100 μg/mL浓度时寿命延长高度显著(P<0.001),其生存曲线向右平移,在第8 d现象较为明显。BC组线虫平均寿命为13.689 d,而HD组线虫平均寿命为16.362 d,延长了19.53%(P<0.001),说明CNEE在100 μg/mL浓度时能高度显著地延缓线虫衰老(P<0.001)。由图1(B)和表2所示,与BC组相比,高剂量CNEE对daf-16突变株线虫的寿命没有显著影响(P>0.05)。daf-16基因调控着经典的抗衰IGF-1信号通路,对寿命的调控具有重要意义。本实验结果显示,100 μg/mL浓度的CNEE对N2线虫有延长寿命的作用,但相同浓度的CNEE对敲除daf-16基因的线虫没有延寿的作用,实验结果表明,CNEE可以延缓线虫衰老,其机制可能与daf-16基因的调控有关。
表 2 CNEE对线虫平均寿命的影响Table 2. Effect of ethanol extract of Clinacanthus nutans on the average life span of nematodes2.1.2 CNEE对线虫生殖能力的影响
生殖能力是最基本的生理能力之一,也是研究衰老的重要指标之一[15]。由表3所示,BC组与HD组的总产卵量分别为201.57和221.43个,HD组总产卵量稍偏高,但两组无统计学差异(P>0.05),说明CNEE在延长N2线虫寿命时,对其生殖能力没有毒性影响。
表 3 CNEE对线虫生殖能力和运动能力的影响Table 3. Effects of ethanol extract of Clinacanthus nutans on the reproductive and athletic ability of nematodes组别 总产卵量(个) 身体弯曲频率(次/20 s) 头部摆动频率(次/min) BC 201.57±72.40 3.88±2.45 5.96±4.15 HD 221.43±61.51ns 4.03±2.09ns 8.82±4.42*** 2.1.3 CNEE对线虫运动能力的影响
研究表明,运动行为指标是反映神经系统功能最基本的功能指标,已被广泛地应用于各种药物、毒物的毒理学评估[23]。在线虫运动行为中,身体弯曲频率和头部摆动频率是最敏感的生理指标[24],因此本实验采用这两项指标来检测CNEE对线虫运动能力的影响。由表3可知,与BC组相比,HD组的身体弯曲频率无显著差异(P>0.05),但头部摆动频率有高度显著差异(P<0.001)。实验说明,CNEE可能通过改变线虫的神经系统健康程度进而影响线虫的运动能力,从而延缓衰老。
2.2 CNEE对线虫抗氧化能力的影响
2.2.1 急性氧化应激实验
自由基和抗氧化系统处于动态平衡中,随着年龄的增长,机体抗氧化能力减退,自由基不断积累,衰老及衰老相关疾病随之产生。多数研究表明[21,25-26],提高抗氧化能力是延缓衰老、治疗衰老相关疾病的重要方法之一。
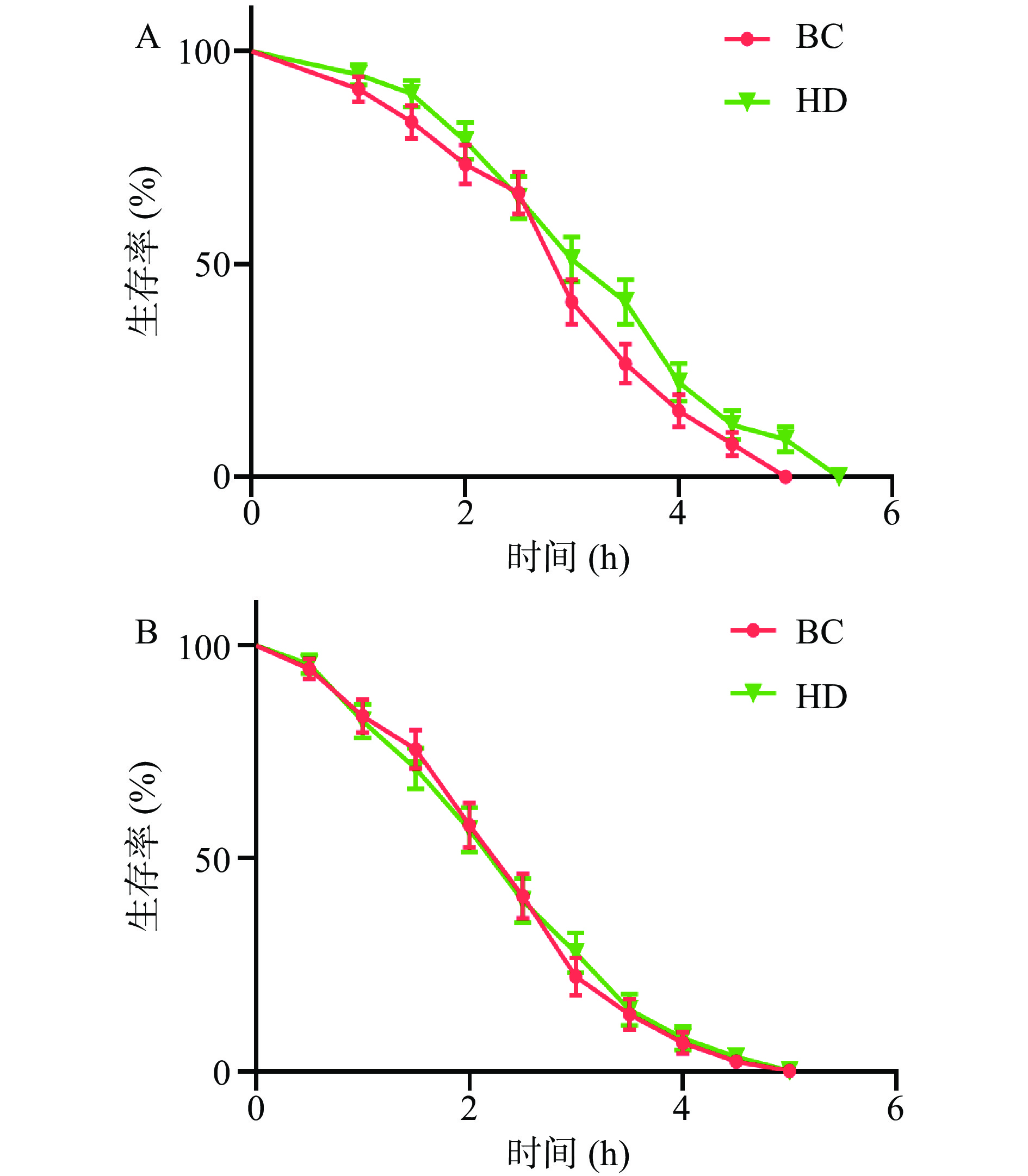
本实验以强氧化剂H2O2构建急性氧化损伤环境,通过测定HD组与BC组线虫的生存率,判断CNEE是否具有提高线虫抗氧化能力的作用,从而探究CNEE延长线虫寿命是否与提高抗氧化能力有关。由表2和表4可知,正常情况下线虫的寿命都在7 d以上,而急性氧化应激条件下线虫的寿命则会大幅缩短,说明本实验以H2O2构建的急性氧化损伤模型是成功的。由表4和图2所示,在3% H2O2急性氧化损伤条件下,HD组N2线虫平均生存3.322 h,而BC组平均生存3.028 h,显著延长了9.71%(P<0.05),且HD组的生存曲线明显向右平移,在第1 h时较为明显。实验说明,CNEE能延长N2线虫在急性氧化损伤条件下的寿命,有效提高线虫抗氧化的能力。同样的条件下,在daf-16突变株线虫中则观察不到HD组与BC组之间的显著差异(P>0.05)。
表 4 氧化应激条件下CNEE对线虫平均寿命的影响Table 4. Effect of ethanol extract of Clinacanthus nutans on the average life span of nematodes under oxidative stress线虫类型 组别 平均寿命(h) N2 BC 3.028±0.120 HD 3.322±0.129* daf-16 BC 2.483±0.116 HD 2.494±0.122ns 2.2.2 CNEE对线虫体内ROS的影响
ROS是体内正常代谢的天然产物,包括过氧化物、超氧化物、羟基自由基等,对维持人体内环境平衡具有重要的作用[27]。但在环境压力(紫外线或热暴露)下,ROS水平会急剧增加,过多的ROS积累会导致氧化与抗氧化动态平衡失调,从而引起细胞损伤甚至凋亡。
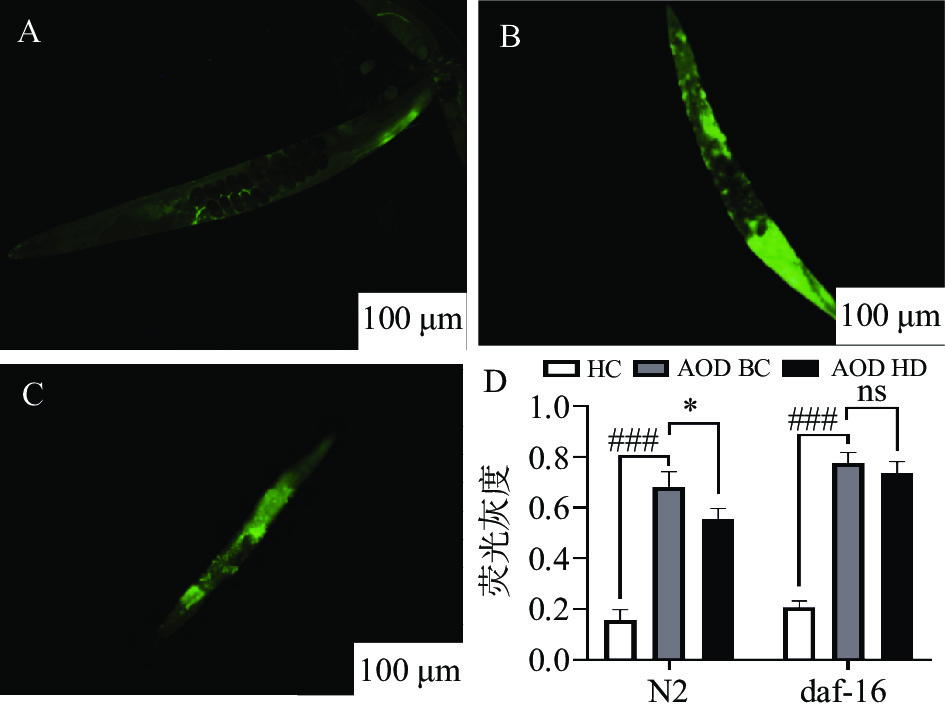
本实验采用2,7-二氯二氢荧光素二乙酸酯(H2DCFDA)荧光探针法检测线虫体内ROS水平[24]。若图片呈现的荧光强度越强,则线虫体内的ROS水平越高,即氧化损伤越严重。图3A为健康线虫的ROS荧光图,图3B和图3C为高温氧化损伤下的ROS荧光图。与BC组相比,HD组的荧光强度明显减小,且两组荧光灰度分析具有统计学差异(P<0.05)。实验说明,CNEE可以改善N2野生型线虫体内ROS堆积的情况,以此减小机体的氧化损伤。在daf-16突变株线虫中则没有观察到显著差异(P>0.05)。
2.2.3 CNEE对抗氧化酶活力的影响
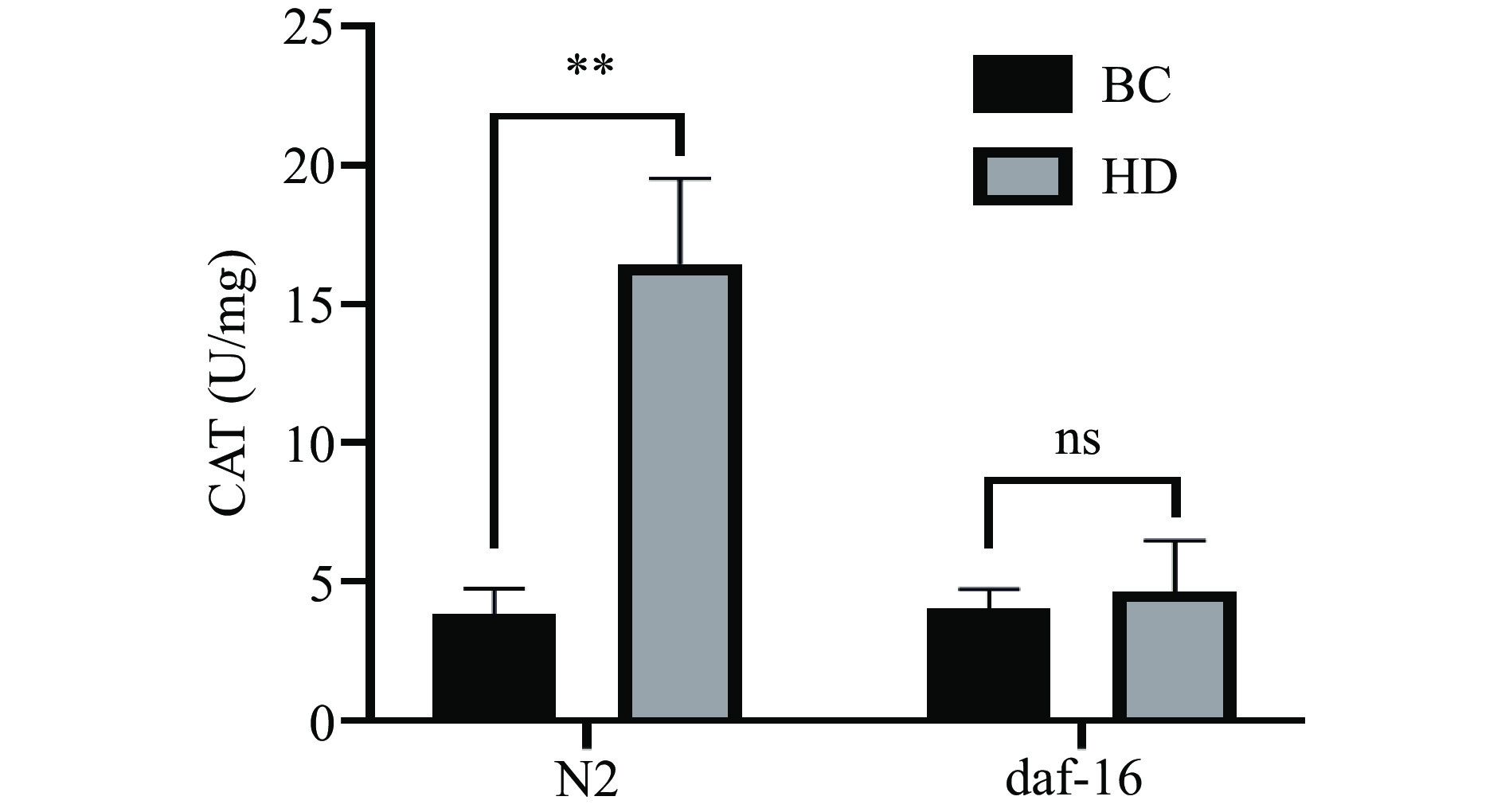
抗氧化系统分为酶类抗氧化系统和非酶类抗氧化系统。其中,CAT是酶类抗氧化系统中重要的抗氧化酶之一。本实验通过检测CNEE对CAT的影响,判断CNEE是否通过提高CAT的活力来影响线虫的抗氧化能力。由图4可知,在N2野生型线虫中,HD组CAT的活力与BC组相比显著提高(P<0.01),而daf-16线虫中CAT的活力没有显著变化(P>0.05)。实验说明,CNEE可以提高N2野生型线虫的CAT活力,进而影响线虫的抗氧化能力。
综合以上三个实验说明,CNEE可以提高N2线虫的抗氧化能力,进而延长线虫的寿命,以此达到抗衰老的作用,其机制与降低ROS水平及提高CAT活力有关。但CNEE没有提高daf-16突变株线虫在氧化损伤条件下的寿命,也没有降低ROS水平、提高CAT活力,说明CNEE抗衰老、抗氧化的作用可能与daf-16基因的调控有关。
2.3 实时荧光定量PCR(qRT-PCR)
IGF-1信号通路是研究得较为深入的寿命通路[28-30],这条通路上的daf-16基因是经典的长寿基因[31-32],调控着众多与抗衰老、抗氧化相关的靶基因,如过氧化氢酶(ctl-1)、热休克蛋白(hsp-16.2)等基因[33]。
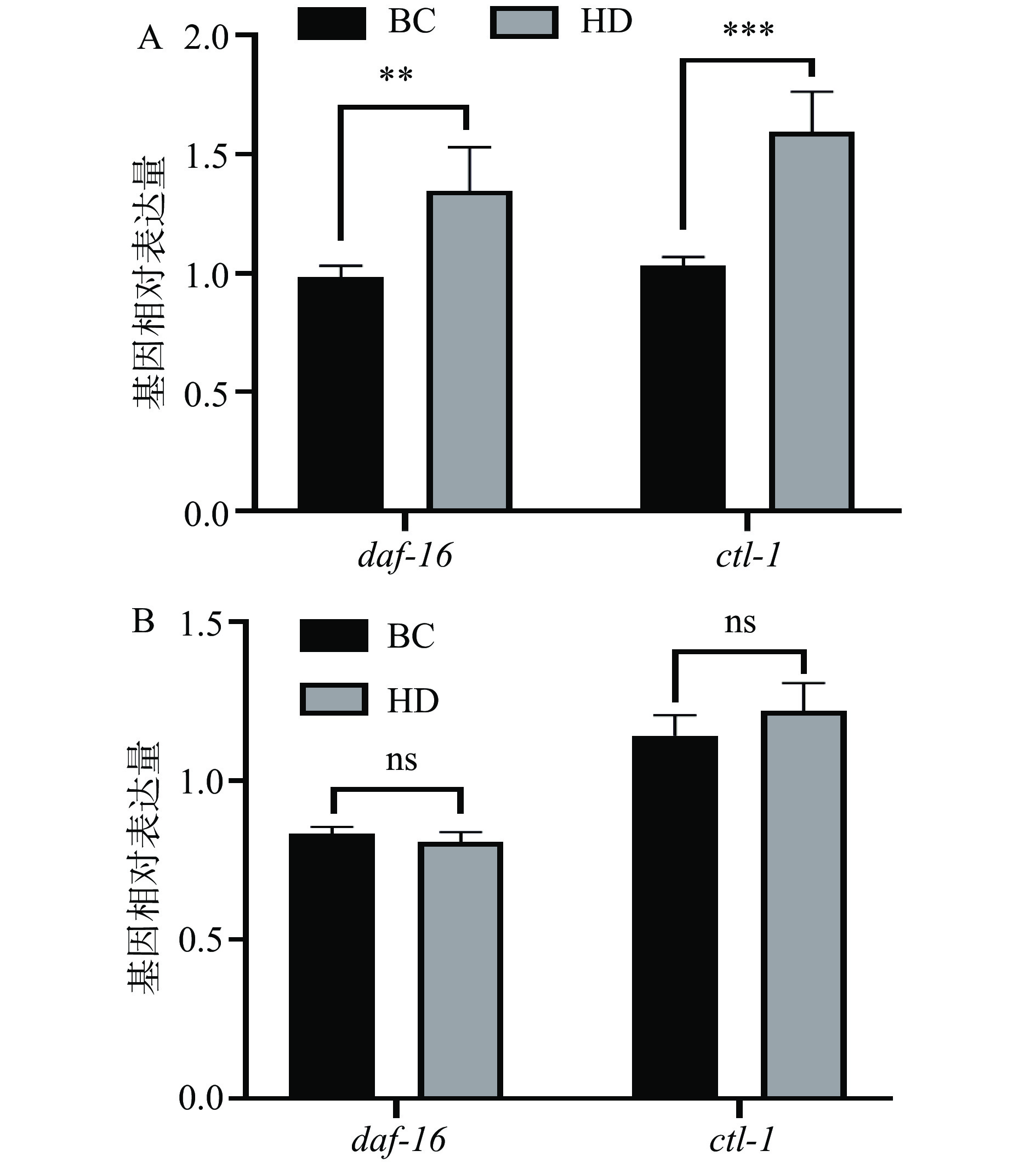
由图5A可知,在N2野生型线虫中,HD组与BC组相比,daf-16基因表达量极显著上调(P<0.01),其下游抗氧化基因ctl-1也呈现高度显著上调趋势(P<0.001)。但在daf-16突变株线虫中(图5B),这两个基因均未表现出显著差异(P>0.05)。该实验结果与寿命实验及抗氧化相关实验的结果相呼应,进一步说明CNEE可能通过调控IGF-1信号通路上的daf-16基因影响线虫的抗氧化能力,进而延缓线虫衰老。
3. 结论
本研究以秀丽隐杆线虫为研究对象,探究忧遁草乙醇提取物对线虫是否具有抗衰老的作用,并初步探究其抗衰老的作用机制。在寿命实验中,忧遁草乙醇提取物在100 μg/mL浓度时具有良好的抗衰老作用,平均寿命高度延长了19.53%(P<0.001)。在产卵实验和运动能力实验中,忧遁草乙醇提取物对线虫的生殖能力没有影响,但对运动能力有显著促进作用(P<0.05)。探究抗氧化能力的实验中,忧遁草乙醇提取物可以显著延长N2线虫在急性氧化应激条件下的寿命(P<0.05),还能有效降低氧化损伤情况下线虫体内ROS的水平(P<0.05),并提高CAT的活力。在以上寿命实验及抗氧化相关实验中,忧遁草乙醇提取物对daf-16突变株线虫没有表现出延寿或者提高抗氧化能力的作用。在qRT-PCR实验中,探究忧遁草乙醇提取物对daf-16长寿基因和ctl-1抗氧化基因的影响,发现该提取物在N2线虫中能显著上调这两个基因的表达水平,但在daf-16线虫中没有明显影响。综上所述,忧遁草乙醇提取物可以提高秀丽隐杆线虫抗衰老的能力,其作用机制可能与daf-16的氧化应激调控有关,具体的作用机制后续还需进一步研究。本研究为忧遁草以后的开发利用提供了理论依据。
-
表 1 秀丽隐杆线虫qRT-qPCR引物序列
Table 1 qRT-PCR primer sequence of Caenorhabditis elegans
基因 上游引物(5'-3') 下游引物(5'-3') act-1 GCTGGACGTGATCTTACTGATTACC GTAGCAGAGCTTCTCCTTGATGTC daf-16 CGGGTGCCTATGGAAACT TTGGAAGAGCCGATGAAG ctl-1 CGGATACCGTACTCGTGATGAT CCAAACAGCCACCCAAATCA 表 2 CNEE对线虫平均寿命的影响
Table 2 Effect of ethanol extract of Clinacanthus nutans on the average life span of nematodes
表 3 CNEE对线虫生殖能力和运动能力的影响
Table 3 Effects of ethanol extract of Clinacanthus nutans on the reproductive and athletic ability of nematodes
组别 总产卵量(个) 身体弯曲频率(次/20 s) 头部摆动频率(次/min) BC 201.57±72.40 3.88±2.45 5.96±4.15 HD 221.43±61.51ns 4.03±2.09ns 8.82±4.42*** 表 4 氧化应激条件下CNEE对线虫平均寿命的影响
Table 4 Effect of ethanol extract of Clinacanthus nutans on the average life span of nematodes under oxidative stress
线虫类型 组别 平均寿命(h) N2 BC 3.028±0.120 HD 3.322±0.129* daf-16 BC 2.483±0.116 HD 2.494±0.122ns -
[1] 刘赫男. 富氢水的制备及丁酸梭菌延长秀丽线虫寿命的机制研究[D]. 合肥: 安徽医科大学, 2020 LIU H N. Preparation of hydrogen-rich water and the mechanism of Clostridium butyricum to prolong the life span of Caenorhabditis elegans[D]. Hefei: Anhui Medical University, 2020.
[2] 黄小兵. 抗衰老化合物筛选及阿司匹林抗衰老活性评价[D]. 昆明: 中科院昆明植物研究所, 2016 HUANG X B. Screening of anti-aging compounds and evaluation of anti-aging activity of aspirin[D]. Kunming: Kunming Institute of Botany, Chinese Academy of Sciences, 2016.
[3] GUO X Y, LI Q Q, SHI J, et al. Perfluorooctane sulfonate exposure causes gonadal developmental toxicity in Caenorhabditis elegans through ROS-induced DNA damage[J]. Chemosphere,2016,155:115−126. doi: 10.1016/j.chemosphere.2016.04.046
[4] SHAY J W. Role of telomeres and telomerase in aging and cancer[J]. Cancer Discovery,2016,6(6):584−593. doi: 10.1158/2159-8290.CD-16-0062
[5] 段佳辉. 忧遁草叶提取物解酒、保肝及抗氧化功能的研究[D]. 无锡: 江南大学, 2019 DUAN J H. Study on the anti-drinking, hepatoprotective and antioxidant functions of the leaf extracts of Clinacanthus nutans[D]. Wuxi: Jiangnan University, 2019.
[6] 王瑶, 钟希文, 张文霞. 鳄嘴花的化学成分及药理作用研究进展[J]. 中国药房,2016,27(1):108−111. [WANG Y, ZHONG X W, ZHANG W X. Advances in the chemical composition and pharmacological effects of Clinacanthus nutans[J]. Chinese Pharmacy,2016,27(1):108−111. [7] 魏瑞. 忧遁草中三萜类物质的提取纯化及功能评价[D]. 天津: 天津科技大学, 2020 WEI R. Extraction, purification and functional evaluation of triterpenoids from Clinacanthus nutans[D]. Tianjin: Tianjin University of Science and Technology, 2020.
[8] 段佳辉, 徐德平, 钱志娟, 等. 忧遁草抗氧化功效与成分的研究[J]. 食品科技,2019,44(3):205−210. [DUAN J H, XU D P, QIAN Z J, et al. Study on the antioxidant efficacy and composition of Clinacanthus nutans[J]. Food Science and Technology,2019,44(3):205−210. [9] 黄壮, 李静, 杜鸿志, 等. 三七醇提取物对秀丽隐杆线虫的降脂作用[J]. 世界科学技术-中医药现代化,2020,22(5):1648−1653. [HUANG Z, LI J, DU H Z, et al. Lipid lowering effect of Panax notoginseng alcohol extract on Caenorhabditis elegans[J]. World Science and Technology-Modernization of Traditional Chinese Medicine,2020,22(5):1648−1653. [10] 刘静. 金钗石斛总生物碱抗秀丽隐杆线虫衰老作用及其机制研究[D]. 遵义: 遵义医科大学, 2019 LIU J. Study on the anti aging effect and mechanism of total alkaloids of Dendrobium nobile on Caenorhabditis elegans[D]. Zunyi: Zunyi Medical University, 2019.
[11] HERNDON L A, WOLKOW C A, DRISCOLL M, et al. Effects of ageing on the basic biology and anatomy of C. elegans[M]. Switzerland in Ageing Lessons from C. elegans, 2017: 9−39.
[12] TISSENBAUM H A. Using C. elegans for aging research[J]. Invertebrate RE Production & Development,2015,59(1):59−63.
[13] 普元柱. 基于蛋白质组学研究秀丽线虫生殖系统调控衰老的机制[D]. 北京: 中国科学院大学, 2017 PU Y Z. Proteomics based study on the mechanism of the reproductive system of Caenorhabditis elegans regulating aging [D]. Beijing: University of Chinese Academy of Sciences, 2017.
[14] 张宗敏. 金钗石斛多糖对秀丽隐杆线虫衰老的影响[D]. 遵义: 遵义医学院, 2018 ZHANG Z M. Effects of Dendrobium nobile polysaccharides on the senescence of C. elegans[D]. Zunyi: Zunyi Medical College, 2018.
[15] 刘春红, 汤燚聪, 高瑜培, 等. 鹿茸乙醇提取物对秀丽隐杆线虫抗衰老的作用[J]. 食品工业科技,2021,42(7):354−359. [LIU C H, TANG Y C, GAO Y P, et al. Anti aging effect of ethanol extract of cartialgenous on C. elegans[J]. Science and Technology of Food Industry,2021,42(7):354−359. [16] LOPEZ-GARCIA G, CILLA A, BARBERA R, et al. Effect of plant sterol and galactooligosaccharides enriched beverages on oxidative stress and longevity in Caenorhabditis elegans[J]. Journal of Functional Foods,2020,65:1−8.
[17] MARIA D N H, JOSE M R M, ADELAIDA E M, et al. Strawberry (Fragaria×ananassa cv. Romina) methanolic extract attenuates Alzheimer's beta amyloid production and oxidative stress by SKN-1/NRF and DAF-16/FOXO mediated mechanisms in C. elegans[J]. Food Chemistry,2022,372:1−12.
[18] 于群. 忧遁草活性成分的提取及其功能评价[D]. 海口: 海南大学, 2017 YU Q. Extraction and functional evaluation of the active ingredients of Clinacanthus nutans[D]. Haikou: Hainan University, 2017.
[19] 杨帆, 肖曼, 陈柏岑, 等. 益智仁提取物延缓秀丽隐杆线虫衰老的研究[J]. 中华中医药学刊,2022,40(2):43−46, 265. [YANG F, XIAO M, CHEN B C, et al. Study on the effect of Alpinia oxyphylla extract on delaying the senescence of C. elegans[J]. Chinese Journal of Traditional Chinese Medicine,2022,40(2):43−46, 265. [20] 金司仪. 三七粉延缓秀丽隐杆线虫衰老的作用机制及其稳定性研究[D]. 武汉: 湖北中医药大学, 2019 JIN S Y. Study on the mechanism and stability of Panax notoginseng powder in delaying the senescence of C. elegans[D]. Wuhan: Hubei University of Traditional Chinese Medicine, 2019.
[21] 黄少杰, 陈宏著, 钟淳菲, 等. 铁皮石斛叶多糖对秀丽隐杆线虫体内抗衰老作用[J]. 食品科学,2022,43(21):203−208. [HUANG S J, CHEN H, ZHONG C F, et al. Anti aging effect of polysaccharides from Dendrobium nobile on C. elegans in vivo[J]. Food Science,2022,43(21):203−208. doi: 10.7506/spkx1002-6630-20211202-031 [22] 付敏, 张旭光, 杨柳, 等. 虾青素调控ROS介导的自噬延长秀丽隐杆线虫寿命作用[J]. 食品工业科技,2022,43(4):373−378. [FU M, ZHANG X G, YANG L, et al. Astaxanthin regulates ROS mediated autophagy to prolong the life span of C. elegans[J]. Science and Technology of Food Industry,2022,43(4):373−378. [23] 李煜, 敬海明, 李国君. 秀丽隐杆线虫神经毒理学研究进展[J]. 中国公共卫生,2013,29(4):622−624. [LI Y, JING H M, LI G J. Research progress in neurotoxicology of C. elegans[J]. China Public Health,2013,29(4):622−624. doi: 10.11847/zgggws2013-29-04-58 [24] 周栋. 内分泌干扰物双酚A对秀丽隐杆线虫的生态毒性效应及其作用机制研究[D]. 上海: 华东理工大学, 2016 ZHOU D. Study on the ecotoxicity and mechanism of endocrine disruptor bisphenol A on C. elegans[D]. Shanghai: East China University of Technology, 2016.
[25] 王力, 肖嵋方, 陈弘培, 等. 牡蛎多肽组分OE-I抗氧化活性及其对秀丽隐杆线虫抗衰老作用[J]. 食品科学,2022,43(3):152−160. [WANG L, XIAO M F, CHEN H P, et al. Antioxidant activity of oyster polypeptide OE-I and its anti-aging effect on C. elegans[J]. Food Science,2022,43(3):152−160. [26] 王锐凡, 雷欣安, 成高丽, 等. 鳄嘴花总黄酮对高糖诱导血管内皮细胞损伤的保护作用及机制研究[J]. 中国循证心血管医学杂志,2019,11(9):1077−1080. [WANG R F, LEI X A, CHENG G L, et al. Study on the protective effect and mechanism of total flavones of Clinacanthus nutans on vascular endothelial cell injury induced by high glucose[J]. Chinese Journal of Evidence Based Cardiovascular Medicine,2019,11(9):1077−1080. [27] TYAGI N, GAMBHIR K, KUMAR S, et al. Interplay of reactive oxygen species (ROS) and tissue engineering: A review on clinical aspects of ROS-responsive biomaterials[J]. Journal of Materials Science,2021,56:16790−16823. doi: 10.1007/s10853-021-06338-7
[28] LIU Y L, ZHOU Z Y, YIN L F, et al. Tangeretin promotes lifespan associated with insulin/ insulin-like growth factor-1 signaling pathway and heat resistance in Caenorhabditis elegans[J]. BioFactors (Oxford, England),2021,48(2):442−453.
[29] LIN C, XIAO J, XI Y, et al. Rosmarinic acid improved antioxidant properties and healthspan via the IIS and MAPK pathways in Caenorhabditis elegans[J]. BioFactors (Oxford, England),2019,45(5):774−787. doi: 10.1002/biof.1536
[30] 宋兵兵. 蓝莓和苹果皮提取物联合抗衰老活性及作用机制研究[D]. 广州: 华南理工大学, 2020 SONG B B. Study on the combined anti-aging activity and mechanism of blueberry and apple peel extracts[D]. Guangzhou: South China University of Technology, 2020.
[31] 蔡洁. 米糠活性肽通过daf-16和skn-1调节线虫寿命与应激能力的研究[D]. 长沙: 中南林业科技大学, 2021 CAI J. Studies on the regulation of rice bran active peptides on C. elegans longevity and stress capacity through daf-16 and skn-1[D]. Changsha: Central South Forestry University, 2021.
[32] WAN Q L, FU X D, DAI W Y, et al. Uric acid induces stress resistance and extends the life span through activating the stress response factor DAF-16/FOXO and SKN-1/NRF2[J]. Aging,2020,12(3):2840−2856. doi: 10.18632/aging.102781
[33] 米象男. 3,4-二羟基苯甲酸甲酯延长秀丽线虫寿命的机制研究[D]. 广州: 暨南大学, 2018 MI X N. Study on the mechanism of methyl 3,4-dihydroxybenzoate prolonging the life span of C. elegans[D]. Guangzhou: Jinan University, 2018.





 下载:
下载:

 下载:
下载:



