Effects of Compound Ratio of Carnauba Wax and Monoglyceride on the Structure and Properties of High-oleic Sunflower Oil Oleogels
-
摘要: 以高油酸葵花籽油为基料油,通过向其添加不同质量比的凝胶剂巴西棕榈蜡(carnauba wax,CW)与单甘酯(monoglyceride,MG)制备凝胶油。固定凝胶剂浓度为5%,探讨不同CW与MG的复配比对制备的高油酸葵花籽油凝胶油微观形态、凝胶晶型、热力学性质、硬度、持油性以及固体脂肪含量(solid fat content,SFC)的影响。结果表明:MG没有影响CW的熔化行为,二者没有形成共结晶,出现了偏晶现象,当CW与MG复配比为9:1时,MG晶体的存在促进了CW的结晶,同时CW的存在会抑制MG晶体的多晶态转变,提高体系的储藏稳定性;少量MG的加入显著降低了CW凝胶油的硬度(P<0.05),当二者复配比为5:5并随着MG含量的增多和CW含量的减少,体系硬度显著增大(P<0.05),在1:9时达到最大硬度137.33 g;MG的加入显著提高了CW凝胶油的持油性(P<0.05),二者复配比为5:5时体系持油性最佳达到100%;CW与MG复配比为3:7时凝胶油在30~37.5 ℃的SFC明显低于CW和MG凝胶油,此时MG的加入对体系口感的改善起到了正向作用。Abstract: Oleogels were prepared by adding different mass ratios of carnauba wax (CW) and monoglyceride (MG) to high-oleic sunflower oil as oil phase. The oleogelator concentration was fixed at 5%, and the effects of different CW and MG mass ratios on the microstructure, X-ray diffraction (XRD) pattern, thermodynamic properties, hardness, oil binding capacity and solid fat content (SFC) of high-oleic sunflower oil oleogels were investigated. The results showed that MG had no effect on the melting behavior of CW, they did not form co-crystallization and appear monotectic behavior. When the mass ratio was 9:1, the presence of MG crystal promoted the crystallization of CW, and the presence of CW inhibited the polycrystalline transition of MG crystal and improved the storage stability of the system. The hardness of CW oleogels was significantly decreased by the addition of a small amount of MG (P<0.05). When the mass ratio was 5:5, the hardness of the system increased significantly with the MG content increasing and the CW content decreasing (P<0.05), reaching the maximum hardness of 137.33 g at 1:9. The addition of MG could significantly improve the oil binding capacity of CW oleogels (P<0.05), and the oil binding capacity of the system reached 100% when the mass ratio of CW to MG was 5:5. When the ratio of CW to MG was 3:7, the SFC of oleogels at 30~37.5 ℃ was significantly lower than that of CW and MG oleogels. At this time, the addition of MG had a positive effect on the improvement of the system taste.
-
Keywords:
- oleogels /
- carnauba wax (CW) /
- monoglyceride (MG) /
- interaction mechanism /
- solid fat content (SFC)
-
油脂是人们日常饮食中不可或缺的一部分,作为重要的能量来源、脂溶性维生素的溶剂以及风味物质的载体,在食品工业和日常膳食中都有重要的地位[1]。我国是世界上最大的食品专用油脂(如焙烤专用油脂、冰激凌专用油脂等塑性脂肪)消费国[2]。塑性脂肪通常经过植物油氢化或酯交换方式获得,具有调控质构特性的功能,可赋予食品独特的风味、口感和功能性[3],常被用于焙烤食品、冰淇淋、糖果馅料、巧克力酱等食品中。然而,不彻底的氢化过程会产生对人体有害的反式脂肪酸,传统塑性脂肪中还含有较多的饱和脂肪酸,在流行病学研究中,反式脂肪酸和饱和脂肪酸会引发心血管疾病[4]。油脂凝胶化从技术上实现了“零反式、低饱和”塑性脂肪替代品的制备,作为更健康的油脂产品,凝胶油成为了食品专用油脂研究的一个热点。凝胶油是一种以液态植物油为连续相,加入少量凝胶剂加热搅拌至完全溶解,再经冷却凝固形成的有机凝胶体系[5]。凝胶剂通过特定的加工条件在晶体、胶束、聚集体或纤维中自组装成三维网络并将液态油固定其中,最终形成热可逆、半固体、可束缚液体油流动的凝胶体系[6]。目前常见的凝胶剂包括天然蜡[7]、单甘酯[8]、植物甾醇[9]、神经酰胺和卵磷脂[10]、植物甾醇和谷维素混合物[11]、乙基纤维素[12]、羟丙基甲基纤维素[13]等。
天然蜡能在较低的浓度下使液态植物油凝胶化,是较为优良的凝胶剂,因其良好的凝胶性而得到广泛研究[14]。研究发现,天然蜡制备的凝胶油存在硬度过硬的问题[15],天然蜡相对较高的熔点也可能会对凝胶油的质构性能产生不利影响,同时蜡质口感也导致消费者对天然蜡制备凝胶油的接受度并不高,这都限制其作为塑性脂肪替代品的应用[16]。巴西棕榈蜡(carnauba wax,CW)来源于巴西棕榈树的叶片,蜡酯是其主要的化学成分(超过60%)[17-18],粘性小,弹性强,是优良的油脂凝胶剂[19]。但研究表明,CW制备的凝胶油具有相对较低的持油性,在食品专用油脂如人造黄油和起酥油的使用中容易出现油相的析出,进而影响使用和食用品质[18],可以考虑将CW与其他类型的凝胶剂进行复配来改善天然蜡基凝胶油。单硬脂酸甘油酯(monoglyceride,MG)是食品中广泛使用的乳化剂,也是常用的低分子量油脂凝胶剂,作为食品中良好的乳化剂和食品添加剂,它可赋予食品在凝胶油方面更多的可能性[20]。已有研究利用CW和MG两种不同类型的凝胶剂分别制备了凝胶油,两种凝胶油均具有良好的氧化稳定性和热性能,与市售人造黄油品质相当[21],杨帅帅等[22]研究了CW和棕榈酸单甘酯(monopalmitate,MP)的比例对凝胶油热性质和结晶动力学的影响,MP-CW作为复合凝胶剂使用时,对凝胶的热性质和结晶过程的影响不是二者单个作用的简单叠加,而是在凝胶形成的过程中MP和CW产生了相互作用,Li等[23]的研究也表明MG和天然蜡之间具有协同效应,可以改善凝胶油的性能,但以上研究均没有讨论复合凝胶剂比例对凝胶油固体脂肪含量(solid fat content,SFC)的影响,SFC是评价食品专用油脂产品功能特性的重要指标之一,为进一步丰富天然蜡-单甘酯凝胶油的研究,本实验选取CW和MG作为凝胶剂制备凝胶油进行研究。
本实验将CW和MG按照一定比例添加到高油酸葵花籽油中,通过一定的加工过程使高油酸葵花籽油形成具有一定塑性的凝胶油,探讨不同CW与MG的复配比对高油酸葵花籽油凝胶油微观形态、凝胶晶型、热力学性质、硬度、持油性以及SFC的影响。初步探究两种凝胶剂复配使用时对凝胶油的结构和性质的变化规律,为天然蜡-单甘酯凝胶油在食品专用油脂如人造奶油和起酥油中的应用提供理论参考,以期研发出更加符合食品专用油脂产品性质和功能的凝胶油产品。
1. 材料与方法
1.1 材料与仪器
高油酸葵花籽油(每100 g液态油含单不饱和脂肪酸82 g) 九三粮油工业集团有限公司;巴西棕榈蜡(食品级)、单硬脂酸甘油酯(食品级,单酯含量98%) 山东优索化工科技有限公司;
JD2000-2L电子天平 沈阳龙腾电子有限公司;RT10多点恒温磁力搅拌器 德国IKA公司;Avanti-J高效离心机 美国贝克曼库尔特公司;Q2000差示扫描量热仪 美国TA;CT-III 4500质构仪 美国博勒飞公司;BX50F-3光学显微镜 日本奥林帕斯公司;MPDDY2094X X-射线衍射仪 荷兰帕纳科公司;AP07R-20-AA2Y恒温制冷水浴 美国Polyscience;Minispecl20/100RTS脉冲核磁共振仪 德国Bruke公司。
1.2 实验方法
1.2.1 凝胶油的制备
凝胶油的制备参考了史逸飞等[24]的方法并稍作修改,CW和MG复配比例的选择参考了杨帅帅等[22]的研究并略作调整:在样品瓶中称取10 g的高油酸葵花籽油,加入0.5 g(占油相质量5%)的CW和MG混合物(mCW:mMG =10:0、9:1、7:3、5:5、3:7、1:9、0:10)作为凝胶剂。将样品瓶置于100 ℃恒温磁力搅拌器,加热搅拌至凝胶剂在油相中完全溶解,室温冷却后将样品瓶转移至5 ℃冰箱中至少冷藏48 h进行后续操作。
1.2.2 微观形态分析
采用光学显微镜对凝胶油的微观结构进行观察。取适量熔融的凝胶油样品点涂于载玻片上,盖上盖玻片,使样品均匀分布,放大400倍对凝胶油结晶形态进行观察,并获取形态学照片[15],使用Image J软件进行图像处理。
1.2.3 晶型分析
采用X-射线衍射法(X-ray diffraction,XRD)对凝胶油晶型进行分析。测试条件:测试温度25 ℃,铜靶(电压40 kV,电流40 mA) ,狭缝宽度1.0 mm,接受狭缝0.1 mm,扫描速率4°/min,扫描范围0~30°。数据处理和分析使用MDI Jade 6.0软件。
1.2.4 热力学性质测定
采用差示扫描量热法(DSC)进行热力学分析,称取3~5 mg凝胶油样品置于专用铝制坩埚中,并以空白坩埚作为对照。首先将样品在100 ℃下保持10 min直至样品完全熔化以消除晶体记忆,随后以10 ℃/min冷却至0 ℃,分析样品的结晶行为;将样品在0 ℃下保持10 min达到平衡,然后在10 ℃/min下加热到100 ℃,分析其熔化行为。
1.2.5 硬度测定
采用直径为1 cm的探头(TA11/1000),以1 mm/s的恒定速度压入凝胶油样品,触发点负载为1 g,下压深度5 mm。硬度值取最大穿透力值,每个样品进行3次重复实验,数据取平均值。
1.2.6 持油性测定
称取1.5 mL离心管的质量,记为A;称取1 g左右熔融状态的凝胶油样品于称重后的离心管中,将离心管于5 ℃冰箱中冷藏24 h,记整体质量为B;冷藏后以10000 r/min的速度在室温环境下离心15 min,将离心后的试管取出,倒置于滤纸上,使析出的油脂充分被滤纸吸收,记样品和试管整体重量为C。持油率根据以下公式计算得出,重复测定6次,数据取平均值[25]。
析油率(%)=(B−A)−(C−A)(B−A)×100 (1) 持油率(%)=100−析油率 (2) 式中:A为空离心管的质量,g;B为离心前凝胶油样品及离心管的总质量,g;C为离心后凝胶油样品及离心管的总质量,g。
1.2.7 SFC测定
将样品移至外径为10 mm的核磁共振管中,高度约为4 cm。每个样品在90 ℃下保持30 min消除晶体记忆,然后转移至0 ℃恒温箱中,在该温度下保持90 min,以保证样品完全固化,随后在10、20、30、32.5、35、37.5、40、50、60、70、80 ℃温度下放置30 min并依次测量其SFC,重复测定3次,数据取平均值。
1.3 数据分析
采用SPSS 23.0软件和Origin 9.0对实验数据进行处理和作图。实验结果基于至少3次独立样品测定,结果表示为平均值±标准差,显著性分析使用Tukey法,置信水平区间为95%。
2. 结果与分析
2.1 不同CW与MG复配比对凝胶油微观形态的影响
由图1可以看出,仅由CW制备的凝胶油呈现放射状的球状晶体,而仅由MG制备的凝胶油形成了舒展且密集的长针状晶体网络,研究表明长枝状结构可以很好地使晶体之间交联形成三维网络结构,从而截留更多的液态油脂[26-27],这与Li等[8]得到的结果相似。CW与MG的复合使用明显改变了凝胶油的微观晶体形态,CW与MG质量比为9:1、7:3、5:5和3:7时,体系出现明显的晶体聚集现象,且随着MG代替CW含量的增加这种聚集状态愈发明显。当体系MG含量较少即CW与MG质量比为9:1时,结晶形态以CW为主导。与单一的CW凝胶油和MG凝胶油相比,将CW与MG复合可以得到更为致密的晶体网络,凝胶体系结构的一致性得到提高,推测可能对体系的质构特性产生影响,这与Li等[23]得到的结论一致。微观结果表明,CW和MG两种凝胶剂并非独立存在,二者会相互影响彼此的结晶形态,凝胶油晶体的形成和形状与凝胶剂的类型和配比有关。
2.2 不同CW与MG复配比对凝胶油晶型的影响
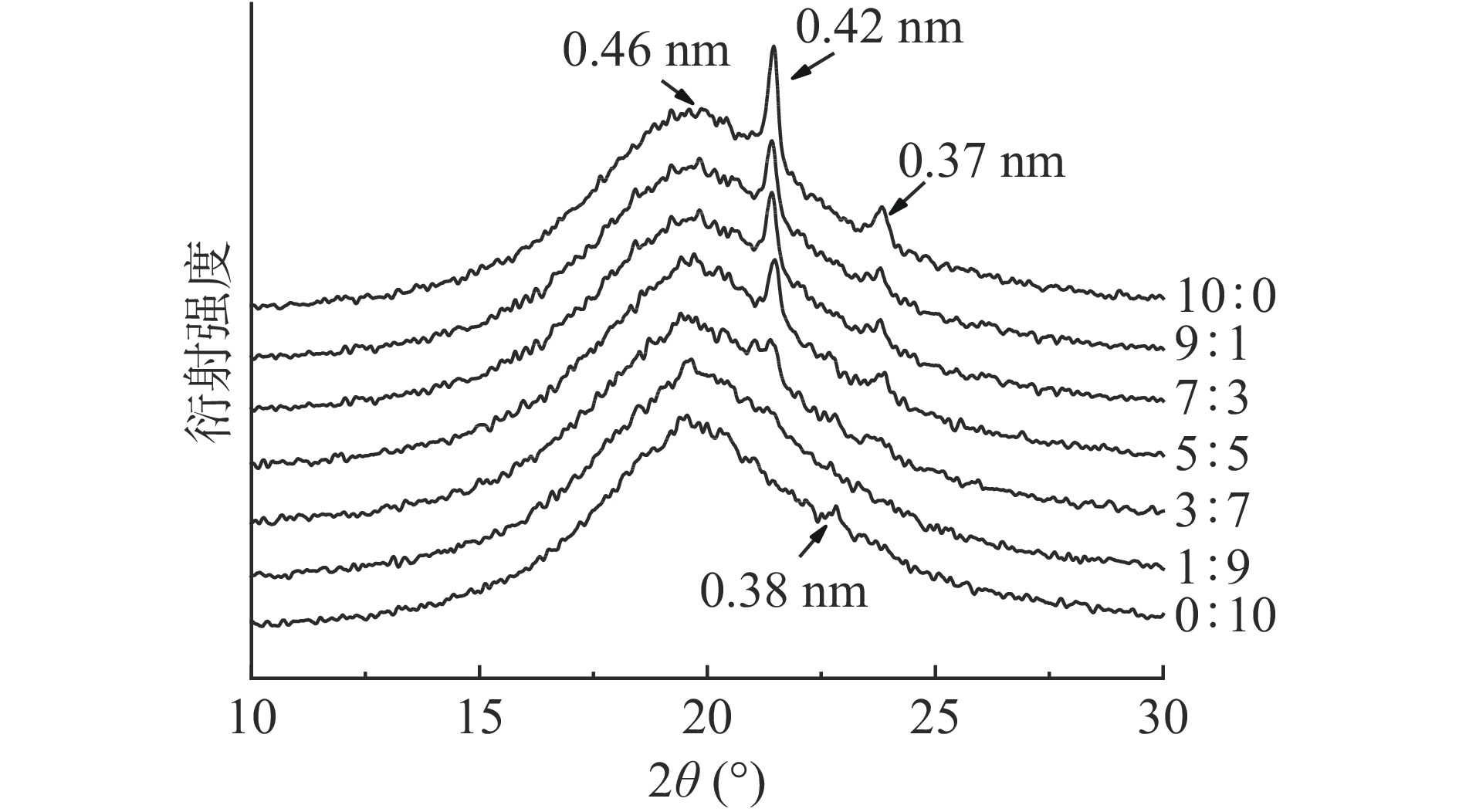
XRD分析常用于研究油脂的同质多晶现象,可获得脂链的堆积情况[28],短间距d值指的是两个衍射晶体平面之间的间距,每种类型的晶体都具有其特定的d值[29]。一般来说,短间距在0.42 nm处为α型晶体的特征峰,0.38和0.42 nm附近强衍射峰为β'型晶体的特征峰,0.46 nm附近强衍射峰为β型晶体的特征峰[30]。有研究表明,对于人造黄油和可涂抹型脂肪制品来说,β'型脂肪晶体的多态形式在凝胶油分散性、光滑的质地、最佳的熔化性和良好的口感方面是首选的,而β型晶体则在巧克力和烘培起酥油制品方面是首选的[7]。
不同凝胶剂复配比例下制备的凝胶油XRD图谱如图2所示,各凝胶油样品在不同区域出现了不同的衍射峰,说明其存在同质多晶现象。七种凝胶油样品都在0.46 nm处出现了强的衍射峰,说明七种凝胶油样品均含有较多的β型晶体。其中CW形成的凝胶油在0.42 nm处存在强衍射峰,在0.37 nm处存在较强衍射峰,说明CW形成的凝胶油含有较多的α、β以及β'型晶体。MG形成的凝胶油在0.38 nm处检测到衍射峰但其强度较弱,说明MG凝胶油除了含有较多β型晶体外还含有少量的β'型晶体,这与Li等[8]的研究结果一致。当二者复配比例在9:1、7:3和5:5时,衍射峰的类型基本不变,强度略有减小,此时CW在结晶体系中占主导地位。当二者复配比例小于5:5时,衍射峰的类型和强度均有明显的变化:3:7比例下,0.42和0.37 nm处的衍射峰迅速减弱,α和β'晶型迅速减少,此时MG在结晶体系中开始占主导地位;1:9比例下,α和β'晶型基本消失。随着CW与MG质量比的降低,凝胶油结构的α和β'晶体衍射峰强度逐渐降低,这是由于CW含量逐渐减少所致。总的来说,CW与MG的复配比会影响整个体系的晶型。
2.3 不同CW与MG复配比对凝胶油热力学性质的影响
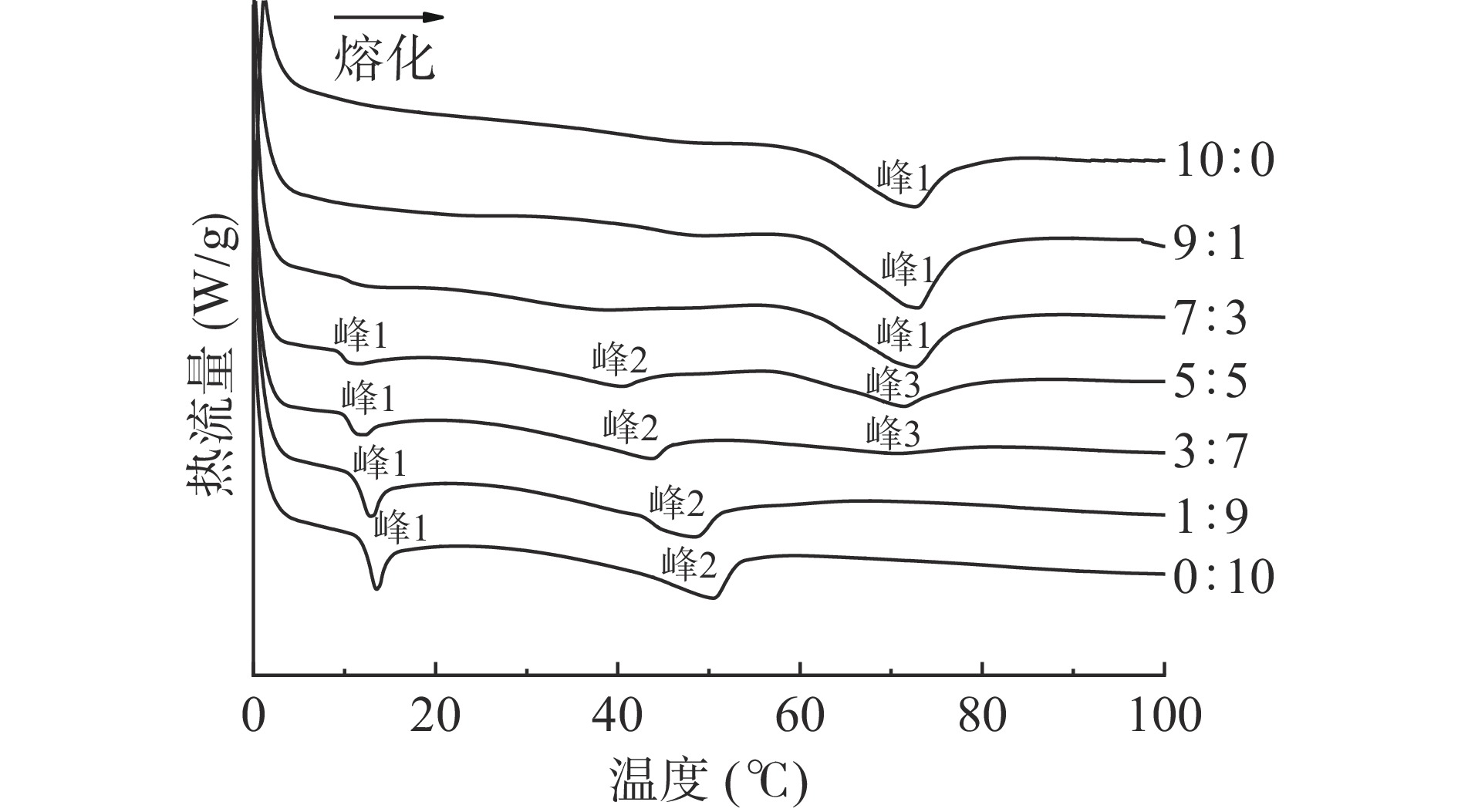
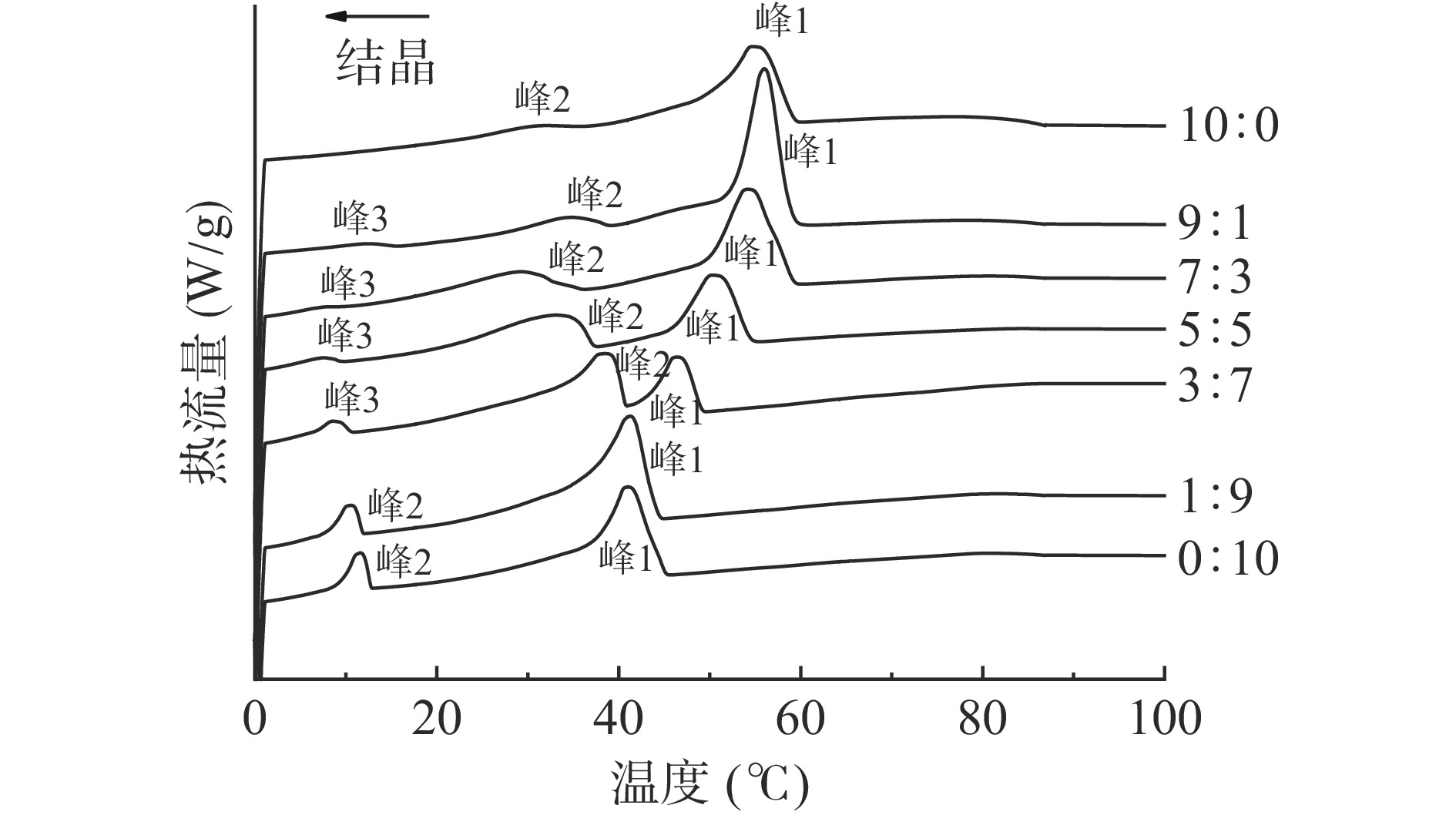
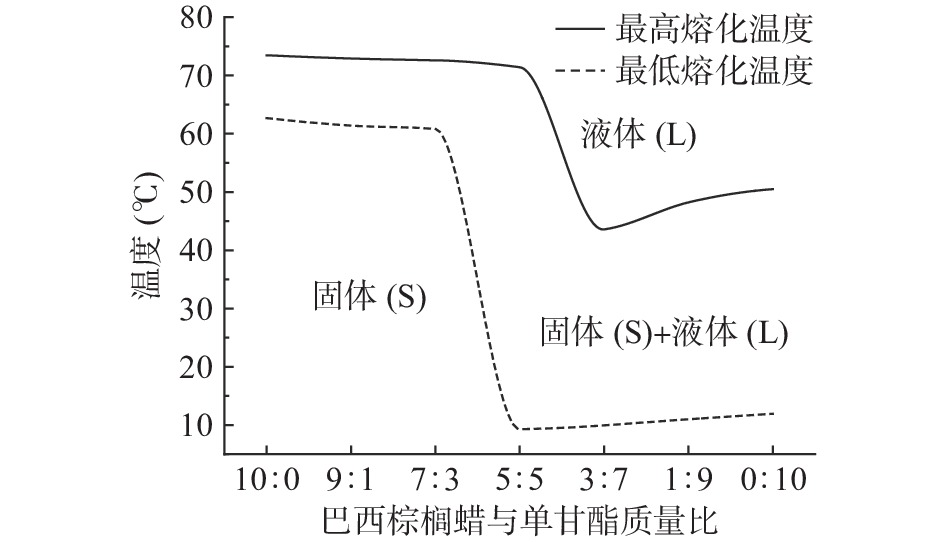
凝胶油熔化-结晶过程中DSC变化曲线如图3和图4所示,峰值温度和焓变数值见表1和表2,整个分析过程包括一次结晶和一次熔化。以熔融曲线绘制的伪相图如图5所示,下方的虚线表示最低的熔化起始温度,上方的实线表示最高熔化温度,实线的上方表示液态,中间部分是固体和液体的共存区域,虚线下方的区域代表固态[14]。
表 1 不同凝胶剂复配比例下凝胶油熔化过程中的峰值温度和熔化焓变Table 1. Peak temperatures and enthalpies of oleogels produced with different mass ratios of CW and MG in melting process样品 峰1 峰2 峰3 Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) 10:0 72.13±1.65a 7.25±0.18a − − − − 9:1 73.31±0.34a 6.52±0.55b − − − − 7:3 74.55±0.06a 3.97±0.76b − − − − 5:5 11.15±0.20d 0.61±0.22d 40.93±0.61c 1.78±0.27b 71.58±0.14a 2.75±0.21a 3:7 11.65±0.12cd 0.71±0.13d 43.47±0.61b 1.78±0.28b 70.43±0.17b 0.71±0.13b 1:9 12.96±0.48bc 1.20±0.26cd 48.40±0.40a 1.78±0.29a − − 0:10 13.78±0.70b 1.63±0.37c 49.80±1.36a 1.78±0.30a − − 注:表中各比例为CW与MG的质量比,同列不同小写字母表示有显著差异(P<0.05),表2同。 表 2 不同凝胶剂复配比例下凝胶油结晶过程中的峰值温度和结晶焓变Table 2. Peak temperatures and enthaplies of oleogels produced with different mass ratios of CW and MG in crystallization process样品 峰1 峰2 峰3 Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) 10:0 58.74±0.48b 7.02±0.21a 30.27±1.48d 0.28±0.02d − − 9:1 59.19±1.33a 6.44±1.09ab 34.80±1.47b 0.70±0.16cd 11.92±0.78a 0.21±0.07b 7:3 54.07±0.26c 4.39±0.77c 28.02±0.92e 1.26±0.53bc 6.92±0.40c 0.07±0.02c 5:5 51.10±0.83d 3.08±0.17d 32.60±0.92c 2.44±0.49a 7.57±0.21bc 0.18±0.05b 3:7 46.13±0.85e 1.19±0.40e 37.82±1.35a 1.65±0.62b 8.17±0.49b 0.37±0.04a 1:9 41.26±0.09f 5.07±0.54c 10.14±0.34f 0.76±0.15cd − − 0:10 40.35±0.72f 5.27±0.54bc 11.18±0.26f 0.86±0.09cd − − 在熔化过程中CW与MG质量比为10:0、9:1和7:3的凝胶油均出现一个吸热峰(图3),峰值温度分别为72.13±1.65、73.31±0.34、74.55±0.06 ℃(表1),少量MG的加入一定程度上提高了CW凝胶油的融化温度,即CW凝胶油的热稳定性有所增强;CW与MG质量比为3:7和5:5时凝胶油出现三个吸热峰(图3),三个峰值温度分别为11.65±0.12、43.47±0.61、70.43±0.17和11.15±0.20、40.93±0.61、71.58±0.14 ℃(表1),其中前两个峰是代表MG的融化峰,第三个峰是代表CW的融化峰;CW与MG质量比为1:9和0:10均出现两个吸热峰(图3),并且以上两个比例的两个吸热峰的峰值温度均随着MG含量的增加出现升高。随着凝胶剂中MG含量的增加,CW与MG质量比为5:5的凝胶油开始出现新的吸热峰,即代表MG的吸热峰开始出现并逐渐增强,而代表CW的吸热峰开始减小并在1:9时完全消失。以上情况表明MG可能没有影响CW的熔化行为,二者并没有形成共结晶,即出现了偏晶行为[31],因此很容易识别出二者的熔化峰。图5的伪相图也揭示了复配凝胶油的偏晶行为。
在结晶过程中CW凝胶油出现一个大的结晶峰和一个小而宽的结晶峰(图4),大的结晶峰可能与CW中的蜡酯含量有关[32],即较高熔点的蜡酯首先结晶,随后次要成分脂肪醇开始结晶;MG凝胶油出现两个结晶峰,第一个峰(40.35±0.72 °C)对应于各向同性→Lα相的转变,第二个峰(11.18±0.26 °C)对应于Lα→亚α相的转变[8,33]。CW与MG质量比为1:9和0:10的凝胶油均出现两个结晶峰,不同于单一CW和MG制备的凝胶油,CW与MG质量比为9:1、7:3、5:5和3:7的凝胶油均出现三个结晶峰。CW与MG质量比为9:1时,体系的第一结晶峰出现右移,即代表CW的结晶温度有所升高,说明此时MG晶体的存在促进了CW的结晶,随着体系中MG含量的增加同时CW含量的减少,MG结晶在体系中占主导地位,促进CW结晶的作用减弱。另一方面,随着CW的加入,与MG的Lα→亚α转变相关的结晶峰温度均向较低的温度转移(表2峰3),这说明CW的存在抑制了MG晶体在凝胶化过程中的多晶态转变[23]。由表1和表2可发现,凝胶油在熔化和结晶过程中的焓值变化不是简单的增加或减少,这说明CW和MG在结晶过程中发生了相互作用。
总的来说,当CW含量较少即CW与MG质量比为1:9时,凝胶油结晶熔化特性与MG制备的凝胶油相似,这可能是因为MG作为凝胶剂是通过自组装形成三维网络结构[34],而CW是通过结晶形成三维网络结构[35],当复合凝胶剂中CW较少时,凝胶油的形成方式是以MG的自组装为主,少量的CW晶体被包裹在MG自组装的三维结构中,所以在DSC分析中表现出MG凝胶油的性质。
2.4 不同CW与MG复配比对凝胶油硬度和持油性的影响
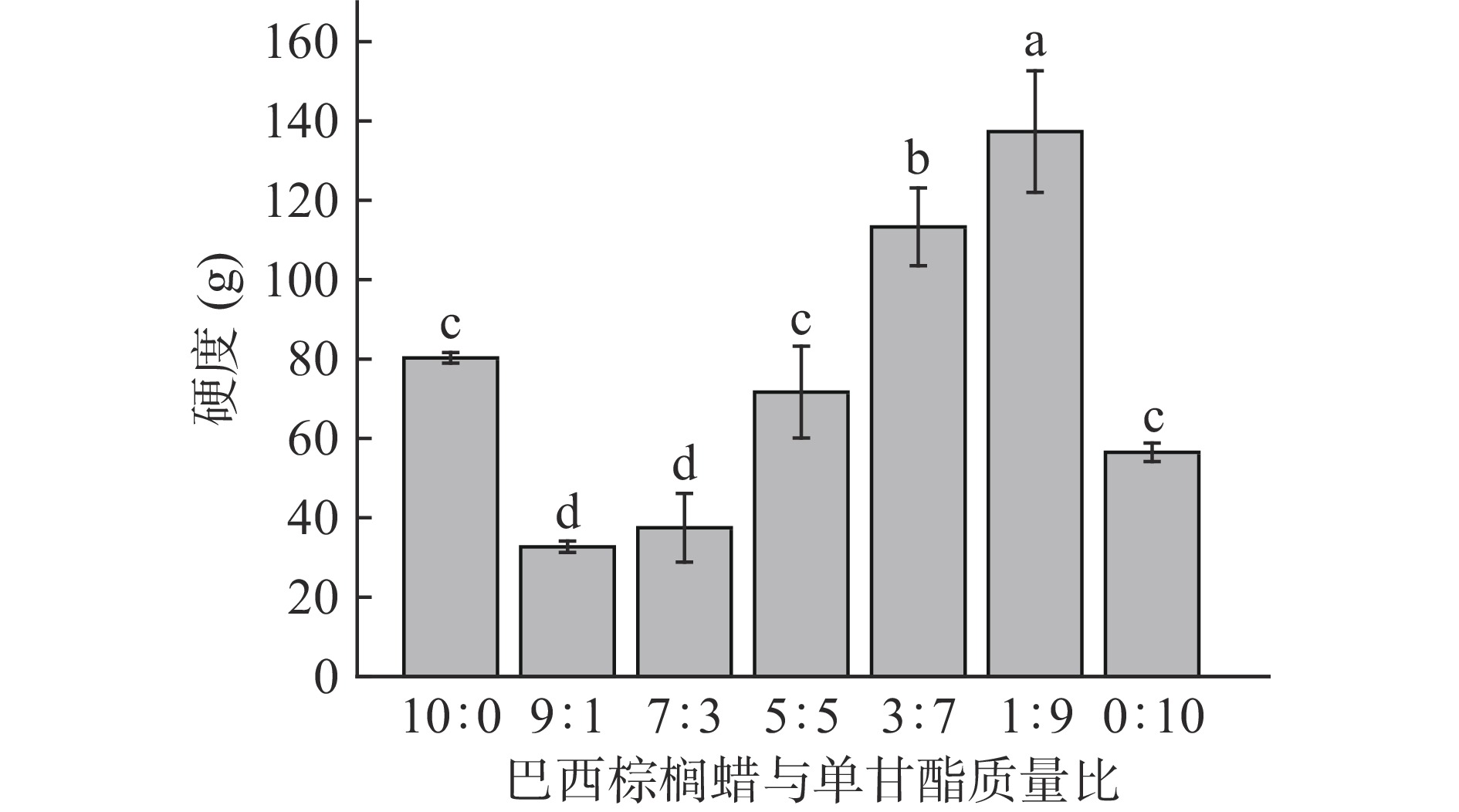
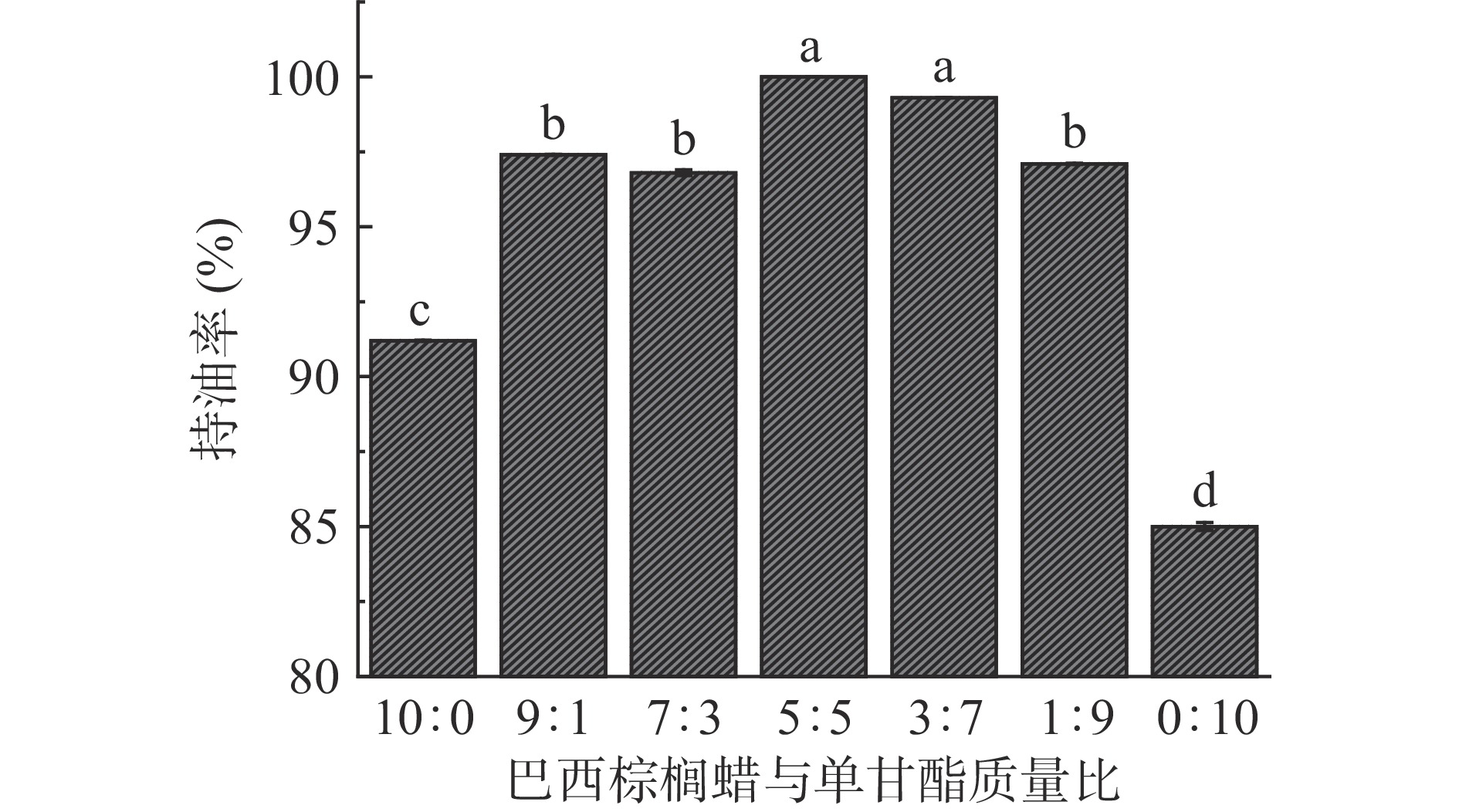
七种凝胶剂复配比例下均能形成稳定的凝胶结构。不同CW与MG质量比的凝胶油硬度如图6所示,持油性如图7所示。当体系中含有少量MG即CW与MG质量比为9:1和7:3时,体系的硬度较CW凝胶油显著下降(P<0.05),这是因为低浓度MG的加入干扰了凝胶结构;当二者质量比达到5:5并随着MG含量的增多和CW含量的减少,体系硬度显著增大(P<0.05),在1:9时达到最大硬度137.33 g,显著高于两种单一凝胶剂制备的凝胶油(P<0.05),这是因为CW和MG在适当的比例下,CW的晶体结构与MG自组装的三维结构相互结合,形成密度较大的小晶体,凝胶体系的一致性得到提高,形成的网络更耐形变,体系硬度增大,这与微观结构的观察结果相符。如图7所示,由MG制备的凝胶油具有相对较低的持油率仅为85%,研究表明MG制备的凝胶油在储存过程中容易发生多晶型转变,在MG凝胶油中β晶型表现出较大的晶体聚集,这损害了凝胶的油结合能力导致体系稳定性降低,持油能力较弱[36],而CW制备的凝胶油在常见的天然蜡基凝胶油中也具有相对较低的持油性[14],与本文得到的结论一致。由图7可以看出,CW与MG复配使用可以显著提高单一凝胶剂凝胶油的持油性(P<0.05),当二者质量比为5:5时体系持油性最佳,持油率达到100%。因此,实际生产中应保持CW与MG质量比在5:5和3:7之间,此时析油率不超过1%,属于可接受范围。
![]() 图 6 不同CW与MG质量比下凝胶油的硬度注:图中不同小写字母表示差异显著(P<0.05),图7同。Figure 6. Hardness of oleogels produced with different mass ratios of CW and MG
图 6 不同CW与MG质量比下凝胶油的硬度注:图中不同小写字母表示差异显著(P<0.05),图7同。Figure 6. Hardness of oleogels produced with different mass ratios of CW and MG整体而言,随着CW与MG质量比的降低,凝胶油的硬度和持油率并非呈现单一的上升或下降趋势,这可能是由于凝胶油的结晶尺寸、结晶形状以及结晶度的改变引起的,体系中固相物质含量发生变化,体系饱和度改变,凝胶油的硬度和持油性产生复杂的变化。此外,还可推断出凝胶油的持油性与硬度并没有必然的联系,即硬度较大的凝胶油不一定具有较高的持油性。
2.5 不同CW与MG复配比对凝胶油SFC的影响
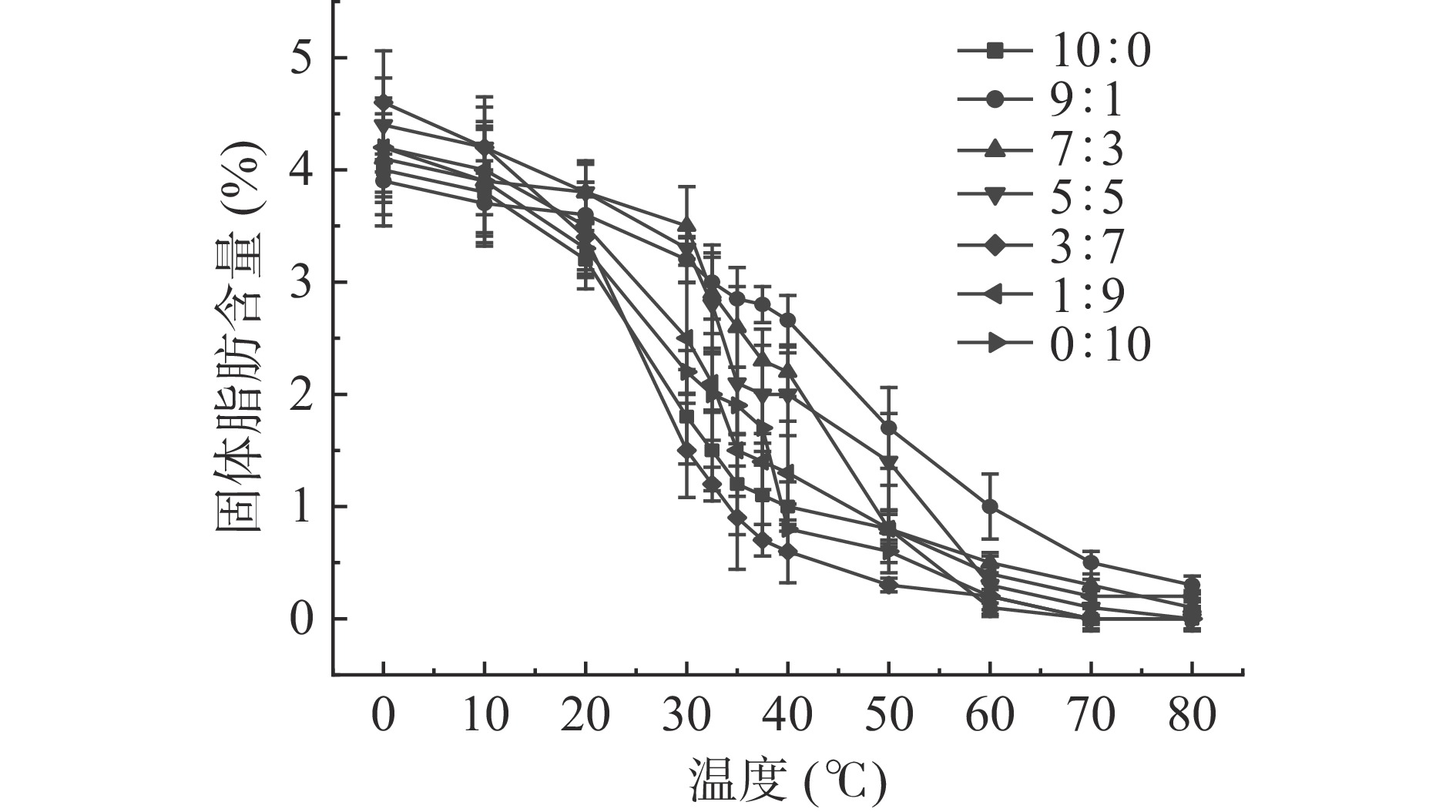
固体脂肪含量(solid fat content,SFC)是指在给定温度下,油相中的总固体含量。SFC曲线通过固体脂肪含量随温度的变化反映出塑性脂肪的熔化范围,提供了有关加工过程中不同温度下脂肪熔化特性的信息,特别是用于评价塑性脂肪在接近体温时的熔化性质即口熔性[37],从而确定其在食品体系中的用途,是评价食品专用油脂产品功能特性的重要指标之一[38]。作为固体脂肪的替代品,SFC值得进一步关注,特别是在室温(20 ℃左右)和体温(37 ℃左右)下。
如图8所示,在5%凝胶剂浓度下,随着温度的升高,所有比例凝胶油的SFC均呈明显下降的趋势。对于CW和MG凝胶油,二者在相同浓度下SFC随温度变化的趋势基本一致,在30~40 ℃下,MG凝胶油的SFC略高于CW凝胶油;一定量MG的加入可以提高CW凝胶油的SFC,一定程度上改善了CW凝胶油固体脂肪含量不足的缺陷。当体系中含有少量MG(9:1和7:3),SFC在0~30 ℃变化较为平缓,说明其SFC在该温度范围内不会发生明显的变化,在室温下有着较为良好的涂抹性,此时7:3比例下的SFC高于9:1;当温度超过30 ℃到达37.5 ℃时,7:3比例下的SFC快速下降,说明其在口腔温度下能够快速熔化,并在温度超过32.5 ℃时开始低于9:1比例下的SFC,但在40 ℃仍有少量的固体脂肪存在,说明其在口腔温度下没能完全熔化,仍有少量的晶体存在,具有少量的蜡质口感[39],可考虑利用甜味剂掩盖极少量的蜡质口感;而9:1比例下的SFC在30~37.5 ℃的变化则相对平缓,当体系温度超过40 ℃,9:1和7:3比例下的SFC再次快速下降,说明此时的晶体结构破坏程度更深,并且在7:3比例下的下降速率大于9:1,并具有相对较低的SFC。当体系MG含量继续增加至5:5时,SFC在30~37.5 ℃的下降速度继续加快并且有着更低的SFC。当体系中含有较多 MG 时,即 CW 与 MG 比例为 3:7和1:9时,SFC在20 ℃的下降速率明显加快,尤其在35 ℃(接近体温)时SFC都到达了更低的水平,其中3:7比例下的凝胶油在30~37.5 ℃的SFC明显低于CW和MG凝胶油,即在口腔温度附近具有相对更少的晶体存在,说明此时MG的加入对凝胶油体系口感的改善起到了正向作用。
3. 结论
不同CW与MG的复配比对高油酸葵花籽油凝胶油的微观形态、凝胶晶型、热力学性质、硬度、持油性以及SFC都有一定的影响。5%浓度下,CW与MG共同存在会相互影响彼此的结晶形态;七种凝胶油样品均含有较多的β型晶体,适宜应用于巧克力或烘培起酥油制品,少量MG的加入会显著降低CW凝胶油的硬度(P<0.05),一定程度上改善了天然蜡基凝胶油硬度过硬的问题,MG晶体会在一定程度上促进CW的结晶,同时CW会抑制MG晶体的多晶态转变,有利于提高凝胶油体系的储藏稳定性,MG的加入也可以显著提高CW凝胶油的持油性(P<0.05),二者复配比为5:5时体系持油性最佳,达到100%,CW与MG比例为3:7时的凝胶油在30~37.5 ℃的SFC明显低于CW和MG凝胶油,此时MG的加入对体系口感的改善起到了正向作用。本研究初步探究了CW和MG两种凝胶剂复配使用时对凝胶油的结构和性质的变化规律,为天然蜡-单甘酯凝胶油在食品专用油脂的应用提供了一定的理论参考,但尚未进行全面且深入的应用研究,是今后重点的研究方向。
-
图 6 不同CW与MG质量比下凝胶油的硬度
注:图中不同小写字母表示差异显著(P<0.05),图7同。
Figure 6. Hardness of oleogels produced with different mass ratios of CW and MG
表 1 不同凝胶剂复配比例下凝胶油熔化过程中的峰值温度和熔化焓变
Table 1 Peak temperatures and enthalpies of oleogels produced with different mass ratios of CW and MG in melting process
样品 峰1 峰2 峰3 Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) 10:0 72.13±1.65a 7.25±0.18a − − − − 9:1 73.31±0.34a 6.52±0.55b − − − − 7:3 74.55±0.06a 3.97±0.76b − − − − 5:5 11.15±0.20d 0.61±0.22d 40.93±0.61c 1.78±0.27b 71.58±0.14a 2.75±0.21a 3:7 11.65±0.12cd 0.71±0.13d 43.47±0.61b 1.78±0.28b 70.43±0.17b 0.71±0.13b 1:9 12.96±0.48bc 1.20±0.26cd 48.40±0.40a 1.78±0.29a − − 0:10 13.78±0.70b 1.63±0.37c 49.80±1.36a 1.78±0.30a − − 注:表中各比例为CW与MG的质量比,同列不同小写字母表示有显著差异(P<0.05),表2同。 表 2 不同凝胶剂复配比例下凝胶油结晶过程中的峰值温度和结晶焓变
Table 2 Peak temperatures and enthaplies of oleogels produced with different mass ratios of CW and MG in crystallization process
样品 峰1 峰2 峰3 Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) Tp(℃) ∆H(J∙g−1) 10:0 58.74±0.48b 7.02±0.21a 30.27±1.48d 0.28±0.02d − − 9:1 59.19±1.33a 6.44±1.09ab 34.80±1.47b 0.70±0.16cd 11.92±0.78a 0.21±0.07b 7:3 54.07±0.26c 4.39±0.77c 28.02±0.92e 1.26±0.53bc 6.92±0.40c 0.07±0.02c 5:5 51.10±0.83d 3.08±0.17d 32.60±0.92c 2.44±0.49a 7.57±0.21bc 0.18±0.05b 3:7 46.13±0.85e 1.19±0.40e 37.82±1.35a 1.65±0.62b 8.17±0.49b 0.37±0.04a 1:9 41.26±0.09f 5.07±0.54c 10.14±0.34f 0.76±0.15cd − − 0:10 40.35±0.72f 5.27±0.54bc 11.18±0.26f 0.86±0.09cd − − -
[1] PEHLIVANOGLU H, DEMIRCI M, TOKER O S, et al. Oleogels, a promising structured oil for decreasing saturated fatty acid concentrations: Production and food-based applications[J]. Critical Reviews in Food Science and Nutrition,2018,58(8):1330−1341. doi: 10.1080/10408398.2016.1256866
[2] 钟金锋, 覃小丽, 刘雄. 凝胶油及其在食品工业中的应用研究进展[J]. 食品科学,2015,36(3):272−279. [ZHONG J F, QIN X L, LIU X. Advances in oleogels and their applications in food industry[J]. Food Science,2015,36(3):272−279. doi: 10.7506/spkx1002-6630-201503051 [3] OSUNA M B, ROMERO A M, AVALLONE C M, et al. Animal fat replacement by vegetable oils in formulations of breads with flour mixes[J]. Journal of Food Science and Technology,2018,55(3):858−867. doi: 10.1007/s13197-017-2888-x
[4] CUI X T, SALEH A S M, YANG S, et al. Oleogels as animal fat and shortening replacers: Research advances and application challenges[J]. Food Reviews International,2022:1−22.
[5] HUGHES N E, MARANGONI A G, WRIGHT A J, et al. Potential food applications of edible oil organogels[J]. Trends in Food Science & Technology,2009,20(10):470−480.
[6] SHAKEEL A, FAROOQ U, GABRIELE D, et al. Bigels and multi-component organogels: An overview from rheological perspective[J]. Food Hydrocolloids,2021,111:106190. doi: 10.1016/j.foodhyd.2020.106190
[7] YILMAZ E, USLU E K, TOKSOZ B. Structure, rheological and sensory properties of some animal wax based oleogels[J]. Journal of Oleo Science,2020,69(10):1317−1329. doi: 10.5650/jos.ess20081
[8] LI J X, GUO R H, BI Y L, et al. Comprehensive evaluation of saturated monoglycerides for the forming of oleogels[J]. LWT,2021,151:112061. doi: 10.1016/j.lwt.2021.112061
[9] SUN P, XIA B, NI Z J, et al. Characterization of functional chocolate formulated using oleogels derived from β-sitosterol with γ-oryzanol/lecithin/stearic acid[J]. Food Chemistry,2021,360:130017. doi: 10.1016/j.foodchem.2021.130017
[10] SHENGLAN G, MINGYUE S, XIANGYANG G, et al. Assembly pattern of multicomponent supramolecular oleogel composed of ceramide and lecithin in sunflower oil: Self-assembly or self-sorting?[J]. Food & Function,2020,11(9):7651−7660.
[11] ASHKAR A, LAUFER S, ROSEN-KLIGVASSER J, et al. Impact of different oil gelators and oleogelation mechanisms on digestive lipolysis of canola oil oleogels[J]. Food Hydrocolloids,2019,97:105218. doi: 10.1016/j.foodhyd.2019.105218
[12] 李英豪, 耿延训, 徐化能. 乙酰化纳米纤维素纤维的制备及其凝胶机制研究[J]. 高校化学工程学报,2018,32(1):208−214. [LI Y H, GENG Y X, XU H N. Preparation of acetylated cellulose nanofibrils and its gelation behavior[J]. Journal of Chemical Engineering of Chinese Universities,2018,32(1):208−214. doi: 10.3969/j.issn.1003-9015.2018.01.028 [13] 姜宗伯, 徐军, 石芬, 等. 羟丙基甲基纤维素和黄原胶浓度对初榨椰子油乳液及其模板油凝胶构建的影响[J]. 食品工业科技,2022,43(7):102−109. [JIANG Z B, XU J, SHI F, et al. Effect of different polysaccharide concentration on the construction of virgin coconut oilgel[J]. Science and Technology of Food Industry,2022,43(7):102−109. [14] SHI Y F, LIU C H, ZHENG Z J, et al. Gelation behavior and crystal network of natural waxes and corresponding binary blends in high-oleic sunflower oil[J]. Journal of Food Science,2021,86(9):3987−4000. doi: 10.1111/1750-3841.15840
[15] 司昀灵, 胡招龙, 邹立强, 等. 单甘酯与蜂蜡复配制备五步蛇蛇油基凝胶油的研究[J]. 中国油脂,2019,44(7):147−152. [SI Y L, HU Z L, ZOU L Q, et al. Preparation of snake (Deinagkistrodon acutus) oil organogel with beeswax and monoglyceride[J]. China Oils and Fats,2019,44(7):147−152. [16] GRAVELLE A J, BLACH C, WEISS J, et al. Structure and properties of an ethylcellulose and stearyl alcohol/stearic acid (EC/SO: SA) hybrid oleogelator system[J]. European Journal of Lipid Science and Technology,2017,119(11):1700069. doi: 10.1002/ejlt.201700069
[17] DE FREITAS C A S, DE SOUSA P H M, SOARES D J, et al. Carnauba wax uses in food: A review[J]. Food Chemistry,2019,291:38−48. doi: 10.1016/j.foodchem.2019.03.133
[18] DOAN C D, TO C M, DE VRIEZE M, et al. Chemical profiling of the major components in natural waxes to elucidate their role in liquid oil structuring[J]. Food Chemistry,2017,214:717−725. doi: 10.1016/j.foodchem.2016.07.123
[19] DOAN C D, TAVERNIER I, OKURO P K, et al. Internal and external factors affecting the crystallization, gelation and applicability of wax-based oleogels in food industry[J]. Innovative Food Science & Emerging Technologies,2018,45:42−52.
[20] 刘国琴, 南阳, 刘新旗. 单甘酯添加量对油脂凝胶物理性质与晶体结构的影响[J]. 华南理工大学学报(自然科学版),2016,44(11):1−6. [LIU G Q, NAN Y, LIU X Q. Effects of monoglyceride addition on physical properties and crystal structure of oleogels[J]. Journal of South China University of Technology (Natural Science Edition),2016,44(11):1−6. [21] UTCU M, YLMAZ E. Oleogels of virgin olive oil with carnauba wax and monoglyceride as spreadable products[J]. Grasas y Aceites,2014,65(3):40. doi: 10.3989/gya.0349141
[22] 杨帅帅, 杨国龙, 刘伟, 等. 棕榈酸单甘酯-巴西棕榈蜡大豆油凝胶热性质及结晶动力学研究[J]. 河南工业大学学报(自然科学版),2020,41(5):9−15, 30. [YANG S S, YANG G L, LIU W, et al. Study on the thermal properties and crystallization behaviors of soybean oleogel formed with monopalmitate and carnauba wax[J]. Journal of Henan University of Technology (Natural Science Edition),2020,41(5):9−15, 30. [23] LI J, GUO R, WANG M, et al. Development and characterization of compound oleogels based on monoglycerides and edible waxes[J]. ACS Food Science & Technology,2022,2(2):302−314.
[24] 史逸飞, 刘春环, 郑召君, 等. 小烛树蜡和日本木蜡对高油酸葵花籽油凝胶油结晶行为的差异比较[J]. 中国油脂,2022,47(2):51−57. [SHI Y F, LIU C H, ZHENG Z J, et al. Comparison of candelilla wax and Japan lacquer wax on crystalline behavior of high-oleic sunflower seed oil oleogels[J]. China Oils and Fats,2022,47(2):51−57. [25] KANAGARATNAM S, ENAMUL HOQUE M, MAT SAHRI M, et al. Investigating the effect of deforming temperature on the oil-binding capacity of palm oil based shortening[J]. Journal of Food Engineering,2013,118(1):90−99. doi: 10.1016/j.jfoodeng.2013.03.021
[26] DASSANAYAKE L S K, KODALI D R, UENO S, et al. 7-Physical properties of organogels made of rice bran wax and vegetable oils[M]//MARANGONI A G, GARTI N. Edible oleogels. AOCS Press. 2011: 149-172.
[27] FAYAZ G, GOLI S A H, KADIVAR M, et al. Potential application of pomegranate seed oil oleogels based on monoglycerides, beeswax and propolis wax as partial substitutes of palm oil in functional chocolate spread[J]. LWT,2017,86:523−529. doi: 10.1016/j.lwt.2017.08.036
[28] 汪鸿, 孙立斌, 张亮, 等. 小烛树蜡油脂凝胶的性质及作用机理研究[J]. 中国粮油学报,2021,36(6):91−95. [WANG H, SUN L B, ZHANG L, et al. Study on the properties and mechanism of oil gel of candelaria wax[J]. Journal of the Chinese Cereals and Oils Association,2021,36(6):91−95. doi: 10.3969/j.issn.1003-0174.2021.06.015 [29] 朱小勇, 孟宗, 李进伟, 等. 凝胶剂种类对凝胶油物性及结晶形态的影响[J]. 中国粮油学报,2013,28(10):37−43. [ZHU X Y, MENG Z, LI J W, et al. Effect of different kinds of gelators on physical properties and crystal morphology of oleogels[J]. Joumal of the Chinese Cereals and Oils Association,2013,28(10):37−43. [30] CHOPIN-DOROTEO M, MORALES-RUEDA J A, DIBILDOX-ALVARADO E, et al. The effect of shearing in the thermo-mechanical properties of candelilla wax and candelilla wax-tripalmitin organogels[J]. Food Biophysics,2011,6(3):359−376. doi: 10.1007/s11483-011-9212-5
[31] JANA S, MARTINI S. Phase behavior of binary blends of four different waxes[J]. Journal of the American Oil Chemists Society,2016,93(4):543−554. doi: 10.1007/s11746-016-2789-6
[32] 张华丹, 张玲云, 周静, 等. 基于三种植物蜡构建大黄鱼鱼油凝胶体系及其微观结构的研究[J]. 食品与发酵工业,2022,48(1):153−160. [ZHANG H D, ZHANG L Y, ZHOU J, et al. Study on the gel system and microstructure of large yellow croaker fish oil based on three kinds of plant wax[J]. Food and Fermentation Industries,2022,48(1):153−160. [33] LUTTON E S. The phases of saturated 1-monoglycerides C14-C22[J]. Journal of the American Oil Chemists' Society,1971,48(12):778−781. doi: 10.1007/BF02609279
[34] CHEN C-H, TERENTJEV E M. Chapter 5-monoglycerides in oils[M]//MARANGONI A G, GARTI N. Edible oleogels (Second Edition). AOCS Press. 2018: 103-131.
[35] BLAKE A I, TORO-VAZQUEZ J F, HWANG H-S. Chapter 6-wax oleogels[M]//MARANGONI A G, GARTI N. Edible oleogels (Second Edition). AOCS Press. 2018: 133-171.
[36] BIN SINTANG M D, DANTHINE S, BROWN A, et al. Phytosterols-induced viscoelasticity of oleogels prepared by using monoglycerides[J]. Food Research International,2017,100:832−840. doi: 10.1016/j.foodres.2017.07.079
[37] OGUTCU M, ARIFOGLU N, YILMAZ E. Storage stability of cod liver oil organogels formed with beeswax and carnauba wax[J]. International Journal of Food Science and Technology,2015,50(2):404−412. doi: 10.1111/ijfs.12612
[38] YILMAZ E, ÖĞÜTCÜ M. Properties and stability of hazelnut oil organogels with beeswax and monoglyceride[J]. Journal of the American Oil Chemists' Society,2014,91(6):1007−1017. doi: 10.1007/s11746-014-2434-1
[39] JANA S, MARTINI S. Physical characterization of crystalline networks formed by binary blends of waxes in soybean oil[J]. Food Research International,2016,89:245−253. doi: 10.1016/j.foodres.2016.08.003
-
期刊类型引用(7)
1. 尹蓉,张倩茹,王俊宇,茹建生,杨德宇,梁志宏. 不同鲜果发酵酒的品质分析. 果树资源学报. 2024(02): 67-73 .  百度学术
百度学术
2. 王喻,姚昕,徐嘉俊,涂勇. 玫瑰茄石榴复合果酒发酵工艺优化及挥发性香气成分分析. 中国酿造. 2024(10): 170-177 .  百度学术
百度学术
3. 邓乔允,夏爽,韩小雨,游义琳,黄卫东,战吉宬. 梨酒中酵母的研究进展. 食品与发酵工业. 2024(21): 349-356 .  百度学术
百度学术
4. 尹蓉,张倩茹,王俊宇,梁志宏. 13个品种红枣发酵酒的品质差异分析. 食品工业科技. 2023(05): 277-284 .  本站查看
本站查看
5. 张卓睿,孙冰瑶,夏明钰,高慧华,程兴月,杨海龙,姜贵全. 刺玫果山荆子桤叶唐棣复合果酒的研制. 中国酿造. 2023(09): 187-192 .  百度学术
百度学术
6. 牛佳佳,张柯,崔巍,郭超峰,徐振玉,鲁云风,苗建银,张四普. 不同品种梨发酵果酒品质评价及挥发性化合物分析. 食品安全质量检测学报. 2022(17): 5468-5476 .  百度学术
百度学术
7. 马烁,赵华. 不同发酵工艺对香水梨酒品质指标及香气成分的影响. 中国酿造. 2022(11): 135-139 .  百度学术
百度学术
其他类型引用(4)








 下载:
下载:
 下载:
下载:



