Determination of Nitrite and Sulfite in Foods by Phenolic Acid-based Gold Nanoparticles Electrode
-
摘要: 基于酚酸良好的还原性和无污染性建立酚酸基纳米金传感体系,以实现亚硝酸盐和亚硫酸盐的灵敏检测。采用不同酚酸还原氯金酸制备纳米金(Gold nanoparticles,AuNPs),通过紫外光谱和交流阻抗法获得还原效果最佳的酚酸为没食子酸(Gallic acid,GA)。利用电沉积法制备GA@AuNPs@Au电极,并由线性扫描伏安法(Linear scanning voltammetry,LSV)表征亚硝酸盐和亚硫酸盐的电化学行为。优化体系条件为:GA浓度1 mmol/L、孵育温度70 ℃、反应时间60 min、pH6.0磷酸盐缓冲溶液浓度0.15 mol/L。亚硝酸盐和亚硫酸盐浓度在0.001~7 mmol/L范围内与氧化峰电流分别呈良好的线性关系(R2>0.994),检出限分别为0.20 μmol/L和0.24 μmol/L(S/N=3)。该修饰电极的重现性和稳定性良好,可用于实际样品中亚硝酸盐和亚硫酸盐的同时测定。Abstract: Based on the good reducibility and non-pollution of phenolic acid, the phenolic acid-based gold nanosensor system was established to realize sensitive detection of nitrite and sulfite. Different phenolic acids were used to reduce chlorauric acid to prepare gold nanoparticles (AuNPs). The optimal phenolic acid was gallic acid (GA) by ultraviolet spectrum and electrochemical impedance spectrum method. The GA@AuNPs@Au electrodes were prepared by electrodeposition and the electrochemical behaviors of nitrite and sulfite were characterized by linear scanning voltammetry (LSV). The optimized system conditions were as follows: GA concentration 1 mmol/L, incubation temperature 70 ℃, reaction time 60 min, pH6.0 phosphate buffer solution concentration 0.15 mol/L. The concentration of nitrite and sulfite in the range of 0.001 to 7 mmol/L showed a good linear relationship with the peak oxidation current (R2>0.994), and the detection limits were 0.20 μmol/L and 0.24 μmol/L (S/N=3), respectively. The modified electrode has good reproducibility and stability, and it can be used for the simultaneous determination of nitrite and sulfite in real samples.
-
Keywords:
- phenolic acid /
- gold nanoparticles /
- modified electrode /
- nitrite /
- sulfite
-
亚硝酸盐(NO2−)和亚硫酸盐(SO32−)是常见的食品添加物。NO2−可通过与肌红蛋白形成亚硝基肌红蛋白,使肉制品保持颜色新鲜,被用作食品着色剂;还可通过分解为NO,与高铁肌红蛋白生成亚硝基肌红蛋白,起到稳定血红蛋白与肌红蛋白结构的作用,被用作食品防腐剂[1]。SO32−可抑制食品的非酶褐变和酶促褐变;同时也能防止食品在生产过程中发生氧化变质、细菌生长等问题,在延长产品保质期方面发挥着重要作用[2]。食品中的NO2−和SO32−除外源添加,还可在食品加工和贮藏过程中由其自身合成[3]。饮用水经长时间加热,其中微量的NO3−受热会被分解为NO2−;食品储存不当时所滋生的大量细菌也可将NO3−转化成NO2−。对于人体而言,摄入过多的NO2−或SO32−会出现头痛、头晕,呼吸麻痹等病症[4]。因此,食品中NO2−和SO32−含量的检测应受到广泛关注。
当前对NO2−和SO32−同时检测的方法有分光光度法[5]、色谱法[6]、荧光法[7]、电化学[8]等,其中比色、光谱和色谱方法分别存在灵敏度低、分析时间长、稳定性差等问题。而电化学法具有简单、快速、高灵敏度等优点。Zhang等[9]采用溶胶-凝胶法和水热法合成了Fe3O4@SiO2纳米颗粒的电化学传感器,用于NO2−和 SO32−的检测,重现性和重复性较好。Bagheri等[10]制备了一种基于多壁碳纳米管还原氧化石墨烯上铜金属纳米颗粒的新型电化学传感器(Cu/MWCNT/RGO),用于NO2−和 SO32−的同时测定。目前电化学方法检测NO2−和SO32−时所使用的修饰电极材料主要集中于金属(Fe、Ni、Cu、Cd)与非金属纳米复合材料(如石墨、碳纳米管),但这些修饰电极材料存在着稳定性差、修饰较难、电极材料不环保等缺陷。而以AuNPs为材料所制备的电化学传感器在灵敏度、选择性、稳定性等方面具有显著优势,可实现对食品中有毒有害物质的测定。Wei等[11]以纳米金颗粒为材料制备了一种金纳米颗粒/石墨化碳毡(AuNPs/GCFE)电化学传感器,可以快速方便地检测NO2−且具有良好的特异性。Yu等[12]以乙二醇(EG)为还原剂,合成了金纳米颗粒还原氧化石墨烯复合材料(AuNPs-rGO),利用所制备的AuNPs-rGO/GCE电极对SO32−含量进行测定。目前AuNPs的制备方法主要基于传统的柠檬酸钠还原法,但该方法所制备的AuNPs稳定性差、分散性不好,且不具备环保性[13]。因此,研究人员关注于利用生物有机体和植物来合成环保绿色的金属纳米粒子。Taib等[14]以木槿叶的水提取物为还原剂和稳定剂,通过绿色生物合成途径合成了AuNPs,并制备了AuNPs/GCE修饰电极实现对NO2−的测定,该电极对NO2−检测限可达到0.11 mmol/L。但基于由绿色生物体合成AuNPs且同时实现NO2−和SO32−测定的研究未见,因此可构建电化学传感体系做进一步探究。
本文利用植物酚酸还原合成分散性良好的纳米金,使其分散在修饰电极表面,构建电传感体系用于食品中NO2−和SO32−的同时检测。通过紫外光谱和电化学表征方法优化酚酸种类,利用荧光光谱对GA还原HAuCl4合成AuNPs的过程进行监控,并采用电沉积方法制备GA@AuNPs@Au修饰电极。以循环伏安法(Cyclic voltammetry,CV)和交流阻抗法(Electrochemical impedance spectrum,EIS)对修饰电极电化学性能进行表征;以LSV法考察孵育温度、反应时间、缓冲溶液种类、缓冲溶液pH、缓冲溶液浓度对NO2−和SO32−检测体系的影响并对各条件进行优化。最后利用稀释至不同浓度梯度的实际样品来考察方法的准确性,以期获得高灵敏度、高稳定性、快速响应的酚酸基纳米金传感器检测体系,为食品中NO2−和SO32−的同时检测提供参考。
1. 材料与方法
1.1 材料与仪器
没食子酸(98%)、高原儿茶酸(98%)、芥子酸(98%)、龙胆酸(99%)、咖啡酸(99.16%)、香草酸(98%)、阿魏酸(98%)、对香豆酸(98%)、氯金酸HAuCl4 阿拉丁试剂有限公司;铁氰化钾、氯化钾 天津市博迪化工股份有限公司;亚硝酸钠、亚硫酸钠 天津市富宇精细化工有限公司;鱿鱼丝 龙口市恒洋食品有限公司;红葡萄酒 山东省格汀酒液集团有限公司;盐田冻虾、卷心菜、辣白菜 购于当地超市;牡丹花茶、迷迭香茶、白梅花茶 滁州良辑贸易有限公司;所用其他试剂均为分析纯。
BSA224S电子天平、BSA2202S电子天平 北京赛多利斯科学仪器有限公司;DHG-9203A 型电热恒温鼓风干燥箱 上海恒科仪器有限公司;HDL洁净工作台 北京东联哈尔仪器制造有限公司;PB-10 pH计 赛丽朵思公司;PGSTAT302N 电化学工作站 瑞士万通中国有限公司;Pt 213 铂电极、R0302 氯化银电极 天津艾达试剂公司;φ=3 mm金盘电极 上海辰华仪器公司;UV-2550 紫外光谱仪 日本岛津公司。
1.2 实验方法
1.2.1 GA还原HAuCl4反应条件的优化
分别在20 mL锥形瓶中加入3 mL 3 mmol/L HAuCl4溶液、1 mL 2 mmol/L pH4.5的乙酸,500 μL 1 mmol/L不同种类的酚酸(高原儿茶酸、香草酸、芥子酸、咖啡酸、龙胆酸、没食子酸、阿魏酸、对香豆酸),水浴(70 ℃,30 min),在紫外光谱400~700 nm波长下扫描。将上述酚酸还原的AuNPs溶液,于−0.8~2.0 V电势内,电沉积扫速为0.15 V/s,扫描圈数25圈,通过EIS对比八种酚酸还原HAuCl4制备的酚酸基AuNPs在电极表面的电子转移速率。
通过紫外光谱(400~800 nm波长下)和EIS,在HAuCl4孵育温度70 ℃、反应时间60 min时,考察不同浓度GA(0.5、1.0、1.5、2.0、2.5、3.0 mmol/L)对还原HAuCl4合成AuNPs的影响;在GA浓度1.0 mmoL/L、反应时间60 min时,考察不同HAuCl4孵育温度(室温、30、40、50、60、70 ℃)对合成AuNPs的影响;在GA浓度1.0 mmoL/L、孵育温度70 ℃,考察不同反应时间(10、20、30、40、50、60、70 min)对合成AuNPs的影响。
1.2.2 荧光光谱监控GA还原HAuCl4合成纳米金过程
在比色皿中加入1 mL 3 mmol/L HAuCl4、1 mL 2mmol/L pH4.5乙酸缓冲液,并滴加梯度体积0~1100 μL的GA(每隔3 min加入100 μL),在275 nm激发波长下测定荧光强度,观察其荧光光谱,设置波长范围为:450~550 nm。室温放置3 min再测试其荧光光谱,所用的激发波长为290 nm,狭缝宽度为5.0 nm/5.0 nm。观察金纳米簇对不同浓度的GA@AuNPs是否产生荧光强度的规律性变化。
1.2.3 修饰电极的制备及对NO2−和SO32−电化学行为考察
根据参考文献[15]制备裸金电极,采用一步电沉积法制备GA@AuNPs@Au。将打磨好的裸金电极置于装有3 mL由GA催化合成的0.9 mmol/L GA@AuNPs溶液中,于0~1.0 V电势内,扫速为0.15 mV/s,扫描圈数为25圈,制备GA@AuNPs@Au修饰电极,通过CV扫描和EIS图谱表征考察电沉积扫速对修饰电极电化学性能。
分别取1 mL 5 mmol/L NO2−、SO32−溶液、2 mL缓冲溶液置于电化学专用瓶中,当缓冲溶液为磷酸盐缓冲液(Phosphate buffered solution,PBS)、缓冲溶液pH6.0,考察不同缓冲液浓度(0.05、0.10、0.15、0.20、0.25、0.30 mol/L);当缓冲溶液浓度为0.15 mol/L PBS时,考察不同PBS pH(5.5、6.0、7.0、8.0、9.0);当缓冲溶液浓度为0.15 mol/L、缓冲溶液pH6.0时考察不同缓冲溶液种类(乙酸盐缓冲溶液、PBS、柠檬酸缓冲溶液)对NO2−和SO32−电化学行为的影响。电势范围0~1.0 V,扫描速度150 mV/s ,对NO2−和SO32−进行LSV测定并分析氧化峰电流变化。NO2−和SO32−的电化学行为过程如图1所示。
1.2.4 NO2−和SO32−标准曲线的测定
分别取5 mmol/L NO2−、SO32−溶液各1 mL,与0.15 mol/L pH6.0的PBS混合均匀后,电势范围为0~1.0 V,扫描速度为150 mV/s ,进行LSV测定。改变NO2−溶液的浓度(0.001、0.05、0.10、0.30、0.50、1.00、3.00、5.00、7.00 mmol/L)重复上述操作。改变SO32−溶液的浓度(0.001、0.05、0.10、0.30、0.50、1.00、3.00、5.00、7.00 mmol/L),进行重复实验。
1.2.5 抗干扰实验及重现性和稳定性
配制5 mmol/L的NO2−和SO32−,100倍浓度(0.5 mol/L)的抗坏血酸、乙醇、葡萄糖、草酸、蔗糖、柠檬酸、NaCl、ZnCl2、MgCl2、CaCl2、LiCl等抗干扰溶液,加入5 mmol/L的NO2−和SO32−各1 mL,再加入2 mL的PBS,用GA@AuNPs@Au修饰电极进行LSV测定,观察峰电流和峰电位有无明显变化。利用修饰电极对含有NO2−和SO32−的样品溶液进行重复测定(10次);并将制备好的修饰电极于室温下放置两周,再对样品溶液进行测定,确定电极的重现性与稳定性。
1.2.6 样品测定
选取新鲜的卷心菜、鱿鱼丝、红葡萄酒、盐田冻虾、辣白菜、牡丹花茶、迷迭香茶、白梅花茶作为样品,准确称取3.00 g,利用LSV法探究不同稀释倍数的样品对测定的影响。采用标准加入法对处理前后样品溶液中NO2−和SO32−的加标回收率进行平行测定3次,计算测定样品中的NO2−和SO32−含量及回收率。
1.3 数据处理
所有实验均重复3次,采用Origin 2021软件作图和SPSS 28.0软件,以LSD法进行显著性分析,显著性水平P<0.05。
2. 结果与分析
2.1 酚酸还原氯金酸制备纳米金优化条件
2.1.1 不同酚酸还原HAuCl4制备AuNPs的影响
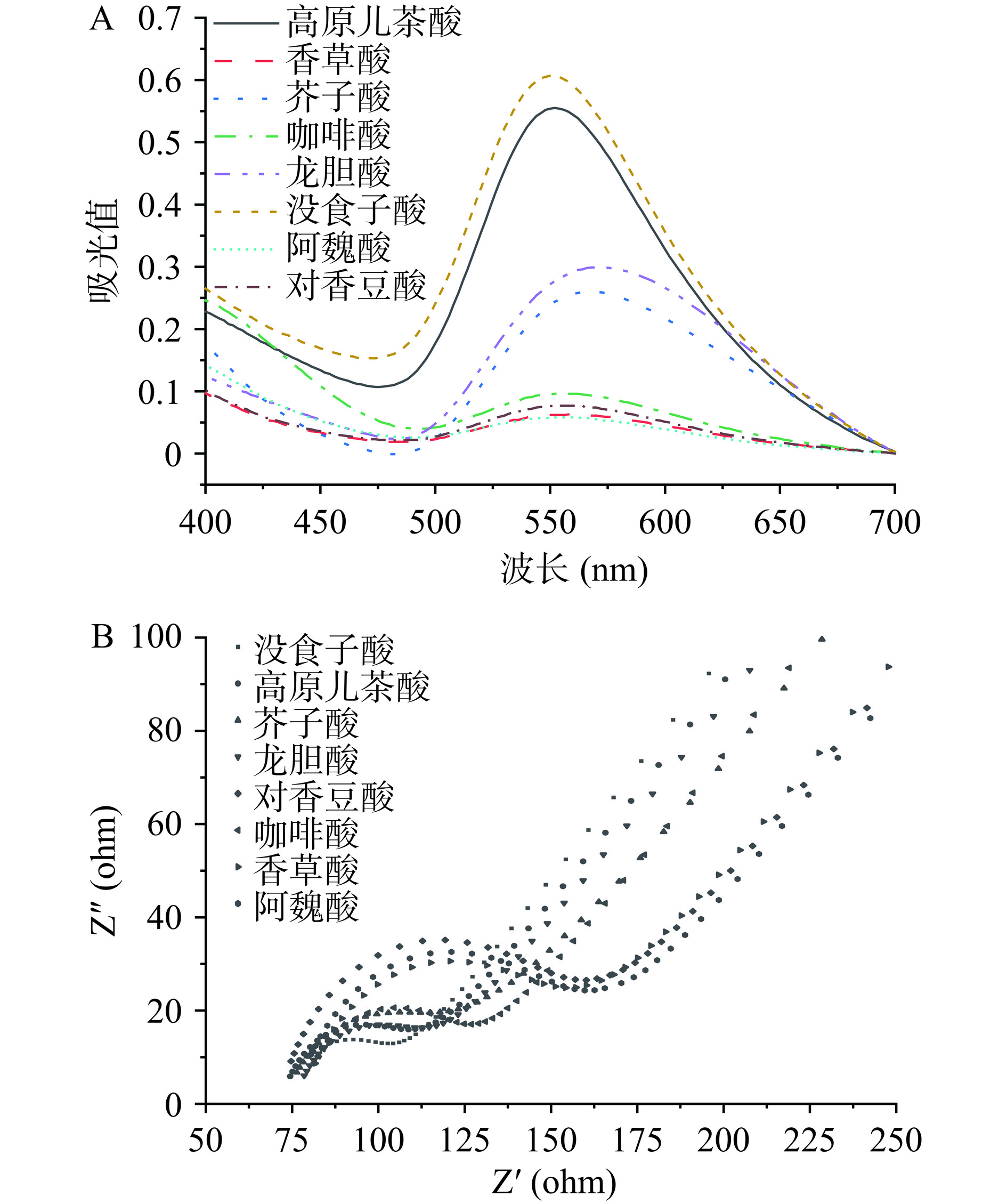
由图2(A)可知,在500~600 nm内,不同酚酸溶液均出现吸收峰,其中GA吸收峰最大。吸收峰值的大小,代表酚酸的还原型强弱。吸收峰值大小与酚酸还原性、合成AuNPs能力相关,吸收峰值越大,粒径越小,其稳定性越高。此外不同酚酸合成AuNPs的能力也与其结构有关,GA因其具有还原性酚羟基故还原性较高,合成AuNPs能力高于其他酚酸[16]。因此选择GA作为催化HAuCl4制备GA@AuNPs的还原剂。
EIS图谱阻抗弧半径半径越小,对电子转移的阻碍作用越小,能够更好地促进电极表面电子的转移[17]。由图2(B)可知,GA还原AuNPs的阻抗弧半径最小,对电子转移速率有显著的提高(P<0.05)。进一步表明了GA还原HAuCl4能力较强,且合成的AuNPs分散性好,减少了纳米金团聚现象。
2.1.2 GA浓度对纳米金合成的影响
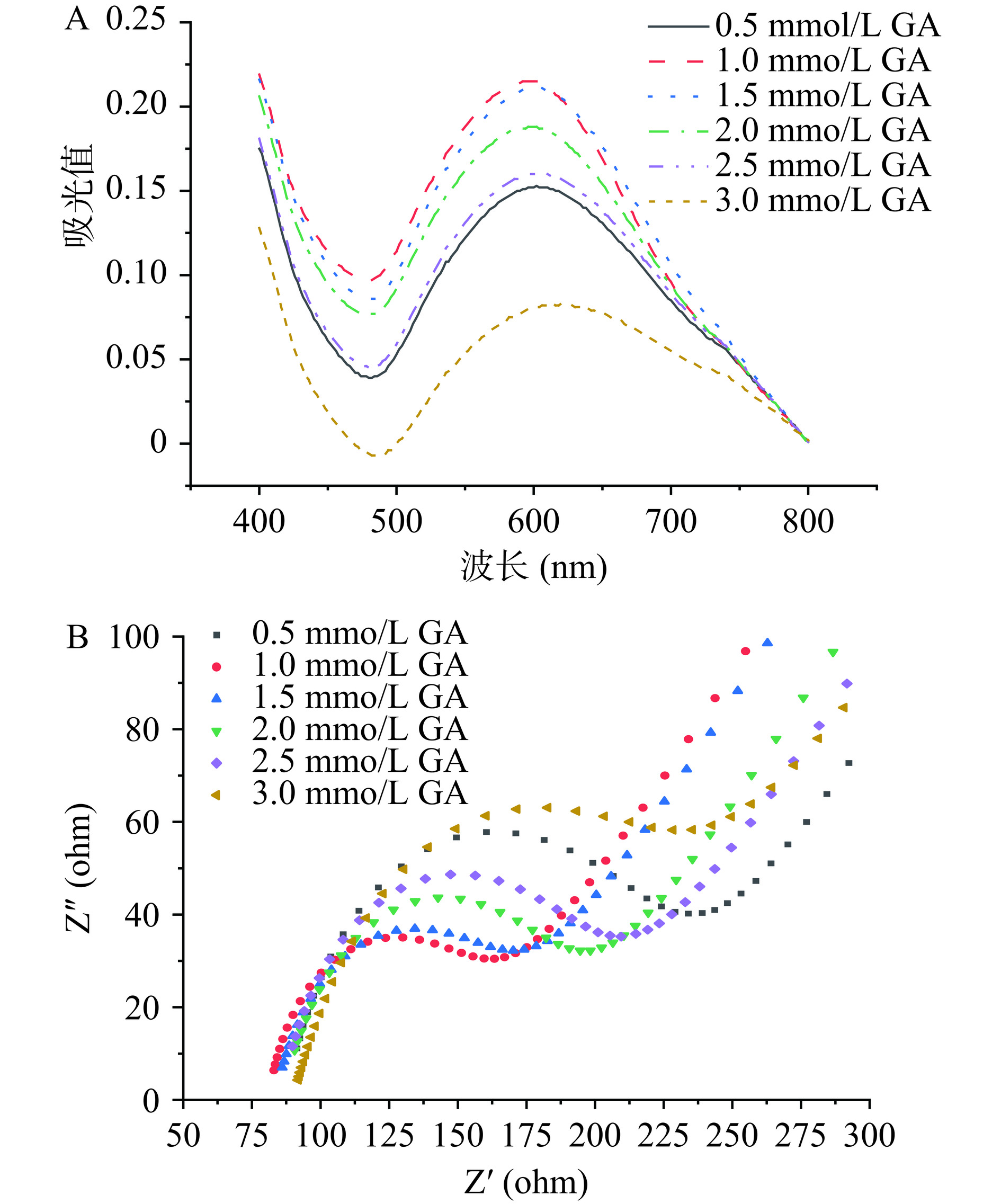
由图3(A)可知,当GA浓度为0.5~1.0 mmol/L时,紫外吸收值增大,是由于随着GA浓度的增加,催化合成的AuNPs发生团聚影响透光率,使紫外吸收值增大;当GA浓度为1.0~3.0 mmol/L时,紫外吸收值降低,这是因为随着GA浓度的增加,光线在溶液中被更多的分子吸收和散射,使得GA@AuNPs的吸光值降低。表明反应体系中GA浓度影响其还原合成AuNPs的量,当GA浓度达到1.0 mmol/L时,紫外吸光值最大。
由图3(B)所示,随着GA浓度的增加阻抗弧半径先减小再逐渐增大。GA浓度0.5 mmol/L阻抗弧半径较大,当浓度增加至1.0 mmol/L时,此时的阻抗弧半径最小,是因为GA量的增加对电子传递的阻碍作用减小,从而促进电极表面电子的转移[18],此外,适当浓度GA催化合成的AuNPs具有高导电性以及较强的表面修饰能力。随着GA浓度继续增加,体系中大量的羧酸存在,导致电极电子传递作用减弱,实验结果与紫外光谱图3(A)中结果相吻合。因此选定GA浓度为1.0 mmol/L。
2.1.3 HAuCl4孵育温度和反应时间的选择
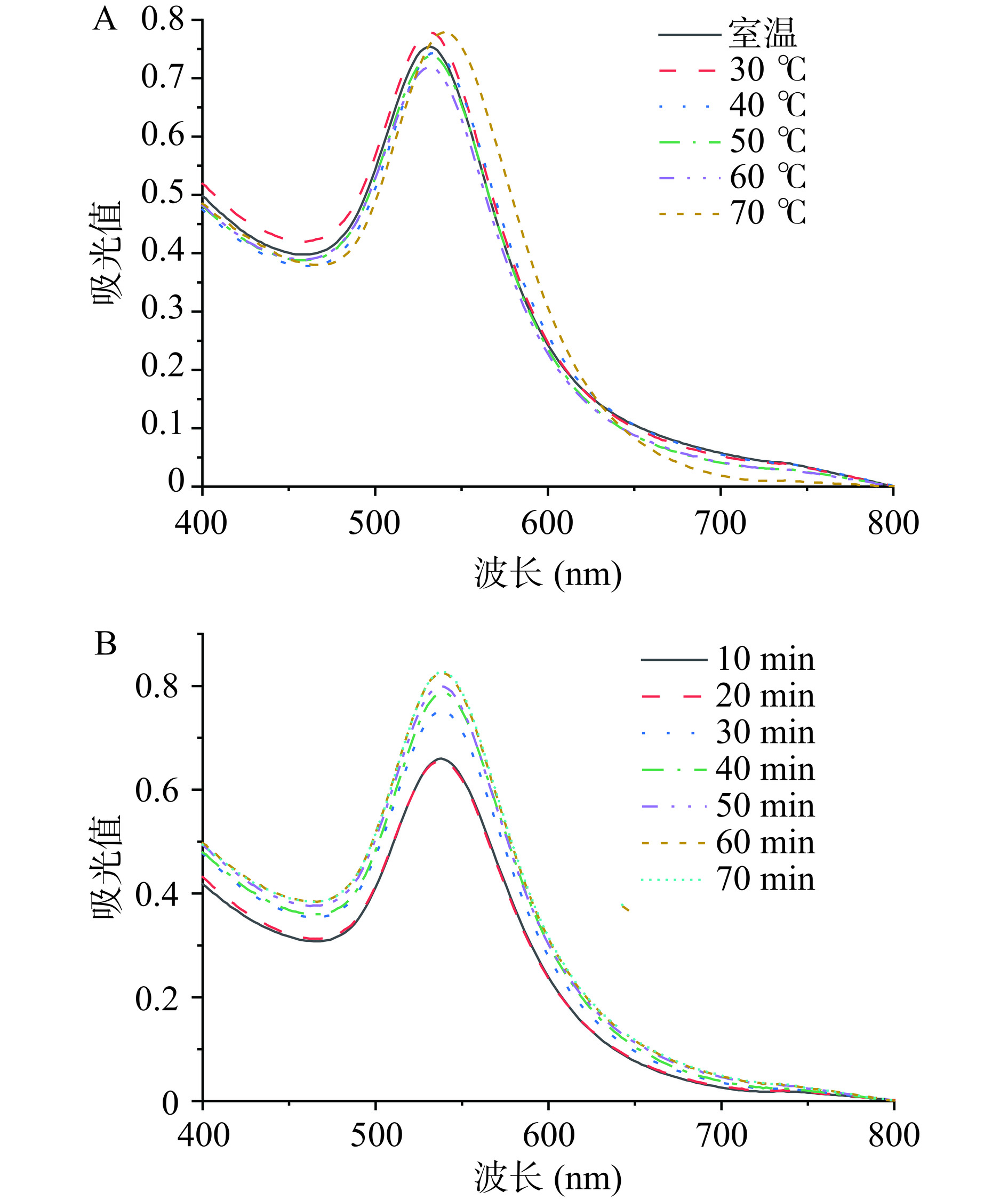
由图4(A)所示,随着HAuCl4孵育温度的升高,GA@AuNPs紫外光谱特征峰对应吸光值在70 ℃时达到最大。说明随着孵育温度的增大,紫外光谱吸收峰值之间存在显著性差异(P<0.05)。孵育温度影响酚酸介导的AuNPs合成,较低的反应温度会导致AuNPs的尺寸较大且形状不规则[19]。同时,较高的孵育温度能够促进GA催化还原HAuCl4合成的AuNPs。因此选择70 ℃作为孵育反应的最佳温度。
由图4(B)所示,随着反应时间的增加,紫外光谱特征峰所对应吸光值也随之增大,且存在显著性差异(P<0.05)。当GA还原HAuCl4的反应时间为60 min时,其吸光值达到最大,体系中合成AuNPs的浓度最大。这与Doan等[20]的研究具有相似的结果,故将GA还原HAuCl4的反应时间确定为60 min。
2.2 荧光光谱监控GA还原HAuCl4合成AuNPs过程
由图5(A)可知,GA还原HAuCl4的荧光发射峰在503 nm处,随着GA浓度的增加发射峰位置不变。由图5(B)可知,随着GA的加入,荧光强度先增大后减小,GA加入量对荧光强度影响显著(P<0.05),GA与AuNPs之间存在相互作用。GA@AuNPs的最大荧光发射波长在503 nm处。由于电子跃迁频率与表面等离子体共振耦合,使特定频率的荧光发射增大[21]。当入射光与金纳米粒子自由电子的振动频率发生共振耦合时,产生表面等离子体共振,显示较强的发射峰[22]。当GA@AuNPs加入量为900 μL时,荧光强度最大。随着GA@AuNPs的加入量的增加,体系荧光物质浓度过大,产生自猝灭现象吸电子基团-COOH,导致荧光强度下降,发生自猝灭现象,此时GA与AuNPs结合形成荧光物质的基态分子聚集体。
2.3 NO2−和SO32−同时检测体系条件的优化
由图6(A)可知,随着PBS浓度的增加,NO2−和SO32−的氧化峰电流呈先上升后降低的趋势,在浓度为0.15 mol/L时电流响应值最高。这是因为随着PBS浓度的增高,溶液中质子数量提高,峰电流升高。然而过量的PBS将阻碍溶液与电极表面的电子传递,导致峰电流降低,峰电位升高[23]。因此,PBS最佳浓度为0.15 mol/L。
![]() 图 6 缓冲溶液浓度(A)、pH(B)和不同缓冲溶液种类(C)对NO2−和SO32−电化学行为影响的LSV注:不同小写字母表示不同条件下差异显著(P<0.05);图8同。Figure 6. LSV of the effects of buffer concentrations (A), pH (B), and different buffer types (C) on the electrochemical behavior of NO2− and SO32−
图 6 缓冲溶液浓度(A)、pH(B)和不同缓冲溶液种类(C)对NO2−和SO32−电化学行为影响的LSV注:不同小写字母表示不同条件下差异显著(P<0.05);图8同。Figure 6. LSV of the effects of buffer concentrations (A), pH (B), and different buffer types (C) on the electrochemical behavior of NO2− and SO32−由图6(B)可知,随着PBS pH的增加,SO32−的氧化峰电流先升高后降低。当PBS的pH改变时,氧化峰电流之间具有显著性差异(P<0.05)。NO2−氧化峰电流随pH增加先逐渐上升后趋于不变。pH6.0时SO32−的氧化峰电流最大,当pH>7.0时,因质子参与了SO32−在电极上的氧化还原反应,峰电流值降低[24]。NO2−氧化峰电流随pH增加先逐渐上升后趋于不变,在高酸性的PBS下会与羧酸基团结合,导致羧酸基团减少,电荷增加,使AuNPs的还原性和稳定性减弱,从而在溶液中的电子转移速率降低,导致缓冲溶液的有效pH不同[25]。为提高检测的准确度,故选择pH6.0的PBS溶液。
由图6(C)可知,GA@AuNPs修饰电极对NO2−和SO32−的响应值随不同种类的缓冲溶液发生改变[26]。对于SO32−,其在乙酸缓冲溶液中响应峰电流值较高,其次是柠檬酸盐缓冲溶液和PBS;而对于NO2−,在PBS溶液中,NO2−具有较高的氧化峰电流,其次是柠檬酸盐缓冲溶液和乙酸缓冲溶液。当缓冲溶液为PBS时,具有显著的氧化峰电流(P<0.05),故选用PBS为缓冲溶液做后续实验。
2.4 GA@AuNPs@Au修饰电极检测NO2−和SO32−标准曲线
如图7所示,在检测体系内,随着NO2−和SO32−浓度升高,氧化峰电流也升高,NO2−浓度与氧化峰电流间存在明显线性关系。采用Origin 2021软件作图,获得NO2−标准曲线方程分别为y1=17.30+0.0281x,R2=0.983(低浓度0.001~0.5 mmol/L);y2=26.56+0.0111x(高浓度0.5~7.0 mmol/L),R2=0.998;此外,在线性范围0.001~7.0 mmol/L内,SO32−浓度和氧化峰电流之间同样存在明显线性关系,其标准曲线方程分别为y1=1.77+0.0062x(低浓度0.001~0.5 mmol/L),R2=0.994;y2=4.33+0.0012x(高浓度0.5~7.0 mmol/L),R2=0.994。采用信噪比(S/N=3)计算其NO2−和SO32−最低检出限分别为0.20 μmol/L和0.24 μmol/L ;定量限分别为0.81 μmol/L和0.67 μmol/L。
为了更好地评估GA@AuNPs@Au电极对SO32−和NO2−检测性能,与其他研究相比(表1),羧酸功能化多壁碳纳米电极中SO32−的检出限为0.215 μmol/L,较本文的略低,但线性范围较窄(400~2800 μmol/L);在AgNPs@PANI/还原氧化石墨烯纳米电极中,其回收率较本文高,检出限较本文低(SO32− 0.077 μmol/L;NO2− 0.056 μmol/L),但线性范围较窄(SO32− 2.7~24.4 μmol/L;NO2− 1.0~28.2 μmol/L)。在本法中SO32−和NO2−的检出限相对较低,线性范围较宽(0.001~7.0 mmol/L),且回收率良好。此外,该修饰电极稳定性、灵敏度高,与其他传感体系具有可比性。
表 1 不同种类修饰电极同时检测NO2−和SO32−的比较Table 1. Comparison of different kinds of modified electrodes for simultaneous detection of NO2− and SO32−修饰电极 SO32−检出限(μmol/L) NO2−检出限(μmol/L) SO32−与NO2−回收率(%) SO32−与NO2−线性范围(μmol/L) 参考文献 GCE/MWCNTs-PDDA-AuNPs 0.03 mg/ L − − 2~200 mg/L [27] Au/OMC/NiHCF 2.50 − 80~110 2.5~50000 [28] GCE/MWCNTs/PTZ-IL 9.30 − 100.9~103 30~1177 [29] CPE/MIL-101(Cr) 0.58 − − 2~70 [30] GCE/p-DAB@ERGO − 0.030 − 7~20000 [31] GCE/GO-COOH/Fe3O4 − 0.37 − 1~85;90~600 [32] GCE/rGO-MoS2-PEDOT − 0.059 98.3~100.80 1~1000 [33] LIG/MWCNTs-COOH-AuNPs − 9.3 90以上 10~140 [34] NGME 0.337 1.44 97.55~100.24 5.0~4000;5.0~4000 [35] GCE/CuO-NS 21.1 13.6 97.0~101.4 50~1600;100~1400 [36] GCE/MWCNTs-COOH 0.215 0.565 102~103.8 400~2800;100~700 [37] GCE/GONRs-AuNPs 1.1 1.3 99.4~107 10~10000;10~10000 [13] GR-CS/AuNPs GCE 1.0 0.25 97.2~102.6 5.0~410;1.0~380 [38] NiCoO/N-GN
AuNPs-MoS2-r GO1.6 1.0 98~104;98~103.2 1~1000;5~5000 [39] AgNPs@PANI/rGO/GCE 0.077 0.056 97.6~102.2;97.8~105.2 2.7~24.4;1.0~28.2 [24] GA@AuNPs@Au 0.24 0.20 98.53~99.80;94.73~99.47 1~7000;1~7000 本文 注:−为未检出;表2、表3同。 2.5 抗干扰实验及重现性和稳定性
抗干扰能力是传感器的重要评价指标。由图8可知,随着抗坏血酸、葡萄糖、草酸、蔗糖、柠檬酸、NaCl、CaCl2、LiCl等抗干扰物质的加入,在100倍浓度的抗干扰物质存在下,检测发现SO32−和NO2−的氧化峰电流变化不显著(P>0.05),说明GA@AuNPs@Au修饰电极具有优异的抗干扰能力。然而,乙醇的加入对修饰电极电流响应有一定程度的抑制作用,这是因为乙醇分子在电极表面形成吸附层,使部分活性位点覆盖,从而降低电极的催化效率[40]。但这种影响仅对电流强度有轻微削弱,对两种物质的检测结果未造成明显影响。表明该修饰电极在复杂环境下仍具备较好的抗干扰能力,对NO2−和SO32−的检测上具有较强的重现性,这与Wan等[41]的实验结果相近。
采用相同的GA@AuNPs@Au对NO2−和SO32−进行重复测定(10次),其平均峰电流分别为3.135×10−5和1.293×10−4;RSD分别为2.58%和2.97%,表明该修饰电极精密度良好。再将制备好的电极置于室温下两周后,NO2−和SO32−测定的氧化峰电流分别为1.587×10−5和5.168×10−5,与初始峰电流相比分别下降4.55%和3.51%(<5%),结果表明该电极具有良好的稳定性。
2.6 实际样品分析
将白梅花茶、迷迭香茶、牡丹花茶、盐田冻虾、鱿鱼丝、红葡萄酒、卷心菜、辣白菜8种实际样品稀释不同倍数,采用LSV分别测定加标后SO32−和NO2−的氧化峰电流。由表2可知,不稀释时多数样品无法检测出峰电流;稀释10倍时,多数样品经加标后均可检出;稀释100倍时,在未加标的情况下,SO32−和NO2−的氧化峰电流响应明显,故将样品按照稀释100倍后进行实际样品的加标回收率测定。
表 2 不同浓度梯度的实际样品中NO2−和SO32−检测值Table 2. NO2−和SO32− detections in real samples with different concentration gradients样品名称 不稀释 稀释10倍 稀释100倍 不加标 加500 μL 加1000 μL 不加标 加500 μL 加1000 μL 不加标 加500 μL 加1000 μL SO32−浓度(mg/L) 白梅花茶 − − − − 13.79 14.21 14.88 19.65 24.65 迷迭香茶 − − − − 12.65 15.78 11.26 16.00 21.04 牡丹花茶 − − − − 12.19 17.69 13.25 18.03 23.03 虾肉 13.73 18.52 23.54 − 17.54 19.87 − 15.42 28.54 红葡萄酒 − 8.86 9.94 − 7.62 9.68 11.65 16.45 21.43 卷心菜 9.98 14.81 19.82 9.94 13.12 15.46 9.92 17.56 18.24 辣白菜 − 3.42 5.66 − 4.97 9.90 − 3.24 5.84 鱿鱼丝 5.86 10.76 15.66 5.44 12.86 17.98 5.14 18.22 19.42 NO2−浓度(mg/L) 白梅花茶 − − − 1.01 4.89 5.12 0.98 5.96 10.87 迷迭香茶 − − − − 5.16 5.71 0.76 5.69 10.61 牡丹花茶 − − − − 0.74 5.98 0.98 5.92 10.90 虾肉 − 4.98 9.91 − 6.81 7.64 − 7.16 12.86 红葡萄酒 − 4.84 7.42 − 5.46 8.42 − 4.99 9.90 卷心菜 − 4.96 9.90 − 4.32 10.68 − 4.64 11.54 辣白菜 − 6.26 9.84 0.96 5.93 10.84 − 6.56 10.12 鱿鱼丝 0.54 5.49 10.40 − 11.76 14.52 − 15.47 18.34 将实际样品进行前处理,采用标准加入法对样品中NO2−和SO32−的加标回收率进行测定,结果如表3所示。
表 3 实际样品的加标回收率和相对标准偏差Table 3. Spike recovery and relative standard deviation (RSD) of actual samples实际样品 实际样品SO32−初始量
(mg/L)实际样品NO2−初始量
(mg/L)加标量
(mg/L)加标回收率(SO32−)
(%)加标回收率(NO2−)
(%)RSD(SO32−)
(%)RSD(NO2−)
(%)白梅花茶 14.88 0.98 5 95.40 99.53 1.72 1.43 10 97.70 98.87 1.41 2.21 迷迭香茶 11.26 0.76 5 94.73 98.53 2.58 2.69 10 97.83 98.53 1.62 2.72 牡丹花茶 13.25 0.98 5 95.60 98.87 1.88 1.98 10 97.77 99.17 1.45 1.73 虾肉 13.73 − 5 95.73 99.53 1.76 1.52 10 98.07 99.07 1.42 1.98 鱿鱼丝 5.86 0.54 5 98.07 99.07 1.00 1.34 10 98.00 98.57 2.21 2.39 红葡萄酒 11.65 − 5 96.00 99.80 2.16 1.22 10 97.80 98.97 1.70 2.25 卷心菜 9.98 − 5 96.67 99.13 2.18 2.57 10 98.43 98.97 1.72 2.16 辣白菜 − 0.96 5 99.47 99.40 1.45 2.07 10 98.97 98.77 2.25 2.78 由表3可知,对8种不同样品中SO32−和NO2−同时测定的加标回收率分别94.73%~99.47%和98.53%~99.80%,RSD均小于5%,根据GB 2760-2014《食品安全国家标准 食品添加剂使用标准》和GB 2762-2022《食品安全国家标准 食品中污染物限量》中,对食品中NO2−和SO32−最大使用量和残留量的规定,8种样品中NO2−和SO32−符合限量标准。实验的准确度较高,且结果可靠,可进行实际应用。
3. 结论
采用酚酸还原HAuCl4合成AuNPs,通过一步电沉积法将GA@AuNPs修饰到裸金电极表面,制备出绿色环保且对电子传递速率快的GA@AuNPs@Au修饰电极。考察了酚酸基纳米金在修饰电极上的电化学行为,并最终得到优化条件,构建的修饰电极传感体系检测NO2−和SO32−的标准曲线呈现出良好的线性关系,检出限分别为0.20 μmol/L和0.24 μmol/L。且该修饰电极的抗干扰能力强,具有良好的重现性与稳定性。同时,通过对不同稀释度样品进行加标回收,SO32−和NO2−的加标回收率良好,表明该修饰电极具有良好的准确性和可靠性。因此,该酚酸基修饰电极可为食品原料及其制品中NO2−和SO32−的检测提供依据。
-
图 6 缓冲溶液浓度(A)、pH(B)和不同缓冲溶液种类(C)对NO2−和SO32−电化学行为影响的LSV
注:不同小写字母表示不同条件下差异显著(P<0.05);图8同。
Figure 6. LSV of the effects of buffer concentrations (A), pH (B), and different buffer types (C) on the electrochemical behavior of NO2− and SO32−
表 1 不同种类修饰电极同时检测NO2−和SO32−的比较
Table 1 Comparison of different kinds of modified electrodes for simultaneous detection of NO2− and SO32−
修饰电极 SO32−检出限(μmol/L) NO2−检出限(μmol/L) SO32−与NO2−回收率(%) SO32−与NO2−线性范围(μmol/L) 参考文献 GCE/MWCNTs-PDDA-AuNPs 0.03 mg/ L − − 2~200 mg/L [27] Au/OMC/NiHCF 2.50 − 80~110 2.5~50000 [28] GCE/MWCNTs/PTZ-IL 9.30 − 100.9~103 30~1177 [29] CPE/MIL-101(Cr) 0.58 − − 2~70 [30] GCE/p-DAB@ERGO − 0.030 − 7~20000 [31] GCE/GO-COOH/Fe3O4 − 0.37 − 1~85;90~600 [32] GCE/rGO-MoS2-PEDOT − 0.059 98.3~100.80 1~1000 [33] LIG/MWCNTs-COOH-AuNPs − 9.3 90以上 10~140 [34] NGME 0.337 1.44 97.55~100.24 5.0~4000;5.0~4000 [35] GCE/CuO-NS 21.1 13.6 97.0~101.4 50~1600;100~1400 [36] GCE/MWCNTs-COOH 0.215 0.565 102~103.8 400~2800;100~700 [37] GCE/GONRs-AuNPs 1.1 1.3 99.4~107 10~10000;10~10000 [13] GR-CS/AuNPs GCE 1.0 0.25 97.2~102.6 5.0~410;1.0~380 [38] NiCoO/N-GN
AuNPs-MoS2-r GO1.6 1.0 98~104;98~103.2 1~1000;5~5000 [39] AgNPs@PANI/rGO/GCE 0.077 0.056 97.6~102.2;97.8~105.2 2.7~24.4;1.0~28.2 [24] GA@AuNPs@Au 0.24 0.20 98.53~99.80;94.73~99.47 1~7000;1~7000 本文 注:−为未检出;表2、表3同。 表 2 不同浓度梯度的实际样品中NO2−和SO32−检测值
Table 2 NO2−和SO32− detections in real samples with different concentration gradients
样品名称 不稀释 稀释10倍 稀释100倍 不加标 加500 μL 加1000 μL 不加标 加500 μL 加1000 μL 不加标 加500 μL 加1000 μL SO32−浓度(mg/L) 白梅花茶 − − − − 13.79 14.21 14.88 19.65 24.65 迷迭香茶 − − − − 12.65 15.78 11.26 16.00 21.04 牡丹花茶 − − − − 12.19 17.69 13.25 18.03 23.03 虾肉 13.73 18.52 23.54 − 17.54 19.87 − 15.42 28.54 红葡萄酒 − 8.86 9.94 − 7.62 9.68 11.65 16.45 21.43 卷心菜 9.98 14.81 19.82 9.94 13.12 15.46 9.92 17.56 18.24 辣白菜 − 3.42 5.66 − 4.97 9.90 − 3.24 5.84 鱿鱼丝 5.86 10.76 15.66 5.44 12.86 17.98 5.14 18.22 19.42 NO2−浓度(mg/L) 白梅花茶 − − − 1.01 4.89 5.12 0.98 5.96 10.87 迷迭香茶 − − − − 5.16 5.71 0.76 5.69 10.61 牡丹花茶 − − − − 0.74 5.98 0.98 5.92 10.90 虾肉 − 4.98 9.91 − 6.81 7.64 − 7.16 12.86 红葡萄酒 − 4.84 7.42 − 5.46 8.42 − 4.99 9.90 卷心菜 − 4.96 9.90 − 4.32 10.68 − 4.64 11.54 辣白菜 − 6.26 9.84 0.96 5.93 10.84 − 6.56 10.12 鱿鱼丝 0.54 5.49 10.40 − 11.76 14.52 − 15.47 18.34 表 3 实际样品的加标回收率和相对标准偏差
Table 3 Spike recovery and relative standard deviation (RSD) of actual samples
实际样品 实际样品SO32−初始量
(mg/L)实际样品NO2−初始量
(mg/L)加标量
(mg/L)加标回收率(SO32−)
(%)加标回收率(NO2−)
(%)RSD(SO32−)
(%)RSD(NO2−)
(%)白梅花茶 14.88 0.98 5 95.40 99.53 1.72 1.43 10 97.70 98.87 1.41 2.21 迷迭香茶 11.26 0.76 5 94.73 98.53 2.58 2.69 10 97.83 98.53 1.62 2.72 牡丹花茶 13.25 0.98 5 95.60 98.87 1.88 1.98 10 97.77 99.17 1.45 1.73 虾肉 13.73 − 5 95.73 99.53 1.76 1.52 10 98.07 99.07 1.42 1.98 鱿鱼丝 5.86 0.54 5 98.07 99.07 1.00 1.34 10 98.00 98.57 2.21 2.39 红葡萄酒 11.65 − 5 96.00 99.80 2.16 1.22 10 97.80 98.97 1.70 2.25 卷心菜 9.98 − 5 96.67 99.13 2.18 2.57 10 98.43 98.97 1.72 2.16 辣白菜 − 0.96 5 99.47 99.40 1.45 2.07 10 98.97 98.77 2.25 2.78 -
[1] NOVAIS C, MOLINA A K, ABREU R M V, et al. Natural food colorants and preservatives:A review, a demand, and a challenge[J]. Journal of Agricultural and Food Chemistry,2022,70(9):2789−2805. doi: 10.1021/acs.jafc.1c07533
[2] GOULD G W, RUSSELL N J. Sulfite[M]//Food Preservatives. Boston, MA:Springer US, 2003:85−101.
[3] RUPP H. Chemical and physical hazards produced during food processing, storage, and preparation[J]. Food Safety Handbook,2003:233−263.
[4] ARCHER M C. Hazards of nitrote, nitrite, ond n-nitroso compounds in human nutrition[J]. Nutr Toxicol,2012,1:327.
[5] KARRAT A, DIGUA K, AMINE A. Development of a simplified spectrophotometric method for nitrite determination in water samples[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2022,267:120574. doi: 10.1016/j.saa.2021.120574
[6] MIURA Y, HATAKEYAMA M, HOSINO T, et al. Rapid ion chromatography of L-ascorbic acid, nitrite, sulfite, oxalate, iodide and thiosulfate by isocratic elution utilizing a postcolumn reaction with cerium (IV) and fluorescence detection[J]. Journal of Chromatography A,2002,956(1−2):77−84. doi: 10.1016/S0021-9673(01)01497-2
[7] WANG P, ZHANG Y, LIU Y, et al. Starch-based carbon dots for nitrite and sulfite detection[J]. Frontiers in Chemistry,2021,9:782238. doi: 10.3389/fchem.2021.782238
[8] DAVIS J, MOORCROFT M J, WILKINs S J, et al. Electrochemical detection of nitrate and nitrite at a copper modified electrode[J]. Analyst,2000,125(4):737−742. doi: 10.1039/a909762g
[9] ZHANG M, YANG Y, GUO W. Electrochemical sensor for sensitive nitrite and sulfite detection in milk based on acid-treated Fe3O4@SiO2 nanoparticles[J]. Food Chemistry,2024,430:137004. doi: 10.1016/j.foodchem.2023.137004
[10] BAGHERI H, HAJIAN A, REZAEI M, et al. Composite of Cu metal nanoparticles-multiwall carbon nanotubes-reduced graphene oxide as a novel and high performance platform of the electrochemical sensor for simultaneous determination of nitrite and nitrate[J]. Journal of Hazardous Materials,2017,324:762−772. doi: 10.1016/j.jhazmat.2016.11.055
[11] WEI W, WU S G. Study of electrooxidation behavior of nitrite on gold nanoparticles/graphitizing carbon felt electrode and its analytical application[J]. Chinese Journal of Analytical Chemistry,2019,47(2):e19014−e19020. doi: 10.1016/S1872-2040(19)61142-4
[12] YU H, FENG X, CHEN X, et al. A highly sensitive determination of sulfite using a glassy carbon electrode modified with gold nanoparticles-reduced graphene oxide nano-composites[J]. Journal of Electroanalytical Chemistry,2017,801:488−495. doi: 10.1016/j.jelechem.2017.08.007
[13] ZHAI T, LI R, ZHANG N, et al. Simultaneous detection of sulfite and nitrite on graphene oxide nanoribbons-gold nanoparticles composite modified electrode[J]. Electroanalysis,2022,34(1):103−110. doi: 10.1002/elan.202100525
[14] TAIB S H M, SHAMELI K, NIA P M, et al. Electrooxidation of nitrite based on green synthesis of gold nanoparticles using Hibiscus sabdariffa leaves[J]. Journal of the Taiwan Institute of Chemical Engineers,2019,95:616−626. doi: 10.1016/j.jtice.2018.09.021
[15] 曹世卿. 植物酚酸络合铁离子强化Fenton氧化菲的机制研究[D]. 兰州:兰州交通大学, 2024. [CAO S Q. Study on the mechanism of Fenton oxidation of phenanthrene enhanced by complexation of iron ions with plant phenolic acids[D]. Lanzhou:Lanzhou Jiaotong University, 2024.] CAO S Q. Study on the mechanism of Fenton oxidation of phenanthrene enhanced by complexation of iron ions with plant phenolic acids[D]. Lanzhou: Lanzhou Jiaotong University, 2024.
[16] 李卉, 李莉. 食品中亚硝酸盐检测方法的研究进展[J]. 食品工业科技,2022,43(23):429−435. [LI Hui, LI Li. Research progress of nitrite detection methods in foods[J]. Science and Technology of Food Industry,2022,43(23):429−435.] LI Hui, LI Li. Research progress of nitrite detection methods in foods[J]. Science and Technology of Food Industry, 2022, 43(23): 429−435.
[17] ALEGRIA E C B A, RIBEIRO A P C, MENDES M, et al. Effect of phenolic compounds on the synthesis of gold nanoparticles and its catalytic activity in the reduction of nitro compounds[J]. Nanomaterials,2018,8(5):320. doi: 10.3390/nano8050320
[18] AHMAD T, KHAN W. Size variation of gold nanoparticles synthesized using tannic acid in response to higher chloroauric acid concentrations[J]. World Journal of Nano Science and Engineering,2013,3(3):62−68. doi: 10.4236/wjnse.2013.33009
[19] PATIL M P, KANG M, NIYONIZIGIYE I, et al. Extracellular synthesis of gold nanoparticles using the marine bacterium Paracoccus haeundaensis BC74171T and evaluation of their antioxidant activity and antiproliferative effect on normal and cancer cell lines[J]. Colloids and Surfaces B:Biointerfaces,2019,183:110455. doi: 10.1016/j.colsurfb.2019.110455
[20] DOAN V D, THIEU A T, NGUYEN T D, et al. Biosynthesis of gold nanoparticles using Litsea cubeba fruit extract for catalytic reduction of 4-nitrophenol[J]. Journal of Nanomaterials,2020,2020:1−10.
[21] LI Z Q, CHEN S, LI J J, et al. Plasmon-enhanced upconversion fluorescence in NaYF4:Yb/Er/Gd nanorods coated with Au nanoparticles or nanoshells[J]. Journal of Applied Physics,2012,111(1):014310. doi: 10.1063/1.3676258
[22] HE Z, LI F, ZUO P, et al. Principles and applications of resonance energy transfer involving noble metallic nanoparticles[J]. Materials,2023,16(8):3083. doi: 10.3390/ma16083083
[23] CHEN H, YANG T, LIU F, et al. Electrodeposition of gold nanoparticles on Cu-based metal-organic framework for the electrochemical detection of nitrite[J]. Sensors and A Ctuators B:Chemical,2019,286:401−407.
[24] KALADEVI G, WILSON P, PANDIAN K. Simultaneous and selective electrochemical detection of sulfite and nitrite in water sources using homogeneously dispersed Ag nanoparticles over PANI/rGO nanocomposite[J]. Journal of the Electrochemical Society,2020,167(2):027514. doi: 10.1149/1945-7111/ab6973
[25] ALIPOUR E, BOLALI F M, NOROUZI S, et al. Electrochemically activated pencil lead electrode as a sensitive voltammetric sensor to determine gallic acid[J]. Food Chemistry,2022,375:131871. doi: 10.1016/j.foodchem.2021.131871
[26] KHOSHBIN Z, HOUSAINDOKHT M R, VERDIAN A, et al. Simultaneous detection and determination of mercury (II) and lead (II) ions through the achievement of novel functional nucleic acid-based biosensors[J]. Biosensors and Bioelectronics,2018,116:130−147. doi: 10.1016/j.bios.2018.05.051
[27] AMATATONGCHAI M, SROYSEE W, CHAIRAM S, et al. Simple flow injection for determination of sulfite by amperometric detection using glassy carbon electrode modified with carbon nanotubes-PDDA-gold nanoparticles[J]. Talanta,2015,133:134−141. doi: 10.1016/j.talanta.2014.07.055
[28] PREECHARUEANGRIT S, THAVARUNGKUL P, KANATHARANA P, et al. Amperometric sensing of sulfite using a gold electrode coated with ordered mesoporous carbon modified with nickel hexacyanoferrate[J]. Journal of Electroanalytical Chemistry,2018,808:150−159. doi: 10.1016/j.jelechem.2017.11.070
[29] MANUSHA P, SENTHILKUMAR S. Design and synthesis of phenothiazine based imidazolium ionic liquid for electrochemical nonenzymatic detection of sulfite in food samples[J]. Journal of Molecular Liquids,2020,301:112412. doi: 10.1016/j.molliq.2019.112412
[30] MASSAH R T, NTEP T J M M, NJANJA E, et al. A metal-organic framework-based amperometric sensor for the sensitive determination of sulfite ions in the presence of ascorbic acid[J]. Microchemical Journal,2021,169:106569. doi: 10.1016/j.microc.2021.106569
[31] KESAVAN S, KUMAR D R, BAYNOSA M L, et al. Potentiodynamic formation of diaminobenzene films on an electrochemically reduced graphene oxide surface:Determination of nitrite in water samples[J]. Materials Science and Engineering:C,2018,85:97−106.
[32] ROSTAMI M, ABDI G, KAZEMI S H, et al. Nanocomposite of magnetic nanoparticles/graphene oxide decorated with acetic acid moieties on glassy carbon electrode:A facile method to detect nitrite concentration[J]. Journal of Electroanalytical Chemistry,2019,847:113239. doi: 10.1016/j.jelechem.2019.113239
[33] MADHUVILAKKU R, ALAGAR S, MARIAPPAN R, et al. Glassy carbon electrodes modified with reduced graphene oxide-MoS2-poly (3,4-ethylene dioxythiophene) nanocomposites for the non-enzymatic detection of nitrite in water and milk[J]. Analytica Chimica Acta,2020,1093:93−105. doi: 10.1016/j.aca.2019.09.043
[34] NASRAOUI S, AL-HAMRY A, TEIXEIRA P R, et al. Electrochemical sensor for nitrite detection in water samples using flexible laser-induced graphene electrodes functionalized by CNT decorated by Au nanoparticles[J]. Journal of Electroanalytical Chemistry,2021,880:114893. doi: 10.1016/j.jelechem.2020.114893
[35] MANIKANDAN V S, LIU Z, CHEN A. Simultaneous detection of hydrazine, sulfite, and nitrite based on a nanoporous gold microelectrode[J]. Journal of Electroanalytical Chemistry,2018,819:524−532. doi: 10.1016/j.jelechem.2018.02.004
[36] SUDHA V, KRISHNAMOORTHY K, KUMAR S M S, et al. Copper oxide nanosheet modified electrodes for simultaneous determination of environmentally hazardous anions[J]. Journal of Alloys and Compounds,2018,764:959−968. doi: 10.1016/j.jallcom.2018.06.077
[37] SUDHA V, KUMAR S M S, THANGAMUTHU R. Simultaneous electrochemical sensing of sulphite and nitrite on acid-functionalized multi-walled carbon nanotubes modified electrodes[J]. Journal of Alloys and Compounds,2018,749:990−999. doi: 10.1016/j.jallcom.2018.03.287
[38] XUE W, HUI L I, MIN W U, et al. Simultaneous electrochemical determination of sulphite and nitrite by a gold nanoparticle/graphene-chitosan modified electrode[J]. Chinese Journal of Analytical Chemistry,2013,41(8):1232−1237. doi: 10.1016/S1872-2040(13)60673-8
[39] 张然. 功能化石墨烯的合成及其用于NO2−及SO32−的电化学检测[D]. 太原:山西大学, 2019. [ZHANG R. Synthesis of functionalized graphene and its use for electrochemical detection of NO2− and SO32−[D]. Taiyuan:Shanxi University, 2019.] ZHANG R. Synthesis of functionalized graphene and its use for electrochemical detection of NO2− and SO32−[D]. Taiyuan: Shanxi University, 2019.
[40] JALAL A H, UMASANKAR Y, GONZALEZ P J, et al. Multimodal technique to eliminate humidity interference for specific detection of ethanol[J]. Biosensors and Bioelectronics,2017,87:522−530.
[41] WAN Y, WANG H, ZHANG L, et al. Highly stable acetylcholinesterase electrochemical biosensor based on polymerized ionic liquids microgel for pesticides detection[J]. Microchimica Acta,2022,189(8):300. doi: 10.1007/s00604-022-05383-6
-
期刊类型引用(1)
1. 刘雅琪,周娜,冯蒙蒙,艾欣,赵磊,赵亮. 负载黑米花色苷的纳米颗粒对Caco-2细胞损伤的保护作用. 食品科学. 2025(03): 102-109 .  百度学术
百度学术
其他类型引用(0)






 下载:
下载:




 下载:
下载:



