Analysis of Composition and Antioxidant Stability of Pitaya Stem Polysaccharide
-
摘要: 目的:以火龙果茎中提取的多糖为研究对象,分析其理化特性和抗氧化活性,并进一步探讨不同储存条件与食品加工方式对其抗氧化稳定性的影响。方法:热水浸提醇沉法制备火龙果茎多糖,分别采用苯酚硫酸法、NaNO2-Al(NO3)3-NaOH显色法、福林酚法和离子色谱法分析多糖的总糖、黄酮和酚类含量以及单糖组成,扫描电子显微镜(SEM)观察多糖微观形态,并以抑制羟基自由基能力为抗氧化指标,通过模拟不同食品储存和加工条件,系统地研究火龙果茎多糖的抗氧化稳定性。结果:热水提取法得到的火龙果茎多糖的得率为7.22%,总糖含量为334.63 mg/g,黄酮和酚类残留量分别为5.91 mg/g和5.05 mg/g,进一步分析其主要由葡萄糖、半乳糖、鼠李糖、半乳糖醛酸、阿拉伯糖和甘露糖等组成,单糖摩尔比为5.27:2.77:0.77:0.71:0.32:0.17;在SEM下,火龙果茎多糖呈现紧密、多孔的不规则形状;火龙果茎多糖具有较好的抗氧化活性,随着多糖质量浓度的增加,其抑制羟基自由基的能力增强(P<0.05)。温度、pH、部分金属离子(钙、钾和钠离子)、部分食品添加剂(柠檬酸、苯甲酸钠和葡萄糖)和杀菌方式对火龙果茎多糖抗氧化稳定性的影响较小;光照对火龙果茎多糖抗氧化稳定性影响较大,随着光照时间的延长,火龙果茎多糖对羟基自由基的抑制能力逐渐降低,故耐光性较差;而增加金属铁、铜离子和蔗糖溶液的质量浓度也会显著(P<0.05)降低火龙果茎多糖抗氧化活性。结论:火龙果茎多糖具有良好的抗氧化稳定性,但是在火龙果茎的储存和食品加工中应避免长期光照、直接接触金属铁离子和铜离子以及高浓度的蔗糖溶液。Abstract: Objective: Pitaya stem polysaccharide (PSP) was applied as raw materials to study the physicochemical properties and antioxidant activity, as well as the effects of different storage and food processing conditions on PSP's antioxidant stability were further explored. Methods: The active polysaccharide from pitaya stem was extracted using hot-water extraction combining with alcohol-precipitation method. Initially, total sugar, total flavonoid and total phenolic contents in PSP were determined using phenol-sulfuric acid method, NaNO2-Al(NO3)3-NaOH method and Folin-Ciocalteu assay, respectively. Monosaccharide composition of PSP was analyzed using ion chromatography, and surface morphology in PSP was characterized using scanning electron microscope (SEM). Then, antioxidant stability of PSP was systematically determined by simulating various food storage and processing conditions, and hydroxyl radical scavenging activity was used as an evaluation index for PSP. Results: The extraction yield of PSP was around 7.22%, total sugar, total flavonoid and total phenolic contents in PSP were 334.63 mg/g, 5.91 mg/g, and 5.05 mg/g, respectively. The PSP mainly consisted of glucose, galactose, rhamnose, galacturonic acid, arabinose and mannose in the following molar ratios: 5.27:2.77:0.77:0.71:0.32:0.17. PSP presented a compact and porous surface with irregular shape as recorded by SEM images. Additionally, PSP possessed good hydroxyl radical scavenging activity, which was increased with the increase of polysaccharide concentration (P<0.05). Temperature, pH, some metal ions (Ca2+, K+ and Na+ metal ions), some food additives (citric acid, sodium benzoate and glucose) and sterilization methods had little impact on the antioxidant activity of PSP. However, light had a great effect on the antioxidant activity of PSP. With the extension of light time, the inhibitory ability of PSP to hydroxyl radical gradually decreased, indicating that PSP had the poor light resistance. Meanwhile, the antioxidant activity of PSP was also significantly decreased with the increasing concentration of Fe3+ and Cu2+ metal ion, as well as sucrose solution (P<0.05). Conclusion: PSP has good antioxidant stability, but continuous light, Fe3+ and Cu2+ metal ions, as well as sucrose might have the greatly adverse effect on the antioxidant activity of PSP. Therefore, the direct contact with these four environmental factors should be avoided during the processing and storage of pitaya stem.
-
Keywords:
- pitaya stem /
- polysaccharide /
- physicochemical properties /
- antioxidant activity /
- stability
-
火龙果属仙人掌科(Cactaceae)多年生攀缘多浆的长日照植物。近年来,我国主要的火龙果种植区域有广西、海南、广东、福建和台湾[1−2],其中广西火龙果种植面积和产量均全国第一。截至目前,广西火龙果种植面积已达到2.5万hm2[3],产量占全国的35.26%[4],成为我国最大的火龙果产区。在规模化和标准化的火龙果种植生产中,为提高火龙果果实品质与产量,需要不断修剪枝条,果实采摘后亦会产生大量的果茎,每公顷火龙果种植地可产出火龙果茎约60吨[5]。然而目前这些火龙果茎未被充分利用,多作为废弃物处理,这不仅造成火龙果园环境二次污染,也导致大量植物资源的浪费。
火龙果茎富含多糖、黄酮、植物甾醇等活性成分[6−7],其中多糖类成分的含量较高[8]。近年来,火龙果茎多糖的研究多集中于提取与分离纯化技术优化[9]、功能活性测定[10]等。马若影等[11]发现火龙果茎多糖具有较强的还原铁离子能力和自由基清除活性。唐雅园等[12]以火龙果茎多糖为原料制备护手霜,发现火龙果茎多糖能提高护手霜的抗氧化能力。此外,梁秋杨等[13]进一步明确了火龙果茎多糖属于天然来源的无毒性成分,可提高机体的特异性免疫应答能力。可见,火龙果茎多糖具有应用于功能食品、食品添加剂、日化用品等领域的潜力。充分研究和利用火龙果茎这一废弃资源,加强火龙果茎综合开发力度,生产高附加值的产品,对保护环境、减少资源浪费和提高火龙果产业经济效益有着重要意义。
自由基是一类强氧化能力的物质,而羟基自由基是生物体内最常见的一种自由基,其极强的氧化能力也成为破坏力最大的一类活性氧自由基[14]。因此,抗氧化剂的摄入在一定程度上能够有效地减少自由基对机体产生的危害。当前,许多植物多糖具有较强的抗氧化活性,如桃金娘、蒲公英、灰树花多糖等[15−16]。然而在实际应用中,储存与加工条件会影响植物多糖的抗氧化活性[17]。可见,研究植物多糖的抗氧化稳定性可有效地开发多糖相关产品,拓宽其加工领域。目前关于火龙果茎多糖抗氧化稳定性的报道鲜少。因此,本文通过模拟不同储存与加工条件,以抑制羟基自由基能力为抗氧化评价指标,考察火龙果茎多糖的抗氧化稳定性,为火龙果茎抗氧化类产品的开发利用提供理论依据。
1. 材料与方法
1.1 材料与仪器
红心火龙果茎 由广西壮族自治区农业科学院武鸣基地提供;16种单糖标准品(岩藻糖Fuc、盐酸氨基半乳糖GalN、鼠李糖Rha、阿拉伯糖Ara、盐酸氨基葡萄糖GlcN、半乳糖Gal、葡萄糖Glc、N-乙酰-D氨基葡萄糖GlcNAc-N、木糖Xyl、甘露糖Man、D-果糖Fru、D-核糖Rib、半乳糖醛酸GalA、L-古罗糖醛酸GulA、葡萄糖醛酸GlcA、D-甘露糖醛酸ManA) 江苏博睿糖生物科技有限公司;羟自由基测试试剂盒(A018-1-1) 南京建成生物工程研究所;无水乙醇、三氯乙酸、正丁醇、浓硫酸、苯酚、氢氧化钠、三氟乙酸、醋酸钠、磷酸氢二钠、柠檬酸、蔗糖、葡萄糖、苯甲酸钠、氯化钙、氯化铜、氯化钾、氯化钠、氯化铁 成都金山化学试剂有限公司;所有试剂均为分析纯。
PILOT10-15M真空冷冻干燥机 北京博医康实验仪器有限公司;RE-52AA旋转蒸发器 上海亚荣生化仪器厂;3-18ks型台式高速冷冻离心机 美国Sigma公司;ICS5000离子色谱仪 美国Thermo Fisher Scientific公司;Sigma 300型扫描电子显微镜 德国Sigma集团;SQ510C高温灭菌锅 雅马拓科技贸易(上海)有限公司;DK-6D恒温水浴锅 常州万顺仪器制造有限公司;UV-1800PC紫外分光光度计 上海美析仪器有限公司。
1.2 实验方法
1.2.1 火龙果茎多糖的制备与分析
1.2.1.1 多糖提取与纯化
参考Tang等[18]的方法。将新鲜的火龙果茎清洗干净后打浆,冷冻干燥后研磨成粉末。火龙果茎粉末与去离子水以1:20(g/mL)混匀,加热浸提(90 ℃,3 h),提取2次,合并两次提取液。提取液经旋转蒸发浓缩后,将浓缩液与95%乙醇以1:3(v/v)混合后进行低温醇沉。静置12 h后收集沉淀,冷冻干燥得火龙果茎多糖,称量并按公式(1)计算火龙果茎多糖得率。
多糖得率(%)=火龙果茎多糖质量(g)火龙果茎原料质量(g)×100 (1) 1.2.1.2 多糖化学成分分析
火龙果茎多糖的总糖含量采用苯酚-硫酸法[19],黄酮残留量采用NaNO2-Al(NO3)3-NaOH显色法[20],酚类残留量采用福林酚比色法[21],按照公式(2)分别计算火龙果茎多糖的总糖含量以及黄酮、酚类残留量。
含量(mg/g)=C×V×Nm×1000 (2) 式中,C为火龙果茎多糖的总糖、黄酮或酚类质量浓度,µg/mL;V为反应体系中火龙果茎多糖溶液的总体积,mL;N为稀释倍数;m为称取火龙果茎粉质量,g。
1.2.1.3 多糖单糖组成分析
采用离子色谱法分析火龙果茎多糖的单糖组成。
样品制备:参考Tang等[18]的方法。精密称取10 mg样品于安瓿瓶中,加入10 mL质量浓度3 mol/L三氟乙酸,置于120 ℃烘箱中水解3 h;取1 mL酸水解溶液至管中,并用N2吹干;加入5 mL去离子水混匀后,将混合液与去离子水以1:9(v/v)混合,高速离心后收集上清液,即为火龙果茎多糖水解液。
色谱条件:采用ICS5000离子色谱系统。色谱柱DionexCarbopacTMPA20,检测器为电化学检测器,柱温30 ℃,流速0.3 mL/min,进样量5 µL。流动相A为超纯水,流动相B为15 mmoL/L NaOH,流动相C为15 mmoL/L NaOH与100 mmoL/L NaOAc混合液。
1.2.1.4 火龙果茎多糖表面微观结构测定
称取火龙果茎多糖,用离子镀膜机进行喷金处理。使用扫描电镜对真空喷金后的多糖样品进行形貌观测。参数设置为:加速电压5 kV。条件为:放大100、500、1000和2000倍下进行观察。
1.2.2 火龙果茎多糖抗氧化活性分析
1.2.2.1 羟基自由基清除能力
采用羟基自由基测试试剂盒测定火龙果茎多糖的羟基自由基清除能力,参照试剂盒说明书进行操作。火龙果茎多糖抑制羟基自由基能力按照公式(3)计算。
抑制羟基自由基能力(U/mL)=A对照−A测定A标准−A空白×C标准×1V样×N (3) 式中,A对照为底物应用液的吸光度值;A标准为0.03% H2O2标准应用液的吸光度值;A测定为火龙果茎多糖溶液的吸光度值;A空白为去离子水的吸光度值;C标准为标准品浓度(8.824 mmol/L);V样为测定时样品的取样量(0.2 mL);N为样品测定的稀释倍数。
1.2.2.2 多糖溶液质量浓度筛选
配制质量浓度1~15 mg/mL的火龙果茎多糖溶液,比较分析火龙果茎多糖溶液的不同质量浓度抑制羟基自由基能力。根据公式(3)计算结果,筛选适宜的多糖溶液质量浓度进行后续的抗氧化稳定性实验。
1.2.3 火龙果茎多糖抗氧化稳定性分析
1.2.3.1 光照对多糖抗氧化稳定性的影响
参考赵广河等[17]的方法,取质量浓度10 mg/mL火龙果茎多糖溶液50 mL置于烧杯中,将杯口用保鲜膜封住。烧杯分别于常温下室内自然光、日光灯和避光条件下放置,每隔2 d取样,测定火龙果茎多糖溶液的抑制羟基自由基能力。
1.2.3.2 温度对多糖抗氧化稳定性的影响
参考葛水莲等[22]的方法,取质量浓度10 mg/mL火龙果茎多糖溶液50 mL置于具塞三角瓶中,分别于40、60、80、100 ℃的水浴锅保温3.5 h,每隔0.5 h取样,测定火龙果茎多糖溶液的抑制羟基自由基能力。
1.2.3.3 pH对多糖抗氧化稳定性的影响
参考赵玲玲等[23]的方法,用不同pH的磷酸氢二钠-柠檬酸缓冲溶液配制火龙果茎多糖溶液(pH=3~8),常温下静置2 h后,测定火龙果茎多糖溶液的抑制羟基自由基能力。
1.2.3.4 金属离子对多糖抗氧化稳定性的影响
参考赵玲玲等[23]的方法,取适量的火龙果茎多糖粉末,分别用质量浓度0.2、0.4、0.6、0.8、1.0、1.2 mg/mL的氯化钙、氯化铜、氯化钾、氯化钠和氯化铁溶液配制多糖溶液,常温下静置2 h后,测定火龙果茎多糖溶液的抑制羟基自由基能力。
1.2.3.5 食品添加剂对多糖抗氧化稳定性的影响
参考杨艾华等[24]的方法,取适量的火龙果茎多糖粉末,分别用柠檬酸溶液(质量浓度0、1、2、3、4、5 mg/mL)、苯甲酸钠溶液(质量浓度0、0.05、0.10、0.15、0.20、0.25 mg/mL)、葡萄糖溶液(质量浓度0、10、20、30、40、50 mg/mL)以及蔗糖溶液(质量浓度0、10、20、30、40、50 mg/mL)配制多糖溶液,常温下静置2 h后,测定各组火龙果茎多糖溶液的抑制羟基自由基能力。
1.2.3.6 杀菌方式对多糖抗氧化稳定性的影响
参考赵广河等[17]的方法,分别用沸水灭菌(100 ℃,10 min)、巴氏灭菌(70 ℃,30 min)、高压灭菌(121 ℃,20 min)和微波灭菌(微波功率2.4 W/g,10 min)方式处理火龙果茎多糖溶液,测定火龙果茎多糖溶液的抑制羟基自由基能力。
1.3 数据处理
除单糖组成分析外,所有试验均做3个重复,结果以平均值±标准差表示。采用Origin 2021绘图,IBM SPSS 22软件进行数据的统计分析,通过单因素方差分析(ANOVE)和Duncan多重比较确定显著性差异,当P<0.05时,认为有显著性差异。
2. 结果与分析
2.1 火龙果茎多糖得率与理化特性分析
2.1.1 多糖得率与组成成分分析
根据公式(1)计算出火龙果茎多糖得率为7.22%±0.25%。以标准品溶液的质量浓度为横坐标、吸光度值为纵坐标绘制总糖、黄酮和酚类标准曲线。葡萄糖标准曲线回归方程及相关系数为y=1.5299x−0.1473(R2=0.9996),芦丁标准曲线回归方程及相关系数为y=0.001x+0.0003(R2=0.9999),没食子酸标准曲线回归方程及相关系数为y=0.017x+0.0096(R2=0.9993)。结果表明,采用热水提醇沉法从火龙果茎冻干粉中获得的提取物中多糖含量为(334.63±7.51)mg/g,火龙果茎多糖中黄酮、酚类等成分的残留量分别为(5.91±0.14)mg/g和(5.05±0.06)mg/g。
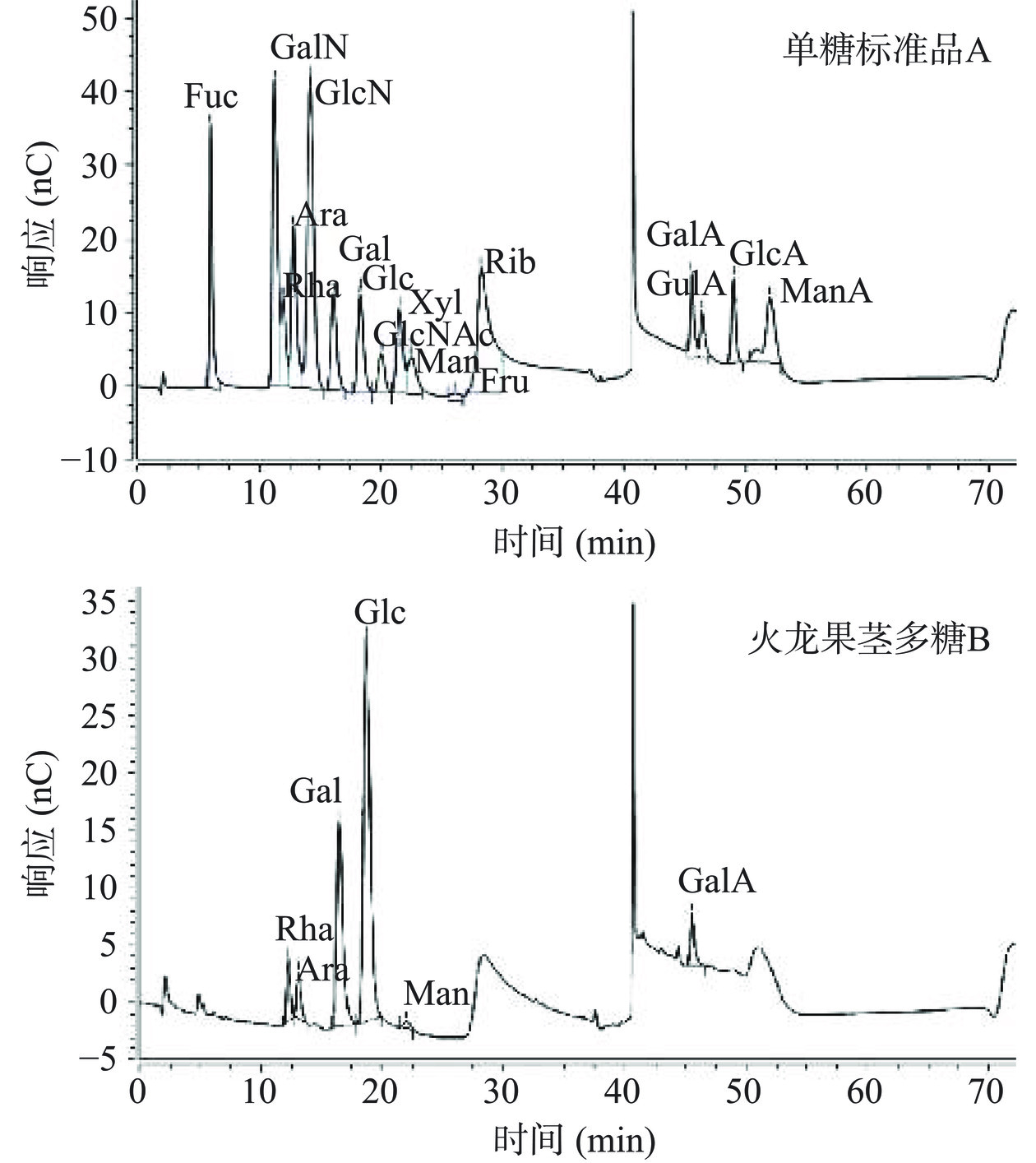
进一步采用离子色谱仪分析火龙果茎多糖的单糖组成。由图1可知,参照单糖标准品图谱,在火龙果茎多糖中检测到6种单糖,分别是Glc、Gal、Rha、GalA、Ara和Man,各单糖摩尔比为5.27:2.77:0.77:0.71:0.32:0.17,其中Glc含量最高,其次为Gal。Tang等[18]对热水提取法制备的火龙果茎多糖进行单糖组成分析,检测到其主要由Gal、Glc、Rha、Ara和Xyl组成,其中以Gal含量最高;王超雪[25]发现超高压提取技术制备的火龙果茎多糖的单糖组成主要为Rha、GlcA、Gal、Glc和GalA,其中以Gal含量最高;马若影[26]采用亚临界水提法制备火龙果茎多糖,结果显示其单糖组成主要为Man、Rha、Glc、Gal、GlcA和Ara,其中Ara为主要单糖。与本实验结果相比,单糖的组成类型与组成比例均存在差异,这可能是由于火龙果茎品种、多糖制备方法、单糖组成分析手段的不同而导致。
2.1.2 多糖表面微观结构分析
图2为不同放大倍率下火龙果茎多糖的扫描电子显微镜图。火龙果茎多糖整体呈大小不均匀的颗粒状,可见分子间具有不同强度的交联作用[27]。火龙果茎多糖表面疏松且具有多孔结构,孔洞较为紧密,孔径呈不规则状。火龙果茎多糖的表面微观特征可能是由于高温提取造成[26]。
2.2 火龙果茎多糖抗氧化活性分析
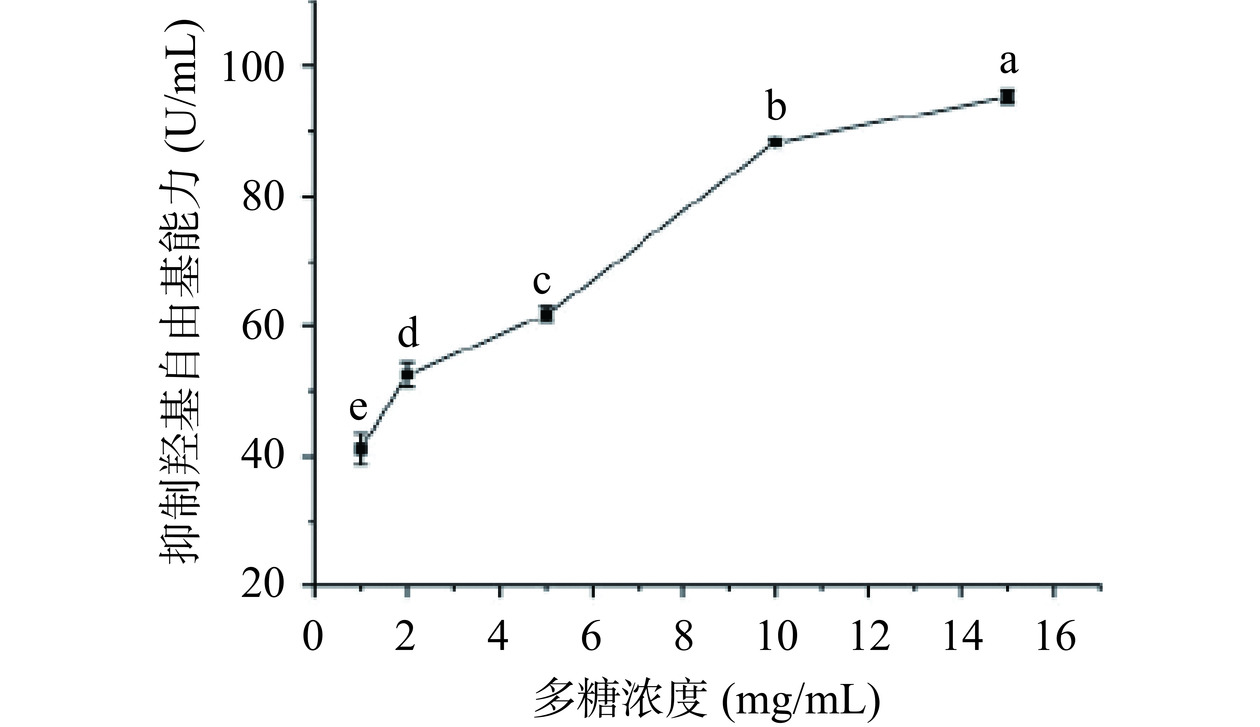
不同质量浓度的火龙果茎多糖溶液对羟基自由基的抑制能力结果见图3。在1~15 mg/mL的质量浓度范围内,随着质量浓度的增加,火龙果茎多糖溶液抑制羟基自由基能力呈现增大趋势(P<0.05),表现出良好的量效关系。王超雪[25]采用超高压提取技术制备火龙果茎多糖,随着浓度的增加其清除羟基自由基的能力亦增强。这与本文测定结果一致。火龙果茎多糖溶液的质量浓度达到10 mg/mL后,抑制羟基自由基能力曲线的变化趋于平缓,故选择质量浓度10 mg/mL的火龙果茎多糖溶液作为后续抗氧化稳定性分析。
2.3 火龙果茎多糖抗氧化稳定性分析
2.3.1 光照对多糖抗氧化稳定性的影响
光照对火龙果茎多糖抗氧化活性的影响见图4。整体来看,光照对火龙果茎多糖的抗氧化活性有较大影响,随着光照时间的延长,火龙果茎多糖抑制羟基自由基的能力显著降低。在持续2 d的日光灯照射下,火龙果茎多糖的羟基自由基抑制能力迅速下降;在第2~10 d中,多糖的抑制羟基自由基能力则呈现缓慢下降的趋势;在第2~6 d自然光和避光条件下,多糖抑制自由基能力显著降低(P<0.05);而在6~10 d中,火龙果茎多糖抑制羟基自由基能力产生不同程度的波动,可能是由于多糖溶液表面张力的作用强度不同,进而影响多糖的抗氧化活性。放置超过10 d后,所有处理条件下的火龙果茎多糖羟基自由基抑制能力显著下降(P<0.05),这可能是因为长时间暴露于强光和(或)高氧环境下导致色素类成分发生进一步氧化和降解[28]。
图4显示,置于避光条件下的火龙果茎多糖的抗氧化活性显著高于经两种光照处理的多糖溶液(P<0.05)。这可能是由于在光度较强的条件下,使火龙果茎多糖在直射光下发生的光解作用[28],并且长时间的光照会破坏多糖-色素结构,火龙果茎多糖中的酚类和黄酮易受到光照的影响而发生降解[29],从而降低其抗氧化活性。另一方面推测由于火龙果茎多糖结构中的羧基受光照影响而发生氧化反应[30],从而降低了多糖的抗氧化能力。因此,火龙果茎多糖的储存与加工过程中,应注意遮光和隔氧保护,以维持火龙果茎多糖的抗氧化活性。
2.3.2 温度对多糖抗氧化稳定性的影响
温度对火龙果茎多糖抗氧化活性的影响见图5。当温度处于40~100 ℃条件下,火龙果茎多糖抑制羟基自由基的能力维持在82~98 U/mL。整体上看,在不同温度条件下,随着加热时间的延长,火龙果茎多糖的抗氧化活性呈现先降低后缓慢升高的变化趋势。在40~80 ℃、加热时间1 h内,火龙果茎多糖的羟基自由基抑制能力缓慢下降,然而在100 ℃、加热时间1 h条件下,多糖抑制自由基能力呈升高趋势。这可能是因为经过此特定条件的热降解处理,多糖分子易形成具有强抗氧化活性的蛋白质-多糖复合物[31],使火龙果茎多糖溶液抗氧化活性获得短暂性提高。加热时间1~2 h,所有温度条件下的火龙果茎多糖抑制羟基自由基能力显著降低(P<0.05)。当加热时间超过3 h后,所有温度条件下的火龙果茎多糖抑制羟基自由基能力显著回升(P<0.05),尤其是在100 ℃、加热时间3.5 h条件下,火龙果茎多糖的抑制羟基自由基能力最高(达到98 U/mL)。这可能是由于火龙果茎多糖里的色素类成分热稳定性差[32],随着加热时间延长至2 h,大多数的色素类成分发生热降解[33],影响其抗氧化活性;另一方面,热降解后的多酚、黄酮等色素类成分与多糖、蛋白质共价或非共价相互作用,形成多酚/黄酮-蛋白质/多糖复合物[32],多组分的相互作用可以提高抗氧化剂的稳定性,使其抗氧化活性得到提高[33]。
2.3.3 pH对多糖抗氧化稳定性的影响
pH对火龙果茎多糖抗氧化活性的影响见图6。整体来看,在pH3~8范围内,火龙果茎多糖的抗氧化活性维持在较高水平,其抑制羟基自由基能力在91.61~94.06 U/mL。随着pH增加,火龙果茎多糖的抑制羟基自由基能力呈现先降低后升高的趋势。当pH<4时,火龙果茎多糖的抑制羟基自由基能力较高;当pH升高到5时,多糖抑制自由基能力下降;而当pH≥6时,多糖抑制自由基能力增高且趋于平缓。这可能是由于在强酸条件下,火龙果茎多糖发生水解作用,水解产物中增加了糖醛酸和蛋白质含量[34],进而提高了多糖溶液的抗氧化活性;另一方面,在不同pH条件下,火龙果茎多糖溶液中的色素类成分亦会发生不同程度的降解[35],因此火龙果茎多糖溶液的抗氧化活性随之产生变化。
2.3.4 金属离子对多糖抗氧化稳定性的影响
金属离子对火龙果茎多糖抗氧化活性的影响见图7。在不同质量浓度(0.2~1.2 mg/mL)的K+、Ca2+和Na+溶液处理下,火龙果茎多糖抑制羟基自由基的能力有一定程度的波动,但是整体来看对多糖的抗氧化活性影响不大。在质量浓度0.2~0.6 mg/mL时,Cu2+溶液对火龙果茎多糖的羟基自由基抑制能力影响不大,而当Cu2+浓度大于0.6 mg/mL时,其抑制自由基能力显著降低(P<0.05)。在不同质量浓度(0.2~1.2 mg/mL)的Fe3+溶液处理下,火龙果茎多糖的羟基自由基抑制能力随Fe3+溶液浓度的增加而快速下降。这可能是由于火龙果茎多糖与不同离子之间的配位能力或配位方式的差异,造成了络合物空间结构的差别[36],从而使火龙果茎多糖的抗氧化活性产生了变化。因此在存储或生产火龙果茎产品的过程中应尽量避免与铁、铜容器接触。
2.3.5 食品添加剂对多糖抗氧化稳定性的影响
常用食品添加剂对火龙果茎多糖抗氧化活性的影响见图8。在不同浓度的柠檬酸(图8A)、苯甲酸钠(图8B)和葡萄糖(图8C)处理下,火龙果茎多糖抑制羟基自由基的能力有一定程度的波动,但是整体对多糖的抗氧化活性影响不大。这可能是因为添加了酸性添加剂(柠檬酸)和碱性添加剂(苯甲酸钠)后,受pH的影响,火龙果茎多糖溶液中的色素类成分发生了降解,而多糖作为多酚、黄酮等色素类成分的载体,故对羟基自由基的影响不明显[37];另一方面推测是由于二者作为防腐剂,多糖-防腐剂混合溶液中的羧基基团易与水的氢键相互作用,例如苯甲酸钠中的羧基可与水分子发生氢键作用,使多糖分子的供氢能力增强,从而保持其良好的抗氧化活性[38]。与柠檬酸、苯甲酸钠和葡萄糖溶液处理不同,当蔗糖溶液浓度大于40 mg/mL时,火龙果茎多糖抑制羟基自由基能力显著下降(图8D)。推测原因可能是葡萄糖作为单糖,已不能再进行水解,因而对火龙果茎多糖的抗氧化活性影响较小;而作为二糖的蔗糖,糖分子与水的竞争增加溶液的粘度,当蔗糖溶液浓度升高时,二者之间的相互作用随之增强[39],因此高浓度的蔗糖溶液会影响多糖的抗氧化活性。可见,在制作火龙果茎加工产品中尽量避免添加高浓度的蔗糖。
2.3.6 杀菌方式对多糖抗氧化稳定性的影响
杀菌方式对火龙果茎多糖抗氧化活性的影响见图9。总体来看,不同杀菌方式对火龙果茎多糖的抗氧化活性有不同的影响,与未灭菌相比,煮沸灭菌和高压灭菌显著提升了火龙果茎多糖的抗氧化能力(P<0.05)。根据产品类型和环境条件选择适宜的杀菌条件,达到最佳的杀菌效果,同时能保留较高的多糖抗氧化活性,节约生产成本的同时有效提高生产效率。因此,在火龙果茎加工产品的生产过程中,可优先选择煮沸灭菌或高压灭菌方式。
3. 结论
以火龙果茎多糖为研究对象,对其理化特性、抗氧化活性和稳定性进行了分析。研究结果显示,热水制备的火龙果茎多糖呈现表面疏松、多孔且不规则型的颗粒结构,主要由Glc、Gal、Rha等单糖组成,具有较好的抗氧化活性,且随着多糖质量浓度的提高,其抗氧化活性随之增加。然而,火龙果茎多糖的抗氧化活性易受到食品加工条件的影响,其中长期光照、金属铁离子和铜离子、高浓度蔗糖条件会显著影响其稳定性,在火龙果茎的贮藏与加工中建议避开此类条件。后续研究将采用细胞模型和动物模型,对火龙果茎多糖的抗氧化活性系统性深入研究与分析,以进一步促进其运用于抗氧化食品和药品中。
-
-
[1] 慕雪, 刘垠泽, 吴恒梅. 白心火龙果果皮多糖提取及抗氧化研究[J]. 中国野生植物资源,2023,42(3):21−25,37. [MU Xue, LIU Yinze, WU Hengmei. Study on extraction and antioxidation of polysaccharide from the peel of Hylocereus undatus pericarp[J]. Chinese Wild Plant Resources,2023,42(3):21−25,37.] doi: 10.3969/j.issn.1006-9690.2023.03.004 MU Xue, LIU Yinze, WU Hengmei. Study on extraction and antioxidation of polysaccharide from the peel of Hylocereus undatus pericarp[J]. Chinese Wild Plant Resources, 2023, 42(3): 21−25,37. doi: 10.3969/j.issn.1006-9690.2023.03.004
[2] 李国胜, 白新鹏. 火龙果茎多糖提取方法比较[J]. 热带农业科学,2021,41(11):61−67. [LI Guosheng, BAI Xinpeng. Comparison of extraction methods for extraction of polysaccharides from pitaya stem[J]. Chinese Journal of Tropical Agriculture,2021,41(11):61−67.] LI Guosheng, BAI Xinpeng. Comparison of extraction methods for extraction of polysaccharides from pitaya stem[J]. Chinese Journal of Tropical Agriculture, 2021, 41(11): 61−67.
[3] 罗卢弟, 蒲美玲, 黄杰, 等. 无刺黄龙火龙果在广西百色的引种表现及栽培技术[J]. 中国果树,2023(10):108−111. [LUO Ludi, PU Meiling, HUANG Jie, et al. Introduction performence and cultivation techniques of ‘wucihuanglong’ pitaya in baise, Guangxi[J]. China Fruits,2023(10):108−111.] LUO Ludi, PU Meiling, HUANG Jie, et al. Introduction performence and cultivation techniques of ‘wucihuanglong’ pitaya in baise, Guangxi[J]. China Fruits, 2023(10): 108−111.
[4] 韦丽兰. 广西火龙果产业现状与发展路径探析[J]. 南方园艺,2023,34(2):58−63. [WEI Lilan. Study of status quo ang development route of Hyocereus undatus industry in guangxi[J]. Southern Horticulture,2023,34(2):58−63.] doi: 10.3969/j.issn.1674-5868.2023.02.011 WEI Lilan. Study of status quo ang development route of Hyocereus undatus industry in guangxi[J]. Southern Horticulture, 2023, 34(2): 58−63. doi: 10.3969/j.issn.1674-5868.2023.02.011
[5] CHRISNASARI R, SUDONO C C, UTAMI M R D, et al. The proximate and phytochemical properties of red pitaya (Hylocereus polyrhizus) stem flour and its potential application as food products[J]. Pertanika Journal of Tropical Agricultural Science,2019,42(3):903−920.
[6] 陈雅芝, 刘瑞, 于章龙, 等. 火龙果茎成分及其抗氧化活性分析[J]. 农产品加工,2020(5):55−58,61. [CHEN Yazhi, LIU Rui, YU Zhanglong, et al. Analysis of components and antioxidant activities of pitaya stem[J]. Farm Products Processing,2020(5):55−58,61.] CHEN Yazhi, LIU Rui, YU Zhanglong, et al. Analysis of components and antioxidant activities of pitaya stem[J]. Farm Products Processing, 2020(5): 55−58,61.
[7] HE C F, LI P, ZHAO H, et al. Extraction optimization of polysaccharides from pitaya stems[J]. Agricultural Science and Technology-Hunan,2011,12(7):947−979.
[8] 何聪芬, 李鹏, 赵进, 等. 火龙果茎多糖的提取及结构鉴定[J]. 食品与发酵工业,2009,35(11):140−143. [HE Congfen, LI Peng, ZHAO Jin, et al. Polysaccharide extraction from the stem of pitaya by microwave-assisted extraction and its structure characterization[J]. Food and Fermentation Industries,2009,35(11):140−143.] HE Congfen, LI Peng, ZHAO Jin, et al. Polysaccharide extraction from the stem of pitaya by microwave-assisted extraction and its structure characterization[J]. Food and Fermentation Industries, 2009, 35(11): 140−143.
[9] 苏敬红, 牛格格, 吴佳琦, 等. 不同干燥方式对火龙果茎多糖理化特性及功能活性的影响[J]. 食品研究与开发,2021,42(15):34−39. [SU Jinghong, NIU Gege, WU Jiaqi, et al. Effects of different drying methods on physicochemical properties and functional activities of polysaccharides from Hylocereus undatus stem[J]. Food Research and Development,2021,42(15):34−39.] doi: 10.12161/j.issn.1005-6521.2021.15.006 SU Jinghong, NIU Gege, WU Jiaqi, et al. Effects of different drying methods on physicochemical properties and functional activities of polysaccharides from Hylocereus undatus stem[J]. Food Research and Development, 2021, 42(15): 34−39. doi: 10.12161/j.issn.1005-6521.2021.15.006
[10] 马若影, 杨慧强, 李国胜, 等. 亚临界水提取红心火龙果茎多糖及其抗氧化活性[J]. 食品工业科技,2017,38(10):286−290. [MA Ruoying, YANG Huiqiang, LI Guosheng, et al. Study on the extraction and antioxidant activity of polysaccharide from red pulp Hylocereus undatus stem by subcritical water[J]. Science and Technology of Food Industry,2017,38(10):286−290.] MA Ruoying, YANG Huiqiang, LI Guosheng, et al. Study on the extraction and antioxidant activity of polysaccharide from red pulp Hylocereus undatus stem by subcritical water[J]. Science and Technology of Food Industry, 2017, 38(10): 286−290.
[11] 马若影, 李幼梅, 邓志勇, 等. 大孔树脂对红心火龙果茎多糖脱色除蛋白及抗氧化活性的影响[J]. 热带作物学报,2018,39(7):1297−1303. [MA Ruoying, LI Youmei, DENG Zhiyong, et al. Effect of macroporous resin on decolorization and deproteinization technology and antioxidant activity of polysaccharide from red pulp Hylocereus undatus stem[J]. Chinese Journal of Tropical Crops,2018,39(7):1297−1303.] doi: 10.3969/j.issn.1000-2561.2018.07.006 MA Ruoying, LI Youmei, DENG Zhiyong, et al. Effect of macroporous resin on decolorization and deproteinization technology and antioxidant activity of polysaccharide from red pulp Hylocereus undatus stem[J]. Chinese Journal of Tropical Crops, 2018, 39(7): 1297−1303. doi: 10.3969/j.issn.1000-2561.2018.07.006
[12] 唐雅园, 何雪梅, 孙健, 等. 火龙果茎多糖在护手霜中的应用及性能评价[J]. 日用化学工业,2022,52(4):410−417. [TANG Yayuan, HE Xuemei, SUN Jian, et al. Application and properties of the polysaccharide from red pulp pitaya stem in hand creams[J]. China Surfactant Detergent & Cosmetics,2022,52(4):410−417.] TANG Yayuan, HE Xuemei, SUN Jian, et al. Application and properties of the polysaccharide from red pulp pitaya stem in hand creams[J]. China Surfactant Detergent & Cosmetics, 2022, 52(4): 410−417.
[13] 梁秋杨, 白新鹏, 李国胜, 等. 火龙果茎多糖对调节小鼠细胞免疫功能的研究及毒性评价[J]. 热带作物学报,2023,44(10):2126−2134. [LIANG Qiuyang, BAI Xinpeng, LI Guosheng, et al. Toxicity evaluation of polysaccharides from pitaya stem on regulating cellular immune function in mice[J]. Chinese Journal of Tropical Crops,2023,44(10):2126−2134.] doi: 10.3969/j.issn.1000-2561.2023.10.024 LIANG Qiuyang, BAI Xinpeng, LI Guosheng, et al. Toxicity evaluation of polysaccharides from pitaya stem on regulating cellular immune function in mice[J]. Chinese Journal of Tropical Crops, 2023, 44(10): 2126−2134. doi: 10.3969/j.issn.1000-2561.2023.10.024
[14] SIHAG S, AJAY P, VINOD S. Antioxidant properties and free radicals scavenging activities of pomegranate (Punica granatum L.) peels:An in-vitro study[J]. Biocatalysis and Agricultural Biotechnology,2022,42:102368. doi: 10.1016/j.bcab.2022.102368
[15] 宋晨光. 植物多糖抗氧化活性研究进展[J]. 中国果菜,2022,42(4):25−33. [SONG Chenguang. Advances in antioxidant activity of plant polysaccharides[J]. China Fruit & Vegetable,2022,42(4):25−33.] SONG Chenguang. Advances in antioxidant activity of plant polysaccharides[J]. China Fruit & Vegetable, 2022, 42(4): 25−33.
[16] ZHANG Y, CHEN Z H, HUANG Z, et al. A comparative study on the structures of Grifola frondosa polysaccharides obtained by different decolourization methods and their in vitro antioxidant activities[J]. Food & Function,2019,10(10):6720−6731.
[17] 赵广河, 陆玺文, 胡梦琪, 等. 桃金娘果实多糖抗氧化稳定性的研究[J]. 食品研究与开发,2021,42(16):65−70. [ZHAO Guanghe, LU Xiwen, HU Mengqi, et al. Study of antioxidant stability of polysaccharides from Rhodomyrtus tomentosa (ait.) Hassk Berries[J]. Food Research and Development,2021,42(16):65−70.] doi: 10.12161/j.issn.1005-6521.2021.16.010 ZHAO Guanghe, LU Xiwen, HU Mengqi, et al. Study of antioxidant stability of polysaccharides from Rhodomyrtus tomentosa (ait.) Hassk Berries[J]. Food Research and Development, 2021, 42(16): 65−70. doi: 10.12161/j.issn.1005-6521.2021.16.010
[18] TANG Y Y, HE X M, LIU G M, et al. Effects of different extraction methods on the structural, antioxidant and hypoglycemic properties of red pitaya stem polysaccharide[J]. Food Chemistry,2023,405:134804. doi: 10.1016/j.foodchem.2022.134804
[19] TARANNUM N, HOSSAIN T J, ALI F, et al. Antioxidant, antimicrobial and emulsification properties of exopolysaccharides from lactic acid bacteria of bovine milk:Insights from biochemical and genomic analysis[J]. LWT,2023,186:115263. doi: 10.1016/j.lwt.2023.115263
[20] 吴冬凡, 庞杜贤, 林清盛. 火龙果果皮总黄酮和多糖的提取工艺及抗氧化研究[J]. 华南师范大学学报(自然科学版),2021,53(5):68−75. [WU Dongfan, PANG Duxian, LIN Qingsheng. On the extraction and antioxidation of total flavonoids and polysaccharides from pitaya peel (Hylocereus undatus ‘Foo−Lon’)[J]. Journal of South China Normal University (Natural Science Edition),2021,53(5):68−75.] doi: 10.6054/j.jscnun.2021077 WU Dongfan, PANG Duxian, LIN Qingsheng. On the extraction and antioxidation of total flavonoids and polysaccharides from pitaya peel (Hylocereus undatus ‘Foo−Lon’)[J]. Journal of South China Normal University (Natural Science Edition), 2021, 53(5): 68−75. doi: 10.6054/j.jscnun.2021077
[21] 孙卉, 康蒙, 陈玉凤, 等. 火龙果果皮多酚及其抗氧化活性研究[J]. 食品安全导刊,2022(31):124−129. [SUN Hui, KANG Meng, CHEN Yufeng, et al. Study on polyphenols and antioxidant activity of Hylocereus undulates Britt peel[J]. China Food Safety Magazine,2022(31):124−129.] doi: 10.3969/j.issn.1674-0270.2022.31.spaqdk202231043 SUN Hui, KANG Meng, CHEN Yufeng, et al. Study on polyphenols and antioxidant activity of Hylocereus undulates Britt peel[J]. China Food Safety Magazine, 2022(31): 124−129. doi: 10.3969/j.issn.1674-0270.2022.31.spaqdk202231043
[22] 葛水莲, 陈建中, 刘娜, 等. 太行菊多糖抗氧化活性及稳定性研究[J]. 食品科技,2020,45(4):169−174. [GE Shuilian, CHEN Jianzhong, LIU Na, et al. Study on antioxidant activity and stability of polysaccharides from Opisthopappus taihangensis[J]. Food Science and Technology,2020,45(4):169−174.] GE Shuilian, CHEN Jianzhong, LIU Na, et al. Study on antioxidant activity and stability of polysaccharides from Opisthopappus taihangensis[J]. Food Science and Technology, 2020, 45(4): 169−174.
[23] 赵玲玲, 张红运, 范宏亮, 等. pH, Na+和Ca2+对大豆种皮果胶类多糖乳化稳定性的影响[J]. 中国粮油学报,2019,34(1):30−36. [ZHAO Lingling, ZHANG Hongyun, FAN Hongliang, et al. Effects of pH, Na+ and Ca2+ on the emulsion stability of soybean hull pectic polysaccharide[J]. Journal of the Chinese Cereals and Oils Association,2019,34(1):30−36.] ZHAO Lingling, ZHANG Hongyun, FAN Hongliang, et al. Effects of pH, Na+ and Ca2+ on the emulsion stability of soybean hull pectic polysaccharide[J]. Journal of the Chinese Cereals and Oils Association, 2019, 34(1): 30−36.
[24] 杨艾华, 宋姗姗, 王微微. 湄潭白茶多糖抗氧化活性及稳定性研究[J]. 食品科技,2021,46(10):194−199. [YANG Aihua, SONG Shanshan, WANG Weiwei. Antioxidant activity and stability of polysaccharides from meitan white tea[J]. Food Science and Technology,2021,46(10):194−199.] doi: 10.3969/j.issn.1005-9989.2021.10.spkj202110031 YANG Aihua, SONG Shanshan, WANG Weiwei. Antioxidant activity and stability of polysaccharides from meitan white tea[J]. Food Science and Technology, 2021, 46(10): 194−199. doi: 10.3969/j.issn.1005-9989.2021.10.spkj202110031
[25] 王超雪. 红心火龙果果皮、茎叶中多糖分离纯化及抗氧化活性研究[D]. 长春:长春师范大学, 2020. [WANG Chaoxue. Separation and purification and antioxidant activities of polysaccharides from peels and leaves of red dragon fruit[D]. Changchun:Changchun Normal University, 2020.] WANG Chaoxue. Separation and purification and antioxidant activities of polysaccharides from peels and leaves of red dragon fruit[D]. Changchun: Changchun Normal University, 2020.
[26] 马若影. 红心火龙果茎中多糖的制备及性能研究[D]. 海口:海南大学, 2019. [MA Ruoying. Study of the preparation and property of polysaccharide from red pulp pitaya stem[D]. Haikou:Hainan University, 2019.] MA Ruoying. Study of the preparation and property of polysaccharide from red pulp pitaya stem[D]. Haikou: Hainan University, 2019.
[27] 董伟, 马生健, 马文欣, 等. 凉粉草多糖的理化性质及其体外抗氧化活性[J]. 食品研究与开发,2023,44(9):52−58. [DONG Wei, MA Shengjian, MA Wenxin, et al. Physicochemical properties and in vitro antioxidant activity of Mesona chinensis polysaccharides[J]. Food Research and Development,2023,44(9):52−58.] doi: 10.12161/j.issn.1005-6521.2023.09.008 DONG Wei, MA Shengjian, MA Wenxin, et al. Physicochemical properties and in vitro antioxidant activity of Mesona chinensis polysaccharides[J]. Food Research and Development, 2023, 44(9): 52−58. doi: 10.12161/j.issn.1005-6521.2023.09.008
[28] 贾庆超, 李妍. 黑蒜类黑精的超声提取工艺优化及其稳定性和抗氧化性研究[J]. 食品工业科技,2023,44(19):235−243. [JIA Qingchao, LI Yan. Study on optimization of ultrasonic extraction technology, stability and antioxidation of melanoidin from black garlic[J]. Science and Technology of Food Industry,2023,44(19):235−243.] JIA Qingchao, LI Yan. Study on optimization of ultrasonic extraction technology, stability and antioxidation of melanoidin from black garlic[J]. Science and Technology of Food Industry, 2023, 44(19): 235−243.
[29] ADRIANA K M, RÚBIA C G C, MIGUEL A P, et al. Bioactive natural pigments’ extraction, isolation, and stability in food applications[J]. Molecules,2023,28(3):1200. doi: 10.3390/molecules28031200
[30] 王宏亮, 惠哲哲, 梁犇, 等. 皂荚叶多糖提取工艺及其抗氧化活性的研究[J]. 中国粮油学报,2023,38(12):176−182. [WANG Hongliang, XI Zhezhe, LIANG Ben, et al. Primary study on extraction technology and antioxidant activity of polysaccharides from Gleditsia sinensis leaves[J]. Journal of the Chinese Cereals and Oils Association,2023,38(12):176−182.] WANG Hongliang, XI Zhezhe, LIANG Ben, et al. Primary study on extraction technology and antioxidant activity of polysaccharides from Gleditsia sinensis leaves[J]. Journal of the Chinese Cereals and Oils Association, 2023, 38(12): 176−182.
[31] VENTER A, FISHER H, STAFFORD G I, et al. Pigmented flower extracts of plant species from the Geraniaceae and Lamiaceae families as natural food colourants:Anthocyanin composition, thermal and oxidative stability[J]. International Journal of Food Science & Technology,2022,57(7):4347−4355.
[32] 熊丹妮, 胡中泽, 刘刚, 等. 米糠多糖提高葡萄籽原花青素热稳定性和抗氧化性的研究[J]. 武汉轻工大学学报,2023,42(2):1−8. [XIONG Danni, HU Zhongze, LIU Gang, et al. Study on enhancing thermal stability and antioxidant activity of grape seeds proanthocyanidin by rice bran polysaccharide[J]. Journal of Wuhan Polytechnic University,2023,42(2):1−8.] doi: 10.3969/j.issn.2095-7386.2023.02.001 XIONG Danni, HU Zhongze, LIU Gang, et al. Study on enhancing thermal stability and antioxidant activity of grape seeds proanthocyanidin by rice bran polysaccharide[J]. Journal of Wuhan Polytechnic University, 2023, 42(2): 1−8. doi: 10.3969/j.issn.2095-7386.2023.02.001
[33] WU Jun, WANG Xiaona, HE Yu, et al. Stability evaluation of gardenia yellow pigment in presence of different phenolic compounds[J]. Food Chemistry,2022,373:131441. doi: 10.1016/j.foodchem.2021.131441
[34] 张宏媛, 钱佳俊, 李哲远, 等. 部分酸水解对桃胶多糖结构和乳化功能的影响[J]. 食品科学,2023,44(4):99−106. [ZHANG Hongyuan, QIAN Jiajun, LI Zheyuan, et al. Effect of partial acid hydrolysis on the structure and emulsifying function of peach gum polysaccharide[J]. Food Science,2023,44(4):99−106.] doi: 10.7506/spkx1002-6630-20220519-259 ZHANG Hongyuan, QIAN Jiajun, LI Zheyuan, et al. Effect of partial acid hydrolysis on the structure and emulsifying function of peach gum polysaccharide[J]. Food Science, 2023, 44(4): 99−106. doi: 10.7506/spkx1002-6630-20220519-259
[35] JIMÉNEZ-GONZÁLEZ O, LÓPEZ-MALO A, GONZÁLEZ-PÉREZ J E, et al. Thermal and pH stability of Justicia spicigera (mexican honeysuckle) pigments:Application of mathematical probabilistic models to predict pigments stability[J]. Food Chemistry:Molecular Sciences,2023,6:100158.
[36] 王世越, 柯钦豪, 周宏福, 等. 多糖的化学修饰及抗氧化性变化的研究进展[J]. 湖北科技学院学报(医学版),2021,35(2):170−173. [WANG Shiyue, KE Qinhao, ZHOU Hongfu, et al. Research progress on chemical modification and antioxidant activity of polysaccharides[J]. Journal of Hubei University of Sciences ang Tecchnology (Medical Sciences),2021,35(2):170−173.] WANG Shiyue, KE Qinhao, ZHOU Hongfu, et al. Research progress on chemical modification and antioxidant activity of polysaccharides[J]. Journal of Hubei University of Sciences ang Tecchnology (Medical Sciences), 2021, 35(2): 170−173.
[37] JIANG wei, SUI Zhujun, ZHU Zhenyuan. Effect of Cordyceps militaris polysaccharide on the solubility, stability and antioxidant properties of dihydromyricetin[J]. Process Biochemistry,2023,130:606−613. doi: 10.1016/j.procbio.2023.05.028
[38] CHEN Wanwen, CHENG hao, XIA Wenshui. Construction of Polygonatum sibiricum polysaccharide functionalized selenium nanoparticles for the enhancement of stability and antioxidant activity[J]. Antioxidants,2022,11(2):240. doi: 10.3390/antiox11020240
[39] RAHUL S, ANANTA M B. Phenolic profile and pigment stability of Hylocereus species grown in north-east india[J]. Journal of Food Composition and Analysis,2023,116:105078. doi: 10.1016/j.jfca.2022.105078
-
期刊类型引用(0)
其他类型引用(1)





 下载:
下载:







 下载:
下载:



