Effects of Ginseng Peptides on Laxative in Mice
-
摘要: 目的:研究人参肽(Ginseng peptides,GPs)对ICR小鼠便秘模型的润肠通便作用,为GPs的进一步开发利用及临床辅助治疗便秘提供理论依据。方法:将60只成年雄性ICR小鼠随机分为6组,分别为空白组(Normal Group,NG)、便秘模型组(Constipation Group,CG)、乳清蛋白组(Whey Protein Group,WPG)、低剂量(Low-dose Group,LG)、中剂量(Medium-dose Group,MG)、高剂量(High-dose Group,HG)GPs组,除NG外采用盐酸洛哌丁胺(Loperamide Hydrochloride,LH)建立小鼠便秘模型,使用GPs连续干预7 d后,观察各组小鼠的小肠蠕动及排便时间、小肠绒毛组织病理学变化等,通过检测各组小鼠的血清P物质(Substance P,SP)和血管活性肠肽(Vasoactive Intestinal Peptide,VIP)等脑肠肽类物质的含量,评价GPs对小鼠便秘的改善作用。结果:相较于模型组,GPs高、中、低剂量组小鼠小肠墨汁推进率显著增加(P<0.01),可缓解便秘小鼠小肠绒毛病理学损伤,GPs高剂量组小鼠首粒黑便排出时间显著缩短(P<0.01),粪便粒数增多(P<0.05),5 h内粪便重量显著增多(P<0.01)。GPs高、中剂量组小鼠的血清P物质(SP)和血管活性肠肽(VIP)含量显著升高(P<0.01),GPs低剂量组可升高便秘小鼠脑肠肽指标SP及VIP的含量(P<0.05)。结论:GPs对便秘小鼠模型具有明显的通便效果,可促进小肠蠕动、缓解小鼠小肠绒毛损伤,促进小鼠脑肠肽指标SP及VIP的表达。Abstract: Objective: To study the moisturizing and laxative effects of ginseng peptides (GPs) on the constipation model of ICR mice, and provide theoretical basis for the further development and utilization of GPs and clinical adjuvant treatment of constipation. Methods: Sixty adult male ICR mice were randomly divided into 6 groups, they were normal group (NG), constipation group (CG), whey protein group (WPG), low-dose GPs group (LG), medium-dose GPs group (MG), high-dose GPs group (HG). Except NG, mouse constipation model was established using loperamide hydrochloride (LH). After 7 consecutive days of intervention with GPs, the small intestine peristalsis and defecation time, as well as pathological changes in the small intestine villus tissue of each group of mice were observed and compared. The improvement effect of GPs on mouse constipation was evaluated by detecting the content of brain gut peptide indicators in the serum of each group of mice, including substance P (SP) and vasoactive intestinal peptide (VIP). Results: Compared with the model group, the high, medium, and low dose groups of GPs significantly increased the small intestine ink advance rate in mice (P<0.01), which could alleviate the pathological damage of small intestine villi in constipated mice. Compared with the model group, the high-dose GPs group significantly shortened the first black stool excretion time (P<0.01), increased the number of fecal particles (P<0.05), and significantly increased fecal weight within 5 hours (P<0.01) in mice. The serum levels of substance P (SP) and vasoactive intestinal peptide (VIP) were significantly increased in the high and medium dose groups of GPs mice (P<0.01), while the low dose group of GPs increased the levels of brain intestinal peptide indicators SP and VIP in constipated mice (P<0.05). Conclusion: GPs has a significant laxative effect on a constipated mouse model, promoting small intestinal peristalsis, alleviating small intestinal villus damage, and promoting the expression of brain gut peptide markers SP and VIP in mice.
-
Keywords:
- ginseng peptides /
- laxative /
- constipation /
- substance P /
- vasoactive intestinal peptide
-
便秘是当今社会极为常见的一种疾病,其症状复杂多样,主要表现为排便困难、粪便干硬、以及明显少于正常次数的排便[1]。当人们饱受便秘困扰时,多数选择用药物来缓解治疗,但常言道:“是药三分毒”。任何药物对于人类而言或多或少会存在一定的副作用,并会产生一定的依赖性。因此,寻找天然、安全、有效的成分治疗便秘势在必行。
肽是由氨基酸排列组合形成的,自然界当中存在着不计其数的氨基酸,随着氨基酸的各种排列组合则会形成无穷的肽,其中小分子的肽可被人体直接吸收,具有许多生理功能,可有效调节身体各项机能[2]。人参肽(Ginseng Peptides,GPs)中含有大量甘氨酸、脯氨酸、丙氨酸和谷氨酸[3],其具有耐缺氧[4]、增强机体免疫力[5]、抗氧化[6]、降血糖[7]、解酒[8]、降血脂[9]、抗疲劳[10] 、调节肠道菌群[11]等诸多生理功能,研究表明小分子肽在体内可不经消化直接被吸收,从而降低肠道消化以及废物排出负担[12]。张亭等[13]利用盐酸洛哌丁胺(Loperamide Hydrochloride,LH)建立小鼠便秘模型,采用核桃低聚肽对其进行干预,并对润肠通便作用和作用机理进行初步研究,结果发现其可调节胃肠道内的激素水平从而达到润肠通便的效果。
目前国内外治疗便秘的药物对肠道有刺激性,易引起药物损伤和肠道依赖性,缺乏更温和安全的治疗[14]。由于肽对人体的安全性、温和性、功效性,本研究在追寻前人的研究基础上,以其为据进行拓展及创新,延申出源于人参中的肽具有润肠通便作用的可能性,因此,实验利用LH建立小鼠便秘模型进而研究GPs的润肠通便作用,为GPs应用于辅助治疗便秘提供理论依据,使得肽广泛的应用于便秘疾病的治疗成为可能。
1. 材料与方法
1.1 材料与仪器
GPs 主要成分为分子量<1000 Da的小分子低聚肽(质量分数>90%),吉林省宏久生物科技股份有限公司;盐酸洛哌丁胺胶囊 西安杨森制药有限公司;阿拉伯树胶 浙江一诺生物科技有限公司;活性炭粉 天津市鼎盛鑫化工有限公司;美国Hilmar9410速溶分离乳清蛋白粉 美国希尔玛乳酪公司;小鼠血管活性肠肽(Vasoactive Intestinal Peptide,VIP)ELISA试剂盒、小鼠P物质(Substance P, SP)ELISA试剂盒 上海源桔生物科技中心;电子秒表计时器 比克曼生物试剂;直尺 鸿泰文具官方旗舰店;一次性注射器 上海琪雅医疗器械有限公司;ICR成年小鼠 雄性、清洁级、60只、体重 18~22 g,辽宁长生生物技术股份有限公司提供(动物许可证号:SCXK(辽)2020-0001)。
BSA2202S电子天平 赛多利斯科学仪器(北京)有限公司;KQ-250DE数控超声波清洗器 昆山市超声仪器有限公司;Neofuge23R台式高速冷冻离心机 上海卢湘仪离心机有限公司。
1.2 实验方法
1.2.1 分组及给药剂量
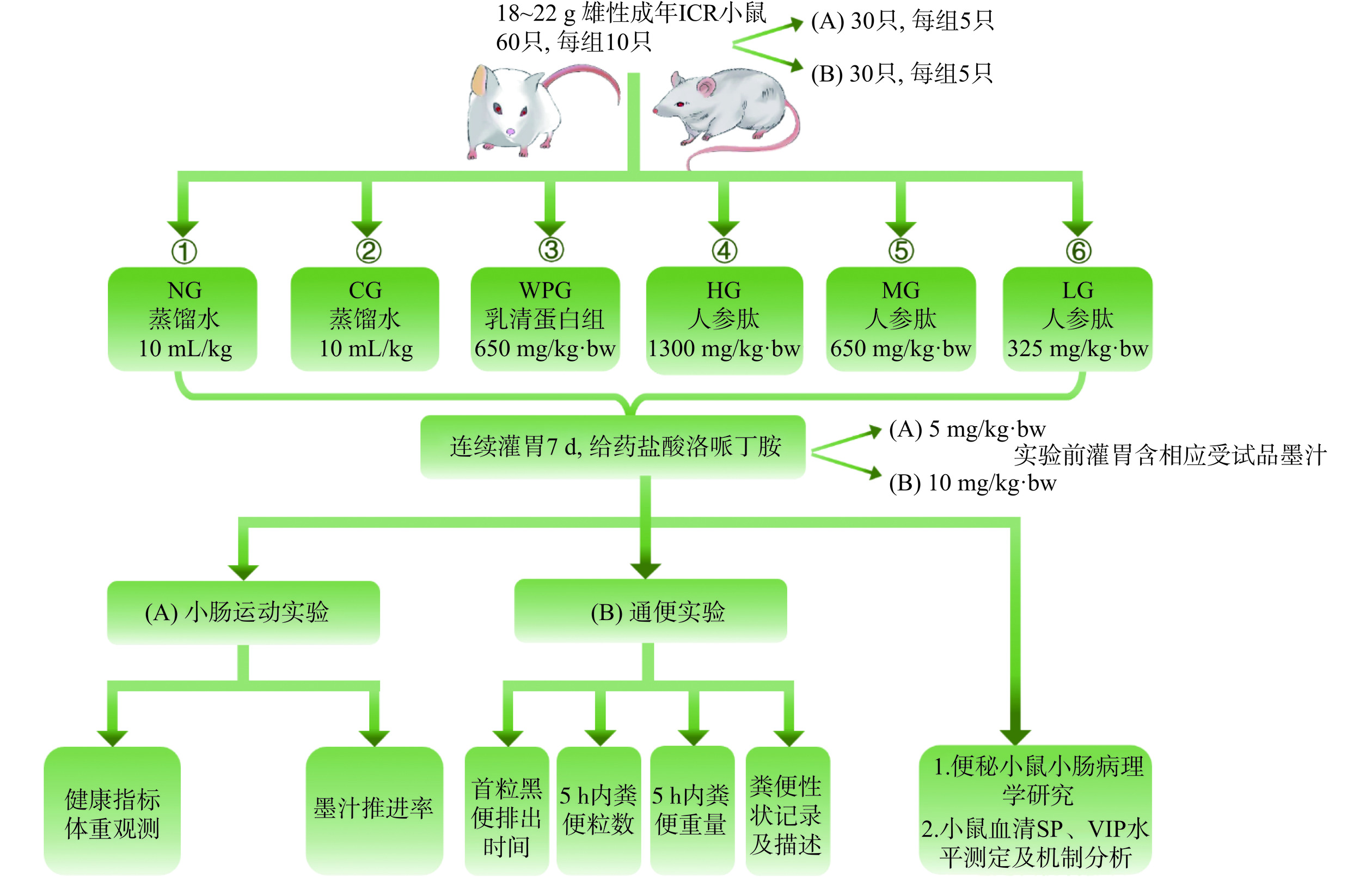
60只ICR小鼠在温度为(22±2)℃、湿度为60%±10%的环境下饲养,动物实验伦理批准号:20200706003。动物实验室每天进行各12 h的明暗更迭,实验前为使小鼠适应周围生长环境对其进行为期7 d的适应性饲养,期间自由饮食。7 d后小鼠们被随机分为A、B两个实验组,每个实验组再随机分为6小组,依次为空白组(Normal Group,NG)、便秘模型组(Constipation Group,CG)、乳清蛋白组(Whey Protein Group,WPG,设置乳清蛋白组是为了排除蛋白质的额外摄入对便秘的影响,以免影响实验结果)、低(Low-dose Group,LG)、中(Medium-dose Group,MG)、高剂量(High-dose Group,HG)GPs组,每组5只。连续7 d灌胃前同一时间测量并记录所有组小鼠体重,各组灌胃物及具体剂量如图1所示[15]。
1.2.2 小肠运动实验(A)
1.2.2.1 小肠蠕动抑制模型的建立
灌胃一定剂量的LH以建立小鼠小肠蠕动抑制模型,以一定时间内小肠的墨汁推进率为指标,来判断模型小鼠的小肠蠕动功能的强弱[13]。根据图1的剂量灌胃各组小鼠相应药物7 d后,对各组小鼠进行禁食16 h操作,期间自由饮水。除空白组灌胃蒸馏水,其余各组均灌胃给药LH 5 mg/kg·bw,进而建立小肠蠕动抑制模型。
1.2.2.2 指标测定方法
给药0.5 h后,除空白组和模型组按照小鼠体重给予墨汁灌胃,其余各组分别给予含相应受试样品的墨汁,按照表1剂量灌胃给药。25 min后迅速脱颈处死小鼠,立即解剖,打开腹腔,完整的拉出整根肠管,找到以胃下端幽门为起始,以回肠末端与盲肠互相交接的回盲部为终止的肠管,剪取此部分肠管将其拉直摆正置于托盘上,使其平行于直尺,进而测量此部分肠管长度为“小肠总长度”,再用同样的方法测量从胃下端幽门至墨汁前沿的长度,记为“墨汁推进长度”。按下式计算墨汁推进率:
表 1 各组小鼠灌胃剂量Table 1. Dosage of mice in each group组别 灌胃剂量(受试物溶于墨汁) NG 墨汁10 mL/kg CG 墨汁10 mL/kg WPG 乳清蛋白650 mg/kg·bw HG GPs 1300 mg/kg·bw MG GPs 650 mg/kg·bw LG GPs 325 mg/kg·bw 墨汁推进率(%)=墨汁推进长度(cm)小肠总长度(cm)×100 1.2.3 通便实验(B)
1.2.3.1 小鼠便秘模型的建立及原理
灌胃一定剂量的LH以建立小鼠便秘模型[13],以各组小鼠的排出首粒排黑便的时间、5 h内所排出的粪便粒数及重量为依据,以此来反映模型小鼠的排便情况,从而进行系统的分析。根据图1的剂量灌胃各组小鼠相应药物7 d后,对各组小鼠进行禁食16 h操作,期间自由饮水。除空白组灌胃蒸馏水,其余各组均灌胃给药LH10 mg/kg·bw,进而建立小鼠便秘模型。
1.2.3.2 指标测定方法
给药LH 0.5 h后,除空白组和模型组按照小鼠体重给予墨汁灌胃,其余各组分别给予含相应受试样品的墨汁,灌胃给药剂量同表1。需注意动物均需单笼饲养,不禁食禁水。每一只以各自的灌胃墨汁结束为开始进行计时,特派一人一只鼠,以达到提高准确率,减少实验过程中带来误差,同时观测人员使用同一型号的计时器精准计时,使用统一的电子天平进行小鼠粪便称重,准确观察并记录每只小鼠排首粒黑便时间、5 h内排黑便粒数、重量,并对粪便性状进行及时的记录。
1.2.4 人参肽对便秘小鼠小肠病理变化的影响
小鼠眼球取血后断颈处死,进行解剖取其空肠1 cm,利用冰冷的生理盐水冲洗后,固定于4%的多聚甲醛溶液中。浸泡24 h以上,依次进行组织脱水、透明、浸蜡与包埋制成蜡块、石蜡切片(厚度为3~5 μm)脱蜡与水化、苏木素染色、分化、返蓝、伊红染色、脱水、浸泡、封片等操作,封片后显微镜下观察各组小肠绒毛病理改变情况。
1.2.5 人参肽对便秘小鼠血清P物质(SP)、血管活性肠肽(VIP)的影响
各组小鼠排便实验结束后,将小鼠眼球取血后断颈处死,室温下血液自然凝固15 min,3000 r/min,低温下离心20 min,收集上清血清备用,保存过程中如若再次出现沉淀浑浊等现象,则需再次离心。具体操作步骤按照小鼠血清P物质(SP)、血管活性肠肽(VIP)ELISA试剂盒严格执行[16]。
1.3 数据处理
各试验均设立三次平行,所得数据以“平均值±标准差”形式表示,利用Orign 2021绘图,Microsoft Excel 2019、SPSS 26数据分析,通过单因素方差分析对数据进行分析,统计学显著性设定P<0.05或P<0.01。
2. 结果与分析
2.1 人参肽对小鼠的体重影响
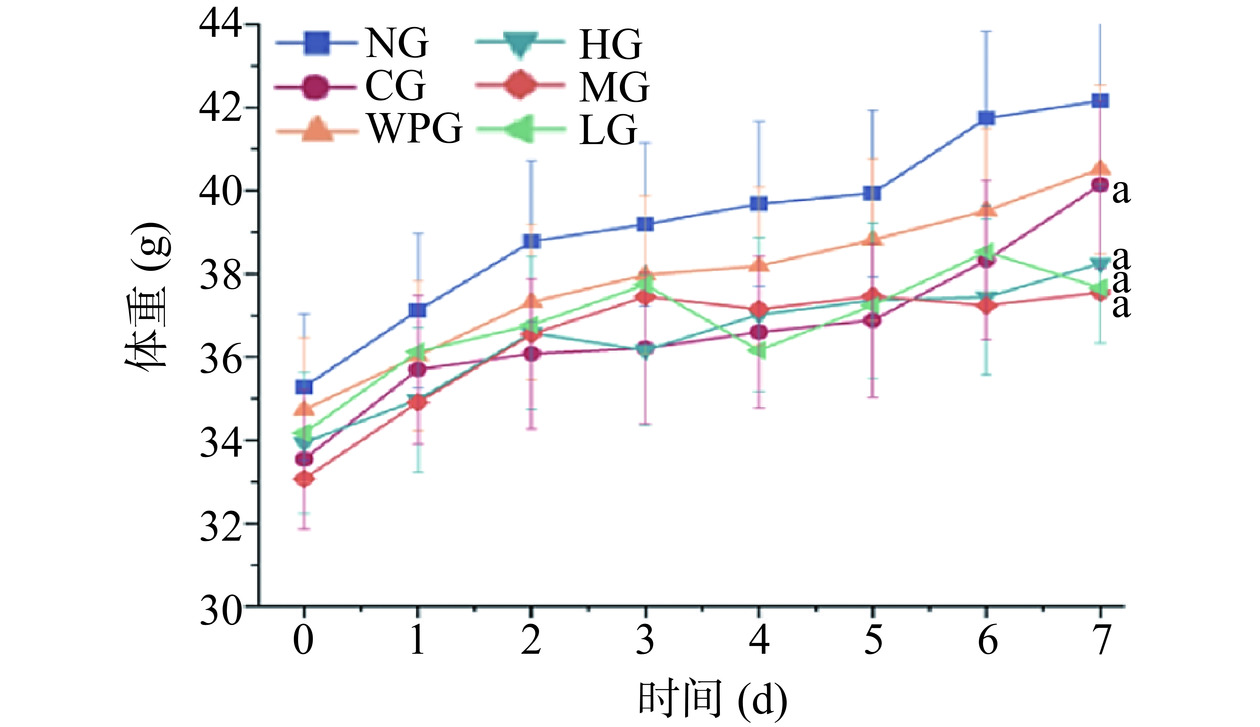
与CG组相比,GPs各剂量组小鼠毛发更有光泽,精神状态良好,无明显攻击性。与NG组相比,HG、MG、LG组小鼠体重显著降低(P<0.01)。由图2可见各组小鼠0~7 d体重的变化趋势,可见GPs各剂量组体重升幅较NG组相对缓慢[17]。综上所述,GPs对小鼠一段时间内的生长发育有明显影响,在灌胃给药过程中发现中、高剂量GPs组的小鼠粪便随着剂量升高,粪便稍显湿润,这可能是中、高剂量GPs组小鼠小肠蠕动相对稍快并且体重稍有下降的原因[18]。
2.2 人参肽对小鼠小肠运动的影响
LH是作用于肠壁的阿片受体,其作用机制是阻止前列腺素和乙酰胆碱的释放,从而抑制结肠的蠕动,并且阻碍肠道当中水分的有效分泌,由此粪便的含水量降低,便可止泻,但也会使粪便干燥[19];LH是建立小鼠便秘模型的常用药[20−22]。
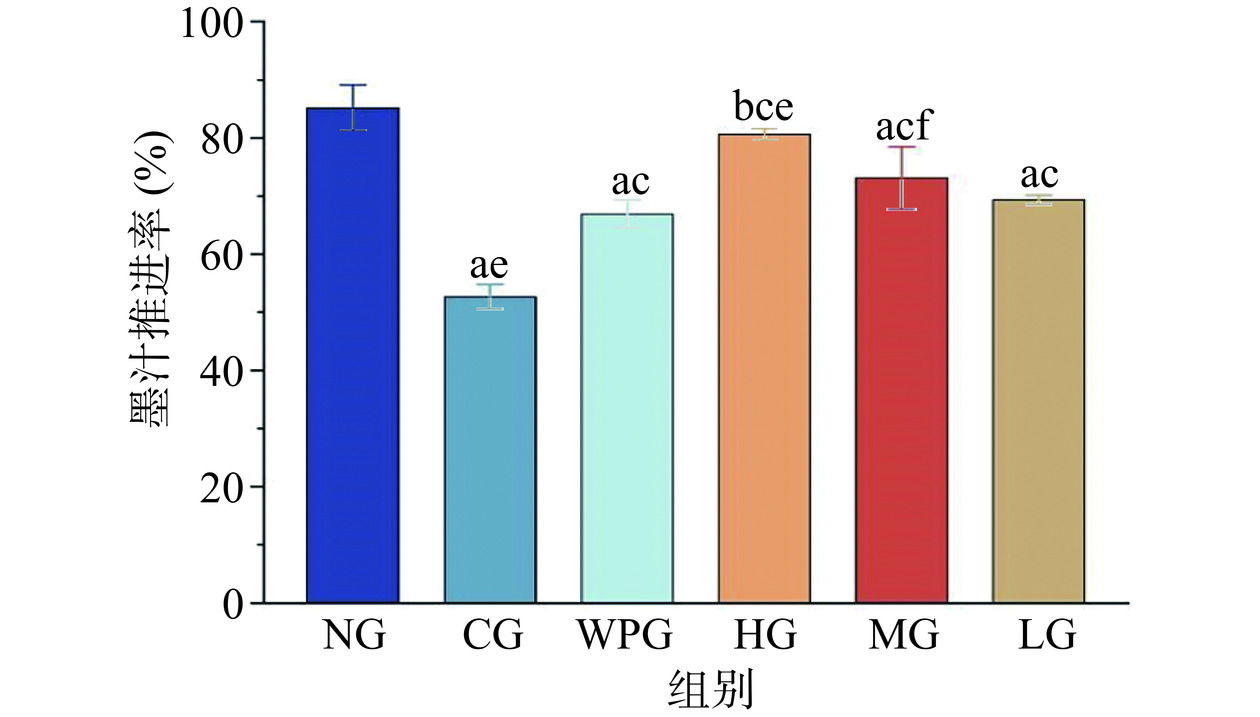
各组小鼠小肠墨汁推进率结果如图3所示。由于CG组墨汁推进率明显低于NG组,因此说明此造模方法可行,造模成功[23]。与CG组比较,WPG组、HG组、MG组、LG组小鼠小肠墨汁推进率显著增加(P<0.01);HG组小鼠小肠墨汁推进率与WPG组相较明显增加(P<0.01),MG组小鼠小肠墨汁推进率也有所增加(P<0.05)。总而言之,中、高剂量的GPs对小鼠的小肠运动具有良性的影响,可有效促进小鼠小肠运动。此结论与张亭等[13]探究核桃低聚肽的润肠通便功能结果相一致,表明低聚肽可以增强小鼠小肠的推动力。
2.3 人参肽对小鼠排便的影响
由表2可知,由于CG组与NG组相较,NG组的小鼠首粒黑便排出的时间明显短于CG组,CG组5 h内的粪便粒数明显有所减少(P<0.01),CG组5 h内排出的粪便重量也显著减轻(P<0.01),这表明此建模方法合理,小鼠便秘模型建立成功。此外,WPG组、HG组、MG组、LG组小鼠首粒黑便排出时间也是显著高于NG组(P<0.01),但其中HG组小鼠首粒黑便排出时间与NG组相差最少而WPG组小鼠首粒黑便排出时间与NG组相差最多[24];其次与NG组相较,WPG组的5 h时粪便粒数和粪便重量均明显降低(P<0.01),说明可排除额外摄入蛋白质影响作用。与CG组比较,HG组小鼠首粒黑便排出时间显著缩短(P<0.01),5 h时粪便粒数(P<0.05)和粪便重量均显著增多(P<0.01);MG组小鼠首粒黑便排出时间明显缩短(P<0.05),5 h内粪便重量显著增多(P<0.01)。综上所述,高剂量的GPs有助于小鼠的排便,具有润肠通便的作用。表3详细记录了小鼠5 h内排出的粪便的性状及对不同性状下可能的原因进行分析。
表 2 GPs对各组小鼠排便的影响Table 2. Effects of GPs on defecation of mice in each group组别 首粒黑便时间(min) 5 h内粪便粒数(粒) 5 h内粪便重量(g) NG 104.30±6.03 9.3±1.53 0.16±0.03 CG 258.20±24.99a 6.5±0.87a 0.08±0.01a WPG 263.70±17.58a 5.9±0.79a 0.09±0.02a HG 183.80±8.81ace 8.6±0.81de 0.19±0.03ce MG 219.00±16.37adf 7.8±0.29f 0.15±0.03ce LG 252.60±26.41a 7.1±1.15 0.12±0.02 注:与NG比较,a:P<0.01,b:P<0.05;与CG比较,c:P<0.01,d:P<0.05;与WPG比较,e:P<0.01,f :P<0.05。 表 3 各组小鼠粪便性状及毛发情况描述及原因分析Table 3. Description and cause analysis of feces and hair of mice in each group组别 粪便性状及毛发情况描述 原因分析 NG 粪便成型、形态完整、湿润度正常、大小均匀、无血丝、毛发柔顺 粪便大小相比于其他组略大,因为其肠道未受损伤,故排便正常,小鼠精神状况良好 CG 粪便不成型、形态不完整、极干、大小不一、呈现拉丝状、排便初期粪便较小、带有血丝、毛发杂乱情况严重 粪便大小相比于其他组略小,因为其肠道受损伤严重,便秘情况严重,故排便困难并伴随损伤,
且小鼠精神状况萎靡WPG 粪便不成型、形态不完整、很干、大小不一、有的呈现拉丝状、排便初期粪便中等大小、带有血丝、毛发杂乱且无光泽 粪便大小相比于模型组稍大,因为其肠道受损而乳清蛋白并不能有效缓解其便秘,便秘情况严重,故排便困难并伴随损伤,小鼠精神状况萎靡 HG 粪便成型、形态完整、较湿润、大小均匀、无血丝,毛发柔顺 粪便大小正常,粪便湿润略粘(可明显看见粪便上的水分),说明其肠道受损伤后,GPs高剂量可以有效缓解便秘情况及有效保护其肠道,故排便正常,但可能剂量略高,使得粪便稍微发粘,
较为湿润,小鼠精神状况前期稍有不活泼,很快排出第一粒黑便后恢复正常MG 粪便成型、形态完整、湿润度正常、大小
均匀与正常组相近、极少数出现血丝、
毛发较柔顺粪便大小正常,粪便湿润度正常,说明其肠道受损伤后,GPs中剂量可以缓解便秘情况,对于极少数出现血丝的情况,可能与剂量略低有关,对肠道还是略有损伤,但不影响整体,小鼠精神状况前期萎靡时间略长于高剂量组,后期正常 LG 粪便部分成型、形态部分完整、略干、大小不一、半数出现血丝、毛发稍有杂乱 粪便大小不正常,粪便略干,说明其肠道受损伤后,GPs低剂量缓解便秘情况不理想但是稍有作用,对于半数出现血丝的情况,可能与剂量低有关,肠道损伤依旧存在,小鼠精神状况前期萎靡时间更长于中剂量组,后期稍有恢复,但依旧不活泼 2.4 人参肽对小鼠小肠绒毛组织结构的影响
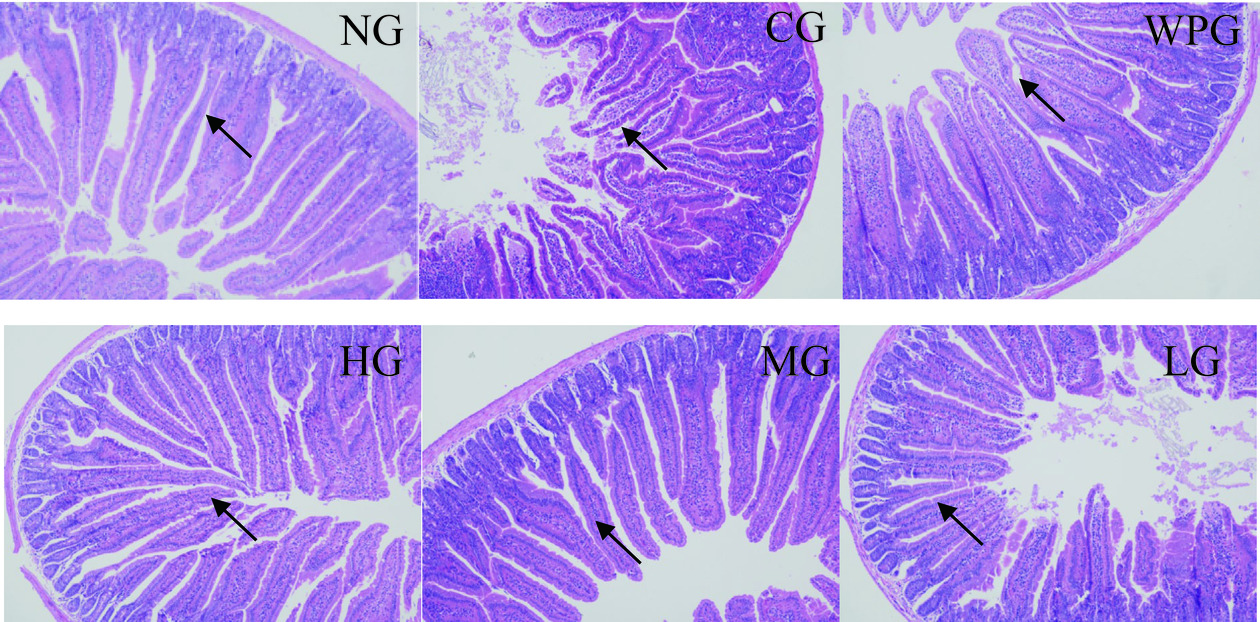
由图4可知,NG组小鼠其小肠绒毛较长且分布紧密;CG组小鼠小肠绒毛有所缩短且分布乱且松散,说明小鼠便秘情况严重并对小肠绒毛造成了一定的损伤;WPG组小鼠小肠绒毛较CG组稍有变长但分布依旧散乱,LG组小鼠的小肠绒毛比WPG组分布更为紧密但长度变化不明显,MG组小鼠小肠绒毛分布致密且长度较CG组明显变长;HG组小鼠小肠绒毛长度基本与NG组无异,分布致密且长度适宜,说明高剂量GPs缓解小肠绒毛的损伤十分有效[24]。综上所述,中、高剂量的GPs可显著缓解LH造成的便秘小鼠小肠绒毛损伤,低剂量的GPs稍有作用但效果不佳。
2.5 人参肽对便秘小鼠血清P物质(SP)、血管活性肠肽(VIP)的影响
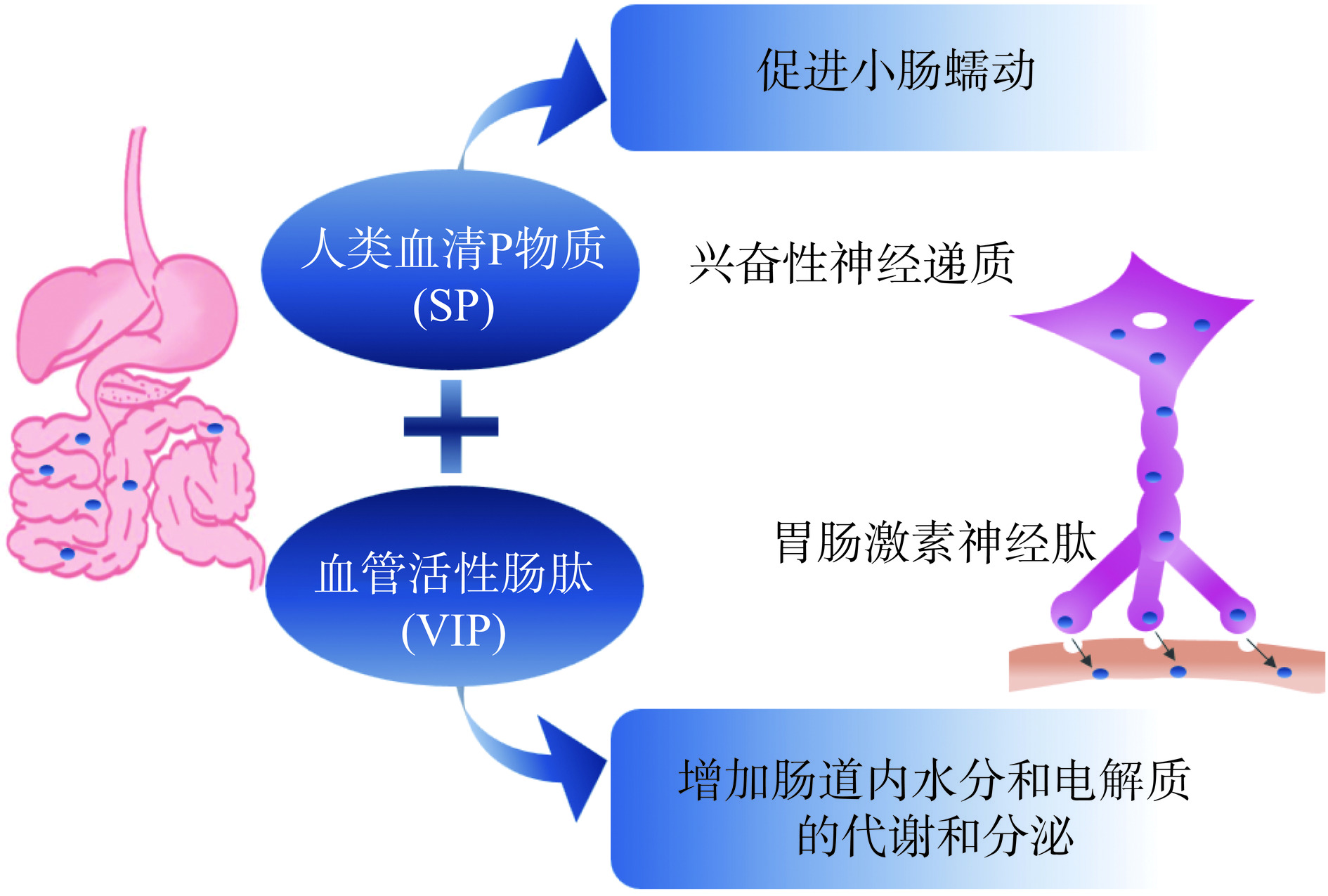
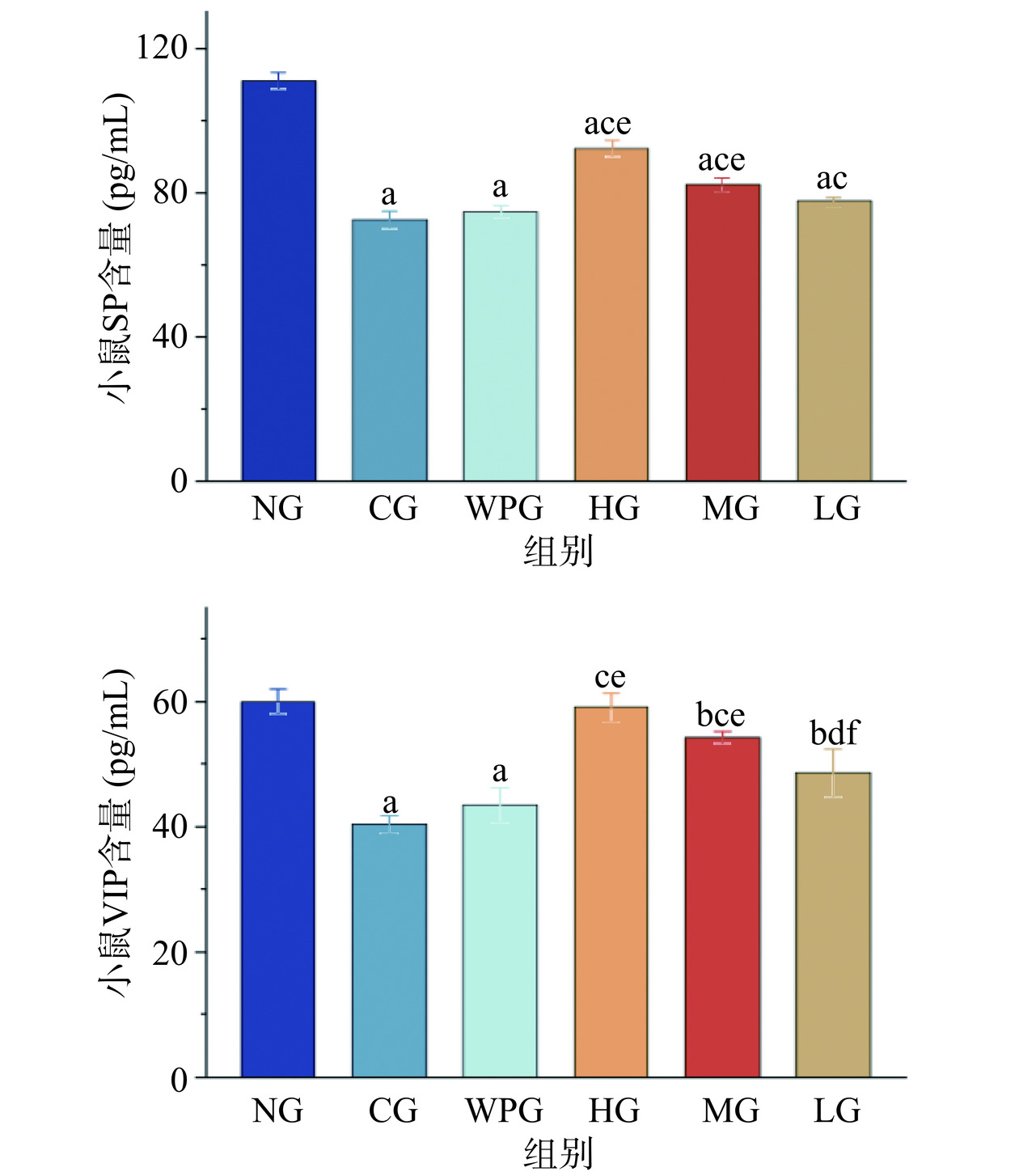
引发便秘疾病的因素复杂多样,有研究表明便秘患者的血清P物质(SP)、血管活性肠肽(VIP)的水平较健康人士有下降的趋势,因此脑肠肽的变化是导致便秘发生的一种机制。SP及VIP是参与机体内胃肠活动的主要脑肠肽,SP属于兴奋性神经递质,对胃肠道平滑肌起到收缩作用,从而促使胃的排空及小肠蠕动[25];VIP可起到调节肠道内水和电解质的代谢的作用,进而增加其分泌,从而预防便秘疾病的发生[26−27],具体机制如图5所示。由图6可知,与NG组相比,各组便秘小鼠的血清SP及VIP含量均明显降低(P<0.01),CG组便秘小鼠两个指标降低率最高,但经过高剂量GPs的治疗便秘小鼠的血清SP及VIP含量明显升高(P<0.01),中剂量的GPs对便秘小鼠的二者含量也有所提升(P<0.01),而低剂量的GPs对便秘小鼠的这两个指标的含量变化影响不明显。综上所述,GPs对便秘小鼠具有润肠通便的作用,其机制与SP和VIP含量的变化有关,二者对小鼠肠道的分泌及小肠蠕动发挥重要作用,此结果与其他学者的相关研究结果相一致[28−30]。
3. 结论
综上所述,GPs对便秘小鼠具有明显的促进小肠蠕动的作用,可对便秘造成的小鼠小肠绒毛损伤起到减缓效果,因此GPs具有润肠通便的作用,其机制可能是处于便秘情况的小鼠随着血清SP和VIP含量升高,调节肠道内水液和电解质的代谢,收缩肠道平滑肌,促进了肠道分泌和小肠蠕动,进而缓解了小鼠的便秘情况,这也为GPs应用于辅助治疗便秘提供了依据。
-
表 1 各组小鼠灌胃剂量
Table 1 Dosage of mice in each group
组别 灌胃剂量(受试物溶于墨汁) NG 墨汁10 mL/kg CG 墨汁10 mL/kg WPG 乳清蛋白650 mg/kg·bw HG GPs 1300 mg/kg·bw MG GPs 650 mg/kg·bw LG GPs 325 mg/kg·bw 表 2 GPs对各组小鼠排便的影响
Table 2 Effects of GPs on defecation of mice in each group
组别 首粒黑便时间(min) 5 h内粪便粒数(粒) 5 h内粪便重量(g) NG 104.30±6.03 9.3±1.53 0.16±0.03 CG 258.20±24.99a 6.5±0.87a 0.08±0.01a WPG 263.70±17.58a 5.9±0.79a 0.09±0.02a HG 183.80±8.81ace 8.6±0.81de 0.19±0.03ce MG 219.00±16.37adf 7.8±0.29f 0.15±0.03ce LG 252.60±26.41a 7.1±1.15 0.12±0.02 注:与NG比较,a:P<0.01,b:P<0.05;与CG比较,c:P<0.01,d:P<0.05;与WPG比较,e:P<0.01,f :P<0.05。 表 3 各组小鼠粪便性状及毛发情况描述及原因分析
Table 3 Description and cause analysis of feces and hair of mice in each group
组别 粪便性状及毛发情况描述 原因分析 NG 粪便成型、形态完整、湿润度正常、大小均匀、无血丝、毛发柔顺 粪便大小相比于其他组略大,因为其肠道未受损伤,故排便正常,小鼠精神状况良好 CG 粪便不成型、形态不完整、极干、大小不一、呈现拉丝状、排便初期粪便较小、带有血丝、毛发杂乱情况严重 粪便大小相比于其他组略小,因为其肠道受损伤严重,便秘情况严重,故排便困难并伴随损伤,
且小鼠精神状况萎靡WPG 粪便不成型、形态不完整、很干、大小不一、有的呈现拉丝状、排便初期粪便中等大小、带有血丝、毛发杂乱且无光泽 粪便大小相比于模型组稍大,因为其肠道受损而乳清蛋白并不能有效缓解其便秘,便秘情况严重,故排便困难并伴随损伤,小鼠精神状况萎靡 HG 粪便成型、形态完整、较湿润、大小均匀、无血丝,毛发柔顺 粪便大小正常,粪便湿润略粘(可明显看见粪便上的水分),说明其肠道受损伤后,GPs高剂量可以有效缓解便秘情况及有效保护其肠道,故排便正常,但可能剂量略高,使得粪便稍微发粘,
较为湿润,小鼠精神状况前期稍有不活泼,很快排出第一粒黑便后恢复正常MG 粪便成型、形态完整、湿润度正常、大小
均匀与正常组相近、极少数出现血丝、
毛发较柔顺粪便大小正常,粪便湿润度正常,说明其肠道受损伤后,GPs中剂量可以缓解便秘情况,对于极少数出现血丝的情况,可能与剂量略低有关,对肠道还是略有损伤,但不影响整体,小鼠精神状况前期萎靡时间略长于高剂量组,后期正常 LG 粪便部分成型、形态部分完整、略干、大小不一、半数出现血丝、毛发稍有杂乱 粪便大小不正常,粪便略干,说明其肠道受损伤后,GPs低剂量缓解便秘情况不理想但是稍有作用,对于半数出现血丝的情况,可能与剂量低有关,肠道损伤依旧存在,小鼠精神状况前期萎靡时间更长于中剂量组,后期稍有恢复,但依旧不活泼 -
[1] 向雪莲, 侯晓华. 《2013年中国慢性便秘诊治指南》重点解读[J]. 中国实用外科杂志,2013(11):940−942. [XIANG Xuelian, HOU Xiaohua. Key interpretation of 2013 Chinese guidelines for the diagnosis and treatment of chronic constipation[J]. Chinese Journal of Practical Surgery,2013(11):940−942.] XIANG Xuelian, HOU Xiaohua. Key interpretation of 2013 Chinese guidelines for the diagnosis and treatment of chronic constipation[J]. Chinese Journal of Practical Surgery, 2013(11): 940−942.
[2] PAVLICEVIC M, MARMIROLI N, MAESTRI E. Immunomodulatory peptides—A promising source for novel functional food production and drug discovery[J]. Peptides,2022,148:170696. doi: 10.1016/j.peptides.2021.170696
[3] 孔箫亭, 毛肇洁, 胡宁, 等. 人参肽的分离纯化及活性分析[J]. 中国食品添加剂, 2022, 33(8):50−57. [KONG Xiaoting, MAO Zhaojie, HU Ning, et al. Isolation, purification and activity analysis of ginseng peptide[J]. Chinese Food Additives, 2022, 33(8):50−57.] KONG Xiaoting, MAO Zhaojie, HU Ning, et al. Isolation, purification and activity analysis of ginseng peptide[J]. Chinese Food Additives, 2022, 33(8): 50−57.
[4] 任金威, 李迪, 孙靖琴, 等. 吉林人参低聚肽对小鼠耐缺氧作用的研究[J]. 中国食物与营养,2018,24(12):54−57. [REN Jinwei, LI Di, SUN Jingqin, et al. Study on hypoxia tolerance of Jilin ginseng oligopeptide in mice[J]. Chinese Food and Nutrition,2018,24(12):54−57.] doi: 10.3969/j.issn.1006-9577.2018.12.013 REN Jinwei, LI Di, SUN Jingqin, et al. Study on hypoxia tolerance of Jilin ginseng oligopeptide in mice[J]. Chinese Food and Nutrition, 2018, 24(12): 54−57. doi: 10.3969/j.issn.1006-9577.2018.12.013
[5] 何丽霞, 刘睿, 任金威, 等. 吉林人参低聚肽的免疫调节作用[J]. 科技导报,2015,33(18):62−67. [HE Lixia, LIU Rui, REN Jinwei, et al. Immunomodulatory effect of oligopeptide of ginseng in Jilin[J]. Science and Technology Review,2015,33(18):62−67.] HE Lixia, LIU Rui, REN Jinwei, et al. Immunomodulatory effect of oligopeptide of ginseng in Jilin[J]. Science and Technology Review, 2015, 33(18): 62−67.
[6] 任金威, 李迪, 陈启贺, 等. 吉林人参低聚肽的抗氧化作用[J]. 食品科学,2017,38(21):195−200. [REN Jinwei, LI Di, CHEN Qihe, et al. Antioxidant effect of oligopeptide of ginseng in Jilin[J]. Food Science,2017,38(21):195−200.] doi: 10.7506/spkx1002-6630-201721031 REN Jinwei, LI Di, CHEN Qihe, et al. Antioxidant effect of oligopeptide of ginseng in Jilin[J]. Food Science, 2017, 38(21): 195−200. doi: 10.7506/spkx1002-6630-201721031
[7] 孙彬, 李迪, 毛瑞雪, 等. 吉林人参低聚肽对糖尿病大鼠的降血糖作用研究[J]. 中国食物与营养,2016,22(10):62−65. [SUN Bin, LI Di, MAO Ruixue, et al. Study on hypoglycemic effect of Jilin ginseng oligopeptide on diabetic rats[J]. Chinese Food and Nutrition,2016,22(10):62−65.] doi: 10.3969/j.issn.1006-9577.2016.10.014 SUN Bin, LI Di, MAO Ruixue, et al. Study on hypoglycemic effect of Jilin ginseng oligopeptide on diabetic rats[J]. Chinese Food and Nutrition, 2016, 22(10): 62−65. doi: 10.3969/j.issn.1006-9577.2016.10.014
[8] 刘睿, 任金威, 陈启贺, 等. 人参低聚肽对急性酒精性肝损伤大鼠的保护作用[J]. 现代预防医学,2016,43(15):2820−2824. [LIU Rui, REN Jinwei, CHEN Qihe, et al. Protective effect of ginseng oligopeptide on acute alcoholic liver injury in rats[J]. Modern Preventive Medicine,2016,43(15):2820−2824.] LIU Rui, REN Jinwei, CHEN Qihe, et al. Protective effect of ginseng oligopeptide on acute alcoholic liver injury in rats[J]. Modern Preventive Medicine, 2016, 43(15): 2820−2824.
[9] 李迪, 刘睿, 李慧, 等. 吉林人参低聚肽对高脂血症大鼠的影响[J]. 食品科学,2017,38(5):227−232. [LI Di, LIU Rui, LI Hui, et al. Effect of Jilin ginseng oligopeptide on hyperlipidemia rats[J]. Food Science,2017,38(5):227−232.] doi: 10.7506/spkx1002-6630-201705037 LI Di, LIU Rui, LI Hui, et al. Effect of Jilin ginseng oligopeptide on hyperlipidemia rats[J]. Food Science, 2017, 38(5): 227−232. doi: 10.7506/spkx1002-6630-201705037
[10] 鲍雷, 王军波, 蔡夏夏, 等. 吉林人参低聚肽抗疲劳作用[J]. 科技导报,2015,33(13):56−60. [BAO Lei, WANG Junbo, CAI Xiaxia, et al. Anti-fatigue effect of oligopeptide of Jilin ginseng[J]. Science and Technology Review,2015,33(13):56−60.] BAO Lei, WANG Junbo, CAI Xiaxia, et al. Anti-fatigue effect of oligopeptide of Jilin ginseng[J]. Science and Technology Review, 2015, 33(13): 56−60.
[11] HAN Caijing, KONG Xiaoting, XIA Xiaohong, et al. Effects of ginseng peptides on the hypoglycemic activity and gut microbiota of a type 2 diabetes mellitus mice model[J]. Journal of Functional Foods, 2023, 111.
[12] 齐慧, 徐君. 低聚肽功能的研究进展[J]. 甘肃农业科技,2012(11):33−36. [QI Hui, XU Jun. Research progress of oligopeptide function[J]. Agricultural Science and Technology in Gansu,2012(11):33−36.] QI Hui, XU Jun. Research progress of oligopeptide function[J]. Agricultural Science and Technology in Gansu, 2012(11): 33−36.
[13] 张亭, 珠娜, 刘睿, 等. 核桃低聚肽润肠通便功能作用[J]. 中国公共卫生,2019,35(9):1225−1228. [ZHANG Ting, ZHU Na, LIU Rui, et al. Function of walnut oligopeptide on bowel laxation[J]. Public Health in China,2019,35(9):1225−1228.] doi: 10.11847/zgggws1119521 ZHANG Ting, ZHU Na, LIU Rui, et al. Function of walnut oligopeptide on bowel laxation[J]. Public Health in China, 2019, 35(9): 1225−1228. doi: 10.11847/zgggws1119521
[14] 黄泽琳, 赵艳, 段纯芬, 等. 白豆蔻水提物对功能性便秘小鼠的通便作用[J/OL]. 现代食品科技: 1−11[2024-10-31]. [HUANG Zelin, ZHAO Yan, DUAN Chunfen, et al. Defecation effect of water extract of white cardamom on mice with functional constipation[J/OL]. Modern food science and technology: 1−11[2024-10-31].] HUANG Zelin, ZHAO Yan, DUAN Chunfen, et al. Defecation effect of water extract of white cardamom on mice with functional constipation[J/OL]. Modern food science and technology: 1−11[2024-10-31].
[15] WANG Liuping, XIE Shiyuan, JIANG Xuan, et al. Therapeutic effects of bombax ceiba flower aqueous extracts against loperamide-induced constipation in mice[J]. Pharmaceutical Biology,2023,61(1):125−134. doi: 10.1080/13880209.2022.2157841
[16] 王旭, 周旭晴, 吴笛, 等. 决明二仁方对不同便秘模型小鼠排便及血清VIP、SP的影响[J]. 湖南中医药大学学报,2022,42(5):732−737. [WANG Xu, ZHOU Xuqing, WU Di, et al. Effects of Jueming erren formula on defecation and serum VIP and SP in mice with different constipation models[J]. Journal of Hunan University of Chinese Medicine,2022,42(5):732−737.] doi: 10.3969/j.issn.1674-070X.2022.05.007 WANG Xu, ZHOU Xuqing, WU Di, et al. Effects of Jueming erren formula on defecation and serum VIP and SP in mice with different constipation models[J]. Journal of Hunan University of Chinese Medicine, 2022, 42(5): 732−737. doi: 10.3969/j.issn.1674-070X.2022.05.007
[17] ZHENG Shuze, GUO Qiang, ZHANG Guimin, et al. Therapeutic effect and mechanism of shouhui tongbian capsules on slow transit constipation model mice[J]. China Journal of Chinese Materia Medica,2021,46(3):520−525.
[18] NAZIR S, KHAN H, KHAN S A, et al. In vivo acute toxicity, laxative and antiulcer effect of the extract of dryopteris ramose[J]. Cellular and Molecular Biology,2021,67(1):9−16. doi: 10.14715/cmb/2021.67.1.2
[19] 姚一博, 王迪, 王钱陶, 等. 盐酸洛哌丁胺诱导的小鼠慢传输型便秘模型的实验研究[J]. 中国实验动物学报,2020,28(3):370−375. [YAO Yibo, WANG Di, WANG Qiantao, et al. Experimental study on slow transit constipation induced by loperamide hydrochloride in mice[J]. Chinese Journal of Experimental Physiology,2020,28(3):370−375.] doi: 10.3969/j.issn.1005-4847.2020.03.012 YAO Yibo, WANG Di, WANG Qiantao, et al. Experimental study on slow transit constipation induced by loperamide hydrochloride in mice[J]. Chinese Journal of Experimental Physiology, 2020, 28(3): 370−375. doi: 10.3969/j.issn.1005-4847.2020.03.012
[20] KAKINO M, IZUTA H, ITO T, et al. Agarwood induced laxative effects via acetylcholine receptors on loperamide-induced constipation in mice[J]. Bioscience, Biotechnology, and Biochemistry,2010,74(8):1550−1555. doi: 10.1271/bbb.100122
[21] CIL O, PHUAN P W, LEE S J, et al. CFTR activator increases intestinal fluid secretion and normalizes stool output in a mouse model of constipation[J]. Cellular and Molecular Gastroenterology and Hepatology,2016,2(3):317−327. doi: 10.1016/j.jcmgh.2015.12.010
[22] 李绿梅, 张娜, 代瑶瑶, 等. 盐酸洛哌丁胺制备小鼠便秘模型的研究[J]. 宁夏医学杂志,2022,44(8):673−675,769. [LI Lümei, ZHANG Na, DAI Yaoyao, et al. Study on preparation of constipation model of mice by loperamide hydrochloride[J]. Ningxia Medical Journal,2022,44(8):673−675,769.] LI Lümei, ZHANG Na, DAI Yaoyao, et al. Study on preparation of constipation model of mice by loperamide hydrochloride[J]. Ningxia Medical Journal, 2022, 44(8): 673−675,769.
[23] KIM J E, PARK J W, KANG M J, et al. Laxative effect of spicatoside A by cholinergic regulation of enteric nerve in loperamide-induced constipation:ICR mice model[J]. Molecules,2019,24(5):896. doi: 10.3390/molecules24050896
[24] UTHIA R, YOLANDA D P, ERIADI A, et al. Laxative activity test of Gynura procumbens (Lour.) merr. leave on white male mice induced by loperamide[J]. Metamorfosa Journal of Biological Sciences,2019,6(2):137−142. doi: 10.24843/metamorfosa.2019.v06.i02.p01
[25] LUDVIGSSON J F, MONTGOMERY S M, EKBOM A, et al. Small-intestinal histopathology and mortality risk in celiac disease[J]. Jama,2009,302(11):1171−1178. doi: 10.1001/jama.2009.1320
[26] 范明明, 韩海瑞, 林伟, 等. 柴术理胃饮对肝郁脾虚型功能性消化不良大鼠胃肠运动及血清SP、VIP含量的影响[J]. 中国医药导刊,2021,23(9):686−691. [FAN Mingming, HAN Hairui, LIN Wei, et al. Effect of Chaishu Liwei Yin on gastrointestinal motility and serum SP and VIP content in rats with functional dyspepsia of liver-Qi and spleen-deficiency type[J]. Chinese Medical Guide Journal,2021,23(9):686−691.] doi: 10.3969/j.issn.1009-0959.2021.09.010 FAN Mingming, HAN Hairui, LIN Wei, et al. Effect of Chaishu Liwei Yin on gastrointestinal motility and serum SP and VIP content in rats with functional dyspepsia of liver-Qi and spleen-deficiency type[J]. Chinese Medical Guide Journal, 2021, 23(9): 686−691. doi: 10.3969/j.issn.1009-0959.2021.09.010
[27] ZHANG Xiaoyu, YANG Huabing, ZHENG Junping, et al. Chitosan oligosaccharides attenuate loperamide-induced constipation through regulation of gut microbiota in mice[J]. Carbohydrate Polymers,2021,253(4):117218.
[28] 朱建东, 冯文哲, 徐漠雨, 等. 加味增液汤对慢传输型便秘大鼠血清SP、MTL、GAS的影响研究[J]. 世界最新医学信息文摘,2019,19(26):19−20. [ZHU Jiandong, FENG Wenzhe, XU Moxue, et al. Effect of Jiaweizeng decoction on serum SP, MTL and GAS in rats with slow transit constipation[J]. The World's Latest Medical Information Digest,2019,19(26):19−20.] ZHU Jiandong, FENG Wenzhe, XU Moxue, et al. Effect of Jiaweizeng decoction on serum SP, MTL and GAS in rats with slow transit constipation[J]. The World's Latest Medical Information Digest, 2019, 19(26): 19−20.
[29] 陈泽芃, 王辰龙, 顾庆龙, 等. 增液八珍汤对慢传输型便秘大鼠模型结肠肌5-HT、AchE、SP及VIP的影响[J]. 中医药信息,2023,40(5):21−26. [CHEN Zepeng, WANG Chenlong, GU Qinglong, et al. Effect of Zengye Bazhen decoction on colonic muscle 5-HT, AchE, SP and VIP in rat model of slow transit constipation[J]. Traditional Chinese medicine information,2023,40(5):21−26.] CHEN Zepeng, WANG Chenlong, GU Qinglong, et al. Effect of Zengye Bazhen decoction on colonic muscle 5-HT, AchE, SP and VIP in rat model of slow transit constipation[J]. Traditional Chinese medicine information, 2023, 40(5): 21−26.
[30] CUI Mengxiao, SUN Yupei, LI Xiaofeng, et al. Effect of electroacupuncture of "Tianshu"(ST25) at different frequencies on electromyography and immunoactivity of SP and VIP of colon in rats with slow transit constipation[J]. Zhen ci yan jiu = Acupuncture Research,2022,47(8):710−714.
-
期刊类型引用(3)
1. 李亚俐,王雪莉,石柳,吴文锦,陈胜,陈朗,郭晓嘉,熊光权,汪兰,孙智达. 壳聚糖-绿原酸复合保鲜剂对冷藏鮰鱼片食用品质的影响. 肉类研究. 2025(01): 42-50 .  百度学术
百度学术
2. 武玫怡,焦文娟,赵甜甜,刘俊,周芳,刘伟峰,张业辉,南海军,陈晓瑛,黄利华. 高静水压与水煮处理对热带海参品质的影响. 肉类研究. 2025(01): 25-33 .  百度学术
百度学术
3. 崔燕,刘韩欣,朱麟,尚海涛,林旭东,陈曙颖,宣晓婷. 超高压杀菌对大黄鱼理化性质及滋味、风味的影响. 食品工业科技. 2025(05): 44-55 .  本站查看
本站查看
其他类型引用(3)





 下载:
下载:
 下载:
下载:



