Phenolic Compounds and Antidiabetic Activity of Raspberry Ethanol Extract from Different Producing Areas
-
摘要: 本文以六个产地(广东、广西、安徽、浙江、江西和四川)的覆盆子为原料,采用乙醇提取法提取覆盆子酚类物质,对比分析酚类物质及其抗糖尿病活性。结果表明,在不同产地中,广东覆盆子总酚含量最高(349.77 μg GAE/mg E),浙江覆盆子总黄酮含量最高(202.55 μg QUE/mg E),四川覆盆子提取物中的水解单宁含量最高(125.07 mg GAE/g E)。从六个产地的覆盆子提取物中鉴定出了34种酚类化合物,主要是鞣花单宁、黄酮和酚酸类物质。活性研究显示,四川覆盆子提取物具有最强的DPPH·清除能力(IC50=63.069 μg/mL)、ABTS+·清除能力(IC50=29.977 μg/mL)和α-葡萄糖苷酶抑制能力(IC50=0.086 mg/mL),安徽覆盆子提取物抑制AGEs形成的能力相对较强(81.91%)。综上,四川产地覆盆子是抗糖尿病药物的优质来源。Abstract: In this paper, phenolic compounds of raspberry from six producing areas (Guangdong, Guangxi, Anhui, Zhejiang, Jiangxi and Sichuan) were extracted by ethanol extraction method, and the phenolic compounds and their antidiabetic activities were compared and analyzed. The results showed that the content of polyphenol of raspberry from Guangdong was the highest (349.77 μg GAE/mg E), Zhejiang raspberry showed the highest total flavonoid content (202.55 μg QUE/mg E), while Sichuan raspberry showed the highest content of hydrolyzed tannin (125.07 mg GAE/g E). Thirty-four different phenolic compounds were identified from raspberry extracts, which were mainly ellagitannins, flavonoids and phenolic acids. Studies on antidiabetic activity showed that the DPPH· (IC50=63.069 μg/mL) and ABTS+· scavenging capacities (IC50=29.977 μg/mL) and the inhibitory effect on α-glycosidase (IC50=0.086 mg/mL) of raspberry extracts from Sichuan were higher than those from other regions, whereas Anhui raspberry extract showed the strongest inhibitory ability of AGEs (81.91%). In summary, raspberry from Sichuan is a high-quality source of anti-diabetes drugs.
-
Keywords:
- raspberry /
- different producing areas /
- phenolic compounds /
- antidiabetic activity
-
药用覆盆子(Rubus chingii Hu)是蔷薇科悬钩子属华东覆盆子的未成熟干燥果实,因叶裂如掌又称掌叶覆盆子。全世界大约有750余种药用覆盆子,大多数种植于北半球温带,少数种植于热带,药用覆盆子在我国主要分布于江苏、浙江、安徽、福建、江西、广西等地[1−2]。近十年来,许多国内外研究发现,药用覆盆子中含有酚酸、黄酮、单宁、多糖、生物碱、萜类及甾体等多种活性成分,其中水解单宁、酚酸、黄酮等酚类物质为其主要活性成分[3−4]。药理研究表明,覆盆子具有抗氧化、降血糖、降血脂、抗癌、抗衰老、改善学习能力、调节性激素水平等作用[5−6]。
然而,受品种、地理位置和生长条件的影响,植物营养成分组成和活性可能存在较大差异。平嘉倩等[7]研究发现不同品种和产地的覆盆子总糖、糖酸比、VC和氨基酸含量差异显著,江西覆盆子的果糖含量、糖酸比最高,福建的最低,但福建覆盆子却含有较高的氨基酸和矿质元素。付彩群等[8]研究发现产地、采收期是造成药用覆盆子酚类化合物含量差异的主要原因,浙江产地覆盆子中鞣花酸含量明显高于江西,而向阳与背阳对覆盆子活性成分含量的影响较小。Park等[9]的研究发现Gokseong的覆盆子具有最高的多酚含量,Jeongeup的覆盆子具有最高的黄酮含量,Gochang、Sunchang、Jeongeup和Jinan等地覆盆子中花色苷的含量要略多于Gokseong和Hoengseong。然而,很少有研究集中在来自不同产地的覆盆子酚类物质组成及活性的差异。
综上,产地不同会导致覆盆子中活性成分含量差异显著,但国内外对覆盆子的研究主要集中在活性成分分离鉴定及种质资源的评价和利用方面,而关于产地对覆盆子酚类物质及活性影响的研究较少。本文采用40%乙醇提取广东、广西、安徽、浙江、江西和四川六个不同产地覆盆子酚类物质,评价不同产地覆盆子提取物中总酚、总黄酮和总水解单宁的含量以及酚类物质的组成,并对比不同产地覆盆子体外抗糖尿病活性,以期获得较优品质的覆盆子,为后续覆盆子的深度加工提供借鉴,促进覆盆子资源的高值化利用。
1. 材料与方法
1.1 材料与仪器
覆盆子 2022年5月于广东、广西、安徽、浙江、江西和四川六个产地采集,江西师范大学生命科学学院袁涛教授鉴定为蔷薇科悬钩子属,晒干后−4 ℃保存备用;无水乙醇 天津永大化学试剂有限公司;牛血清白蛋白、葡萄糖、没食子酸、槲皮素、维生素C(VC)标准品、三氯化铝、碳酸钠、碘酸钾、福林酚 北京索莱宝科技有限公司;α-葡萄糖苷酶(100 U)、对硝基苯基-D-吡喃葡萄糖苷(PNPG)、阿卡波糖、2,2'-联氨-双(3-乙基苯并噻唑啉-6-磺酸)二胺盐(ABTS)、1,1-二苯基-2-三硝基苯肼(DPPH) 美国Sigma公司;甲酸、乙腈 色谱纯,阿拉丁;所有实验用水均为双蒸水。
KH-500DE型数控超声波清洗器 昆山禾创超声仪器有限公司;RV10型旋转蒸发仪 德国IKA有限公司;Synergy H1型酶标仪 美国Biotek仪器有限公司;F-7000型荧光分光光度计 日本日立有限公司;ESJ200-4型电子天平 沈阳龙腾电子有限公司;5430R型离心机 艾本德中国有限公司;Triple TOF 5600+液相色谱-质谱联用仪 AB SCIEX仪器有限公司。
1.2 实验方法
1.2.1 覆盆子提取物的制备
参照前期优化的方法提取覆盆子中的酚类物质[5],将六个产地的药用覆盆子粉碎成粉末后,按1:10的料液比(g/mL)加入40%乙醇,混匀后于KH-500DE数控超声波清洗器中400 W,50 ℃超声提取1 h,抽滤,收集上清液,残渣再在相同条件下提取一次,合并所有上清液,旋转蒸发浓缩后冷冻干燥至粉末状,制得覆盆子提取物样品,于4 ℃冷藏备用。
1.2.2 总酚含量的测定
参照文献步骤,采用福林酚法检测样品的总酚含量[10]。取200 μL 0.25 mg/mL样品与0.1 mL 福林酚试剂于试管中室温反应5 min,加入0.3 mL 20%的碳酸钠溶液和1.0 mL双蒸水,避光反应25 min后,采用酶标仪测定反应体系在765 nm处的吸光值。空白组以双蒸水代替碳酸钠溶液,以没食子酸为标准品绘制标准曲线,结果以没食子酸当量(μg GAE/mg E)表示。
1.2.3 总黄酮含量的测定
采用三氯化铝比色法测定样品中总黄酮的含量[11]。取100 μL 1.0 mg/mL的样品与100 μL 10%三氯化铝于酶标板中混匀,室温反应15 min后,采用Synergy H1酶标仪测反应体系在430 nm处的吸光值。乙醇代替三氯化铝溶液的反应体系为空白组,以槲皮素为标准品绘制标准曲线,结果以槲皮素当量(μg QUE/mg E)表示。
1.2.4 总水解单宁含量的测定
采用碘酸钾法测定样品中水解单宁的含量[10]。取100 μL 1.0 mg/mL样品与150 μL 5%碘酸钾溶液于酶标板中混匀,室温反应15 min后,测其在550 nm的吸光值。以乙醇代替碘酸钾溶液的反应体系为空白组,以没食子酸为标准品作标准曲线,结果以没食子酸当量表示(mg GAE/g E)。
1.2.5 不同产地覆盆子提取物HPLC-MS/MS分析
将不同产地覆盆子提取物粉末溶解在甲醇中,配制成2 mg/mL的溶液,经0.22 μm滤膜过滤后采用AB Exion LC高效液相色谱-TripleTOF 5600+高分辨质谱联用仪(AB Sciex)测定提取物中酚类物质。利用PeakView对样品进行MS/MS数据分析,通过将获得的数据与参考文献和Scifinder、Metlin数据库中记录的数据进行匹配,对化合物的结构进行初步鉴定,并通过峰面积对化合物进行定量分析。
高效液相色谱参数:色谱柱为SHIM-PACK GIST C18 (75 mm×2.1 mm);流动相A为0.1%甲酸水溶液,流动相B为乙腈溶液;梯度洗脱程序条件为0~6 min 4% B,6~32 min 4%~16.5% B,32~45 min 16.5% B;检测波长为254 nm;柱温为35 ℃;流速为0.3 mL/min;进样量为5 μL。
质谱参数:电喷雾离子源为负离子模式,550 ℃ ESI离子源;质量扫描范围为50~2000 Da,离子源雾化气为50 psi,离子源加热辅助气为35 psi;一级质谱去簇电压为−80 V,碰撞能为−10 eV;二级质谱去簇电压为−80 V,CE为−40±20 eV。
1.2.6 自由基清除能力测定
采用DPPH和ABTS法比较样品的自由基清除能力[11]。取50 μL适宜浓度的样品与150 μL新鲜配制的DPPH·溶液(0.15 mmol/L)或ABTS+·溶液于酶标板中混匀并进行稀释,室温避光孵育30 min(DPPH·溶液)或6 min(ABTS+·溶液)后,分别于517 nm和734 nm处测定吸光值。乙醇代替自由基溶液的反应体系为样品空白组,以VC作阳性对照。采用Origin 2018计算样品清除DPPH和ABTS+自由基半抑制浓度,结果用IC50值(μg/mL)表示。
1.2.7 α-葡萄糖苷酶抑制能力测定
参考Tan等[5]方法测定样品的α-葡萄糖苷酶抑制能力。取50 µL适宜浓度样品与100 µL 0.1 U/mL α-葡萄糖苷酶于酶标板中倍稀,室温反应6 min后加入50 µL 5.0 mmol/L pNPG反应10 min,最后加入100 µL 0.2 mol/L 碳酸钠终止反应,并于405 nm处测定吸光值(Ai),以不加酶和样品的反应体系为空白组(Aj),不加样品的反应体系为控制组(Ac),阿卡波糖为阳性对照。按照公式(1)计算样品中α-葡萄糖苷酶抑制能力,结果用IC50值(mg/mL)表示。
(1) 1.2.8 晚期糖基化终末产物(AGEs)抑制能力测定
采用牛血清白蛋白(BSA)-葡萄糖反应体系评价样品抑制AGEs形成能力[12]。将200 μL提取物(1 mg/mL)与1.0 mL BSA(20 mg/mL)、1.0 mL葡萄糖溶液(500 mmol/L)于10 mL棕色带盖玻璃瓶中混匀,恒温培养箱中37 ℃孵育4周后取出,冰水浴终止反应。最后用0.1 mol/L pH7.4的磷酸盐缓冲溶液稀释10倍后,采用F-7000荧光分光光度计测定稀释液在激发波长340 nm,发射波长420 nm处的荧光值。以氨基胍为阳性对照,按照公式(2)计算样品对AGEs的抑制率。
(2) 式中:FIs表示含有样品、蛋白和糖的反应体系的荧光强度;FIc表示不含样品的反应体系的荧光强度;FIb表示不含样品和蛋白的反应体系的荧光强度;FInb表示不含蛋白的反应体系的荧光强度。
1.3 数据处理
所有实验重复三次,结果用平均值±标准偏差表示,采用SPSS 13.0中的单因素方差分析和t-检验进行统计分析,P<0.05认为具有显著性差异,所有图形用Origin 8.0绘制。
2. 结果与分析
2.1 总酚、总黄酮和总水解单宁含量分析
六个产地药用覆盆子提取物的总酚、水解单宁、总黄酮含量如表1所示。广东和安徽产的覆盆子提取物中的总酚含量最高,为349.77和345.16 μg GAE/mg E,广西和四川覆盆子提取物的总酚含量最低,为294.47和285.16 μg GAE/mg E,且两者之间不存在显著性差异(P>0.05)。浙江覆盆子提取物中的总黄酮含量最高,达202.55 μg QUE/mg E,其次为广西、江西和广东覆盆子提取物,含量为156.92~153.51 μg QUE/mg E,且三者之间不存在显著性差异(P>0.05),四川覆盆子提取物的总黄酮含量最低,仅112.77 μg QUE/mg E。四川覆盆子提取物中的可水解单宁含量最高,为125.07 mg GAE/g E,其次为广西和浙江覆盆子提取物,广东和安徽覆盆子提取物中的水解单宁含量最低,为62.07 mg GAE/g E和64.87 mg GAE/g E,且两者之间不存在显著性差异(P>0.05)。
表 1 六个产地覆盆子提取物的总酚、水解单宁、总黄酮含量Table 1. Total phenols, hydrolyzed tannins and total flavonoids content of raspberry extracts from six producing areas成分 广东 广西 安徽 浙江 江西 四川 总酚
(μg GAE/mg E)349.77±18.76a 294.47±9.82b 345.16±14.33a 343.47±7.14a 300.07±13.82b 285.16±19.93b 总黄酮
(μg QUE/mg E)153.51±18.50b 156.92±6.67b 137.07±12.35b 202.55±15.12a 154.70±4.01b 112.77±16.20c 总水解单宁
(mg GAE/g E)62.07±4.20d 98.33±5.40b 64.87±2.84d 91.13±5.37bc 79.60±15.32c 125.07±3.89a 注:同一行中的不同小写字母表示样品间的差异显著(P<0.05)。 2.2 主要化学成分分析
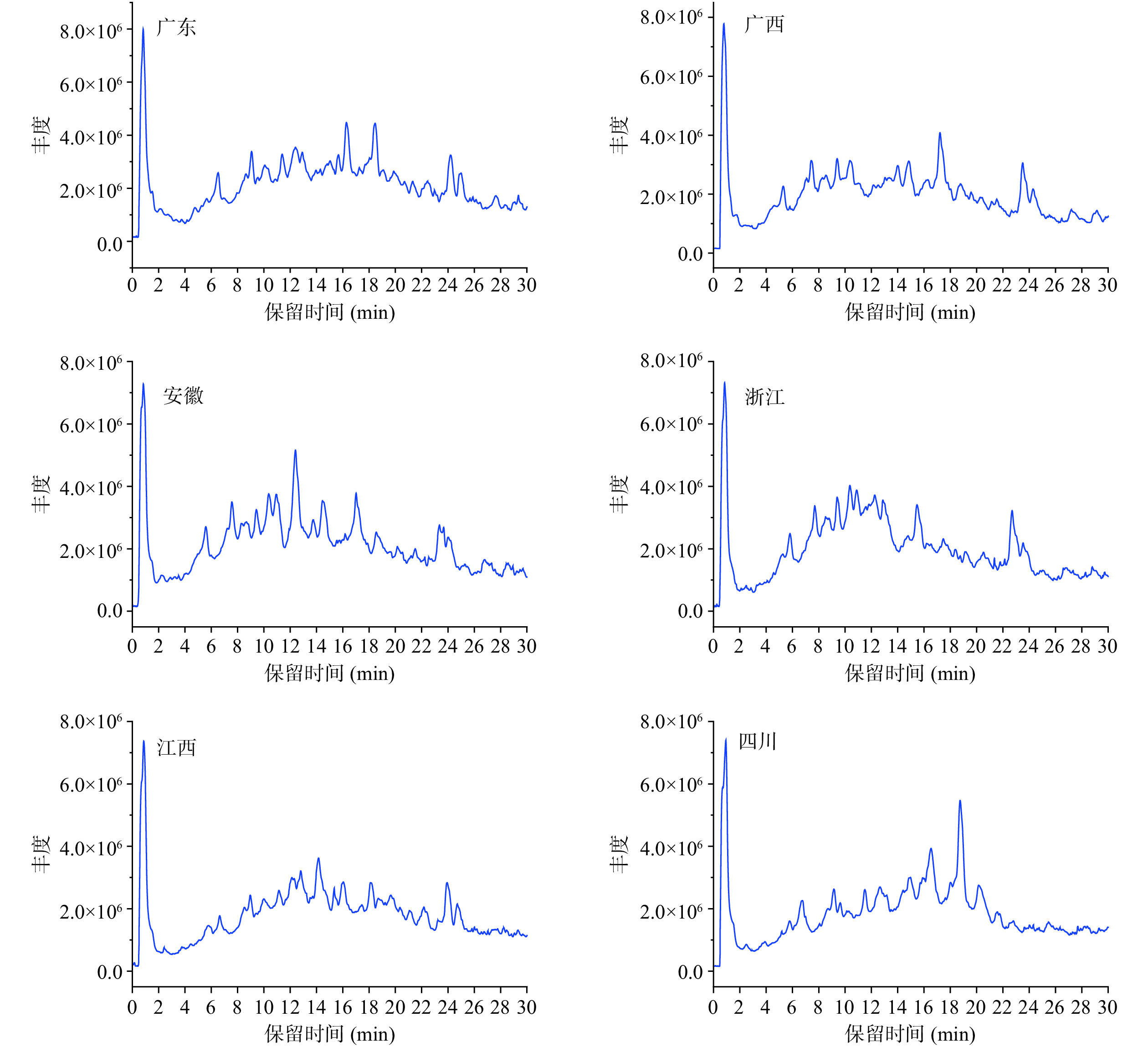
为了比较六个产地覆盆子之间的差异,本文检测了六个产地覆盆子提取物中酚类物质,色谱图如图1所示。从覆盆子提取物鉴定出34个酚类化合物,主要是鞣花单宁、黄酮和酚酸类物质(表2)。
表 2 六个产地覆盆子提取物的定性定量分析Table 2. Qualitative and quantitative analysis of raspberry extracts from six producing areas化合物 保留时间
(min)母离子 分子式 碎片离子
(m/z)含量(峰面积×105) 分类 广东 广西 安徽 浙江 江西 四川 六羟基二苯基葡萄糖 1.79 481 C27H14O9 301, 275, 231 × 8.9 × × × × 鞣花单宁 白屈菜酸 2.43 183 C7H4O6 139, 83, 67 11.8 × 11.8 14.1 8.8 18.3 酚酸 没食子酸 3.89 169 C7H6O5 125, 79 × × 17.8 × 10.5 24.1 酚酸 月见草素C 5.8 783 C34H24O22 481, 301, 275 22.8 42.9 53.2 80.4 0.3 × 鞣花单宁 Valoneic acid dilactone 7.06 469 C21H10O13 451, 379, 301 38.1 36.5 30.0 × × × 鞣花单宁 月见草素C异构体 7.41 783 C34H24O22 481, 301, 275 79.3 81.5 76.4 79.7 × × 鞣花单宁 原花青素B4 8.28 577 C30H26O12 425, 289, 161 × 29.4 34.7 45.2 × × 黄酮 表儿茶素 8.51 289 C15H14O6 245, 187 × 40.7 38.7 × × × 黄酮 Galloyl-HHDP-glucose 8.54 633 C27H22O18 463, 301, 275, 161 × × × × 17.3 13.2 鞣花单宁 花梗鞣素 9.15 783 C34H24O22 633, 331, 301, 275 89.5 × × 5.3 53 57.3 鞣花单宁 原花青素B2 10.24 577 C30H26O12 425, 289, 161 47.1 × × × 33.7 24.3 黄酮 非西替尼-儿茶素 10.41 561 C30H26O11 289, 271, 245, 125 × 59.8 52.8 62.2 × × 黄酮 报春黄甙 10.87 449 C28H18O6 287, 269, 259, 125 × 40.9 63.9 67 × × 黄酮 短叶苏木酚酸 11.17 291 C13H8O8 247, 219, 203, 175 × × × × 52.4 76.7 酚酸 木麻黄素 11.49 633 C27H21O18 301 × × × × × 8.3 鞣花单宁 柚皮素己糖苷 11.58 433 C21H21O10 271, 253 × × × 9.4 × × 黄酮 非西替尼儿茶素 12.39 561 C30H26O11 471, 435, 363, 289 77.6 × × × 62.8 × 黄酮 二氢山柰酚-O-半乳糖苷 12.83 449 C21H22O11 287, 269, 259, 125 54.3 × × × 34.8 31.8 黄酮 木麻黄鞣宁 16.54 935 C41H28O26 633,301, 229 75.7 23.8 5.6 43.6 × 90.4 鞣花单宁 木麻黄鞣亭 17.26 935 C41H28O26 635, 569, 301, 229 0.2 107.9 39.2 8.6 1.6 88.8 鞣花单宁 芦丁 18.43 609 C27H30O16 301, 271, 179 27 39 × 45.6 28.4 × 黄酮 鞣花酸戊糖苷 18.77 433 C19H14O12 300, 301, 271 48.6 × × 18.9 40.1 × 鞣花单宁 鞣花酸 19.64 301 C14H6O8 257, 229, 157 105.1 135.8 133.1 134.8 111.5 149 鞣花单宁 槲皮素-3-O-半乳糖苷 20.36 463 C21H20O12 301, 271, 255, 161 × 31.6 × 37.6 14.7 × 黄酮 异荭草素阿拉伯糖苷 21.17 579 C26H28O15 447, 285, 255 × 19.3 × × × × 黄酮 山奈酚-3-O-洋槐糖苷 21.52 593 C27H30O15 285, 255, 195 45.5 30.6 30 233.1 45.8 × 黄酮 鞣花酸己糖醛酸 21.56 477 C21H18O13 301, 179 × × × × × 42.4 鞣花单宁 二氢山柰酚 22.25 287 C15H12O6 259, 243, 173 × × 4.1 × × × 黄酮 山奈酚-己糖苷 22.71 447 C21H20O11 285, 255, 227, 151 × 8.5 14.2 18.2 15 × 黄酮 柑属苷B 22.98 567 C27H36O13 491, 476, 341 9.9 × × 9 × × 黄酮 山奈酚-3-O-芸香糖苷 23.52 593 C27H30O15 327, 285, 255, 195 45.5 205.1 122.3 × 139.4 × 黄酮 山奈酚-己糖苷 24.98 447 C21H20O11 285, 227, 193, 151 95.4 84.1 74.3 113.4 15 × 黄酮 芹菜素鼠李糖苷 25.49 461 C21H18O12 415, 269, 161, 101 × × × × × 15 黄酮 橄榄脂素-葡萄糖苷 27.2 537 C26H34O12 341, 326, 149 21.1 17.7 21.4 19 × 11.3 黄酮 注:表中×表示未检出。 鞣花单宁是悬钩子属植物中的一类主要活性成分。通过对比母离子、离子碎片可以推断化合物的初步结构。鞣花单宁在负离子模式下的特征碎片离子包括:没食子酰基(m/z 151),hexahydroxydiphenoyl(HHDP)基团(m/z 301),HHDP-葡萄糖部分(m/z 463、301和161)和没食子酰葡萄糖基(m/z 331)。六个产地都含有丰富的鞣花单宁,共鉴定出12种鞣花单宁,主要包括鞣花酸、木麻黄鞣宁、花梗鞣素、galloyl-HHDP-glucose、鞣花酸己糖醛酸等,其中四川产地含量占比最高,占其总酚类化合物的56%。卢遇[13]通过HPLC-QTOF-MS/MS技术从覆盆子中鉴定了26个酚类物质成分,其中鞣花单宁是覆盆子中主要活性成分,这与本文结果相一致。
黄酮类化合物也是覆盆子中的主要酚类物质,共鉴定出19种黄酮类化合物,主要以黄酮苷形式存在。包括原花青素二聚体、表儿茶素、报春黄甙、柚皮素己糖苷、芦丁、槲皮素-3-O-半乳糖苷、异荭草素阿拉伯糖苷、山奈酚-3-O-洋槐糖苷、山奈酚-3-O-芸香糖苷、芹菜素鼠李糖苷等。除了四川产地,其他五个产地的黄酮类化合物含量的都相对较高,占其总酚类化合物的38%以上。其中浙江产地的含量最高,达55%左右。覆盆子中酚酸含量较少,共鉴定出3种酚酸,分别为白屈菜酸、没食子酸和短叶苏木酚酸。
2.3 自由基清除能力
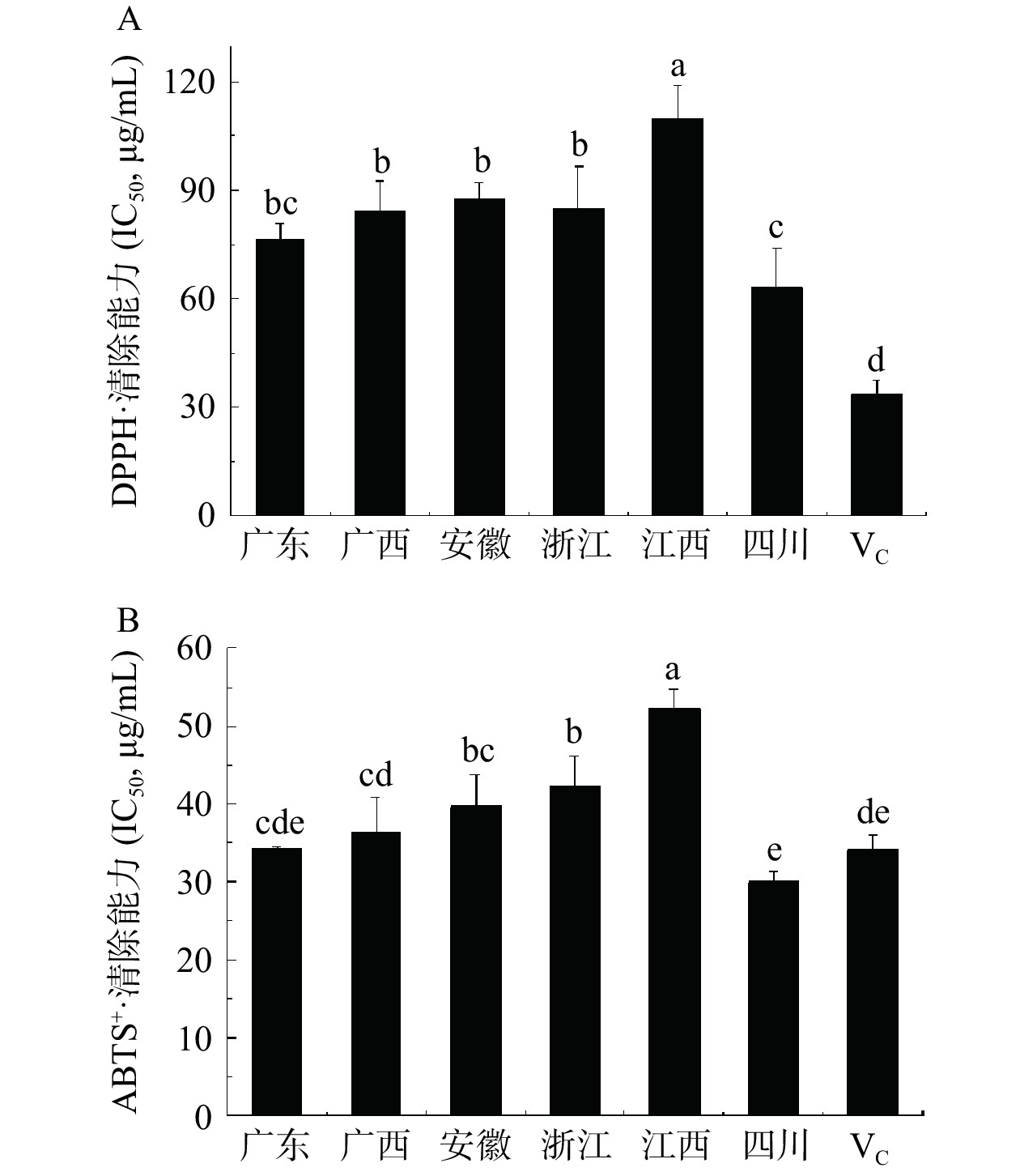
活性氧自由基(ROS)是人体的正常代谢物,但是过多的ROS在体内积累会造成器官的氧化损伤,从而诱发各种慢性疾病,如炎症、癌症、糖尿病、高血压等[14]。膳食中的多酚、黄酮类物质都是良好的天然自由基清除剂[15]。常用的体外自由基清除能力评价方法包括测定O2-·、·OH、DPPH·、ABTS+·等,本研究采用最常用的DPPH和ABTS法探究了不同产地覆盆子提取物的DPPH·和ABTS+·清除能力[16−17]。六个产地药用覆盆子提取物对DPPH·和ABTS+·清除能力如图2所示,IC50值越小,表示达到半数清除率时所需浓度越小,自由基清除能力越强,该产地覆盆子自由基清除能力越强。和阳性对照VC相比,不同产地覆盆子DPPH·和ABTS+·清除能力差异较大,四川覆盆子的DPPH·和ABTS+·清除能力最强,IC50值分别为63.069和29.977 μg/mL,广东、广西、安徽和浙江覆盆子提取物的DPPH·清除能力相差较小,江西覆盆子提取物的DPPH·和ABTS+·清除能力最弱,IC50值分别为109.750和52.230 μg/mL。张露等[10]研究发现江西德兴所产覆盆子醇溶多酚提取物的DPPH·的IC50值约为80 μg/mL,与本实验结果类似。吴峰华等[18]报道表明浙江覆盆子醇溶提取物的DPPH·的IC50值约为0.177±0.0078 mg/mL,与本实验不尽相同,也许是由于采摘的时间不同。
![]() 图 2 六个产地覆盆子提取物的DPPH·(A)和ABTS+·(B)清除能力注:图中不同小写字母表示差异显著P<0.05,图3同。Figure 2. DPPH· (A) and ABTS+· (B) scavenging capacity of raspberry extracts from six producing areas
图 2 六个产地覆盆子提取物的DPPH·(A)和ABTS+·(B)清除能力注:图中不同小写字母表示差异显著P<0.05,图3同。Figure 2. DPPH· (A) and ABTS+· (B) scavenging capacity of raspberry extracts from six producing areasMansouri等[19]证明悬钩子果实的自由基清除能力可能与其酚类、黄酮类、单宁和花青素含量有关,Muniyandi等[20]证明覆盆子的自由基清除能力与其所含酚类、黄酮类、单宁类化合物含量相关,曾小艳等[21]、谢欣梅等[22-23]证明原花青素、覆盆子酮、覆盆子提取物可以有效降低大鼠血糖,因此产地的不同影响了覆盆子中酚类、黄酮类、单宁类等化合物的含量,进而导致覆盆子间自由基清除能力的差异。覆盆子活性功能由其含有的活性成分决定,已有研究发现药用覆盆子中的主要活性物质为水解单宁[13],四川产地覆盆子提取物中水解单宁含量最高,这可能是四川产地覆盆子提取物具有最高自由基清除能力的原因。
2.4 α-葡萄糖苷酶抑制能力
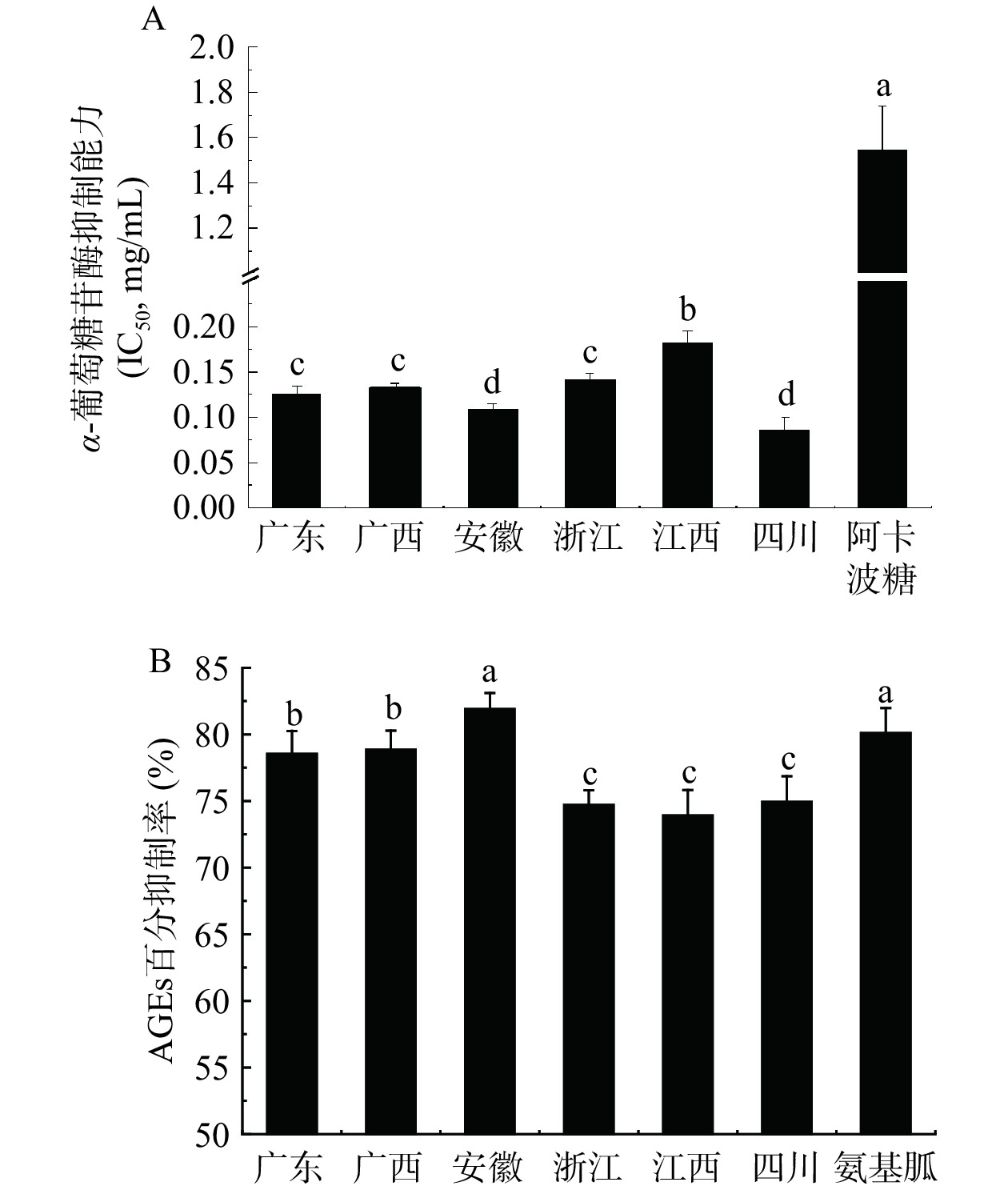
II型糖尿病的产生被认为与促胰岛素分泌和影响胰岛素敏感性的关键酶有关,如α-葡萄糖苷酶、蛋白酪氨酸磷酸酶、AGEs等[24−25]。α-葡萄糖苷酶可以水解多糖中的α-(1→4)-糖苷键,释放葡萄糖,而α-葡萄糖苷酶抑制剂则能抑制其活性,从而使机体葡萄糖释放速率下降,有效地降低血糖浓度[13]。不同产地药用覆盆子提取物的α-葡萄糖苷酶抑制能力如图3A所示。和阳性对照阿卡波糖(IC50=1.547 mg/mL)相比,六个产地覆盆子对α-葡萄糖苷酶均具有较强的抑制作用。四川和安徽覆盆子对α-葡萄糖苷酶具有最强抑制效果,IC50值分别为0.086和0.109 mg/mL。广东、广西和浙江覆盆子的α-葡萄糖苷酶抑制能力次之,IC50达0.125~0.142 mg/mL。江西覆盆子的α-葡萄糖苷酶抑制能力最弱,IC50值为0.182 mg/mL。Chen等[26]发现河北产地的覆盆子提取物具有很好的α-葡萄糖苷酶的抑制能力,是降糖药阿卡波糖的9倍,与本文报道的江西覆盆子类似(8.5倍)。该结果为覆盆子作为α-葡萄糖苷酶抑制剂资源和降血糖功能食品的开发提供了科学依据,但其具体降血糖成分和作用机制需要进一步研究。
2.5 AGEs抑制能力
AGEs是由还原糖及其衍生物(如甘油醛,乙醇醛,甲基乙二醛和乙醛)与蛋白质或脂质发生非酶糖基化生成的终末期产物,机体内AGEs的积累会与蛋白质发生交联,引发糖尿病的一系列并发症,延缓衰老和缓解糖尿病并发症的有效方法之一便是抑制AGEs的累积[27]。本研究以不同产地覆盆子对AGEs的抑制活性作为其抑制糖尿病并发症的重要指标。以抑制AGEs生成为指标,对不同产地的覆盆子提取物进行抑制糖基化活性检测,结果如图3B所示,不同产地药用覆盆子提取物对AGEs的形成具有很强的抑制效果,当提取物为1 mg/mL时,其对AGEs形成的抑制率达到了73.92%~81.91%。安徽覆盆子的AGEs抑制率最高,达到81.91%,与阳性对照氨基胍无显著差异(P>0.05)。广东和广西覆盆子的AGEs抑制率次之(78.54%~78.85%),江西、四川和浙江覆盆子的AGEs抑制率最低(74.94%~73.92%)。
3. 结论
不同产地覆盆子间总酚、总黄酮和总水解单宁含量存在差异,其中广东和安徽覆盆子提取物总酚含量最高,广西和四川产地的最低;浙江覆盆子提取物总黄酮含量最高,广西、江西和广东产地次之,四川产地的最低;四川覆盆子提取物总水解单宁含量最高,广西和浙江产地次之,广东和安徽产地的最低。从六个产地的覆盆子提取物中鉴定出34种酚类物质,主要是鞣花单宁、黄酮和酚酸类物质,四川覆盆子提取物含有最丰富的鞣花单宁。不同产地覆盆子提取物都具有一定自由基清除能力、α-葡萄糖苷酶抑制活性以及AGEs抑制能力,其中四川覆盆子的DPPH·和ABTS+·清除能力和α-葡萄糖苷酶抑制活性远高于其他产地,而安徽覆盆子提取物的AGEs抑制能力略高于其他产地。本文仅对部分产地覆盆子酚类物质及其抗糖尿病活性进行了初步研究,对于不同产地体内抗糖尿病活性及机制还有待进一步研究。
-
图 2 六个产地覆盆子提取物的DPPH·(A)和ABTS+·(B)清除能力
注:图中不同小写字母表示差异显著P<0.05,图3同。
Figure 2. DPPH· (A) and ABTS+· (B) scavenging capacity of raspberry extracts from six producing areas
表 1 六个产地覆盆子提取物的总酚、水解单宁、总黄酮含量
Table 1 Total phenols, hydrolyzed tannins and total flavonoids content of raspberry extracts from six producing areas
成分 广东 广西 安徽 浙江 江西 四川 总酚
(μg GAE/mg E)349.77±18.76a 294.47±9.82b 345.16±14.33a 343.47±7.14a 300.07±13.82b 285.16±19.93b 总黄酮
(μg QUE/mg E)153.51±18.50b 156.92±6.67b 137.07±12.35b 202.55±15.12a 154.70±4.01b 112.77±16.20c 总水解单宁
(mg GAE/g E)62.07±4.20d 98.33±5.40b 64.87±2.84d 91.13±5.37bc 79.60±15.32c 125.07±3.89a 注:同一行中的不同小写字母表示样品间的差异显著(P<0.05)。 表 2 六个产地覆盆子提取物的定性定量分析
Table 2 Qualitative and quantitative analysis of raspberry extracts from six producing areas
化合物 保留时间
(min)母离子 分子式 碎片离子
(m/z)含量(峰面积×105) 分类 广东 广西 安徽 浙江 江西 四川 六羟基二苯基葡萄糖 1.79 481 C27H14O9 301, 275, 231 × 8.9 × × × × 鞣花单宁 白屈菜酸 2.43 183 C7H4O6 139, 83, 67 11.8 × 11.8 14.1 8.8 18.3 酚酸 没食子酸 3.89 169 C7H6O5 125, 79 × × 17.8 × 10.5 24.1 酚酸 月见草素C 5.8 783 C34H24O22 481, 301, 275 22.8 42.9 53.2 80.4 0.3 × 鞣花单宁 Valoneic acid dilactone 7.06 469 C21H10O13 451, 379, 301 38.1 36.5 30.0 × × × 鞣花单宁 月见草素C异构体 7.41 783 C34H24O22 481, 301, 275 79.3 81.5 76.4 79.7 × × 鞣花单宁 原花青素B4 8.28 577 C30H26O12 425, 289, 161 × 29.4 34.7 45.2 × × 黄酮 表儿茶素 8.51 289 C15H14O6 245, 187 × 40.7 38.7 × × × 黄酮 Galloyl-HHDP-glucose 8.54 633 C27H22O18 463, 301, 275, 161 × × × × 17.3 13.2 鞣花单宁 花梗鞣素 9.15 783 C34H24O22 633, 331, 301, 275 89.5 × × 5.3 53 57.3 鞣花单宁 原花青素B2 10.24 577 C30H26O12 425, 289, 161 47.1 × × × 33.7 24.3 黄酮 非西替尼-儿茶素 10.41 561 C30H26O11 289, 271, 245, 125 × 59.8 52.8 62.2 × × 黄酮 报春黄甙 10.87 449 C28H18O6 287, 269, 259, 125 × 40.9 63.9 67 × × 黄酮 短叶苏木酚酸 11.17 291 C13H8O8 247, 219, 203, 175 × × × × 52.4 76.7 酚酸 木麻黄素 11.49 633 C27H21O18 301 × × × × × 8.3 鞣花单宁 柚皮素己糖苷 11.58 433 C21H21O10 271, 253 × × × 9.4 × × 黄酮 非西替尼儿茶素 12.39 561 C30H26O11 471, 435, 363, 289 77.6 × × × 62.8 × 黄酮 二氢山柰酚-O-半乳糖苷 12.83 449 C21H22O11 287, 269, 259, 125 54.3 × × × 34.8 31.8 黄酮 木麻黄鞣宁 16.54 935 C41H28O26 633,301, 229 75.7 23.8 5.6 43.6 × 90.4 鞣花单宁 木麻黄鞣亭 17.26 935 C41H28O26 635, 569, 301, 229 0.2 107.9 39.2 8.6 1.6 88.8 鞣花单宁 芦丁 18.43 609 C27H30O16 301, 271, 179 27 39 × 45.6 28.4 × 黄酮 鞣花酸戊糖苷 18.77 433 C19H14O12 300, 301, 271 48.6 × × 18.9 40.1 × 鞣花单宁 鞣花酸 19.64 301 C14H6O8 257, 229, 157 105.1 135.8 133.1 134.8 111.5 149 鞣花单宁 槲皮素-3-O-半乳糖苷 20.36 463 C21H20O12 301, 271, 255, 161 × 31.6 × 37.6 14.7 × 黄酮 异荭草素阿拉伯糖苷 21.17 579 C26H28O15 447, 285, 255 × 19.3 × × × × 黄酮 山奈酚-3-O-洋槐糖苷 21.52 593 C27H30O15 285, 255, 195 45.5 30.6 30 233.1 45.8 × 黄酮 鞣花酸己糖醛酸 21.56 477 C21H18O13 301, 179 × × × × × 42.4 鞣花单宁 二氢山柰酚 22.25 287 C15H12O6 259, 243, 173 × × 4.1 × × × 黄酮 山奈酚-己糖苷 22.71 447 C21H20O11 285, 255, 227, 151 × 8.5 14.2 18.2 15 × 黄酮 柑属苷B 22.98 567 C27H36O13 491, 476, 341 9.9 × × 9 × × 黄酮 山奈酚-3-O-芸香糖苷 23.52 593 C27H30O15 327, 285, 255, 195 45.5 205.1 122.3 × 139.4 × 黄酮 山奈酚-己糖苷 24.98 447 C21H20O11 285, 227, 193, 151 95.4 84.1 74.3 113.4 15 × 黄酮 芹菜素鼠李糖苷 25.49 461 C21H18O12 415, 269, 161, 101 × × × × × 15 黄酮 橄榄脂素-葡萄糖苷 27.2 537 C26H34O12 341, 326, 149 21.1 17.7 21.4 19 × 11.3 黄酮 注:表中×表示未检出。 -
[1] 王小蓉, 汤浩茹, 邓群仙. 中国树莓属植物多样性及品种选育研究进展[J]. 园艺学报,2006,33(1):7. [WANG X R, TANG H R, DENG Q X. Advancement in research of genetic diversity of bramble (Rubus L.) and its breeding in China[J]. Acta Horticulturae Sinica,2006,33(1):7.] doi: 10.3321/j.issn:0513-353X.2006.01.048 WANG X R, TANG H R, DENG Q X. Advancement in research of genetic diversity of bramble (Rubus L.) and its breeding in China[J]. Acta Horticulturae Sinica, 2006, 33(1): 7. doi: 10.3321/j.issn:0513-353X.2006.01.048
[2] 汪传佳, 徐小静, 康志雄, 等. 覆盆子资源开发利用研究综述[J]. 浙江林业科技,2004(1):66−69. [WANG C J, XU X J, KANG Z X, et al. Summary on utilization of raspberry resources[J]. Journal of Zhejiang Forestry Science & Technology,2004(1):66−69.] doi: 10.3969/j.issn.1001-3776.2004.01.019 WANG C J, XU X J, KANG Z X, et al. Summary on utilization of raspberry resources[J]. Journal of Zhejiang Forestry Science & Technology, 2004(1): 66−69. doi: 10.3969/j.issn.1001-3776.2004.01.019
[3] ZHANG T T, YANG L, JIANG J G. Bioactive comparison of main components from unripe fruits of Rubus chingii Hu and identification of the effective component[J]. Food & Function,2015,6(7):2205−2214.
[4] YU G, LUO Z, WANG W, et al. Rubus chingii Hu:A review of the phytochemistry and pharmacology[J]. Frontiers in Pharmacology,2019,10:799−821. doi: 10.3389/fphar.2019.00799
[5] TAN J, WANG D, LU Y, et al. Metabolic enzyme inhibitory abilities, in vivo hypoglycemic ability of palmleaf raspberry fruits extracts and identification of hypoglycemic compounds[J]. Food Science and Human Wellness,2023,12(4):1232−1240. doi: 10.1016/j.fshw.2022.10.005
[6] SHENG J Y, WANG S Q, LIU K H, et al. Rubus chingii Hu:An overview of botany, traditional uses, phytochemistry, and pharmacology[J]. Chinese Journal of Natural Medicines,2020,18(6):401−416. doi: 10.1016/S1875-5364(20)30048-0
[7] 平嘉倩, 闫翠香, 朱伊婧, 等. 不同产地悬钩子果实营养成分分析[J]. 现代园艺,2022,45(5):38−39,42. [PING J Q, YAN C X, ZHU Y J, et al. Analysis of nutrients in raspberry fruits from different producing areas[J]. Modern Horticulture,2022,45(5):38−39,42.] doi: 10.3969/j.issn.1006-4958.2022.05.013 PING J Q, YAN C X, ZHU Y J, et al. Analysis of nutrients in raspberry fruits from different producing areas[J]. Modern Horticulture, 2022, 45(5): 38−39,42. doi: 10.3969/j.issn.1006-4958.2022.05.013
[8] 付彩群, 黄道明, 郑露盼, 等. 不同产地、采收期、种植条件对覆盆子有效成分含量的影响研究[J]. 药品评价,2021,18(12):728−730. [FU C Q, HUANG D M, ZHENG L P, et al. Study on the effect of different producing area, harvesting time and planting conditions on the content of active components in Rubus chingii Hu[J]. Drug Evaluation,2021,18(12):728−730.] FU C Q, HUANG D M, ZHENG L P, et al. Study on the effect of different producing area, harvesting time and planting conditions on the content of active components in Rubus chingii Hu[J]. Drug Evaluation, 2021, 18(12): 728−730.
[9] PARK S J, HYUN S H, SUH H W, et al. Differentiation of black raspberry fruits according to species and geographic origins by genomic analysis and H-1-NMR-based metabolic profiling[J]. Journal of the Korean Society for Applied Biological Chemistry,2012,55(5):633−642. doi: 10.1007/s13765-012-2062-0
[10] 张露, 王夜寒, 梅强根, 等. 覆盆子不同多酚组成及抗氧化、抗糖尿病活性[J]. 食品科学,2022(18):192−199. [ZHANG L, WANG Y H, MEI Q G, et al. Composition and antioxidant and antidiabetic activities of different polyphenol fractions from the fruits of Rubus chingii Hu[J]. Food Science,2022(18):192−199.] doi: 10.7506/spkx1002-6630-20210821-275 ZHANG L, WANG Y H, MEI Q G, et al. Composition and antioxidant and antidiabetic activities of different polyphenol fractions from the fruits of Rubus chingii Hu[J]. Food Science, 2022(18): 192−199. doi: 10.7506/spkx1002-6630-20210821-275
[11] 张露, 刘鹏飞, 涂宗财, 等. 香榧不同部位提取物的抗氧化和酶抑制活性比较分析[J]. 食品科学,2018,39(10):78−83. [ZHANG L, LIU P F, TU Z C, et al. Comparison of antioxidant activity and enzyme inhibitory activity of different plant parts of Torreya grandis cv. Merrillii[J]. Food Science,2018,39(10):78−83.] doi: 10.7506/spkx1002-6630-201810013 ZHANG L, LIU P F, TU Z C, et al. Comparison of antioxidant activity and enzyme inhibitory activity of different plant parts of Torreya grandis cv. Merrillii[J]. Food Science, 2018, 39(10): 78−83. doi: 10.7506/spkx1002-6630-201810013
[12] ZHANG L, DENG M, WANG S Y, et al. Mitigation of Paeoniae Radix Alba extracts on H2O2-induced oxidative damage in HepG2 cells and hyperglycemia in zebrafish, and identification of phytochemical constituents[J]. Frontiers in Nutrition,2023,10:1135759. doi: 10.3389/fnut.2023.1135759
[13] 卢遇. 覆盆子中降血糖成分提取分离和主要活性成分鉴定[D]. 南昌:江西师范大学, 2020. [LU Y. Extraction and fraction of hypoglycemic components from Rubus chingii Hu and identification of major bioactive compounds[D]. Nanchang:Jiangxi Normal University, 2020.] LU Y. Extraction and fraction of hypoglycemic components from Rubus chingii Hu and identification of major bioactive compounds[D]. Nanchang: Jiangxi Normal University, 2020.
[14] NAPOLITANO G, FASCIOLO G, VENDITTI P. Mitochondrial management of reactive oxygen species[J]. Antioxidants,2021,10(11):1824. doi: 10.3390/antiox10111824
[15] SANTHAKUMAR A B, BULMER A C, SINGH I. A review of the mechanisms and effectiveness of dietary polyphenols in reducing oxidative stress and thrombotic risk[J]. Journal of Human Nutrition and Dietetics,2014,27(1):1−21. doi: 10.1111/jhn.12177
[16] 王荣, 罗倩, 冯怡. DPPH、ABTS和FRAP微量法测定山奈酚的抗氧化能力[J]. 广州化工,2021,49(3):58−59,63. [WANG R, LUO Q, FENG Y. Determination of antioxidant effects of kaempferol by micro-model of DPPH, ABTS and FRAP assay[J]. Guangzhou Chemical Industry,2021,49(3):58−59,63.] doi: 10.3969/j.issn.1001-9677.2021.03.019 WANG R, LUO Q, FENG Y. Determination of antioxidant effects of kaempferol by micro-model of DPPH, ABTS and FRAP assay[J]. Guangzhou Chemical Industry, 2021, 49(3): 58−59,63. doi: 10.3969/j.issn.1001-9677.2021.03.019
[17] MUNTEANU I G, APETREI C. Analytical methods used in determining antioxidant activity:A review[J]. International Journal of Molecular Sciences,2021,22(7):3380. doi: 10.3390/ijms22073380
[18] 吴峰华, 刘相真, 杨虎清, 等. 覆盆子醇提物及其不同极性部位抗氧化活性研究[J]. 中国食品学报,2012,12(2):24−29. [WU F H, LIU X Z, YANG H Q, et al. Study on antioxidant activity of ethanol extract and its different polarity fractions from Rubus chingii Hu[J]. Journal of Chinese Institute of Food Science and Technology,2012,12(2):24−29.] doi: 10.3969/j.issn.1009-7848.2012.02.004 WU F H, LIU X Z, YANG H Q, et al. Study on antioxidant activity of ethanol extract and its different polarity fractions from Rubus chingii Hu[J]. Journal of Chinese Institute of Food Science and Technology, 2012, 12(2): 24−29. doi: 10.3969/j.issn.1009-7848.2012.02.004
[19] MANSOURI A, EMBAREK G, KOKKALOU E, et al. Phenolic profile and antioxidant activity of the Algerian ripe date palm fruit (Phoenix dactylifera)[J]. Food Chemistry,2005,89(3):411−420. doi: 10.1016/j.foodchem.2004.02.051
[20] MUNIYANDI K, GEORGE E, SATHYANARAYANAN S, et al. Phenolics, tannins, flavonoids and anthocyanins contents influenced antioxidant and anticancer activities of Rubus fruits from Western Ghats, India[J]. Food Science and Human Wellness,2019,8(1):73−81. doi: 10.1016/j.fshw.2019.03.005
[21] 曾小艳, 李永平, 赵钰, 等. 覆盆子原花青素对2型糖尿病大鼠糖脂代谢及抗氧化作用影响的研究[J]. 现代中药研究与实践,2022,36(1):18−21. [ZENG X Y, LI Y P, ZHAO Y, et al. Study on the effect of raspberry proanthocyanidins on glucose and lipid metabolism and anti-oxidation in type 2 diabetic rats[J]. Research and Practice on Chinese Medicines,2022,36(1):18−21.] ZENG X Y, LI Y P, ZHAO Y, et al. Study on the effect of raspberry proanthocyanidins on glucose and lipid metabolism and anti-oxidation in type 2 diabetic rats[J]. Research and Practice on Chinese Medicines, 2022, 36(1): 18−21.
[22] 谢欣梅, 庞晓斌, 李晓婷. 覆盆子酮对糖尿病模型小鼠的降血糖作用及其机制研究[J]. 中国药学杂志,2012,47(23):1899−1904. [XIE X M, PANG X B, LI X T. Hypoglycemic effect and mechanism of raspberry ketone on diabetic model mice[J]. Chinese Pharmaceutical Journal,2012,47(23):1899−1904.] XIE X M, PANG X B, LI X T. Hypoglycemic effect and mechanism of raspberry ketone on diabetic model mice[J]. Chinese Pharmaceutical Journal, 2012, 47(23): 1899−1904.
[23] 谢欣梅, 庞晓斌. 覆盆子提取物对2型糖尿病大鼠糖脂代谢的影响及对肝脏保护作用的研究[J]. 中成药,2013,35(3):460−465. [XIE X M, PANG X B. Effects of Rubi Fructus extract on glucose and blood lipid metabolisms and protective effects on liver in type 2 diabetic rats[J]. Chinese Traditional Patent Medicine,2013,35(3):460−465.] doi: 10.3969/j.issn.1001-1528.2013.03.007 XIE X M, PANG X B. Effects of Rubi Fructus extract on glucose and blood lipid metabolisms and protective effects on liver in type 2 diabetic rats[J]. Chinese Traditional Patent Medicine, 2013, 35(3): 460−465. doi: 10.3969/j.issn.1001-1528.2013.03.007
[24] 岳丹伟. 白扁豆花黄酮类化合物分离鉴定及其抗氧化、降糖活性研究[D]. 芜湖:安徽工程大学, 2021. [YUE D W. Study on chemical constituents, antioxidant and hypoglycemic activities of flavonoids from Flos Dolichoris Lablab L. [D]. Wuhu:Anhui Engineering University, 2021.] YUE D W. Study on chemical constituents, antioxidant and hypoglycemic activities of flavonoids from Flos Dolichoris Lablab L. [D]. Wuhu: Anhui Engineering University, 2021.
[25] SUN H, SAEEDI P, KARURANGA S, et al. IDF diabetes atlas:Global, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045 [J]. Diabetes Research and Clinical Practice, 2022, 183:109119.
[26] CHEN Y, CHEN Z Q, GUO Q W, et al. Identification of ellagitannins in the unripe fruit of Rubus chingii Hu and evaluation of its potential antidiabetic activity[J]. Journal of Agricultural and Food Chemistry,2019,67(25):7025−7039. doi: 10.1021/acs.jafc.9b02293
[27] KUZAN A. Toxicity of advanced glycation end products[J]. Biomedical Reports,2021,14(5):1−8.
-
期刊类型引用(0)
其他类型引用(1)





 下载:
下载:
 下载:
下载:



