Research Progress on Extraction, Purification and Biological Activities of Sugarcane Polyphenols
-
摘要: 甘蔗是我国最重要的糖料作物,具有良好的营养价值、药用价值和经济价值。甘蔗中富含酚类物质,具有抗氧化、抗炎、降血糖等多种生理功能。本文重点综述了甘蔗多酚的提取方法以及新型提取技术在植物多酚中的应用,介绍了甘蔗多酚纯化方法的原理及特点,并对其抗氧化、降血糖、抗炎、抗癌、抗菌等重要生物活性的研究情况进行了阐述。总结发现甘蔗多酚提取纯化方法较为传统,虽然具有多种生物活性,但其活性作用机制尚未明晰,应关注甘蔗多酚提取纯化新技术以及活性机制研究,以促进甘蔗多酚的开发利用以及甘蔗副产物的精深加工。Abstract: Sugarcane is the most vital sugar crop in China, with excellent nutritional, medicinal and economic value. Sugarcane is rich in phenolic compounds, which have a variety of physiological functions, such as antioxidant, anti-inflammatory, and hypoglycemic. This paper focuses on the extraction of sugarcane polyphenols and the application of novel extraction techniques to plant polyphenols. In addition, principles and properties of purification methods for sugarcane polyphenols are presented, and important biological activities including antioxidant, hypoglycaemic, anti-inflammatory, anti-cancer and anti-bacterial properties are described. The extraction and purification of sugarcane polyphenols is found to be relatively routine. Although sugarcane polyphenols have a variety of biological activities, the mechanisms of their activity have not been fully elucidated. There is a need to focus on new extraction and purification techniques for sugarcane polyphenols and mechanisms of their activity to facilitate the development and utilization of sugarcane polyphenols and deep processing of sugarcane byproducts.
-
Keywords:
- sugarcane polyphenols /
- extraction /
- purification /
- biological activities
-
甘蔗(Saccharum officinarum L.),属禾本科甘蔗属,是一种重要的多年生草本植物,广泛种植于热带或亚热带地区[1]。据国家统计局统计,2022年我国甘蔗总产量达10810.14万吨,仅次于玉米、稻谷和小麦。事实上,甘蔗除含有蔗糖、葡萄糖和果糖外,还富含多酚、氨基酸、维生素等多种活性成分,已被证明具有良好的药用价值[2]。我国著名医学家李时珍在《本草纲目》中以“蔗,脾之果也。其浆甘寒,能泻火热”来介绍甘蔗。印度一直将甘蔗作为治疗黄疸、炎症、便秘、脓毒性休克等疾病的药用植物载入典籍[3]。近年来,甘蔗的药用价值日益引起人们关注[4]。
植物多酚大多具有抗氧化应激作用,对由氧化应激损伤引起的衰老[5]、糖尿病[6]、炎症[7]、肿瘤[8]等一系列疾病具有较好的治疗效果。研究表明,甘蔗的生物活性,包括抗菌[9]、抗癌[10]、抗炎[11]及抗氧化[12]作用等,主要是通过酚类化合物的存在来介导的。如表1所示,甘蔗中主要的酚类化合物,包括黄酮类(芹菜素、木犀草素、柚皮素等)和酚酸类(没食子酸、香草酸、阿魏酸等)。
但是,目前关于甘蔗多酚提取、分离纯化方面的研究仍聚焦于传统方法,对其生物活性的研究主要集中在功效方面,而活性作用机制尚不清晰。本文对近年来甘蔗多酚的提取、纯化方法和生物活性等研究情况进行系统介绍,并结合当前植物活性成分提取新技术发展趋势,对甘蔗多酚提取技术与分离纯化方法未来发展进行展望,以期为甘蔗多酚的进一步研究应用提供参考,也为甘蔗资源多元高值化利用提供新思路。
1. 甘蔗多酚的提取技术
甘蔗多酚作为一种来源丰富,极具营养和药用功效的天然成分,具有巨大的发展潜力和良好的应用前景。因此,研究甘蔗多酚的提取方法具有重要的应用价值。目前甘蔗多酚类物质的提取方法主要包括溶剂萃取法、超声波辅助提取法、微波辅助提取法、生物酶法等,下面对每种提取方法进行简要综述。
1.1 溶剂萃取法
溶剂萃取法是依据“相似相溶”的原理,利用多酚在不同溶剂中的溶解度存在差异来进行分离[13]。常用的提取溶剂包括水、甲醇、乙醇、乙酸乙酯、丙酮等。水是一种用于提取生物体内活性成分的良好溶剂,但在多酚提取中并不适用。由于植物中的多酚会与蛋白质或多糖等大分子借助氢键和疏水键结合,形成稳定的分子络合物,因此所用溶剂必须具有使氢键断裂的作用才能有效地将酚类化合物提取出来[14]。甘蔗多酚提取研究常选用甲醇、乙醇、丙酮、乙酸乙酯等有机溶剂中的一种或混合几种作为提取溶剂。孙晓雪[15]选用乙醇提取甘蔗梢多酚。闫怀锋等[16]采用混合溶剂(甲醇、丙酮、水)提取甘蔗皮中的花色苷。
在溶剂萃取法中,因为植物细胞壁结构致密且成分复杂等原因增加了传质阻力,故单一溶剂萃取效率低;虽然多元有机溶剂萃取法可能提高多酚提取率,但因溶剂回收困难、消耗量大且存在毒性等缺点,难以实现工业应用,因此在实际多酚提取过程中常与强化辅助提取手段结合。
1.2 超声波和微波辅助提取法
超声波辅助提取法是指在溶剂萃取法提取中,利用超声波空化产生的剪切力,机械地打破植物细胞壁,加快酚类物质的扩散溶解,从而提高多酚的提取效率[17]。微波辅助提取法提取的作用机制包括离子传导和偶极旋转两种能量转移机制,离子传导和偶极子旋转使物料迅速升温,细胞破裂,胞外溶剂能够更好地渗透到细胞中溶解内溶物[18]。
目前,超声波辅助提取法和微波辅助提取法在甘蔗多酚的提取研究中应用较为广泛。Feng等[19]、阎欲晓等[20]和赵毅[21]分别研究了超声波辅助乙醇提取法提取甘蔗皮、甘蔗叶和甘蔗渣多酚的工艺。韦巧艳等[22]和杨谷良等[23]均采用微波辅助乙醇提取法,分别研究了甘蔗叶多酚和甘蔗渣多酚的提取工艺。上述研究的甘蔗多酚提取量存在显著差异,其中甘蔗皮多酚高达8670 mg/100 g[19],甘蔗渣多酚提取量为285.3 mg/100 g[21],可见甘蔗原料部位的选择对多酚提取量具有较大影响。此外,提取方法也是造成差异的可能因素。超声波辅助提取法和微波辅助提取法提取甘蔗叶多酚,提取量分别为1134 mg/100 g[20]和1062.8 mg/100 g[22]。
相对于传统溶剂萃取法,超声波和微波辅助提取法提取率高,提取时间缩短,有机溶剂用量少且提取能耗降低。同时,超声波和微波辅助提取法的提取温度不高,这有利于保护多酚类化合物的化学结构和生物活性。但是,超声波和微波辅助提取法存在噪音或辐射污染问题。有研究表明,噪音污染可能是心血管疾病的影响因素[24],而微波辐射可能易引起人体疲劳、头痛、记忆力衰退等神经衰弱症状[25]。
1.3 生物酶法
生物酶法提取主要是利用生物酶将细胞壁某些特定成分溶解,使细胞壁破裂,促进细胞内多酚扩散至溶剂中,从而达到提取目的。因此,酶的选择非常关键,必须要根据细胞壁的结构和化学组成选择合适的酶,才能有效地破坏细胞壁结构。张思原等[26]采用果胶酶和纤维素酶(果胶酶:纤维素酶为2:3)组成的复合酶来提取甘蔗梢多酚,当pH为5.0、加酶量为1.6%、提取温度为56 ℃、提取时间为30 min时,多酚提取量达471 mg/100 g。生物酶法具有操作条件温和、高效等优势,并可最大程度地保护多酚功能活性,但是生物酶价格较高且提取过程需增加脱酶环节,难以实现工业化应用。
上述甘蔗多酚提取技术虽能有效提取多酚类物质,但存在提取率低、纯度低等问题。因此,有必要结合当前国内外植物多酚提取技术新的研究进展,提出开发甘蔗多酚绿色提取技术发展新思路,以促进甘蔗多酚提取技术工业化生产应用,实现甘蔗多酚资源化利用。
2. 新型提取技术在植物多酚中的应用
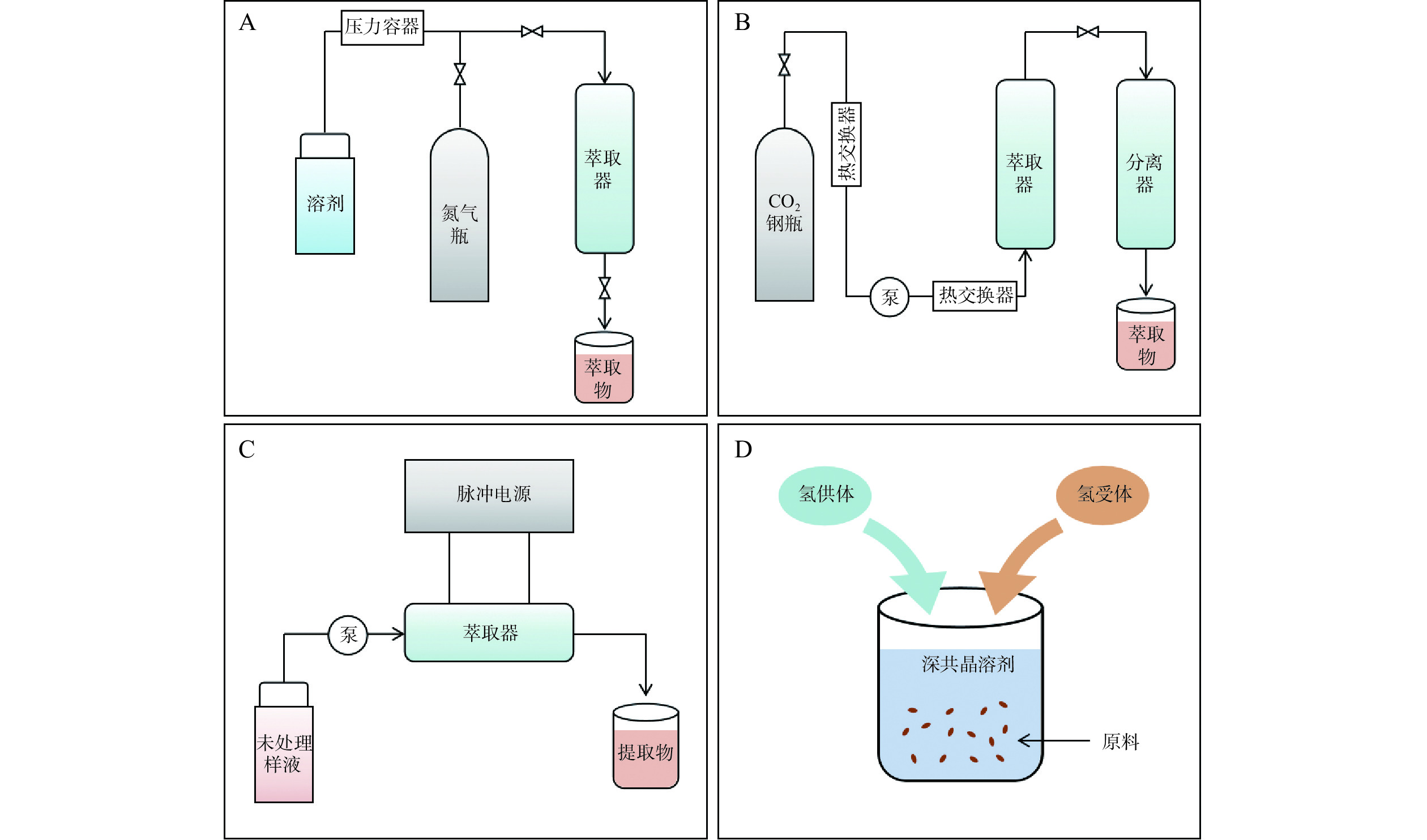
目前,多种新型提取技术在其他植物多酚提取研究中已经得到应用,其中加压液体提取法(图1A)、超临界流体萃取法(图1B)、高压脉冲电场提取法(图1C)及深共晶溶剂提取法(图1D)等的应用最为广泛。下面对几种新型提取技术原理和应用情况进行简要综述。
2.1 加压液体提取法
加压液体提取法是利用外加压力提高提取溶剂的沸点,提高酚类化合物在溶剂中的溶解度和扩散速度,从而提高多酚的提取量[27]。由于植物细胞壁坚韧,施加一定压力能够加速细胞壁的破除,使得酚类物质更好地溶出。研究表明,与常规方法相比,加压液体提取法具有显著优势。Dobroslavi´c等[28]采用静态加压热水提取方法提取月桂叶中的多酚类物质,提取的总酚含量达到46.34 mg/g,远高于超声波辅助提取法(36.74 mg/g)。Domínguez-Rodríguez等[29]比较发现,加压液体提取法对甜樱桃果渣多酚的提取效果(14±1 mg/100 g)显著优于常规方法(8.30±0.05 mg/100 g)。此外,酶辅助加压热水提取法提取甜樱桃果渣多酚的提取量达到加压热水提取法的五倍[29]。可见,采用复合法提取可能达到“1+1>2”的效果,一定程度上弥补了单一提取法的不足。
2.2 超临界流体萃取法
超临界流体萃取法是利用流体在超临界状态(压力和温度均高于热力学临界值时)下,兼有液体与气体高渗透力、高溶解力和强穿透力的特性来提高多酚提取率[30]。目前,超临界流体萃取法在植物多酚中的应用越来越广泛,如葡萄籽多酚[31]、可可籽多酚[32]和玫瑰多酚[33]等,均以CO2为萃取剂。Phan等[34]使用超临界CO2萃取技术提取越南桂花叶多酚,提取量达87.42±1.33 mg/g,最佳提取时间与温度分别为2 h和45 ℃,明显优于索氏抽提法(6 h,85 ℃)。因此超临界流体萃取法被认为是一种具有广阔应用前景的绿色、高效提取方法。
2.3 高压脉冲电场提取法
高压脉冲电场是一种利用高强度外加电场导致细胞膜“电穿孔”的新兴技术,使用这项技术进行提取能够使植物组织表面形成大量的孔隙,提高渗透性,促进酚类物质的释放[35]。Athanasiadis等[36]对比研究了高压脉冲电场辅助乙醇溶液与纯溶剂(乙醇溶液)对丹参叶多酚提取效果的影响,发现脉冲电场能够显著提高丹参叶多酚的提取效率,其中总酚含量提高了73.23%,迷迭香酸含量提高了403.1%。Lakka等[37]研究脉冲电场对犬蔷薇多酚提取的影响,发现不同电场强度(1.2~2.0 kV/cm)均能显著提高犬蔷薇多酚的提取量,其中1.4 kV/cm电场强度的提取量提高了63.79%。高压脉冲电场以耗时短、能耗低、温升小等优点,在植物多酚提取领域受到广泛关注。当前,解决其稳定性低、成本高等问题是高压脉冲电场规模化发展的关键。
2.4 深共晶溶剂萃取法
作为一种绿色、低成本、易合成的溶剂,近年来,深共晶溶剂(DES)常被用于植物黄酮和酚酸等生物活性物质的提取。DES是由氢键受体(如氯化胆碱)与氢键供体(天然植物基有机离子,如氨基酸、羧酸、糖)通过氢键作用形成的共晶混合物,其熔点比每个单一组分的熔点低,从而增大溶剂扩散系数,使操作温度范围变宽,有利于多酚类化合物的提取[38]。Liu等[39]采用超声波辅助深共晶剂萃取技术从鸡矢藤中提取多酚,所得总黄酮含量达27.09 mg/g,提取率相较于传统溶剂(水、乙醇、甲醇)法分别提高了51%、52%、100%,且所得提取物抗氧化活性更强。研究表明,与传统溶剂相比,DES具有较强的溶解结构多糖的能力,从而更好地破除细胞壁,使得溶剂渗入物料内部溶解多酚[40]。因此,深共晶溶剂可能替代传统有机溶剂成为实现甘蔗多酚绿色高效提取的一个重要突破点。
近年来,在天然产物的提取方面,因微波/超声波辅助提取法、加压液体提取法、超临界流体萃取法及脉冲电场辅助提取法等具有明显优点,因此已逐渐取代传统溶剂萃取法。然而,截止至今,甘蔗多酚的提取仍局限于传统方法,不仅得率低且其生物活性也受到一定影响,因此很有必要根据甘蔗原料特性与酚类物质性质等,借鉴其他植物多酚提取新方法,开发新型的甘蔗多酚高效、节能及绿色的提取技术,为早日实现甘蔗多酚高值化利用提供技术支撑。
3. 甘蔗多酚的分离纯化方法
由上述提取方法所得的多酚实质是粗提物,还含有糖类、蛋白质、脂类等非酚类物质,成分复杂,纯度不高,会影响其活性甚至限制其于高端产业的应用,因此必须对其进行分离纯化处理。目前多酚粗提物分离纯化主要包括多酚富集和多酚组分分离两个过程。多酚富集过程是将多酚粗提物中的蛋白质、糖类、脂类等非酚类物质去除,使多酚含量显著提高,通常借助有机溶剂来实现。多酚组分分离主要是依据多酚结构或构象特性、电荷特性、分子量以及对配基的亲和力的差异。目前用于甘蔗多酚分离纯化的方法主要有萃取法、吸附法、层析法以及色谱法等。本文对每种方法的原理及应用效果进行简要综述。
3.1 多酚富集
3.1.1 萃取法
萃取法是利用多酚于不同溶剂中溶解度存在明显差异来进行分离,是一种初级分离方法,可实现多酚富集。常用萃取溶剂主要有正丁醇、乙酸乙酯、石油醚等。卢连香等[41]采用正丁醇来对乙醇醇沉粗提液进行纯化,发现正丁醇相的甘蔗叶总黄酮含量明显高于水相。Zheng等[42]分别采用石油醚、乙酸乙酯和正丁醇来对甘蔗渣乙醇粗提物进行萃取,发现乙酸乙酯馏分(EAF)的总酚和总黄酮含量均显著高于石油醚馏分(PEF)和正丁醇馏分(BuF),且氧化自由基吸收能力也显著强于PEF、BuF和阳性对照VC。Feng等[19]对比研究乙酸乙酯萃取法和大孔树脂吸附法对甘蔗多酚的纯化效果,发现乙酸乙酯萃取法更具有优势。
3.1.2 吸附法
吸附法是利用酚类物质与固体吸附剂之间的相互作用力,使之与吸附剂结合,从而达到分离纯化的目的[43]。由于大孔树脂吸附法具有选择性好、理化性质稳定、操作简单且易再生等优势,目前常被用于甘蔗多酚的纯化。区惠敏等[44]对比了XAD-5、AB-8、NKA-9和D101四种树脂对甘蔗多酚的吸附和解吸性能,发现NKA-9效果最优:吸附量达49.22 mg/g,分别是相同条件下XAD-5、AB-8和D101的1.17倍、2.51倍、2.73倍;2 h解吸率达74.51%,分别比相同条件下XAD-5、AB-8和D101提高了近2.36%、31.51%、33.1%。Ou等[45]在使用活性炭对甘蔗渣中阿魏酸进行富集研究中发现,粉末活性炭对阿魏酸吸附能力显著优于颗粒活性炭,能回收极低浓度的阿魏酸。
3.2 多酚组分分离
上述萃取法和吸附法对多酚纯化主要作用是实现多酚的富集,需要对其进一步分离纯化才可能获得高纯度多酚物质。目前甘蔗多酚的纯化研究主要采用层析法和色谱法。
3.2.1 层析法
层析法是利用不同组分理化性质的差异,使各组分在固定相和流动相间分配系数不同,从而达到分离纯化的目的[46]。目前层析法常用的填料有葡聚糖凝胶、聚酰胺树脂、硅胶等,填料的选择主要根据多酚的极性强弱来进行确定,如硅胶适用于分离极性大的酚类化合物。Sun等[47]先采用硅胶柱对甘蔗多酚进行纯化,获得25个馏分,再使用葡聚糖凝胶(LH-20)进一步纯化,共获得8种酚类化合物。李思佳等[48]使用聚酰胺柱对甘蔗多酚进行纯化,甘蔗多酚纯度可达到86.15%。Ou等[49]采用阴离子交换树脂对蔗渣碱水解物中的香豆酸进行纯化,香豆酸纯度达89.7%。
3.2.2 色谱法
色谱法是利用待分离物质不同组分在固定相与流动相中分配系数、吸附能力等亲和能力的不同来实现分离的。目前,色谱法常用于甘蔗酚酸的分离纯化。Geng等[50]应用固相在线萃取-高速逆流色谱(HSCCC)新工艺,从甘蔗果皮粗提物分离香豆酸和阿魏酸,纯度分别可达95.4%和84%。Fang等[51]建立了一种基于pH-区带逆流色谱技术的甘蔗皮酚酸分离方法,其中咖啡酸、阿魏酸和对香豆酸三种酚酸的纯度分别达到93.4%、94.6%和98.8%。
随着甘蔗多酚在食品、保健、医药及化妆品等领域应用日益广泛,其分离纯化研究成为重点内容。上述纯化方法存在产品纯度低或成本高等问题。为了提高多酚的纯度,降低操作成本,纯化过程应当是选择性的和可逆的,如在线实时监测实现纯化操作与检测同步进行,溶剂回收以降低成本。
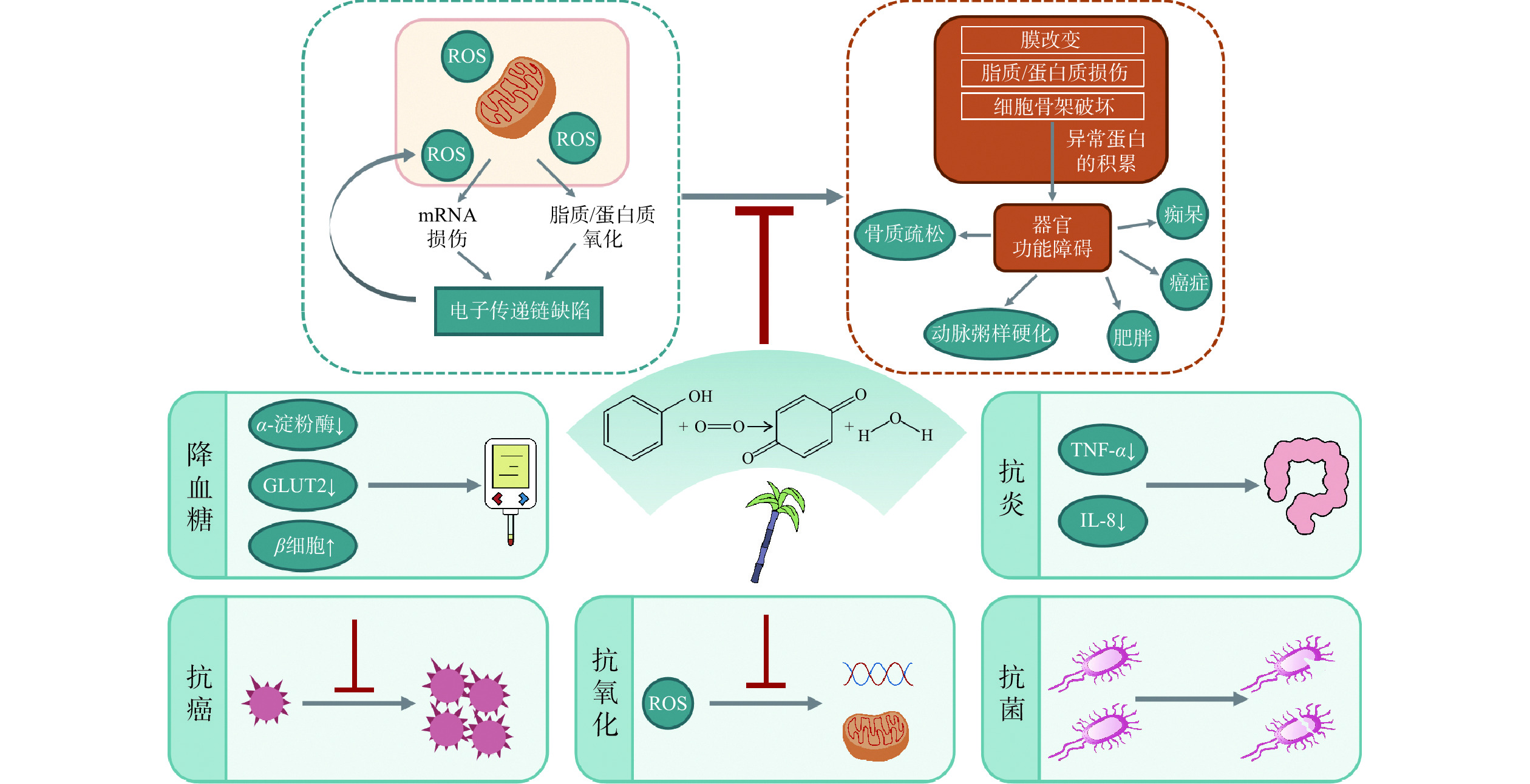
4. 甘蔗多酚的生物活性
多酚因其具有多羟基结构,能中和体内自由基,使自由基还原成为稳定的物质,从而有效地防止自由基连锁反应,延缓或抑制多种疾病[52−54]。大量研究表明,甘蔗多酚具有抗氧化、降血糖、抗炎、抗癌、抗菌等多种生物活性(图2)。
4.1 抗氧化活性
活性氧(ROS)是一种具有细胞内信使功能的自由基,可以调节生物系统内的多种机制,在机体中扮演着“双刃剑”的角色[55−56]。近年来的研究表明,ROS在破坏癌细胞中发挥关键作用[57−59]。然而,当机体在物理、化学、生物等应激作用下,会产生大量ROS并积蓄,导致机体无法依靠自身的防御系统来维持ROS平衡,则机体内氧化系统发生失衡,进而引发机体氧化损伤,体内蛋白质、核酸、脂类等生物分子遭到破坏,从而诱发一系列生理性病变[60−61]。因此,清除体内过量的自由基和抑制大量自由基的生成对人体而言至关重要。
研究表明,甘蔗多酚具有良好的自由基清除能力。Zheng等[62]通过比较研究发现,甘蔗渣多酚的氧自由基吸收能力(ORAC)(10860 μmol TE/g)显著高于VC(10213 μmol TE/g)。甘蔗酚类提取物抗氧化能力的强弱与多酚、黄酮等含量息息相关。Deseo等[63]发现纯化后的甘蔗糖蜜多酚的ABTS+自由基清除率、ORAC值、细胞抗氧化活性(CAA)分别是粗提物的约30倍、12倍和2.5倍。Asikin等[64]研究发现纯化后的糖蜜多酚活性达到原蔗汁的200倍。相对于蔗汁而言,甘蔗糖蜜因蒸发浓缩效应,其酚类化合物含量更高,因此被认为是抗氧化剂的优质原料。
甘蔗多酚作为一种天然的、具有优越抗氧化活性的抗氧化剂,还具有来源丰富、绿色、安全等优势,应用前景广阔。但是,目前关于甘蔗多酚抗氧化活性的研究仍聚焦于体外,为了进一步了解甘蔗多酚的抗氧化功能,还需要开展体内研究来深入分析其抗氧化作用机制,以期为其后期开发利用提供理论依据。
4.2 降血糖活性
糖尿病是一种代谢性疾病,其特点是由于胰岛素分泌不足和糖代谢功能障碍而导致血糖水平异常升高[65−66]。研究表明,长期处于高血糖状态会使机体积蓄活性氧(ROS),会改变酶活性和降低体内抗氧化水平,从而导致糖尿病发生[67−68]。因此,富含抗氧化剂的天然资源,可能在糖尿病的治疗中发挥关键作用。
研究显示,甘蔗多酚具有优越的降血糖活性,其降糖能力显著优于罗格列酮[62]。甘蔗多酚通过抑制碳水化合物水解酶活性来减少人体吸收。Huang等[69]研究发现甘蔗糖蜜酒精废液中的丁香酸能够有效抑制α-葡萄糖苷酶,2-羟基-5-甲氧基苯甲酸和龙胆酸对α-淀粉酶表现出较强的抑制作用。Zheng等[62]发现甘蔗渣多酚对蔗糖酶和麦芽糖酶有较强的抑制作用。此外,甘蔗多酚可以通过抑制果糖和葡萄糖转运体GLUT2来抑制人体吸收,还可以使功能失调的β细胞的胰岛素生成水平恢复[65]。
甘蔗多酚是一种天然活性成分,其与目前被临床应用于糖尿病治疗的药物不同的是,对胃肠道的副作用较小[70]。虽然目前的研究已经揭示了甘蔗多酚降血糖功能的部分作用机制,但仍有可能存在其他潜在机制,如微生物组或其他细胞通路的作用,因此需要进一步开展研究来补充完善。
4.3 抗炎活性
炎症反应是机体内一种重要的自我防御机制,是由一系列的传感器和效应器介导的,包括受体、信号级联和分泌的效应器蛋白。甘蔗多酚具有较好的抗炎活性,其作用机制主要是抑制促炎因子的形成。Bucio-Noble等[11]利用结肠癌细胞炎症模型研究发现,富含多酚的甘蔗乙醇提取物通过抑制NFκB的磷酸化,减少促炎细胞因子IL-8的分泌,从而达到抗炎的功效。Ji等[71]研究发现富含多酚的甘蔗提取物通过抑制促炎细胞因子TNF-α的表达,激活Nrf2-ARE转录途径来起到抗炎功效。此外,研究表明炎症与氧化应激密切相关。氧化应激能够导致信号转导增强,从而激活促炎细胞因子。因此,甘蔗多酚的抗炎活性可能是因为其优越的抗氧化活性。
目前甘蔗多酚抗炎活性的研究主要聚焦于对促炎因子表达的抑制,而对抗炎细胞因子的影响研究较少,因此,还需要从不同角度深入开展研究,明晰甘蔗多酚抗炎作用机理。
4.4 抗癌活性
癌症是人类致死的重要原因之一。目前抗癌药物的作用机制包括抑制癌细胞增殖或杀死癌细胞以及调节机体免疫力等。大量研究显示甘蔗多酚具有较好的抑制癌细胞增殖活性。Zheng等[42]从甘蔗渣中分离得到的单体酚(木犀草素、对香豆酸和原儿茶酸)对人乳腺癌MCF-7细胞具有良好的抗增殖活性。Lee等[72]发现富含多酚的甘蔗叶水提物能够诱导肝癌HepG2细胞的凋亡。赵毅[21]研究发现甘蔗多酚对CACO-2结肠癌细胞和HepG2肝癌细胞生长均有较好的抑制作用;甘蔗多酚通过上调促凋亡蛋白Bax的表达和下调抗凋亡蛋白Bcl-2的表达来抑制HepG2肝癌细胞的生长,而对CACO-2结肠癌细胞增殖的抑制机理并未详细阐述。
目前关于甘蔗多酚抗癌活性的研究仅局限于少数几种癌细胞,对肺癌细胞系(A59)、宫颈癌细胞系(HeLa)等高发的、常见的癌细胞生长的影响尚未有研究报道。此外,目前研究的重点仍为抗癌效果,其抗癌作用机理尚不清晰。因此,后续研究应聚焦于甘蔗多酚对不同癌细胞增殖的影响及其抗癌机理。
4.5 抗菌活性
研究显示,甘蔗多酚对几种常见的食源性致病菌具有良好的抑制作用。Juttuporn等[73]发现甘蔗渣多酚对金黄色葡萄球菌和大肠杆菌的生长具有抑制效果。Zhao等[74]研究发现富含酚类化合物的甘蔗渣提取物对金黄色葡萄球菌、单核增生李斯特菌、大肠杆菌和鼠伤寒沙门氏菌均具有显著的抑菌活性。甘蔗多酚与细菌细胞膜蛋白相互作用,破坏细胞结构,导致内部细胞质成分泄露,从而达到抑制细菌生长的作用。
相较于抗氧化、降血糖、抗炎活性等方面的研究,目前关于甘蔗多酚抗菌活性的研究信息十分有限。上述研究表明甘蔗多酚对细菌具有较强的抑制能力,但对霉菌、酵母等真菌生长的影响尚未报道。因此,还需要通过深入研究来加强甘蔗多酚抗菌活性的理论支撑。
综上所述,甘蔗多酚作为一种具有多种功效的活性成分,在治疗慢性病方面具有巨大的潜力。但是,目前甘蔗多酚活性机制尚未完全明晰。因此在研究拓宽甘蔗多酚功能活性广度的同时,也应当强化深度研究,如进一步探索甘蔗多酚结构与功能内在关联,并解析相应构效关系等。此外,甘蔗多酚的剂量研究也是其应用于慢性病治疗必不可少的一环。
5. 结语与展望
甘蔗多酚具有抗氧化、降血糖、抗炎、抗癌等多种生物学活性,在食品、医药领域具有广阔的应用前景。但是目前甘蔗多酚的提取和纯化方法较为传统,提取效率较低、安全性较差。甘蔗多酚虽然具有良好的生物学活性,但是关于其活性作用机制的研究尚未明晰。为贯彻绿色低碳环保理念,充分利用甘蔗资源,发挥甘蔗多酚的功效活性,提出以下几点展望:a.研究深共晶溶剂等绿色溶剂以及超临界流体萃取等新型技术在甘蔗多酚提取上的可行性,以实现甘蔗多酚的绿色高效提取。b.参考其它天然产物的纯化方法,如膜分离技术等,研究并分析其在甘蔗多酚纯化应用的可行性;同时以“在高纯度与低成本之间建立平衡点”为原则开发一种甘蔗多酚分离纯化新方法。c.进一步开展甘蔗多酚活性的体内研究,为现有的甘蔗多酚生物活性提供强有力的证据支持;明晰甘蔗多酚的组成、分子结构及其构效关系,深入分析甘蔗多酚活性作用机制;挖掘甘蔗多酚在活性方面更多的可能性,拓宽甘蔗多酚的应用领域。
-
-
[1] WANG J, XIAO X M, LIU L, et al. Mapping sugarcane plantation dynamics in Guangxi, China, by time series Sentinel-1, Sentinel-2 and Landsat images[J]. Remote Sensing of Environment,2020,247:111951. doi: 10.1016/j.rse.2020.111951
[2] ALI S E, YUAN Q, WANG S P, et al. More than sweet:A phytochemical and pharmacological review of sugarcane (Saccharum officinarum L.)[J]. Food Bioscience, 2021, 44 (Part B):101431.
[3] KHARE C P. Indian medicinal plants:An illustrated dictionary[M]. Berlin/Heidelberg:Springer-Verlag and Springer Science &Business Media, 2008:567.
[4] SINGH A, LAL U R, MUKHTAR H M, et al. Phytochemical profile of sugarcane and its potential health aspects[J]. Pharmacognosy Reviews,2015,9(17):45−54. doi: 10.4103/0973-7847.156340
[5] LIU L M, GUO P S, WANG P X, et al. The review of anti-aging mechanism of polyphenols on caenorhabditis elegans[J]. Frontiers in Bioengineering and Biotechnology,2021,9:635768. doi: 10.3389/fbioe.2021.635768
[6] GANDHI G R, VASCONCELOS A B S, WU D T, et al. Citrus flavonoids as promising phytochemicals targeting diabetes and related complications:A systematic review of in vitro and in vivo studies[J]. Nutrients,2020,12(10):2907. doi: 10.3390/nu12102907
[7] TRUONG V L, JEONG W S. Antioxidant and anti-inflammatory roles of tea polyphenols in inflammatory bowel diseases[J]. Food Science and Human Wellness,2022,11(3):502−511. doi: 10.1016/j.fshw.2021.12.008
[8] HUANG X X, WANG Y, YANG W H, et al. Regulation of dietary polyphenols on cancer cell pyroptosis and the tumor immune microenvironment[J]. Frontiers in Nutrition,2022,9:974896. doi: 10.3389/fnut.2022.974896
[9] WILLIAMS I O, ONYENWEAKU E O, ATANGWHO I J. Nutritional and antimicrobial evaluation of Saccharum officinarum consumed in Calabar, Nigeria[J]. African Journal of Biotechnology,2016,15(33):1789−1795. doi: 10.5897/AJB2015.14877
[10] 郑瑞. 甘蔗多酚抗氧化、降血糖、抗肿瘤细胞增殖活性研究[D]. 广州:华南理工大学, 2017. [ZHENG Rui. Research on the antioxidant, antihyperglycemic and antiproliferative activities of phenolics from sugarcane (Saccharum officinarum L.)[D]. Guangzhou:South China University of Technology, 2017.] ZHENG Rui. Research on the antioxidant, antihyperglycemic and antiproliferative activities of phenolics from sugarcane (Saccharum officinarum L.)[D]. Guangzhou: South China University of Technology, 2017.
[11] BUCIO-NOBLE D, KAUTTO L, KRISP C, et al. Polyphenol extracts from dried sugarcane inhibit inflammatory mediators in an in vitro colon cancer model[J]. Journal of Proteomics,2018,177:1−10. doi: 10.1016/j.jprot.2018.02.009
[12] KADAM U S, GHOSH S B, DE S, et al. Antioxidant activity in sugarcane juice and its protective role against radiation induced DNA damage[J]. Food Chemistry,2008,106(3):1154−1160. doi: 10.1016/j.foodchem.2007.07.066
[13] AKOWUAH G A, ISMAIL Z, NORHAYATI I, et al. The effects of different extraction solvents of varying polarities on polyphenols of Orthosiphon starnineus and evaluation of the free radical-scavenging activity[J]. Food Chemistry,2005,93(2):311−317. doi: 10.1016/j.foodchem.2004.09.028
[14] HU Y Y, YAN B, CHEN Z S, et al. Recent technologies for the extraction and separation of polyphenols in different plants:A review[J]. Journal of Renewable Materials,2022,10(6):1471−1490. doi: 10.32604/jrm.2022.018811
[15] 孙晓雪. 甘蔗梢中酚类物质的提取与应用研究[D]. 南宁:广西大学, 2007. [SUN Xiaoxue. Study on extraction and application of polyphenol in sugarcane tip[D]. Nanning:Guangxi University, 2007.] SUN Xiaoxue. Study on extraction and application of polyphenol in sugarcane tip[D]. Nanning: Guangxi University, 2007.
[16] 闫怀锋, 赵振刚. 甘蔗皮花色苷的提取及辅色剂对花色苷的辅色作用研究[J]. 现代食品科技,2017,33(9):176−182,108. [YAN Huaifeng, ZHAO Zhengang. Extraction of anthocyanins from sugarcane rind and co-pigmentation effect of co-pigments on anthocyanins[J]. Modern Food Science and Technology,2017,33(9):176−182,108.] YAN Huaifeng, ZHAO Zhengang. Extraction of anthocyanins from sugarcane rind and co-pigmentation effect of co-pigments on anthocyanins[J]. Modern Food Science and Technology, 2017, 33(9): 176−182,108.
[17] VINATORU M. An overview of the ultrasonically assisted extraction of bioactive principles from herbs[J]. Ultrasonics Sonochemistry,2001,8(3):303−313. doi: 10.1016/S1350-4177(01)00071-2
[18] FEKI F, KLISUROVA D, MASMOUDI M A, et al. Optimization of microwave assisted extraction of simmondsins and polyphenols from jojoba (Simmondsia chinensis) seed cake using Box-Behnken statistical design[J]. Food Chemistry,2021,356:129670. doi: 10.1016/j.foodchem.2021.129670
[19] FENG S M, LUO Z S, TAO B P, et al. Ultrasonic-assisted extraction and purification of phenolic compounds from sugarcane (Saccharum officinarum L.) rinds[J]. LWT - Food Science and Technology,2015,60(2):970−976. doi: 10.1016/j.lwt.2014.09.066
[20] 阎欲晓, 吴国燕, 杨龙, 等. 甘蔗叶多酚物质的超声提取及生理活性研究[J]. 食品研究与开发,2012,33(4):63−66. [YAN Yuxiao, WU Guoyan, YANG Long, et al. Ultrasonic-assisted extraction and physiological activities of polyphenols from sugar cane leaves[J]. Food Research and Development,2012,33(4):63−66.] doi: 10.3969/j.issn.1005-6521.2012.04.017 YAN Yuxiao, WU Guoyan, YANG Long, et al. Ultrasonic-assisted extraction and physiological activities of polyphenols from sugar cane leaves[J]. Food Research and Development, 2012, 33(4): 63−66. doi: 10.3969/j.issn.1005-6521.2012.04.017
[21] 赵毅. 甘蔗多酚分离鉴定及生物活性研究[D]. 广州:华南理工大学, 2015. [ZHAO Yi. Study on isolation and identification of sugarcan polyphenols and their biological activity[D]. Guangzhou:South China University of Technology, 2015.] ZHAO Yi. Study on isolation and identification of sugarcan polyphenols and their biological activity[D]. Guangzhou: South China University of Technology, 2015.
[22] 韦巧艳, 李小梅, 覃逸明, 等. 微波辅助提取甘蔗叶总黄酮的工艺优化及其抗氧化性[J]. 饲料研究,2021,44(7):92−97. [WEI Qiaoyan, LI Xiaomei, QIN Yiming, et al. Optimization of microwave-assisted extraction of total flavonoids from sugarcane leaves and its antioxidant activities evaluation[J]. Feed Research,2021,44(7):92−97.] WEI Qiaoyan, LI Xiaomei, QIN Yiming, et al. Optimization of microwave-assisted extraction of total flavonoids from sugarcane leaves and its antioxidant activities evaluation[J]. Feed Research, 2021, 44(7): 92−97.
[23] 杨谷良, 黄春保, 潘敏雄, 等. 甘蔗多酚对胆固醇诱导高血脂大鼠的影响[J]. 江西农业大学学报,2017,39(5):996−1001. [YANG Guliang, HUANG Chunbao, PAN Minxiong, et al. The influence of sugarcane polyphenols on cholesterol-induced hyperlipidemia rat[J]. Acta Agriculturae Universitatis Jiangxiensis,2017,39(5):996−1001.] YANG Guliang, HUANG Chunbao, PAN Minxiong, et al. The influence of sugarcane polyphenols on cholesterol-induced hyperlipidemia rat[J]. Acta Agriculturae Universitatis Jiangxiensis, 2017, 39(5): 996−1001.
[24] GUHA A K, GOKHALE S. Urban workers' cardiovascular health due to exposure to traffic-originated PM2.5 and noise pollution in different microenvironments[J]. Science of the Total Environment, 2023, 859(Part 1):160268.
[25] JAUCHEM J R. A literature review of medical side effects from radio-frequency energy in the human environment:Involving cancer, tumors, and problems of the central nervous system[J]. Journal of Microwave Power and Electromagnetic Energy,2003,38(2):103−123. doi: 10.1080/08327823.2003.11688492
[26] 张思原, 黄慧玲, 周永升, 等. 二次回归正交旋转组合设计优化复合酶法提取甘蔗梢多酚工艺[J]. 南方农业学报,2016,47(3):459−465. [ZHANG Siyuan, HUANG Huiling, ZHOU Yongsheng, et al. Optimization for compound enzymatic extraction process of polyphenols from sugarcane top by quadratic regression orthogonal rotation combination design[J]. Journal of Southern Agriculture,2016,47(3):459−465.] doi: 10.3969/j:issn.2095-1191.2016.03.459 ZHANG Siyuan, HUANG Huiling, ZHOU Yongsheng, et al. Optimization for compound enzymatic extraction process of polyphenols from sugarcane top by quadratic regression orthogonal rotation combination design[J]. Journal of Southern Agriculture, 2016, 47(3): 459−465. doi: 10.3969/j:issn.2095-1191.2016.03.459
[27] MUSTAFA A, TURNER C. Pressurized liquid extraction as a green approach in food and herbal plants extraction:A review[J]. Analytica Chimica Acta,2011,703(1):8−18. doi: 10.1016/j.aca.2011.07.018
[28] DOBROSLAVI´C E, GAROFULI´C I E, ŠEPAROVI´C J, et al. Pressurized liquid extraction as a novel technique for the isolation of Laurus nobilis L. leaf polyphenols[J]. Molecules,2022,27(16):5099. doi: 10.3390/molecules27165099
[29] DOMÍNGUEZ-RODRÍGUEZ G, GARCÍA M C, MARINA M L, et al. Pressurized liquid extraction combined with enzymatic-assisted extraction to obtain bioactive non-extractable polyphenols from sweet cherry (Prunus avium L.) pomace[J]. Nutrients,2021,13(9):3242. doi: 10.3390/nu13093242
[30] MARTÍN E G, HERNÁNDEZ T F, ROMERO A, et al. Influence of the extraction method on the recovery of bioactive phenolic compounds from food industry by-products[J]. Food Chemistry,2022,378:131918. doi: 10.1016/j.foodchem.2021.131918
[31] DA PORTO C, NATOLINO A. Supercritical fluid extraction of polyphenols from grape seed (Vitis vinifera):Study on process variables and kinetics[J]. The Journal of Supercritical Fluids,2017,130:239−245. doi: 10.1016/j.supflu.2017.02.013
[32] SARMENTO L A V, MACHADO R A F, PETRUS J C C, et al. Extraction of polyphenols from cocoa seeds and concentration through polymeric membranes[J]. The Journal of Supercritical Fluids,2008,45(1):64−69. doi: 10.1016/j.supflu.2007.11.007
[33] DA PORTO C, DECORTI D, NATOLINO A. Application of a supercritical CO2 extraction procedure to recover volatile compounds and polyphenols from Rosa damascena[J]. Separation Science and Technology,2015,50(8):1175−1180. doi: 10.1080/01496395.2014.965833
[34] PHAN L T M, NGUYEN K T P, VUONG H T, et al. Supercritical fluid extraction of polyphenols from Vietnamese Callisia fragrans leaves and antioxidant activity of the extract[J]. Journal of Chemistry,2020,2020(11):9548401.
[35] PUÉRTOLAS E, CREGENZÁN O, LUENGO E, et al. Pulsed-electric-field-assisted extraction of anthocyanins from purple-fleshed potato[J]. Food Chemistry,2013,136(3-4):1330−1336. doi: 10.1016/j.foodchem.2012.09.080
[36] ATHANASIADIS V, LAKKA A, PALAIOGIANNIS D, et al. Pulsed electric field and Salvia officinalis L. leaves:A successful combination for the extraction of high value added compounds[J]. Foods,2021,10(9):2014. doi: 10.3390/foods10092014
[37] LAKKA A, BOZINOU E, STAVROPOULOS G, et al. Enhancement of polyphenols recovery from Rosa canina, Calendula officinalis and Castanea sativa using pulsed electric field[J]. Beverages,2021,7(3):63. doi: 10.3390/beverages7030063
[38] BOATENG I D. Evaluating the status quo of deep eutectic solvent in food chemistry. Potentials and limitations[J]. Food Chemistry,2023,406:135079. doi: 10.1016/j.foodchem.2022.135079
[39] LIU Y X, ZHE W, ZHANG R F, et al. Ultrasonic-assisted extraction of polyphenolic compounds from Paederia scandens (Lour.) Merr. using deep eutectic solvent:Optimization, identification, and comparison with traditional methods[J]. Ultrasonics Sonochemistry,2022,86:106005. doi: 10.1016/j.ultsonch.2022.106005
[40] OZTURKA B, PARKINSONA C, MIQUEL M G. Extraction of polyphenolic antioxidants from orange peel waste using deep eutectic solvents[J]. Separation and Purification Technology,2018,206:1−13. doi: 10.1016/j.seppur.2018.05.052
[41] 卢连香, 丁世磊, 杨方方, 等. 甘蔗叶总黄酮超声辅助离子液体提取工艺及其纯化研究[J]. 饲料研究,2022,45(14):95−99. [LU Lianxiang, DING Shilei, YANG Fangfang, et al. Ultrasonic-assisted ionic liquid extraction and purification of total flavonoids from sugarcane leaves[J]. Feed Research,2022,45(14):95−99.] LU Lianxiang, DING Shilei, YANG Fangfang, et al. Ultrasonic-assisted ionic liquid extraction and purification of total flavonoids from sugarcane leaves[J]. Feed Research, 2022, 45(14): 95−99.
[42] ZHENG R, SU S, LI J B, et al. Recovery of phenolics from the ethanolic extract of sugarcane (Saccharum officinarum L.) baggase and evaluation of the antioxidant and antiproliferative activities[J]. Industrial Crops & Products,2017,107:360−369.
[43] KAMMERER J, BOSCHET J, KAMMERER D R, et al. Enrichment and fractionation of major apple flavonoids, phenolic acids and dihydrochalcones using anion exchange resins[J]. LWT-Food Science and Technology,2011,44(4):1079−1087. doi: 10.1016/j.lwt.2010.10.008
[44] 区惠敏, 郭娟, 龚玉石, 等. 甘蔗渣多酚的纯化及抗氧化活性研究[J]. 现代食品科技,2013,29(7):1596−1600,1590. [OU Huimin, GUO Juan, GONG Yushi, et al. Purification and antioxidant activity of sugarcane pomace polyphenols[J]. Modern Food Science and Technology,2013,29(7):1596−1600,1590.] OU Huimin, GUO Juan, GONG Yushi, et al. Purification and antioxidant activity of sugarcane pomace polyphenols[J]. Modern Food Science and Technology, 2013, 29(7): 1596−1600,1590.
[45] OU S Y, LUO Y L, XUE F, et al. Seperation and purification of ferulic acid in alkaline-hydrolysate from sugarcane bagasse by activated charcoal adsorption/anion macroporous resin exchange chromatography[J]. Journal of Food Engineering,2007,78(4):1298−1304. doi: 10.1016/j.jfoodeng.2005.12.037
[46] 郑百良. 谷糠酚类物质提取、分离及活性研究[D]. 洛阳:河南科技大学, 2022. [ZHENG Bailiang. Study on extraction, separation and activity of polyphenols from foxtail millet bran[D]. Luoyang:Henan University of Science and Technology, 2022.] ZHENG Bailiang. Study on extraction, separation and activity of polyphenols from foxtail millet bran[D]. Luoyang: Henan University of Science and Technology, 2022.
[47] SUN J, HE X M, ZHAO M M, et al. Antioxidant and nitrite-scavenging capacities of phenolic compounds from sugarcane (Saccharum officinarum L.) tops[J]. Molecules,2014,19(9):13147−13160. doi: 10.3390/molecules190913147
[48] 李思佳, 孙卫东, 张业辉, 等. 蔗梢中多酚化合物的分离纯化及对冷鲜肉的保鲜作用[J]. 食品工业,2020,41(1):172−175. [LI Sijia, SUN Weidong, ZHANG Yehui, et al. Separation and purification of polyphenols from sugarcane top and freshness of cold meat[J]. The Food Industry,2020,41(1):172−175.] LI Sijia, SUN Weidong, ZHANG Yehui, et al. Separation and purification of polyphenols from sugarcane top and freshness of cold meat[J]. The Food Industry, 2020, 41(1): 172−175.
[49] OU S Y, LUO Y L, HUANG C H, et al. Production of coumaric acid from sugarcane bagasse[J]. Innovative Food Science and Emerging Technologies,2009,10(2):253−259. doi: 10.1016/j.ifset.2008.10.008
[50] GENG P, FANG Y T, XIE R L, et al. Separation of phenolic acids from sugarcane rind by online solid-phase extraction with high-speed counter-current chromatography[J]. Journal of Separation Science,2017,40(4):991−998. doi: 10.1002/jssc.201600887
[51] FANG Y T, LI Q, CAO A C, et al. Isolation and purification of phenolic acids from sugarcane (Saccharum officinarum L.) rinds by pH-zone-refining counter-current chromatography and their antioxidant activity evaluation[J]. Food Analytical Methods,2017,10:2576−2584. doi: 10.1007/s12161-017-0824-3
[52] 洪鑫月, 吴健妹, 罗小乔, 等. 多酚化合物对黄嘌呤氧化酶抑制作用的研究进展[J]. 食品与机械,2021,37(2):1−8. [HONG Xinyue, WU Jianmei, LUO Xiaoqiao, et al. Research progress of inhibitory effects of polyphenolic compounds on xanthine oxidase[J]. Food & Machinery,2021,37(2):1−8.] HONG Xinyue, WU Jianmei, LUO Xiaoqiao, et al. Research progress of inhibitory effects of polyphenolic compounds on xanthine oxidase[J]. Food & Machinery, 2021, 37(2): 1−8.
[53] 曲敏, 陈强, 孙冰玉, 等. 多酚的功能性质及与蛋白质、多糖相互作用研究进展[J]. 食品工业科技,2021,42(11):405−413. [QU Min, CHEN Qiang, SUN Bingyu, et al. Advances in studies on the functional properties of polyphenols and their interactions with proteins and polysaccharides[J]. Science and Technology of Food Industry,2021,42(11):405−413.] QU Min, CHEN Qiang, SUN Bingyu, et al. Advances in studies on the functional properties of polyphenols and their interactions with proteins and polysaccharides[J]. Science and Technology of Food Industry, 2021, 42(11): 405−413.
[54] BERNATONIENE J, KOPUSTINSKIENE D M. The role of catechins in cellular responses to oxidative stress[J]. Molecules,2018,23(4):965−976. doi: 10.3390/molecules23040965
[55] SAUER H, WARTENBERG M, HESCHELER J. Reactive oxygen species as intracellular messengers during cell growth and differentiation[J]. Cellular Physiology and Biochemistry,2001,11(4):173−186. doi: 10.1159/000047804
[56] HALLIWELL B. Reactive oxygen species in living systems:Source, biochemistry, and role in human disease[J]. The American Journal of Medicine,1991,91(3):S14−S22. doi: 10.1016/0002-9343(91)90279-7
[57] CHEUNG E C, VOUSDEN K H. The role of ROS in tumour development and progression[J]. Nature Reviews Cancer,2022,22:280−297. doi: 10.1038/s41568-021-00435-0
[58] SAHOO B M, BANIK B K, BORAH P, et al. Reactive oxygen species (ROS):Key components in cancer therapies[J]. Anti-Cancer Agents in Medicinal Chemistry,2022,22(2):215−222. doi: 10.2174/1871520621666210608095512
[59] ARFIN S, JHA N K, JHA S K, et al. Oxidative stress in cancer cell metabolism[J]. Antioxidants,2021,10(5):642. doi: 10.3390/antiox10050642
[60] PHULL A R, NASIR B, HAQ I U, et al. Oxidative stress, consequences and ROS mediated cellular signaling in rheumatoid arthritis[J]. Chemico-Biological Interactions,2018,281:121−136. doi: 10.1016/j.cbi.2017.12.024
[61] TAN B L, NORHAIZAN M E, LIEW W P P, et al. Antioxidant and oxidative stress:A mutual interplay in age-related diseases[J]. Frontiers in Pharmacology,2018,9:1162. doi: 10.3389/fphar.2018.01162
[62] ZHENG R, SU S, ZHOU H F, et al. Antioxidant/antihyperglycemic activity of phenolics from sugarcane (Saccharum officinarum L.) bagasse and identification by UHPLC-HR-TOFMS[J]. Industrial Crops and Products,2017,101:104−114. doi: 10.1016/j.indcrop.2017.03.012
[63] DESEO M A, ELKINSA A, ROCHFORTA S, et al. Antioxidant activity and polyphenol composition of sugarcane molasses extract[J]. Food Chemistry,2020,314:126180. doi: 10.1016/j.foodchem.2020.126180
[64] ASIKIN Y, TAKAHASHI M, MISHIMA T, et al. Antioxidant activity of sugarcane molasses against 2, 2’-azobis(2-amidinopropane) dihydrochloride-induced peroxyl radicals[J]. Food Chemistry,2013,141(1):466−472. doi: 10.1016/j.foodchem.2013.03.045
[65] JI J, YANG X, FLAVEL M, et al. Antioxidant and anti-diabetic functions of a polyphenol-rich sugarcane extract[J]. Journal of the American College of Nutrition,2019,38(8):670−680. doi: 10.1080/07315724.2019.1587323
[66] SHEN W, XU Y, LU Y. Inhibitory effects of citrus flavonoids on starch digestion and antihyperglycemic effects in HepG2 cells[J]. Journal of Agricultural and Food Chemistry,2012,60(38):9609−9619. doi: 10.1021/jf3032556
[67] MOHAN Y, JESUTHANKARAJ G N, RAMASAMY N, et al. Antidiabetic and antioxidant properties of Triticum aestivum in streptozotocin-induced diabetic rats[J]. Advances in Pharmacological and Pharmaceutical Sciences,2013,2013:716073.
[68] KANG M H, LEE M S, CHOI M K, et al. Hypoglycemic activity of Gymnema sylvestre extracts on oxidative stress and antioxidant status in diabetic rats[J]. Journal of Agricultural and Food Chemistry,2012,60(10):2517−2524. doi: 10.1021/jf205086b
[69] HUANG Z, CHEN Y N, HUANG R M, et al. Identification and structure-activity relationship of recovered phenolics with antioxidant and antihyperglycemic potential from sugarcane molasses vinasse[J]. Foods,2022,11(19):3131. doi: 10.3390/foods11193131
[70] ALI S E, GEDAILY R A E, MOCAN A, et al. Profiling metabolites and biological activities of sugarcane (Saccharum officinarum Linn.) juice and its product molasses via a multiplex metabolomics approach[J]. Molecules,2019,24(5):934. doi: 10.3390/molecules24050934
[71] JI J, FLAVEL M, YANG X, et al. A polyphenol rich sugarcane extract as a modulator for inflammation and neurological disorders[J]. Pharma Nutrition,2020,12:100187. doi: 10.1016/j.phanu.2020.100187
[72] LEE C P, CHEN Z T, YU P Y, et al. Identification of bioactive compounds and comparison of apoptosis induction of three varieties of sugarcane leaves[J]. Journal of Functional Foods,2012,4(1):391−397. doi: 10.1016/j.jff.2012.01.011
[73] JUTTUPORN W, THIENGKAEW P, RODKLONGTAN A, et al. Ultrasound-assisted extraction of antioxidant and antibacterial phenolic compounds from steam-exploded sugarcane bagasse[J]. Sugar Tech,2018,20(5):599−608. doi: 10.1007/s12355-017-0582-y
[74] ZHAO Y, CHEN M S, ZHAO Z G, et al. The antibiotic activity and mechanisms of sugarcane (Saccharum officinarum L.) bagasse extract against food-borne pathogens[J]. Food Chemistry,2015,185:112−118. doi: 10.1016/j.foodchem.2015.03.120



























 下载:
下载:
 下载:
下载:



