A Review of Protein-Lipids/Polysaccharides as a Delivery System of Bioactives in Food: Formation Mechanism and Application
-
摘要: 一些生物活性物质因难溶于水且生物利用率较低而使其应用受限,近年来如何有效递送生物活性物质广受关注。然而,脂质、多糖和蛋白质作为常用的食品级载体基质在单独使用时往往存在局限性,限制了它们在递送系统中的有效性。蛋白质-脂质和蛋白质-多糖偶联是用于制造新型递送系统的新兴技术,相较于单一的一元载体,多元偶联物在体内具有更好的协同作用,在提高递送系统封装效率的同时提高整个系统的稳定低,从而最大限度地发挥产品功能性质和生物活性。本文主要综述了脂质、多糖和蛋白质作为递送系统的重要性和局限性,横向对比了单一基质与多复合载体基质之间的优缺点,蛋白质-脂质/多糖二元基质作为主要研究对象,对其偶联机制、方法及其在营养递送中的作用优势进行了探讨,并对未来的研究方向进行了展望。Abstract: Some bioactive substances are insoluble in water and have low bioavailability, which limits their application. In recent years, how to effectively deliver bioactive substances has attracted wide attention. However, the commonly used food-grade encapsulation carriers, lipids, polysaccharides and proteins, often have limitations when used alone, which limits their effectiveness in delivery systems. Coupling protein with lipid or polysaccharide is an emerging technology for the manufacture of new delivery systems. Compared with a single carrier, these multivariate conjugates have better synergistic effects in vivo, which improves stability and encapsulation efficiency of delivery systems, and can maximize the functional properties and biological activities of products. This paper mainly reviews the importance and limitations of lipids, polysaccharides and proteins as delivery systems, and horizontally compares the advantages and disadvantages between single matrix and multi-composite carrier matrix. The coupling of protein-lipid/polysaccharide binary matrix is taken as the main research object, and the coupling mechanism, coupling method and its advantages in nutrition delivery are discussed. The future research direction is also prospected.
-
随着营养观念的健全,人们对现代食品的营养需求更加清晰全面,因此现代食品的发展趋向于加入具有健康益处的生物活性物质。生物活性物质通常从天然来源提取,包括维生素、矿物质、多酚、omega-3脂肪酸和植物甾醇等。但生物活性物质对氧气、光、热和水等环境因素敏感,不稳定性限制了相关产品深度开发和应用[1]。在补充这些生物活性物质时,普通的片剂和口服液难以保证其稳定释放和吸收,一方面因为一些疏水性物质因难溶于水导致封装困难或封装效率不高,另一方面,大部分生物活性物质在口服消化过程中,胃肠道的温度、pH等环境因素会使其化学结构发生改变,进而影响生物活性[2]。如何维持生物活性物质在胃肠道的稳定性并确保在适当的靶点处进行释放是保证其生物活性功效的决定性问题。生物活性物质递送系统是克服上述诸多问题的有力工具,其中蛋白质、脂质、多糖作为常见的输送载体,能通过共价或非共价的结合机制封装营养素,提高包埋量、生物可及性和利用度。但目前已有的一元载体存在着局限性,多元载体的出现一定程度上可以解决单一基质递送系统的问题。因此,本文主要针对蛋白质-脂质/多糖形成的生物活性物质递送系统,概述一元、多元递送载体的组成,详述了复合载体的制备方法和原理,较为系统地阐释了复合载体封装递送生物活性物质的效果及原理。
1. 生物活性物质递送系统载体基质
递送系统是将功能成分(营养素、生物活性成分)封装在载体基质内形成的复合体系,封装会增强生物活性物质的稳定性、生物可及性、吸收和转化,所有这些都有助于提高生物利用度。因此载体基质在递送系统中至关重要。载体基质可以由一种或多种食品基质构成,根据组成成分的种类丰富度,可以分成一元或二元、三元等多元输送载体基质。各递送系统载体的结构、基质构成以及优缺点如表1所示。
表 1 不同类型载体基质优缺点Table 1. Advantages and disadvantages of different types of carrier matrix基质构成 结构 缺点 优点 蛋白质 纳米纤维
纳米颗粒
水凝胶蛋白质对离子浓度、电荷、温度等环境因素
高度敏感,易变性或聚集良好的乳化性、凝胶性、
低毒性和较高的生物相容性脂质 乳液
脂质体
固体脂质纳米颗粒(SLNs)
纳米结构脂质体(NLCs)价格昂贵成本较高,酸性条件下易分解 优异的生物相容性和乳化性能 多糖 水凝胶
纳米颗粒
乳液复杂的食品体系中难以维持稳定性 来源广泛,加工成本低,结构易于修饰 二元复合载体
(蛋白-脂质基)乳液
凝胶
纳米颗粒
脂质体价格昂贵成本较高 提高疏水性活性物质的生物可及性 二元复合载体
(蛋白-多糖基)凝胶
乳液
纳米颗粒不易于封装疏水性物质 封装效率更高,稳定性强 三元复合载体基质 乳液
凝胶
纳米颗粒
脂质体制备方法复杂,成本较高 高稳定性且易于缓释,封装效率较高 1.1 一元输送载体基质
1.1.1 蛋白质基
蛋白质具有较高的营养价值,具有较好的起泡性、乳化性、凝胶性、低毒性和较高的生物相溶性等性质[3],蛋白质的表面具有与多种生物活性化合物相互作用的官能团,可促进疏水或亲水生物活性分子(例如维生素、多酚、抗氧化剂、色素)、益生菌以及易挥发气体的体内递送。递送系统中常见的蛋白质基质可以分为动物蛋白和植物蛋白[4]。动物蛋白中应用最广泛的是明胶和牛乳蛋白(即乳清蛋白、β-乳球蛋白、牛血清白蛋白、酪蛋白等)[5]。
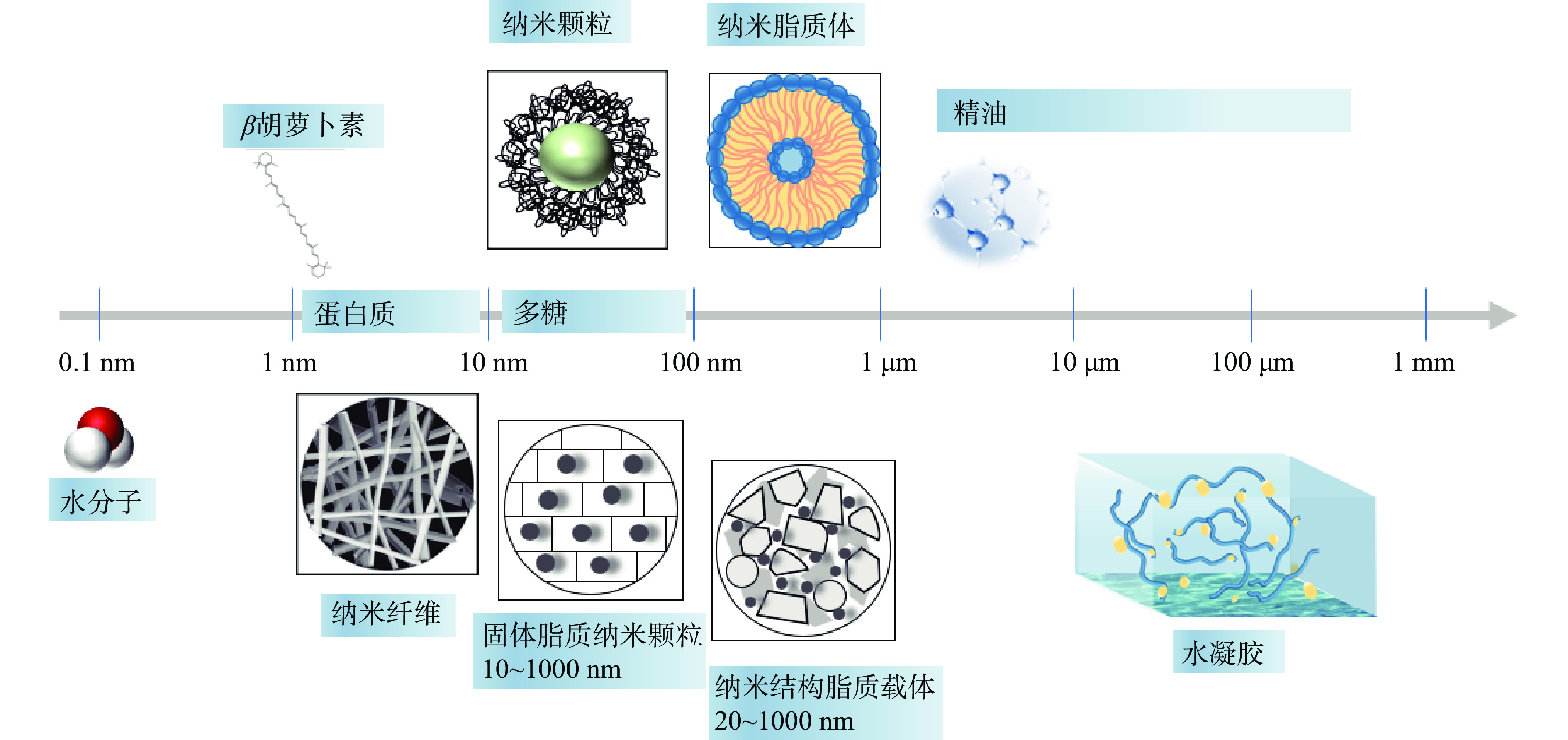
在蛋白质基递送系统中,通常以纳米纤维、纳米颗粒和水凝胶等形式包埋或吸附生物活性物质进行有效递传(如图1所示)。其中,纳米纤维广义上是指纤维直径小于1000 nm的超微细纤维[6],蛋白纳米纤维通常使用静电纺丝技术制备,是将结构性蛋白浸泡在二甲基甲酰胺等有机溶剂中,破坏其难以纺织的高级结构和相互作用力,在电场力和表面张力共同作用下不断伸长最终形成纤维结构,具有理想的生物相容性、低毒性、降解性和溶剂分解能力[7]。Deng等[8]采用杂化静电纺丝法制备了明胶/玉米醇溶蛋白纳米纤维,表现出了更好的柔韧性和疏水性,可以递送水溶性较差的生物活性物质。蛋白基纳米颗粒是直径小于1000 nm的胶体颗粒,也是聚合物纳米颗粒的一种,活性物质主要通过包裹在纳米颗粒内部或吸附在表面而进行输送[9]。例如Liu等[10]制备乳清蛋白纳米颗粒递送大豆异黄酮,结果表明乳清蛋白纳米颗粒输送载体能够显著提高大豆异黄酮的稳定性、抗氧化活性和生物可利用性。水凝胶是一种半固态复合物,由亲水性的聚合物组成的三维网络结构,其形态介于固体和液体之间,并具有固态和液态的双重性质[11],其中水是分散相,至少占凝胶总重量的70%,凝胶基质和生物活性物质作为连续相。基于生物聚合物的水凝胶往往具有较高含量的官能团,包括羟基、氨基和羧酸基团,这些官能团的存在有利于水凝胶网络的形成[1]。Cao等[12]在低电场中制备了大豆分离蛋白水凝胶,具有较好的硬度、弹性和咀嚼度以及耐溶胀性,除了能够递送活性物质外,还能够有效提高产品的感官品质。
尽管大多食品蛋白质具有物理化学功能属性,适用于封装各种亲水和疏水性生物活性化合物,但对环境因素高度敏感。例如,基于蛋白质的载体倾向于在其等电点附近、高离子强度或高于其热变性的温度下聚集,这意味着在常规的食品热加工条件下,不同的环境应力都可能会促使蛋白质变性,进而影响其功能性[13]。因此,基于蛋白质基质的输送载体在生产、储存和利用过程中蛋白质极易发生结构变化致使其实际递送效果不佳[14]。
1.1.2 脂质基
脂质具有生物可降解性、生物相容性以及优异的乳化性能,可作为营养素递送系统的载体而广泛应用于工业大规模化的生产中[15],其常用的脂质主要包括油酸、卵磷脂、亚麻酸和亚油酸等[16]。脂质作为载体基质功用繁多,既可以作为人体所需营养素,封包运载目标对象的同时,进行脂肪酸的补给;又可以作为脂质体和纳米颗粒的稳定剂,提高整个系统的稳定性;还可以提高生物可及性,延长运输时间。
常见的基于脂质的输送系统主要包括脂质体、乳液、纳米乳液、固体脂质纳米颗粒(SLNs)和纳米结构脂质载体(NLCs)[17](如图1所示)。其中,脂质体是由脂质和/或磷脂分子组成的封闭、连续的双分子层结构生物相容性囊泡[9]。Tripathy等[18]制备了大豆卵磷脂和大豆甾醇脂质体用于封装积雪草提取物,研究其稳定性,发现大豆甾醇会诱导产生较大的分子间相互作用,形成了紧凑、稳定的脂质体结构,从而可以保护内部的积雪草提取物。固体脂质纳米颗粒(SLNs)和纳米结构脂质载体(NLCs)是脂质纳米颗粒的两个种类,平均直径在50~400 nm之间,由脂质组成并由表面活性剂稳定。两者的区别在于组成的不同,SLNs仅由固体脂质组成,而NLCs中除了固体脂质通常还有液体脂质[19]。Aditya等[20]分别制备封装了槲皮素的SLNs和NLCs,研究发现槲皮素在这两个在载体中封装率都可以达到90%以上,但NLCs(~60%)比SLNs(~35%)的生物利用度高。
虽然脂质作为递送载体在性能方面具有一定的优越性,但是脂质在酸性条件下容易分解,且价格昂贵[21]。特别是脂质用于制备乳液时,其稳定性差并且纯度难以控制[22]。SLNs作为递送系统还存在颗粒易聚集、载药量低、储存过程中多晶型转化后生物活性成分泄漏等缺点[15]。
1.1.3 多糖基
多糖作为生物活性物质递传载体基质应用广泛,因其来源广,在动植物和微生物中均可获取,加工成本较低[23];且多糖是具有α或β糖苷键的大分子聚合物,结构上更易于修饰,易与生物活性物质作用,使得活性物质的封包率更高;相较于蛋白质和脂质载体基质[24],多糖又因其分子量较高,可以在形成三维网络包封结构的同时增加体系的粘度,提高生物活性物质的稳定性,在较大的pH和温度范围内依然能够保持稳定[25]。除此之外,一些天然多糖(例如果胶和半乳糖)的亲水碳水化合物链中会含有蛋白质或非极性基团,使其具备良好的乳化特性[26]。另一方面多糖用作递送系统时,还可同时发挥多种生物活性功能,如免疫调节、抗肿瘤、调节肠道菌群、抗氧化等[27]。
常见的多糖载体基质主要包括:壳聚糖、海藻酸盐、果胶、黄原胶和透明质酸等。例如海藻酸盐作为未修饰的天然多糖可以用于制备水凝胶,易于与天然抗氧化剂、添加剂、防腐剂等物质结合,进而维持食物的挥发性风味化合物并延长食品的保质期[28];Chuysinuan等[29]通过制备复合壳聚糖/水解胶原蛋白/透明质酸水凝胶封包咖啡酸物质,结果表明咖啡酸胃肠释放量显著提高至80%,且此递送系统具有优异的溶胀性能,且表现出较强的抗氧化活性。
尽管多糖递送载体基质相较于蛋白质和脂质基质在生物活性物质稳定和包封方面效果更佳,但在食品复杂体系中(如含油脂的乳状液)往往存在着界面吸附困难,界面层容易崩解等问题,这可能是因为一些多糖的高度亲水性和复杂的大分子构象,致使其界面结构易受食品加工条件的影响[30],所以多糖载体往往还需要通过共价或非共价结合蛋白质或其他分子形成复合体系,才能拓展其应用范围。
1.2 多元复合输送载体基质
一元运载基质在用作封包递送时存在着系统稳定性较差或者是运载对象有限等诸多问题,而多元运载基质的出现恰好可以解决这些问题。
其中,二元载体基质目前较为常见的是蛋白-脂质基和蛋白-多糖基。蛋白-脂质基载体既可以解决两者单一载体不稳定、难贮藏的问题,又可以提高疏水性活性物质的运载量。其中蛋白-脂质基主要通过蛋白包裹脂质体的形式复合,例如Pan等[31]制备了装载虾青素的乳清分离蛋白包被脂质体的递送系统,与一元脂质体载物基质相比,二元复合递送系统中的虾青素在体外消化中表现出更高的生物利用度,此外乳清分离蛋白涂层还可保护脂质体免受崩解破坏。蛋白-多糖基递送系统常常通过这两种基质共价复合形成,可改善蛋白质不耐受强酸、强碱和高温的问题,体系的乳化能力、抗菌性能及热稳定性更强。例如,Fu等[32]分别用牛血清白蛋白(BSA-)和牛血清白蛋白-葡萄糖复合物(GBSA-)对姜黄素进行封包,相较于单一的BSA作为封包载体,与葡萄糖的共价结合会增加BSA的空间位阻和表面亲水性,因此在高温、高离子浓度和pH2.0~7.0的环境中仍然保持着稳定的状态。Kutzli等[33]研究了豌豆分离蛋白与麦芽糊精经糖基化形成的复合输送载体,结果发现与对照组单豌豆蛋白载体相比,加热后的复合系统(pH2~7)具有更高的溶解度。
三元复合输送运载基质种类较多,包括蛋白质-多糖-脂质基、蛋白质-蛋白质-多糖基、蛋白质-多糖-多糖基等。Liu等[34]将亲水性海藻酸钠通过静电相互作用涂覆在酪蛋白酸盐-玉米醇溶蛋白纳米颗粒上,形成蛋白质-蛋白质-多糖结构的递送载体,体外胃肠道稳定性实验表明,海藻酸盐包被可以保护纳米复合物在模拟胃液中免受酶水解,确保递送物质到达小肠被吸收。Zhuang等[35]研究不同浓度的魔芋葡甘聚糖(KGM)对由聚甘油聚蓖麻油酸酯(PGPR)和乳清分离蛋白(WPI)稳定的乳液凝胶封装葡萄籽原花青素的影响,研究发现相较于二元乳液凝胶系统,KGM的添加会改善乳液凝胶的持水性、流变性和质构性能;特别是在1.5%或1.75% KGM时,储存14 d后氢的颜色和电位表现出最稳定的水平。在体外消化过程中,KGM的添加也会延缓蛋白质和油滴的水解,进而提高了葡萄籽原花青素的生物利用度。目前,对于三元运载体的研究,一般都是对原有的二元载体进行针对性的优化,稳定性、封装率或生物可及性方面确实存在优势,但关于三元运载基质系统的研究还不成规模,有待进一步探索。
2. 复合递送系统的形成机制
2.1 蛋白质-脂质复合递送系统的形成机制
在输送系统中,脂质-蛋白质可使用多种技术进行偶联。例如脱溶剂、静电偶联、高压均质和化学偶联[36]。图2显示了最近文献中在药物和营养保健物质递送应用中,用于偶联脂质-蛋白质基质的各类技术手段。
2.1.1 脱溶剂法
脱溶剂法主要通过热力学动力驱动脂质与蛋白质发生自组装,在搅拌蛋白和脂质混合液的过程中加入脱水溶剂,使蛋白质脱水导致构象拉伸最终形成纳米颗粒[37]。Liu等[38]使用脱溶法制备负载维生素B12的脂质-白蛋白纳米颗粒,根据体外消化实验和吸收率的研究得出结论为这种纳米颗粒改善了维生素B12的口服吸收。然而由于这种方法在制备载体的过程中使用了脱溶剂而存在食用安全问题,因此目前在食品中的应用并不广泛,主要用于药品递送。
2.1.2 静电偶联法
静电偶联使蛋白脂质结合的机理是当蛋白质的pH高于或低于等电点时,蛋白质具有负电荷或正电荷,此时脂质带相反电荷,因而可以通过静电相互作用与蛋白质结合。Pan等[31]通过调节pH将乳清分离蛋白偶联包裹在装载虾青素的脂质体表面,在体外消化模型的研究中发现,乳清分离蛋白包衣可以在消化过程中保护脂质体,包被后负载虾青素的脂质体在胃肠道中稳定。
2.1.3 脂膜水合法
脂膜水合法可以用于制备单层囊泡的分散体系,直径在25~1000 nm不等。其过程是将脂质溶解在有机溶液中,后置于旋转蒸发器上干燥以获得脂质薄膜,将温度调节高于变相温度,使薄膜脱落封装蛋白水溶液或是蛋白纳米颗粒[39]。Chen等[40]研究了水合脂膜法制备大豆分离蛋白水解物脂质体,发现结合大豆分离蛋白水解物后的脂质体一方面可以有效地抑制脂质氧化产物的形成和积累,另一方面还能降低脂质体表面电位,以保持脂质体系统的稳定性。在用脂膜水合法制备样品时,蛋白质和脂质的比例也会影响样品的稳定性、封包效率等,Li等[41]用大豆油体相关蛋白(SOP)和大豆卵磷脂封包木犀草素,在脂质/SOP比为1:0.2时比1:0.8的粒径显著降低且分布均匀,SOP与磷脂的协同也提高了脂质体的封包性能。
2.1.4 高压均质法
高压均质作为蛋白质-脂质的偶联方法,常用于制备稳定乳液和悬浮液,其流程是在强烈的湍流和剪切流场下,蛋白质-脂质混合溶液中的脂质相被打散,形成小液滴,此时蛋白质包裹这些脂质形成大分子层以稳定这些脂质小液滴,从而降低脂质的聚结速率,最终形成稳定的生物活性物质包封系统[37]。例如Lüdtke等[42]将不同配比大豆分离蛋白、乳清分离蛋白、三酰甘油、大豆卵磷脂通过预乳化形成预乳液,再经过不同压力、循环次数的高压均质形成载物系统,研究发现均质压力的增大在一定程度上可以促进油滴的破裂,循环次数的增加则会促进新界面的形成和液滴表面蛋白的涂层形成,最终形成结构更加稳定的纳米结构脂质载体。高压均质的压强大小和时间,会影响运载系统的形成状态,Chang等[43]采用高压均质分别制备了三种蛋白稳定的纳米乳液以封装沙棘果肉油,发现当压力从70 MPa变为100 MPa,循环次数从1变为4时,观察到3种蛋白质稳定的纳米乳液的粒径显著减小,而在后续稳定性实验中也进一步证明,随着压强的增加,循环次数的增加,运载体系愈加稳定。
2.1.5 化学偶联法
化学偶联主要通过脂质的羧基和蛋白质的胺基之间形成酰胺键而偶联蛋白质和脂质。化学偶联与其他方法之间的主要区别在于化学偶联主要依赖于共价键的形成,而其他方法则主要是基于静电相互作用、疏水相互作用[36]。例如Pooja等[44]使用硬脂胺将氨基引入固体脂质纳米颗粒,以促进与小麦胚芽凝集素的羧基的结合。此外由于蛋白质存在胺和羧基可发生自聚合,因而通常在脂质和蛋白质偶联形成酰胺键之前,要优先活化脂质的羧基官能团,以促进蛋白质和脂质之间的高效偶联[45]。Zhu等[45]将白藜芦醇封装在玉米醇溶蛋白-聚甘油偶联物稳定的纳米乳液中,在白藜芦醇添加量为偶联物的10%时封效率超过90%,且在34 d储存期间表现出较高的稳定性,该课题组在先前的研究中发现偶联物的乳化性能显著改善,这意味着更好的乳化活性;同样,在对环境敏感性(如宽pH范围、高离子强度和高温)的实验中表现出更优异的稳定性[46]。
2.2 蛋白质-多糖复合递送系统的形成机制
2.2.1 静电相互作用
蛋白质和多糖之间的络合机制主要源于带相反电荷聚合物之间的静电相互作用。二者形成复合物后,可溶性物质继续聚集并降低体系的自由能,直至复合物尺寸增大,呈不溶状态,再通过非共价和氢键相互作用引起液-液相分离和凝聚。Zhang等[47]研究制备了大豆分离蛋白-金针菇多糖水性复合体系,研究发现适量的金针菇多糖会降低大豆分离蛋白溶液的浊度,并且在静电力的作用下会自发结合,可用于保护和输送生物活性物质。
另一方面,一些环境因素也会影响蛋白质和多糖之间的静电复合效果,如体系的pH、离子强度、生物聚合物浓度和蛋白质与多糖的比例[48]。还有一些其他因素,如温度、压力,甚至搅拌,也被证明会诱导凝聚现象,静电复合程度降低,影响生物活性物质的包封效果[49]。Zhang等[47]研究了不同离子强度下制备的大豆分离蛋白-金针菇多糖水性复合体系的浊度、粘弹性等功能性质,结果发现低NaCl浓度(<50 mmol/L)会使蛋白质β折叠结构含量增加,蛋白质和多糖间的静电相互作用增强,更有利于复合体系致密结构的形成;此外,当大豆分离蛋白/金针菇多糖比为10:1和15:1时,复合聚结趋于饱和,蛋白质-多糖复合物表现出类似固体的特性。
2.2.2 共价相互作用
蛋白质和多糖之间可通过共价作用形成不可逆的蛋白质-多糖复合物,且二者之间具有较强的特异性[50]。这种共价相互作用主要通过糖基化反应实现,即在适当的低水活性和热处理下,蛋白质分子的赖氨基残基和多糖的羧基共价结合形成酰胺[51]。例如Yang等[52]通过大豆蛋白-大豆多糖美拉德反应形成稳定乳液,包封柠檬醛,喷雾干燥使其微胶囊化。所得微粒粉末含有46%的柠檬醛。与非包封柠檬醛相比,大豆蛋白-大豆多糖乳液和胶囊显著降低了喷雾干燥过程中和后续储存过程中柠檬醛的损失。和分子间静电相互作用不同的是蛋白-多糖共价相互作用受离子强度和pH的影响较小,但糖链的长度和蛋白质分子的性质对糖基化蛋白质-多糖偶联物的形成有很大的影响,例如酪蛋白等未折叠的蛋白质通常比折叠的蛋白质(例如溶菌酶)与多糖结构的反应更为迅速。Yang等[53]将酪蛋白分别与两种多糖偶联,在加热处理中随着时间的增加,复合物中α螺旋和β折叠的含量显著降低,而无规卷曲的含量却在增加,这是因为蛋白质分子空间结构展开并松弛,有利于糖基化。Borah等[54]制备了叶酸功能化支链淀粉-白蛋白纳米凝胶,支链淀粉-白蛋白分别在79 ℃、60%的相对湿度时共价结合产生白蛋白-叶酸官能团支链淀粉和白蛋白-玉米支链淀粉两种不同的共价复合物,其主要原因便是反应条件的不同进而影响糖化程度,形成不同复合物。糖链堆叠的数据表明纳米凝胶通过酰胺键克服了对照组天然自组装在能量上不可持续的问题,这也印证了糖链和蛋白结构对共价复合影响较大。
3. 复合输送载体在生物活性物质递传方面的应用
生物活性成分是从天然动植物来源获得的功能成分,具有一种或多种生物活性,具有增强免疫力、缓减疾病症状和协同药物作用进而协助疾病治疗的作用。这些生物活性成分通常也被制备成保健品而应用于食品、药品领域,如矿物质、天然色素、氨基酸、酚类混合物等[55]。然而由于大多数生物活性物质在直接口服时,会受到人体内波动的pH、酶、代谢反应、粘膜和胃肠道屏障的影响,常在未到达作用靶点前就发生降解,影响了其生物活性,从而导致生物可及性、口服效果不佳等问题。近年来研究发现,将生物活性物质封装在载体基质中可实现其在人体内的有效递送,增强其生物利用度,目前此方面研究较多的生物活性物质为多酚类、维生素类及其他类。
3.1 递传多酚类生物活性物质
多酚是植物的次生代谢产物,主要包括酚酸和类黄酮,可防止活性氧引起的氧化应激,具有良好的抗氧化、抗炎、防癌等生物活性[56]。多酚的结构完整性和递送的生物可及性会决定其作用的有效性,但多酚对热敏感容易氧化,食物制备方法和胃肠道的极性环境限制了多酚的应用,因此通过封装来保证多酚在体内的有效释放受到了广泛的关注。
多酚主要通过非共价相互作用(即范德华力、氢键、疏水和静电相互作用)的形式与和递送载体作用而实现其有效传递[57]。非共价相互作用的类型和强度会影响多酚负载效果,因此蛋白-脂质/多糖复合体系在作为负载多酚的递送系统时,需要考虑多酚和蛋白质之间的相互作用对递送系统稳定性、生物利用度的影响。例如Tao等[58]制备了包封山奈酚(KAE)和单宁酸(TA)的卵清蛋白-海藻酸钠(OVA-SA)复合载体等5种纳米颗粒,其中负载了山奈酚的OVA-SA纳米颗粒(pOVA-KAE-SA)多酚负载量更多,说明其多酚包埋效果更好,能有效提高多酚的生物利用度,究其原因是pOVA-KAE-SA粒径较小且ζ电位较高,即纳米颗粒表面电荷最多,静电斥力最强。此外,KAE和TA在嵌入时会暴露更多的羟基与卵清蛋白的极性基团形成氢键,进一步增强非共价相互作用。因此pOVA-KAE-SA纳米颗粒载体更易负载和稳定多酚,体系结构也最为稳定。
此外,不同蛋白质的种类也会影响封装多酚的效果。以姜黄素为例,许多蛋白质均可以作为多元运载基质的成分,但包封效果各不相同。玉米醇溶蛋白、酪蛋白和低密度脂蛋白都有相应的疏水基团,对于封装疏水性多酚姜黄素都有着天然的优势,但玉米醇溶蛋白和酪蛋白对温度、pH和离子强度的稳定性相对较低,例如Hua等[59]制备了负载姜黄素的酪蛋白-果胶纳米复合物,其负载能力为93%,在果胶涂层的帮助下,姜黄素在模拟胃液中的释放明显延迟,说明其耐酸能力大大提高。酪蛋白虽然可作为姜黄素的运载基质,但载体结构极易在贮藏过程中出现不可逆的展开或与脂蛋白之间形成共价二硫键,导致姜黄素的释放,因此,酪蛋白往往以多元复合输送载体的形式包封姜黄素。例如Xu等[60]制备了姜黄素、酪蛋白和大豆可溶性多糖三元复合纳米颗粒,姜黄素负载效率为97%,由于多糖表面的存在,该系统在30 ℃下储存25 d后具有良好的物理稳定性和姜黄素化学稳定性。还有许多酚类物质,包括芦丁在内的黄酮和类黄酮的生物活性物质,对于其封装递送都有一定量的研究。
3.2 递传维生素类生物活性物质
维生素是人类健康的基本要素,需要从食物中摄取,能够包封维生素的食品或保健品一直是人们研究的热点。根据维生素的溶解特性,可将其分为脂溶性维生素(维生素A、D、E等)和水溶性维生素(例如维生素B和维生素C),不同类型的维生素其包封方式也有所不同,且由于维生素对热和氧化剂十分敏感,易被破坏,如何延长并保护维生素的活性,保证其有效地吸收是包封方法选择的关键。
脂溶性维生素因为难溶于水,所以在常规食品中较难递传,因此需要通过乳化的形式包埋递送。一方面,封包可以提高脂溶维生素稳定性,Santos等[61]制备了微胶囊来封包维生素D3,可将维生素D3较低的变性温度提高到130 ℃,因其封包过程不仅是物理混合,还存在分子间相互作用,维生素或可与蛋白质之间形成氢键,热稳定性因此提高;另一方面,封包可以避免维生素过早地在胃部释放,提高小肠的吸收率。维生素A因其特有的低极性而导致水溶性很差,在运输和储存过程中容易降解或失去活性,Falsafi等[62]采用不同方式制备乳清分离蛋白(WPI)-阿拉伯胶(GA)混合物,再经过静电纺丝技术封装β-胡萝卜素,均表现出了较高的物理稳定性,可进一步探究静电纺丝在封装脂溶性维生素方面的潜力。维生素E对高温、光、氧和碱性条件敏感,加上水溶性差,限制了维生素E的应用,Neves等[63]通过冷冻干燥油菜籽或椰子水包油乳液获得的微粒有效地封装了α生育酚,在TIM-1模拟消化模型评估中发现,封装后的α-生育酚的总体生物可利用性明显提高。
从水溶性维生素的角度讲,纳米颗粒是常用的封包手段。Liu等[38]以全大麦蛋白层、磷脂层和α-生育酚层为原料制备具有三层结构的脂质-蛋白质复合纳米颗粒用以递送维生素B12。磷脂层和α生育酚层由大麦蛋白层以支架方式分离稳定并得到亲水性维生素B12被封装在内部水隔室中,这种结构可以克服与脂质体和基于溶液的输送系统的大多数缺点如在胃环境中的稳定性较差,极易发生维生素泄漏。另一方面,由于活性化合物和纳米颗粒输送系统的亲和力较强,纳米颗粒封装亲水性维生素的效果更佳。大麦蛋白与维生素B12的偶联可进一步提高维生素B12的包封效率,增强胃环境中的消化抵抗力和维生素B12的受控释放。日常生活中对维生素C的需求十分广泛,但其极易降解,Baek等[64]将维生素C分别封包进改性壳聚糖和纤维素纳米晶体中,大大提高了封装效率高达90.3%±0.42%,稳定性也大大提升,贮藏第14 d,仅有10%逸出。
3.3 递传其他生物活性物质
其他的生物活性物质包括一些不饱和脂肪酸或富含必需脂肪酸的油类、萜类、植物色素和生物碱。
比如鱼油,富含多不饱和脂肪酸对预防心血管疾病等方面有积极的作用,但存在气味难闻、水溶性差和氧化不稳定等问题,采用递送系统封装可以解决这些问题,Li等[65]使用由不同浓度大豆分离蛋白(SPI)和磷脂酰胆碱(PC)、鱼油组成稳定的纳米乳液,研究发现,纳米乳液粒径和PDI随SPI浓度增加,呈先降低后升高的趋势,原因是当SPI浓度过低时,不能完全覆盖油滴表面;过高时,蛋白质聚集形成亚胶束使得粒径和PDI增加,进而使蛋白质絮凝。从热稳定性和均质压力稳定性的结果来看,都是粒径和PDI值最小时最稳定(2% SPI)。此外,在储存稳定性和氧化稳定性的测试中SPI-PC纳米乳也表现出良好的特性,这是由于SPI/PC表面的电荷密度更高,静电排斥性更强,对脂质氧化的抑制效果更好。
又如花青素(ACNs)是天然来源的水溶性着色剂,广泛存在于浆果、一些蔬菜、谷物和其他具有鲜艳色彩的植物中,包括红色、紫色和蓝色调[66]。ACNs稳定性很差,易受pH、光、热、抗坏血酸、金属离子、糖、氧和酶等不利环境因素的影响,这些因素会降低其生物活性并变质其颜色,从而限制其在食品中的应用[67]。Liu等[68]通过逐层自组装成功制备成负载花青素的β-环糊精(β-CD)-盐酸壳聚糖(CHC)/羧甲基壳聚糖(CMC)双纳米配合物,相比较于负载ACNs的β-CD纳米络合物,双纳米配合物在不利环境条件(光、热、pH和抗坏血酸)中表现出更优异的稳定性;在模拟胃肠道消化过程中也能够完成ACNs的持续释放。Cui等[69]通过糖基化制备牛血清白蛋白(BSA)/酪蛋白(CA)-羧甲基纤维素偶联物,多元基质的复合不仅提高了系统的溶解度、热稳定性和发泡能力,糖化蛋白和羧甲基纤维素形成的复合物还对花青素的热稳定性具有积极的促进作用,具有减少褪色、提高保留率和保持花青素抗氧化活性等特点,对花青素的应用保藏具有深远的意义。
还有很多的生物活性物质,由于难溶解、难吸收或稳定性差等问题而应用受限,都可以通过封装达到提高可及性和生物利用度的目的。
4. 总结
本文概述了蛋白质、脂质和多糖作为一元输送载体在输送生物活性物质方面的主要效果和机制,阐释了一元和多元在递送系统中各自存在的优缺点,总结发现蛋白-脂质/多糖多元复合系统具有更好的稳定性和递送潜力,其中蛋白-脂质复合物可以通过静电偶联、脂膜水合、脱溶剂法、化学偶联、高压均质等方法制备,蛋白-多糖复合输送载体则可以通过共价偶联和静电相互作用复合形成。这些复合递送系统能够负载多酚、维生素、鱼油、植物色素等多种生物活性成分,且可有效提高生物活性物质的包封率、稳定性和生物可及性。然而除了负载多酚的载物系统方面具有较为深入的研究外,关于其他生物活性成分递传物质的研究还较少;此外,许多研究通过针对性改善二元基质的不足而制备出有特异优势的三元载体,但对于三元载体的制备方法、优缺点以及能否取代二元载体并没有系统深入的研究,因此未来可针对这些方面进行更加系统和深入的研究。
-
表 1 不同类型载体基质优缺点
Table 1 Advantages and disadvantages of different types of carrier matrix
基质构成 结构 缺点 优点 蛋白质 纳米纤维
纳米颗粒
水凝胶蛋白质对离子浓度、电荷、温度等环境因素
高度敏感,易变性或聚集良好的乳化性、凝胶性、
低毒性和较高的生物相容性脂质 乳液
脂质体
固体脂质纳米颗粒(SLNs)
纳米结构脂质体(NLCs)价格昂贵成本较高,酸性条件下易分解 优异的生物相容性和乳化性能 多糖 水凝胶
纳米颗粒
乳液复杂的食品体系中难以维持稳定性 来源广泛,加工成本低,结构易于修饰 二元复合载体
(蛋白-脂质基)乳液
凝胶
纳米颗粒
脂质体价格昂贵成本较高 提高疏水性活性物质的生物可及性 二元复合载体
(蛋白-多糖基)凝胶
乳液
纳米颗粒不易于封装疏水性物质 封装效率更高,稳定性强 三元复合载体基质 乳液
凝胶
纳米颗粒
脂质体制备方法复杂,成本较高 高稳定性且易于缓释,封装效率较高 -
[1] ĐORĐEVIĆ V, BALANČ B, BELŠČAK-CVITANOVIĆ A, et al. Trends in encapsulation technologies for delivery of food bioactive compounds[J]. Food Engineering Reviews,2015,7:452−490. doi: 10.1007/s12393-014-9106-7
[2] MOHAMMADIAN M, WALY M I, MOGHADAM M, et al. Nanostructured food proteins as efficient systems for the encapsulation of bioactive compounds[J]. Food Science and Human Wellness,2020,9(3):199−213. doi: 10.1016/j.fshw.2020.04.009
[3] MAVIAH M B J, FAROOQ M A, MAVLYANOVA R, et al. Food protein-based nanodelivery systems for hydrophobic and poorly soluble compounds[J]. An Official Journal of the American Association of Pharmaceutical Scientists,2020,21:1−11.
[4] TANG C H. Nanocomplexation of proteins with curcumin:From interaction to nanoencapsulation (A review)[J]. Food Hydrocolloids,2020,109:106106. doi: 10.1016/j.foodhyd.2020.106106
[5] FATHI M, DONSI F, MCCLEMENTS D J. Protein-based delivery systems for the nanoencapsulation of food ingredients[J]. Comprehensive Reviews in Food Science and Food Safety,2018,17(4):920−936. doi: 10.1111/1541-4337.12360
[6] 荣令爽, 李宇鑫, 曹云刚, 等. 静电纺丝蛋白基纳米纤维的研究进展[J]. 食品工业科技,2022,43(10):450−457. [RONG L S, LI Y X, CAO Y G, et al. Research progress on electrospun protein-based nanofibers[J]. Science and Technology of Food Industry,2022,43(10):450−457.] RONG L S, LI Y X, CAO Y G, et al . Research progress on electrospun protein-based nanofibers[J]. Science and Technology of Food Industry,2022 ,43 (10 ):450 −457 .[7] ROSTAMI M, BEHESHTIZADEH N, RANJBAR F E, et al. Recent advances in electrospun protein fibers/nanofibers for the food and biomedical applications[J]. Advances in Colloid and Interface Science,2023,311:102827. doi: 10.1016/j.cis.2022.102827
[8] DENG L, ZHANG X, LI Y, et al. Characterization of gelatin/zein nanofibers by hybrid electrospinning[J]. Food Hydrocolloids,2018,75:72−80. doi: 10.1016/j.foodhyd.2017.09.011
[9] CHEN J, HU L. Nanoscale delivery system for nutraceuticals:Preparation, application, characterization, safety, and future trends[J]. Food Engineering Reviews,2020,12(1):14−31. doi: 10.1007/s12393-019-09208-w
[10] LIU Q, SUN Y, CHENG J, et al. Development of whey protein nanoparticles as carriers to deliver soy isoflavones[J]. LWT,2022,155:112953. doi: 10.1016/j.lwt.2021.112953
[11] 苏丹, 宋子悦, 杨杨, 等. 大豆蛋白基水凝胶的研究进展[J]. 食品工业科技,2022,43(3):402−410. [SU D, SONG Z Y, YANG Y, et al. Research progress of soybean protein hydrogels[J]. Science and Technology of Food Industry,2022,43(3):402−410.] SU D, SONG Z Y, YANG Y, et al . Research progress of soybean protein hydrogels[J]. Science and Technology of Food Industry,2022 ,43 (3 ):402 −410 .[12] CAO M, LIAO L, ZHANG X, et al. Electric field-driven fabrication of anisotropic hydrogels from plant proteins:Microstructure, gel performance and formation mechanism[J]. Food Hydrocolloids,2023,136:108297. doi: 10.1016/j.foodhyd.2022.108297
[13] ABAEE A, MOHAMMADIAN M, JAFARI S M. Whey and soy protein-based hydrogels and nano-hydrogels as bioactive delivery systems[J]. Trends in Food Science & Technology,2017,70:69−81.
[14] BOURBON A I, PEREIRA R N, PASTRANA L M, et al. Protein-based nanostructures for food applications[J]. Gels,2019,5(1):9. doi: 10.3390/gels5010009
[15] DA SILVA SANTOS V, RIBEIRO A P B, SANTANA M H A. Solid lipid nanoparticles as carriers for lipophilic compounds for applications in foods[J]. Food Research International,2019,122:610−626. doi: 10.1016/j.foodres.2019.01.032
[16] BARROSO L, VIEGAS C, VIEIRA J, et al. Lipid-based carriers for food ingredients delivery[J]. Journal of Food Engineering,2021,295:110451. doi: 10.1016/j.jfoodeng.2020.110451
[17] ASSADPOUR E, MAHDI JAFARI S. A systematic review on nanoencapsulation of food bioactive ingredients and nutraceuticals by various nanocarriers[J]. Critical Reviews in Food Science and Nutrition,2019,59(19):3129−3151. doi: 10.1080/10408398.2018.1484687
[18] TRIPATHY S, SRIVASTAV P P. Encapsulation of Centella asiatica leaf extract in liposome:Study on structural stability, degradation kinetics and fate of bioactive compounds during storage[J]. Food Chemistry Advances,2023,2:100202. doi: 10.1016/j.focha.2023.100202
[19] SOUTO E B, FANGUEIRO J F, FERNANDES A R, et al. Physicochemical and biopharmaceutical aspects influencing skin permeation and role of SLN and NLC for skin drug delivery[J]. Heliyon,2022,8(2):e08938. doi: 10.1016/j.heliyon.2022.e08938
[20] ADITYA N P, MACEDO A S, DOKTOROVOVA S, et al. Development and evaluation of lipid nanocarriers for quercetin delivery:A comparative study of solid lipid nanoparticles (SLN), nanostructured lipid carriers (NLC), and lipid nanoemulsions (LNE)[J]. LWT-Food Science and Technology,2014,59(1):115−121. doi: 10.1016/j.lwt.2014.04.058
[21] SHADE C W. Liposomes as advanced delivery systems for nutraceuticals[J]. Integrative Medicine:A Clinician's Journal,2016,15(1):33.
[22] LI J, WANG X, ZHANG T, et al. A review on phospholipids and their main applications in drug delivery systems[J]. Asian Journal of Pharmaceutical Sciences,2015,10(2):81−98. doi: 10.1016/j.ajps.2014.09.004
[23] MUNGURE T E, ROOHINEJAD S, BEKHIT A E D, et al. Potential application of pectin for the stabilization of nanoemulsions[J]. Current Opinion in Food Science,2018,19:72−76. doi: 10.1016/j.cofs.2018.01.011
[24] DEDHIA N, MARATHE S J, SINGHAL R S. Food polysaccharides:A review on emerging microbial sources, bioactivities, nanoformulations and safety considerations[J]. Carbohydrate Polymers,2022,287:119355. doi: 10.1016/j.carbpol.2022.119355
[25] GRUMEZESCU A M, HOLBAN A M. Biopolymers for food design[M]. Academic Press, 2018.
[26] DICKINSON E. Hydrocolloids at interfaces and the influence on the properties of dispersed systems[J]. Food Hydrocolloids,2003,17(1):25−39. doi: 10.1016/S0268-005X(01)00120-5
[27] WU Q, LUO M, YAO X, et al. Purification, structural characterization, and antioxidant activity of the COP-W1 polysaccharide from Codonopsis tangshen Oliv[J]. Carbohydrate Polymers,2020,236:116020. doi: 10.1016/j.carbpol.2020.116020
[28] GHEORGHITA PUSCASELU R, LOBIUC A, DIMIAN M, et al. Alginate:From food industry to biomedical applications and management of metabolic disorders[J]. Polymers,2020,12(10):2417. doi: 10.3390/polym12102417
[29] CHUYSINUAN P, THANYACHAROEN T, THONGCHAI K, et al. Preparation of chitosan/hydrolyzed collagen/hyaluronic acid based hydrogel composite with caffeic acid addition[J]. International Journal of Biological Macromolecules,2020,162:1937−1943. doi: 10.1016/j.ijbiomac.2020.08.139
[30] MELANIE H, TAARJI N, ZHAO Y, et al. Formulation and characterisation of O/W emulsions stabilised with modified seaweed polysaccharides[J]. International Journal of Food Science & Technology,2020,55(1):211−221.
[31] PAN L, LI H, HOU L, et al. Gastrointestinal digestive fate of whey protein isolate coated liposomes loading astaxanthin:Lipolysis, release, and bioaccessibility[J]. Food Bioscience,2022,45:101464. doi: 10.1016/j.fbio.2021.101464
[32] FU J, SUN C, TAN Z, et al. Nanocomplexes of curcumin and glycated bovine serum albumin:The formation mechanism and effect of glycation on their physicochemical properties[J]. Food Chemistry,2022,368:130651. doi: 10.1016/j.foodchem.2021.130651
[33] KUTZLI I, GRIENER D, GIBIS M, et al. Influence of Maillard reaction conditions on the formation and solubility of pea protein isolate-maltodextrin conjugates in electrospun fibers[J]. Food Hydrocolloids,2020,101:105535. doi: 10.1016/j.foodhyd.2019.105535
[34] LIU Q, HAN C, TIAN Y, et al. Fabrication of curcumin-loaded zein nanoparticles stabilized by sodium caseinate/sodium alginate:Curcumin solubility, thermal properties, rheology, and stability[J]. Process Biochemistry,2020,94:30−38. doi: 10.1016/j.procbio.2020.03.017
[35] ZHUANG H, LI X, WU S, et al. Fabrication of grape seed proanthocyanidin-loaded W/O/W emulsion gels stabilized by polyglycerol polyricinoleate and whey protein isolate with konjac glucomannan:Structure, stability, and in vitro digestion[J]. Food Chemistry,2023,418:135975. doi: 10.1016/j.foodchem.2023.135975
[36] DISSANAYAKE T, SUN X, ABBEY L, et al. Recent advances in lipid-protein conjugate-based delivery systems in nutraceutical, drug, and gene delivery[J]. Food Hydrocolloids for Health,2022,2:100054. doi: 10.1016/j.fhfh.2022.100054
[37] GABER M, MEDHAT W, HANY M, et al. Protein-lipid nanohybrids as emerging platforms for drug and gene delivery:Challenges and outcomes[J]. Journal of Controlled Release,2017,254:75−91. doi: 10.1016/j.jconrel.2017.03.392
[38] LIU G, YANG J, WANG Y, et al. Protein-lipid composite nanoparticles for the oral delivery of vitamin B12:Impact of protein succinylation on nanoparticle physicochemical and biological properties[J]. Food Hydrocolloids,2019,92:189−197. doi: 10.1016/j.foodhyd.2018.12.020
[39] AHMAD H, ARYA A, AGRAWAL S, et al. Novel lipid nanostructures for delivery of natural agents with antioxidant, antiinflammatory and antistroke potential:Perspectives and outcomes[M]. Nanostructures for Oral Medicine. Elsevier, 2017:577−605.
[40] CHEN C, SUN-WATERHOUSE D, ZHAO J, et al. Method for loading liposomes with soybean protein isolate hydrolysate influences the antioxidant efficiency of liposomal systems:Adding after liposomes formation or before lipid film hydration[J]. Food Hydrocolloids,2022,129:107629. doi: 10.1016/j.foodhyd.2022.107629
[41] LI R, PU C, SUN Y, et al. Interaction between soybean oleosome-associated proteins and phospholipid bilayer and its influence on environmental stability of luteolin-loaded liposomes[J]. Food Hydrocolloids,2022,130:107721. doi: 10.1016/j.foodhyd.2022.107721
[42] LÜDTKE F L, STAHL M A, GRIMALDI R, et al. Optimization of high pressure homogenization conditions to produce nanostructured lipid carriers using natural and synthetic emulsifiers[J]. Food Research International,2022,160:111746. doi: 10.1016/j.foodres.2022.111746
[43] CHANG M, GUO Y, JIANG Z, et al. Sea buckthorn pulp oil nanoemulsions fabricated by ultra-high pressure homogenization process:A promising carrier for nutraceutical[J]. Journal of Food Engineering,2020,287:110129. doi: 10.1016/j.jfoodeng.2020.110129
[44] POOJA D, KULHARI H, KUNCHA M, et al. Improving efficacy, oral bioavailability, and delivery of paclitaxel using protein-grafted solid lipid nanoparticles[J]. Molecular Pharmaceutics,2016,13(11):3903−3912. doi: 10.1021/acs.molpharmaceut.6b00691
[45] ZHU P, HE J, HUANG S, et al. Encapsulation of resveratrol in zein-polyglycerol conjugate stabilized O/W nanoemulsions:Chemical stability, in vitro gastrointestinal digestion, and antioxidant activity[J]. LWT,2021,149:112049. doi: 10.1016/j.lwt.2021.112049
[46] HE J, WANG M, ZHU P, et al. Novel polyglycerol-10 dialdehyde mediated cross-linking of sodium caseinate:Preparation, characterization, and improved emulsifying properties[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2022,647:128957. doi: 10.1016/j.colsurfa.2022.128957
[47] ZHANG J, DU H, MA N, et al. Effect of ionic strength and mixing ratio on complex coacervation of soy protein isolate/Flammulina velutipes polysaccharide[J]. Food Science and Human Wellness,2023,12(1):183−191. doi: 10.1016/j.fshw.2022.07.006
[48] LI H, WANG T, HU Y, et al. Designing delivery systems for functional ingredients by protein/polysaccharide interactions[J]. Trends in Food Science & Technology,2022,119:272−287.
[49] CHEN B, GUO Z, MIAO S, et al. Preparation and characterization of lotus seed starch-fatty acid complexes formed by microfluidization[J]. Journal of Food Engineering,2018,237:52−59. doi: 10.1016/j.jfoodeng.2018.05.020
[50] YI J, LAM T I, YOKOYAMA W, et al. Controlled release of β-carotene in β-lactoglobulin-dextran-conjugated nanoparticles’ in vitro digestion and transport with Caco-2 monolayers[J]. Journal of Agricultural and Food Chemistry,2014,62(35):8900−8907. doi: 10.1021/jf502639k
[51] GEORGE D, MAHESWARI P U, BEGUM K M M S. Chitosan-cellulose hydrogel conjugated with L-histidine and zinc oxide nanoparticles for sustained drug delivery:Kinetics and in-vitro biological studies[J]. Carbohydrate Polymers,2020,236:116101. doi: 10.1016/j.carbpol.2020.116101
[52] YANG Y, NIU F, CUI S W, et al. Spray-drying microencapsulation of citral with soy protein-soy polysaccharide Maillard reaction products:Stability and release characteristics[J]. Food Hydrocolloids,2022,132:107842. doi: 10.1016/j.foodhyd.2022.107842
[53] YANG S, ZHANG G, CHU H, et al. Changes in the functional properties of casein conjugates prepared by Maillard reaction with pectin or arabinogalactan[J]. Food Research International,2023,165:112510. doi: 10.1016/j.foodres.2023.112510
[54] BORAH P K, DAS A S, MUKHOPADHYAY R, et al. Macromolecular design of folic acid functionalized amylopectin–albumin core–shell nanogels for improved physiological stability and colon cancer cell targeted delivery of curcumin[J]. Journal of Colloid and Interface Science,2020,580:561−572. doi: 10.1016/j.jcis.2020.07.056
[55] BAO C, JIANG P, CHAI J, et al. The delivery of sensitive food bioactive ingredients:Absorption mechanisms, influencing factors, encapsulation techniques and evaluation models[J]. Food Research International,2019,120:130−140. doi: 10.1016/j.foodres.2019.02.024
[56] GUNATHILAKE K D P P, RANAWEERA K K D S, RUPASINGHE H P V. Effect of different cooking methods on polyphenols, carotenoids and antioxidant activities of selected edible leaves[J]. Antioxidants,2018,7(9):117. doi: 10.3390/antiox7090117
[57] ZHOU S D, LIN Y F, XU X, et al. Effect of non-covalent and covalent complexation of (-)-epigallocatechin gallate with soybean protein isolate on protein structure and in vitro digestion characteristics[J]. Food Chemistry,2020,309:125718. doi: 10.1016/j.foodchem.2019.125718
[58] TAO X, SHI H, CAO A, et al. Influence of polyphenol-metal ion-coated ovalbumin/sodium alginate composite nanoparticles on the encapsulation of kaempferol/tannin acid[J]. International Journal of Biological Macromolecules,2022,209:1288−1297. doi: 10.1016/j.ijbiomac.2022.04.108
[59] HUA C, YU W, YANG M, et al. Casein-pectin nanocomplexes as a potential oral delivery system for improving stability and bioactivity of curcumin[J]. Colloid and Polymer Science,2021,299:1557−1566. doi: 10.1007/s00396-021-04858-x
[60] XU G, LI L, BAO X, et al. Curcumin, casein and soy polysaccharide ternary complex nanoparticles for enhanced dispersibility, stability and oral bioavailability of curcumin[J]. Food Bioscience,2020,35:100569. doi: 10.1016/j.fbio.2020.100569
[61] SANTOS M B, DE CARVALHO M G, GARCIA-ROJAS E E. Carboxymethyl tara gum-lactoferrin complex coacervates as carriers for vitamin D3:Encapsulation and controlled release[J]. Food Hydrocolloids,2021,112:106347. doi: 10.1016/j.foodhyd.2020.106347
[62] FALSAFI S R, ROSTAMABADI H, NISHINARI K, et al. The role of emulsification strategy on the electrospinning of β-carotene-loaded emulsions stabilized by gum arabic and whey protein isolate[J]. Food Chemistry,2022,374:131826. doi: 10.1016/j.foodchem.2021.131826
[63] NEVES I C O, SILVA S H, OLIVEIRA N L, et al. Effect of carrier oil on α-tocopherol encapsulation in ora-pro-nobis ( Pereskia aculeata Miller) mucilage-whey protein isolate microparticles[J]. Food Hydrocolloids,2020,105:105716. doi: 10.1016/j.foodhyd.2020.105716
[64] BAEK J, RAMASAMY M, WILLIS N C, et al. Encapsulation and controlled release of vitamin C in modified cellulose nanocrystal/chitosan nanocapsules[J]. Current Research in Food Science,2021,4:215−223. doi: 10.1016/j.crfs.2021.03.010
[65] LI Y, LI M, QI Y, et al. Preparation and digestibility of fish oil nanoemulsions stabilized by soybean protein isolate-phosphatidylcholine[J]. Food Hydrocolloids,2020,100:105310. doi: 10.1016/j.foodhyd.2019.105310
[66] CHEN J, XU B, SUN J, et al. Anthocyanin supplement as a dietary strategy in cancer prevention and management:A comprehensive review[J]. Critical Reviews in Food Science and Nutrition,2022,62(26):7242−7254. doi: 10.1080/10408398.2021.1913092
[67] ENARU B, DREȚCANU G, POP T D, et al. Anthocyanins:Factors affecting their stability and degradation[J]. Antioxidants,2021,10(12):1967. doi: 10.3390/antiox10121967
[68] LIU R, WANG X, YANG L, et al. Coordinated encapsulation by β-cyclodextrin and chitosan derivatives improves the stability of anthocyanins[J]. International Journal of Biological Macromolecules,2023,242:125060. doi: 10.1016/j.ijbiomac.2023.125060
[69] CUI H, ZANG Z, JIANG Q, et al. Utilization of ultrasound and glycation to improve functional properties and encapsulated efficiency of proteins in anthocyanins[J]. Food Chemistry,2023,419:135899. doi: 10.1016/j.foodchem.2023.135899





 下载:
下载:

 下载:
下载:



