Effects of Polyonatum cyrtonema Hua. Polysaccharide on Intestinal Microorganisms Based on in Vitro-Simulated Digestion and Fermentation Model
-
摘要: 本研究采用模拟消化模型结合体外粪便菌群厌氧发酵模型,通过16S rDNA基因高通量测序分析肠道菌群结构,并通过GC-MS法测定短链脂肪酸含量的变化,从而探究多花黄精多糖(Polyonatum cyrtonema Hua. Polysaccharide,PCP)的益生元活性。结果显示:PCP经体外口腔、胃、小肠模拟消化,其未发生明显的变化。PCP经体外发酵能够迅速降低发酵液的pH。肠道菌群PCoA分析表明,PCP具有改变肠道菌群结构作用,且与菊粉具有一定类似性。在门水平上,相对于空白对照组PCP能显著(P<0.05)增加厚壁菌门(Firmicutes)和放线菌门(Actinomycetes)的相对丰度,显著(P<0.05)降低变形菌门(Proteobacteria)的相对丰度;在属水平上,PCP能显著(P<0.05)增加有益菌双歧杆菌(Bifidobacterium)和巨单胞菌(Megamonas)等菌群相对丰度,显著(P<0.05)降低条件致病菌肠球菌属(Enterobacter)和志贺氏菌(Escherichia-Shigella)的相对丰度。同时,PCP促进短链脂肪酸的产生,其中,乙酸和丙酸含量显著(P<0.05)增加。本研究表明多花黄精多糖可能通过调节肠道菌群,促进短链脂肪酸产生。Abstract: An in vitro simulation of digestion and fermentation model with feces bacteria was used to explore the probiotic capacity of Polyonatum cyrtonema Hua. polysaccharide (PCP) by 16S rDNA gene sequencing and determining changes in short-chain fatty acids via GC-MS. The results showed that the digestibility of PCP was not obviously found by in vitro simulating saliva-gastrointestinal digestion model. The addition of PCP could rapidly reduce the pH of fermentation broth. PCoA analysis showed that PCP had the effect of altering gut microbiota, which was similar with inulin. At the phylum level, compared to the blank control group, the relative abundance of Firmicutes and Actinomycetes was significantly increased (P<0.05) in the PCP group, while that of Proteobacteria was significantly decreased (P<0.05). At the genus level, the growth of beneficial bacteria Bifidobacterium and Megamonas was significantly promoted (P<0.05), while the growth of opportunistic bacteria Enterobacter and Escherichia-Shigella was significantly inhibited (P<0.05). Moreover, PCP greatly increased the contents of short-chain fatty acids, among which the contents of acetic acid and propionic acid were significantly increased (P<0.05). The present results suggest that PCP may enhance the production of short-chain fatty acids via gut microbiome regulation.
-
近年研究表明肠道微生物与人类健康密切相关,肠道细菌生态系统对人体疾病、免疫调控等方面起着重要的作用[1−3]。从肠道微生物和代谢产物的角度诠释益生元对肠道微生物群的调节作用已成为研究的热点 [4−6]。已有研究表明中药中的有效成分如多糖,能够对肠道菌群失调起到一定调节作用[7]。
多花黄精(Polyonatum cyrtonema Hua.)作为一种历史悠久且药食同源的药材[8],是中国药典收载的黄精基原植物之一,其多糖具有较好的药理作用和应用价值[9−12]。多花黄精多糖(Polyonatum cyrtonema Hua. Polysaccharide,PCP)的分子量为2~7 kDa,主要由果聚糖及半乳聚糖组成[13−14]。研究发现PCP的结构组成与菊粉(Inulin,INU)结构相似[15],INU是一种优质的益生元和膳食纤维,不会被胃肠道内源酶消化,能够调节肠道菌群平衡[16],因此,本研究推测PCP具有潜在的抗消化性和益生元活性。但目前对于PCP对肠道微生物的影响少有文献报道,目前仅有研究通过单一菌株的培养模式下,发现多花黄精多糖对双歧杆菌(Bifidobacterium)、乳杆菌(actobacillus)等有益菌有着促进生长的作用[16],但这种研究方式没有考虑肠道中多种微生物以及代谢物之间的相互作用。
因此,本研究以从多花黄精中提取的多糖为原料,以INU作为阳性对照,通过体外模拟消化模型研究其抗消化特性,并采用体外厌氧发酵模型,探究PCP对pH、微生物结构数量及代谢产物短链脂肪酸的影响,为多花黄精产品在食品中的推广应用提供基础数据,为多花黄精益生元食品的开发提供参考依据。
1. 材料与方法
1.1 材料与仪器
多花黄精(福建省三明市宁化县人工栽培,品种编号 FJ-105-1) 福建省三明农科院提供;无水乙醇 AR,上海泰坦(Titan)科技股份有限公司;乙酸、丙酸、丁酸等标准品 >99%,上海梯希爱(TCI)化成工业发展有限公司;α-淀粉酶(100 U/mg)、胃蛋白酶(3000 U/g)、胃脂肪酶(3000 U/g)、胰酶(4000 U/g) 美国西格玛奥德里奇公司;胆盐 阿拉丁试剂(上海)有限公司;DNAzol 基因组DNA 快速提取试剂盒 上海美吉逾华生物医药科技有限公司;其他试剂 国药集团化学试剂有限公司;粪便样品 年龄为22~25岁的志愿者(男性、女性各三人 ,签署参与本研究项目的知情同意书)的粪便,所选志愿者身体状况良好、健康,饮食正常,6个月内无肠道疾病,且2周内未服用过益生菌或抗生素;发酵培养基的制备[17] 0.1 mol/L无菌磷酸盐缓冲液1 L(pH6.8) 2 g蛋白胨,2 g酵母浸提物,0.1 g NaCl,0.04 g K2HPO4,0.04 g KH2PO4,0.01 g MgSO4·7H2O,0.01 g CaC12·6H2O,2 g NaHCO3,2 mL 吐温−80,0.02 g血红素,10 μL维生素K1,0.5 g胆盐,0.5 g半胱氨酸。
XMTD-204型恒温水浴锅 天津市欧诺仪器有限公司;Infinite M200PRO型多功能酶标仪 奥地利帝肯有限公司;VS-8401型超净操作台 上海博讯实业有限公司;LRH-250型生化培养箱 上海一恒科技有限公司;FE-28型pH计 上海梅特勒-托利多仪器有限公司;TQ8040型气相色谱仪 日本岛津公司;TGL-16M型台式冷冻离心机 湖南湘仪实验室仪器开发有限公司。
1.2 实验方法
1.2.1 黄精多糖的制备
取干燥多花黄精生品粉碎,过60目筛,按料液比1:25 (g/g)加水,于80 ℃加热2 h,4000 r/min离心15 min收集上清,加入无水乙醇,使提取液中乙醇浓度达到75%,于4 ℃过夜沉淀,离心(6000 r/min,20 min)收集沉淀后冻干,即获得水提多糖[18]。制备的多糖经蒽酮硫酸法[19]分析提取PCP多糖含量为83.1%,其它组分包括糖醛酸(8.8%)、蛋白质(3.6%)、多酚类(4.5%)。PCP多糖经凝胶渗透色谱(Gel Permeation Chromatography,GPC)[20]分析其Mw为4.2 kDa,多糖经过三氟乙酸水解,高效液相色谱仪(High Performance Liquid Chromatography,HPLC)测定单糖组成[21]为葡萄糖71.21%、木糖 13.21%、半乳糖4.57%、甘露糖4.47%、岩藻糖 4.15%、果糖2.39%。
1.2.2 黄精多糖的体外模拟消化实验
1.2.2.1 模拟口腔、胃肠道消化
模拟唾液、模拟胃液和模拟小肠液及三段式体外消化模型参考文献[22]的方法并略作修改,以INU作为对照。
模拟口腔消化:用HCl(6 mol/L)将模拟唾液pH调至6.8,在37 ℃的水浴中预热0.5 h后,将50 mL多糖样品(15.0 mg/mL)、CaCl2溶液(0.25 mL,0.3 mmol/L)和α-淀粉酶溶液(75 U/mL,5 mL)加入40 mL模拟唾液中,加入超纯水定容至100 mL后于37 ℃水浴孵育5 min,后用HCl(6 mol/L)将pH调至3.0。
模拟胃消化:将80 mL模拟胃液于37 ℃水浴中预热,加入上一阶段模拟口腔消化液、CaCl2溶液(0.05 mL,0.3 mmol/L)、胃蛋白酶溶液(2000 U/mL,5 mL)、胃脂肪酶溶液(60 U/mL,5 mL)和超纯水补充至100 mL,在37 ℃下孵育4 h。用NaOH(6 mol/L)将pH调至7.0。
模拟肠道消化:在37 ℃水浴中预热40 mL模拟小肠液,加入上一段模拟消化液、胆盐溶液(25 mL,10 mmol/L)、CaCl2溶液(0.4 mL,0.3 mmol/L)、胰酶溶液(5 g,100 U/mL)和超纯水补充至200 mL,37 ℃孵育6 h,沸水灭活酶。在模拟消化培养基中加入超纯水作为空白对照组。
1.2.2.2 总糖和还原糖测定
将胃模拟消化4 h和小肠模拟消化6 h样品分别测定总糖和还原糖含量,总糖含量采用苯酚硫酸法测定[23],分别取0、0.1、0.2、0.4、0.6、0.8、1.0 mL葡萄糖标准溶液(0.1 mg/mL)于试管中,用蒸馏水补足至1 mL,混匀后加入0.5 mL 5%苯酚溶液混匀,再加入2.5 mL浓硫酸溶液,混匀后放于沸水浴15 min,冷却后于490 nm处检测吸光度,获得标准曲线为y=9.6407x+0.0353(R2=0.999),样品加样量为1 mL,操作过程同前,根据标准曲线计算出总糖含量。还原糖含量采用3,5-二硝基水杨酸(DNS)方法测定[23],分别取0、0.2、0.4、0.6、0.8、1.0 mL葡萄糖标准溶液(1 mg/mL)于定容管中,用蒸馏水补足至2 mL,然后加入3 mL DNS试剂,混匀后沸水浴中加热5 min,冷却后用蒸馏水定容至25 mL,摇匀后在520 nm处检测吸光度值,绘制标准曲线为y=1.2975x−0.0313(R2=0.997)。样品加样量为2 mL,操作过程同前,根据标准曲线计算出还原糖含量。
1.2.3 黄精多糖的体外厌氧发酵
1.2.3.1 粪便处理
将粪便取样器、一次性手套、镊子、牛皮纸、自封袋、EP管离心管、试剂瓶等采样工具提前灭菌,在厌氧操作箱中将采集的6位志愿者的新鲜粪便等量混合,取混合粪样10 g加入到100 mL无菌磷酸盐缓冲液(PBS,pH6.8)中按1:10稀释,加几粒无菌玻璃珠涡旋振荡混匀配制成粪便悬液。稀释的粪液用4 层无菌纱布过滤取滤液为菌源液,所有新鲜粪便样品的采集和处理需在1 h内完成。
1.2.3.2 体外厌氧发酵
体外厌氧发酵方法参考文献[24−25]并对方法进行一定的改进,以基础发酵液为空白对照组,以1%(w/v)INU作为阳性对照,以1%(w/v)PCP作为实验组,并以1:9(v:v)的接种量接入菌源液,于37 ℃厌氧培养箱内培养,每组实验5个重复。分别在发酵 0、6、12、24 h后取样,用0.4 mL 0.5%硫酸铜或20%乙腈停止微生物的发酵。
1.2.3.3 pH的测定
厌氧发酵0、6、12、24 h对空白对照组和实验组分别取样,使用pH计对样品进行pH的测定。
1.2.3.4 总糖和还原糖测定
对发酵0、6、12、24 h空白对照组和实验组分别取样,离心后(4000×g离心15 min)取上清液,按1.2.2.2方法,测定发酵液的总糖和还原糖的含量。
1.2.4 16S rDNA基因及生物信息学分析
发酵24 h后的发酵液于8000×g离心15 min,取离心后得到的菌泥沉淀,保存于−80 ℃冰箱中,用于肠道菌群测序。使用DNAzol 基因组DNA 快速提取试剂盒提取菌泥沉淀中肠道微生物中的DNA,用琼脂糖凝胶电泳(1%)对抽提的DNA进行检测,检测合格的样品由上海美吉生物医药科技有限公司检测,通过Illumina MiSeq PE300平台对进行肠道菌群进行测序(引物序列为:338F(5′-ACTCCTACGGGAGGCAGCAG-3′);806R(5′-GGACTACHVGGGTWTCTAAT-3′)),得到 16S rDNA 数据。
16S rDNA数据分析方法:MiSeq/Novaseq测序得到的PE reads进行样本拆分后,首先根据测序质量对双端Reads进行质控和过滤,同时根据双端Reads之间的Overlap关系进行拼接,获得质控拼接之后的优化数据。然后使用序列降噪方法(DADA2/Deblur等)处理优化数据,获得ASV(Amplicon Sequence Variant)代表序列和丰度信息,使用Majorbio在线云平台(www.majorbio.com)对微生物数据进行α、β多样性的分析;运用ANOSIM进行各组之间的多样性差异检验分析;采用 Kruskal-Wallis(KW)sum-rank test 进行物种组间差异显著性分析;对各组样本群落组成进行分类学可视化分析。
1.2.5 短链脂肪酸(SCFAs)的测定
样液使用0.22 μm膜过滤,装入进样瓶待用。采用GC-MS测定,色谱条件:岛津Rtx-WAX 色谱柱(30 m×0.25 mm,0.25 μm);进样口温度250 ℃;柱温100 ℃;离子源温度220 ℃;接口温度250 ℃,升温程序:100 ℃以 7.5 ℃/min的速率升温至140 ℃,保持4 min,再以60 ℃/min 升温至 200 ℃;样品进样量1 μL;载气He;分流比10:1;流速2 mL/min;溶剂延迟1.5 min;Q3 Scan方式采集1.5 min到9.5 min,质量扫描范围m/z 20.0~300.0。分别配制浓度梯度在0.25~32 mmol/L范围内的乙酸、丙酸、丁酸标准溶液,采用外标法定量分析。
1.3 数据处理
本研究实验数据以平均值±标准差表示;运用SPSS 21.0软件的单因素方差分析方法(ANOVA)进行显著性分析(P<0.05 表示差异有统计学意义);通过Origin2021软件进行作图。高通量测序的原始数据进行质控、过滤、去嵌合体,得到有效数据,进行分类操作单元的划分,菌群结构差异及微生物种类差异通过美吉生物云平台分析。
2. 结果与分析
2.1 黄精多糖的体外抗消化特性
通过模拟口腔、胃、小肠消化液,对PCP进行体外消化,结果见表1。INU和PCP在三段消化过程中总糖含量几乎无变化(P>0.05),在口腔与小肠模拟消化后还原糖含量没有显著性变化(P>0.05)。在模拟胃消化过程中INU还原糖含量显著升高(P<0.05),可能是在酸性环境下INU的部分糖苷键断裂成为单糖或寡糖[26],少量多糖被降解为还原糖,而PCP则无显著变化(P>0.05),表明INU与PCP具有一定的抗消化特性,且PCP的抗消化能力更强,PCP能够不被消化系统降解,进入结肠后可能被微生物利用并发酵,具有益生元的潜能。
表 1 不同消化时间的总糖含量、还原糖含量变化Table 1. Changes in total sugar content and reducing sugar content at different digestion times组别 总糖含量(mg/mL) 还原糖含量(mg/mL) INU PCP INU PCP 唾液消化 0 min 1.51±0.02a 1.40±0.02a 0.35±0.02a 0.27±0.00a 5 min 1.50±0.01a 1.42±0.03a 0.39±0.02a 0.27±0.01a 胃液消化 0 h 1.25±0.02a 1.15±0.06a 0.38±0.07a 0.54±0.14a 2 h 1.24±0.01a 1.14±0.05a 0.45±0.11b 0.52±0.08a 4 h 1.24±0.02a 1.14±0.07a 0.54±0.03b 0.50±0.01a 肠液消化 0 h 0.59±0.07a 0.57±0.01a 0.34±0.02a 0.21±0.01a 2 h 0.59±0.05a 0.57±0.04a 0.34±0.02a 0.21±0.01a 4 h 0.58±0.07a 0.57±0.00a 0.32±0.01a 0.19±0.02a 6 h 0.58±0.04a 0.57±0.01a 0.33±0.01a 0.20±0.01a 注:不同字母表示不同时间点同组内差异显著,P<0.05;表2同。 2.2 发酵过程中pH、总糖和还原糖的变化
肠道微生物体外厌氧发酵和肠道内发酵在细菌数量、组成、多样性和代谢产物等方面都相似[27−28]。因此,本研究通过体外粪便菌群厌氧发酵模型,探究PCP对肠道菌群调节与利用的影响,肠道微生物能够利用不被消化的碳水化合物,产生有机酸、短链脂肪酸等一系列代谢产物,进而改变肠道生境的酸碱度[29],不同时间的发酵液pH、总糖和还原糖含量结果如表2所示。
表 2 体外发酵过程pH、总糖含量、还原糖含量变化Table 2. Changes in pH, total sugar content and reducing sugar content during in vitro fermentation时间(h) CON INU PCP pH 0 7.09±0.03a 6.96±0.02a 7.08±0.02a 6 7.49±0.10a 4.36±0.06b 4.63±0.03b 12 7.74±0.15a 4.27±0.05b 4.28±0.02c 24 7.44±0.04a 4.24±0.03b 4.25±0.01c 总糖含量(mg/mL) 0 0.20±0.03a 8.03±0.08a 8.10±0.03a 6 0.17±0.02ab 5.88±0.03b 6.68±0.35b 12 0.13±0.05bc 5.53±0.12c 5.99±0.31c 24 0.10±0.05c 5.01±0.12d 4.30±0.21d 还原糖含量(mg/mL) 0 0.28±0.01a 1.95±0.02b 1.43±0.01d 6 0.17±0.02b 2.77±0.03a 2.06±0.05a 12 0.20±0.02ab 1.42±0.02c 1.60±0.03c 24 0.21±0.07ab 2.64±0.13a 1.80±0.18b 由表2可知,空白对照组pH变化没有显著性差异(P>0.05),而PCP组和INU组的pH在6 h急剧下降后趋于稳定,同时,前6 h总糖含量快速下降且还原糖有一定上升,表明肠道微生物能够利用PCP、INU作为碳源生长,并产生大量有机酸与短链脂肪酸类等代谢产物,导致整个发酵体系中的pH下降;而后总糖含量下降趋缓,pH也变化不明显,表明肠道微生物生长进入稳定期。上述结果表明,INU和PCP能够被肠道菌群作为碳源利用,促进产酸。
2.3 黄精多糖体外发酵对肠道菌群α、β多样性的影响
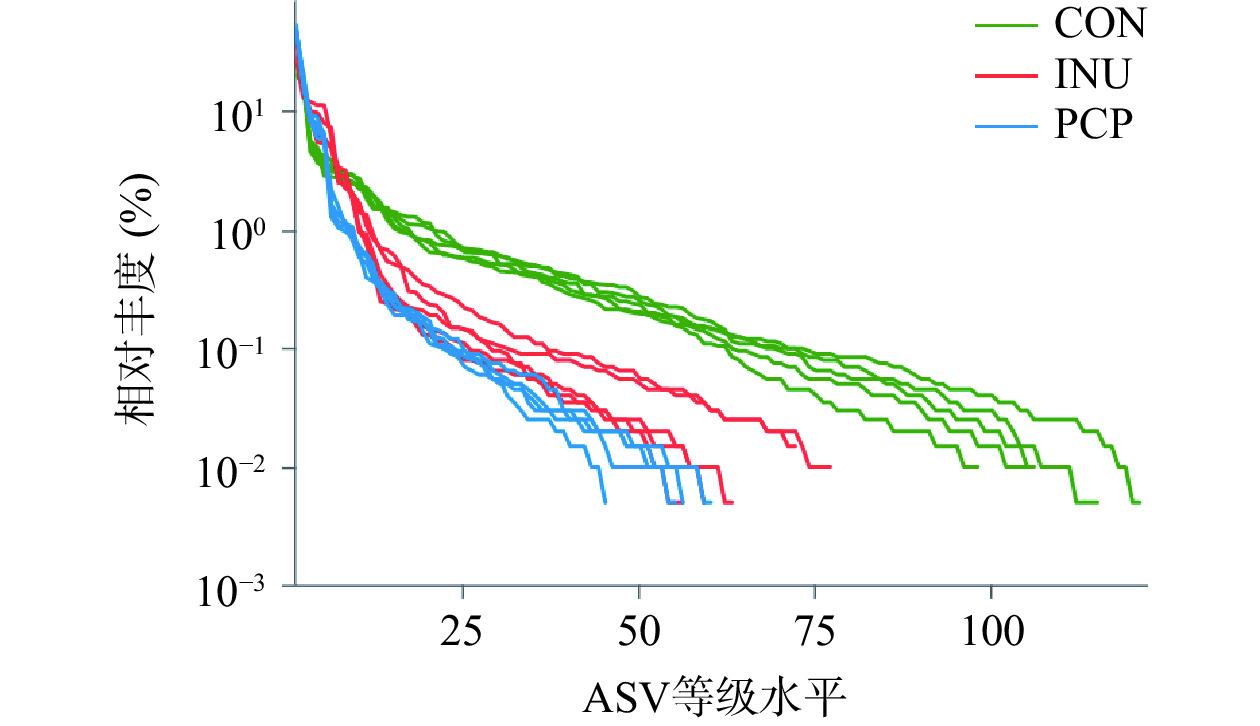
本研究采用16S多样性测序技术,进一步探究PCP对肠道菌群结构的影响。Rank-Abundance曲线能够说明物种丰度和群落均匀度。在水平方向,物种的丰富度由曲线的宽度来反映,物种的丰富度越高,曲线在横轴上的范围越大;曲线的平滑程度反映了样本中物种的均匀度,曲线越平缓,群落中物种分布越均匀[30]。如图1所示,三组在ASV等级水平上的宽度较大,说明物种丰富度高;从纵轴来看,曲线较平缓,说明样本中物种分布较为均匀,取得的测序结果适宜用于分析。
Alpha多样性分析可以表明肠道微生物群的均匀度和丰富度,ACE指数与Chao1指数反映菌群丰度,Shannon指数和Simpson指数反映菌群多样性[31]。由图2可知,PCP组、INU组与CON组相比,呈现类似的影响,Shannon指数、ACE指数与Chao1指数显著降低(P<0.05),而Simpson指数显著上升(P<0.05),这说明PCP与INU可降低肠道菌群的丰富度和多样性。这与先前INU在小鼠实验的结果一致,可能由于其促进某些有益肠道菌群增殖有关[32]。
主坐标分析(PCoA)代表了各组间肠道菌群的差异性,由图3可知,主成分PC1与PC2占比分别为88.78%、7.04%。三组间区别明显,说明发酵24 h后,发酵液中的肠道菌群发生显著变化,表明PCP能够调控肠道菌群组成和结构。此外,PCP和INU两组在PC1轴位置相近,而在PC2轴上距离较远,这表明两者对肠道菌群调控作用虽然有所差异但具有较大的相似性。
2.4 黄精多糖体外发酵对肠道菌群丰度的影响
如图4所示,16S rDNA基因测序表明了PCP基于体外发酵模型能够在门水平上改变肠道菌群组成。相对于CON组,PCP组和INU组中厚壁菌门(Firmicutes)和放线菌门(Actinobacteria)相对丰度显著增加(P<0.05),变形菌门(Proteobacteria)相对丰度显著减少(P<0.05)。厚壁菌门通常能够利用多糖产生SCFAs,并有助于抑制病原菌的增长[33]。放线菌门中包含益生菌如双歧杆菌,能够通过产生醋酸盐保护宿主免受肠道致病性感染[34]。变形菌门包括很多病原菌,如大肠杆菌、志贺氏菌等,易导致肠道微生物失调,与糖尿病、炎症和癌症正相关,进而影响宿主的机体健康[35]。
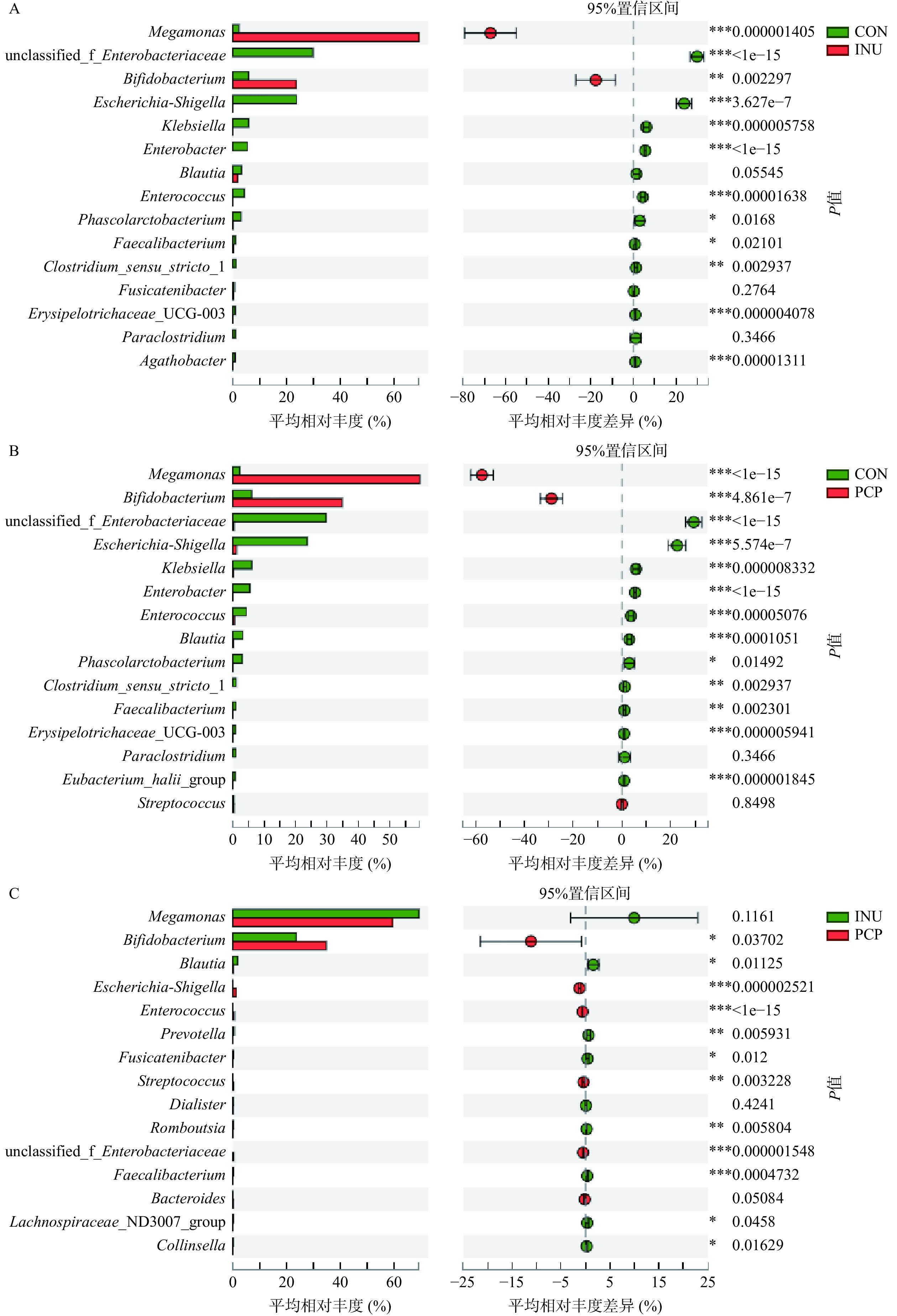
采用Student’s t-test 检验对丰度前25的菌属进行显著性差异比较分析,结果如图5所示,INU组或PCP组相较于CON组,巨单胞菌属(Megamonas)、双歧杆菌属(Bifidobacterium)、大肠杆菌属(Enterobacteriaceae)、志贺氏菌属(Escherichia-Shigella)、克雷伯氏菌属(Klebsiella)、肠杆菌属(Enterobacter)、肠球菌属(Enterococcus)、经黏液真杆菌属(Blautia)、丹毒丝菌属(Erysipelotrichaceae)、霍氏真杆菌属(Eubacterium_hallii_group)、普拉梭菌(Faecalibacterium)共10种菌属均存在显著性差异(P<0.05)。
与CON组相比,INU组的巨单胞菌属(Megamonas)和双歧杆菌属(Bifidobacterium)的相对丰度显著增加(P<0.05)、志贺氏菌属(Escherichia-Shigella)、克雷伯氏菌属(Klebsiella)、肠杆菌属(Enterobacter)、肠球菌属(Enterococcus)、丹毒丝菌属(Erysipelotrichaceae_UCG-003)等相对丰度显著降低(P<0.05)。通过对比PCP组与CON组显著差异菌属,可以发现,PCP组在属水平上对菌群调节作用与INU相似,PCP与INU两组中最为优势为巨单胞菌属(Megamonas)和双歧杆菌属(Bifidobacterium)。研究表明,巨单胞菌的增殖可以通过竞争能量摄入抑制有害细菌的生长,其主要代谢产物为乙酸和丙酸[36]。双歧杆菌和肠球菌属是益生菌,具有增强免疫,阻止有害菌黏附以及帮助宿主消化吸收营养物质等多种生理功能[37−38]。因此,PCP可能通过促进双歧杆菌和肠球菌等有益菌的增殖,抑制大肠杆菌、志贺氏菌的增殖,来调节肠道微生态并发挥益生元活性。
此外,PCP与INU对肠道菌群调节趋势相似但调节能力有所差异,PCP组中双歧杆菌属(Bifidobacterium)的相对丰度显著高于INU组(P<0.05),除巨单胞菌属(Megamonas)、拟杆菌属(Bacteroides)、戴阿利斯特杆菌属(Dialister)外,PCP组与INU组的其它主要优势菌群均有显著差异(P<0.05)。
2.5 发酵过程中SCFAs的变化
SCFAs作为人体肠道菌群的发酵产物,能够起到维持肠道水电解质平衡、抑制病原微生物、调节菌群平衡和抗炎等重要作用[39]。膳食中的碳水化合物是肠道微生物发酵产生SCFAs的主要底物[40]。如表3所示,经过体外厌氧发酵24 h后,PCP组的乙酸含量显著高于INU组(P<0.05),是CON组的6.7倍,这可能与PCP促进产乙酸的双歧杆菌、巨单胞菌丰度显著增加(P<0.05)有关,乙酸通常被认为是双歧杆菌等有益菌的发酵产物,能够通过激活G蛋白偶联受体调节肠道菌群环境,并能够作为周围组织的能量来源[33,41]。
表 3 体外发酵过程中不同 SCFAs 含量的变化(mmol/L)Table 3. Changes in different SCFAs content during in vitro fermentation (mmol/L)SCFAs 组别 发酵时间(h) 0 6 12 24 乙酸 CON 2.8±0.1a 5.0±0.2b 4.6±0.4b 4.9±0.3b INU 2.8±0.10a 7.2±0.2c 11.8±0.1e 28.7±0.4f PCP 2.8±0.1a 10.4±0.3d 11.9±0.2e 32.7±0.9g 丙酸 CON 0.9±0.1a 1.7±0.1b 3.1±0.1c 4.4±0.5d INU 0.9±0.1a 10.2±0.3g 11.7±0.4h 15.8±0.2j PCP 0.9±0.1a 7.9±0.2e 12.1±0.9i 9.4±0.2f 丁酸 CON 0.8±0.1ab 0.5±0.1a 1.8±0.2e 0.8±0.1b INU 0.8±0.1ab 1.2±0.1c 1.6±0.1d 1.1±0.4c PCP 0.8±0.1ab 0.6±0.1a 1.6±0.1e 0.6±0.3a 总酸 CON 4.5±0.1a 7.2±0.2b 9.5±0.6c 10.1±0.7c INU 4.5±0.1a 18.6±0.5d 25.1±0.4e 45.6±1.0g PCP 4.5±0.1a 18.9±0.4d 25.6±0.6e 42.7±0.8f 注:不同字母表示所有组别同一类短链脂肪酸含量有显著差异(P<0.05)。 此外,经过24 h发酵,丙酸在PCP和INU组均有显著增加(P<0.05),这可能与巨单胞菌有关,巨单胞菌可产乙酸和丙酸[33],PCP和INU均能显著增加巨单胞菌丰度(P<0.05)。丙酸经肠道细菌产生后,可被人体吸收进入血液随后转运至肝脏,下调肝脏和血浆中的脂肪酸含量,抑制免疫过度激活,提高胰岛素敏感性,并对肝癌细胞有抗增殖作用[42]。丁酸可以由肠道细菌代谢未消化的碳水化合物产生,也可通过对乙酸及乳酸的转化产生,与结肠细胞的抗炎和抗肿瘤作用相关[43],丁酸在三组中虽有显著差异(P<0.05),但整体含量占比低。此外,PCP组中总的SCFAs含量显著增加(P<0.05),与CON组相比,增加了3.2倍。SCFAs的产生能够降低周围环境的pH,有利于双歧杆菌等益生菌的生长[44]。
3. 结论
本研究通过体外模拟口腔、胃与小肠消化与体外粪便细菌发酵模型,探究了PCP的抗消化特性及其对于肠道菌群结构与短链脂肪酸代谢产物的影响。本研究发现,PCP与INU具有相似的活性,具有抗消化性,能够到达结肠被肠道菌群所利用,并能调节肠道菌群结构的活性,促进双歧杆菌等有益菌群增殖,促进乙酸与丙酸等短链脂肪酸代谢产物含量,是一种潜在的益生元。本研究为多花黄精多糖作为功能因子开发应用提供了理论依据,同时,后续研究需要进一步明确多糖功效成分的结构,并进一步通过体内实验验证其活性功效。
-
表 1 不同消化时间的总糖含量、还原糖含量变化
Table 1 Changes in total sugar content and reducing sugar content at different digestion times
组别 总糖含量(mg/mL) 还原糖含量(mg/mL) INU PCP INU PCP 唾液消化 0 min 1.51±0.02a 1.40±0.02a 0.35±0.02a 0.27±0.00a 5 min 1.50±0.01a 1.42±0.03a 0.39±0.02a 0.27±0.01a 胃液消化 0 h 1.25±0.02a 1.15±0.06a 0.38±0.07a 0.54±0.14a 2 h 1.24±0.01a 1.14±0.05a 0.45±0.11b 0.52±0.08a 4 h 1.24±0.02a 1.14±0.07a 0.54±0.03b 0.50±0.01a 肠液消化 0 h 0.59±0.07a 0.57±0.01a 0.34±0.02a 0.21±0.01a 2 h 0.59±0.05a 0.57±0.04a 0.34±0.02a 0.21±0.01a 4 h 0.58±0.07a 0.57±0.00a 0.32±0.01a 0.19±0.02a 6 h 0.58±0.04a 0.57±0.01a 0.33±0.01a 0.20±0.01a 注:不同字母表示不同时间点同组内差异显著,P<0.05;表2同。 表 2 体外发酵过程pH、总糖含量、还原糖含量变化
Table 2 Changes in pH, total sugar content and reducing sugar content during in vitro fermentation
时间(h) CON INU PCP pH 0 7.09±0.03a 6.96±0.02a 7.08±0.02a 6 7.49±0.10a 4.36±0.06b 4.63±0.03b 12 7.74±0.15a 4.27±0.05b 4.28±0.02c 24 7.44±0.04a 4.24±0.03b 4.25±0.01c 总糖含量(mg/mL) 0 0.20±0.03a 8.03±0.08a 8.10±0.03a 6 0.17±0.02ab 5.88±0.03b 6.68±0.35b 12 0.13±0.05bc 5.53±0.12c 5.99±0.31c 24 0.10±0.05c 5.01±0.12d 4.30±0.21d 还原糖含量(mg/mL) 0 0.28±0.01a 1.95±0.02b 1.43±0.01d 6 0.17±0.02b 2.77±0.03a 2.06±0.05a 12 0.20±0.02ab 1.42±0.02c 1.60±0.03c 24 0.21±0.07ab 2.64±0.13a 1.80±0.18b 表 3 体外发酵过程中不同 SCFAs 含量的变化(mmol/L)
Table 3 Changes in different SCFAs content during in vitro fermentation (mmol/L)
SCFAs 组别 发酵时间(h) 0 6 12 24 乙酸 CON 2.8±0.1a 5.0±0.2b 4.6±0.4b 4.9±0.3b INU 2.8±0.10a 7.2±0.2c 11.8±0.1e 28.7±0.4f PCP 2.8±0.1a 10.4±0.3d 11.9±0.2e 32.7±0.9g 丙酸 CON 0.9±0.1a 1.7±0.1b 3.1±0.1c 4.4±0.5d INU 0.9±0.1a 10.2±0.3g 11.7±0.4h 15.8±0.2j PCP 0.9±0.1a 7.9±0.2e 12.1±0.9i 9.4±0.2f 丁酸 CON 0.8±0.1ab 0.5±0.1a 1.8±0.2e 0.8±0.1b INU 0.8±0.1ab 1.2±0.1c 1.6±0.1d 1.1±0.4c PCP 0.8±0.1ab 0.6±0.1a 1.6±0.1e 0.6±0.3a 总酸 CON 4.5±0.1a 7.2±0.2b 9.5±0.6c 10.1±0.7c INU 4.5±0.1a 18.6±0.5d 25.1±0.4e 45.6±1.0g PCP 4.5±0.1a 18.9±0.4d 25.6±0.6e 42.7±0.8f 注:不同字母表示所有组别同一类短链脂肪酸含量有显著差异(P<0.05)。 -
[1] GEVERS D, KUGATHASAN S, DENSON L A, et al. The treatment naive microbiome in new-onset Crohn’s disease[J]. Cell Host Microbe,2014,15(3):382−392. doi: 10.1016/j.chom.2014.02.005
[2] LIU R, CHEN X, DU Y, et al. Serum microRNA expression profile as a biomaker in the diagnosis and prognosis of pancreatic cancer[J]. Clinical Chemistry and Laboratory Medicine,2012,58(3):610−618.
[3] THAISS C A, ZEEVI D, LEVY M, et al. Transkingdom control of microbiota diurnal oscillations promotes metabolic homeostasis[J]. Cell,2014,159(3):514−529. doi: 10.1016/j.cell.2014.09.048
[4] SUEZ J, KOREM T, ZEEVI D, et al. Artificial sweeteners induce glucose intolerance by altering the gut microbiota[J]. Nature,2014,514(7521):181−186. doi: 10.1038/nature13793
[5] CHASSAING B, KOREN O, GOODRICH J K, et al. Dietary emulsifiers impact the mouse gut microbiota promoting colitis and metabolic syndrome[J]. Nature,2015,519(7541):92−96. doi: 10.1038/nature14232
[6] HUMPHREYS K J, CONLON M A, YOUNG G P, et al. Dietary manipulation of oncogenic microRNA expression inhuman rectal mucosa:A randomized trial[J]. Cancer Prevention Research,2014,7(8):786−795. doi: 10.1158/1940-6207.CAPR-14-0053
[7] WU D T, YUAN Q, GUO H, et al. Dynamic changes of structural characteristics of Snow Chrysanthemum polysaccharides during in vitro digestion and fecal fermentation and related impacts on gut microbiota[J]. Food Research International,2021,141:109888−109898. doi: 10.1016/j.foodres.2020.109888
[8] 张凯, 张昭, 范永芳, 等. 药食同源药材黄精、玉竹营养及生物活性成分分析[J]. 中国现代中药,2022,24(8):1463−1472. [ZHANG K, ZHANG Z, FAN Y F, et al. Nutritional and bioactive components of Polygonati Rhizoma and Polygonati Odorati Rhizoma with medicinal and edible property[J]. Modern Chinese Medicine,2022,24(8):1463−1472.] ZHANG K, ZHANG Z, FAN Y F, et al. Nutritional and bioactive components of Polygonati Rhizoma and Polygonati Odorati Rhizoma with medicinal and edible property[J]. Modern Chinese Medicine, 2022, 24(8): 1463−1472.
[9] 国家药典委员会. 中国药典[S]. 一部. 2020:319-320. [Chinese Pharmacopoeia Commission. Chinese pharmacopoeia[S]. I. 2020:319−320.] Chinese Pharmacopoeia Commission. Chinese pharmacopoeia[S]. I. 2020: 319−320.
[10] YUAN L R, YE Y L. Study on anti-oxidant effect of Polygonatum polysaccharide in vitro[J]. Taiwan Pharmaceutical,2020,241(2):22−25.
[11] LUO Y, FANG Q, LAI Y, et al. Polysaccharides from the leaves of Polygonatum sibiricum Red. regulate the gut microbiota and affect the production of short-chain fatty acids in mice[J]. AMB Express,2022,12(1):1−10. doi: 10.1186/s13568-021-01341-2
[12] 杨明琛, 袁梦欣, 陆维, 等. 黄精多糖体外消化特性及对Ⅱ型糖尿病小鼠肠道菌群的调节作用[J]. 现代食品科技, 2021, 37(8):14-21. [YANG M C, YUAN M X, LU W, et al. In vitro digestion properties of Polygonatum sibiricum polysaccharide and its regulatory action on the gut microbiota in T2DM mice[J]. Modern Food Science and Technology, 2021, 37(8):14−21. [13] ZHAO P, ZHOU H F, ZHAO C C, et al. Purification, characterization and immunomodulatory activity of fructans from Polygonatum odoratum and P. cyrtonema[J]. Carbohydrate Polymers,2019,214:44−52. doi: 10.1016/j.carbpol.2019.03.014
[14] LIU X X, WAN Z J, SHI L, et al. Preparation and antiherpetic activities of chemically modified polysaccharides from Polygonatum cyrtonema Hua.[J]. Carbohydrate Polymers,2011,83:737−742. doi: 10.1016/j.carbpol.2010.08.044
[15] 赖鲸慧, 祝元婷, 陈媛, 等. 乳酸菌代谢低聚果糖/菊粉途径及机理的研究进展[J]. 食品科学,2022,43(9):364−372. [LAI J H, ZHU Y T, CHEN Y, et al. Recent progress in understanding metabolic pathways and mechanisms of fructooligosaccharides/inulin by lactic acid bacteria[J]. Food Science,2022,43(9):364−372.] LAI J H, ZHU Y T, CHEN Y, et al. Recent progress in understanding metabolic pathways and mechanisms of fructooligosaccharides/inulin by lactic acid bacteria[J]. Food Science, 2022, 43(9): 364−372.
[16] JZA B, HC A, LAN L B, et al. Structures of fructan and galactan from Polygonatum cyrtonema and their utilization by probiotic bacteria[J]. Carbohydrate Polymers 2021, 262:118219.
[17] DING Y, YAN Y, PENG Y, et al. In vitro digestion under simulated saliva, gastric and small intestinal conditions and fermentation by human gut microbiota of polysaccharides from the fruits of Lycium barbarum[J]. International Journal of Biological Macromolecules,2019,125:751−760. doi: 10.1016/j.ijbiomac.2018.12.081
[18] YU L, WANG Y, TANG Q, et al. Structural characterization of a Polygonatum cyrtonema Hua tuber polysaccharide and its contribution to moisture retention and moisture-proofing of porous carbohydrate material[J]. Molecules,2022,27(15):5015. doi: 10.3390/molecules27155015
[19] 谢存一, 李剑梅, 郭玲玲, 等. 桑黄发酵液胞外多糖含量测定方法的比较及优化[J]. 食用菌,2022,44(6):69−73. [XIE C Y, LI J M, GUO L L, et al. Comparison and optimization of determination methods of extracellular polysaccharides in fermentation broth of Sanghuang mushroom[J]. Edible Fungi,2022,44(6):69−73.] doi: 10.3969/j.issn.1000-8357.2022.06.023 XIE C Y, LI J M, GUO L L, et al. Comparison and optimization of determination methods of extracellular polysaccharides in fermentation broth of Sanghuang mushroom[J]. Edible Fungi, 2022, 44(6): 69−73. doi: 10.3969/j.issn.1000-8357.2022.06.023
[20] 丁银蒙, 刘晶, 马青修, 等. 羊毛脂中游离羊毛醇和残留农药的含量测定[J]. 中国现代应用药学,2023,40(14):1976−1982. [DING Yinmeng, LIU Jing, MA Qingxiu, et al. Determination of free lanolin alcohol and residual pesticides in lanolin[J]. Chinese Journal of Modern Applied Pharmacy,2023,40(14):1976−1982.] DING Yinmeng, LIU Jing, MA Qingxiu, et al. Determination of free lanolin alcohol and residual pesticides in lanolin[J]. Chinese Journal of Modern Applied Pharmacy, 2023, 40(14): 1976−1982.
[21] 王森森, 平清伟, 盛雪茹, 等. 国产色谱柱HPLC法测定竹子乙醇精炼液中单糖与小分子脂肪酸[J]. 大连工业大学学报,2022(2):41. [WANG Sensen, PING Qingwei, SHENG Xueru, et al. Determination of monosaccharides and fatty acidswith low molecular weight in ethanol refining liquor of bamboo by HPLC[J]. Journal of Dalian Polytechnic University,2022(2):41.] WANG Sensen, PING Qingwei, SHENG Xueru, et al. Determination of monosaccharides and fatty acidswith low molecular weight in ethanol refining liquor of bamboo by HPLC[J]. Journal of Dalian Polytechnic University, 2022(2): 41.
[22] BRODKORB A, EGGER L, ALMINGER M, et al. INFOGEST static in vitro simulation of gastrointestinal food digestion[J]. Nature Protocols,2019,14:991−1014. doi: 10.1038/s41596-018-0119-1
[23] CHEN G, XIE M, WAN P, et al. Digestion under saliva, simulated gastric and small intestinal conditions and fermentation in vitro by human intestinal microbiota of polysaccharides from Fuzhuan brick tea[J]. Food Chemistry,2018,244:331−339. doi: 10.1016/j.foodchem.2017.10.074
[24] LI Y Q, MU H L, ANDERSEN J E T, et al. New human milk fat substitutes from butterfat to improve fat absorption[J]. Food Research International,2010,43(3):739−744. doi: 10.1016/j.foodres.2009.11.006
[25] ZHANG X, ZHU X L, SUN Y K, et al. Fermentation in vitro of EGCG, GCG and EGCG3 isolated from Oolong tea by human intestinal microbiota[J]. Food Research International,2013,54:1589−1595. doi: 10.1016/j.foodres.2013.10.005
[26] 许威, 罗登林, 陈瑞红, 等. 菊粉酸降解动力学研究[J]. 食品科学,2012,33(15):95−98. [XU W, LUO D L, CHEN R H, et al. Kinetic studies on acid catalyzed hydrolysis of inulin[J]. Food Science,2012,33(15):95−98.] XU W, LUO D L, CHEN R H, et al. Kinetic studies on acid catalyzed hydrolysis of inulin[J]. Food Science, 2012, 33(15): 95−98.
[27] 支梓鉴, 俞邱豪, 程焕, 等. 肠道微生物体外发酵模型研究进展及其在食品中的应用[J]. 食品工业科技,2016,37(14):353−358. [ZHI X J, YU Q H, CHEN H, et al. Advances in vitro fermentation model of gut microbiota and its applications in food[J]. Food and Beverage Industry,2016,37(14):353−358.] ZHI X J, YU Q H, CHEN H, et al. Advances in vitro fermentation model of gut microbiota and its applications in food[J]. Food and Beverage Industry, 2016, 37(14): 353−358.
[28] DUAN H, YU Q, NI Y, et al. Effect of Agaricus bisporus polysaccharides on human gut microbiota during in vitro fermentation:An integrative analysis of microbiome and metabolome[J]. Foods,2023,12(4):859. doi: 10.3390/foods12040859
[29] KRAUTKRAMER K A, FAN J, BÄCKHED F. Gut microbial metabolites as multi-kingdom intermediates[J]. Nature Reviews Microbiology,2021,19(2):77−94. doi: 10.1038/s41579-020-0438-4
[30] LIU J, SUI Y, SHI Y J, et al. High throughput sequencing analysis of biogeographical distribution of bacterial communities in the black soils of northeast China[J]. Soil Biology and Biochemistry,2014,70:113−122. doi: 10.1016/j.soilbio.2013.12.014
[31] MA Y, JIANG S, ZENG M. In vitro simulated digestion and fermentation characteristics of polysaccharide from oyster (Crassostrea gigas), and its effects on the gut microbiota[J]. Food Research International,2021,149:110646. doi: 10.1016/j.foodres.2021.110646
[32] SONG X, ZHONG L, LYU N, et al. Inulin can alleviate metabolism disorders in ob/ob mice by partially restoring leptin-related pathways mediated by gut microbiota[J]. Genomics, Proteomics & Bioinformatics,2019,17:64−75.
[33] BENSCH H M, TOLF C, WALDENSTRÖM J, et al. Bacteroidetes to Firmicutes:Captivity changes the gut microbiota composition and diversity in a social subterranean rodent[J]. Animal microbiome,2023,5:9. doi: 10.1186/s42523-023-00231-1
[34] VENTURA M, TURRONI F, SINDEREN V. Bifidobacteria of the human gut[M]. Diet-Microbe Interactions in the Gut, Amsterdam:Elsevier Inc, 2015:41−51.
[35] NARI S, TAE W W, JIN-WOO B. Proteobacteria:Microbial signature of dysbiosis in gut microbiota[J]. Trends in Biotechnology,2015,33(9):496−503. doi: 10.1016/j.tibtech.2015.06.011
[36] ZHOU J L, ZHANG Q, ZHAO Y Z, et al. The relationship of Megamonas species with nonalcoholic fatty liver disease in children and adolescents revealed by metagenomics of gut microbiota[J]. Scientific Reports,2022,12(1):22001. doi: 10.1038/s41598-022-25140-2
[37] SADEGHPOUR H F, HU H. Bifidobacterium:Host–microbiome interaction and mechanism of action in preventing common gut-microbiota-associated complications in preterm infants:A narrative review[J]. Nutrients,2023,15(3):709. doi: 10.3390/nu15030709
[38] MENARD S, CANDALH C, BAMBOU J C, et al. Lactic acid bacteria secrete metabolites retaining anti-inflammatory properties after intestinal transport[J]. Gut,2004,53(6):821−828. doi: 10.1136/gut.2003.026252
[39] XIAO Suwei, JIANG Shu, QIAN Dawei, et al. Modulation of microbially derived short-chain fatty acids on intestinal homeostasis, metabolism, and neuropsychiatric disorder[J]. Applied Microbiology and Biotechnology,2020,104(2):589−601. doi: 10.1007/s00253-019-10312-4
[40] WONG J M, DE SOUZA R, KENDALL C W, et al. Colonic health:Fermentation and short chain fatty acids[J]. Journal of Clinical Gastroenterology,2006,40(3):235−243. doi: 10.1097/00004836-200603000-00015
[41] MÜLLER M, HERNÁNDEZ M A, GOOSSENS G H, et al. Circulating but not faecal short-chain fatty acids are related to insulin sensitivity, lipolysis and GLP-1 concentrations in humans[J]. Scientific Reports,2019,9:12515. doi: 10.1038/s41598-019-48775-0
[42] AL-LAHHAM S, ROELOFSEN H, PRIEBE M G, et al. Regulation of adipokine production in human adipose tissue by propionic acid[J]. European Journal of Clinical Investigation,2010,40(5):401−407. doi: 10.1111/j.1365-2362.2010.02278.x
[43] ZENG H, DAVID T, CHENG W, et al. Butyrate inhibits cancerous Hct116 colon cell proliferation but to a lesser extent in noncancerous ncm460 colon cells[J]. Nutrients,2017,9(1):25−38. doi: 10.3390/nu9010025
[44] CHEN Y, LIU Y, SARKER W, et al. Structural characterization and antidiabetic potential of a novel heteropolysaccharide from Grifola frondosa via IRS1/PI3K-JNK signaling pathways[J]. Carbohydrate Polymers,2018,198(15):452−461.
-
期刊类型引用(1)
1. 张露,王修俊,何春霞,胡荣念,陈艳琳. 发酵青小米辣护色工艺条件优化及品质分析. 中国酿造. 2025(02): 199-205 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:



 下载:
下载:



