Analysis of Volatile Components of Kombucha in Different Regions
-
摘要: 本研究采用顶空固相微萃取法结合气相色谱-质谱技术,通过强极性色谱柱DB-WAX分离鉴定康普茶的挥发性成分,使用香气活性值(odor activity value,OAV)结合化学计量学,以探究不同地区康普茶的挥发性物质构成和特征性差异物质。结果表明:不同地区康普茶挥发性物质存在明显差异,共鉴定出56种挥发性物质,主要为醇类、酸类、酯类和酚类物质,借助于香气活性值筛选出32种对康普茶风味有贡献的物质(OAV≥1),不同地区康普茶除乌鲁木齐和威海康普茶外异戊酸乙酯的OAV都较高,对不同地区康普茶的风味构成有重要作用。同时使用偏最小二乘判别分析(partial least squares discrimination analysis,PLS-DA),筛选出17种变量重要性大于1的差异标记物。基于OAV和PLS-DA结果,筛选出14种康普茶的特征性差异物质:3-甲基-1-丁醇、2-乙基-1-己醇、苯乙醇、壬醇、乙酸、3-甲基丁酸、辛酸、乙酸乙酯、乙酸异戊酯、辛酸乙酯、苯乙酸乙酯、呋喃甲醛、2,6-二叔丁基对甲苯酚和4-乙基苯酚。研究结果将为康普茶的优质化生产以及特色品牌的构建提供理论参考依据。Abstract: In this study, headspace solid phase micro-extraction (HS-SPME) combined with gas chromatography-mass spectrometry (GC-MS) was adopted to separate and identify the volatile components of Kombucha by using polar column DB-WAX. Then, odor activity value (OAV) combined with stoichiometry was used to explore the volatile substance composition and characteristic differential substances of Kombucha in different regions. The results showed that there were significant differences between the volatile substances of Kombucha in different regions. A total of 56 kinds of volatile substances were detected, mainly alcohols, acids, esters and phenols. The OAV results showed that 32 kinds of substances contributed to the flavor for Kombucha (OAV≥1), the OAV of ethyl isovalerate of Kombucha in different regions was highest except for Urumqi and Weihai, it might play an important role in the flavor composition of Kombucha in different regions. Furthermore, with partial least squares discrimination analysis (PLS-DA), 17 variables with importance values greater than 1 as differential markers were identifed. By integrating the results of OAV and PLS-DA, a total of 14 characteristic compounds of Kombucha were screened out, namely 3-methyl-1-butanol, 2-ethyl-1-hexanol, phenethyl alcohol, nonanol, acetic acid, 3-methylbutyric acid, caprylic acid, ethyl acetate, isopentyl acetate, ethyl caprylate, ethyl phenylacetate, furan formaldehyde, 2,6-di-tert-butyl-p-cresol, and 4-ethylphenol. The research results will provide theoretical reference for the standardization, high-quality production and construction of characteristic brands of Kombucha.
-
康普茶是糖茶水经酵母、乳酸菌和醋酸菌的共生菌群发酵而成的茶饮料[1],酸甜爽口且风味独特,具有保护肝脏、抗菌、抗氧化和抗癌等功效[2−3]。复杂的微生物共生关系及其发酵过程促进了康普茶独特风味的形成,包括醇、醛的形成,以及醇、醛向酸、酯的转化[4],这些化学物质的形成与转化,是决定康普茶品质与风味的重要因素之一[5]。
近年来,鉴于康普茶的健康效益以及独特风味,研究者们对其展开了广泛的研究,主要包括康普茶的发酵条件及其影响[6−7]、工艺优化及新产品的研发[8−9]、微生物菌群及代谢[10−12]、化学成分及其保健功效[13−15]。随着消费者对康普茶感官品质要求的进一步提高,其挥发性成分的研究也越来越受到重视。邓雯瑾等[16]研究发现康普茶挥发性物质发酵前以醇类、萜烯类和含氮化合物为主,发酵后醇类和酯类等挥发性物质有所增加。袁磊等[17]对其优化工艺后的康普茶进行测定,检测到19种风味成分,其中醇类7种、酯类6种、酸类4种、酚类1种、烷烃1类。Phetxumphou等[18]通过系统完整的感官描述性分析,发现低温高糖条件下发酵的康普茶更加香甜浓稠。康普茶作为一种风味饮品,其风味品质在生产过程具有重要意义,因此,对不同地区的康普茶的挥发性物质构成进行更深入的探究,继而选择优质康普茶作为发酵液用于发酵生产具有重要意义。
为研究不同地区康普茶的风味特征,采用顶空固相微萃取法(HS-SPME)提取挥发性化合物,结合气相色谱-质谱(GC-MS)技术,通过DB-WAX 色谱柱分离鉴定康普茶的挥发性成分,并使用香气活性值法(OAV)结合偏最小二乘判别分析(PLS-DA)[19−20],以探究不同地区康普茶的挥发性物质构成,明晰不同地区康普挥发性成分的差异,为康普茶的优质化生产以及特色品牌构建提供理论参考。
1. 材料与方法
1.1 材料与仪器
康普茶 来自8个地区,包括华东地区:威海(WH)、合肥(HF);东北地区:哈尔滨(HRB)、沈阳(SY);中南地区:桂林(GL)、长沙(CS);西北地区:乌鲁木齐(WLMQ)、西安(XA),均购于淘宝,为家庭自酿康普茶,样品于2021年10月发酵完毕,每个地区样品取3个不同发酵罐中刚发酵好的康普茶。样品贮存于4 ℃冰箱待测定;正己烷、甲醇、1,2-二氯苯标品、正构烷烃混标(C7~C40) 色谱纯,浓度为1000 μg/mL,上海Sigma-Aldrich公司。
Agilent 7890B-5977B气质联用仪、DB-WAX色谱柱(30 m×0.25 mm×0.25 μm) 美国Agilent公司;手动SPME进样器、50/30 μm DVB/CAR/PDMS固相微萃取头 美国Supelco公司;DF-101S恒温磁力搅拌器 河南予华仪器有限公司;PL203电子天平 梅特勒-托利多仪器(上海)有限公司。
1.2 实验方法
1.2.1 顶空固相微萃取处理
参考Al-Mohammadi等[21]的方法略作修改。准确称量康普茶样品5.00 g,置于20 mL顶空瓶中,同时加入500 µL溶于甲醇的内标物1,2-二氯苯(1.3048 µg/µL)。随后,立即用聚四氟乙烯/硅橡胶隔垫密封。将密封完成的顶空瓶放置到集热式磁力搅拌器中,于50 ℃条件下平衡10 min,紧接着将DVB/CAR/PDMS(50/30 μm)萃取纤维针插入顶空瓶中,伸出纤维涂层,于距离样品上表面约1 cm处吸附萃取25 min。萃取结束后,立即收回纤维涂层,并拔出固相微萃取纤维针,于250 ℃条件下,在GC进样口热解析7.5 min,进行挥发性化合物的分析。每个地区样品独立测定3次,结果表示为含量±标准差。
1.2.2 GC-MS分析
GC条件:参考Flaig等[22]和Allegrone等[23]的方法,采用DB-WAX(30 m×0.25 mm×0.25 μm)强极性色谱柱分离、鉴定康普茶的挥发性化合物,载气为高纯氦气(纯度>99.999%),载气流速为1.5 mL/min,整个过程采用不分流模式进样。
升温程序[24]:起始柱温40 ℃,保持3 min,然后以5 ℃/min的速率升温至75 ℃并保持5 min,再以5 ℃/min的速率升温至110 ℃保持5 min,最后以10 ℃/min的速率升温至230 ℃保持5min。
MS条件:采用电子轰击(Electron impact,EI)电离源,电子能量为70 eV,离子源温度为230 ℃,全扫描模式,核质比扫描范围为35~500 m/z。
定性方法:将GC-MS分析得到的各化合物色谱峰的质谱信息与NIST 14标准谱库进行检索比对,匹配指数大于80%作为物质鉴定标准,同时,结合文献报道的已知化合物进行确认;将正构烷烃(C7~C40)以与样品相同的升温程序进行分析,根据正构烷烃混标物质的保留时间,计算化合物的Kováts保留指数(Kováts index,KI),结合文献以及数据库中的KI,对未知化合物进行鉴定。KI按照公式(1)计算:
KIx=100×n+RTx−RTnRTn+1−RTn×100 (1) 式中:KIx,待测物质x的保留指数;RTx,待测物质x的保留时间;RTn,碳原子数为n的正构烷烃的保留时间;RTn+1,碳原子数为n+1的正构烷烃的保留时间;RTn<RTx<RTn+1。
定量方法:采用内标法进行半定量,根据峰面积与浓度的关系计算得到未知化合物的浓度;每个样品独立测定三次,浓度按照公式(2)计算:
Cx=f′x×AxAis×mx×mis×1000000 (2) 式中:Cx,未知化合物x的含量,ng/g;Ax,未知化合物x的峰面积;Ais为内标物的峰面积;mx,用于萃取的康普茶样品的质量,g;mis,加入内标物is的质量,mg;f′x,未知化合物x对内标物is的相对质量校正因子;本试验中未知化合物x的相对质量校正因子均为1;1000000为单位换算系数。
1.2.3 OAV计算
在各种挥发性成分定量的基础上,根据参考文献中各挥发性物质在水中的风味阈值[25],OAV按公式(3)计算[26]:
OAVx=wxOTx (3) 式中:Wx,康普茶香气组分x的含量,ng/g;OTx,香气组分x在水中的香气阈值,μg/kg。
1.3 数据处理
使用Rx64 4.1.0软件进行挥发性成分的热图(Heatmap)分析;使用SIMCA 14.1进行偏最小二乘判别分析。
2. 结果与分析
2.1 不同地区康普茶挥发性成分分析
采用静态顶空固相微萃取-气相色谱-质谱联用双柱法对8个地区的康普茶挥发性成分进行分离鉴定,共检测出挥发性物质56种(表1),包括22种醇类物质、6种酸类物质、13种酯类物质、9种醛类物质、4种酚类物质以及2种酮类物质。另外,不同地区检测出的康普茶挥发性物质种类也不相同,其中合肥康普茶含有挥发性物质种类最为丰富,有34种,其次为威海康普茶,有31种;长沙康普茶27种,哈尔滨和沈阳康普茶都为26种;桂林和西安康普茶分别为25种和24种;乌鲁木齐康普茶种类最少,仅为19种。
表 1 不同地区康普茶挥发性成分定性定量结果(ng/g)Table 1. Qualitative and quantitative results of volatile components of Kombucha in different regions (ng/g)编号 物质 RI计算/文献 定性方式 威海 合肥 哈尔滨 沈阳 桂林 长沙 乌鲁木齐 西安 C 醇类 C1 3-甲基-1-丁醇 1247/1237 RI、MS 1494.15±65.05 4639.67±29.01 957.15±114.13 1914.03±51.20 2005.26±185.56 2645.44±50.56 2.57±0.12 3661.62±276.69 C2 2-庚醇 − MS 56.42±5.28 46.57±3.15 − − − − − − C3 反式芳樟醇氧化物 − MS 163.07±21.38 91.63±10.29 101.58±7.67 317.57±57.31 − − − − C4 2-壬醇 − MS 31.16±2.90 − − − − − − − C5 2-乙基-1-己醇 1525/1522 RI、MS 80.96±4.23 163.74±4.48 83.48±2.70 − 64.09±2.15 8313.34±19.29 − 58.25±3.62 C6 芳樟醇 1557/1549 RI、MS 142.13±8.11 − − 250.21±2.01 194.18±7.55 431.67±6.17 − − C7 L-薄荷醇 1649/1651 RI、MS 239.43±4.17 61.73±5.23 458.48±8.36 − − − − − C8 alpha-松油醇 − MS 151.45±14.67 − 125.10±6.56 231.95±10.82 73.35±7.32 103.16±4.19 − − C9 苯乙醇 1900/1912 RI、MS 445.43±4.83 1270.47±2.95 843.8±63.95 1349.03±42.68 711.99±91.41 1074.75±62.66 254.37±4.67 2146.86±182.52 C10 庚乙二烯乙二醇 − MS 44.82±4.77 39.89±0.19 127.24±4.08 − 26.01±4.35 − − − C11 乙醇 906/900 RI、MS 1334.8±88.90 404.38±18.39 390.27±387.44 29745.77±646.13 14570.05±746.18 30371.18±621.43 1331.18±79.16 21720.71±671.73 C12 2-壬烯-1-醇 − MS − − 117.68±5.77 − − − − 48.02±4.26 C13 2-甲基丙醇 − MS − 237.77±12.98 − 227.30±6.09 − 222.96±2.91 − 182.24±16.51 C14 正己醇 1364/1371 RI、MS − 127.57±2.11 − − 47.28±2.47 − − − C15 辛醇 1565/1561 RI、MS − 65.42±9.60 − − − − − − C16 壬醇 1665/1668 RI、MS − 103.15±12.75 − − 300.80±15.79 425.22±29.93 − 83.47±4.51 C17 月桂醇 − MS − − − 122.02±5.07 32.79±3.12 − − 76.85±4.16 C18 反-2-十一烯醇 − MS − − − 68.17±3.72 − − − − C19 3-甲基-2-己醇 − MS − − − − − − 146.84±5.95 − C20 6-甲基-1-庚醇 − MS − − − − − 557.27±47.42 − − C21 5-乙基-2-庚醇 − MS − − − − − 113.24±28.22 − − C22 樟脑 − MS − − 73.92±1.77 − − − − − S 酸类 S1 乙酸 1458/1460 RI、MS 7646.17±127.59 17194.52±481.23 35874.82±153.73 14185.25±150.93 11283.22±208.87 14050.22±565.88 25958.86±918.84 20431.72±307.55 S2 2-甲基丙酸 − MS 79.13±2.28 464.74±16.39 182.31±5.72 156.44±5.88 − − − 172.38±5.62 S3 3-甲基丁酸 − MS 584.75±43.70 4623.79±256.66 3579.84±290.04 809.61±16.15 706.71±59.97 808.12±63.54 1306.17±70.88 2146.46±68.73 S4 辛酸 2086/2089 RI、MS 690.74±141.06 43.15±1.25 126.89±3.88 − − 845.09±21.52 − − S5 己酸 1828/1827 RI、MS − − 89.64±2.09 − − 257.21±12.77 − − S6 4-甲基-2-氧代戊酸 − MS − 66.14±2.76 − − − − − − Z 酯类 Z1 乙酸乙酯 898/891 RI、MS 12330.73±206.42 39387.18±664.82 27916.21±985.52 26319.06±379.36 12544.15±669.16 27510.56±229.48 − 19840.95±736.82 Z2 2-甲基丁酸乙酯 − MS 61.06±3.99 154.42±6.53 − − − − − − Z3 乙酸异戊酯 1104/1112 RI、MS 614.20±21.38 3851.04±107.94 1460.44±68.66 902.61±56.02 723.41±56.49 1911.01±54.58 − 2171.39±65.46 Z4 正己酸乙酯 1243/1246 RI、MS 189.63±2.05 621.77±94.11 − 62.15±3.21 36.86±4.61 355.14±36.37 − 61.74±4.68 Z5 乳酸乙酯 − MS 42.20±5.67 196.21±3.21 − − − − − − Z6 辛酸乙酯 1445/1441 RI、MS 600.85±40.74 − − − − 126.41±4.22 − − Z7 乙酸异龙脑酯 − MS 37.37±4.90 69.46±1.83 − − − − − − Z8 苯乙酸乙酯 1786/1779 RI、MS 314.71±10.20 731.72±34.46 432.61±5.02 965.61±15.92 161.57±7.92 401.17±4.07 79.78±0.73 276.99±20.23 Z9 乙酸苯乙酯 1795/1801 RI、MS 73.57±2.34 438.15±16.24 447.21±19.69 286.39±4.50 134.17±8.72 281.41±8.28 148.15±12.71 424.12±18.85 Z10 异戊酸乙酯 1060/1064 RI、MS 381.24±5.39 1253.42±59.19 260.07±16.41 406.76±7.28 148.2±12.73 412.89±22.85 − 219.77±4.55 Z11 丁酸乙酯 − MS − 80.74±6.26 − − − − − − Z12 水杨酸甲酯 − MS − − − 81.52±2.87 − − − − Z13 3-呋喃甲酸甲酯 − MS − − − − − − 146.15±9.09 − Q 醛类 Q1 壬醛 1397/1400 RI、MS 97.50±15.38 52.05±4.04 − 350.56±3.28 64.77±3.69 486.53±7.07 37.53±0.88 53.67±3.94 Q2 2,5-二甲基苯甲醛 − MS 435.65±38.82 430.7±11.55 454.41±17.68 267.31±7.74 335.29±21.66 175.10±4.59 1487.23±127.39 200.02±7.75 Q3 正辛醛 − MS − − − 220.08±3.32 − 310.64±28.45 − − Q4 苯甲醛 1534/1530 RI、MS − 104.78±1.22 231.03±7.56 − − − 705.59±7.18 69.74±8.11 Q5 4-丙基苯甲醛 − MS − 101.23±9.29 − 190.76±20.48 85.41±6.89 116.05±12.59 − 59.76±4.82 Q6 呋喃甲醛 − MS − − − − − − 16157.25±249.55 − Q7 5-甲基呋喃醛 − MS − − − − − − 264.41±6.93 − Q8 2,6-二甲基苯甲醛 − MS − − − − − − 55342.1±260.03 − Q9 5-羟甲基糠醛 − MS − − − − − − 166.65±4.12 − F 酚类 F1 2,6-二叔丁基对
甲苯酚− MS 1766.20±76.65 1846.08±53.80 1791.56±7.47 766.29±38.66 1622.11±89.21 − 1536.26±223.05 1786.96±121.39 F2 4-乙基苯酚 − MS 766.18±112.32 − 164.64±6.93 − 61.52±1.73 420.09±6.36 − − F3 2,4-二叔丁基苯酚 − MS 237.5±30.24 210.64±20.08 273.44±15.65 323.76±13.82 481.66±33.33 343.01±11.08 5438.37±96.02 202.53±8.01 F4 乙基麦芽酚 − MS 550.09±2.95 − − − − − − − T 酮类 T1 3-羟基-2-丁酮 − MS − 123.83±7.06 444.23±38.48 68.80±8.32 126.78±11.79 − − 161.48±2.72 T2 环己酮 − MS − − − − − − 565.59±20.64 − 注:−表示某物质RI无法计算或未检测出;RI文献值来源于https://webbook.nist.gov/数据库。 进一步的分析表明,8个地区康普茶共同含有的挥发性物质有9种,分别为苯乙醇、3-甲基-1-丁醇、乙醇、乙酸、3-甲基丁酸、苯乙酸乙酯、乙酸苯乙酯、2,5-二甲基苯甲醛、2,4-二叔丁基苯酚。Zhao等[5]和袁磊等[17]的研究中检测出的风味物质有乙醇、苯乙醇、乙酸、乙酸乙酯等,这与本研究结果较为一致。
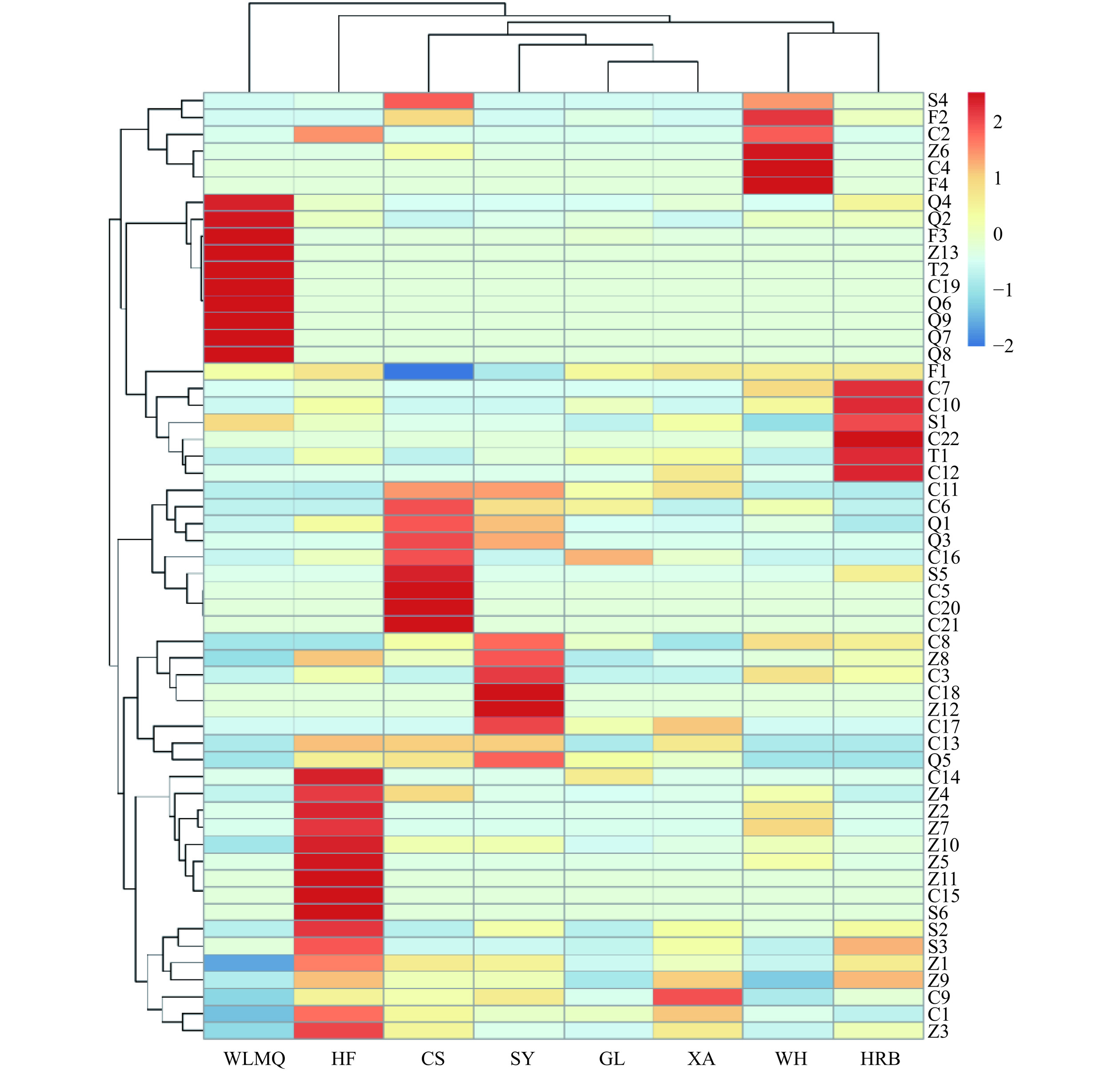
不同地区康普茶的挥发性成分热图分析如图1所示,其中不同的颜色强度代表了香气成分含量的标准化值,红色表示高含量,蓝色表示低含量,可见康普茶中挥发性物质的含量和种类呈现出一定的地区差异性。相关聚类分析结果显示,西安、桂林、沈阳和长沙康普茶挥发性物质组成较为类似,威海和哈尔滨康普茶挥发性物质组成较为类似,但这6个地区康普茶与乌鲁木齐和合肥康普茶挥发性物质相差较大。总的来说,来自中南地区(桂林和长沙)的康普茶在挥发性物质的组成上具有一定相似性,来自华东、东北、西北地区的康普茶未发现明显的地域相关性。
2.2 不同地区康普茶挥发性成分组成差异分析
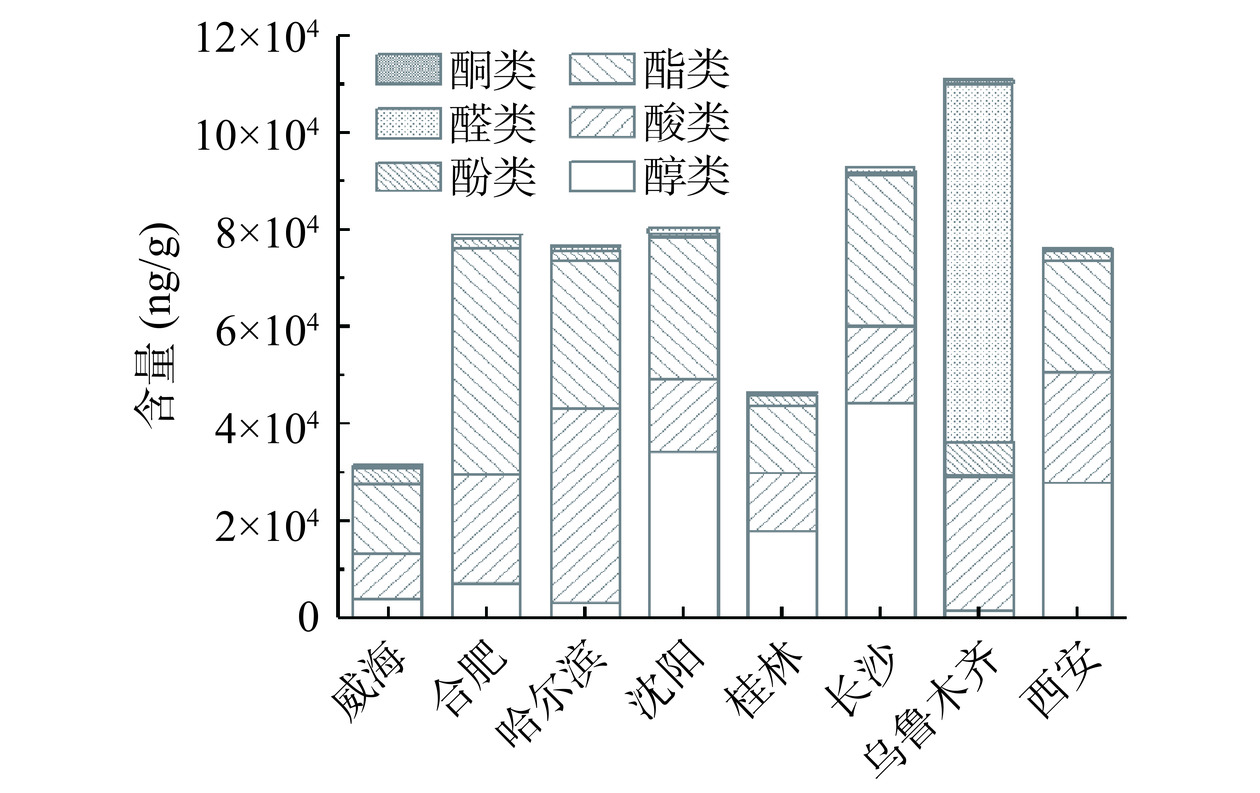
8个地区康普茶挥发性物质组成类别相似(图2),主要为醇类、酸类、酯类和酚类。长沙康普茶醇类挥发性物质含量最高,为44258.01 ng/g,占其挥发性物质总量超过47%,沈阳、西安和桂林康普茶醇类挥发性物质含量较高,分别为34226.05、27978.02和18025.80 ng/g,占其挥发性物质总含量均超过36%;哈尔滨和乌鲁木齐康普茶酸类挥发性物质含量较高,分别为39853.47和27265.03 ng/g,占其挥发性物质总含量的52%和25%,其中乌鲁木齐康普茶醛类和酚类挥发性物质含量最高,分别为74160.76和6974.63 ng/g,占其挥发性物质的总量的66%和6%,威海康普茶酚类挥发性物质含量为3319.97 ng/g,但占其挥发性物质总量的10%;合肥康普茶酯类挥发性物质含量最高,为46784.11.62 ng/g,占其挥发性物质的总量超过59%,长沙和哈尔滨康普茶酯类挥发性物质含量较高,为30998.59和30516.53 ng/g,占其挥发性物质总量超过33%,威海康普茶酯类挥发性物质含量为14645.56 ng/g,占其挥发性物质总量超过46%;西安康普茶醇类、酸类和酯类挥发性物质含量分布均匀,分别占其挥发性物质的总量的37%、30%和30%。挥发性物质总含量为乌鲁木齐>长沙>沈阳>合肥>哈尔滨>西安>桂林>威海。
不同地区康普茶中某些醇类挥发性物质带有典型的花果香味,其中乙醇(甜香)在5种康普茶(沈阳、桂林、西安、乌鲁木齐和长沙)的醇类挥发性物质中含量最高,占比均超过68%,而在其他3种康普茶(威海、合肥和哈尔滨)的醇类挥发性物质中,3-甲基-1-丁醇(威士忌酒、麦芽、苹果香气)含量最高,占比均超过29%,苯乙醇(玫瑰、丁香香气)在西安康普茶的醇类挥发性物质中含量较高,占比超过7%;在威海、沈阳、桂林和长沙康普茶检测出芳樟醇(花香、薰衣草香气),在威海、合肥、哈尔滨和沈阳康普茶中检测出反式芳樟醇氧化物(花香),有研究报道某些红茶菌菌种中的酿酒酵母可以水解糖苷键化合物,释放芳樟醇[5,7],推测芳樟醇及其氧化物是由于发酵过程中酵母菌的代谢而产生。乌鲁木齐、哈尔滨和合肥康普茶醇类挥发性物质总含量较低(均≤10%),可能是微生物转化或发生酯化等生化反应[5],但其中合肥康普茶醇类挥发性物质达12种,高级醇种类较其他地区康普茶多,这对其康普茶的风味有积极影响[17]。
不同地区康普茶中主要酸类挥发性物质是乙酸和3-甲基丁酸,它们具有比较尖锐的酸味[6],乙酸在8个地区康普茶的酸类挥发性物质中占比均超过76%,3-甲基丁酸占比均超过4%,两者含量远高于其他酸类挥发性物质,这与赵振军等[27]的研究结果一致。酸类物质的差异也与红茶菌微生物代谢有关,如在发酵过程中,醋酸菌利用乙醇生成乙酸,将葡萄糖转化为葡萄糖酸和葡萄糖醛酸;乳酸菌利用酵母菌的代谢产物生长繁殖,并产生乳酸[28]。在所有地区康普茶的挥发性物质中并未检测到乳酸,Zhang等[29]研究6种不同基底的康普茶也未检测到乳酸,但本研究中在威海和合肥康普茶中检测到了具有花果香味的乳酸乙酯。赵振军等[27]和蒋立文等[30]的研究发现,康普茶中总游离氨基酸含量随着发酵时间延长略有增加,这些游离氨基酸是最重要的芳香前体物质,如:某些支链氨基酸(亮氨酸、异亮氨酸和缬氨酸等)分解后可转化为有麦芽香气的酯类物质、有果香和酒精味的醇类物质或呈现酸甜味、腐败味、水果味或黄油味的酸类物质,推测乙酸(酸味),2-甲基丙酸(黄油和奶酪味),3-甲基丁酸(酸味和奶酪味),正辛酸(奶酪香和甜香)由此产生。
不同地区康普茶中主要酯类挥发性物质是乙酸乙酯(菠萝香气)和乙酸异戊酯(苹果香气),乙酸乙酯在7个地区康普茶(除乌鲁木齐康普茶外)的酯类挥发性物质中含量最高,占比均超过84%,乙酸异戊酯次之(除沈阳和乌鲁木齐康普茶),占比均超过4%。在沈阳康普茶中,苯乙酸乙酯(菠萝香气)的含量仅次于乙酸乙酯,3-呋喃甲酸甲酯和乙酸苯乙酯(玫瑰蜂蜜香气)是乌鲁木齐康普茶的主要挥发性酯类物质。酯类物质是康普茶中重要的挥发性化合物,大多可产生令人愉悦的水果香和花香[16],本研究中,具有典型苹果香气的2-甲基丁酸乙酯、丁酸乙酯、乙酸异戊酯和正己酸乙酯,具有典型菠萝香气的乙酸乙酯和辛酸乙酯,具有典型玫瑰香气的乙酸苯乙酯和苯乙酸乙酯等均检测出。相关研究表明红茶菌菌种中能促进产生花香、植物清香和果香风味物质的微生物多为酵母,推测酯类香气物质的产生与酵母菌的代谢密切相关[4]。
不同地区康普茶中主要的酚类挥发性物质是2,6-二叔丁基对甲苯酚,具有特殊的烤麦片味,其在6个地区(除乌鲁木齐和长沙外)康普茶的酚类挥发性物质中占比均超过52%,在乌鲁木齐和长沙康普茶中,2,4-二叔丁基苯酚是主要酚类挥发性物质,占比均超过45%。酚类物质较其他挥发性物质类别含量都较低(均<10%)。据相关文献报道[31],康普茶经发酵后,酚类物质总含量增加,可能是因为多酚在红茶菌共生体系中复杂酶的作用下被降解为小分子物质;此外酚类物质的含量也与茶叶种类有关,如在相同条件下,以绿茶发酵的康普茶酚类物质较红茶发酵的康普茶酚类物质含量高。经溯源发现,沈阳、西安、长沙康普茶的发酵基底为金骏眉,乌鲁木齐康普茶的发酵基底为滇红红茶,故推测酚类挥发性物质含量低的原因可能是采用的茶叶品种酚类物质含量较低。
不同地区康普茶中醛类(均<1.7%)和酮类(均<0.6%)挥发性物质含量相对较低,其中乌鲁木齐康普茶比较特殊,醛类挥发性物质占比超过67%,其中2,6-二甲基苯甲醛和呋喃甲醛(杏仁香甜香)的含量显著高于其他醛类挥发性物质,含量所占比例分别为75%和22%。乌鲁木齐和长沙康普茶中未检测出酮类挥发性物质,其他6个地区康普茶中酮类挥发性物质种类较少,均为1~2种,袁磊等[17]用红茶菌发酵红茶,发酵液中未检出酮类物质,与本实验结果类似。
2.3 不同地区康普茶挥发性香气物质OAV分析
OAV是代表香气化合物对样品风味贡献程度大小的一个比值,研究中认为当OAV≥1时,该香气化合物对样品风味有贡献,且OAV值越大,则其贡献越大[32],通过计算各香气物质的OAV对其进行筛选。如表2所示,对康普茶风味有贡献的特征性物质(OAV≥1)有32种。
表 2 不同地区康普茶香气物质OAV及香气描述Table 2. OAV and aroma description of Kombucha aroma substances in different regions香气物质 威海 合肥 哈尔滨 沈阳 桂林 长沙 乌鲁木齐 西安 香气描述 3-甲基-1-丁醇 1.52 4.73 <1 1.95 2.05 2.70 <1 3.74 威士忌酒香气、麦芽香、焦糖香 反式芳樟醇氧化物 2.72 1.53 1.69 5.29 <1 <1 <1 <1 花香 2-乙基-1-己醇 <1 <1 <1 <1 <1 27.71 <1 <1 玫瑰香、草本植物清香 芳樟醇 37.40 <1 <1 65.84 51.10 113.6 <1 <1 香菜、花卉、薰衣草、柠檬、玫瑰 L-薄荷醇 2.39 <1 4.58 <1 <1 <1 <1 <1 薄荷味 alpha-松油醇 1.76 <1 1.45 2.70 <1 1.20 <1 <1 油脂味,茴香,薄荷 苯乙醇 1.14 3.26 2.16 3.46 1.83 2.76 <1 5.50 蜂蜜味、玫瑰味、丁香味 壬醇 <1 1.45 <1 <1 <1 <1 <1 <1 草本植物清香、花香 月桂醇 <1 6.45 <1 <1 18.80 26.56 <1 5.22 脂肪、蜡 3-甲基-2-己醇 <1 <1 <1 <1 <1 <1 1.81 <1 —— 乙酸 6.37 14.33 29.90 11.82 9.40 11.71 21.63 17.03 酸味 2-甲基丙酸 1.58 9.29 3.65 3.13 <1 <1 <1 3.45 黄油味、奶酪味 3-甲基丁酸 1.19 9.44 7.31 1.65 1.44 1.65 2.67 4.38 酸味、奶酪味 辛酸 1.38 <1 <1 <1 <1 1.69 <1 <1 奶酪香、甜香 乙酸乙酯 2.64 8.44 5.98 5.64 2.69 5.90 <1 4.25 菠萝香气 2-甲基丁酸乙酯 969.21 2451.11 <1 <1 <1 <1 <1 <1 苹果香气 乙酸异戊酯 27.92 175.05 66.38 41.03 32.88 86.86 <1 98.70 苹果香气 正己酸乙酯 189.63 621.77 <1 62.15 36.86 355.14 <1 61.74 苹果香气 辛酸乙酯 31.13 <1 <1 <1 <1 6.55 <1 <1 菠萝香气、花香 苯乙酸乙酯 2.02 4.70 2.78 6.21 1.04 2.58 <1 1.78 水果香、甜香 乙酸苯乙酯 3.87 23.06 23.54 15.07 7.06 14.81 7.79 22.32 玫瑰香、蜂蜜味、烟草味 异戊酸乙酯 886.60 2914.93 604.81 945.95 344.65 960.21 <1 511.09 水果香 水杨酸甲酯 <1 2.02 <1 <1 <1 <1 <1 <1 薄荷味 丁酸乙酯 <1 <1 <1 <1 <1 <1 60.9 <1 苹果香 2,6-二叔丁基对甲苯酚 1.77 1.85 1.79 <1 1.62 <1 1.54 1.79 烤麦片味 4-乙基苯酚 36.48 <1 7.84 <1 2.93 20 <1 <1 酚味、香料气味 壬醛 6.50 3.47 <1 23.37 4.32 32.44 2.5 3.58 柑橘香气、草本植物清香 2,5-二甲基苯甲醛 2.18 2.15 2.27 1.34 1.68 <1 7.44 1.00 —— 辛醛 <1 <1 <1 31.90 <1 45.02 <1 <1 —— 苯甲醛 <1 <1 <1 <1 <1 <1 2.02 <1 杏仁味、焦糖香 呋喃甲醛 <1 <1 <1 <1 <1 <1 5.39 <1 面包香、杏仁味、甜香 3-羟基-2-丁酮 <1 8.85 31.73 4.91 9.06 <1 <1 11.53 黄油味、奶油味 注:香气描述来源于https://www.femaflavor.org/。 威海、合肥、哈尔滨、沈阳、桂林、长沙、乌鲁木齐和西安康普茶分别有22、20、16、18、17、19、10、16种OAV大于1的香气物质。具有酸味的3-甲基丁酸、乙酸,具有花香(玫瑰)的乙酸苯乙酯,这3种香气物质在8种康普茶中OAV均大于1,它们对康普茶的风味形成具有重要作用。2-甲基丁酸乙酯(苹果香气)是威海康普茶中OAV最大的香气物质,丁酸乙酯(苹果香气)是乌鲁木齐康普茶中OAV最大的香气物质,异戊酸乙酯(水果香气)是其他6种康普茶中OAV最大的香气物质,表明它们对康普茶香气的贡献较大,是重要的特征风味物质。除乌鲁木齐康普茶外,苯乙醇(蜂蜜和玫瑰香气)、乙酸乙酯(菠萝香气)、乙酸异戊酯(苹果香气)和苯乙酸乙酯(菠萝和花香)在其他7个地区康普茶中OAV均大于1,与之类似的还有壬醛(柑橘香气和草本植物香气),在7个地区康普茶中(除哈尔滨康普茶外)OAV均大于1。
康普茶风味酸甜爽口,苯乙醇(蜂蜜香气)、2-甲基丙酸和乙酸(酸味)对其风味轮廓的形成具有重要作用。乙醇阈值较高,为2000 mg/kg,OAV虽然小于1,但也是关键的香气物质。2-乙基-1-己醇(玫瑰、草本植物清香)、壬醇(草本植物清香、花香)、3-甲基-2己醇、丁酸乙酯(苹果香气)、水杨酸甲酯(薄荷香气)、苯甲醛(杏仁、焦糖)、呋喃甲醛(面包、杏仁、甜香)的OAV均只在1种康普茶中大于1,与之类似的还有L-薄荷醇(薄荷味)、辛酸(奶酪香、甜香)和辛酸乙酯(菠萝香气、花香)等香气物质的OAV在少数康普茶中大于1,表明不同香气物质对康普茶香气的贡献程度不同,不同地区的康普茶的关键香气物质也具有一定的相似性和差异性。
2.4 不同地区康普茶差异性成分分析
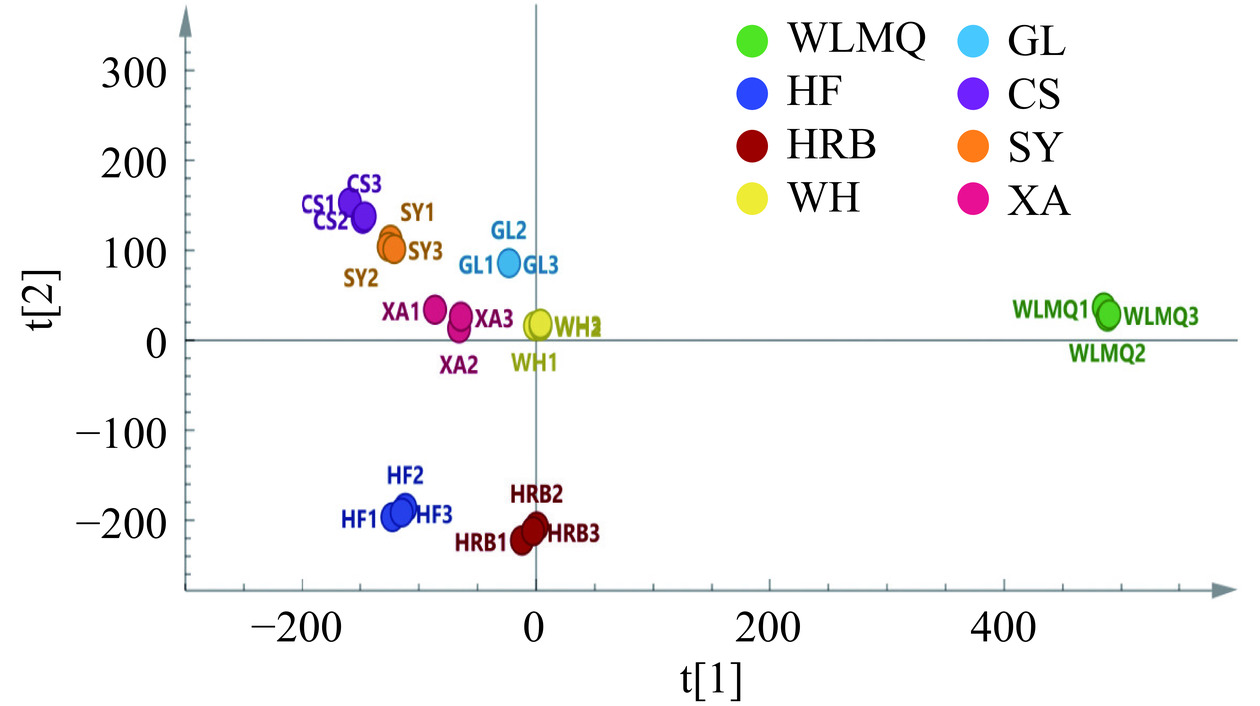
PLS-DA是一种有监督的判别分析统计学方法,可以对复杂数据进行降维处理,从而实现其可视化、判别和预测。将不同地区康普茶挥发性物质的含量作为Y变量进行PLS-DA建模。拟合模型预测成分的累计统计量R2X=0.997,模型解释率R2Y=0.990,预测能力参数Q2=0.983,都接近1,表明其稳定可靠,具有较好的解释度[33]。如图3所示,不同地区康普茶样品在PLS-DA得分图上区分较好,组内差异较小,组间分布分散。长沙、沈阳、桂林、西安和威海康普茶分布在第二象限附近,哈尔滨以及合肥康普茶分布在第三象限附近,乌鲁木齐康普茶分布在第一象限,不同地区的康普茶有较为明显的区分。
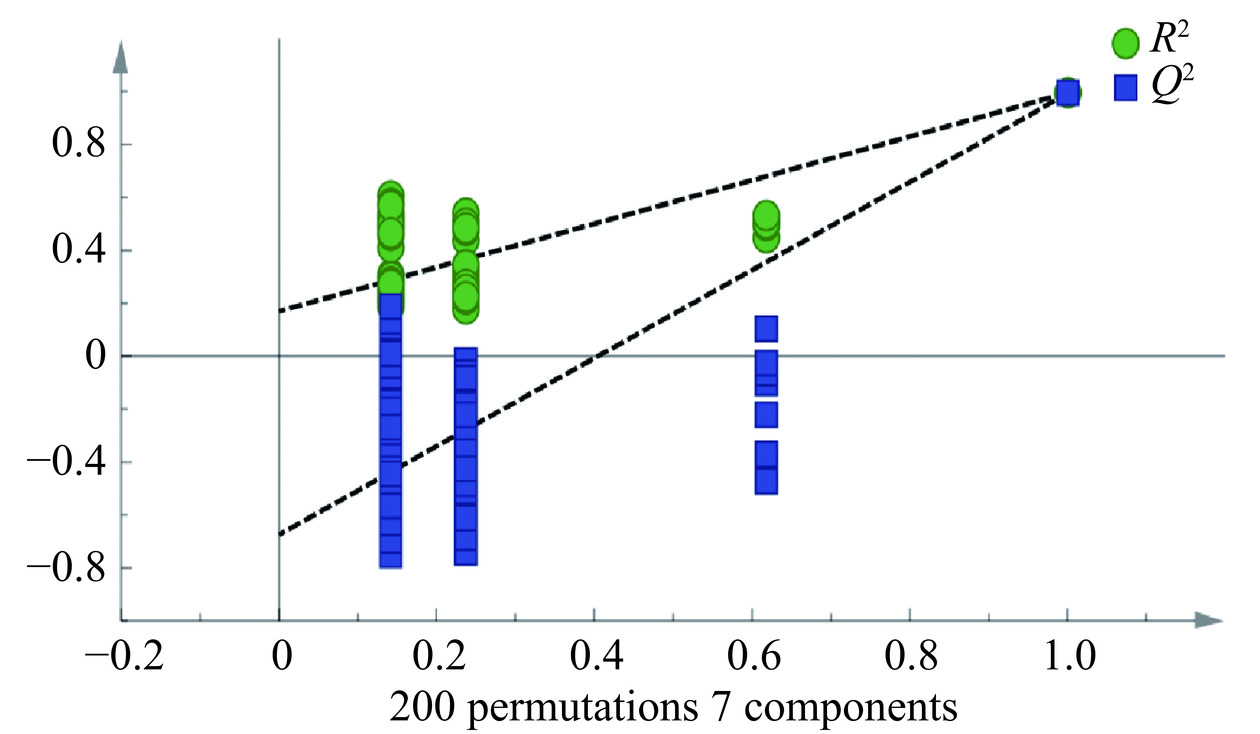
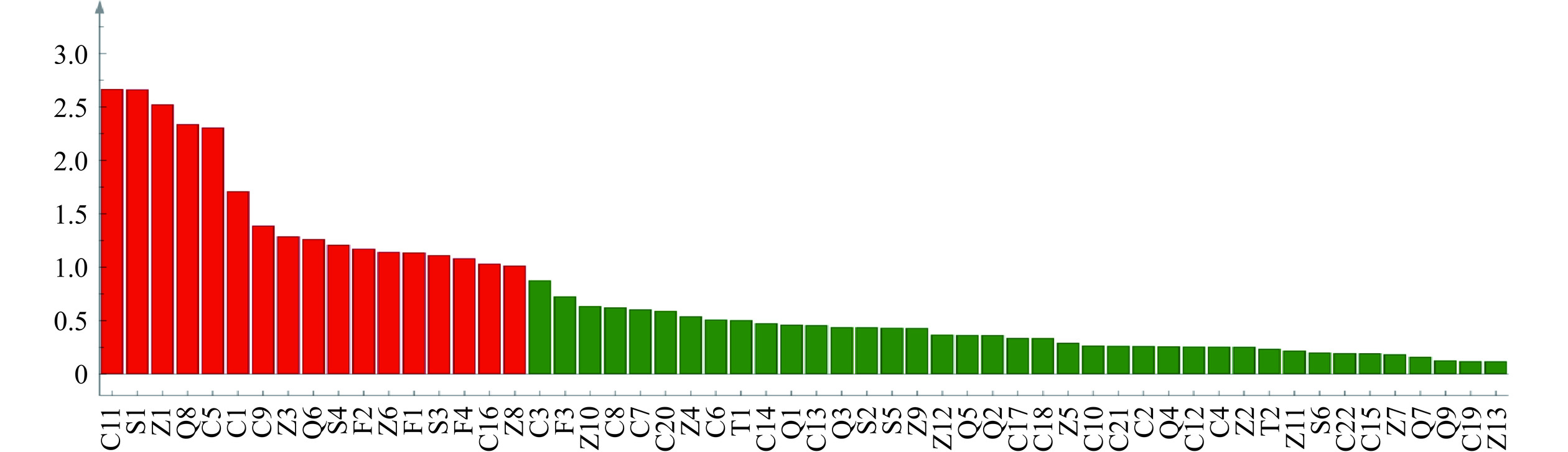
对建立的模型进行200次置换检验,如图4所示,Q2与y轴的交点在负半轴,表明该模型有效,未过拟合,可以用于解释不同地区康普茶挥发性物质的差异。为明确不同地区康普茶差异的关键物质,计算VIP以确定各物质对康普茶风味的贡献度。VIP≥1的风味物质具有较大的贡献,定义其为差异标志物[34],根据图5可知筛选出17种VIP≥1的差异标志物,分别为5种醇类(具有威士忌酒香的3-甲基-1-丁醇、具有玫瑰和草本植物清香的2-乙基-1-己醇、具有蜂蜜和玫瑰香气的苯乙醇、具有甜香的乙醇、具有草本植物清香的壬醇),3种酸类(具有酸味的乙酸、具有奶酪香的3-甲基丁酸和辛酸),4种酯类(具有菠萝香气的乙酸乙酯、乙酸异戊酯和辛酸乙酯、具有水果香气和甜香的苯乙酸乙酯),2种醛类(具有杏仁甜香的呋喃甲醛、2,6-二甲基苯甲醛),3种酚(具有烤麦片味的2,6-二叔丁基对甲苯酚、具有香料气味的4-乙基苯酚、乙基麦芽酚)。其中乙醇、乙酸和乙酸乙酯是 VIP 最高的三种物质,表明其对不同地区康普茶的风味差异影响较大。
结合OAV分析结果,17种VIP≥1的差异标志物中有14种物质OAV≥1,最终确定14种康普茶特征性差异物质:3-甲基-1-丁醇、2-乙基-1-己醇、苯乙醇、壬醇、乙酸、3-甲基丁酸、辛酸、乙酸乙酯、乙酸异戊酯、辛酸乙酯、苯乙酸乙酯、呋喃甲醛、2,6-二叔丁基对甲苯酚和4-乙基苯酚。
3. 结论
本研究以不同地区的康普茶为研究对象,对其挥发性物质组成进行分析,结果表明8个地区的康普茶挥发性物质含量与种类存在较大差异。共检测出挥发性物质56种,8个地区共同含有的挥发性物质有9种,分别为苯乙醇、3-甲基-1-丁醇、乙醇、乙酸、3-甲基丁酸、苯乙酸乙酯、乙酸苯乙酯、2,5-二甲基苯甲醛和2,6-二叔丁基对甲苯酚。
基于OAV分析,鉴定了32种呈香物质(OAV≥1),主要由醇类、酸类、酯类和醛类组成,与前人[17,30]研究结果一致,以草本植物清香、花木香、酸味和水果香气(包括苹果和菠萝香气)为主,其中水果香气具有重要地位,如2-甲基丁酸乙酯(苹果香气)是威海康普茶中OAV最大的香气物质,丁酸乙酯(苹果香气)是乌鲁木齐康普茶中OAV最大的香气物质,异戊酸乙酯(水果香气)是其他6种康普茶中OAV最大的香气物质,因而表明它们在不同地区的康普茶风味中有重要作用;采用PLS-DA分析进一步筛选出8个地区康普茶中的差异性标志物,分别为5种醇类,3种酸类,4种酯类,2种醛类,3种酚,并结合OAV分析结果可最终确定14种康普茶特征性差异物质。
本研究采用顶空固相微萃取结合气相色谱串联质谱技术,对不同地区康普茶的挥发性成分进行检测,运用OAV以及PLS-DA方法探究了不同地区康普茶的挥发性物质的种类和构成,并比较了它们的差异性,但使用的分析方法也存在一定局限性,如一些香气物质阈值缺乏等,后续将会采用不同的方法,对其特征香气进行深入探究。此外,康普茶中的挥发性香气物质的含量与种类受红茶菌中微生物组成和种群动态变化的影响,这种特殊的群落共生关系又与初始茶类型、初始糖浓度和发酵温度等因素有关,因而后续研究各因素对挥发性香气物质的影响以及发酵过程中微生物演替和香气物质变化的效应关系对于康普茶的优质化生产也十分重要。
-
表 1 不同地区康普茶挥发性成分定性定量结果(ng/g)
Table 1 Qualitative and quantitative results of volatile components of Kombucha in different regions (ng/g)
编号 物质 RI计算/文献 定性方式 威海 合肥 哈尔滨 沈阳 桂林 长沙 乌鲁木齐 西安 C 醇类 C1 3-甲基-1-丁醇 1247/1237 RI、MS 1494.15±65.05 4639.67±29.01 957.15±114.13 1914.03±51.20 2005.26±185.56 2645.44±50.56 2.57±0.12 3661.62±276.69 C2 2-庚醇 − MS 56.42±5.28 46.57±3.15 − − − − − − C3 反式芳樟醇氧化物 − MS 163.07±21.38 91.63±10.29 101.58±7.67 317.57±57.31 − − − − C4 2-壬醇 − MS 31.16±2.90 − − − − − − − C5 2-乙基-1-己醇 1525/1522 RI、MS 80.96±4.23 163.74±4.48 83.48±2.70 − 64.09±2.15 8313.34±19.29 − 58.25±3.62 C6 芳樟醇 1557/1549 RI、MS 142.13±8.11 − − 250.21±2.01 194.18±7.55 431.67±6.17 − − C7 L-薄荷醇 1649/1651 RI、MS 239.43±4.17 61.73±5.23 458.48±8.36 − − − − − C8 alpha-松油醇 − MS 151.45±14.67 − 125.10±6.56 231.95±10.82 73.35±7.32 103.16±4.19 − − C9 苯乙醇 1900/1912 RI、MS 445.43±4.83 1270.47±2.95 843.8±63.95 1349.03±42.68 711.99±91.41 1074.75±62.66 254.37±4.67 2146.86±182.52 C10 庚乙二烯乙二醇 − MS 44.82±4.77 39.89±0.19 127.24±4.08 − 26.01±4.35 − − − C11 乙醇 906/900 RI、MS 1334.8±88.90 404.38±18.39 390.27±387.44 29745.77±646.13 14570.05±746.18 30371.18±621.43 1331.18±79.16 21720.71±671.73 C12 2-壬烯-1-醇 − MS − − 117.68±5.77 − − − − 48.02±4.26 C13 2-甲基丙醇 − MS − 237.77±12.98 − 227.30±6.09 − 222.96±2.91 − 182.24±16.51 C14 正己醇 1364/1371 RI、MS − 127.57±2.11 − − 47.28±2.47 − − − C15 辛醇 1565/1561 RI、MS − 65.42±9.60 − − − − − − C16 壬醇 1665/1668 RI、MS − 103.15±12.75 − − 300.80±15.79 425.22±29.93 − 83.47±4.51 C17 月桂醇 − MS − − − 122.02±5.07 32.79±3.12 − − 76.85±4.16 C18 反-2-十一烯醇 − MS − − − 68.17±3.72 − − − − C19 3-甲基-2-己醇 − MS − − − − − − 146.84±5.95 − C20 6-甲基-1-庚醇 − MS − − − − − 557.27±47.42 − − C21 5-乙基-2-庚醇 − MS − − − − − 113.24±28.22 − − C22 樟脑 − MS − − 73.92±1.77 − − − − − S 酸类 S1 乙酸 1458/1460 RI、MS 7646.17±127.59 17194.52±481.23 35874.82±153.73 14185.25±150.93 11283.22±208.87 14050.22±565.88 25958.86±918.84 20431.72±307.55 S2 2-甲基丙酸 − MS 79.13±2.28 464.74±16.39 182.31±5.72 156.44±5.88 − − − 172.38±5.62 S3 3-甲基丁酸 − MS 584.75±43.70 4623.79±256.66 3579.84±290.04 809.61±16.15 706.71±59.97 808.12±63.54 1306.17±70.88 2146.46±68.73 S4 辛酸 2086/2089 RI、MS 690.74±141.06 43.15±1.25 126.89±3.88 − − 845.09±21.52 − − S5 己酸 1828/1827 RI、MS − − 89.64±2.09 − − 257.21±12.77 − − S6 4-甲基-2-氧代戊酸 − MS − 66.14±2.76 − − − − − − Z 酯类 Z1 乙酸乙酯 898/891 RI、MS 12330.73±206.42 39387.18±664.82 27916.21±985.52 26319.06±379.36 12544.15±669.16 27510.56±229.48 − 19840.95±736.82 Z2 2-甲基丁酸乙酯 − MS 61.06±3.99 154.42±6.53 − − − − − − Z3 乙酸异戊酯 1104/1112 RI、MS 614.20±21.38 3851.04±107.94 1460.44±68.66 902.61±56.02 723.41±56.49 1911.01±54.58 − 2171.39±65.46 Z4 正己酸乙酯 1243/1246 RI、MS 189.63±2.05 621.77±94.11 − 62.15±3.21 36.86±4.61 355.14±36.37 − 61.74±4.68 Z5 乳酸乙酯 − MS 42.20±5.67 196.21±3.21 − − − − − − Z6 辛酸乙酯 1445/1441 RI、MS 600.85±40.74 − − − − 126.41±4.22 − − Z7 乙酸异龙脑酯 − MS 37.37±4.90 69.46±1.83 − − − − − − Z8 苯乙酸乙酯 1786/1779 RI、MS 314.71±10.20 731.72±34.46 432.61±5.02 965.61±15.92 161.57±7.92 401.17±4.07 79.78±0.73 276.99±20.23 Z9 乙酸苯乙酯 1795/1801 RI、MS 73.57±2.34 438.15±16.24 447.21±19.69 286.39±4.50 134.17±8.72 281.41±8.28 148.15±12.71 424.12±18.85 Z10 异戊酸乙酯 1060/1064 RI、MS 381.24±5.39 1253.42±59.19 260.07±16.41 406.76±7.28 148.2±12.73 412.89±22.85 − 219.77±4.55 Z11 丁酸乙酯 − MS − 80.74±6.26 − − − − − − Z12 水杨酸甲酯 − MS − − − 81.52±2.87 − − − − Z13 3-呋喃甲酸甲酯 − MS − − − − − − 146.15±9.09 − Q 醛类 Q1 壬醛 1397/1400 RI、MS 97.50±15.38 52.05±4.04 − 350.56±3.28 64.77±3.69 486.53±7.07 37.53±0.88 53.67±3.94 Q2 2,5-二甲基苯甲醛 − MS 435.65±38.82 430.7±11.55 454.41±17.68 267.31±7.74 335.29±21.66 175.10±4.59 1487.23±127.39 200.02±7.75 Q3 正辛醛 − MS − − − 220.08±3.32 − 310.64±28.45 − − Q4 苯甲醛 1534/1530 RI、MS − 104.78±1.22 231.03±7.56 − − − 705.59±7.18 69.74±8.11 Q5 4-丙基苯甲醛 − MS − 101.23±9.29 − 190.76±20.48 85.41±6.89 116.05±12.59 − 59.76±4.82 Q6 呋喃甲醛 − MS − − − − − − 16157.25±249.55 − Q7 5-甲基呋喃醛 − MS − − − − − − 264.41±6.93 − Q8 2,6-二甲基苯甲醛 − MS − − − − − − 55342.1±260.03 − Q9 5-羟甲基糠醛 − MS − − − − − − 166.65±4.12 − F 酚类 F1 2,6-二叔丁基对
甲苯酚− MS 1766.20±76.65 1846.08±53.80 1791.56±7.47 766.29±38.66 1622.11±89.21 − 1536.26±223.05 1786.96±121.39 F2 4-乙基苯酚 − MS 766.18±112.32 − 164.64±6.93 − 61.52±1.73 420.09±6.36 − − F3 2,4-二叔丁基苯酚 − MS 237.5±30.24 210.64±20.08 273.44±15.65 323.76±13.82 481.66±33.33 343.01±11.08 5438.37±96.02 202.53±8.01 F4 乙基麦芽酚 − MS 550.09±2.95 − − − − − − − T 酮类 T1 3-羟基-2-丁酮 − MS − 123.83±7.06 444.23±38.48 68.80±8.32 126.78±11.79 − − 161.48±2.72 T2 环己酮 − MS − − − − − − 565.59±20.64 − 注:−表示某物质RI无法计算或未检测出;RI文献值来源于https://webbook.nist.gov/数据库。 表 2 不同地区康普茶香气物质OAV及香气描述
Table 2 OAV and aroma description of Kombucha aroma substances in different regions
香气物质 威海 合肥 哈尔滨 沈阳 桂林 长沙 乌鲁木齐 西安 香气描述 3-甲基-1-丁醇 1.52 4.73 <1 1.95 2.05 2.70 <1 3.74 威士忌酒香气、麦芽香、焦糖香 反式芳樟醇氧化物 2.72 1.53 1.69 5.29 <1 <1 <1 <1 花香 2-乙基-1-己醇 <1 <1 <1 <1 <1 27.71 <1 <1 玫瑰香、草本植物清香 芳樟醇 37.40 <1 <1 65.84 51.10 113.6 <1 <1 香菜、花卉、薰衣草、柠檬、玫瑰 L-薄荷醇 2.39 <1 4.58 <1 <1 <1 <1 <1 薄荷味 alpha-松油醇 1.76 <1 1.45 2.70 <1 1.20 <1 <1 油脂味,茴香,薄荷 苯乙醇 1.14 3.26 2.16 3.46 1.83 2.76 <1 5.50 蜂蜜味、玫瑰味、丁香味 壬醇 <1 1.45 <1 <1 <1 <1 <1 <1 草本植物清香、花香 月桂醇 <1 6.45 <1 <1 18.80 26.56 <1 5.22 脂肪、蜡 3-甲基-2-己醇 <1 <1 <1 <1 <1 <1 1.81 <1 —— 乙酸 6.37 14.33 29.90 11.82 9.40 11.71 21.63 17.03 酸味 2-甲基丙酸 1.58 9.29 3.65 3.13 <1 <1 <1 3.45 黄油味、奶酪味 3-甲基丁酸 1.19 9.44 7.31 1.65 1.44 1.65 2.67 4.38 酸味、奶酪味 辛酸 1.38 <1 <1 <1 <1 1.69 <1 <1 奶酪香、甜香 乙酸乙酯 2.64 8.44 5.98 5.64 2.69 5.90 <1 4.25 菠萝香气 2-甲基丁酸乙酯 969.21 2451.11 <1 <1 <1 <1 <1 <1 苹果香气 乙酸异戊酯 27.92 175.05 66.38 41.03 32.88 86.86 <1 98.70 苹果香气 正己酸乙酯 189.63 621.77 <1 62.15 36.86 355.14 <1 61.74 苹果香气 辛酸乙酯 31.13 <1 <1 <1 <1 6.55 <1 <1 菠萝香气、花香 苯乙酸乙酯 2.02 4.70 2.78 6.21 1.04 2.58 <1 1.78 水果香、甜香 乙酸苯乙酯 3.87 23.06 23.54 15.07 7.06 14.81 7.79 22.32 玫瑰香、蜂蜜味、烟草味 异戊酸乙酯 886.60 2914.93 604.81 945.95 344.65 960.21 <1 511.09 水果香 水杨酸甲酯 <1 2.02 <1 <1 <1 <1 <1 <1 薄荷味 丁酸乙酯 <1 <1 <1 <1 <1 <1 60.9 <1 苹果香 2,6-二叔丁基对甲苯酚 1.77 1.85 1.79 <1 1.62 <1 1.54 1.79 烤麦片味 4-乙基苯酚 36.48 <1 7.84 <1 2.93 20 <1 <1 酚味、香料气味 壬醛 6.50 3.47 <1 23.37 4.32 32.44 2.5 3.58 柑橘香气、草本植物清香 2,5-二甲基苯甲醛 2.18 2.15 2.27 1.34 1.68 <1 7.44 1.00 —— 辛醛 <1 <1 <1 31.90 <1 45.02 <1 <1 —— 苯甲醛 <1 <1 <1 <1 <1 <1 2.02 <1 杏仁味、焦糖香 呋喃甲醛 <1 <1 <1 <1 <1 <1 5.39 <1 面包香、杏仁味、甜香 3-羟基-2-丁酮 <1 8.85 31.73 4.91 9.06 <1 <1 11.53 黄油味、奶油味 注:香气描述来源于https://www.femaflavor.org/。 -
[1] KITWETCHAROEN H, PHUNG L T, KLANRIT P, et al. Kombucha healthy drink—recent advances in production, chemical composition and health benefits[J]. Fermentation,2023,9(1):48. doi: 10.3390/fermentation9010048
[2] BORTOLOMEDI B M, PAGLARINI C S, BROD F C A. Bioactive compounds in Kombucha:A review of substrate effect and fermentation conditions[J]. Food Chemistry,2022,385:132719. doi: 10.1016/j.foodchem.2022.132719
[3] de MIRANDA J F, RUIZ L F, SILVA C B, et al. Kombucha:A review of substrates, regulations, composition, and biological properties[J]. Journal of Food Science,2022,87(2):503−527. doi: 10.1111/1750-3841.16029
[4] 檀馨悦, 黎琪, 王晴, 等. 红茶菌中风味物质相关功能微生物的研究进展[J]. 食品科学,2020,41(11):327−335. [TAN X Y, LI Q, WANG Q, et al. Progresses in functional microorganisms associated with flavor compounds in Kombucha tea[J]. Food Science,2020,41(11):327−335.] doi: 10.7506/spkx1002-6630-20191022-235 TAN X Y, LI Q, WANG Q, et al. Progresses in functional microorganisms associated with flavor compounds in Kombucha tea[J]. Food Science, 2020, 41(11): 327−335. doi: 10.7506/spkx1002-6630-20191022-235
[5] ZHAO Z J, SUI Y C, WU H W, et al. Flavour chemical dynamics during fermentation of Kombucha tea[J]. Emirates Journal of Food and Agriculture,2018,30(9):732−741.
[6] SKNEPNEK A, TOMIC S, MILETI D, et al. Fermentation characteristics of novel Coriolus versicolor and Lentinus edodes Kombucha beverages and immunomodulatory potential of their polysaccharide extracts[J]. Food Chemistry,2020,342(5):128344.
[7] LÜ H P, ZHONG Q S, LIN Z, et al. Aroma characterisation of Pu-erh tea using headspace-solid phase microextraction combined with GC/MS and GC-Olfactometry[J]. Food Chemistry,2012,130(4):1074−1081. doi: 10.1016/j.foodchem.2011.07.135
[8] 杨婧娟, 赵声兰, 马雅鸽, 等. 红茶菌复合发酵饮品的配方优化及发酵工艺研究[J]. 食品科技,2019,44(11):109−115. [YANG J J, ZHAO S L, MA Y G, et al. Research on formula optimization and fermentation condition of Kombucha fermented beverage[J]. Food Science and Technology,2019,44(11):109−115.] YANG J J, ZHAO S L, MA Y G, et al. Research on formula optimization and fermentation condition of Kombucha fermented beverage[J]. Food Science and Technology, 2019, 44(11): 109−115.
[9] ZOU C, LI R Y, CHEN J X, et al. Zijuan tea-based Kombucha:Physicochemical, sensorial, and antioxidant profile[J]. Food Chemistry,2021,363(9):130322.
[10] 徐伟, 葛阳阳, 陈翠婷, 等. 基于宏基因组技术分析传统红茶菌中菌群组成及其主要代谢通路[J]. 食品工业科技,2018,39(5):119−123,129. [XU W, GE Y Y, CHEN C T, et al. Microorganism composition and main metabolic pathways analysis of traditional Kombucha by metagenomic technology[J]. Science and Technology of Food Industry,2018,39(5):119−123,129.] XU W, GE Y Y, CHEN C T, et al. Microorganism composition and main metabolic pathways analysis of traditional Kombucha by metagenomic technology[J]. Science and Technology of Food Industry, 2018, 39(5): 119−123,129.
[11] ARIKAN M, MITCHELL A L, FINN R D, et al. Microbial composition of Kombucha determined using amplicon sequencing and shotgun metagenomics[J]. Journal of Food Science,2020,85(2):455−464. doi: 10.1111/1750-3841.14992
[12] 黎琪, 王晴, 檀馨悦, 等. 利用扩增子测序技术分析不同红茶菌中微生物多样性[J]. 食品与发酵工业,2021,47(18):267−274. [LI Q, WANG Q, TAN X Y, et al. Analysis of microbial diversity from different Kombucha using amplicon sequencing[J]. Food and Fermentation Industries,2021,47(18):267−274.] LI Q, WANG Q, TAN X Y, et al. Analysis of microbial diversity from different Kombucha using amplicon sequencing[J]. Food and Fermentation Industries, 2021, 47(18): 267−274.
[13] JAYME C S J, MEIRELES M I, DE L B, et al. Kombucha:Formulation, chemical composition, and therapeutic potentialities[J]. Current Research in Food Science,2022,5:360−365. doi: 10.1016/j.crfs.2022.01.023
[14] IVANIŠOVÁ E, MEŇHARTOVÁ K, TERENTJEVA M, et al. The evaluation of chemical, antioxidant, antimicrobial and sensory properties of Kombucha tea beverage[J]. Journal of Food Science and Technology,2020,57(5):1840−1846. doi: 10.1007/s13197-019-04217-3
[15] AHMED R F, HIKAL M S, ABOU-TALEB K A. Biological, chemical and antioxidant activities of different types Kombucha[J]. Annals of Agricultural Sciences,2020,65(1):35−41.
[16] 邓雯瑾, 李启明. 红茶菌饮料工艺优化及发酵前后香气成分分析[J]. 食品与发酵科技,2020,56(3):35−40,77. [DENG W J, LI Q M. Optimization of Kombucha beverage technology and analysis of aroma components before and after fermentation[J]. Food and Fermentation Sciences and Technology,2020,56(3):35−40,77.] DENG W J, LI Q M. Optimization of Kombucha beverage technology and analysis of aroma components before and after fermentation[J]. Food and Fermentation Sciences and Technology, 2020, 56(3): 35−40,77.
[17] 袁磊, 张国华, 何国庆. 发酵条件对红茶菌发酵品质及风味的影响[J]. 食品科学,2017,38(2):92−97. [YUAN L, ZHANG G H, HE G Q. Effects of fermentation conditions on quality and flavor of Kombucha[J]. Food Science,2017,38(2):92−97.] doi: 10.7506/spkx1002-6630-201702015 YUAN L, ZHANG G H, HE G Q. Effects of fermentation conditions on quality and flavor of Kombucha[J]. Food Science, 2017, 38(2): 92−97. doi: 10.7506/spkx1002-6630-201702015
[18] PHETXUMPHOU K, VICK R, BLANC L, et al. Processing condition effects on sensory profiles of Kombucha through sensory descriptive analysis[J]. Journal of the American Society of Brewing Chemists,2022,81:99−108.
[19] 赵玉, 张玉环, 李建科, 等. GC-O结合OAV鉴定陇南初榨橄榄油关键香气成分[J]. 食品科学,2022,43(8):184−189. [ZHAO Y, ZHANG Y H, LI J K, et al. Identification of key aroma compounds in Longnan virgin olive oil by GC-O coupled with OAV analysis[J]. Food Science,2022,43(8):184−189.] ZHAO Y, ZHANG Y H, LI J K, et al. Identification of key aroma compounds in Longnan virgin olive oil by GC-O coupled with OAV analysis[J]. Food Science, 2022, 43(8): 184−189.
[20] 陶小庆, 陈钰, 欧阳宇彤, 等. 铜仁市不同区域绿茶香气有机成分分析[J]. 广东化工,2022,49(6):180−184. [TAO X Q, CHEN Y, OUYANG Y T, et al. Analysis of aroma components of green buds in different areas of Tongren City[J]. Guangdong Chemical Industry,2022,49(6):180−184.] doi: 10.3969/j.issn.1007-1865.2022.06.059 TAO X Q, CHEN Y, OUYANG Y T, et al. Analysis of aroma components of green buds in different areas of Tongren City[J]. Guangdong Chemical Industry, 2022, 49(6): 180−184. doi: 10.3969/j.issn.1007-1865.2022.06.059
[21] AL-MOHAMMADI A R, ISMAIEL A A, IBRAHIM R A, et al. Chemical constitution and antimicrobial activity of Kombucha fermented beverage[J]. Molecules,2021,26(16):5026. doi: 10.3390/molecules26165026
[22] FLAIG M, QI S, WEI G D, et al. Characterization of the key odorants in a high-grade Chinese green tea beverage (Camellia sinensis; Jingshan cha) by means of the sensomics approach and elucidation of odorant changes in tea leaves caused by the tea manufacturing process[J]. Journal of Agricultural and Food Chemistry,2020,68(18):5168−5179.
[23] ALLEGRONE G, BELLIARDO F, CABELLA P. Comparison of volatile concentrations in hand-squeezed juices of four different lemon varieties[J]. Journal of Agricultural and Food Chemistry,2006,54(5):1844−1848. doi: 10.1021/jf051206s
[24] YAN T, LIN J, ZHU J, et al. Aroma analysis of Fuyun 6 and Jinguanyin black tea in the Fu'an area based on E-nose and GC–MS[J]. European Food Research and Technology,2022,248:947−961. doi: 10.1007/s00217-021-03930-8
[25] 里奥·范海默特. 化合物香味阈值汇编[M]. 北京:科学出版社, 2015. [VAN GEMERTLJ. Compound fragrance threshold compilation[M]. Beijing:Science Press, 2015.] VAN GEMERTLJ. Compound fragrance threshold compilation[M]. Beijing: Science Press, 2015.
[26] MAO S, LU C, LI M, et al. Identification of key aromatic compounds in Congou black tea by partial least-square regression with variable importance of projection scores and gas chromatography–mass spectrometry/gaschromatography–olfactometry[J]. Journal of the Science of Food and Agriculture,2018,98(14):5278−5286. doi: 10.1002/jsfa.9066
[27] 赵振军, 周黎, 刘勤晋. 红茶菌发酵普洱茶茶汤过程中主要成分变化[J]. 食品科学,2010,31(1):79−83. [ZHAO Z J, ZHOU L, LIU Q J. Variations in major components of Pu-erh tea infusion during fermentation by Kombucha culture[J]. Food Science,2010,31(1):79−83.] ZHAO Z J, ZHOU L, LIU Q J. Variations in major components of Pu-erh tea infusion during fermentation by Kombucha culture[J]. Food Science, 2010, 31(1): 79−83.
[28] 邱卫华. 红茶菌微生物群落多样性及其分析方法的研究进展[J]. 食品工业科技,2019,40(24):311−317. [QIU W H. Research advances on microbial diversity and its analytical methods of Kombucha[J]. Science and Technology of Food Industry,2019,40(24):311−317.] QIU W H. Research advances on microbial diversity and its analytical methods of Kombucha[J]. Science and Technology of Food Industry, 2019, 40(24): 311−317.
[29] ZHANG J, VAN MULLEM J, DIAS D R, et al. The chemistry and sensory characteristics of new herbal tea-based Kombuchas[J]. Journal of Food Science,2021,86(3):740−748. doi: 10.1111/1750-3841.15613
[30] 蒋立文, 刘德华, 廖卢燕, 等. 红茶菌发酵过程中主要化学成分变化的研究[J]. 食品科学,2007,28(3):238−240. [JIANG L W, LIU D H, LIAO L Y, et al. Study on changes in major components during tea fungus fermentation[J]. Food Science,2007,28(3):238−240.] doi: 10.3321/j.issn:1002-6630.2007.03.056 JIANG L W, LIU D H, LIAO L Y, et al. Study on changes in major components during tea fungus fermentation[J]. Food Science, 2007, 28(3): 238−240. doi: 10.3321/j.issn:1002-6630.2007.03.056
[31] JAYABALAN R, RADOMIR V M, JASMINA S V, et al. A review on Kombucha tea-microbiology, composition, fermentation, beneficial effects, toxicity, and tea fungus[J]. Comprehensive Reviews in Food Science and Food Safety,2014,13(4):538−550. doi: 10.1111/1541-4337.12073
[32] 刘登勇, 周光宏, 徐幸莲. 确定食品关键风味化合物的一种新方法:“ROAV”法[J]. 食品科学,2008,344(7):370−374. [LIU D Y, ZHOU G H, XU X L. "ROAV" method:A new method for determining key odor compounds of rugao ham[J]. Food Science,2008,344(7):370−374.] doi: 10.3321/j.issn:1002-6630.2008.07.082 LIU D Y, ZHOU G H, XU X L. "ROAV" method: A new method for determining key odor compounds of rugao ham[J]. Food Science, 2008, 344(7): 370−374. doi: 10.3321/j.issn:1002-6630.2008.07.082
[33] 杨镰, 邓静, 朱建仓, 等. 五种产香酵母对发酵耙豌豆挥发性风味物质的影响[J]. 食品与发酵工业,2024,50(9):276−284. [YANG L, DENG J, ZHU J C, et al. Effect of five aroma-producing yeasts on volatile flavor compounds of fermented pulpy peas[J]. Food and Fermentation Industries,2024,50(9):276−284.] YANG L, DENG J, ZHU J C, et al. Effect of five aroma-producing yeasts on volatile flavor compounds of fermented pulpy peas[J]. Food and Fermentation Industries, 2024, 50(9): 276−284.
[34] LIU D, QI Y, ZHAO N, et al. Multivariate analysis reveals effect of glutathione-enriched inactive dry yeast on amino acids and volatile components of kiwi wine[J]. Food Chemistry,2020,329:127086. doi: 10.1016/j.foodchem.2020.127086
-
期刊类型引用(2)
1. 李嘉灏,曾瑶英,熊玉帛,佘杰海,余焯均,郭航宇,熊雯,龚林,周文化. 基于HS-SPME-GC-MS及电子舌对预制梅菜扣肉关键性风味与过熟味评价分析. 食品工业科技. 2024(21): 234-245 .  本站查看
本站查看
2. 郑训培,覃业优,巢瑾,蒋立文,李跑,刘洋. 常温低温发酵对二次发酵辣椒酱品质的影响比较. 食品安全质量检测学报. 2023(22): 210-219 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:
 下载:
下载:
