Change of the Volatile Compounds from Celery Leaves during Storage Based on HS-SPME-GC-MS and E-nose
-
摘要: 采用顶空固相微萃取技术结合气相色谱-质谱联用(headspace solid phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)和电子鼻技术分析了20.0 ℃贮藏期间芹菜叶片挥发性物质的组成和含量的变化。结果显示,采用HS-SPME-GC-MS技术从芹菜中共检测到108种挥发性物质,单萜类(43.2%~52.92%)和苯酞类(19.93%~28.97%)为主要组分,其中D-柠檬烯含量丰富(6600.64~48566.12 μg/kg)。新鲜芹菜总挥发性物质含量为165682.48 μg/kg,贮藏9 d后含量下降了40.92%,单萜类和苯酞类物质分别下降了9.72%和上升了8.98%。OAV分析结果表明芹菜叶片中共有31种OAV>1的特征挥发性物质,0~7 d特征挥发性物质有31种且组成相同,第9 d特征挥发性物质减少至29种,贮藏期间总OAV值呈下降趋势。聚类分析结果表明,0~3 d芹菜叶片以薄荷香和青草香为主,第7 d具有甜香、木香和樟脑香,第9 d后以辛辣和药草气味为主。基于电子鼻检测结果的主成分分析可以清晰区分不同贮藏时间芹菜叶片的香气,基于Pearson相关性分析,引起电子鼻响应值变化的物质主要是芹菜中萜类、醇类、芳香型挥发性物质(r≥0.80,P<0.05)。本研究的结果阐明了贮藏期间芹菜叶片挥发性物质组成和含量的变化规律,为贮藏期间芹菜新鲜度的判断提供了理论基础。Abstract: Headspace solid phase microextraction-gas chromatography-mass spectrometry (HS-SPME-GC-MS) and electronic nose (E-nose) were performed to investigate change of volatile compounds in celery leaves during storage at 20.0 ℃. The results indicated that a total of 108 volatile compounds were identified by HS-SPME-GC-MS, mainly including monoterpenes (43.2%~52.92%) and phthalides (19.93%~28.97%), in which D-limonene was abundant (6600.64~48566.12 μg/kg). The total volatile substance content of fresh celery was 165682.48 μg/kg, which decreased by 40.92% after 9 days of storage. The percent of monoterpenes and phthalides decreased by 9.72% and increased by 8.98% respectively during storage. In celery leaves, 31 substances were detected according to OAV>1. There were 31 kinds of the same characteristic volatile substances during 0~7 d and the number of characteristic volatile substances decreased to 29 at 9 d. During storage, the total OAV value decreased. The cluster analysis confirmed that the celery leaves were mainly minty and grassy odour during 0~3 d, and sweet, wood and camphorated odour at 7 d. After the 9th day, the aroma of celery leaves was spicy and herbal odour. The PCA of E-nose response data showed that E-nose could distinguish the aroma of celery leaves during different storage period. Based on Pearson correlation analysis, the main substances causing changes in the response value of E-nose were terpenoids, alcohols and aromatic volatile compounds of celery (r≥0.80, P<0.05). This study elucidates the changes of composition and content of volatile substances in celery leaves during storage, providing theoretical basis for judging the freshness of celery during storage.
-
芹菜(Apium graveolens L.)是伞形科重要蔬菜作物之一,近年来我国芹菜种植面积保持在1000万亩以上,总产量大于2500万吨[1]。研究表明,芹菜中膳食纤维可有效改善人们的肠胃功能,维生素C、维生素B2的含量远高于大白菜等蔬菜[2],其中的芹菜素、槲皮素和木犀草素等黄酮类物质具有抗炎、抗氧化和心血管保护功能[3]。
芹菜因其独特的风味而受到消费者的喜爱,但芹菜组织脆嫩、含水量高,采后易受机械伤害,失水萎蔫,随贮藏时间延长会发生腐败变质,产生异味,因此贮藏期间芹菜香气的变化是评价其品质的重要指标,确定贮藏期间芹菜特征香气成分,可为贮藏期间芹菜新鲜度的判断提供理论基础。迄今为止,关于芹菜籽、芹菜精油和加工后芹菜的挥发性物质研究较多,但对于新鲜芹菜叶片中的特征挥发性物质的组成及贮藏期间采后芹菜叶片挥发性物质的变化规律鲜有研究报道。鲍辰卿等[4]采用气相色谱-质谱/嗅闻联用仪分析4种芹菜籽油树脂,鉴定出洋川芎内酯、β-瑟林烯等物质是芹菜籽油树脂中的关键香气成分。Sellami等[5]采用顶空固相微萃取技术结合气相色谱-质谱联用分析提取的芹菜精油,鉴定出主要挥发性物质为Z-3-丁基苯酞(27.8%~38.4%)和3-丁基-4,5-二氢苯酞(34.2%~41.0%)。程碧君等[6]采用HS-SPME-GC-MS检测干燥后的芹菜叶粉,发现芹菜叶粉挥发性成分主要由柠檬烯(88.03%)和月桂烯(4.09%)组成。目前果蔬的香气成分分析技术主要有电子鼻和顶空固相微萃取技术结合气相色谱-质谱联用(headspace solid phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)等[7−8]。电子鼻(E-nose)能快捷无损区分样品[9],表征挥发性物质整体特征,但无法准确定性定量分析,而顶空固相微萃取-气相色谱-质谱联用技术可以进行挥发性物质定性定量检测[10]。HS-SPME-GC-MS结合电子鼻可以更全面、准确地分析贮藏期间芹菜叶片中挥发性物质组成和含量变化。
本研究采用顶空固相微萃取-气相色谱-质谱联用技术和电子鼻对新鲜和贮藏期间芹菜叶片香气进行分析,结合挥发性物质香气活性值(odour active values,OAV)筛选芹菜的特征挥发性物质,通过主成分分析(principal component analysis,PCA)和聚类分析(cluster analysis,CA)探究贮藏期间芹菜叶片挥发性物质的变化规律,为进一步明确采后芹菜的香气特征提供了理论基础。
1. 材料与方法
1.1 材料与仪器
芹菜 采于江苏宿迁生产基地,品种为‘瑞斯特’,采收时间2022年11月4日;3-辛醇(98%) 购于麦克林公司;正构烷烃(C7~C40标准品) 购于安谱实验公司。
PEN3型电子鼻 德国AIRSENSE公司;TriPlus 300 型顶空自动进样器、TSQ 9000 三重四极杆GC-MS/MS 美国Thermo Scientific公司;萃取头(60 μm DVB/CAR/PDMS) 美国Supelco公司。
1.2 实验方法
1.2.1 芹菜样品的处理
采收的芹菜以冷藏运输方式在4 h内运送至实验室。挑选大小基本一致、无机械伤、无黄叶和病虫害的芹菜,置于常温(20.0±1.0 ℃)、相对湿度90%±5%条件下贮藏,于0、3、7、9 d取样。每次实验样品3000 g。将采集的芹菜叶片,液氮冷冻后磨成粉末存放于−20 ℃冰箱;所有样品采集后,集中进行挥发性物质的测定。实验设三个生物学重复样品。
1.2.2 芹菜挥发性物质的萃取
HS-SPME萃取芹菜中挥发性物质,参考田震等[11]方法并做了改动。通过HS-SPME萃取芹菜叶片中的挥发性物质,将1 g芹菜叶片粉末,20 μL内标物3-辛醇(0.8 mg/mL)加到20 mL顶空瓶中,于50 ℃孵化5 min。65 μm PDMS/DVB固相微萃取头伸入顶空瓶40 mm,顶空萃取45 min,提取挥发性物质后,自动进样至气相色谱-质谱(GC-MS)系统,250 ℃解吸5 min。
1.2.3 GC-MS条件
条件参考Wu等[12]、Cai等[13]方法并略做修改。GC条件:采用HP-5石英毛细柱(30 m×0.25 mm×0.25 μm),载气为He,流速1 mL/min,不分流;升温程序:从初始温度40 ℃开始,以5 ℃/min的加热速率升温至136 ℃,维持3 min,然后1 ℃/min升温至140 ℃,维持6 min,最后10 ℃/min升高到240 ℃,维持1 min。
MS条件:在电子电离(EI)条件下,质谱的离子源温度为300 ℃,电子能70 eV,扫描范围33~500 amu。
1.2.4 芹菜挥发性物质的定性定量分析
通过NIST与Wiley标准谱库对GC-MS检测结果进行分析,选择匹配度大于80%的物质;将正构烷烃标准品按1.2.3条件进样,得到正构烷烃的保留时间,对各化合物的保留指数(RI)进行计算,并结合数据库中化合物保留指数对比鉴定。
RI=100n+100(tx−tn)/(tn+1−tn) (1) 式中:tx表示待测物质的保留时间,min,tn表示待测物质流出前正构烷烃的保留时间,min,tn+1表示待测物质流出后正构烷烃的保留时间,min,且tn<tx<tn+1,n表示碳原子数。
根据内标法(3-辛醇作为内标)对挥发性物质做定量分析,公式如下:
Ci=Cis×AiAis (2) 式中:Ci表示任一组分的含量,μg/kg,Cis表示3-辛醇的质量浓度,μg/kg;Ai表示任一组分的峰面积,Ais表示3-辛醇的峰面积。
1.2.5 芹菜香气活力值OAV的计算
通过计算香气活力值评估挥发性物质的贡献,OAV值≥1的化合物通常被认为对香气特征有很大贡献。OAV值计算公式如下:
OAV=CiTi (3) 式中:Ci表示任一组分的含量,μg/kg;Ti表示该物质在水中的阈值,μg/kg。
1.2.6 电子鼻测定
参考Wu等[12]方法并进行修改。称1 g芹菜叶片粉末于20 mL顶空瓶中,用PTFE硅胶垫盖密封并室温(20.0±1.0 ℃)平衡30 min。样品采集时间:180 s;传感器清洗时间:60 s;进样流量:150 mL/min。设置5个生物学重复。PEN3 E-nose各个传感器及对应的性能描述如表1所示[14]。
表 1 电子鼻传感器性能描述Table 1. Function description of E-nose sensors传感器名称 性能描述 W1C 对芳香性化合物敏感 W5S 对氮氧化物敏感 W3C 对氨类、芳香族化合物敏感 W6S 对氢类物质敏感 W5C 对烷烃、芳香族化合物敏感 W1S 对甲基类敏感 W1W 对无机硫化物、萜烯类敏感 W2S 对醇类、部分芳香族化合物敏感 W2W 对芳香族化合物、有机硫化物敏感 W3S 对烷烃敏感 1.3 数据处理
电子鼻数据为5次生物学重复测定的平均值,GC-MS数据为3次生物学重复测定的平均值。利用Origin 2022b绘制雷达图、主成分分析(PCA)和Pearson相关性分析,使用SPSS 17.0统计软件进行数据分析,以P<0.05表示差异显著。
2. 结果与分析
2.1 贮藏期间芹菜叶片挥发性物质的HS-SPME-GC-MS分析
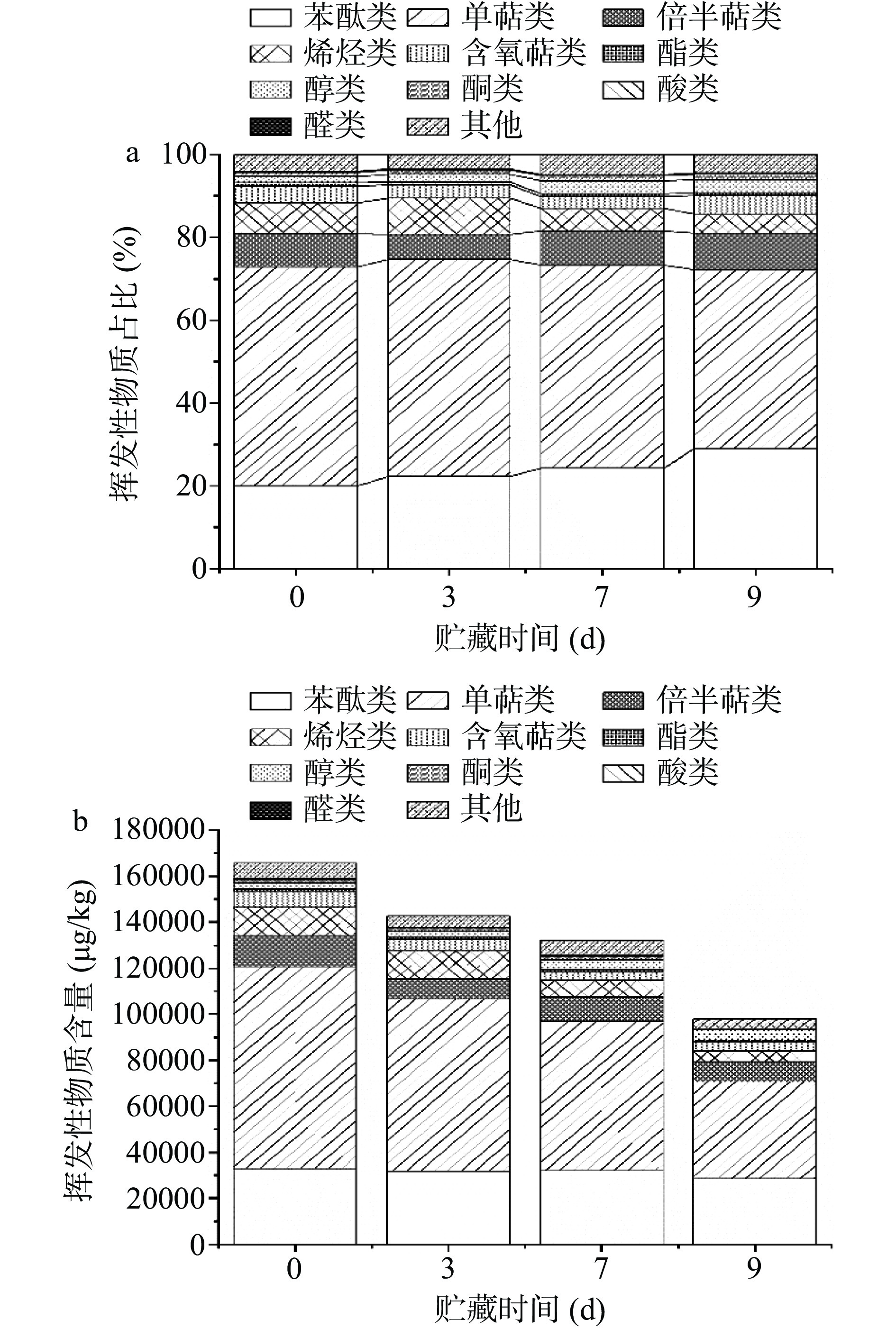
利用HS-SPME与GC-MS联用的方法,分析贮藏期间芹菜挥发性物质成分及含量。共鉴定出108种化合物(表2),新鲜和贮藏期间芹菜挥发性物质均稳定在105种以上,远多于文献报道的74种[15];108种物质中醇类21种、倍半萜类21种、酯类12种、单萜类11种、烯烃类7种、苯酞类6种、酮类6种、酸类4种、含氧萜类化合物4种、醛类2种和14种其他类物质,其中醇类和倍半萜类物质种类数量远大于现有文献报道[15−16]。贮藏期间芹菜中新增的挥发性物质有α-愈创烯、3-(2,6,6-三甲基-1-环己烯基)-2-丙烯-1-醇和5,7-十二烷二炔-1,12-二醇,其中后两种物质为醇类。由图1可知,新鲜芹菜总挥发性物质含量为165682.48 μg/kg,其中单萜类和苯酞类物质是主要的挥发性物质,占比分别为52.92%、19.93%,与Turner等[17]、Xia等[18]研究结果相似。贮藏9 d期间总挥发性物质含量下降了40.92%,主要是单萜类物质和烯烃类物质含量减少,其中减少最多的单萜类物质下降了51.76%。
表 2 不同贮藏时间芹菜叶片的挥发性物质组成和含量Table 2. Composition and content of volatile compounds in celery leaves during storage序号 名称 保留指数 鉴定方式 含量(μg/kg) 计算值 参考值 0 d 3 d 7 d 9 d 1 α-蒎烯 936 931 MS/RI 222.64±0.55 68.08±3.03 89.57±3.51 48.88±3.78 2 β-蒎烯 981 980 MS/RI 5209.18±185.08 5332.69±23.36 9975.71±528.39 6671.74±11.19 3 D-柠檬烯 1055 1031 MS/RI 48566.12±1907.83 18653.08±133.41 6600.64±210.84 8983.19±30.34 4 (R)-异香芹萜烯 1031 1028 MS/RI 11860.51±988.06 29213.47±728.91 26106.4±929.24 13106.58±118.35 5 罗勒烯 1048 1026 MS/RI 2349.49±126.39 2321.74±244.13 2313.26±111.98 913.78±48.57 6 γ-松油烯 1060 1056 MS/RI 2105.67±6.21 1322.57±134.56 1227.52±8.66 939.57±26.37 7 别罗勒烯 1129 1129 MS/RI 16651.89±78.57 17433.27±533.26 17151.4±2004.12 11087.91±1981.47 8 萜品油烯 1088 1083 MS/RI 104.74±0.03 71.05±0.72 47.28±1.72 25.72±0.41 9 左旋香芹酮 1246 − MS 161.42±12.12 108.99±0.25 152.31±11.75 70.03±2.56 10 1,3,8-对薄荷-三烯 1027 1118 MS/RI 232.47±17.24 96.28±9.87 731.14±40.51 360.43±29.17 11 2-甲基-1-(2,2,3-三甲基
环亚丙基)-1-丙烯1143 − MS 210.92±0.01 149.2±5.2 354.63±11.23 85.23±4.77 单萜类(11种) 87675.05 74770.42 64749.86 42293.06 12 β-榄香烯 1391 1366 MS/RI 291.29±37.73 339.89±28.56 266±5.88 225.1±21.76 13 罗汉柏烯 1412 1429 MS/RI 121.95±14.53 126.97±8.84 85.28±2.46 69.99±5.89 14 雪松烯 1426 1433 MS/RI 31.11±3.56 24.6±3.56 22.68±0.27 15.82±0.64 15 石竹烯 1433 1415 MS/RI 1709.07±68.73 1254.44±109.76 2105.93±49.56 1795.75±71.18 16 环庚烯 1440 1531 MS/RI 157.17±2.51 172.99±9.24 152.73±7.62 121.78±3.58 17 γ-榄香烯 1443 1441 MS/RI 188.49±9.41 89.14±0.02 158.98±0.2 123.87±33 18 α-愈创烯 1455 1438 MS/RI ND 39.43±1.01 30.26±2.16 20.02±4.63 19 (-)-异丁香烯 1474 1428 MS/RI 107.6±19.11 114.45±9.74 96.4±1.96 75.44±12.68 20 α-律草烯 1455 1451 MS/RI 2065.02±78.45 1191.26±84.63 1746.71±422.22 1821.48±237.06 21 β-长叶蒎烯 1510 1405 MS/RI 138.88±23.79 73.4±8.62 84.93±3.13 65.34±7.81 22 α-姜烯 1532 1480 MS/RI 1588.4±249.32 194.68±19.23 1042.92±15 796.09±8.95 23 β-瑟林烯 1572 1486 MS/RI 2375.8±28.65 1145.92±15.94 1759.27±183.17 1304.21±115.83 24 α-芹子烯 1597 1505 MS/RI 3154.13±152.76 2809.29±73.4 2167.21±41.07 1382.34±73.62 25 Α-布黎烯 1603 1505 MS/RI 31.99±4.7 25.96±5.2 26.7±1.45 23.13±2.3 26 β-姜黄烯 1607 1512 MS/RI 370.67±2.11 222.73±25.59 320.66±29.78 187.3±7.55 27 α-衣兰油烯 1612 1449 MS/RI 84.16±2.03 82.83±3.69 72.89±0.83 57.2±4.42 28 Δ-杜松烯 1616 1486 MS/RI 96.79±9.02 95.56±3.11 82.09±2.72 54.27±7.58 29 3,7(11)-蛇床二烯 1638 1527 MS/RI 68.72±2.99 69.01±7 51.03±2.41 41.73±5.1 30 Α-姜黄烯 1607 1486 MS/RI 493.05±37.72 421.97±18.77 416.22±1.82 355.53±48.19 31 β-橄榄烯 1629 1381 MS/RI 41.57±4.1 11.53±0.22 21.79±1.68 14.3±5.64 32 愈创木烯 1630 1504 MS/RI 23.92±5.22 48.45±0.68 35.06±5.04 17.79±1.49 倍半萜类(21种) 13139.78 8554.5 10745.74 8568.48 33 α-红没药烯 1271 − MS 34.57±0.89 19.87±2.33 39.19±7.09 20.67±4.62 34 14-羟基石竹烯氧化物 1680 − MS 87.06±8.6 48.98±1.16 59.09±1.92 36.99±1.69 35 反式氧化柠檬烯 1139 − MS 6535.03±114.78 4600.21±118.43 3452.99±328.7 4190.53±160.46 36 二氧化萜二烯 1289 1294 MS/RI 116.28±6.18 71.98±7.68 58.12±2.34 75.12±4.66 含氧萜类(4种) 6772.94 4741.04 3609.39 4323.31 37 波斯菊萜 1080 1132 MS/RI 48.08±2.88 75.97±3.37 105±6.92 55.7±1.54 38 对伞花烃 1153 1026 MS/RI 171.63±4.39 130.84±8.09 147.45±17.86 106.29±6.4 39 5-戊基-1,3-环己二烯 1160 1161 MS/RI 4344.89±177.57 2305.22±178.3 1155.44±112.72 798.2±44.27 40 1,2,3,6-四甲基双环[2.2.2]-2,5-辛二烯 1351 − MS 40.72±1.99 33.44±3.42 45.82±5.88 36.86±5.87 41 3-苯基-1,4-环己二烯 1410 − MS 101.84±12.4 27.4±5.31 28.21±0.26 45.68±2.52 42 新植二烯 1827 1836 MS/RI 7689.84±368.98 9817.77±384.98 5808.3±338.97 3524.76±295 43 3,7,11,15-四甲基-2-十六烯 1809 − MS 121.28±17.51 65.99±4.2 44.31±2.26 14.58±0.85 烯烃类(7种) 12518.28 12456.63 7334.53 4582.07 44 正丁基苯酞 1621 1629 MS/RI 5578.92±208.39 4036.19±187.99 3931.33±66.97 3317.37±176.35 45 3-六氢-丁基苯酞 1597 1645 MS/RI 237.35±29.12 337.67±38.22 401.32±7.05 451.51±106.04 46 Z-亚丁基苯酞 1772 1666 MS/RI 112.69±9.28 141.3±17.26 190.14±26.64 199.43±16.58 47 洋川芎内酯A 1811 − MS 14479.04±3308.34 13161.95±336.64 5961.69±455.57 5702.18±210.15 48 瑟丹酸内酯 1823 1726 MS/RI 12379.44±350.65 13844.74±2648.78 20911.30±499.93 17696.24±1321.43 49 (E)-藁本内酯 1833 1809 MS/RI 237.05±5.26 289.91±14.08 609.89±62.96 993.16±149.77 苯酞类(6种) 33024.49 31811.76 32005.65 28359.89 50 惕各酸紫苏醇 1008 − MS 180.22±2.83 140.6±8.34 165.51±22.5 152.45±27.46 51 芥子醇 1058 1295 MS/RI 16.15±1.71 4.41±0.34 7.37±0.56 10.67±2.6 52 桃金娘烯醇 1091 1191 MS/RI 87.66±10.76 36.61±1.28 54.06±5.68 25.02±0.84 53 3-(2,6,6-三甲基-1-环己烯基)-
2-丙烯-1-醇1180 − MS ND 4.58±0.43 5.23±0.6 4.7±0.84 54 顺式-马鞭烯醇 1118 1141 MS/RI 142.79±6.92 114.83±1.14 135.87±0.54 85.94±4.08 55 反式-薄荷基-2,8-二烯-1-醇 1122 1100 MS/RI 157.39±1.34 189.32±8.15 247.92±7.67 142.32±2.04 56 对-䓝-1,5-二烯-1-醇 1173 1170 MS/RI 154.7±15.11 390.59±5.41 832.26±4.9 769.64±25.85 57 异香芹醇 1229 1231 MS/RI 24.49±0.24 14.6±0.38 10.55±0.13 6.41±0.58 58 (Z)-3,7,11-三甲基-2,10-十二碳烯-1-醇 1867 1668 MS/RI 57.7±3.84 64.68±4.06 120.82±7.62 127.52±41.27 59 (1R,3S,5S,7R)-2,8-二亚甲基-5-丙-1-烯-2-基环癸烷-1,3,7-三醇 1496 − MS 19.55±0.73 13.98±1.32 14.35±1.63 14.79±2.34 60 10-羟基香叶醇 1199 2652 MS 37.13±8.04 68.83±1.16 94.31±10.79 68.92±3.87 61 正三十七醇 1214 − MS 20.27±4.4 2.29±0.05 4.98±0.38 11.37±0.6 62 反式-香芹醇 1221 1219 MS/RI 482.49±14.88 580.33±23.78 734.71±36.12 378.79±8.1 63 (Z)-异香芹醇 1229 1231 MS/RI 33.16±1.37 33.77±2.75 24.22±4.09 21.23±0.57 64 5,7-十二烷二炔-1,12-二醇 1226 1724 MS/RI ND 19.29±0.6 16.86±0.51 7.49±2.65 65 柠檬烯二醇 1341 1321 MS/RI 264.69±37.94 186.99±5.72 193.69±0.08 92.89±9.77 66 Α-菖蒲醇 1718 1648 MS/RI 34.06±1.69 14.5±0.78 15.99±0.9 10.97±1.98 67 紫苏醇 1617 1302 MS/RI 236.43±45.61 195.03±11.96 336.02±13.19 233.27±29.71 68 L-紫苏醇 1198 1994 MS 124.19±10.66 100.78±9 111.27±10.47 77.21±2.98 69 叶绿醇 1830 2116 MS/RI 341.05±31.03 451.87±3.19 926.89±59.99 770.95±52.55 70 13-十七炔-1-醇 1965 − MS 47.39±3.4 18.62±1.29 64.32±3.8 66.68±3.78 醇类(21种) 2461.51 2646.5 4117.2 3079.23 71 (+)-二氢青芹酮 1206 1242 MS/RI 734.62±2.07 626.51±8.88 532.89±57.25 461.66±43.1 72 5-甲基-2-癸烯-4-酮 1286 − MS 44.22±4.8 174.54±3.59 231.26±35.49 126.26±8.43 73 香叶基丙酮 1464 1452 MS/RI 119.96±8.96 113.63±9.41 123.88±1.52 82.53±4.96 74 2-丁基-5-甲基-3-(2-甲基-2-丙烯基)环己酮 1622 − MS 60.76±1.91 46.01±3.01 33.55±8.47 22.92±7.64 75 1,1-二甲基-1,2,3,5,7,8,9,9a-八氢-
6-苯并环庚烯酮1777 − MS 851.09±77.1 585.71±1.43 778.34±80.78 503.21±18.35 76 5-烃基-10,10-二甲基-6-甲基双环
[7.2.0]-2-十一酮1911 − MS 4.13±0.7 2.84±0.29 7.96±0.1 7.6±1.29 酮类(6种) 1814.78 1549.24 1707.88 1204.18 77 碳酸环己烯酯 852 − MS 215.48±14.33 108.82±8.49 116.48±12.71 28.31±2.2 78 2,5-十八碳二炔酸甲酯 1092 − MS 29.5±3.04 19.52±1.68 17.47±3.5 11.97±0.83 79 异胆酸乙酯 2058 − MS 7.69±1.62 6.22 4.75±0.99 3.25±0.78 80 乙酸芳樟酯 984 1246 MS/RI 101.26±5.47 140.21±13.13 162.83±14.68 162.6±9.84 81 (-)-乙酸香芹酯 1328 1339 MS/RI 567.43±48.44 428.11±1.81 451.9±36.37 384.15±47.25 82 9-十八烯-12-炔酸甲酯 1367 − MS 15.31±2.13 15.58±1.17 13.06±0.51 7.92±1.26 83 (E)-10-十七烯-8-炔酸甲酯 1366 − MS 23.27±1.69 ND ND ND 84 14-去氧-12-羟基穿心莲内酯 1698 − MS 30.69±0.53 17.88±0.74 26.25±0.78 12.3±1.29 85 10,13-十八碳二炔酸甲酯 1701 − MS 23.63±2.73 13.86±1.71 20.54±0.59 15.43±1.97 86 10,12-十八碳二炔酸甲酯 1764 − MS 62±14.55 19.96±1.82 27.88±1.19 20.92±3.01 87 反式-乙酸松香芹酯 1248 1298 MS/RI 103.06±8.31 108.91±6.45 75.06±10.21 82.56±11.55 88 (S,E)-2,5-二甲基-4-乙烯基-2,5-
二烯-1-乙酸酯1274 − MS 57.77±1.73 62.14±0.59 59.32±6.97 44.73±8.25 酯类(12种) 1237.09 941.21 975.54 774.14 89 2-异丙烯基-5-甲基-4-烯己醛 1074 − MS 169.22±21.49 108.12±7.98 66.7±6.06 45.97±5.11 90 5β-胆甾-3-酮乙缩醛 1899 − MS 2.67±0.27 1.53±0.14 1.7±0.39 1.26±0.28 醛类(2种) 171.89 109.65 68.4 47.23 91 10,12-二十八二炔酸 1336 − MS 25.31±2.14 19.83±1 44.09±0.82 16.42±0.17 92 6-乙烯基-4,5,6,7-四氢-3,6-二
甲基-5-苯并呋喃乙酸1845 − MS 204.35±13.29 196.56±10.47 146.89±11.16 219.25±6.76 93 十九碳烯酸 1804 − MS 16.44±0.77 6.06±0.7 7.08±0.03 ND 94 环丙烷丁酸 1918 − MS 35.86±3.57 6.37±1.19 16.06±1.46 10.93±1.53 酸类(4种) 281.96 228.82 214.12 246.6 95 1-亚甲基-1H-茚 1189 1098 MS/RI 468.2±23.92 461.74±14.24 625.45±63.8 357±27.05 96 6-甲基四氢化萘 1269 1247 MS/RI 30.26±3.3 33.57±2.66 40.57±3.73 27.33±2.44 97 五甲基苯 1281 1281.8 MS/RI 155.45±16.68 138.37±23.19 170.46±18.45 122.88±13.84 98 黄樟素 1292 1288 MS/RI 1008.32±8.51 758.45±19.82 858.14±62.6 589.47±71.13 99 2,6-二甲基萘 1457 1400 MS/RI 53.84±1.04 68.52±6.26 114.82±32.02 56.48±0.21 100 1-乙基萘 1478 1400 MS/RI 76.33±7.89 61.7±4.28 70.29±11.73 65.43±11.32 101 4a,8-甲基-2-(丙基-1-烯-2-基)-
1,2,3,4,4a,5,6,7-八氢萘1520 1492 MS/RI 112.51±31.92 92.05±1.77 42.06±8.68 72.75±9 102 3-(2-甲基-1-丙烯基)-1H-茚 1620 − MS 48.52±2.9 26.29±0.23 62.55±2.16 29.89±1.84 103 3,4-二乙基联苯 1784 1692 MS/RI 10.54±0.38 8.42±0.37 11.22±0.45 9.18±1.14 104 1,1,3a-三甲基-7-甲基-十氢-1H-环丙[a]萘 1633 1692 MS/RI 90.48±19.99 111.09±8.23 17.59±5.14 77.46±0.77 105 缬草素 1627 1536.9 MS/RI 24.54±2.02 27.33±3.94 20.13±3.08 37.1±4.39 106 9,10-二氢-11,12-二羧酸-9,10-二乙基蒽 1881 − MS 73.46±9.06 46.17±7.77 91.05±10.9 107.97±0.9 107 1-甲基萘 1300 1325 MS/RI 4413.75±21.74 3068.44±75.95 4279.1±349.46 2853.03±236.66 108 4,6,6-三甲基-2-(3-甲基-1,3-二
烯基)-3-氧杂三环[5.1.0.]丁烷1876 − MS 18.51±2.34 12.6±1.72 16.48±1.99 8.81±0.79 其他(14种) 6584.71 4914.74 6419.91 4414.78 总计 165682.48 142724.51 131948.22 97892.97 注:“保留指数”中“参考值”来自https://webbook.nist.gov;“−”表示未查到;“鉴定方式”中“MS”表示质谱定性;“RI”表示保留指数定性;“ND”表示该物质未被检出。 单萜类物质是芹菜挥发性物质中含量最高的物质,贮藏期间含量和占比呈下降趋势,含量从87675.05 μg/kg降低至42293.06 μg/kg,占比从52.92%下降至43.20%。其中具有清新的柑橘、薄荷气味的D-柠檬烯和提供青草香和橙花油香气的别罗勒烯是单萜类物质中占比较大的挥发性物质[19]。贮藏期间芹菜叶片中D-柠檬烯和别罗勒烯分别占挥发性物质总量的55.39%~21.24%、10.05%~11.32%,D-柠檬烯含量下降了81.5%,别罗勒烯第9 d含量较第0 d下降了33.41%。
倍半萜类物质在新鲜芹菜中含量为13139.78 μg/kg,贮藏期间占比从第0 d的7.93%下降到第3 d的5.99%,第9 d增大至8.75%。倍半萜类物质中丁香、松油香的β-瑟林烯和木香的石竹烯被认为是芹菜香气重要的贡献者[20]。贮藏期间β-瑟林烯和石竹烯含量在第3 d分别下降了51.77%、26.6%,第7 d含量上升,分别是第3 d的1.5倍、1.6倍。
苯酞类物质是芹菜中主要的挥发性物质,贮藏期间占比逐渐上升,从19.93%增加至28.97%,含量从33024.49 μg/kg降低至28359.89 μg/kg。具有药草香和芹菜特殊气味的苯酞类物质洋川芎内酯A和瑟丹酸内酯被文献报道为芹菜特征香气物质[21]。新鲜芹菜中洋川芎内酯A和瑟丹酸内酯含量分别为14479.04、12379.44 μg/kg。贮藏期间洋川芎内酯A呈下降趋势,下降了60.62%,瑟丹酸内酯含量上升了42.95%。
贮藏期间芹菜中的烯烃类物质种类较少,含量占比为7.56%~4.68%;醇类、酯类、醛类、酸类和酮类物质含量较少,共占比为3.60%~5.47%。
本研究还检测到目前少有报道的(R)-异香芹萜、α-芹子烯、α-律草烯、新植二烯和1-甲基萘等物质。(R)-异香芹萜具有类似柠檬的香气[22],在新鲜芹菜中含量丰富,为11860.51 μg/kg。淡丁香气味的α-芹子烯和甜橙香气的α-律草烯[12],贮藏期间含量分别下降了56.17%、11.79%。新植二烯具有清香气且刺激性较强[23],新鲜芹菜中新植二烯含量为7689.84 μg/kg,贮藏期间含量降低了54.16%。1-甲基萘有类似萘的特殊气味[24],贮藏期间含量下降了35.36%。
2.2 贮藏期间芹菜特征挥发性物质的OAV分析
HS-SPME-GC-MS分析获得的各物质含量并不能确定贮藏期间芹菜的关键和特征性挥发性物质,故而采用挥发性物质香气活性值(OAV)对贮藏期间芹菜关键挥发性物质进行筛选。当OAV值≥1时,该化合物对芹菜整体香气有一定影响,当OAV值>10时认为该化合物对芹菜整体香气贡献极大。如表3所示,贮藏期间芹菜共有31种挥发性物质OAV值大于1,主要是萜类和苯酞类物质,0~7 d特征挥发性物质有31种且组成相同,第9 d特征挥发性物质减少了2种,减少的是萜品油烯和对伞花烃。
表 3 不同贮藏时间芹菜叶片OAV>1的特征挥发性物质Table 3. Characteristic volatile compounds with OAV higher than 1 in celery leaves during storage化合物 阈值(μg/kg) OAV值 气味描述 0 d 3 d 7 d 9 d 桃金娘烯醇 7 12.52 5.23 7.72 3.57 檀木香、薄荷香 L-紫苏醇 8 15.52 12.60 13.91 9.65 奶香,甜香 10-羟基香叶醇 40 0.93 1.72 2.36 1.72 甜香,玫瑰花香 反式-香芹醇 250 1.93 2.32 2.94 1.52 辛辣,香菜气味,薄荷香 香叶基丙酮 60 2.00 1.89 2.06 1.38 清香,略带甜蜜的玫瑰香 (-)-乙酸香芹酯 46 12.34 9.31 9.82 8.35 薄荷香,草药香 α-蒎烯 6 37.11 11.35 14.93 8.15 清香,木香 β-蒎烯 140 37.21 38.09 71.26 47.66 青草香,带一点辛辣 D-柠檬烯 34 1428.42 548.62 194.14 264.21 柑橘香,松树气味,薄荷香 罗勒烯 34 69.10 68.29 68.04 26.88 甜香,草香,木香 γ-松油烯 260 8.10 5.09 4.72 3.61 油脂气味,木香,柑橘香 别罗勒烯 34 489.76 512.74 504.45 326.12 草香、花香并伴有橙花油香气 萜品油烯 41 2.55 1.73 1.15 0.63 松木香气,微带甜的柑橘香 左旋香芹酮 7 24.09 16.27 22.73 10.45 草香,薄荷脑香 对薄荷-1,3,8-三烯 39 5.92 2.45 18.60 9.17 木香,樟脑香 石竹烯 55 31.07 22.81 38.29 32.65 甜味,木香,胡椒气味 β-瑟林烯 1000 2.38 1.15 1.76 1.30 草香 (-)-异丁香烯 10 10.76 11.45 9.64 7.54 丁香香气,松木气味 α-律草烯 120 17.21 9.93 14.56 15.18 淡的丁香气味 α-芹子烯 1000 3.15 2.81 2.17 1.38 橘香、甜香和泥土香 Δ-杜松烯 2 64.53 63.71 54.73 36.18 木香 α-红没药烯 5 6.57 3.78 7.45 3.93 果香 反式氧化柠檬烯 100 65.35 46.00 34.53 41.91 果香,柑橘香 对伞花烃 120 1.43 1.09 1.23 0.89 柠檬香,小茴香气味 2,6-二甲基萘 10 5.38 6.85 11.48 5.65 沥青气味 1-甲基萘 8 551.72 383.56 534.89 356.63 有类似萘的特殊气味 正丁基苯酞 70 79.70 57.66 56.16 47.39 芹菜香味,草香 3-六氢-丁基苯酞 70 3.39 4.82 5.73 6.45 药草香,芹菜气味 洋川芎内酯A 140 103.42 94.01 42.58 40.73 药草香 瑟丹酸内酯 270 45.85 51.28 77.45 65.54 药草香,芹菜气味 (E)-藁本内酯 140 1.69 2.07 4.36 7.09 甜香,辛辣 注:所用阈值参考文献[25−27],挥发性物质气味描述见http://www.flavornet.org/index.html。 新鲜(0 d)芹菜叶片中,D-柠檬烯、别罗勒烯、1-甲基萘和洋川芎内酯A的OAV值大于100,提示这些物质可能是新鲜芹菜的关键香气成分。贮藏期间,D-柠檬烯的OAV值呈下降趋势,别罗勒烯OAV值第0、3、7 d基本不变,第9 d开始下降,表明贮藏期间芹菜叶片中薄荷香强度逐渐降低,草香和橙花油香气减弱。新鲜芹菜中10-烃基香叶醇OAV值<1,贮藏9 d后萜品油烯、对伞花烃的OAV值<1,表明具有玫瑰花香的10-烃基香叶醇是贮藏1~9 d芹菜的特征挥发性物质,提供松木香的萜品油烯和提供柠檬香的对伞花烃是新鲜和贮藏1~7 d的芹菜的特征挥发性物质。具有药草香和芹菜气味的苯酞类物质瑟丹酸内酯在第7 d的OAV值较大,表明第7 d芹菜叶片中药草香和芹菜气味浓郁。此外,贮藏期间具有类似萘特殊气味的1-甲基萘OAV值(356.63~551.72)较大。
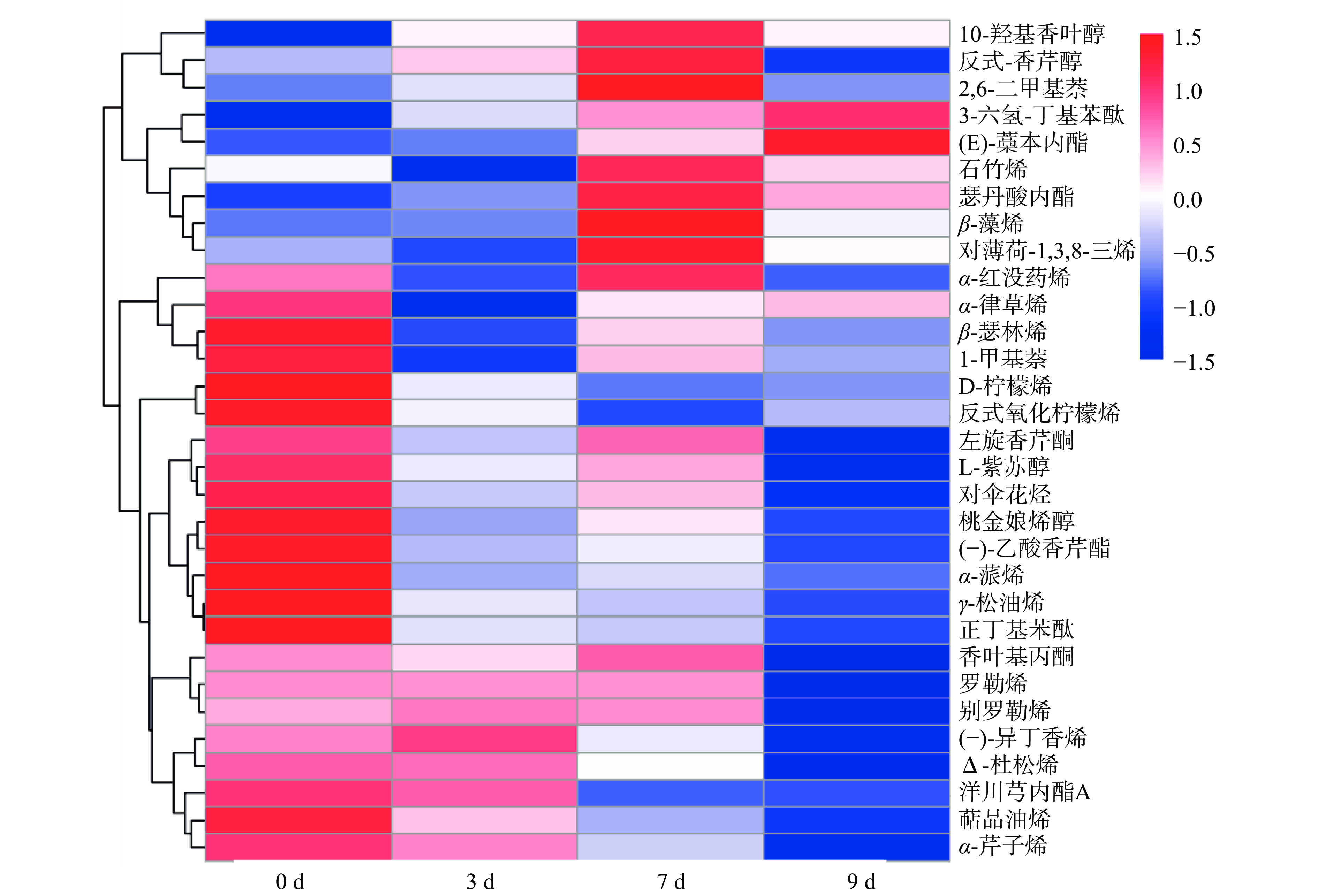
根据31种关键挥发性物质的OAV值绘制热图,并通过层次聚类对其进行分析(图2),结果表明芹菜香气0 d以桃金娘烯醇、(-)-乙酸香芹酯、α-蒎烯、D-柠檬烯、β-瑟林烯等为主要特征挥发性物质,具有薄荷香和青草香;(-)-异丁香烯是第3 d的主要差异物质,提供了丁香香气;第7 d主要以10-羟基香叶醇、β-蒎烯、对薄荷-1,3,8-三烯、石竹烯、瑟丹酸内酯为主要特征挥发性物质,具有甜香、木香和樟脑香;第9 d以3-六氢-丁基苯酞、(E)-藁本内酯为关键香气物质,具有辛辣和药草气味。通过芹菜特征挥发性物质的变化判断芹菜的新鲜程度,为确定芹菜的最佳货架期提供了理论基础。
2.3 电子鼻分析贮藏期间芹菜叶片挥发性物质
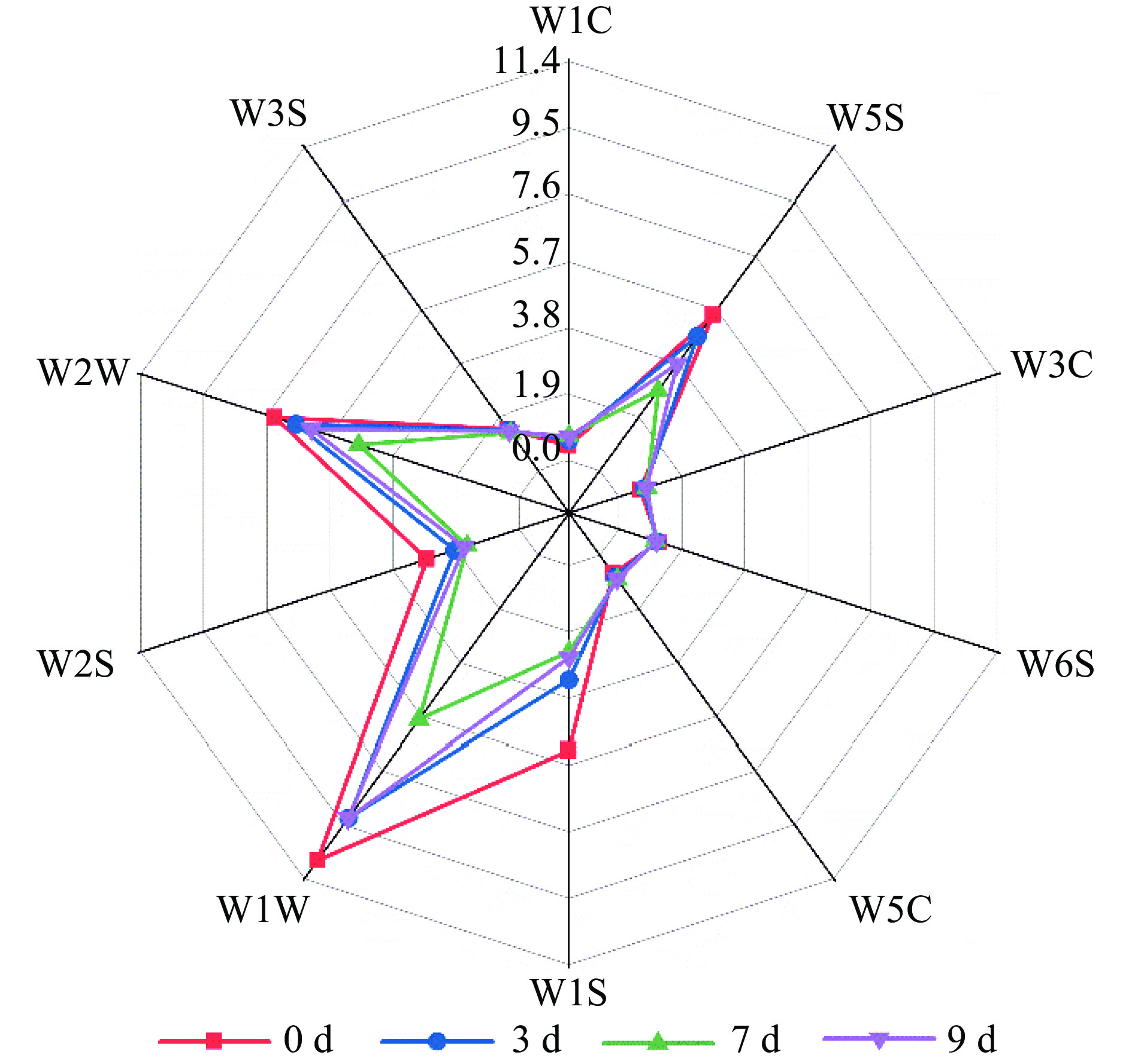
对新鲜和贮藏不同时间后的芹菜叶粉进行电子鼻检测。贮藏期间,芹菜气味在10个传感器上的响应值不同(图3)。新鲜(0 d)芹菜在各传感器上响应值最大,说明芹菜刚采收后气味更浓郁。不同贮藏时期芹菜气味的变化主要体现在W5S、W1S、W1W、W2S、W2W传感器上,这些传感器对氮氧化物、萜烯类、醇类和部分芳香族化合物响应敏感,表明贮藏期间芹菜中氮氧化物、萜烯类、醇类和部分芳香族挥发性物质存在差异。
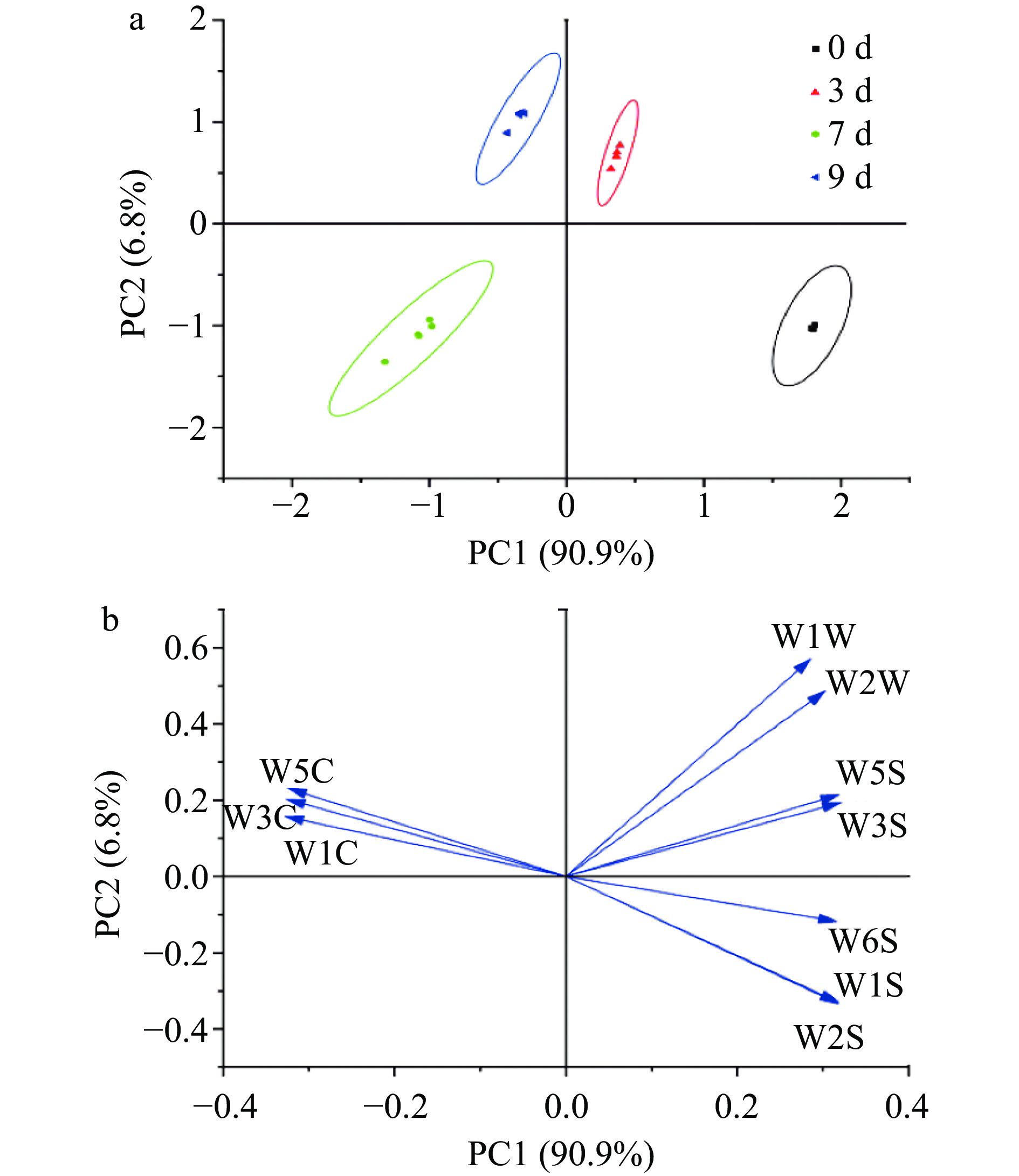
采用主成分分析对电子鼻响应值数据进行分析,结果见图4。PC1的贡献率为90.9%,PC2贡献率为6.8%,总贡献率97.9%,说明PCA可以很好地反映样本信息。第0、3、7、9 d分布在不同象限,提示贮藏期间芹菜挥发性成分存在差异。第3、9 d在PC2轴位置接近,表明两者的主要挥发性物质相似;第3、7、9 d在PC1轴上与0 d区分明显,故新鲜芹菜挥发性物质与第3、7、9 d的芹菜存在显著差异。另外,W1S、W2S对于第四象限贡献值较大,可以更好地识别第0 d的样品。
2.4 HS-SPME-GC-MS与电子鼻相关性分析
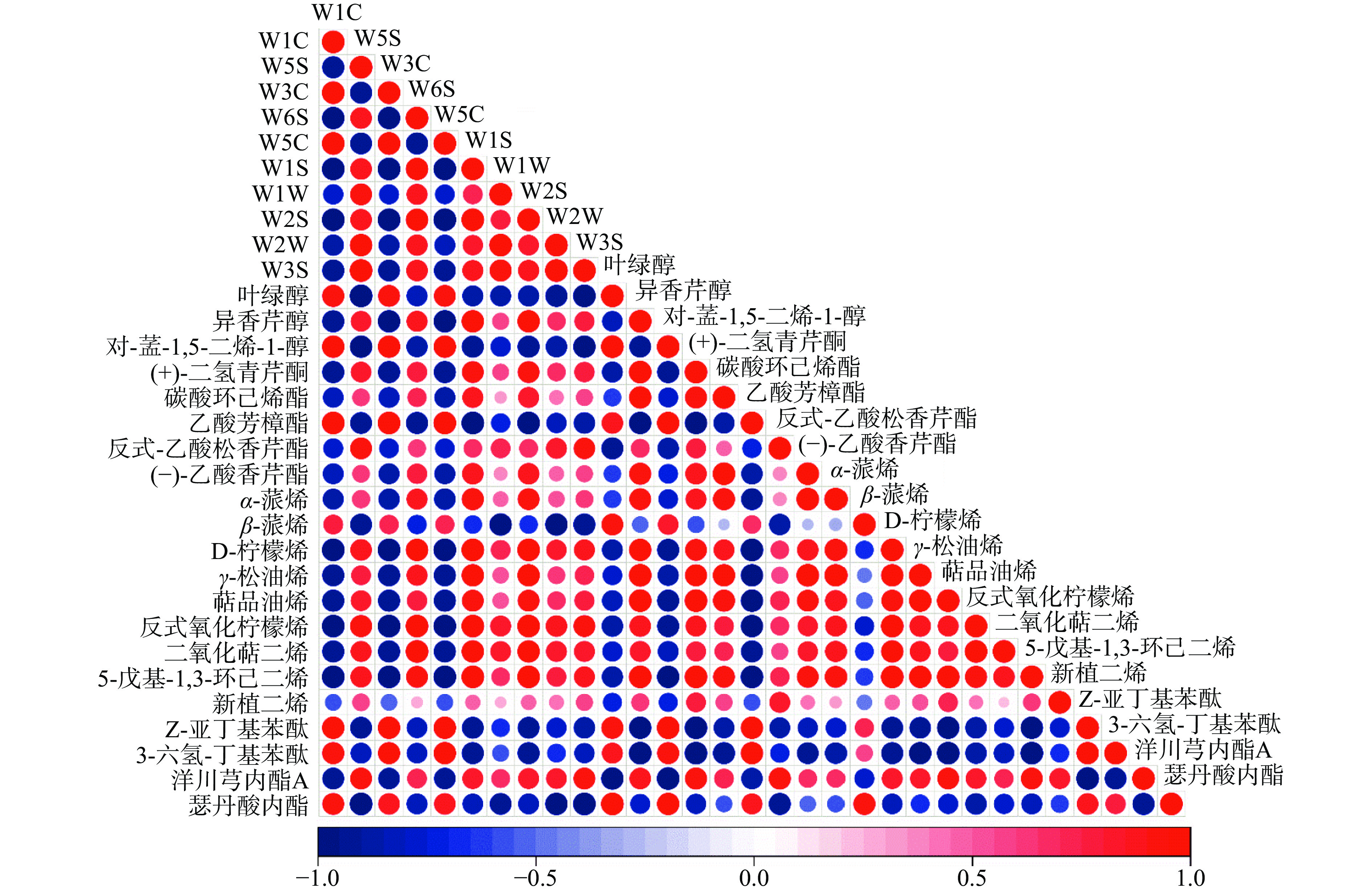
以HS-SPME-GC-MS鉴定含量较高的21种化合物与10个电子鼻感应器响应值进行Pearson相关性分析,结果见图5。W1C、W3C、W5C与乙酸芳樟酯、Z-亚丁基苯酞、3-六氢-丁基苯酞成正相关,表明W1C、W3C、W5C传感器对芳香族化合物敏感;W1W、W6S与D-柠檬烯、反式氧化柠檬烯、二氧化萜二烯成正相关,表明两个传感器对萜烯类化合物响应较大,W1S、W2S感应器响应值与异香芹醇、γ-松油烯、5-戊基-1,3-环己二烯含量成正相关,但W1S、W2S乙酸芳樟酯成负相关。W1C、W3C、W5C、W1W、W2S传感器识别出的挥发性物质与其性能描述基本一致,表明引起电子鼻传感器响应值变化的物质主要是萜类、醇类、芳香型挥发性物质(r≥0.80,P<0.05)。结合贮藏期间具有关联性物质的变化,电子鼻技术可应用于芹菜品质变化的快速判别。
3. 讨论与结论
Turner等[15]比较了2018年和2020年收获芹菜的挥发性物质,分别鉴定出65种、74种化合物,其中单萜类物质占比最大,分别为55%、88%。Reale等[16]测定四种不同芹菜的挥发性物质,检测到白芹、黑芹、野生型芹菜和普通芹菜挥发性物质分别有18、16、13、18种,四种芹菜中柠檬烯含量最高,相对含量达到50%。本研究以冬季采收的芹菜叶片为材料,利用HS-SPME-GC-MS鉴定出更多的挥发性物质数量,共检测出108种化合物,鉴定出的挥发性物质种类远多于文献的报道,其中主要是单萜类和醇类物质数量多于现有报道[15−16]。此外,芹菜特征挥发性物质1-甲基萘是本研究检测到的特有物质,鲜有文献报道。造成这些差异的原因可能与芹菜基因型、收获季节、品种、取样部位、提取和分析方法的不同等有关。
贮藏期间,芹菜叶片中挥发性物质的含量总体呈逐渐下降趋势,且萜类物质占比逐渐减小,苯酞类和醇类物质占比逐渐增加。研究报道萜类物质在空气易被氧化生成含氧化物、萜烯醇类等,其中柠檬烯氧化后生成香芹醇,紫苏醇等氧化衍生物[28]。推测贮藏期间芹菜叶片中萜类物质占比减少,醇类物质占比增加,与柠檬烯等萜类物质被氧化为香芹醇和紫苏醇等醇类物质有关。另外,Song等[29]研究结果表明萜类物质合成与萜类合酶有关,因此贮藏期间芹菜叶片中萜类物质含量减少可能与萜类合酶活性降低有关。目前关于植物中苯酞的生物合成的途径尚未明确,Yan等[30]研究表明茉莉酸、脱落酸等植物激素在调节苯酞类物质的合成中起着重要作用,推测芹菜叶片中苯酞类物质含量的变化可能与植物激素调节有关。Wu等[12]利用GC-MS比较4 ℃和20 ℃贮藏条件下菊花脑挥发性物质差异,发现低温延缓了菊花脑挥发性物质的损失。李雪等[31]研究不同贮藏温度油麦菜采后香气成分变化,结果表明4 ℃贮藏可以减缓油麦菜香气成分的释放。基于以上研究,推测贮藏温度可能影响采后芹菜中的挥发性物质,在后续的研究中将探讨不同温度下贮藏对芹菜挥发性物质的影响。
GC-MS与电子鼻结合已广泛应用于果蔬的香气成分鉴定,GC-MS可以分析贮藏期间芹菜叶片中挥发性化合物的种类和含量变化,但无法分析样品香气成分整体特征变化[32]。而电子鼻可以识别样品整体香气轮廓,具有简便、无损、高效的特点[9]。电子鼻结合贮藏期间芹菜叶片特征挥发性物质的变化,可快速判别芹菜品质的变化。
本研究采用HS-SPME-GC-MS和电子鼻技术分析20.0 ℃贮藏期间芹菜叶片挥发性物质的变化,共鉴定出108种挥发性物质,单萜类和苯酞类物质为主要组分,新鲜芹菜总挥发性物质含量为165682.48 μg/kg,贮藏期间芹菜总挥发性物质含量逐渐降低,下降了40.92%,其中单萜类物质占比增大,苯酞类物质占比减小。结合OAV值分析,得到D-柠檬烯和洋川芎内酯A等31种OAV>1的特征挥发性物质,芹菜香气0~3 d主要以D-柠檬烯等萜类物质的新鲜青草香为主,3 d至第7 d以10-羟基香叶醇、瑟丹酸内酯等醇类和苯酞类物质的甜香和木香为主,第9 d则以(E)-藁本内酯等苯酞类物质刺激性的辛辣风味为主。PCA结果表明电子鼻可以区分不同贮藏时间芹菜叶片的香气,HS-SPME-GC-MS结合电子鼻技术可以更加全面、准确地分析贮藏期间芹菜叶片挥发性物质组成和含量及变化规律,本研究结果为明确芹菜的香气特征和判别采后芹菜品质提供了理论基础。
-
表 1 电子鼻传感器性能描述
Table 1 Function description of E-nose sensors
传感器名称 性能描述 W1C 对芳香性化合物敏感 W5S 对氮氧化物敏感 W3C 对氨类、芳香族化合物敏感 W6S 对氢类物质敏感 W5C 对烷烃、芳香族化合物敏感 W1S 对甲基类敏感 W1W 对无机硫化物、萜烯类敏感 W2S 对醇类、部分芳香族化合物敏感 W2W 对芳香族化合物、有机硫化物敏感 W3S 对烷烃敏感 表 2 不同贮藏时间芹菜叶片的挥发性物质组成和含量
Table 2 Composition and content of volatile compounds in celery leaves during storage
序号 名称 保留指数 鉴定方式 含量(μg/kg) 计算值 参考值 0 d 3 d 7 d 9 d 1 α-蒎烯 936 931 MS/RI 222.64±0.55 68.08±3.03 89.57±3.51 48.88±3.78 2 β-蒎烯 981 980 MS/RI 5209.18±185.08 5332.69±23.36 9975.71±528.39 6671.74±11.19 3 D-柠檬烯 1055 1031 MS/RI 48566.12±1907.83 18653.08±133.41 6600.64±210.84 8983.19±30.34 4 (R)-异香芹萜烯 1031 1028 MS/RI 11860.51±988.06 29213.47±728.91 26106.4±929.24 13106.58±118.35 5 罗勒烯 1048 1026 MS/RI 2349.49±126.39 2321.74±244.13 2313.26±111.98 913.78±48.57 6 γ-松油烯 1060 1056 MS/RI 2105.67±6.21 1322.57±134.56 1227.52±8.66 939.57±26.37 7 别罗勒烯 1129 1129 MS/RI 16651.89±78.57 17433.27±533.26 17151.4±2004.12 11087.91±1981.47 8 萜品油烯 1088 1083 MS/RI 104.74±0.03 71.05±0.72 47.28±1.72 25.72±0.41 9 左旋香芹酮 1246 − MS 161.42±12.12 108.99±0.25 152.31±11.75 70.03±2.56 10 1,3,8-对薄荷-三烯 1027 1118 MS/RI 232.47±17.24 96.28±9.87 731.14±40.51 360.43±29.17 11 2-甲基-1-(2,2,3-三甲基
环亚丙基)-1-丙烯1143 − MS 210.92±0.01 149.2±5.2 354.63±11.23 85.23±4.77 单萜类(11种) 87675.05 74770.42 64749.86 42293.06 12 β-榄香烯 1391 1366 MS/RI 291.29±37.73 339.89±28.56 266±5.88 225.1±21.76 13 罗汉柏烯 1412 1429 MS/RI 121.95±14.53 126.97±8.84 85.28±2.46 69.99±5.89 14 雪松烯 1426 1433 MS/RI 31.11±3.56 24.6±3.56 22.68±0.27 15.82±0.64 15 石竹烯 1433 1415 MS/RI 1709.07±68.73 1254.44±109.76 2105.93±49.56 1795.75±71.18 16 环庚烯 1440 1531 MS/RI 157.17±2.51 172.99±9.24 152.73±7.62 121.78±3.58 17 γ-榄香烯 1443 1441 MS/RI 188.49±9.41 89.14±0.02 158.98±0.2 123.87±33 18 α-愈创烯 1455 1438 MS/RI ND 39.43±1.01 30.26±2.16 20.02±4.63 19 (-)-异丁香烯 1474 1428 MS/RI 107.6±19.11 114.45±9.74 96.4±1.96 75.44±12.68 20 α-律草烯 1455 1451 MS/RI 2065.02±78.45 1191.26±84.63 1746.71±422.22 1821.48±237.06 21 β-长叶蒎烯 1510 1405 MS/RI 138.88±23.79 73.4±8.62 84.93±3.13 65.34±7.81 22 α-姜烯 1532 1480 MS/RI 1588.4±249.32 194.68±19.23 1042.92±15 796.09±8.95 23 β-瑟林烯 1572 1486 MS/RI 2375.8±28.65 1145.92±15.94 1759.27±183.17 1304.21±115.83 24 α-芹子烯 1597 1505 MS/RI 3154.13±152.76 2809.29±73.4 2167.21±41.07 1382.34±73.62 25 Α-布黎烯 1603 1505 MS/RI 31.99±4.7 25.96±5.2 26.7±1.45 23.13±2.3 26 β-姜黄烯 1607 1512 MS/RI 370.67±2.11 222.73±25.59 320.66±29.78 187.3±7.55 27 α-衣兰油烯 1612 1449 MS/RI 84.16±2.03 82.83±3.69 72.89±0.83 57.2±4.42 28 Δ-杜松烯 1616 1486 MS/RI 96.79±9.02 95.56±3.11 82.09±2.72 54.27±7.58 29 3,7(11)-蛇床二烯 1638 1527 MS/RI 68.72±2.99 69.01±7 51.03±2.41 41.73±5.1 30 Α-姜黄烯 1607 1486 MS/RI 493.05±37.72 421.97±18.77 416.22±1.82 355.53±48.19 31 β-橄榄烯 1629 1381 MS/RI 41.57±4.1 11.53±0.22 21.79±1.68 14.3±5.64 32 愈创木烯 1630 1504 MS/RI 23.92±5.22 48.45±0.68 35.06±5.04 17.79±1.49 倍半萜类(21种) 13139.78 8554.5 10745.74 8568.48 33 α-红没药烯 1271 − MS 34.57±0.89 19.87±2.33 39.19±7.09 20.67±4.62 34 14-羟基石竹烯氧化物 1680 − MS 87.06±8.6 48.98±1.16 59.09±1.92 36.99±1.69 35 反式氧化柠檬烯 1139 − MS 6535.03±114.78 4600.21±118.43 3452.99±328.7 4190.53±160.46 36 二氧化萜二烯 1289 1294 MS/RI 116.28±6.18 71.98±7.68 58.12±2.34 75.12±4.66 含氧萜类(4种) 6772.94 4741.04 3609.39 4323.31 37 波斯菊萜 1080 1132 MS/RI 48.08±2.88 75.97±3.37 105±6.92 55.7±1.54 38 对伞花烃 1153 1026 MS/RI 171.63±4.39 130.84±8.09 147.45±17.86 106.29±6.4 39 5-戊基-1,3-环己二烯 1160 1161 MS/RI 4344.89±177.57 2305.22±178.3 1155.44±112.72 798.2±44.27 40 1,2,3,6-四甲基双环[2.2.2]-2,5-辛二烯 1351 − MS 40.72±1.99 33.44±3.42 45.82±5.88 36.86±5.87 41 3-苯基-1,4-环己二烯 1410 − MS 101.84±12.4 27.4±5.31 28.21±0.26 45.68±2.52 42 新植二烯 1827 1836 MS/RI 7689.84±368.98 9817.77±384.98 5808.3±338.97 3524.76±295 43 3,7,11,15-四甲基-2-十六烯 1809 − MS 121.28±17.51 65.99±4.2 44.31±2.26 14.58±0.85 烯烃类(7种) 12518.28 12456.63 7334.53 4582.07 44 正丁基苯酞 1621 1629 MS/RI 5578.92±208.39 4036.19±187.99 3931.33±66.97 3317.37±176.35 45 3-六氢-丁基苯酞 1597 1645 MS/RI 237.35±29.12 337.67±38.22 401.32±7.05 451.51±106.04 46 Z-亚丁基苯酞 1772 1666 MS/RI 112.69±9.28 141.3±17.26 190.14±26.64 199.43±16.58 47 洋川芎内酯A 1811 − MS 14479.04±3308.34 13161.95±336.64 5961.69±455.57 5702.18±210.15 48 瑟丹酸内酯 1823 1726 MS/RI 12379.44±350.65 13844.74±2648.78 20911.30±499.93 17696.24±1321.43 49 (E)-藁本内酯 1833 1809 MS/RI 237.05±5.26 289.91±14.08 609.89±62.96 993.16±149.77 苯酞类(6种) 33024.49 31811.76 32005.65 28359.89 50 惕各酸紫苏醇 1008 − MS 180.22±2.83 140.6±8.34 165.51±22.5 152.45±27.46 51 芥子醇 1058 1295 MS/RI 16.15±1.71 4.41±0.34 7.37±0.56 10.67±2.6 52 桃金娘烯醇 1091 1191 MS/RI 87.66±10.76 36.61±1.28 54.06±5.68 25.02±0.84 53 3-(2,6,6-三甲基-1-环己烯基)-
2-丙烯-1-醇1180 − MS ND 4.58±0.43 5.23±0.6 4.7±0.84 54 顺式-马鞭烯醇 1118 1141 MS/RI 142.79±6.92 114.83±1.14 135.87±0.54 85.94±4.08 55 反式-薄荷基-2,8-二烯-1-醇 1122 1100 MS/RI 157.39±1.34 189.32±8.15 247.92±7.67 142.32±2.04 56 对-䓝-1,5-二烯-1-醇 1173 1170 MS/RI 154.7±15.11 390.59±5.41 832.26±4.9 769.64±25.85 57 异香芹醇 1229 1231 MS/RI 24.49±0.24 14.6±0.38 10.55±0.13 6.41±0.58 58 (Z)-3,7,11-三甲基-2,10-十二碳烯-1-醇 1867 1668 MS/RI 57.7±3.84 64.68±4.06 120.82±7.62 127.52±41.27 59 (1R,3S,5S,7R)-2,8-二亚甲基-5-丙-1-烯-2-基环癸烷-1,3,7-三醇 1496 − MS 19.55±0.73 13.98±1.32 14.35±1.63 14.79±2.34 60 10-羟基香叶醇 1199 2652 MS 37.13±8.04 68.83±1.16 94.31±10.79 68.92±3.87 61 正三十七醇 1214 − MS 20.27±4.4 2.29±0.05 4.98±0.38 11.37±0.6 62 反式-香芹醇 1221 1219 MS/RI 482.49±14.88 580.33±23.78 734.71±36.12 378.79±8.1 63 (Z)-异香芹醇 1229 1231 MS/RI 33.16±1.37 33.77±2.75 24.22±4.09 21.23±0.57 64 5,7-十二烷二炔-1,12-二醇 1226 1724 MS/RI ND 19.29±0.6 16.86±0.51 7.49±2.65 65 柠檬烯二醇 1341 1321 MS/RI 264.69±37.94 186.99±5.72 193.69±0.08 92.89±9.77 66 Α-菖蒲醇 1718 1648 MS/RI 34.06±1.69 14.5±0.78 15.99±0.9 10.97±1.98 67 紫苏醇 1617 1302 MS/RI 236.43±45.61 195.03±11.96 336.02±13.19 233.27±29.71 68 L-紫苏醇 1198 1994 MS 124.19±10.66 100.78±9 111.27±10.47 77.21±2.98 69 叶绿醇 1830 2116 MS/RI 341.05±31.03 451.87±3.19 926.89±59.99 770.95±52.55 70 13-十七炔-1-醇 1965 − MS 47.39±3.4 18.62±1.29 64.32±3.8 66.68±3.78 醇类(21种) 2461.51 2646.5 4117.2 3079.23 71 (+)-二氢青芹酮 1206 1242 MS/RI 734.62±2.07 626.51±8.88 532.89±57.25 461.66±43.1 72 5-甲基-2-癸烯-4-酮 1286 − MS 44.22±4.8 174.54±3.59 231.26±35.49 126.26±8.43 73 香叶基丙酮 1464 1452 MS/RI 119.96±8.96 113.63±9.41 123.88±1.52 82.53±4.96 74 2-丁基-5-甲基-3-(2-甲基-2-丙烯基)环己酮 1622 − MS 60.76±1.91 46.01±3.01 33.55±8.47 22.92±7.64 75 1,1-二甲基-1,2,3,5,7,8,9,9a-八氢-
6-苯并环庚烯酮1777 − MS 851.09±77.1 585.71±1.43 778.34±80.78 503.21±18.35 76 5-烃基-10,10-二甲基-6-甲基双环
[7.2.0]-2-十一酮1911 − MS 4.13±0.7 2.84±0.29 7.96±0.1 7.6±1.29 酮类(6种) 1814.78 1549.24 1707.88 1204.18 77 碳酸环己烯酯 852 − MS 215.48±14.33 108.82±8.49 116.48±12.71 28.31±2.2 78 2,5-十八碳二炔酸甲酯 1092 − MS 29.5±3.04 19.52±1.68 17.47±3.5 11.97±0.83 79 异胆酸乙酯 2058 − MS 7.69±1.62 6.22 4.75±0.99 3.25±0.78 80 乙酸芳樟酯 984 1246 MS/RI 101.26±5.47 140.21±13.13 162.83±14.68 162.6±9.84 81 (-)-乙酸香芹酯 1328 1339 MS/RI 567.43±48.44 428.11±1.81 451.9±36.37 384.15±47.25 82 9-十八烯-12-炔酸甲酯 1367 − MS 15.31±2.13 15.58±1.17 13.06±0.51 7.92±1.26 83 (E)-10-十七烯-8-炔酸甲酯 1366 − MS 23.27±1.69 ND ND ND 84 14-去氧-12-羟基穿心莲内酯 1698 − MS 30.69±0.53 17.88±0.74 26.25±0.78 12.3±1.29 85 10,13-十八碳二炔酸甲酯 1701 − MS 23.63±2.73 13.86±1.71 20.54±0.59 15.43±1.97 86 10,12-十八碳二炔酸甲酯 1764 − MS 62±14.55 19.96±1.82 27.88±1.19 20.92±3.01 87 反式-乙酸松香芹酯 1248 1298 MS/RI 103.06±8.31 108.91±6.45 75.06±10.21 82.56±11.55 88 (S,E)-2,5-二甲基-4-乙烯基-2,5-
二烯-1-乙酸酯1274 − MS 57.77±1.73 62.14±0.59 59.32±6.97 44.73±8.25 酯类(12种) 1237.09 941.21 975.54 774.14 89 2-异丙烯基-5-甲基-4-烯己醛 1074 − MS 169.22±21.49 108.12±7.98 66.7±6.06 45.97±5.11 90 5β-胆甾-3-酮乙缩醛 1899 − MS 2.67±0.27 1.53±0.14 1.7±0.39 1.26±0.28 醛类(2种) 171.89 109.65 68.4 47.23 91 10,12-二十八二炔酸 1336 − MS 25.31±2.14 19.83±1 44.09±0.82 16.42±0.17 92 6-乙烯基-4,5,6,7-四氢-3,6-二
甲基-5-苯并呋喃乙酸1845 − MS 204.35±13.29 196.56±10.47 146.89±11.16 219.25±6.76 93 十九碳烯酸 1804 − MS 16.44±0.77 6.06±0.7 7.08±0.03 ND 94 环丙烷丁酸 1918 − MS 35.86±3.57 6.37±1.19 16.06±1.46 10.93±1.53 酸类(4种) 281.96 228.82 214.12 246.6 95 1-亚甲基-1H-茚 1189 1098 MS/RI 468.2±23.92 461.74±14.24 625.45±63.8 357±27.05 96 6-甲基四氢化萘 1269 1247 MS/RI 30.26±3.3 33.57±2.66 40.57±3.73 27.33±2.44 97 五甲基苯 1281 1281.8 MS/RI 155.45±16.68 138.37±23.19 170.46±18.45 122.88±13.84 98 黄樟素 1292 1288 MS/RI 1008.32±8.51 758.45±19.82 858.14±62.6 589.47±71.13 99 2,6-二甲基萘 1457 1400 MS/RI 53.84±1.04 68.52±6.26 114.82±32.02 56.48±0.21 100 1-乙基萘 1478 1400 MS/RI 76.33±7.89 61.7±4.28 70.29±11.73 65.43±11.32 101 4a,8-甲基-2-(丙基-1-烯-2-基)-
1,2,3,4,4a,5,6,7-八氢萘1520 1492 MS/RI 112.51±31.92 92.05±1.77 42.06±8.68 72.75±9 102 3-(2-甲基-1-丙烯基)-1H-茚 1620 − MS 48.52±2.9 26.29±0.23 62.55±2.16 29.89±1.84 103 3,4-二乙基联苯 1784 1692 MS/RI 10.54±0.38 8.42±0.37 11.22±0.45 9.18±1.14 104 1,1,3a-三甲基-7-甲基-十氢-1H-环丙[a]萘 1633 1692 MS/RI 90.48±19.99 111.09±8.23 17.59±5.14 77.46±0.77 105 缬草素 1627 1536.9 MS/RI 24.54±2.02 27.33±3.94 20.13±3.08 37.1±4.39 106 9,10-二氢-11,12-二羧酸-9,10-二乙基蒽 1881 − MS 73.46±9.06 46.17±7.77 91.05±10.9 107.97±0.9 107 1-甲基萘 1300 1325 MS/RI 4413.75±21.74 3068.44±75.95 4279.1±349.46 2853.03±236.66 108 4,6,6-三甲基-2-(3-甲基-1,3-二
烯基)-3-氧杂三环[5.1.0.]丁烷1876 − MS 18.51±2.34 12.6±1.72 16.48±1.99 8.81±0.79 其他(14种) 6584.71 4914.74 6419.91 4414.78 总计 165682.48 142724.51 131948.22 97892.97 注:“保留指数”中“参考值”来自https://webbook.nist.gov;“−”表示未查到;“鉴定方式”中“MS”表示质谱定性;“RI”表示保留指数定性;“ND”表示该物质未被检出。 表 3 不同贮藏时间芹菜叶片OAV>1的特征挥发性物质
Table 3 Characteristic volatile compounds with OAV higher than 1 in celery leaves during storage
化合物 阈值(μg/kg) OAV值 气味描述 0 d 3 d 7 d 9 d 桃金娘烯醇 7 12.52 5.23 7.72 3.57 檀木香、薄荷香 L-紫苏醇 8 15.52 12.60 13.91 9.65 奶香,甜香 10-羟基香叶醇 40 0.93 1.72 2.36 1.72 甜香,玫瑰花香 反式-香芹醇 250 1.93 2.32 2.94 1.52 辛辣,香菜气味,薄荷香 香叶基丙酮 60 2.00 1.89 2.06 1.38 清香,略带甜蜜的玫瑰香 (-)-乙酸香芹酯 46 12.34 9.31 9.82 8.35 薄荷香,草药香 α-蒎烯 6 37.11 11.35 14.93 8.15 清香,木香 β-蒎烯 140 37.21 38.09 71.26 47.66 青草香,带一点辛辣 D-柠檬烯 34 1428.42 548.62 194.14 264.21 柑橘香,松树气味,薄荷香 罗勒烯 34 69.10 68.29 68.04 26.88 甜香,草香,木香 γ-松油烯 260 8.10 5.09 4.72 3.61 油脂气味,木香,柑橘香 别罗勒烯 34 489.76 512.74 504.45 326.12 草香、花香并伴有橙花油香气 萜品油烯 41 2.55 1.73 1.15 0.63 松木香气,微带甜的柑橘香 左旋香芹酮 7 24.09 16.27 22.73 10.45 草香,薄荷脑香 对薄荷-1,3,8-三烯 39 5.92 2.45 18.60 9.17 木香,樟脑香 石竹烯 55 31.07 22.81 38.29 32.65 甜味,木香,胡椒气味 β-瑟林烯 1000 2.38 1.15 1.76 1.30 草香 (-)-异丁香烯 10 10.76 11.45 9.64 7.54 丁香香气,松木气味 α-律草烯 120 17.21 9.93 14.56 15.18 淡的丁香气味 α-芹子烯 1000 3.15 2.81 2.17 1.38 橘香、甜香和泥土香 Δ-杜松烯 2 64.53 63.71 54.73 36.18 木香 α-红没药烯 5 6.57 3.78 7.45 3.93 果香 反式氧化柠檬烯 100 65.35 46.00 34.53 41.91 果香,柑橘香 对伞花烃 120 1.43 1.09 1.23 0.89 柠檬香,小茴香气味 2,6-二甲基萘 10 5.38 6.85 11.48 5.65 沥青气味 1-甲基萘 8 551.72 383.56 534.89 356.63 有类似萘的特殊气味 正丁基苯酞 70 79.70 57.66 56.16 47.39 芹菜香味,草香 3-六氢-丁基苯酞 70 3.39 4.82 5.73 6.45 药草香,芹菜气味 洋川芎内酯A 140 103.42 94.01 42.58 40.73 药草香 瑟丹酸内酯 270 45.85 51.28 77.45 65.54 药草香,芹菜气味 (E)-藁本内酯 140 1.69 2.07 4.36 7.09 甜香,辛辣 注:所用阈值参考文献[25−27],挥发性物质气味描述见http://www.flavornet.org/index.html。 -
[1] LI M Y, FENG K, HOU X L, et al. The genome sequence of celery ( Apium graveolens L.), an important leaf vegetable crop rich in apigenin in the Apiaceae family[J]. Horticulture Research,2020,7(1):9−19. doi: 10.1038/s41438-019-0235-2
[2] SCHNEEMAN B O. Dietary fiber-comments on interpreting recent research[J]. Journal of the American Dietetic Association,1987,87(9):1163−1163. doi: 10.1016/S0002-8223(21)03292-2
[3] YAO H, XU W Z, SHI X L, et al. Dietary flavonoids as cancer prevention agents[J]. Journal of Environmental Science and Health Part C-environmental Carcinogenesis & Ecotoxicology Reviews,2011,29(1):1−31.
[4] 鲍辰卿, 顾文博, 杨程, 等. 气相色谱-质谱-嗅辨法辨析4种芹菜籽油树脂中关键香气成分[J]. 食品安全质量检测学报,2023,14(1):204−210. [BAO Chenqing, GU Wenbo, YANG Cheng, et al. Identification of key aroma components in 4 kinds of celery seed oleoresin by gas chromatography-mass spectroscopy-olfactometry[J]. Journal of Food Safety & Quality,2023,14(1):204−210.] BAO Chenqing, GU Wenbo, YANG Cheng, et al . Identification of key aroma components in 4 kinds of celery seed oleoresin by gas chromatography-mass spectroscopy-olfactometry[J]. Journal of Food Safety & Quality,2023 ,14 (1 ):204 −210 .[5] SELLAMI I H, BETTAIEB I, BOURGOU S, et al. Essential oil and aroma composition of leaves, stalks and roots of celery ( Apium graveolens var. dulce) from Tunisia[J]. Journal of Essential Oil Research,2012,24(6):513−521. doi: 10.1080/10412905.2012.728093
[6] 程碧君, 李天娇. 顶空-气质联用对芹菜叶粉贮藏过程中挥发性成分变化研究[J]. 食品研究与开发,2020,41(15):46−50. [CHENG Bijun, LI Tianjiao. Study on changes of volatile compounds composition of celery leaves powder during storage by HS-GC-MS[J]. Food Research and Development,2020,41(15):46−50.] CHENG Bijun, LI Tianjiao . Study on changes of volatile compounds composition of celery leaves powder during storage by HS-GC-MS[J]. Food Research and Development,2020 ,41 (15 ):46 −50 .[7] FORNEY C F, JORDAN M A, PENNELL K M, et al. Controlled atmosphere storage impacts fruit quality and flavor chemistry of five cultivars of highbush blueberry ( Vaccinium corymbosum)[J]. Postharvest Biology and Technology,2022,194(112073):1−10.
[8] BAKIR S, HALL R D, MUMM R, et al. Effect of drying treatments on the global metabolome and health-related compounds in tomatoes[J]. Food Chemistry,2023,403(134123):1−10.
[9] WANG C, FU C, LI Y, et al. Integrated volatilomic profiles and chemometrics provide new insights into the spatial distribution and aroma differences of volatile compounds in seven Toona sinensis cultivars[J]. Food Chemistry,2023,407:135116−135128. doi: 10.1016/j.foodchem.2022.135116
[10] SUN P, XU B, WANG Y, et al. Characterization of volatile constituents and odorous compounds in peach ( Prunus persica L) fruits of different varieties by gas chromatography-ion mobility spectrometry, gas chromatography-mass spectrometry, and relative odor activity value[J]. Frontiers in Nutrition,2022,9(965796):1−9.
[11] 田震, 徐亚元, 李大婧, 等. 基于SPME-GC-MS分析不同干燥方式对香葱挥发性成分的影响[J]. 食品工业科技,2021,42(4):232−244. [TIAN Zhen, XU Yayuan, LI Dajing, et al. Analysis of volatile components in dried chives by SPME-GC-MS[J]. Science and Technology of Food Industry,2021,42(4):232−244.] TIAN Zhen, XU Yayuan, LI Dajing, et al . Analysis of volatile components in dried chives by SPME-GC-MS[J]. Science and Technology of Food Industry,2021 ,42 (4 ):232 −244 .[12] WU Y, YU H, YU X, et al. Comparison of volatile compounds in Chrysanthemum nankingense during storage based on HS-SPME-GC-MS and E-nose[J]. Journal of Food Measurement and Characterization,2023,17(3):3134−3148. doi: 10.1007/s11694-023-01847-2
[13] CAI H, HAN S, JIANG L, et al. 1-MCP treatment affects peach fruit aroma metabolism as revealed by transcriptomics and metabolite analyses[J]. Food Research International,2019,122:573−584. doi: 10.1016/j.foodres.2019.01.026
[14] 吴玉珍, 王洁琼, 余海涛, 等. 基于HS-SPME-GC-MS和OAV值分析不同干燥方式菊花脑的挥发性物质差异[J]. 食品科学,2022,44(8):1−16. [WU Yuzhen, YU Haitao, YU Xiaoyu, et al. Analysis of volatile components of fresh and different dried Chrysanthemum nankingense based on headspace solid phase microextraction-gas chromatography-mass spectrometry and OAV[J]. Food Science,2022,44(8):1−16.] WU Yuzhen, YU Haitao, YU Xiaoyu, et al . Analysis of volatile components of fresh and different dried Chrysanthemum nankingense based on headspace solid phase microextraction-gas chromatography-mass spectrometry and OAV[J]. Food Science,2022 ,44 (8 ):1 −16 .[15] TURNER L, LIGNOU S, GAWTHROP F, et al. Investigating the relationship of genotype and climate conditions on the volatile composition and sensory profile of celery (Apium graveolens)[J]. Foods,2021,10(13356):1−25.
[16] REALE S, DI CECCO V, DI DONATO F, et al. Characterization of the volatile profile of cultivated and wild-type Italian celery ( Apium graveolens L.) varieties by HS-SPME/GC-MS[J]. Applied Sciences-Basel,2021,11(13):1−11.
[17] TURNER L, LIGNOU S, GAWTHROP F, et al. Investigating the factors that influence the aroma profile of Apium graveolens:A review[J]. Food Chemistry,2021,345(128673):1−41.
[18] XIA R R, WANG L, XIN G, et al. Preharvest and postharvest applications of 1-MCP affect umami taste and aroma profiles of mushrooms ( Flammulina velutipes)[J]. LWT-Food Science and Technology,2021,144:1−8.
[19] TURNER L, WAGSTAFF C, GAWTHROP F, et al. Consumer acceptability and sensory profile of three new celery ( Apium graveolens) hybrids and their parental genotypes[J]. International Journal of Molecular Sciences,2021,22(1356124):13561−13585.
[20] TURNER L, DAWDA D, WAGSTAFF C, et al. Influence of harvest maturity on the aroma quality of two celery (Apium graveolens) genotypes[J]. Food Chemistry,2021,365(130515):1−41.
[21] MARONGIU B, PIRAS A, PORCEDDA S, et al. Isolation of the volatile fraction from Apium graveolens L. (Apiaceae) by supercritical carbon dioxide extraction and hydrodistillation:chemical composition and antifungal activity[J]. Natural Product Research,2013,27(17):1521−1527. doi: 10.1080/14786419.2012.725402
[22] GUIJARRO-REAL C, RODRIGUEZ-BURRUEZO A, PROHENS J, et al. HS-SPME analysis of the volatiles profile of water celery ( Apium nodiflorum), a wild vegetable with increasing culinary interest[J]. Food Research International,2019,121:765−775. doi: 10.1016/j.foodres.2018.12.054
[23] 杜康. 云南烟草精油的提取及新植二烯的纯化工艺研究[D]. 昆明:昆明理工大学, 2020. [DU Kang. Study on extraction of Yunnan tobacco essential oil and purification technology of neophytadiene[D]. Kunming:Kunming University of Science and Technology, 2020.] DU Kang. Study on extraction of Yunnan tobacco essential oil and purification technology of neophytadiene[D]. Kunming: Kunming University of Science and Technology, 2020.
[24] WANG Q, QIN D, HUANG G, et al. Identification and characterization of the key volatile flavor compounds in black teas from distinct regions worldwide[J]. Journal of Food Science,2022,87(8):3433−3446. doi: 10.1111/1750-3841.16248
[25] 里奥·范海默特. 化合物香味阈值汇编[M]. 北京:科学出版社, 2015:1−229. [VANHERIMER L. Compilations of flavour threshold values in water and other media[M]. Beijing:China Science and Technology Press, 2015:1−229.] VANHERIMER L. Compilations of flavour threshold values in water and other media[M]. Beijing: China Science and Technology Press, 2015: 1−229.
[26] OGURO D, WATANABE H. Asymmetric synthesis and sensory evaluation of sedanenolide[J]. Bioscience Biotechnology and Biochemistry,2011,75(8):1502−1505. doi: 10.1271/bbb.110206
[27] 郑宗昊, 张向争, 傅芳浩, 等. 基于HS-SPME-GC-MS技术的不同品种(系)橄榄香气成分研究[J]. 食品工业科技,2022,43(23):282−290. [ZHENG Zonghao, ZHANG Xiangzheng, FU Fanghao, et al. Study on aroma components of Canarium album of different cultivars based on HS-SPME-GC-MS[J]. Science and Technology of Food Industry,2022,43(23):282−290.] ZHENG Zonghao, ZHANG Xiangzheng, FU Fanghao, et al . Study on aroma components of Canarium album of different cultivars based on HS-SPME-GC-MS[J]. Science and Technology of Food Industry,2022 ,43 (23 ):282 −290 .[28] DUETZ W A, BOUWMEESTER H, VAN BEILEN J B, et al. Biotransformation of limonene by bacteria, fungi, yeasts, and plants[J]. Applied Microbiology and Biotechnology,2003,61(4):269−277. doi: 10.1007/s00253-003-1221-y
[29] SONG C, LIU Y, SONG A, et al. The Chrysanthemum nankingense genome provides insights into the evolution and diversification of chrysanthemum flowers and medicinal traits[J]. Molecular Plant,2018,11(12):1482−1491. doi: 10.1016/j.molp.2018.10.003
[30] YAN J, WANG H, WANG Y, et al. Integrated metabolome and transcriptome analysis reveals candidate genes involved in metabolism of terpenoids and phthalides in celery seeds[J]. Industrial Crops and Products,2021,172(114011):1−9.
[31] 李雪, 韩燕, 许晶冰, 等. 顶空固相微萃取-气质联用法研究油麦菜采后香气成分的变化[J]. 食品与发酵工业,2020,46(8):254−260. [LI Xue, HAN Yan, XU Jingbing, et al. Analysis of aroma components dynamic changes during the storage of the leaf-used lettuce by HS-SPME-GC-MS method[J]. Food and Fermentation Industries,2020,46(8):254−260.] LI Xue, HAN Yan, XU Jingbing, et al . Analysis of aroma components dynamic changes during the storage of the leaf-used lettuce by HS-SPME-GC-MS method[J]. Food and Fermentation Industries,2020 ,46 (8 ):254 −260 .[32] CHEN Q, SONG J, BI J, et al. Characterization of volatile profile from ten different varieties of Chinese jujubes by HS-SPME/GC-MS coupled with E-nose[J]. Food Research International,2018,105:605−615. doi: 10.1016/j.foodres.2017.11.054
-
期刊类型引用(2)
1. 刘爱成,杨惠仪,王奕雯,吴旭辉,陈馨萍,岳小萱,李墨翰,岳喜庆. 超声处理对乳清蛋白致敏性及结构的影响. 中国乳品工业. 2024(06): 17-22 .  百度学术
百度学术
2. 谭永曌,张迪,吉宏武,刘书成. 凡纳滨对虾热处理过程中虾青素酯与肌原纤维蛋白的结合作用. 广东海洋大学学报. 2024(06): 73-79 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:
 下载:
下载:



