Improving Effect of Ligustilide on Dextran Sodium Sulfate-induced Ulcerative Colitis
-
摘要: 目的:探究蒿本内酯(ligustilide,Lig)对葡聚糖硫酸钠(dextran sodium sulfate,DSS)诱导溃疡性结肠炎(ulcerative colitis,UC)小鼠的改善作用及机制。方法:将60只雄性SPF级C57BL/6小鼠随机分成6组,分别为空白组、DSS组、阳性药柳氮磺吡啶(sulfasalazine,SASP)组、Lig低、中、高剂量组。DSS组小鼠自由饮用3% DSS水溶液7 d复制UC模型,同时对Lig低、中、高剂量组小鼠灌胃给予药物干预治疗。通过记录小鼠每日体重和结肠长度,检测疾病活动指数(disease activity index,DAI)评分,采用酶联免疫吸附测定试剂盒定量检测血清中TNF-α、IL-6和IL-1β的表达水平,检测结肠中TLR4/NF-κB蛋白表达水平,并结合苏木素-伊红染色实验,探究Lig对小鼠UC的作用及机制。结果:与空白组比较,DSS组小鼠体重显著减轻(P<0.05),结肠长度显著缩短(P<0.05),DAI评分显著升高(P<0.05),肠道出现大量炎症性浸润现象,且结肠组织中TNF-α、IL-6和IL-1β表达水平显著升高(P<0.05);与DSS组比较,Lig中剂量组和高剂量组小鼠的肠道组织中TNF-α、IL-6和IL-1β的表达以及TLR4/NF-κB信号均被显著抑制(P<0.05),表明Lig中剂量组和高剂量组小鼠肠道损伤得到显著改善。结论:Lig能有效改善DSS诱导的小鼠UC,其机制可能是抑制NF-κB信号通路的激活。Abstract: Objective: To research the therapeutic effects and mechanisms of ligustilide (Lig) in improving dextran sodium sulfate (DSS)-induced ulcerative colitis (UC) in mice. Methods: Intervention of lig was delivered in sixty male SPF C57 BL/6 mice and the mice were differentiated in six groups according to the dose of lig as: Control group, DSS group, positive control group (treated with sulfasalazine, SASP), low-dose lig group, medium-dose lig group, and high-dose lig group. The UC in DSS mice was induced by a 3% DSS solution through oral administration for 7 days, in the meanwhile, the low, medium, and high-dose lig groups were received gavage feeding of lig and oral administration of 3% DSS solution. Before and after the intervention, the body weight, colon length, and the disease activity index (DAI) score were collected for assessment of UC. Furthermore, the expression levels of TLR4/NF-κB proteins in colon and serum TNF-α, IL-6, and IL-1β were quantitatively measured using enzyme-linked immunosorbent (ELISA) assays. Additionally, histological examination was performed to investigate the effects and mechanisms of lig in improving UC in mice by hematoxylin-eosin staining. Results: Compared to the control group, significantly reduced body weight (P<0.05), shorter colon length (P<0.05), increased DAI score (P<0.05). And there was a large amount of inflammatory infiltration in the intestine, the expression level of TNF-α, IL-6, and IL-1β in the colon significantly increased (P<0.05). Compared with DSS group, significant suppression of the TLR4/NF-κB signaling pathway in the intestinal tissue, serum TNF-α, IL-6, and IL-1β expression (P<0.05) were observed in the medium and high-dose lig groups, which indicated a significant improvement in intestinal damage. Conclusion: Lig would be able to effectively improve DSS-induced UC in mice. Moreover, the results showed that the mechanism of lig improving DSS-induced UC was possibly involved with the inhibition of the NF-κB signaling pathway.
-
Keywords:
- ligustilide /
- ulcerative colitis /
- dextran sodium sulfate /
- inflammatory factor
-
溃疡性结肠炎(Ulcerative colitis,UC)是一种病因尚不十分清楚的非特异性肠道炎症疾病,其主要临床表现是腹泻、脓血便、腹痛和里急后重等症状[1]。它的发病率日益增高,是全球性消化内科常见的疑难病之一,在我国的发病率为11.6/10万[2]。UC的发病机制目前尚不明确,主要与遗传、环境、感染、肠道菌群失调以及免疫应答等因素有关[3]。我国西药治疗UC取得了一定的疗效,治疗药物主要包括类固醇、免疫调节剂等,但引起恶心、腹泻和腹痛等不良反应仍然存在,治疗方法也存在一定的局限性,比如部分患者后期需要手术干预[4]。因此,开发有效药物治疗UC是一个亟待解决的重要问题。
随着我国中药现代化建设步伐的加快,传统中医药及其有效成分在新药研发领域中的研究成为当下的主要热点之一。藁本内酯(ligustilide,Lig),是从中草药川芎和当归中提取的有效成分之一,具有多种生物活性和药理作用,对心脑血管、循环系统及免疫功能均有较强的药理作用,有很强的解痉、平喘、镇静作用,能改善微循环、松弛平滑肌、抑菌、提高机体免疫调节等功能[5−6]。除被广泛应用于医学领域外,Lig还被用作食品添加剂,常用于饮料、酒类等食品中,以提高其香味及质感。此外,也有研究表明Lig对食品质量具有保护作用,如抑制食品的褐变、氧化等[7−8]。因此,Lig在食品工业中有着广泛的应用前景。大量的研究显示,Lig因抑制NF-κB的激活与减少炎症因子的释放表现出强大的抗炎药理活性,可治疗多种炎症相关疾病,如Lig通过介导PI3K/AKT/mTOR信号通路对脑缺血再灌注损伤大鼠模型的神经发挥保护作用[9],Lig通过抑制NLRP3炎症小体的激活改善阿霉素诱导的炎症心肌损伤[10],Lig对干扰素α诱导的人脑血管外膜成纤维细胞增殖及凋亡通过lncRNA NKILA来发挥改善作用[11]。然而,还没有研究报道Lig可以通过激活TLR4/NF-κB信号改善UC。
本研究拟使用葡聚糖硫酸钠(dextran sodium sulfate,DSS)构建UC小鼠模型,探索Lig对DSS诱导UC小鼠的改善作用,并阐明其可能的分子机制,为Lig的临床开发和利用提供理论依据,为提高UC患者的生活质量提供新的治疗策略。
1. 材料与方法
1.1 材料与仪器
60只C57 BL/6小鼠,6~8周龄,雄性,体重(22±2) g 购自上海市公共卫生临床中心,动物生产许可证号: SCXK(沪)2020-0002,常温环境饲养于温度(22±2) ℃,湿度40%~60%,12 h光照/黑暗循环的条件中,动物福利伦理审查批文号为SPF 2022049;Lig 纯度98%,成都曼思特生物科技有限公司;DSS MW36000-50000 美国MP Biomedicals生物有限公司;苏木素-伊红染色试剂盒 北京索莱宝科技有限公司生产;IL-6、TNF-α、IL-1β试剂盒 上海朗顿生物技术有限公司。
EVOS M5000型智能细胞成像系统 美国Thermo Fisher Scientific公司;ELX-800型酶标仪 美国BIO-TEK公司;FSH-2型可调高速电动匀浆器 江苏金坛市佳美仪器有限公司;Microfugu 20R型高速冷冻离心机 美国Beckman Coulter公司;RE-5289型数显恒温水浴锅 常州市国旺仪器制造有限公司;FA1004B型电子天平 上海精密科学仪器有限公司。
1.2 实验方法
1.2.1 动物造模及给药方法
将60只雄性 C57BL/6小鼠随机分为6组,每组10只,分别为空白组、DSS组、阳性药柳氮磺吡啶(sulfasalazine,SASP)组和Lig低、中、高剂量组(低剂量组:50 mg/kg;中剂量组:100 mg/kg;高剂量组:200 mg/kg[12])。适应性饲养1周后,每日称量并记录小鼠体重,除空白组外,其余组小鼠连续7 d饮用3% DSS溶液诱导UC模型[13],同时Lig低、中、高剂量组小鼠给予相应剂量药物,溶于10%生理盐水中灌胃干预治疗,空白组和DSS组小鼠以相同的方式给予等体积的生理盐水。
1.2.2 UC小鼠取材及测量结肠长度和质量
第8 d,腹腔注射适量戊巴比妥钠麻醉后,眶窦采血,解剖小鼠,测量结肠从直肠近端到回盲部的长度和质量,远端结肠组织立即用4%多聚甲醛溶液在4 ℃冰箱固定过夜,第2 d用于做石蜡切片。
1.2.3 观察UC小鼠病理组织形态
取部分结肠用4%多聚甲醛固定,石蜡包埋,切片进行苏木素-伊红染色组织学评估。将石蜡切片脱蜡,按照试剂盒说明书步骤对组织进行染色,用中性树胶对切片封片,在100倍光镜下以不同的视野在相同的设置下观察结肠组织的病理学改变。
1.2.4 UC小鼠的相关指数评价
在整个实验过程中,每天观察并记录小鼠的体重减轻、排便情况和直肠出血情况。参照文献[14]的方法,对造模后大鼠体重下降率、大便性状及大便隐血情况进行疾病活动指数(disease activity index,DAI)评分,以评估UC的严重程度(表1)。DAI=(体重+大便形态+大便出血)/3。小鼠麻醉取血后,取结肠组织并剖开,0.9% NaCl冲洗干净,观察结肠黏膜。根据文献[15]操作方法进行结肠损伤指数(colon and mesentery injury,CMDI)评分。按照文献[16]方法操作,观察结肠组织病理学,并进行结肠组织学指数(histological,HS)评分。结肠切片染色的组织学评价分级如下:0级:无炎症迹象;1级:低白细胞浸润;2级:中度白细胞浸润;3级:高白细胞浸润,中度纤维化,高血管密度,结肠壁增厚,中度杯状细胞丢失,局灶性隐窝丢失;4级:白细胞透壁浸润,杯状细胞大量丢失,广泛纤维化,弥漫性隐窝丢失。
表 1 DAI的评分标准Table 1. Scoring criteria for DAI评分 体重下降(%) 大便性状 便血情况 0 <1 正常 阴性 1 ≥1~5 软便 阴性 2 ≥5~10 软便 隐血阳性 3 ≥10~20 腹泻 隐血阳性 4 ≥20 腹泻 血便 1.2.5 血清中炎症因子TNF-α、IL-6和IL-1β水平的测定
在实验进行的第8 d,取小鼠静脉血放置于无菌离心管中,室温静置40 min,于4 ℃、2500 r/min条件下离心15 min,收集管中的上层血清,使用酶联免疫吸附测定试剂盒测定血清液中的TNF-α、IL-6和IL-1β水平,多余血清置于−80 ℃冰箱保存备用。
1.2.6 UC小鼠结肠组织中蛋白免疫印迹分析
称取100 mg结肠组织,用含有蛋白酶和磷酸酶抑制剂的十二烷基硫酸钠样品缓冲液匀浆,收集上清,测定蛋白浓度,制备样品进行电泳、电转及5%脱脂奶粉封闭的过程后,在4 ℃下孵育一抗过夜,第2天室温孵育二抗1 h,最后在凝胶成像仪下进行显影,使用Image J分析软件对蛋白条带的灰度值进行分析。
1.3 数据处理
采用GraphPad Prism 8.0.2软件进行统计学分析,计量资料以均数±标准差(±s)表示,多组间比较采用单因素方差分析,当数据满足正态分布和方差齐性时,两两比较用LSD检验,当数据不满足正态分布或方差齐性时,两两比较用Dunnett’s检验,P< 0.05为差异有统计学意义。
2. 结果与分析
2.1 Lig对UC小鼠一般情况的影响
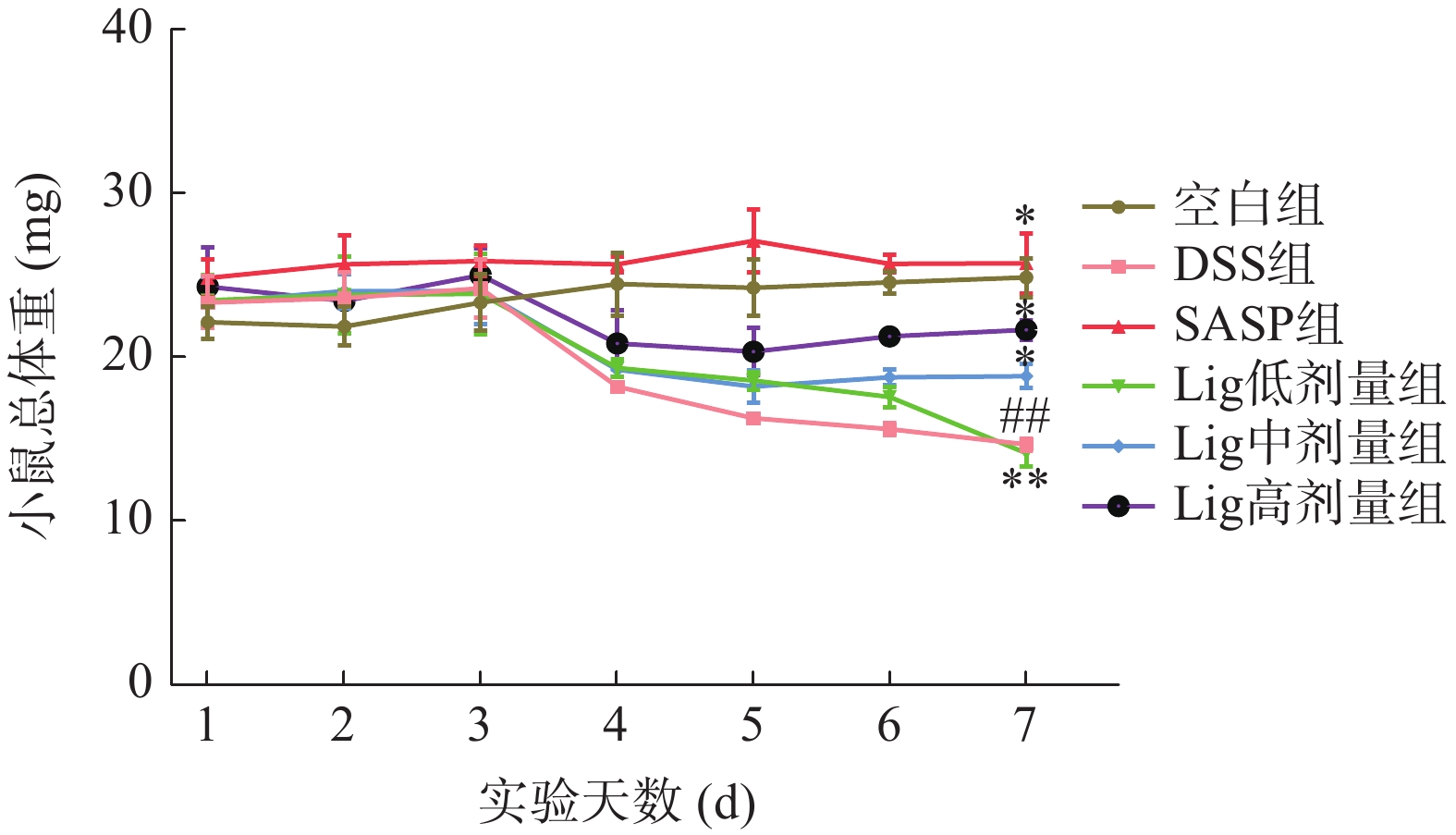
结肠炎是一种疾病,其特征是慢性和反复发作的肠道炎症。通过使用小鼠模型模拟结肠炎,可以更好地了解该疾病的发病机制,以及治疗性药物的疗效。DSS是一种常用的诱导结肠炎的化学品,可以损伤肠道黏膜并引发炎症反应[17]。在这项实验中,其使用可使小鼠模型表现出与结肠炎患者相似的症状。如图1所示,与空白组比较,DSS组小鼠饮食量明显减少,造模第3 d个别小鼠便稀;小鼠体重在第4 d显著降低(P<0.05),毛发失去光泽,精神萎靡;造模第5 d出现不同程度的腹泻、便血、肛门血染等现象。与DSS组比较,Lig各剂量组小鼠状态均有所好转,进食量逐渐增多,大便性状逐渐开始好转,Lig低剂量组小鼠体重显著升高(P<0.05),Lig中和高剂量组小鼠体重极显著升高,差异具有统计学意义(P<0.01),与董晶等[3]研究结果一致,充分说明Lig能够改善UC小鼠的病理状况。
2.2 Lig对UC小鼠DAI、CMDI和HS的影响
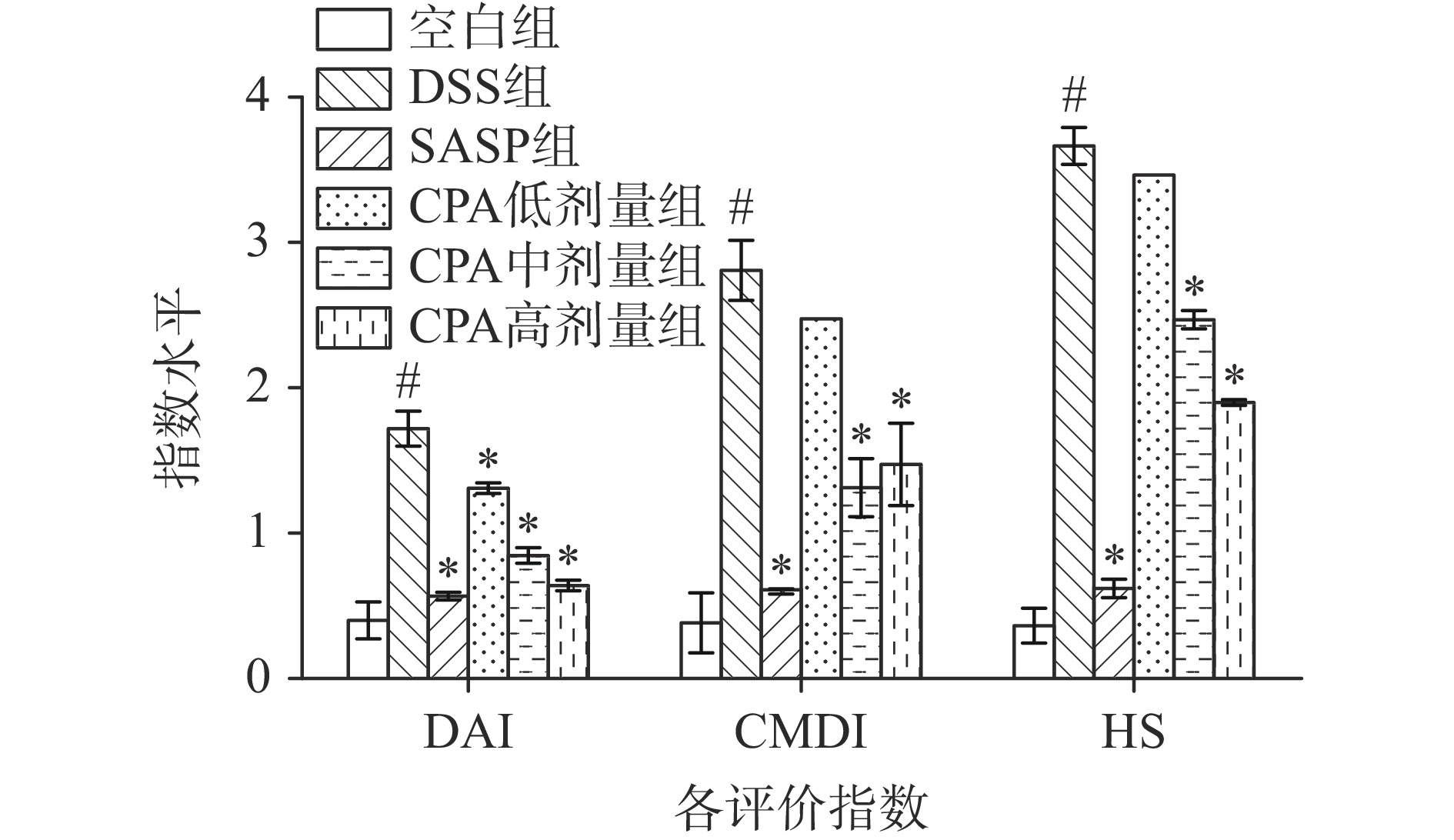
DAI、CMDA和HS是评价结肠炎症状严重程度和疗效的常用指标,具有很高的临床应用价值。DAI是结合患者的体重下降百分率、大便黏稠度和大便出血三种情况进行综合评分,将3项结果的总分除以3即得到DAI值[18]。CMDI是结肠长度反映慢性炎症和损伤修复的间接指标[19]。HS主要通过结肠组织病理切片观察各组大鼠结肠病变情况评分[20]。如图2所示,与空白组比较,DSS组小鼠的DAI、CMDA和HS三个指数评分均明显增加,差异均有统计学意义(P<0.05),说明其处于较为严重的结肠炎状态。与DSS组比较,Lig中、高剂量实验组的DAI、CMDA和HS三个指数评分显著降低,差异均有统计学意义(P<0.05),提示Lig对结肠炎具有一定的治疗效果,而Lig低剂量组的DAI、CMDA和HS三个指标无显著性差异,说明Lig的作用剂量具有一定的关键性。与Wang等[21]的研究结果一致,充分说明Lig对UC小鼠的结肠组织起到一定改善作用。
2.3 Lig对UC小鼠结肠长度重量比的影响
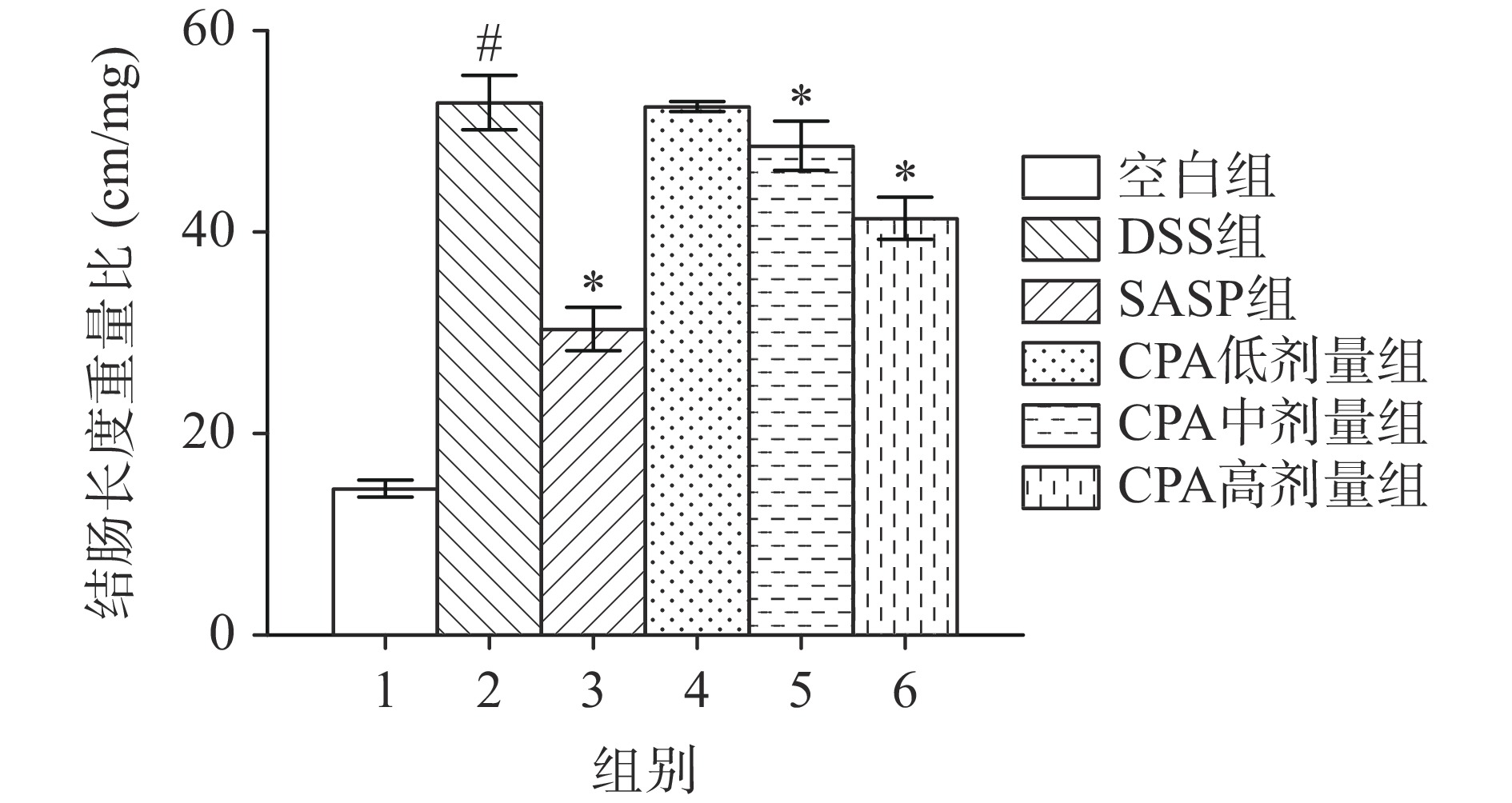
结肠长度的变化可以反映肠道炎症的程度和对肠道组织的损伤程度。在结肠炎模型中,由于炎症反应的存在,结肠黏膜会出现不同程度的缩短或者变形,导致结肠总长度的减小[22]。肠道组织的重量变化可以反映结肠气肿和水肿等病理过程。在结肠炎模型中,由于炎症反应导致的组织水肿和充血会使得结肠重量显著增加,因此测量结肠重量可以反映结肠炎症的程度,并帮助评估治疗效果[23]。如图3所示,与空白组比较,DSS组小鼠的结肠平均长度显著缩短,结肠重量明显增加,结肠长度重量比显著增加,差异具有统计学意义(P<0.05);与DSS组比较,Lig中和高剂量组小鼠的结肠平均长度显著增长,结肠重量明显减少,结肠长度重量比显著降低,差异具有统计学意义(P<0.05),与董晶等[3]研究结果一致,说明显著改善了DSS作用引起的结肠长度缩短的病症,其中Lig各剂量组间相比,Lig高剂量组治疗效果优于其余两组。
2.4 Lig对UC小鼠的结肠病理组织损伤的影响
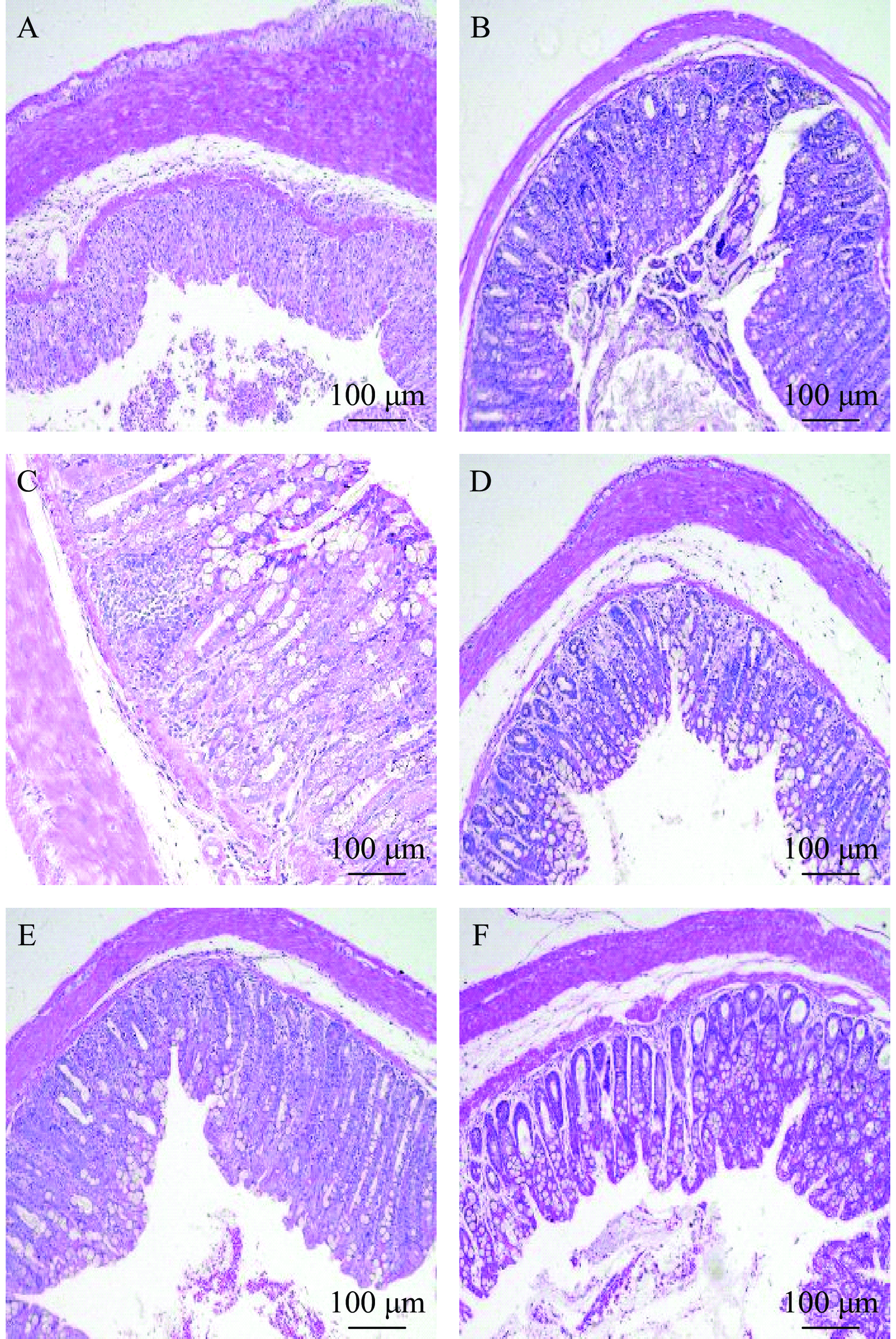
炎性细胞浸润是大多数结肠炎的典型特征,以白细胞的浸润为主。炎性细胞浸润可能导致肠壁变厚,肠道管腔受压迫并产生炎性假性息肉。肠壁增厚和肌肉层病理变化:在炎症的特定阶段,结肠黏膜下层间质细胞或炎性细胞的增生可能导致肠壁明显的增厚[24]。如图4所示,与空白组比较,DSS组小鼠的结肠组织出现明显的上皮细胞损伤,包括隐窝结构弥漫性损伤、杯状细胞丢失和大量中性粒细胞浸润至固有层;与DSS组比较,Lig中、高剂量组小鼠具有相对完整的隐窝结构,上皮变形较少,炎症细胞浸润较少;Lig低剂量组小鼠则表现出较明显的组织损伤,隐窝结构部分损伤,炎症细胞浸润较多。与Nameer等[25]的实验结果一致,表明Lig可以对UC小鼠的结肠病理组织损伤程度发挥一定改善作用。
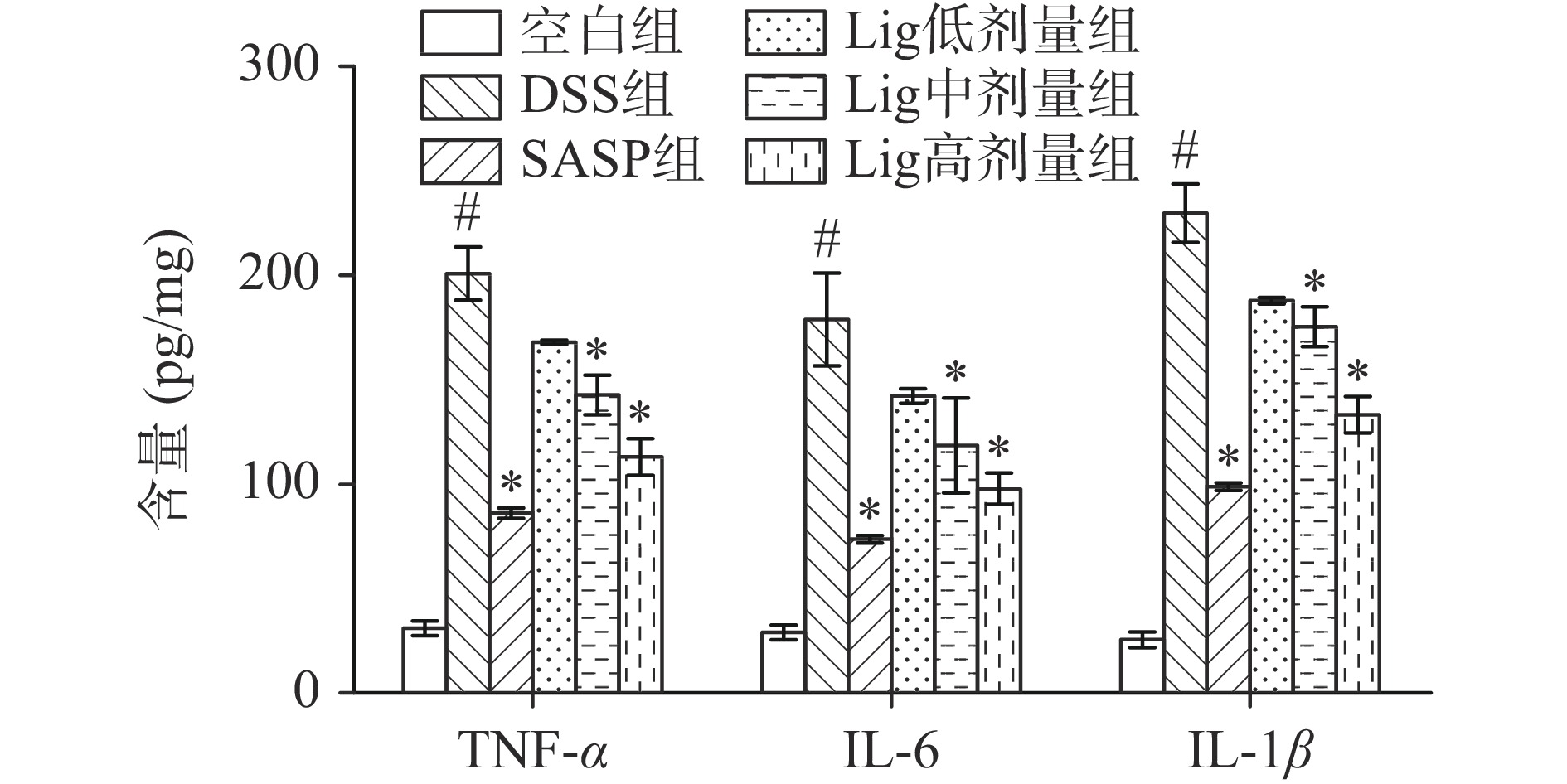
2.5 Lig对UC小鼠血清中TNF-α、IL-6和IL-1β水平的影响
TNF-α、IL-6和IL-1β是三种重要的炎症因子,它们在免疫系统中起到重要的作用。TNF-α能够诱导炎症反应、增强免疫细胞的活性,是重要的调节剂,可以引起全身性症状和导致组织损伤[26]。在炎症过程中,IL-6可以增加白细胞数量和活性,促进其他免疫因子的产生,参与身体的免疫应答[27]。IL-1β可以促进炎症細胞的增殖和释放[28]。如图5所示,与空白组比较,DSS组小鼠结肠中促炎细胞因子TNF-α、IL-6和IL-1β的表达显著升高(P<0.05);与DSS组相比,Lig中、高剂量组小鼠结肠中TNF-α、IL-6和IL-1β的表达水平显著降低(P<0.05)。以上结果与董晶等[3]研究结果一致,表明Lig可显著抑制DSS所致UC的炎症因子表达升高,且Lig高剂量的治疗效果最佳。
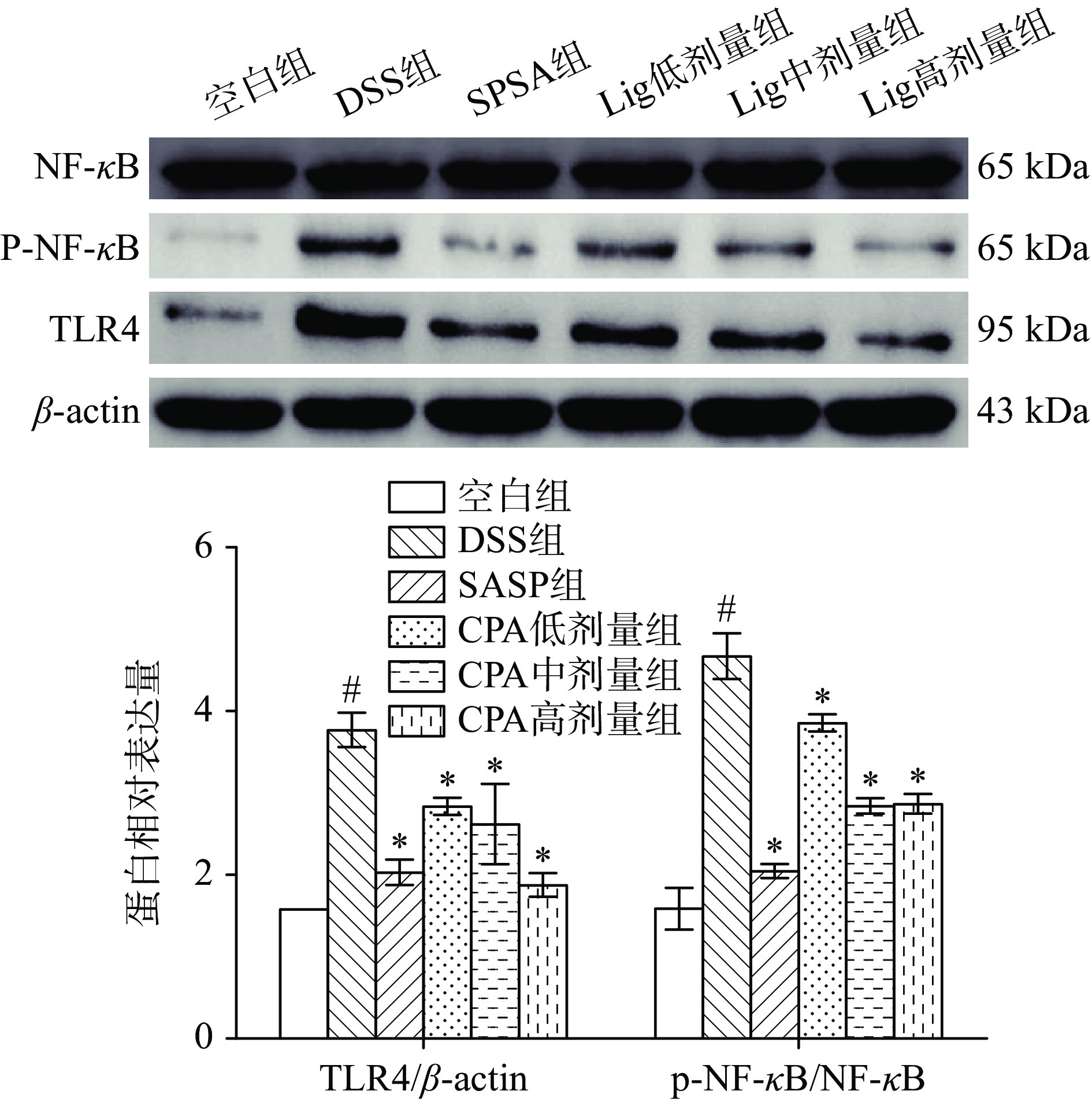
2.6 Lig对UC小鼠结肠中TLR4/NF-κB信号通路的影响
TLR4/NF-κB信号通路与细胞因子的产生密切相关。各种外源源性危险信号可激活TLR4受体并进一步诱导下游转录因子NF-κB活化,最终促进促炎因子和趋化因子的产生。如图6所示,与空白组比较,DSS组小鼠结肠TLR4蛋白的表达和NF-κB蛋白的磷酸化显著升高(P<0.05);与DSS组比较,SASP组和Lig高剂量组小鼠结肠TLR4蛋白的表达和NF-κB蛋白的磷酸化显著降低(P<0.05),而Lig低和中剂量对UC小鼠结肠组织中蛋白表达无显著性区别。上述结果与Ma等[29]研究结果一致,表明Lig治疗UC可能与抑制NF-κB信号通路相关,可抑制炎症因子释放,减缓炎症反应的发生。
3. 讨论与结论
UC是一种反复发作的慢性肠道非特异性炎症反应,常常会引发免疫系统失调,在不同程度上可引起从直肠到近端结肠的连续黏膜炎症[1]。Lig作为中药当归的主要有效成分之一,具有镇静、镇痛、解热及抗炎药理作用。本研究通过给予小鼠喂喝3% DSS水溶液复制UC模型,小鼠若出现便血和体重下降,结肠上皮细胞坏死、溃疡和炎症细胞浸润等情况,说明建模成功。观察小鼠一般情况、体重及其结肠长度进行DAI等相关指数分析,通过测定血清中各种细胞因子水平,结合苏木素-伊红染色判断结肠损伤程度,发现Lig对UC小鼠的改善作用机制可能与抑制NF-κB信号通路相关。
DAI是一种用于评估疾病活性的指标,常用于评估慢性肠道炎症疾病,如UC和克罗恩病的临床状况[14]。CMDI是结肠长度反映慢性炎症和损伤修复的间接指标[15]。HS主要通过结肠组织病理切片观察各组大鼠结肠病变情况评分[16]。本试验结果表明,与空白组相比,DSS组小鼠的DAI、CMDI和HS指数水平显著升高(P<0.05),与DSS组相比,Lig中和高剂量DAI、CMDI和HS三个指数水平显著降低(P<0.05),其中高剂量Lig的治疗效果最明显,与Wang等[21]的研究结果一致,充分说明Lig可以改善小鼠UC的病理情况。
TNF-α是TNF超家族的原型成员,主要由巨噬细胞和单核细胞分泌,是炎症反应和相关疾病的产生和发展中的主要促炎细胞因子[26]。IL-6是一种具有184个氨基酸的四螺旋多效细胞因子,该蛋白质由成纤维细胞、单核细胞、巨噬细胞、T细胞和内皮细胞合成,其合成和分泌在炎症条件下诱导,在免疫反应、炎症和造血中起着重要作用[27]。IL-1β是抗微生物免疫以及自身免疫炎症的关键介质、有效的促炎因子,对于宿主反应和对病原体的抵抗至关重要,还会加剧慢性疾病和急性组织损伤期间的损害[28]。
本试验结果表明,与空白组相比,DSS组小鼠血清中TNF-α、IL-6、IL-1β的表达水平显著升高(P<0.05);与DSS组相比,Lig中和高剂量能有效抑制UC小鼠TNF-α、IL-6、IL-1β的表达水平,表明Lig治疗UC可能与抑制炎症因子释放,达到炎症缓解。越来越多的证据表明TLR4/NF-κB通路在结肠炎发病中发挥重要作用,抑制TLR4/NF-κB通路可以改善DSS所致的UC[30],例如MA等[29]报道白头翁皂苷B4可通过抑制 TLR4/NF-κB/MAPK信号通路预防小鼠UC;JIANG等[31]也报道了黄芩苷可通过抑制TLR4/NF-κB信号通路对大鼠UC发挥抗炎作用。因此,我们推测Lig的抗炎作用可能是通过抑制TLR4介导的NF-κB通路的激活而实现的。本实验中,与空白组相比,DSS组小鼠结肠组织TLR4蛋白表达量和NF-κB磷酸化水平显著升高,Lig干预能显著减少DSS引起的上述效应,这些体外结果表明,抑制TLR4/NF-κB信号通路以减轻炎症反应发生可能是Lig发挥抗UC的重要机制。
本实验虽然存在未设定体内细胞实验论证以及给药治疗时间太短等缺陷,但是通过查阅文献[12]复制UC小鼠模型等系列实验充分说明Lig能有效缓解DSS诱导的小鼠UC,机制可能是通过抑制NF-κB的表达及活化,进而抑制促炎因子TNF-α、IL-1β、IL-6的释放。由此推断,Lig缓解UC小鼠的机制可能与NF-κB信号通路有关,有望成为预防和治疗UC的辅助药物。
-
表 1 DAI的评分标准
Table 1 Scoring criteria for DAI
评分 体重下降(%) 大便性状 便血情况 0 <1 正常 阴性 1 ≥1~5 软便 阴性 2 ≥5~10 软便 隐血阳性 3 ≥10~20 腹泻 隐血阳性 4 ≥20 腹泻 血便 -
[1] HENRY H R, STEPHANIE B, YU B, et al. Pharmacological inhibition of NPY receptors illustrates dissociable features of experimental colitis in the mouse DSS model:Implications for preclinical evaluation of efficacy in an inflammatory bowel disease model[J]. Public Library of Science One,2019,14(8):1−22.
[2] YE Y L, PANG Z, CHEN W C, et al. The epidemiology and risk factors of inflammatory bowel disease[J]. International Journal of Clinical and Experimental Medicine,2019,12(9):1−12.
[3] 董晶, 王帅珂, 吴苹, 等. 鱼腥草多酚对葡聚糖硫酸钠(DSS)诱导小鼠溃疡性结肠炎的改善作用[J]. 现代食品科技,2021,37(12):7−13. [DONG J, WANG S K, WU P, et al. Effects of polygonum hydropiper polyphenols on the improvement of dextran sulfate sodium (DSS)-induced colitis in mice[J]. Modern Food Science and Technology,2021,37(12):7−13.] DONG J, WANG S K, WU P, et al . Effects of polygonum hydropiper polyphenols on the improvement of dextran sulfate sodium (DSS)-induced colitis in mice[J]. Modern Food Science and Technology,2021 ,37 (12 ):7 −13 .[4] ZHONG W T, LU X L, SHI H T, et al. Distinct microbial pop ulations exist in th mucosa-associated microbiota of diarrhea predominant irritable bowel syndrome and ulcerative colitis[J]. Journal of Clinical Gastroenterology,2019,53(9):660−672. doi: 10.1097/MCG.0000000000000961
[5] WANG H F, WU L J, ZHANG B, et al. Ligustilide ameliorates inflammatory pain and suppresses the NF- κB pathway in rats[J]. Inflammation Research,2021,70(5):513−522.
[6] WU Q, MAO Z G, LIU J, et al. Ligustilide attenuates ischemia reperfusion-induced hippocampal neuronal apoptosis via activating the PI3K/Akt pathway[J]. Frontiers in Pharmacology,2020,11(6):979−989.
[7] MA Q, CUI Y, DU H, et al. Ligustilide improves sensory and physicochemical qualities and inhibits microbial growth of chilled mutton[J]. Meat Science,2019,150:37−44.
[8] ZHANG X, SU X, WU N, et al. Ligustilide extends the shelf life of fresh-cut Chinese yam through inhibiting browning and microbial growth[J]. Food Chemistry,2018,248:239−247.
[9] 崔江波, 杨静, 王培福, 等. 蒿本内酯介导PI3K/AKT /mTOR信号通路对脑缺血再灌注损伤大鼠的神经保护机制研究[J]. 川北医学院学报,2021,36(7):826−831. [CUI J B, YANG J, WANG P F, et al. Protective mechanism of huperzine mediated PI3K/AKT/mTOR signaling pathway on neurological damage in rats with cerebral ischemia-reperfusion injury[J]. Journal of North Sichuan Medical College,2021,36(7):826−831.] CUI J B, YANG J, WANG P F, et al . Protective mechanism of huperzine mediated PI3K/AKT/mTOR signaling pathway on neurological damage in rats with cerebral ischemia-reperfusion injury[J]. Journal of North Sichuan Medical College,2021 ,36 (7 ):826 −831 .[10] 孙嘉, 刘冰, 张陆勇. 藁本内酯对阿霉素所致心肌损伤的保护作用[J]. 中药新药与临床药理,2021,32(12):1776−1784. [SUN J, LIU B, ZHANG L Y. Protective effects of gao ben neizun against doxorubicin-induced myocardial injury[J]. Chinese Journal of New Drugs and Clinical Pharmacology,2021,32(12):1776−1784.] SUN J, LIU B, ZHANG L Y . Protective effects of gao ben neizun against doxorubicin-induced myocardial injury[J]. Chinese Journal of New Drugs and Clinical Pharmacology,2021 ,32 (12 ):1776 −1784 .[11] ZHANG W Q, LI X, WANG Y, et al. Lig has a protective effect on interferon-alpha induced proliferation and apoptosis of human brain vascular adventitial fibroblasts primarily through lncRNA NKILA[J]. Chinese Journal of New Drugs and Clinical Pharmacology,2021,32(12):1776−1784.
[12] WANG X, MA J, PENG L, et al. Artemisinin mitigates experimental murine colitis via adjusting thelper cell balance[J]. International Immunopharmacology,2018,64:264−271. doi: 10.1016/j.intimp.2018.09.008
[13] QU C, YUAN Z W, YU X T, et al. Patchouli alcohol ameliorates dextran sodium sulfate-induced experimental colitis and suppresses tryptophan catabolism[J]. Pharmacological Research,2017,121:70−82. doi: 10.1016/j.phrs.2017.04.017
[14] 吴铭, 宋家乐, 任源, 等. 芸薹属紫菜蔬乙醇提取物对葡聚糖硫酸钠致小鼠结肠炎的预防作用[J]. 现代食品科技,2019,9:159−168. [WU M, SONG J L, REN Y, et al. Preventive effect of ethanol extract from orphyra spinach on sodium polysulfate-induced colitis in mice[J]. Modern Food Science and Technology,2019,9:159−168.] WU M, SONG J L, REN Y, et al . Preventive effect of ethanol extract from orphyra spinach on sodium polysulfate-induced colitis in mice[J]. Modern Food Science and Technology,2019 ,9 :159 −168 .[15] WU G R, FAN L Q, LI Y, et al. Correlation of endoscopic findings with the colonic mucosal injury score and correlation of the colonic mucosal injury score with clinical indicators in patients with ulcerative colitis[J]. World Journal of Gastroenterology,2019,25(44):6529−6542.
[16] YU Y, GONG R, MU Y, et al. Galangin attenuates inflammation and preserves barrier integrity in mice with DSS-induced acute colitis[J]. Frontiers in Pharmacology,2021,12:621930.
[17] MEHMET G, MUSTAFA C, HUSEYIN O, et al. Protective effects of tyrosol against DSS-Induced ulcerative colitis in rats[J]. Inflammation,2019,42(5):1680−1691. doi: 10.1007/s10753-019-01028-8
[18] VERSTOCKT B, VERSTOCKT S, CREYNS B, et al. Monocytes from inflammatory bowel disease patients exhibit impaired interleukin-10 secretion and increased inflammatory cytokines expression and are targets of vitamin D[J]. Clinical and Experimental Immunology,2020,199(1):55−65.
[19] MOUSAVI S, KARKHANEH M, RAZZAGHI Z, et al. Zinc supplementation for the treatment of ulcerative colitis:A systematic review and meta-analysis of randomized controlled trials[J]. Journal of Trace Elements in Medicine and Biology,2020,60:126484.
[20] MASALHA M, ROSENZWEIG S, BASAR H, et al. The gut microbiota promotes hepatic fatty acid desaturation and elongation in mice[J]. Nature Communications,2021,12(1):380.
[21] WANG J, WANG M, ZHANG X, et al. The effect of β-carotene on acute ulcerative colitis induced by dextran sulfate sodium in mice[J]. European Journal of Pharmacology,2020,879:173094.
[22] YAN X, LIU F, LI X, et al. Prophylactic effect of Bacillus coagulans on colitis and its mechanisms in mice[J]. Frontiers in Immunology,2021,12:657792.
[23] CHI L, ZHANG J, TAN X, et al. Protective effect of hydrogen sulfide on dextran sulfate sodium-induced ulcerative colitis in mice[J]. Biochemical and Biophysical Research Communications,2020,532(3):326−332.
[24] NEURATH M F. Current and emerging therapeutic targets for IBD[J]. Nature Reviews Gastroenterology & Hepatology,2019,16(11):713−738.
[25] NAMEER K S, KUMAR, NIENKE Z, et al. Impaired fatty acid β-oxidation due to carnitine deficiency drives hepatic steatosis in celiac disease[J]. Cell Reports,2021,34(7):108788.
[26] LI Y H, LI Y C, LI X D, et al. Protein kinase type 2 is involved in lipopolysaccharide-Induced TNF- α production in macrophages through toll-like receptor 4[J]. Mediators of Inflammation,2017,2017:3948062.
[27] DIRKSA, STEFAN R J. IL-6 pathway in the liver:From physiopathology to therapy[J]. Journal of Hepatology,2016,64(6):1403−1415. doi: 10.1016/j.jhep.2016.02.004
[28] QIN S, WEN J, BAI X C, et al. Asperlin inhibits lipopolysaccharide-induced inflammatory response by down-regulating MAPK and NF- κB pathways in RAW 264.7 cells[J]. Molecules,2019,24(5):861.
[29] MA H M, ZHOU M J, DUAN W B, et al. Anemoside B4 prevents acute ulcerative colitis through inhibiting of TLR4/NF-kappaB/MAPK signaling pathway[J]. International Immunopharmacology,2020,87:106794. doi: 10.1016/j.intimp.2020.106794
[30] DEJBAN P, NIKRAVANGOLSEFID N, CHAMANARA M, et al. The role of medicinal products in the treatment of inflammatory bowel diseases (IBD) through inhibition of TLR4/NF-kappaB pathway[J]. Phytotherapy Research,2021,35(2):835−845. doi: 10.1002/ptr.6866
[31] JIANG J, CAO X, LU X, et al. Puerarin ameliorated experimental colitis via suppressing dendritic cell maturation and TLR4/MyD88/NF- κB pathway[J]. International Immunopharmacology,2020,86:106421.





 下载:
下载:
 下载:
下载:



