Extraction of Volatile Compounds and Analysis of Aroma Characteristics in Fenggang Zinc-Selenium Tea
-
摘要: 为探究凤冈锌硒茶加工过程中挥发性成分变化。采用顶空固相微萃取结合气相色谱-质谱联用技术对凤冈锌硒茶加工过程中挥发性组分进行检测,优化提取条件,利用主成分分析和正交偏最小二乘法回归分析,对凤冈锌硒茶加工过程中的挥发性组分进行判定、区分和筛选。结果表明,提取工艺采用茶水比为1:6(g/mL),通过50/30 μm CAR/DVB/PDMS固相微萃取针在90 ℃条件下萃取70 min为佳。GC-MS共鉴定出91种挥发性成分,共有挥发性组分37种,醇类、酮类、酯类和醛类是构成凤冈锌硒茶香气的主要挥发性组分,其中醇类物质最丰富,含量最高。主成分分析可将凤冈锌硒茶加工前分为一类,加工后分为一类;正交偏最小二乘法回归分析表明15种挥发性组分对凤冈锌硒茶气味贡献较大。茉莉酮、(S)-氧化芳樟醇、α-紫罗酮、水杨酸甲酯、甲基庚烯酮、(E)-氧化芳樟醇、雪松醇、β-环柠檬醛、2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇、乙酰水杨酸甲酯等香气物质对构成凤冈锌硒茶特征香气品质具有重要作用。该研究可为凤冈锌硒茶的生产加工、质量控制提供理论依据。Abstract: In order to explore the variation of volatile components of Fenggang zinc-selenium tea during the production process. The combination of headspace solid phase microextraction (HS-SPME) with gas chromatography-mass spectrometry (GC-MS) was applied to detecte volatile components of Fenggang zinc-selenium tea during the production process, and optimize the extracting conditions. Principal component analysis and orthogonal partial least squares discriminant analysis were used to determine, distinguish and screen the volatile components of Fenggang zinc-selenium tea during the production process. The results showed that the best extraction process was as follows: Ratio of raw material to water was 1:6 (g/mL), extraction fiber 50/30 μm CAR/DVB/PDMS, extraction temperature at 90 ℃, extraction time for 70 min. A total of 91 volatile substances were identified by GC-MS that there were 37 kinds of common characteristic volatile components in the Fenggang zinc-selenium tea during the production process. Alcohols, ketones, esters and aldehydes were the main volatile components constituting the aroma of Fenggang zinc-selenium tea, among which alcohols were the most abundant and the highest content. Fenggang zinc-selenium tea could be divided into one category before processing and one category after processing by principal component analysis, and orthogonal partial least squares discriminant analysis showed that 15 volatile components contributed significantly to the odor of Fenggang zinc-selenium tea. Jasmonone, (S)-oxidized linalool, α-ionone, methyl salicylate, methyl heptenone, (E)-oxidized linalool, cedarol, β-cyclic citral, 2-pyrrol 6-trimethyl-6-vinyl tetrahydro-2H-furan-3-ol and methyl acetylsalicylate played an important role in the characteristic aroma quality of Fenggang zinc-selenium tea. This study can provide a theoretical basis for the production, processing, quality control of Fenggang zinc-selenium tea.
-
香气对茶叶品质的形成有着至关重要的作用,其主要由挥发性组分决定。挥发性组分的成分类别、含量高低主要由原料和加工技术等因素决定。在检测风味物质方面,相较于其他方法,顶空固相微萃取[1-2](Headspace solid-phase microextraction,HS-SPME)-气相色谱-质谱(Gas chromatography-mass spectrometry,GC-MS)联用法简单方便、灵敏度高、选择性好,已被广泛应用于各种样品的挥发性组分检测,为样品的品质分析提供依据。
凤冈锌硒茶是贵州特色茶类之一,属国家地理标志产品,其主要生产地区集中于贵州凤冈地区。由于茶树品种、产地、季节和采制方法的不同,凤冈锌硒茶形成了自己独特的品质特征。成品外形扁平直滑,色泽翠绿或谷黄、汤色翠黄绿,香气栗香,滋味醇和甘甜,其加工流程为鲜叶-摊青-杀青-做形(理条)-干燥-提香(炒干)-精选-成品。目前针对凤冈锌硒茶研究的文献大多数研究集中在其活性的作用机制[3],如王晓宁等[4]研究凤冈锌硒茶对小鼠代谢调节的机制,也有文献研究通过电子鼻对湄潭翠芽茶、石阡苔茶、凤冈锌硒茶、都匀毛尖进行鉴别[5]。但对于凤冈锌硒茶活性成分,以及加工过程中凤冈锌硒茶挥发性组分的含量差异及其类别变化规律方面的研究少有报道。
因此,为探索凤冈锌硒茶挥发性组分以及探究加工过程中挥发性组分的变化规律,本研究以凤冈锌硒茶为原料,优化其挥发组分提取条件;基于HS-SPME-GC-MS技术对凤冈锌硒茶加工过程中挥发性组分进行测定,利用主成分分析[6](Principal component analysis,PCA)和正交偏最小二乘判别分析法(Orthogonal partial least squares discriminant analysis,OPLS-DA)[7]对凤冈锌硒茶进行判定、区分和筛选,通过变量重要性因子(投影)(Variable importance for the projection,VIP)[8]找出加工过程中的标志性化合物,以此探究加工过程中凤冈锌硒茶挥发性组分的差异,为综合评价凤冈锌硒茶的品质提供参考,为凤冈锌硒茶的生产、质量控制提供理论依据。
1. 材料与方法
1.1 材料与仪器
凤冈锌硒茶原料(茶青) 杀青后半成品,成品各7批,2022年4月收集于贵州省遵义市凤冈县;甲醇、乙腈 色谱纯,安徽天地高纯溶剂公司;超纯水 Milli-Q 纯水器。
8890GC-7000D型气相色谱质谱联用仪 美国Agilent公司;磁力加热搅拌器、顶空进样瓶、固相微萃取手动进样手柄、85 μm PA、100 μm PDMS、50/30 μm CAR/DVB/PDMS固相微萃取头 美国Supelco公司。
1.2 实验方法
1.2.1 样品处理
鲜叶原料采摘后,其加工流程为鲜叶-摊青(原料)-杀青(半成品)-做形(理条)-干燥-提香(炒干)-精选-成品(成品),原料、杀青后半成品、成品经研磨后装于自封袋中于4 ℃保存。
1.2.2 萃取方法
参考李永迪等[9]的条件,精密称取样品,置于15 mL SPME萃取瓶中,加入热水,并使用带有聚四氟乙烯顶空隔垫的钳口盖密封顶空瓶,置于恒温炉平衡。将固相微萃取针插入萃取瓶中,边平衡边萃取70 min,随后将萃取头插入到GC进样口,在250 ℃的条件下解吸5 min。为防止样品间的污染,萃取头于进样前在300 ℃老化5 min,萃取结束后在300 ℃老化20 min。
1.2.3 萃取方法优化
1.2.3.1 萃取头对挥发性成分的影响
固定提取时间为60 min,茶水比为1:7(g/mL),提取温度为90 ℃,考察85 μm PA、100 μm PDMS、50/30 μm CAR/DVB/PDMS萃取头对挥发性成分的影响。
1.2.3.2 提取时间对挥发性成分的影响
固定茶水比为1:7(g/mL),提取温度为90 ℃,采用50/30 μm CAR/DVB/PDMS萃取头,考察时间50、60、70、80 min对挥发性成分的影响。
1.2.3.3 茶水比对挥发性成分的影响
固定提取时间为70 min,提取温度为90 ℃,采用50/30 μm CAR/DVB/PDMS萃取头,考察茶水比1:5、1:6、1:7、1:8(g/mL)对挥发性成分的影响。
1.2.3.4 温度对挥发性成分的影响
固定提取时间为70 min,茶水比为1:7(g/mL),采用50/30 μm CAR/DVB/PDMS萃取头,考察温度70、80、90、100 ℃对挥发性成分的影响。
1.2.4 GC-MS/MS条件
GC条件石英毛细管色谱柱:Agilent HP-5MS(250 μm×0.25 μm,30 m);载气为高纯氦气(纯度不小于99.999%);恒流体积流量:1.0 mL/min,进样口温度250 ℃,不分流进样,溶剂延迟3 min。升温程序:35 ℃保持2 min,以3 ℃/min升至60 ℃保持3 min,以2 ℃/min升至100 ℃,以5 ℃/min升至150 ℃保持1 min,以8 ℃/min升至250 ℃保持6 min。
MS条件离子源:电子轰击源(EI),离子源温度230 ℃,四级杆温度150 ℃,质谱接口温度250 ℃,电子能量70 eV,扫描方式为全扫描模式(SCAN):扫描范围m/z 45~460。
1.3 数据处理
将各色谱峰对应的质谱图与NIST 17标准谱库比对进行定性挥发性物质。采用面积归一化法定量。数据统计采用Excel 2010,图表绘制采用Origin 2018,主成分分析和正交偏最小二乘法回归分析采用SIMCA 14.1。
2. 结果与分析
2.1 萃取条件对凤冈锌硒茶挥发性成分的影响
2.1.1 不同萃取头对凤冈锌硒茶挥发性成分测定的影响
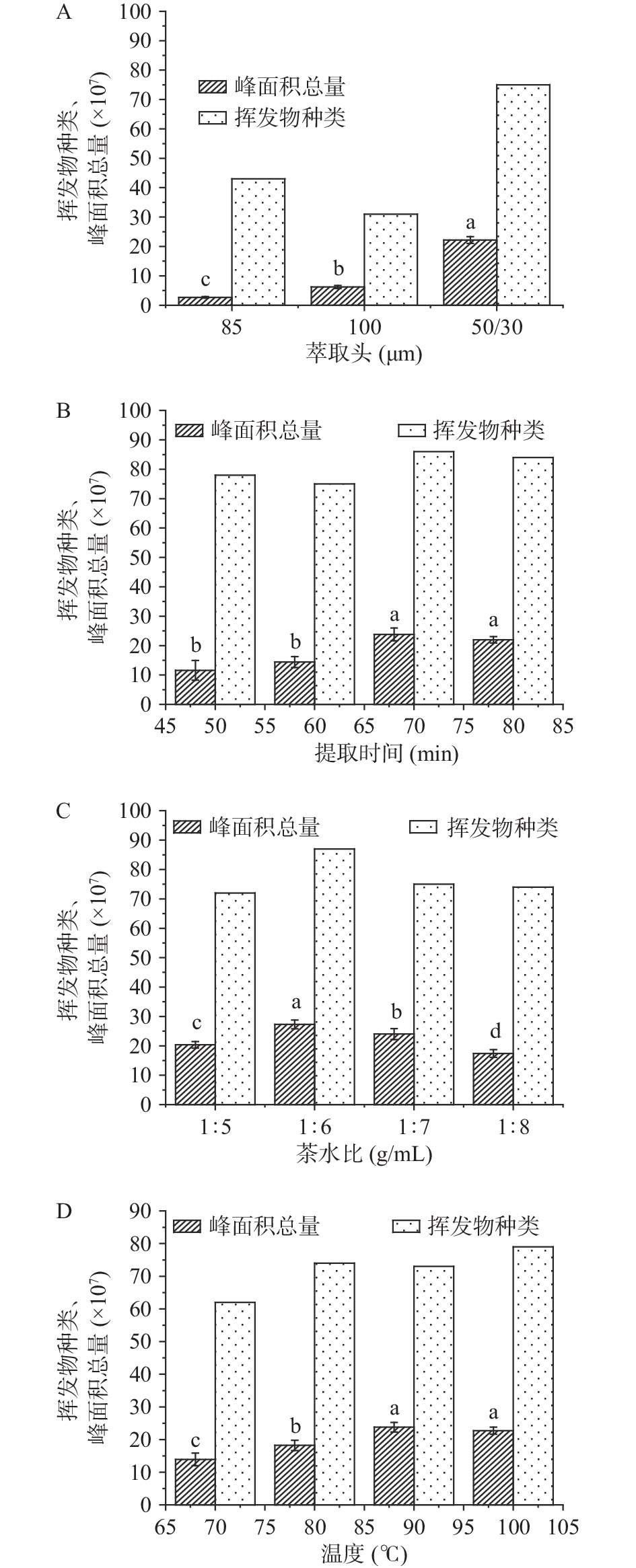
本实验考察了3种不同类型的固相微萃取头对凤冈锌硒茶香气组分数量及总峰面积的影响,结果如图1A所示。50/30 μm CAR/DVB/PDMS萃取头明显比85 μm PA、100 μm PDMS萃取头吸附到的峰面积总量和挥发物数量多,这是因为固相微萃取头的吸附强度主要取决于涂层材料的性质和厚度,涂层的极性不同,对不同极性香气物质的吸附差异性很大[10]。而50/30 μm CAR/DVB/PDMS萃取头因兼有极性和非极性涂层,所以吸附范围较广,这与茶叶香气组成复杂、各组分之间极性差异很大的特点相适应。因此,选用50/30 μm CAR/DVB/PDMS萃取头捕集凤冈锌硒茶香气组分。
2.1.2 不同提取时间对凤冈锌硒茶挥发性成分测定的影响
由图1B可知,提取时间对峰面积总量影响较大,大致呈先上升后下降的趋势,在提取时间为70 min时峰面积总量和挥发物种类均达到最大,分别为23.80×107、86种。在80 min分钟时峰面积总量(21.99×107)和挥发物数目为(84种)与70 min时差异不明显,主要是由于随着平衡时间的增加挥发物浓度会增加直到平衡,但随着平衡时间的继续增加,原来挥发出来的物质会重新溶解在样品当中,造成挥发物浓度的下降,而挥发物种类变化不大。因此,选择提取时间为70 min进行实验。
2.1.3 茶水比对凤冈锌硒茶挥发性成分测定的影响
由如图1C所示,随着茶水比的增加,凤冈锌硒茶挥发性成分的总峰面积和挥发物数量呈现先增加后减少的趋势。在茶水比为1:6(g/mL)时,总峰面积(27.30×107)和挥发物数量(87种)达到最大。与其他茶水比的总峰面积(24.03×107~17.41×107)相比较,差异显著,且其他茶水比的挥发物数量(72~75)远小于茶水比1:6(g/mL)。合适的水量能使纤维头在样品瓶中有最大的吸附量。若水量过少则会有少量样品没有完全浸没,水量过多,多余的水会使液面上方的顶空体积减小,影响挥发性物质的挥发。故选择茶水比为1:6(g/mL)进行萃取较为合适。
2.1.4 不同萃取温度对凤冈锌硒茶挥发性成分测定的影响
经GC-MS分析获得样品的挥发物的数量和总峰面积,结果见图1D。萃取温度对凤冈锌硒茶香气的萃取效果影响明显。随着温度升高,挥发物数量与总峰面积明显增大。当温度在80~90 ℃时,挥发物数目变化不大;当温度达到90 ℃时,峰面积达到最大(23.79×107),此时化合物数目为73种;随后继续升高温度至100 ℃时,化合物数目(79种)大于90 ℃时的挥发物数目,而总峰面积无明显差异。原因是在较低的萃取温度下,茶叶香气的挥发速度较慢,达到香气平衡所需时间较长,从而影响分析结果的准确性。相反,在较高萃取温度下,分子热运动加剧,茶叶香气的挥发速度增大,达到香气平衡所需时间缩短;但温度过高则会使香气组分发生异构化或通过热裂解途径产生新的香气组分,同时温度高产生的水蒸气会影响萃取头的使用寿命,还会促使萃取头固有组分的解析,从而降低萃取头萃取分析组分的能力。因此,选择萃取温度为90 ℃。
2.2 加工过程中凤冈锌硒茶挥发性成分分析
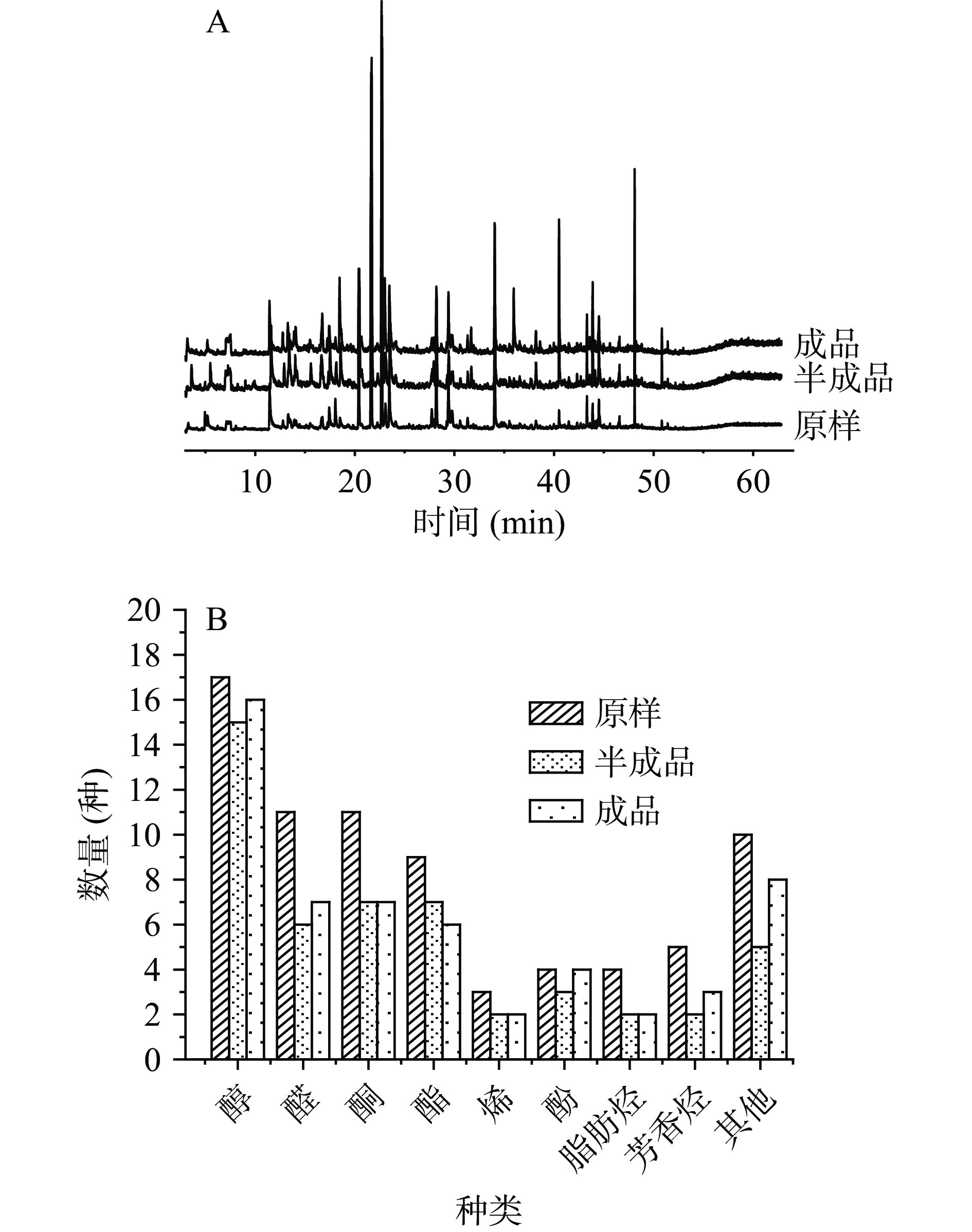
通过上述的提取检测条件,对凤冈锌硒茶挥发性组分进行分析,得出的总离子流色谱图见图2A。经谱库搜索质谱解析,在凤冈锌硒茶加工过程中共分离鉴定出91种挥发性成分,包含醇类(22种)、醛类(12种)、酮类(13种)、酯类(11种)、烯类(3种)、酚类(5种)、脂肪烃(4种)、芳香烃(6种)、和其他类(15种)等9种类型的挥发性物质,其挥发性组分在加工前后的数量分布见图2B。对于分离鉴定出的91种挥发性成分的定性和定量结果见表1,其中检测到的共有化合物为37种,相对含量较高的挥发性成分有14种,分别为1-辛烯-3-醇、苯甲醇、(E)-氧化芳樟醇、(S)-氧化芳樟醇、芳樟醇、2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇、苯乙醇、香叶醇、苯甲醛、苯乙醛、茉莉酮、β-紫罗酮、3,5,5-三甲基-1-己烯和5-戊基间苯二酚,这与前人研究结果类似[11]。绿茶原料经过杀青等工艺后,挥发性组分的总量、组分种类大多呈下降趋势,这表明加工对凤冈锌硒茶绿茶香气有较大的影响,但香气总量与组分的变化速率并不一致。在原料中挥发性组分共有74种,半成品检出挥发性组分共有49种,在成品中检出55种挥发性组分。半成品与原料相比,各成分均在减少,减少大小依次为其它=醛类>酮>芳香烃>醇、酯、脂肪烃>酚、烯类;成品与原料相比,酯类减少,醇、醛、酚、芳香烃、其他类增加,酮、烯、芳香烃保持不变。
表 1 凤冈锌硒茶中挥发性成分组成及其相对含量(%)Table 1. Composition and relative content of volatile components in the Fenggang zinc-selenium tea (%)种类 保留时间(min) 化合物名称 分子式 原样 半成品 成品 醇 5.36 反-3-己烯醇 C6H12O 0.53±0.38 0.89±0.91 0.10±0.19 5.56 3-己烯-1-醇 C6H12O 0.15±0.39 − 0.11±0.30 6.50 正己醇 C6H14O 0.03±0.07 − − 13.16 环丁基甲醇 C5H10O − − 0.33±0.88 13.35 1-辛烯-3-醇 C8H16O 1.87±0.79 7.22±6.40 3.79±2.81 17.49 苯甲醇 C7H8O 2.52±0.81 2.38±1.47 1.75±0.51 20.34 (2Z)-2-辛烯-1-醇 C8H16O − 0.85±2.25 − 20.44 (E)-氧化芳樟醇 C10H18O2 8.58±1.89 5.58±1.01 6.01±3.18 20.67 1-辛炔-3-醇 C8H14O − − 0.21±0.55 20.69 正辛醇 C8H18O 0.11±0.20 0.34±0.89 − 21.68 (S)-氧化芳樟醇 C10H18O2 21.36±4.58 12.10±3.15 12.58±8.01 22.72 芳樟醇 C10H18O 16.07±5.90 15.81±6.95 14.67±3.34 23.08 二氢芳樟醇 C10H16O − 1.83±2.53 3.59±2.23 23.50 苯乙醇 C8H10O 5.30±1.30 5.80±0.90 7.91±7.84 24.04 苏合香醇 C8H10O 0.60±0.34 0.21±0.41 0.80±1.41 27.81 6-乙烯基-2,2,6-三甲基-四氢吡喃-3-醇 C10H18O2 1.06±0.75 − − 28.19 2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇 C10H18O2 5.48±0.93 4.51±1.43 4.18±1.00 29.25 α-松油醇 C10H18O 0.11±0.19 0.42±0.62 0.10±0.26 33.57 橙花醇 C10H18O 0.08±0.22 − − 34.08 香叶醇 C10H18O 6.80±3.61 5.45±2.35 5.80±2.06 42.31 (E,Z)-金合欢醇 C13H22O 0.05±0.14 − − 46.58 雪松醇 C15H26O 0.52±0.14 1.05±0.38 0.77±0.60 醛 5.00 2-己烯醛 C6H10O 1.13±0.53 − − 8.18 庚醛 C7H14O 0.19±0.14 − − 11.56 苯甲醛 C7H6O 5.37±1.74 4.83±3.19 6.05±2.71 18.11 苯乙醛 C8H8O 2.96±0.97 2.32±2.20 1.13±0.91 18.66 3,4-二甲基-1H-吡咯-2-甲醛 C7H9NO 0.07±0.19 2.70±3.82 0.18±0.48 20.70 丙烯醛 C3H4O 0.01±0.03 − 0.04±0.09 20.74 巴豆醛 C4H6O − 0.03±0.07 − 29.25 2-羟基-4-甲基苯甲醛 C8H8O2 0.22±0.59 − − 29.83 藏花醛 C10H14O 1.03±0.49 0.68±0.55 0.88±0.40 30.59 癸醛 C10H20O 0.23±0.60 − 0.37±0.97 31.33 β-环柠檬醛 C10H16O 0.90±0.22 1.28±0.42 1.29±0.63 34.75 2,4,6-三甲基苯甲醛 C10H12O 0.18±0.17 − 0.03±0.07 酮 6.23 双乙烯酮 C4H4O2 0.01±0.03 − − 6.64 2-庚酮 C7H14O 0.02±0.04 − 0.05±0.13 12.96 1,1,1-三氟-2-丁酮 C4H5F3O 0.03±0.08 − − 14.03 甲基庚烯酮 C8H14O 0.33±0.20 1.64±1.13 1.35±0.90 20.09 苯乙酮 C8H8O 0.03±0.06 0.01±0.02 0.07±0.18 21.63 3,5-辛二烯-2-酮 C8H12O − 0.36±0.97 0.10±0.25 22.67 (3E,5E)-辛-3,5-二烯-2-酮 C8H12O − 0.11±0.29 − 26.29 5-乙基-6-甲基庚-3-烯-2-酮 C10H18O 0.10±0.18 − − 40.00 大马士酮 C13H18O 0.11±0.15 − − 40.51 茉莉酮 C11H16O 1.04±0.25 3.50±2.46 5.31±1.21 41.45 α-紫罗酮 C13H20O 0.42±0.15 0.08±0.22 0.10±0.27 42.33 香叶基丙酮 C13H22O 0.20±0.29 0.84±1.60 0.24±0.64 43.31 β-紫罗酮 C13H20O 1.39±0.49 1.65±0.87 1.90±0.69 酯 6.50 甲酸己酯 C7H14O2 0.03±0.07 0.13±0.33 − 23.06 顺-3-己烯基丁酯 C10H18O2 − 0.65±1.18 − 28.55 苯乙酸甲酯 C9H10O2 − 0.05±0.13 − 29.24 乙酸松油酯 C12H20O2 0.05±0.14 − 0.11±0.28 29.40 水杨酸甲酯 C8H8O3 4.15±2.80 0.80±0.76 2.04±1.24 29.60 乙酰水杨酸甲酯 C10H10O4 1.25±1.31 0.45±0.8 0.36±0.62 34.64 丁二酸二甲酯 C6H10O4 0.00±0.01 − − 36.50 α-甲基-1H-茚-1-甲醇乙酸酯 C13H14O2 0.02±0.05 0.20±0.54 − 44.55 二氢猕猴桃内酯 C11H16O2 0.59±0.29 0.80±1.21 0.29±0.38 50.48 水杨酸辛酯 C15H22O3 0.04±0.11 0.07±0.19 0.12±0.32 51.42 邻苯二甲酸二异丁酯 C16H22O4 0.12±0.18 0.80±1.40 0.36±0.37 烯 12.83 3,5,5-三甲基-1-己烯 C9H18 0.46±0.46 3.23±4.17 1.69±1.86 16.89 (+)-柠檬烯 C10H16 0.23±0.29 0.49±0.98 1.04±1.30 31.92 松油烯 C10H16 0.04±0.11 − − 酚 18.72 对氨基邻甲酚 C7H9NO 0.23±0.40 0.81±1.38 3.45±3.25 44.12 2,5-双(1,1-二甲基乙基)苯酚 C14H22O 0.10±0.18 − − 44.13 2,4-二叔丁基苯酚 C14H22O 0.15±0.19 − 0.08±0.21 44.51 5-戊基间苯二酚 C11H16O2 1.35±0.90 2.79±2.68 1.36±1.28 41.41 4-仲丁基-2,6-二叔丁基苯酚 C18H30O − − 0.27±0.72 脂肪烃 17.31 2,2,6-三甲基环庚烷 C9H16O 0.64±0.31 1.13±0.63 1.07±0.52 35.53 2-甲基十一烷 C12H26 0.08±0.21 − − 36.57 十三烷 C13H28 0.05±0.14 0.59±1.39 0.08±0.20 37.77 3-乙基-3-甲基庚烷 C10H22 0.02±0.05 0.11±0.30 − 芳香烃 22.22 2-丙酰呋喃 C7H8O2 0.10±0.11 − 0.01±0.04 23.06 呋喃 C4H4O 0.08±0.22 − − 23.11 5-甲基-2-乙酰基呋喃 C7H8O2 0.02±0.05 − − 35.67 2-甲基萘 C11H10 0.05±0.07 0.04±0.11 0.03±0.09 40.93 1,6-二甲基奈 C12H12 − 0.30±0.79 0.02±0.06 40.95 1,2-二甲基萘 C12H12 0.03±0.07 0.05±0.14 − 其他 12.75 乙烯醚 C4H6O − 0.05±0.13 − 3.50 N-乙基吡咯 C6H9N − 0.78±2.06 0.62±1.27 6.49 1-甲基-1H-四唑 C2H4N4 0.00±0.01 − − 13.51 丙酸酐 C6H10O3 − 0.09±0.25 − 14.01 甲酰肼 CH4N2O 0.02±0.06 − − 18.47 2,6-二甲基-3-羟基吡啶2,6-二甲基-3-羟基吡啶 C7H9NO − − 0.86±2.26 18.99 二甲胺嗪 C6H9N3 0.14±0.36 − 0.56±1.48 25.45 N-乙基琥珀酰亚胺 C6H9NO2 0.47±0.26 − − 23.07 2H-Pyran-3(4H)-one, 6-ethenyldihydro-2,2,6-trimethyl- C10H16O2 1.74±2.03 − 0.56±1.47 35.20 壬酸 C9H18O2 0.04±0.11 − − 35.53 Dodecane, 4,6-dimethyl- C14H30 0.12±0.22 − 0.11±0.29 35.97 吲哚 C8H7N − − 2.35±2.29 37.75 2-乙基己酸酐 C16H30O3 0.01±0.02 − − 43.01 苊 C12H10 0.22±0.23 0.42±0.55 0.09±0.19 51.11 咖啡因 C8H10N4O2 0.18±0.25 0.41±0.54 0.70±1.42 注:“−”为未检测出成分。 在凤冈锌硒茶中,醇类化合物的种类和相对含量均最高,常带有特殊的花香和果香[12-13],对凤冈锌硒茶香气形成有着关键作用。在原样中共有峰的相对含量由高到低的顺序是:芳樟醇及其氧化物>香叶醇>2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇>苯乙醇>苯甲醇>1-辛烯-3-醇>苏合香醇>反-3-己烯醇>雪松醇>α-松油醇。芳樟醇及其氧化物在加工过程前后的相对含量均最大。这与石亚丽等[14]研究结果有所区别,其文献研究表明香叶醇含量远大于芳樟醇的含量。从原样到成品过程中,具有花香气味的芳樟醇[15]及其氧化物呈现减少趋势,二氢芳樟醇逐渐增多,香叶醇相对含量在5.45%~6.80%之间。可能是由于芳樟醇被氧化而生成了芳樟醇的氧化物或者其他醇类物质,使得醇种类或含量发生明显变化,同时在酶的作用下水解,使得花果香的萜烯醇类游离出来,这可能是凤冈锌硒茶的栗香形成的基础。在凤冈锌硒茶的摊青、杀青等加工过程中,由于茶叶的失水和缓慢氧化,糖苷类水解[16]产生的苯甲醇等主要的挥发性物质增加,使得凤冈锌硒茶香气形成。而正己醇、6-乙烯基-2,2,6-三甲基-四氢吡喃-3-醇、橙花醇、(E,Z)-金合欢醇仅存在于原样中,在加工过程和成品中均未被检测出;环丁基甲醇,1-辛炔-3-醇仅在成品中检测到。
在醛类化合物中,含有苦杏仁味的苯甲醛相对含量较高,相对含量在4.83~6.05%之间。因在40~50 ℃条件下完成干燥,使得低沸点的固脂肪族醇醛类物质如苯甲醛等在此温度下相对含量较高。具有果香、清香的β-环柠檬醛[17]在加工前后均被检测到,且在成品中含量最高,可能由于醇类物质不稳定,通过氧化和酶解后形成醛,使其相对含量发生了改变。通过高温产生的美拉德反应使具有花香味的苯乙醛相对含量有所增加[18],为凤冈锌硒茶香气的主要特征成分。巴豆醛仅仅存在于加工过程;2-己烯醛、庚醛、2-羟基-4-甲基苯甲醛仅在样品中被检测出。
酮类化合物使茶叶具有清甜香或甜香[19]。其中茉莉酮、α-紫罗酮、β-紫罗酮、甲基庚烯酮、苯乙酮、香叶基丙酮在原样、半成品、成品中均被检测到。茉莉酮、β-紫罗酮在检测中呈现逐渐增加的趋势,香叶基丙酮、甲基庚烯酮在检测中呈现先增加后减少的趋势;α-紫罗酮呈现逐渐减少的趋势。茉莉酮有果香、花香和茉莉花的气味[20],在成品中相对含量达到最高。杀青是凤冈锌硒茶加工过程中的关键工序,这一过程使得茶叶中类胡萝卜素香气前体和脂肪酸类香气前体降解,导致香叶基丙酮、茉莉酮等芳香物质相对含量增加;同时因杀青而产生的酶促和热裂解作用,使凤冈锌硒茶产生了对茶叶香气起关键作用的类胡萝卜衍生物-紫罗酮系化合物[21],主要是具有花果香的β-紫罗酮,这些过程共同促使了凤冈锌硒茶香气的形成,这与YANG等[22]研究类似。双乙烯酮、1,1,1-三氟-2-丁酮、5-乙基-6-甲基庚-3-烯-2-酮、大马士酮仅在原样中被检测到。(3E,5E)-辛-3,5-二烯-2-酮仅在半成品中被检测出。
在酯类化合物中,水杨酸甲酯,乙酰水杨酸甲酯,二氢猕猴桃内酯,水杨酸辛酯,邻苯二甲酸二异丁酯在加工前后均被检测出。具有清香、花果香的二氢猕猴桃内酯[23]呈现先增加后减少的趋势,对凤冈锌硒茶香气的形成具有重要作用。具有清香味的水杨酸甲酯[24-25]在酯类化合物中的相对含量相对较高,在0.8%~4.15%之间。原样中具有青草气息的水杨酸甲酯含量较高,使得原样中青草气明显。通过杀青等工艺后,使茶叶减少青草气成分从而显现茶香[26]。丁二酸二甲酯仅在原样中检测出;顺-3-己烯基丁酯、苯乙酸甲酯仅在半成品中检测出。
在烯类和酚类化合物中,3,5,5-三甲基-1-己烯、(+)-柠檬烯、对氨基邻甲酚在原料、半成品、成品中均被检测出。具有新鲜橙子与柠檬香气的(+)-柠檬烯[24],对凤冈锌硒茶香气的形成有一定的贡献。对氨基邻甲酚在加工过程中呈现逐渐增多的趋势;3,5,5-三甲基-1-己烯、5-戊基间苯二酚在检测中呈现先增加后减少的趋势。松油烯、2,5-双(1,1-二甲基乙基)苯酚仅在原样中被检测出。
在脂肪烃、芳香烃类化合物中,2,2,6-三甲基环庚烷、十三烷、2-甲基萘在加工过程中均被检测出。2-甲基萘可能作为某些化合物的载体而不参与凤冈锌硒茶香气的形成。由于脂肪烃、芳香烃类化合物的相对含量占比较小,可能对凤冈锌硒茶气味的贡献不大。
在其他类化合物中,苊和咖啡因在加工过程中均被检测出。成品中吲哚的相对含量为2.35%,是绿茶香气品质形成的重要化合物,这与WANG等[27]的研究结果一致。当其浓度较低时会呈现出花香等令人愉悦的味道[28];当浓度较高时,会表现出刺激气味。在杀青、做形等工序中,产生了美拉德、机械损伤胁迫等作用,形成具有焦香、甜香、花香等气味的吲哚类、吡嗪类、吡咯类及呋喃类等[29],对凤冈锌硒茶气味具有重要作用。1-甲基-1H-四唑、甲酰肼、N-乙基琥珀酰亚胺、壬酸、2-乙基己酸酐仅在原样中被检测出;乙烯醚、丙酸酐仅在半成品中被检测出。
2.3 主成分分析和OPLS-DA分析
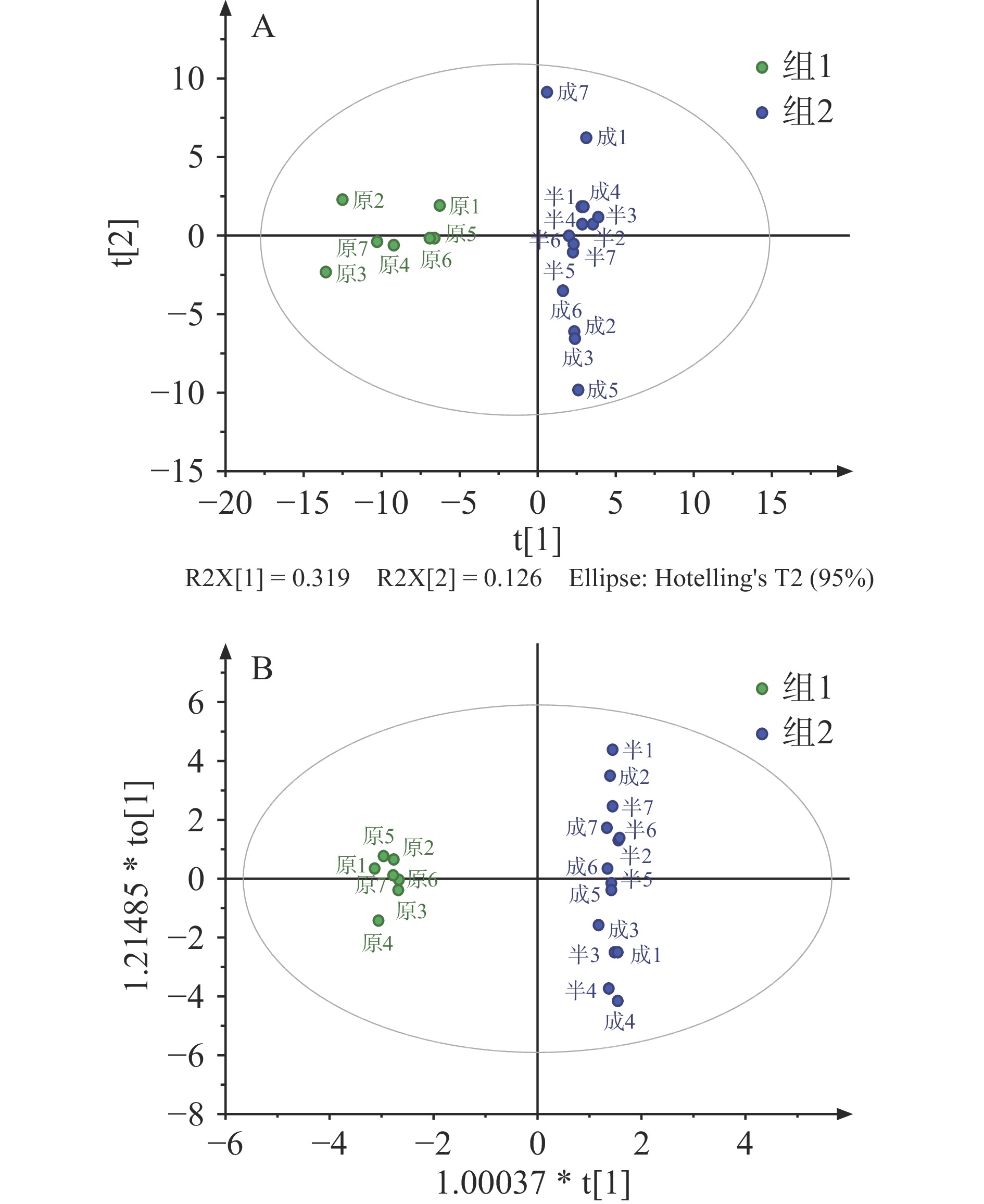
凤冈锌硒茶在加工过程中挥发性成分的变化在得分散点图上实现了较好的区分,其中,原样均分布在横轴负半轴(第二、三象限),聚集程度较高,归为1类;而半成品和成品分布在横轴的正半轴(第一、四象限),半成品和成品之间差异不明显,聚为1类,见图3A。由此体现了凤冈锌硒茶在加工前后香气存在一定的差异性。
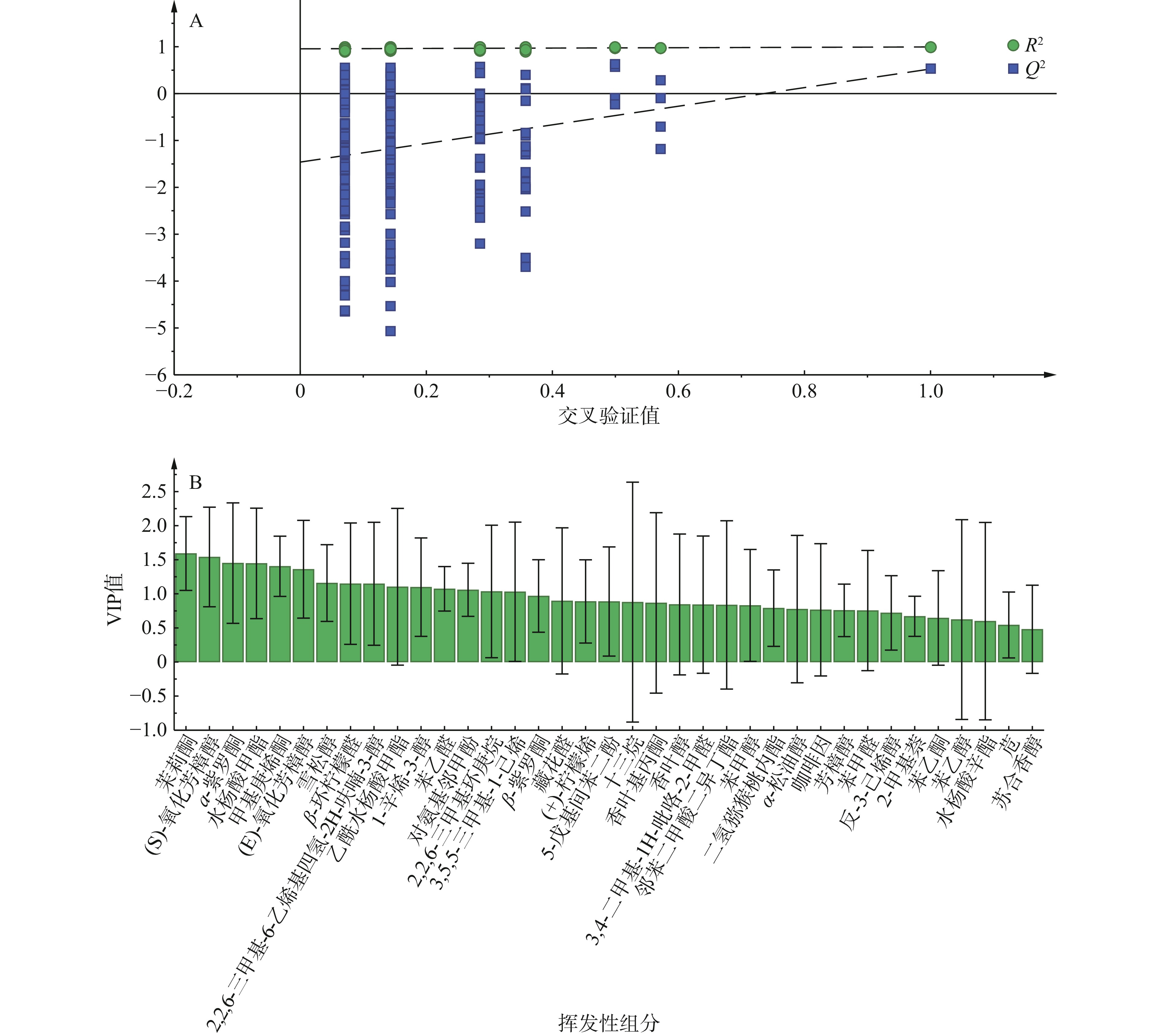
通过OPLS-DA筛选凤冈锌硒茶的标志性挥发性组分[30]。以37个共有挥发性组分作为因变量,加工前后的类别作为自变量,对凤冈锌硒茶加工过程进行OPLS-DA分析,见图3B,所有样本均在95%置信区间内,原样分布在左侧象限,半成品和成品分布在右侧象限,能对加工前后的凤冈锌硒茶样品进行有效区分。进一步,采用200次响应的置换检验证模型是否过拟合,其拟合参数为R2X=0.721,R2Y=0.996,Q2=0.526,其中Q2>0.5,R2Y-R2X<0.3,代表该模型较可靠且稳定性良好[31],可用于加工过程中凤冈锌硒茶的判别分析。如图4A所示,Q2的回归线截距为负值,且所有的R2值和Q2值均是模拟值低于原始值,上述结果说明该模型稳定性较好,未出现过拟合现象,具有较好的预测能力,该结果可用于茶叶香气的加工过前后的鉴别分析。
变量重要性因子(VIP)表示挥发性成分对样本的贡献度,从而筛选出重要的特征物质,一般认为VIP>1表示该变量具有重要作用[32],且VIP值越大,说明该变量在加工前后样本间的差异越显著。由图4B、表2可以看出,VIP值大于1的挥发性成分共有15种,分别为茉莉酮、(S)-氧化芳樟醇、α-紫罗酮、水杨酸甲酯、甲基庚烯酮、(E)-氧化芳樟醇、雪松醇、β-环柠檬醛、2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇、乙酰水杨酸甲酯、1-辛烯-3-醇、苯乙醛、对氨基邻甲酚、2,2,6-三甲基环庚烷和3,5,5-三甲基-1-己烯等,上述15种VIP大于1的标志差异性挥发性成分,可作为区分加工过程中凤冈锌硒茶的标志物。
表 2 变量重要性因子(VIP值)Table 2. Variable importance for the projection (VIP values)化合物名称 VIP值 Y误差 化合物名称 VIP值 Y误差 茉莉酮 1.59 0.54 十三烷 0.88 1.76 (S)-氧化芳樟醇 1.54 0.73 香叶基丙酮 0.87 1.32 a-紫罗酮 1.45 0.88 香叶醇 0.84 1.03 水杨酸甲酯 1.45 0.81 3,4-二甲基-1H-
吡咯-2-甲醛0.84 1.01 甲基庚烯酮 1.40 0.44 邻苯二甲酸二异丁酯 0.84 1.23 (E)-氧化芳樟醇 1.36 0.72 苯甲醇 0.83 0.82 雪松醇 1.16 0.56 二氢猕猴桃内酯 0.79 0.56 β-环柠檬醛 1.15 0.89 α-松油醇 0.78 1.08 2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇 1.15 0.90 咖啡因 0.77 0.97 乙酰水杨酸甲酯 1.10 1.15 芳樟醇 0.76 0.39 1-辛烯-3-醇 1.10 0.72 苯甲醛 0.75 0.88 苯乙醛 1.07 0.33 反-3-己烯醇 0.72 0.55 对氨基邻甲酚 1.06 0.39 2-甲基萘 0.67 0.29 2,2,6-三甲基环庚烷 1.03 0.97 苯乙酮 0.65 0.69 3,5,5-三甲基-1-己烯 1.03 1.02 苯乙醇 0.62 1.47 β-紫罗酮 0.97 0.53 水杨酸辛酯 0.60 1.45 藏花醛 0.90 1.07 苊 0.54 0.48 (+)-柠檬烯 0.89 0.61 苏合香醇 0.48 0.65 5-戊基间苯二酚 0.89 0.80 3. 结论
本研究采用HS-SPME-GC-MS技术,通过优化提取条件,对加工前后的凤冈锌硒茶的挥发性组分进行分析与归类,探究挥发性组分在加工过程中的变化规律。结果表明,醇类(22种)、酮类(13种)、酯类(11种)和醛类(12种)是构成凤冈锌硒茶香气的主要挥发性组分。在加工前后共检测出91种挥发性组分,其中共有挥发性化合物有37种,相对含量超过1%的共有13种。主成分分析表明,因加工过程中挥发性组分的不同,使得凤冈锌硒茶加工前后的差异较大,可将加工前分为一类,加工后归为一类。OPLS-DA分析表明具有贡献作用的挥发性成分共有15种,其中关键香气(VIP>1.5)为茉莉酮、(S)-氧化芳樟醇。这15种标志差异性挥发性组分,可作为区分加工过程种凤冈锌硒茶的标志物。凤冈锌硒茶品质除了受原料、加工工艺等影响外,茶树的生长环境、贮藏条件等也会对其品质产生影响,目前有关凤冈锌硒茶品质与生长环境关系、贮藏条件的研究较少,还需进一步研究。本研究检测指标和样本数量有限,不一定完全适用于凤冈锌硒茶的鉴别分析,因而需要进一步收集凤冈锌硒茶的指标信息进行综合性评价,为凤冈锌硒茶的生产、质量控制提供理论依据。
-
表 1 凤冈锌硒茶中挥发性成分组成及其相对含量(%)
Table 1 Composition and relative content of volatile components in the Fenggang zinc-selenium tea (%)
种类 保留时间(min) 化合物名称 分子式 原样 半成品 成品 醇 5.36 反-3-己烯醇 C6H12O 0.53±0.38 0.89±0.91 0.10±0.19 5.56 3-己烯-1-醇 C6H12O 0.15±0.39 − 0.11±0.30 6.50 正己醇 C6H14O 0.03±0.07 − − 13.16 环丁基甲醇 C5H10O − − 0.33±0.88 13.35 1-辛烯-3-醇 C8H16O 1.87±0.79 7.22±6.40 3.79±2.81 17.49 苯甲醇 C7H8O 2.52±0.81 2.38±1.47 1.75±0.51 20.34 (2Z)-2-辛烯-1-醇 C8H16O − 0.85±2.25 − 20.44 (E)-氧化芳樟醇 C10H18O2 8.58±1.89 5.58±1.01 6.01±3.18 20.67 1-辛炔-3-醇 C8H14O − − 0.21±0.55 20.69 正辛醇 C8H18O 0.11±0.20 0.34±0.89 − 21.68 (S)-氧化芳樟醇 C10H18O2 21.36±4.58 12.10±3.15 12.58±8.01 22.72 芳樟醇 C10H18O 16.07±5.90 15.81±6.95 14.67±3.34 23.08 二氢芳樟醇 C10H16O − 1.83±2.53 3.59±2.23 23.50 苯乙醇 C8H10O 5.30±1.30 5.80±0.90 7.91±7.84 24.04 苏合香醇 C8H10O 0.60±0.34 0.21±0.41 0.80±1.41 27.81 6-乙烯基-2,2,6-三甲基-四氢吡喃-3-醇 C10H18O2 1.06±0.75 − − 28.19 2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇 C10H18O2 5.48±0.93 4.51±1.43 4.18±1.00 29.25 α-松油醇 C10H18O 0.11±0.19 0.42±0.62 0.10±0.26 33.57 橙花醇 C10H18O 0.08±0.22 − − 34.08 香叶醇 C10H18O 6.80±3.61 5.45±2.35 5.80±2.06 42.31 (E,Z)-金合欢醇 C13H22O 0.05±0.14 − − 46.58 雪松醇 C15H26O 0.52±0.14 1.05±0.38 0.77±0.60 醛 5.00 2-己烯醛 C6H10O 1.13±0.53 − − 8.18 庚醛 C7H14O 0.19±0.14 − − 11.56 苯甲醛 C7H6O 5.37±1.74 4.83±3.19 6.05±2.71 18.11 苯乙醛 C8H8O 2.96±0.97 2.32±2.20 1.13±0.91 18.66 3,4-二甲基-1H-吡咯-2-甲醛 C7H9NO 0.07±0.19 2.70±3.82 0.18±0.48 20.70 丙烯醛 C3H4O 0.01±0.03 − 0.04±0.09 20.74 巴豆醛 C4H6O − 0.03±0.07 − 29.25 2-羟基-4-甲基苯甲醛 C8H8O2 0.22±0.59 − − 29.83 藏花醛 C10H14O 1.03±0.49 0.68±0.55 0.88±0.40 30.59 癸醛 C10H20O 0.23±0.60 − 0.37±0.97 31.33 β-环柠檬醛 C10H16O 0.90±0.22 1.28±0.42 1.29±0.63 34.75 2,4,6-三甲基苯甲醛 C10H12O 0.18±0.17 − 0.03±0.07 酮 6.23 双乙烯酮 C4H4O2 0.01±0.03 − − 6.64 2-庚酮 C7H14O 0.02±0.04 − 0.05±0.13 12.96 1,1,1-三氟-2-丁酮 C4H5F3O 0.03±0.08 − − 14.03 甲基庚烯酮 C8H14O 0.33±0.20 1.64±1.13 1.35±0.90 20.09 苯乙酮 C8H8O 0.03±0.06 0.01±0.02 0.07±0.18 21.63 3,5-辛二烯-2-酮 C8H12O − 0.36±0.97 0.10±0.25 22.67 (3E,5E)-辛-3,5-二烯-2-酮 C8H12O − 0.11±0.29 − 26.29 5-乙基-6-甲基庚-3-烯-2-酮 C10H18O 0.10±0.18 − − 40.00 大马士酮 C13H18O 0.11±0.15 − − 40.51 茉莉酮 C11H16O 1.04±0.25 3.50±2.46 5.31±1.21 41.45 α-紫罗酮 C13H20O 0.42±0.15 0.08±0.22 0.10±0.27 42.33 香叶基丙酮 C13H22O 0.20±0.29 0.84±1.60 0.24±0.64 43.31 β-紫罗酮 C13H20O 1.39±0.49 1.65±0.87 1.90±0.69 酯 6.50 甲酸己酯 C7H14O2 0.03±0.07 0.13±0.33 − 23.06 顺-3-己烯基丁酯 C10H18O2 − 0.65±1.18 − 28.55 苯乙酸甲酯 C9H10O2 − 0.05±0.13 − 29.24 乙酸松油酯 C12H20O2 0.05±0.14 − 0.11±0.28 29.40 水杨酸甲酯 C8H8O3 4.15±2.80 0.80±0.76 2.04±1.24 29.60 乙酰水杨酸甲酯 C10H10O4 1.25±1.31 0.45±0.8 0.36±0.62 34.64 丁二酸二甲酯 C6H10O4 0.00±0.01 − − 36.50 α-甲基-1H-茚-1-甲醇乙酸酯 C13H14O2 0.02±0.05 0.20±0.54 − 44.55 二氢猕猴桃内酯 C11H16O2 0.59±0.29 0.80±1.21 0.29±0.38 50.48 水杨酸辛酯 C15H22O3 0.04±0.11 0.07±0.19 0.12±0.32 51.42 邻苯二甲酸二异丁酯 C16H22O4 0.12±0.18 0.80±1.40 0.36±0.37 烯 12.83 3,5,5-三甲基-1-己烯 C9H18 0.46±0.46 3.23±4.17 1.69±1.86 16.89 (+)-柠檬烯 C10H16 0.23±0.29 0.49±0.98 1.04±1.30 31.92 松油烯 C10H16 0.04±0.11 − − 酚 18.72 对氨基邻甲酚 C7H9NO 0.23±0.40 0.81±1.38 3.45±3.25 44.12 2,5-双(1,1-二甲基乙基)苯酚 C14H22O 0.10±0.18 − − 44.13 2,4-二叔丁基苯酚 C14H22O 0.15±0.19 − 0.08±0.21 44.51 5-戊基间苯二酚 C11H16O2 1.35±0.90 2.79±2.68 1.36±1.28 41.41 4-仲丁基-2,6-二叔丁基苯酚 C18H30O − − 0.27±0.72 脂肪烃 17.31 2,2,6-三甲基环庚烷 C9H16O 0.64±0.31 1.13±0.63 1.07±0.52 35.53 2-甲基十一烷 C12H26 0.08±0.21 − − 36.57 十三烷 C13H28 0.05±0.14 0.59±1.39 0.08±0.20 37.77 3-乙基-3-甲基庚烷 C10H22 0.02±0.05 0.11±0.30 − 芳香烃 22.22 2-丙酰呋喃 C7H8O2 0.10±0.11 − 0.01±0.04 23.06 呋喃 C4H4O 0.08±0.22 − − 23.11 5-甲基-2-乙酰基呋喃 C7H8O2 0.02±0.05 − − 35.67 2-甲基萘 C11H10 0.05±0.07 0.04±0.11 0.03±0.09 40.93 1,6-二甲基奈 C12H12 − 0.30±0.79 0.02±0.06 40.95 1,2-二甲基萘 C12H12 0.03±0.07 0.05±0.14 − 其他 12.75 乙烯醚 C4H6O − 0.05±0.13 − 3.50 N-乙基吡咯 C6H9N − 0.78±2.06 0.62±1.27 6.49 1-甲基-1H-四唑 C2H4N4 0.00±0.01 − − 13.51 丙酸酐 C6H10O3 − 0.09±0.25 − 14.01 甲酰肼 CH4N2O 0.02±0.06 − − 18.47 2,6-二甲基-3-羟基吡啶2,6-二甲基-3-羟基吡啶 C7H9NO − − 0.86±2.26 18.99 二甲胺嗪 C6H9N3 0.14±0.36 − 0.56±1.48 25.45 N-乙基琥珀酰亚胺 C6H9NO2 0.47±0.26 − − 23.07 2H-Pyran-3(4H)-one, 6-ethenyldihydro-2,2,6-trimethyl- C10H16O2 1.74±2.03 − 0.56±1.47 35.20 壬酸 C9H18O2 0.04±0.11 − − 35.53 Dodecane, 4,6-dimethyl- C14H30 0.12±0.22 − 0.11±0.29 35.97 吲哚 C8H7N − − 2.35±2.29 37.75 2-乙基己酸酐 C16H30O3 0.01±0.02 − − 43.01 苊 C12H10 0.22±0.23 0.42±0.55 0.09±0.19 51.11 咖啡因 C8H10N4O2 0.18±0.25 0.41±0.54 0.70±1.42 注:“−”为未检测出成分。 表 2 变量重要性因子(VIP值)
Table 2 Variable importance for the projection (VIP values)
化合物名称 VIP值 Y误差 化合物名称 VIP值 Y误差 茉莉酮 1.59 0.54 十三烷 0.88 1.76 (S)-氧化芳樟醇 1.54 0.73 香叶基丙酮 0.87 1.32 a-紫罗酮 1.45 0.88 香叶醇 0.84 1.03 水杨酸甲酯 1.45 0.81 3,4-二甲基-1H-
吡咯-2-甲醛0.84 1.01 甲基庚烯酮 1.40 0.44 邻苯二甲酸二异丁酯 0.84 1.23 (E)-氧化芳樟醇 1.36 0.72 苯甲醇 0.83 0.82 雪松醇 1.16 0.56 二氢猕猴桃内酯 0.79 0.56 β-环柠檬醛 1.15 0.89 α-松油醇 0.78 1.08 2,2,6-三甲基-6-乙烯基四氢-2H-呋喃-3-醇 1.15 0.90 咖啡因 0.77 0.97 乙酰水杨酸甲酯 1.10 1.15 芳樟醇 0.76 0.39 1-辛烯-3-醇 1.10 0.72 苯甲醛 0.75 0.88 苯乙醛 1.07 0.33 反-3-己烯醇 0.72 0.55 对氨基邻甲酚 1.06 0.39 2-甲基萘 0.67 0.29 2,2,6-三甲基环庚烷 1.03 0.97 苯乙酮 0.65 0.69 3,5,5-三甲基-1-己烯 1.03 1.02 苯乙醇 0.62 1.47 β-紫罗酮 0.97 0.53 水杨酸辛酯 0.60 1.45 藏花醛 0.90 1.07 苊 0.54 0.48 (+)-柠檬烯 0.89 0.61 苏合香醇 0.48 0.65 5-戊基间苯二酚 0.89 0.80 -
[1] 张鹏云, 李蓉, 李浩洋, 等. 顶空固相微萃取-气相色谱串联质谱结合保留指数分析杭白菊挥发性成分[J]. 食品与发酵工业,2019,45(1):202−209. [ZHANG P Y, LI R, LI H Y, et al. Analysis of voltatile compounds in Chrsanthemum moriflium Ramat by HS-SPME-GC MS/MS combing retenyion index[J]. Food and Fermentation Industries,2019,45(1):202−209. ZHANG P Y, LI R, LI H Y, et al. Analysis of voltatile compounds in Chrsanthemum moriflium Ramat by HS-SPME-GC MS/MS combing retenyion index[J]. Food and Fermentation Industries, 2019, 45(1): 202-209.
[2] 徐飞, 李俄艳, 初众, 等. 顶空固相微萃取-气质联用分析香荚兰浸膏风味组分的条件优化[J]. 热带作物学报,2019,40(2):348−358. [XU F, LI E Y, CHU Z, et al. Optimization of flavor components of Vanilla concentrate by headspace solid phase microextraction-GC mass spectrometry analysis[J]. Chinese Journal of Tropical Crops,2019,40(2):348−358. XU F, LI E Y, CHU Z, et al. Optimization of flavor components of Vanilla concentrate by headspace solid phase microextraction-GC mass spectrometry analysis[J]. Chinese Journal of Tropical Crops, 2019, 40(2): 348-358.
[3] YU J, YANG J, LI M, et al. Protective effects of Chinese Fenggang zinc selenium tea on metabolic syndrome in high-sucrose-high-fat diet-induced obese rats[J]. Scientific Report,2018,8(1):3528. doi: 10.1038/s41598-018-21913-w
[4] 王晓宁, 赵茹茹, 张建永. 基于代谢组学技术研究凤冈锌硒茶对正常大鼠机体代谢调节规律[J]. 食品工业科技,2020,41(6):99−105. [WANG X N, ZHAO R R, ZHANG J Y. Global metabolic regulation of Fenggang zinc-selenium tea in normal rat based on metabolomics technology[J]. Science and Technology of Food Industry,2020,41(6):99−105. WANG X N, ZHAO R R, ZHANG J Y. Global metabolic regulation of Fenggang zinc-selenium tea in normal rat based on metabolomics technology[J]. Science and Technology of Food Industry, 2020, 41(6): 99-105.
[5] 罗冬兰, 邵勇, 巴良杰, 等. 贵州四种名优茶叶的电子鼻鉴别与香气成分分析[J]. 保鲜与加工,2020,20(3):183−190. [LUO D L, SHAO Y, BA L J, et al. Electronic nose identification and analysis of aroma components of four famous and excellent teas in Guizhou[J]. Storage and Process,2020,20(3):183−190. LUO D L, SHAO Y, BA L J, et al. Electronic nose identification and analysis of aroma components of four famous and excellent teas in Guizhou[J]. Storage and Process, 2020, 20(3): 183-190.
[6] 杨纯, 颜鸿飞, 吕小园, 等. 元素指纹图谱用于安化黑茶的原产地判别[J]. 食品科学,2020,41(16):286−291. [YANG C, YAN H F, LÜ X Y, et al. Geographical origin discrimination of Anhua dark tea by elemental fingerprint[J]. Food Science,2020,41(16):286−291. YANG C, YAN H F, LU X Y, et al. Geographical origin discrimination of Anhua dark tea by elemental fingerprint[J]. Food Science, 2020, 41(16): 286-291.
[7] 林家正, 涂政, 陈琳, 等. 红光萎凋对茶叶挥发性成分及其成品红茶品质的影响[J]. 茶叶科学,2021,41(3):393−405. [LIN J Z, TU Z, CHEN L, et al. The effect of red light withering on the volatile components of leaves and quality of blank tea product[J]. Journal of Tea Science,2021,41(3):393−405. LIN J Z, TU Z, CHEN L, et al. The effect of red light withering on the volatile components of leaves and quality of blank tea product[J]. Journal of Tea Science, 2021, 41(3): 393-405.
[8] 蒋宾, 鄢远珍, 刘琨毅, 等. 云南和福建白茶差异比较研究[J]. 西南大学学报(自然科学版),2021,43(4):62−72. [JIANG B, YAN Y Z, LIU K Y, et al. Comparison of the difference between Yunnan and Fujian white tea[J]. Journal of Southwest University(Natural Science Edition),2021,43(4):62−72. JIANG B, YAN Y Z, LIU K Y, et al. Comparison of the difference between Yunnan and Fujian white tea[J]. Journal of Southwest University(Natural Science Edition), 2021, 43(04): 62-72.
[9] 李永迪, 黄燕, 刘杏益, 等. 同时蒸馏萃取法和顶空固相微萃取法提取茯砖茶挥发性成分的比较分析[J]. 食品工业科技,2018,39(24):246−252. [LI Y D, HUANG Y, LIU X Y, et al. Comparative analysis of volatile components in fu brick tea by simultaneous distillation and headspace solid-phase micro-extraction[J]. Science and Technology of Food Industry,2018,39(24):246−252. LI Y D, HUANG Y, LIU X Y, et al. Comparative analysis of volatile components in fu brick tea by simultaneous distillation and headspace solid-phase micro-extraction[J]. Science and Technology of Food Industry, 2018, 39(24): 246-252.
[10] ERDEM P, TAĞAÇ A A, BOZKURT S S, et al. Chitosan and dicationic ionic liquid intercalated clay-coated solid-phase microextraction fiber for determination of sixteen polycyclic aromatic hydrocarbons in coffee and tea samples[J]. Talanta,2021,235:122764. doi: 10.1016/j.talanta.2021.122764
[11] WANG M Q, MA W J, SHI J, et al. Characterization of the key aroma compounds in Longjing tea using stir bar sorptive extraction (SBSE) combined with gas chromatography-mass spectrometry (GC-MS), gas chromatography-olfactometry (GC-O), odor activity value (OAV), and aroma recombination[J]. Food Research International,2020,130:108908. doi: 10.1016/j.foodres.2019.108908
[12] 蒋容港, 黄燕, 金友兰, 等. 茯砖茶呈香挥发性物质及其来源[J]. 食品与生物技术学报,2021,40(9):101−111. [JIANG R G, HUANG Y, JIN Y L, et al. Study of aroma compounds and their source in fu brick tea[J]. Journal of Food Science and Biotechnology,2021,40(9):101−111. JIANG R G, HUANG Y, JIN Y L, et al. Study of aroma compounds and their source in fu brick tea[J]. Journal of Food Science and Biotechnology, 2021, 40(9): 101-111.
[13] YANG P, SONG H, LIN Y, et al. Differences of characteristic aroma compounds in Rougui tea leaves with different roasting temperatures analyzed by switchable GC-O-MS and GC×GC-O-MS and sensory evaluation[J]. Food & Function,2021,12(11):4797−4807.
[14] 石亚丽, 白艳, 马婉君, 等. 安吉白茶挥发性成分及关键呈香成分分析[J]. 食品科学,2022,43(20):261−268. [SHI Y L, BAI Y, MA W J, et al. Analysis of volatile components and key aroma-active compounds of Anjibaicha[J]. Food Science,2022,43(20):261−268. SHI Y L, BAI Y, MA W J, et al. Analysis of volatile components and key aroma-active compounds of Anjibaicha[J]. Food Science, 2022, 43(20): 261-268.
[15] YANG Y, RONG Y, LIU F, et al. Rapid characterization of the volatile profiles in Pu-erh tea by gas phase electronic nose and microchamber/thermal extractor combined with TD-GC-MS[J]. Journal of Food Science,2021,86(6):2358−2373. doi: 10.1111/1750-3841.15723
[16] LIU H, XU Y, WU J, et al. GC-IMS and olfactometry analysis on the tea aroma of Yingde black teas harvested in different seasons[J]. Food Research International (Ottawa, Ont.),2021,150(Pt A):110784.
[17] 苏丹, 黄刚骅, 李亚莉, 等. 紫娟(熟茶)人工发酵过程中挥发性香气组分特征分析[J]. 食品科学,2021,42(12):166−172. [SU D, HUANG G H, LI Y L, et al. Charateristic aroma components in ripe Zijuan tea during aritificial fermentation[J]. Food Science,2021,42(12):166−172. SU D, HUANG G H, LI Y L, et al. Charateristic aroma components in ripe zijuan tea during aritificial fermentation[J]. Food Science, 2021, 42(12): 166-172.
[18] ZHANG W, CAO J, LI Z, et al. HS-SPME and GC/MS volatile component analysis of Yinghong No. 9 dark tea during the pile fermentation process[J]. Food Chemistry,2021,357:129654. doi: 10.1016/j.foodchem.2021.129654
[19] 马士成, 王梦琪, 刘春梅, 等. 六堡茶挥发性成分中关键香气成分分析[J]. 食品科学,2020,41(20):191−197. [MA S C, WNAG M Q, LIU C M, et al. Analysis of volatile composition and key aroma compounds of Liupao tea[J]. Food Science,2020,41(20):191−197. MA S C, WNAG M Q, LIU C M, et al. Analysis of volatile composition and key aroma compounds of Liupao tea[J]. Food Science, 2020, 41(20): 191-197.
[20] 崔继来, 周洁, 周倩倩, 等. 信阳毛尖茶品质成分分析[J]. 信阳师范学院学报(自然科学版),2022,35(2):259−268. [CUI J L, ZHOU J, ZHOU Q Q, et al. The quality compounds analysis of Xinyang Maojian tea[J]. Journal of Xinyang Normal University(Natural Science Edition),2022,35(2):259−268. CUI J L, ZHOU J, ZHOU Q Q, et al. The quality compounds analysis of Xinyang maojian tea[J]. Journal of Xinyang Normal University(Natural Science Edition), 2022, 35(2): 259-268.
[21] ZHU J, NIU Y, XIAO Z. Characterization of the key aroma compounds in Laoshan green teas by application of odour activity value (OAV), gas chromatography-mass spectrometry-olfactometry (GC-MS-O) and comprehensive two-dimensional gas chromatography mass spectrometry (GC×GC-qMS)[J]. Food Chemistry,2021,339:128136. doi: 10.1016/j.foodchem.2020.128136
[22] YANG Y Q, YIN H X, YUAN H B, et al. Characterization of the volatile components in green tea by IRAE-HS-SPME/GC-MS combined with multivariate analysis[J]. PLoS One,2018,13(3):e0193393. doi: 10.1371/journal.pone.0193393
[23] 欧阳珂, 张成, 廖雪利, 等. 基于感官组学分析玉米香型南川大茶树工夫红茶特征香气[J]. 茶叶科学,2022,42(3):397−408. [OUYANG K, ZHANG C, LIAO X L, et al. Characterization of the key aroma in corn-scented congou blank tea manufactured from Camellia nanchunaica by sensory omics techniques[J]. Journal of Tea Science,2022,42(3):397−408. OUYANG K, ZHANG C, LIAO X L, et al. Characterization of the key aroma in corn-scented congou blank tea manufactured from Camellia nanchunaica by sensory omics techniques[J]. Journal of Tea Science, 2022, 42(3): 397-408.
[24] 蔺志远, 施江, 谭俊峰, 等. 提香温度对绿茶(香茶)干燥效能及风味品质的影响[J]. 食品科学,2020,41(23):153−158. [LIN Z Y, SHI J, TAN J F, et al. Effect of drying temperature on drying efficiency, energy consumption and flavor quality of Xiangcha, a kind of green tea[J]. Food Science,2020,41(23):153−158. LIN Z Y, SHI J, TAN J F, et al. Effect of drying temperature on drying efficiency, energy consumption and flavor quality of xiangcha, a kind of green tea[J]. Food Science, 2020, 41(23): 153-158.
[25] GUO X, HO C T, WAN X, et al. Changes of volatile compounds and odor profiles in Wuyi rock tea during processing[J]. Food Chemistry,2021,341(Pt 1):128230.
[26] QI D, MIAO A, CAO J, et al. Study on the effects of rapid aging technology on the aroma quality of white tea using GC-MS combined with chemometrics: In comparison with natural aged and fresh white tea[J]. Food Chemistry,2018,265:189−199. doi: 10.1016/j.foodchem.2018.05.080
[27] WANG J, LI X, WU Y, et al. HS-SPME/GC-MS reveals the season effects on volatile compounds of green tea in high-latitude region[J]. Foods (Basel, Switzerland),2022,11(19):3016.
[28] 韦康, 王丽鸳, 余继忠, 等. 基于GC-MS对中茗66和龙井43的香气成分比较分析[J]. 食品与生物技术学报,2019,38(8):39−45. [WEI K, WANG L Y, YU J Z, et al. Comparative analysis of aroma components in tea cultivar Zhongming66 and Longjing43 by GC-MS[J]. Journal of Food Science and Biotechnology,2019,38(8):39−45. WEI K, WANG L Y, YU J Z, et al. Comparative analysis of aroma components in tea cultivar zhongming66 and longjing43 by GC-MS[J]. Journal of Food Science and Biotechnology, 2019, 38(8): 39-45.
[29] QI K, XU M, YIN H, et al. Online monitoring the key intermediates and volatile compounds evolved from green tea roasting by synchrotron radiation photoionization mass spectrometry[J]. Journal of the American Society for Mass Spectrometry,2021,32(6):1402−1411. doi: 10.1021/jasms.1c00012
[30] 韩沙沙, 郑伟, 南易, 等. 基于UHPLC-Q-TOF/MS-E技术分析武夷岩茶的化学成分[J]. 现代食品科技,2022,38(6):234−247,190. [HAN S S, ZHENG W, NAN Y, et al. Analysis of chemical components of Wuyi rock tea based on UHPLC-Q-TQF/MSE[J]. Modern Food Science and Technology,2022,38(6):234−247,190. HAN S S, ZHENG W, NAN Y, et al. Analysis of chemical components of Wuyi rock tea based on UHPLC-Q-TQF/MSE[J]. Modern Food Science and Technology, 2022, 38(6): 234-247, 190.
[31] 谢关华, 陆安霞, 欧阳珂, 等. GC-MS结合化学计量学用于探究六大茶类香气形成的差异[J]. 食品与发酵工业,2021,47(20):260−270. [XIE G H, LU A X, OUYANG K, et al. Analysis of the aroma formation in six categories of teas by GC-MS combined with chemometrics[J]. Food and Fermentation Industries,2021,47(20):260−270. XIE G H, LU A X, OUYANG K, et al. Analysis of the aroma formation in six categories of teas by GC-MS combined with chemometrics [J]. Food and Fermentation Industries, 2021, 47(20): 260-270.
[32] 岳翠男, 秦丹丹, 蔡海兰, 等. 赣北工夫红茶滋味特征及关键化合物分析[J]. 食品与发酵工业,2021,47(2):260−267. [YUE C N, QIN D D, CAI H L, et al. Taste characteristics and key compounds analysis of Congou black tea in northern Jiangxi Province[J]. Food and Fermentation Industries,2021,47(2):260−267. YUE C N, QIN D D, CAI H L, et al. Taste characteristics and key compounds analysis of Congou blacktea in northern Jiangxi province[J]. Food and Fermentation Industries, 2021, 47(2): 260-267.
-
期刊类型引用(1)
1. 郭智鑫,郝丹丹,卞建明,谢秋涛,孙亚丽,汪凯,李高阳,朱向荣. GC-MS结合化学计量学方法分析桂花净油分子蒸馏馏分的挥发性成分. 食品工业科技. 2024(07): 276-285 .  本站查看
本站查看
其他类型引用(1)





 下载:
下载:
 下载:
下载:



