Optimization of Purification of Tea Polyphenols with Macroporous Adsorption Resin and Research of Their Antioxidant Activity
-
摘要: 为优化大孔吸附树脂纯化茶多酚的最佳工艺条件,通过对比14种不同类型大孔吸附树脂的静态吸附-解吸特性,在筛选出适宜的树脂型号后,利用单因素与响应面试验确定最佳提纯工艺要求,并进一步考察了树脂的重复使用和再生次数。同时,以VC为对照采用体外实验考察纯化前、后茶多酚的抗氧化活性。结果表明,LX-8树脂对茶多酚的吸附-解吸效果最好,可重复使用5次、再生6次。其最佳纯化工艺条件:100 mL浓度为6.4 mg/mL,pH5.4的茶汤以1.0 mL/min流速上样至LX-8树脂后,经180 mL 76%乙醇溶液以1.0 mL/min流速解吸,在该条件下茶多酚的回收率为86.9%,纯度为74.6%。体外抗氧化活性试验结果表明,纯化后茶多酚的总抗氧化能力、清除DPPH·和·OH的能力均有显著性增加,且随着浓度的增大,其抗氧化能力增强,其总抗氧化能力(1 mg/mL)为80.59 U/mL,对DPPH·和·OH清除能力的IC50值分别为0.0326和0.4167 mg/mL。虽然低于VC的抗氧化活性,但均高于纯化前的茶多酚,说明通过该工艺,能够显著提高茶多酚的抗氧化活性,且当纯化后茶多酚浓度为1 mg/mL时,其DPPH·清除率已经接近VC的DPPH·清除率,本研究为茶多酚的工业化生产和开发利用提供理论参考。Abstract: To optimize the technical condition for purification of tea polyphenols with macroporous adsorption resin, the static adsorption and desorption performance of macroporous adsorption resin of fourteen types were compared to select the best type of resin. The optimal purification process conditions were determined by single factor and response surface experiments, and the reuse and regeneration times of the resin were further investigated. Meanwhile, the antioxidant activities of tea polyphenols before and after purification were investigated by in vitro experiments with VC as the control. The results showed that LX-8 resin had the best adsorption-desorption effect on tea polyphenols, which could be reused 5 times and regenerated 6 times. The optimum purification conditions were as below: The sample concentration of 6.4 mg/mL, the sample pH value of 5.4, the loading volume of 100 mL, the sample flow rate of 1.0 mL/min, ethanol concentration of 76% eluting agent volume of 180 mL, and desorption rate of 1.0 mL/min. Under these conditions, the recovery rate of tea polyphenols was 86.9% and the purity was 74.6%. In vitro antioxidant activity studies revealed that the total antioxidant capacity, DPPH· scavenging capacity and ·OH scavenging capacity of the purified tea polyphenols were significantly increased. And with the increase of polyphenol concentration, its antioxidant capacity enhanced. The total antioxidant capacity of the purified tea polyphenol (1 mg/mL) was 80.59 U/mL. The IC50 of the purified tea polyphenol on scavenging ability of DPPH· and ·OH were 0.0326 and 0.4167 mg/mL respectively. Although the antioxidant activity of pure extract was lower than that of VC, it was higher than that of crude extract, indicating that the antioxidant activity of tea polyphenols could be significantly improved by this process, and when the concentration of the purified tea polyphenol was 1 mg/mL, its DPPH· scavenging rate was close to that of VC. This research provided a theoretical reference for the industrial production and utilization of tea polyphenols.
-
Keywords:
- tea polyphenols /
- macroporous adsorption resin /
- purification /
- regeneration /
- antioxidant activity
-
茶是以山茶科植物茶树上的芽和叶为原料,经过一系列加工制成的产品[1],其活性成分有茶多酚、咖啡碱、黄酮类物质、氨基酸等[2]。研究发现,茶多酚作为绿茶中含量最高的有效成分,占茶叶干重的20%~30%[3],具有改善肠道结构[4]、抗糖化[5]、抑制病毒靶点[6]、抗氧化[7]等功效,但若想被广泛应用于医学领域,则需要对茶多酚进行纯化,因此,选择合适的纯化工艺,提高茶多酚的纯度是目前的研究方向。
目前提纯茶多酚的方法主要有离子沉淀法、膜过滤法、树脂吸附法、柱色谱法等[1],而树脂吸附法因其工艺简单、耗能少、绿色高效等优点被广泛应用。高海荣等[8]以粗老绿茶为原料,选择XDA-5大孔树脂提纯茶多酚,产品得率为10%,纯度为70%;吴婕等[9]采用HPD-826树脂分离纯化甜茶多酚,所得纯度约81.2%;曹雪文[10]选择DM-16X树脂进行吸附分离,动态洗脱率可达91.63%,茶多酚含量为76.57%。随着科技的不断发展,树脂吸附技术不断优化,但现存的主要问题是大孔吸附树脂前处理时间长、树脂用量大,价格昂贵,导致难以进行大规模生产。此外,在现有的研究中,工艺优化后对树脂的重复使用及再生效果的进一步探究很少。
本研究以绿茶为原料,采用树脂吸附法纯化茶多酚,通过单因素和响应面优化最佳纯化工艺,在此基础上考察树脂的重复使用和再生情况,以期提高茶多酚的纯度,为树脂吸附法纯化茶多酚的工业化生产提供理论依据。此外,进一步通过总抗氧化能力、清除DPPH·和·OH三种方式综合评价纯化前后茶多酚的抗氧化活性,为茶多酚的后续开发利用提供数据参考。
1. 材料与方法
1.1 材料与仪器
绿茶 眉茶,湖北五峰采花茶业科技园;甲醇、碳酸钠、乙醇、盐酸、氢氧化钠、硫酸亚铁、水杨酸 分析纯,西陇科学股份有限公司;2,2-二苯基-1-三硝基苯肼(DPPH) 分析纯,上海源叶生物科技有限公司;没食子酸标准品 色谱纯,上海源叶生物科技有限公司;30%过氧化氢溶液 分析纯,成都市科腾化学品有限公司;T-AOC检测试剂盒 生工生物工程(上海)股份有限公司;福林酚、抗坏血酸 分析纯,国药集团化学试剂有限公司;LX-B14、XDA-8G、SP207、LX-8 西安蓝晓科技新材料科技股份有限公司;HZW635、HZW636 上海华震科技有限公司;ADS-17、AB-8、X-5、D101、H103、HPD100、HPD450、D301 上海源叶生物科技有限公司。
XCS-HJSG-3定制型恒温搅拌三联水浴锅 陕西鑫昌实验仪器设备有限公司;ME204电子天平、FE28 pH计、HE53水分测定仪 瑞士梅特勒-托利多公司;5910R台式高速离心机 德国Eppendorf公司;754紫外可见分光光度计 上海光谱仪器有限公司;玻璃层析柱(30 mm×300 mm) 建湖县军明玻璃仪器厂;ZQZY-98CV振荡培养箱 上海知楚仪器有限公司。
1.2 实验方法
1.2.1 茶浸提液制备
参考文献[11],采用热水提取法进行制备,具体操作如下:茶叶粉碎过60目筛,称取一定质量的茶末,按1:20(g/mL)料液比在90 ℃下浸提35 min,三层纱布过滤,收集茶浸提液,待浸提液冷却至37 ℃后于5000 r/min条件下离心10 min,取上清液浓缩、干燥备用。
1.2.2 茶多酚含量测定
参考《GB/T 8313-2018 茶叶中茶多酚和儿茶素类含量的检测方法》进行测定。
茶多酚回收率的计算公式如下:
回收率(%)=纯化后茶多酚含量纯化前茶多酚含量×100 1.2.3 树脂的静态吸附-解吸性能比较
分别称取5.0 g经预处理[12]后的14种不同型号的大孔吸附树脂(LX-B14、XDA-8G、LX-8、SP207、D301、HZW635、HZW636、ADS-17、AB-8、X-5、D101、H103、HPD100、HPD450)置于250 mL三角瓶内,加入100 mL茶汤(6.92 mg/mL),于25 ℃、120 r/min的振荡培养箱中吸附24 h,滤纸过滤,检测吸附后溶液中茶多酚浓度(c1),计算树脂的吸附量和吸附率。将过滤的树脂用纯水冲洗后装入三角瓶中,各加入100 mL 80%乙醇,于25 ℃、120 r/min的振荡培养箱中解吸24 h,滤纸过滤,检测解吸后溶液中茶多酚浓度,计算树脂的解吸量和解吸率。计算公式如下[13]:
吸附量(mgg)=(c0−c1)×v0m×w 吸附率(%)=c0−c1c0×100 解吸量(mgg)=c2×v1m×w 解吸率(%)=c2c0−c1×100 式中:c0为原溶液中的茶多酚浓度,mg/mL;c1为吸附后溶液中茶多酚浓度,mg/mL;c2为解吸后溶液中茶多酚浓度,mg/mL;v0为茶汤体积,mL;v1为解吸液体积,mL;m为湿树脂质量,g;w为湿树脂干物质,%。
1.2.4 吸附等温曲线
配制浓度为1、2、3、4、5 mg/mL的茶多酚溶液25 mL,分别倒入150 mL三角瓶中,加入1 g处理后的 LX-8树脂,于25、35、45 ℃的振荡培养箱中,充分吸附后过滤,取滤液测其茶多酚浓度,计算各自的饱和吸附量,以饱和吸附浓度为横坐标(x),饱和吸附量为纵坐标(y),绘制三个温度下的吸附等温曲线,并以Langmuir和Freundlich方程进行拟合,描述LX-8树脂对茶多酚的吸附特性[14]。
1.2.5 吸附动力学曲线
准确称量5 g处理后的LX-8树脂置于250 mL三角瓶中,加入100 mL,3 mg/mL的茶多酚溶液,于25 ℃、120 r/min的振荡培养箱中进行静态吸附,每30 min测定一次溶液中的茶多酚浓度,计算其吸附量,画出吸附动力学曲线,并用拟一级和拟二级动力学模型进行拟合[15],阐明LX-8树脂对茶多酚的吸附机理。
1.2.6 单因素实验
1.2.6.1 茶汤pH对LX-8树脂吸附效果的影响
称取30 g经预处理后的LX-8树脂,装填进层析柱中,量取5份浓度为6.24 mg/mL的茶汤100 mL,分别调节其pH为3.37、4.37、5.37(原茶汤pH)、6.37、7.37,以1 mL/min流速上样,待充分吸附后,收集流出液,计算树脂的吸附率,考察不同茶汤pH对LX-8树脂吸附效果的影响。
1.2.6.2 茶汤浓度对LX-8树脂吸附效果的影响
称取30 g经预处理后的LX-8树脂,装填进层析柱中,分别制备5份上样液浓度为4.25、5.16、6.24、7.32、8.30 mg/mL的茶汤100 mL,调节其pH为5.37,以1 mL/min流速上样,待充分吸附后,收集流出液,计算树脂的吸附率,考察不同茶汤浓度对LX-8树脂吸附效果的影响。
1.2.6.3 泄露曲线的绘制
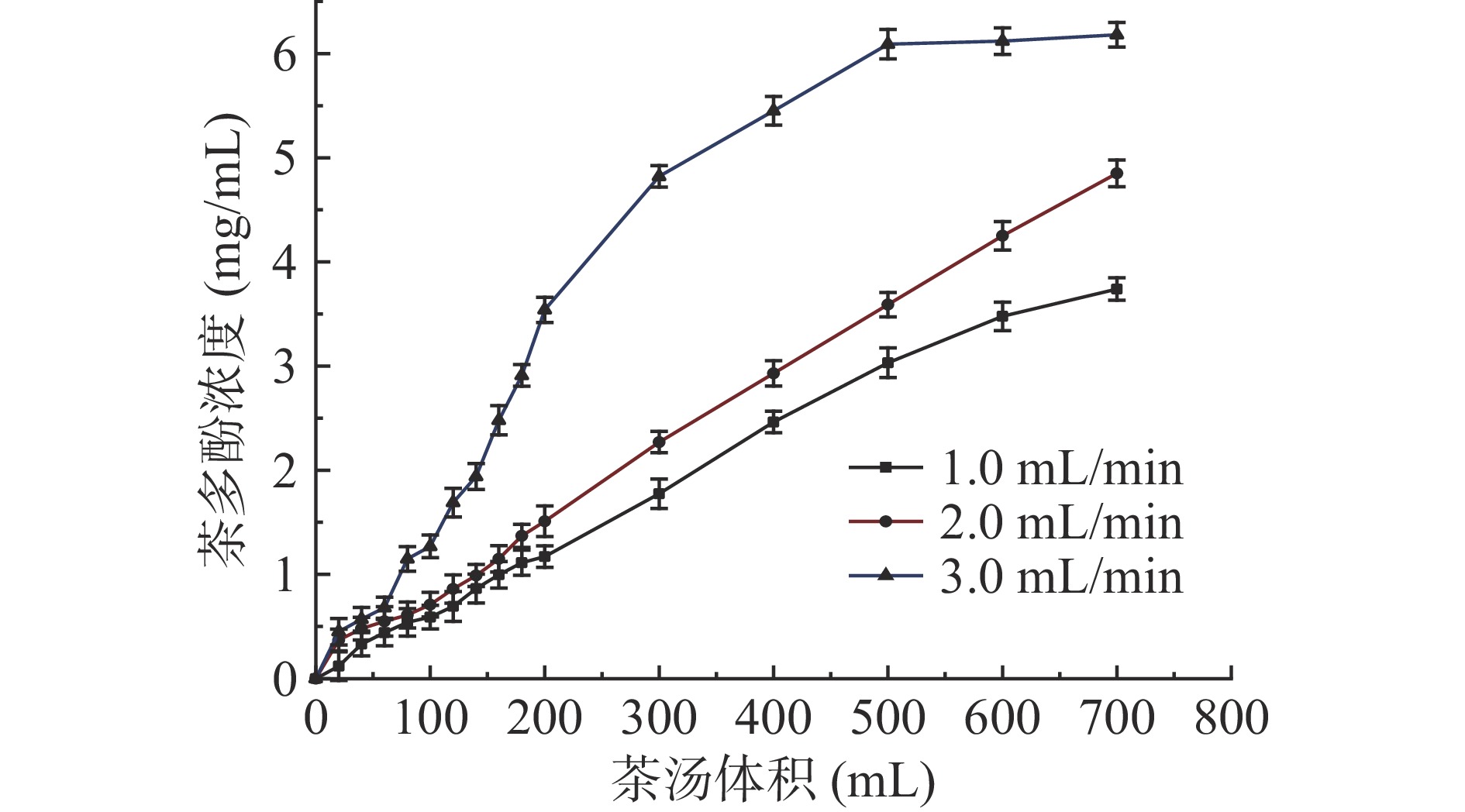
称取30 g经预处理后的LX-8树脂,装填进层析柱中,选择浓度为6.24 mg/mL、pH为5.37的茶汤,分别以1、2、3 mL/min不同流速上样,待充分吸附后,每20 mL收集一次流出液,测定其茶多酚浓度,以茶汤体积为横坐标(x),浓度为纵坐标(y),绘制不同流速下的泄露曲线。
1.2.6.4 乙醇浓度对LX-8树脂解吸效果的影响
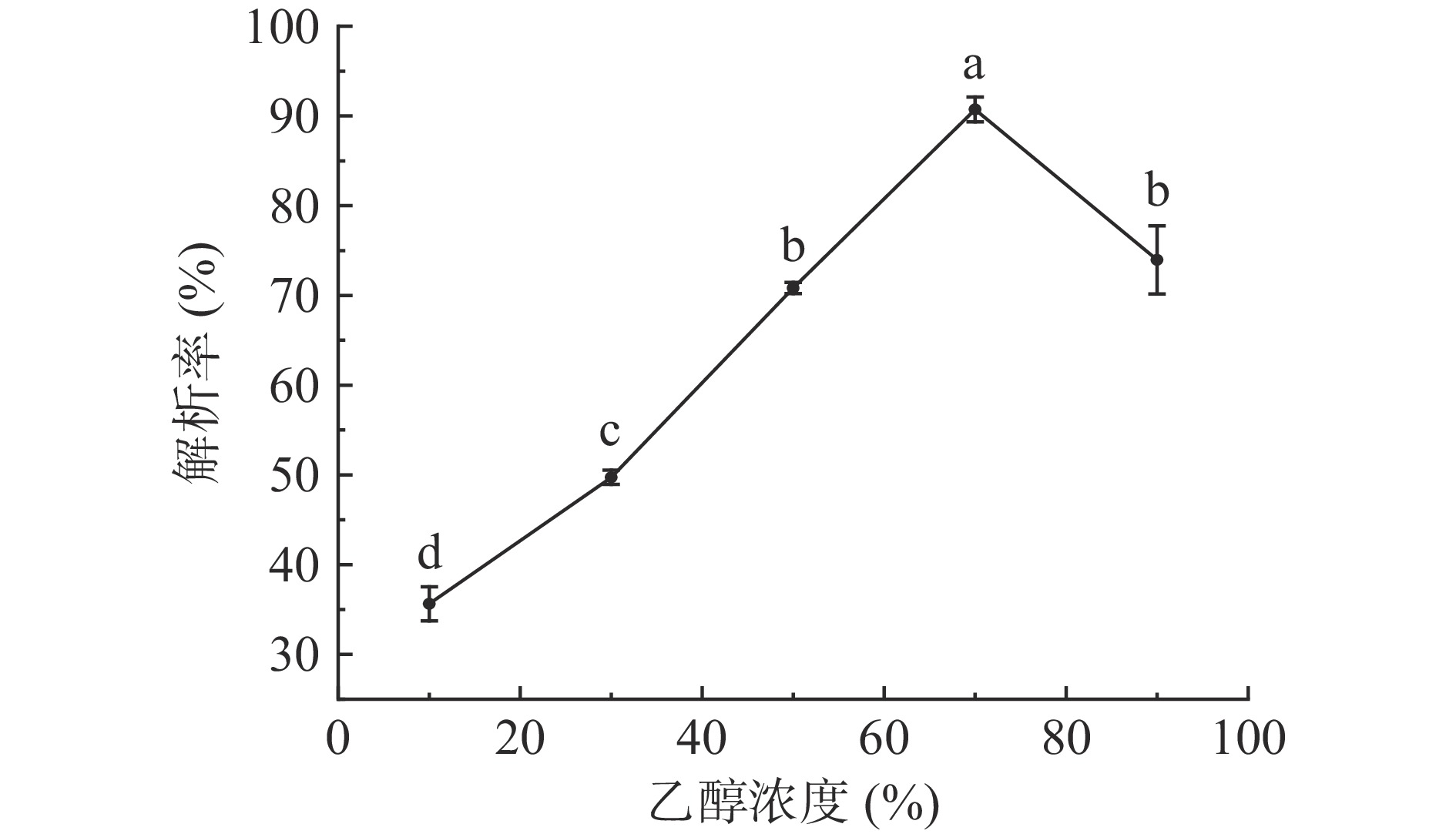
称取30 g经预处理后的LX-8树脂,装填进层析柱中,选择浓度为6.24 mg/mL、pH为5.37的茶汤100 mL,以1 mL/min流速上样,待充分吸附后,分别以10%、30%、50%、70%和90%乙醇溶液各100 mL解吸,解吸流速为 1 mL/min,收集流出液,计算树脂的解吸率,考察不同乙醇浓度对LX-8树脂解吸效果的影响。
1.2.6.5 解吸曲线的绘制
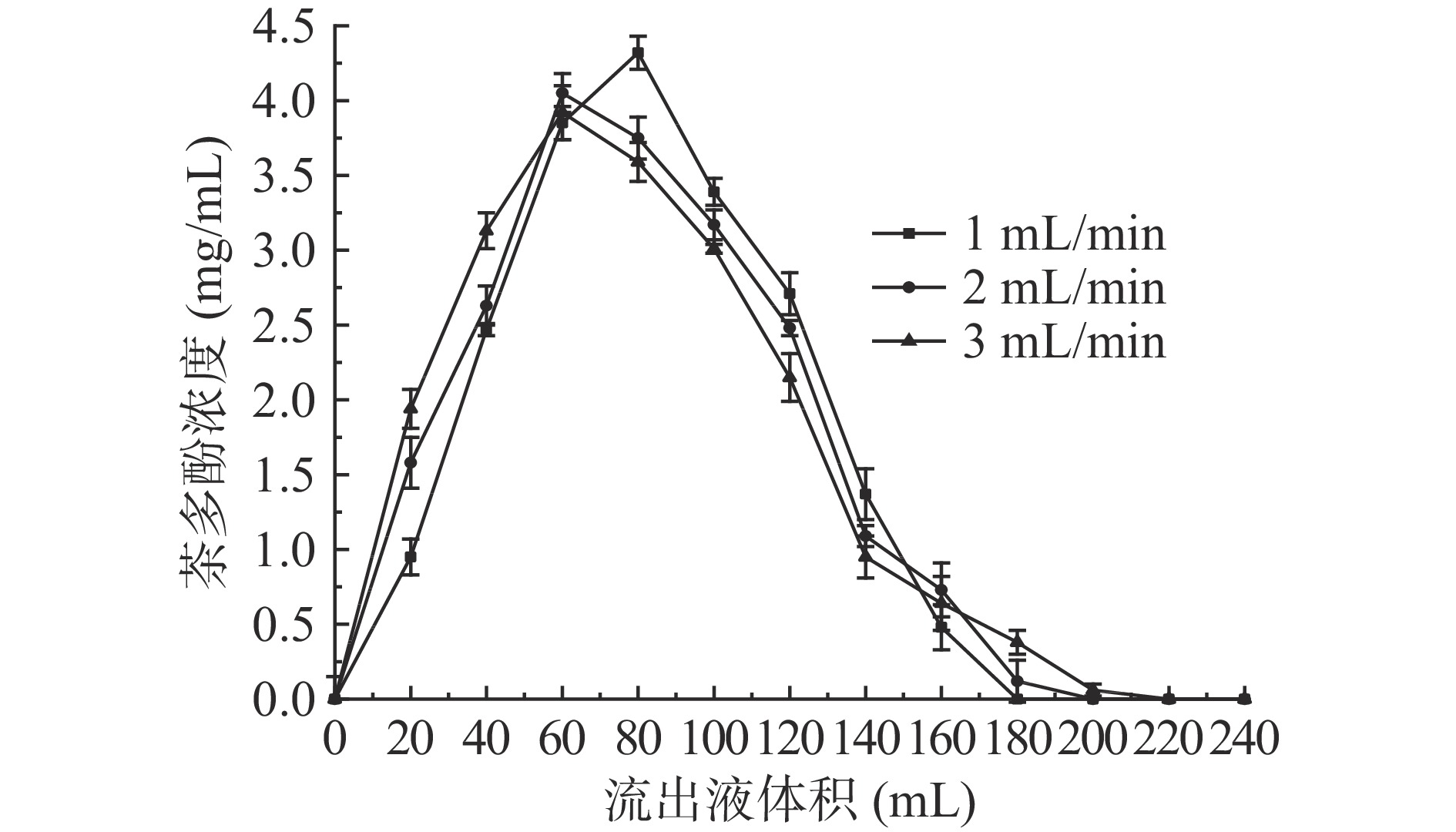
称取30 g经预处理后的LX-8树脂,装填进层析柱中,选择浓度为6.24 mg/mL、pH为5.37的茶汤100 mL,以1 mL/min流速上样,待充分吸附后,选择70%乙醇作为解吸溶液,分别以1、2、3 mL/min不同流速进行解吸,每20 mL收集一次流出液,测定其茶多酚浓度,以流出液体积为横坐标(x),浓度为纵坐标(y),绘制不同流速下的解吸曲线。
1.2.7 响应面试验
在单因素实验的基础上,确定茶汤体积100 mL、吸附流速1 mL/min、解吸液体积180 mL、解吸流速1 mL/min,以pH(A)、茶汤浓度(B)、乙醇浓度(C)为自变量,茶多酚回收率(Y)为响应指标,进行三因素三水平响应面试验(Response surface methodology,RSM)设计,RSM因素与水平见表1。
表 1 Box-Behnken试验设计因素与水平Table 1. Factors and levels of Box-Behnken experiments design水平 A pH B茶汤浓度(mg/mL) C 乙醇浓度(%) −1 4.37 5.16 60 0 5.37 6.24 70 1 6.37 7.32 80 1.2.8 树脂重复使用和再生实验
1.2.8.1 树脂柱重复使用次数考察
按照1.2.7优化的最佳工艺进行茶多酚的吸附、洗脱,洗脱后连续上样,以树脂的吸附量和吸附率为指标,考察LX-8树脂在不经过再生的情况下可以重复使用的次数。
1.2.8.2 再生实验考察
对已使用的树脂,先用3%的盐酸浸洗2 h,然后用3倍柱体积的盐酸通柱,并用净水洗至接近中性,再用5%的氢氧化钠浸洗2 h,用同样的方法通柱、洗至中性,树脂即再生完毕[16]。继续进行吸附、解吸,以树脂的吸附量、吸附率为指标,考察再生后树脂的吸附情况。
1.2.9 抗氧化活性实验
1.2.9.1 总抗氧化能力测定
参照T-AOC检测试剂盒(比色法)进行总抗氧化能力测定。
1.2.9.2 DPPH·清除率测定
参考文献[17-18]并稍作修改,移取375 μmol/L DPPH·乙醇溶液8 mL和2 mL不同浓度的待测样品溶液(纯化前、纯化后、VC)于玻璃试管中,振荡混匀,室温避光反应40 min,用无水乙醇作空白参比,在515 nm处测定其吸光值,并计算DPPH·清除率,计算公式如下:
DPPH⋅清除率(%)=(1−A1−A2A0)×100 式中:A0为不加待测样品溶液,仅加DPPH·乙醇溶液时的吸光值;A1为待测样品溶液加DPPH·乙醇溶液时的吸光值;A2为待测样品溶液的吸光值。
1.2.9.3 ·OH清除率测定
参考文献[19-20]并稍作修改,移取4 mL不同浓度的待测样品溶液(纯化前、纯化后、VC)于玻璃试管中,依次加入2 mL 9 mmol/L FeSO4、2 mL 9 mmol/L 水杨酸-乙醇溶液和2 mL 8.8 mmol/L H2O2溶液,在37 ℃恒温水浴锅中反应20 min,用蒸馏水作空白参比,在510 nm处测定其吸光值,并计算·OH清除率,计算公式如下:
⋅OH清除率(%)=(1−A1−A2A0)×100 式中:A0为蒸馏水代替待测样品溶液时的吸光值;A1为待测样品溶液的吸光值;A2为蒸馏水代替H2O2溶液的吸光值。
1.3 数据处理
每组实验均重复3次,结果以“平均数±标准差”的形式表示。采用Excel 2020软件处理数据,Origin 2018软件进行绘图,Design-Expert 8.0.6软件进行响应面设计,SPSS 20.0进行方差分析,检验水平α=0.05。
2. 结果与分析
2.1 树脂的静态吸附-解吸性能比较
不同类型的树脂对茶多酚的吸附效果不同,因此选取14种不同极性的树脂,考察其对茶多酚静态吸附和解吸效果,结果见表2。由表2可以发现,极性树脂对茶多酚的吸附率普遍都比非极性树脂的吸附率高,这是因为树脂“相似相溶”的原理[21],茶多酚因其含有大量酚羟基和糖苷链,具有较强的极性和亲水性,所以易于被极性树脂所吸附[12]。其中吸附效果最好的是LX-B14,其次是D301和LX-8,三种树脂的吸附率分别为90.85%、90.69%、90.65%。但LX-8的解吸率可达90.26%,明显高于LX-B14和D301,可能存在的原因是解吸率的大小主要取决于树脂与被吸附物质的结合力的强弱[22],D301和LX-B14两种树脂的极性太大,对茶多酚的吸附作用太强,导致乙醇溶液难以将茶多酚解吸下来。综合吸附率和解吸率,选择LX-8树脂进行后续茶多酚的纯化。
表 2 14种大孔树脂的静态吸附和解吸效果Table 2. Static adsorption and desorption effects of 14 macroporous resins树脂型号 极性 吸附量(mg/g) 吸附率(%) 解吸量(mg/g) 解吸率(%) LX-B14 极性 39.20±0.55b 90.85±1.27a 28.52±0.65b 72.77±0.86ef XDA-8G 极性 21.86±0.23f 68.80±0.72b 17.26±0.29d 78.95±1.98d LX-8 极性 33.09±0.27c 90.65±0.74a 29.87±0.69a 90.26±1.92ab SP207 极性 25.83±0.26e 58.20±0.59d 16.89±0.93d 65.39±3.59g D301 极性 41.76±0.30a 90.69±0.66a 11.46±0.87e 27.44±1.88h HZW635 极性 26.59±0.69de 68.07±1.78b 20.87±0.50c 78.56±3.84d HZW636 极性 27.01±0.80d 62.64±1.86c 20.35±0.97c 75.46±5.88de ADS-17 中极性 1.90±0.53h 3.42±0.96e 1.54±0.44f 81.12±1.97cd HPD450 中极性 2.90±0.82gh 4.69±1.32e 1.96±0.52f 67.84±1.72fg AB-8 弱极性 2.35±0.48gh 4.87±0.98e 2.11±0.38f 90.26±4.24ab X-5 非极性 2.66±0.37gh 4.39±0.62e 2.04±0.32f 76.72±2.23de D101 非极性 2.24±0.41h 4.83±0.89e 1.92±0.44f 85.09±4.57bc H103 非极性 3.33±0.86g 5.17±1.32e 2.10±0.46f 63.65±2.83g HPD100 非极性 2.89±0.56gh 5.32±1.02e 2.64±0.55f 91.02±1.83a 注:同列不同字母表示差异显著(P<0.05)。 2.2 吸附等温曲线
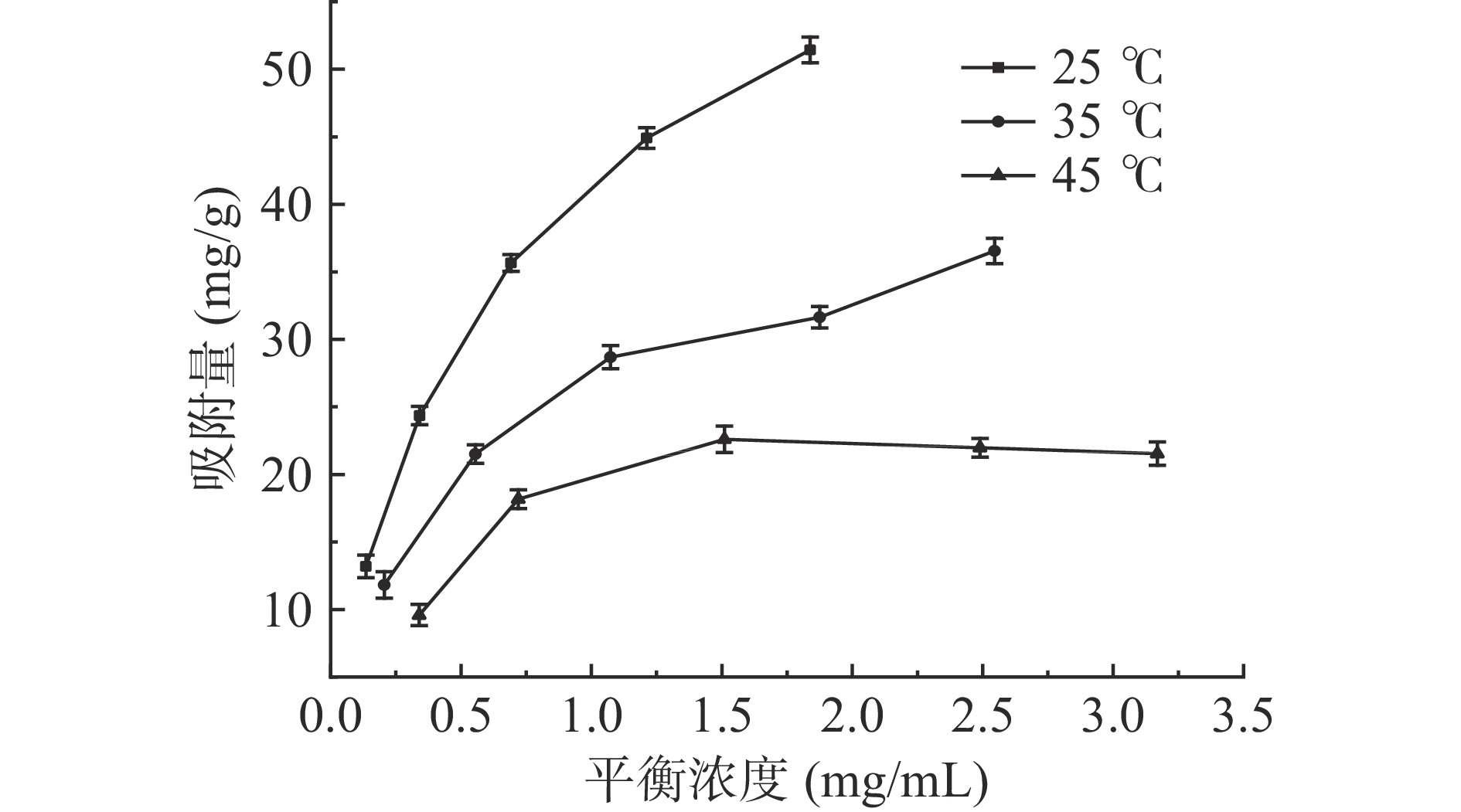
为了考察茶多酚在LX-8树脂上的吸附效果,并且揭示其吸附行为,配制不同浓度茶多酚(1、2、3、4、5 mg/mL)溶液,用LX-8树脂分别在 25、35、45 ℃下吸附,达到吸附平衡。可以得到LX-8树脂对茶汤中茶多酚的吸附等温线如图1所示。吸附量随着底物浓度的增加而增大,且在同一底物浓度下,温度越低,吸附量越高,表明茶多酚的吸附是放热过程,温度的降低有利于吸附的进行。将静态等温实验所得1/qe~1/Ce及lnqe~lnCe关系分别进行线性拟合[23],根据Langmuir方程和Freundlich方程计算模型参数,结果如表3、表4所示。
表 3 不同温度下的Langmuir模型拟合参数Table 3. Fitting parameters of Langmuir models at different temperatures表 4 不同温度下的Freundlich模型拟合参数Table 4. Fitting parameters of Freundlich models at different temperatures温度(℃) Freundlich方程 KF 1/n R2 25 lnqe=0.4806InCe−3.4963 0.03 0.4806 0.9831 35 lnqe=0.5678InCe−3.2386 0.04 0.5678 0.9805 45 lnqe=0.6557InCe−2.814 0.06 0.6557 0.9235 在25 ℃下,LX-8树脂上茶多酚的Langmuir和Freundlich方程的R2分别为0.9984和0.9831。其中Langmuir方程的R2更大,说明Langmuir模型更适合来描述在1~5 mg/mL 浓度范围内,LX-8树脂对茶多酚的吸附情况。
2.3 吸附动力学曲线
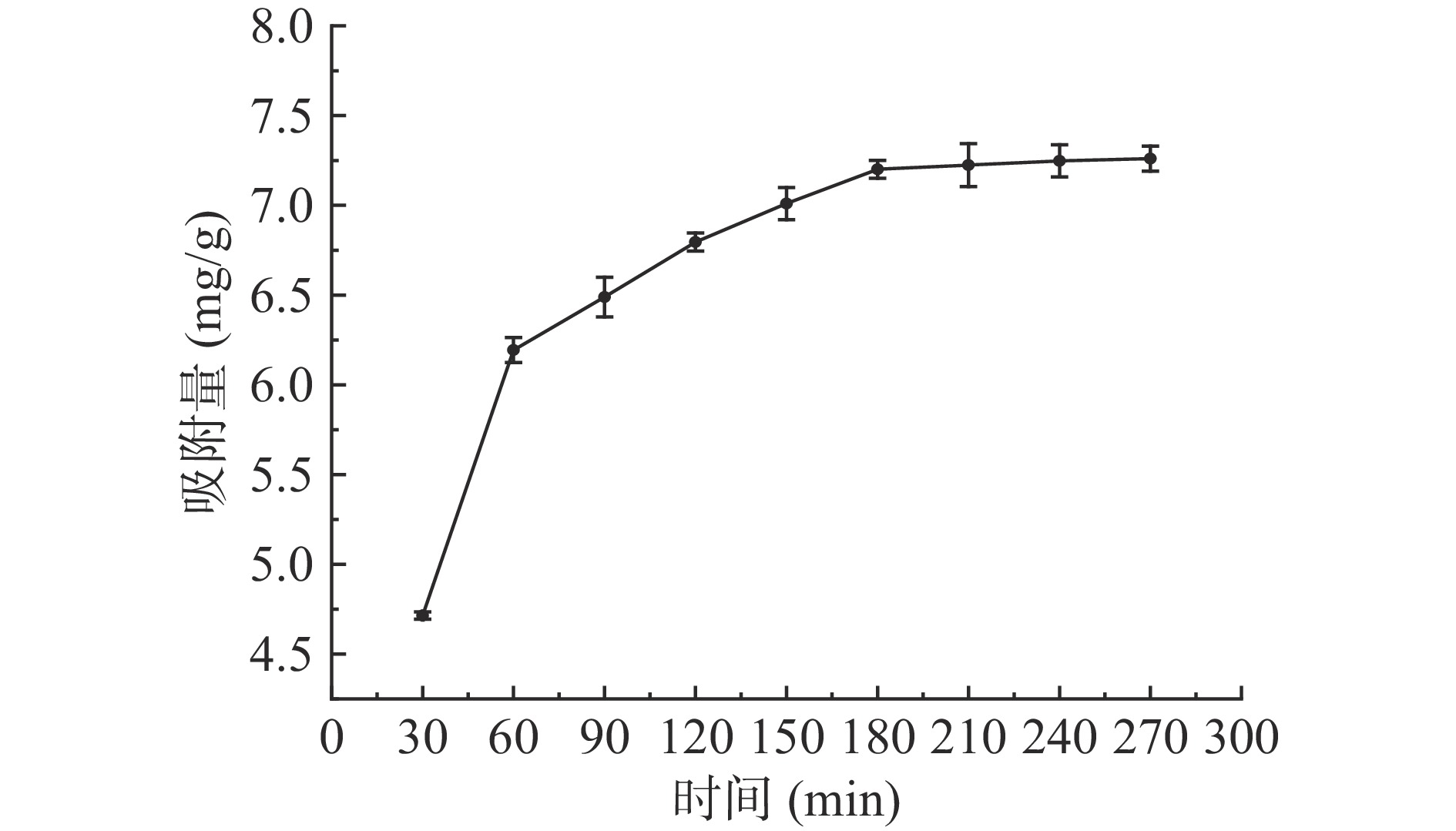
在25 ℃下,LX-8树脂对茶汤中茶多酚的静态吸附曲线如图2所示。由图2可得,吸附时间增加,其吸附量也相应的增加,在30~60 min内,增长速率最快,60~180 min内增长速率变缓,180~270 min内,增长速率逐渐接近一条直线。
选择拟一级和拟二级动力学模型来探究LX-8树脂对茶汤中茶多酚的吸附动力学特征和吸附原理,其中,拟一级和拟二级动力学模型可以描述大部分的吸附特征[24],因此结合LX-8树脂对茶多酚的吸附数据,通过对这两种模型进行线性拟合,可以更加清晰地阐述LX-8树脂对茶多酚的吸附原理。从表5中可以看出,二级动力学模型的决定系数最大,为0.9996,表明二级动力学模型能更好地描述LX-8树脂对茶多酚的吸附过程。
表 5 吸附动力学模型拟合参数Table 5. Fitting parameters of adsorption kinetics models拟合模型 拟合方程 qe k R2 一级动力学 ln(qe-qt)=−0.3252t+1.2 3.32 0.325 0.846 二级动力学 t/qt=0.1285t+2.2022 7.78 0.008 0.9996 2.4 单因素实验
2.4.1 茶汤pH对树脂吸附率的影响
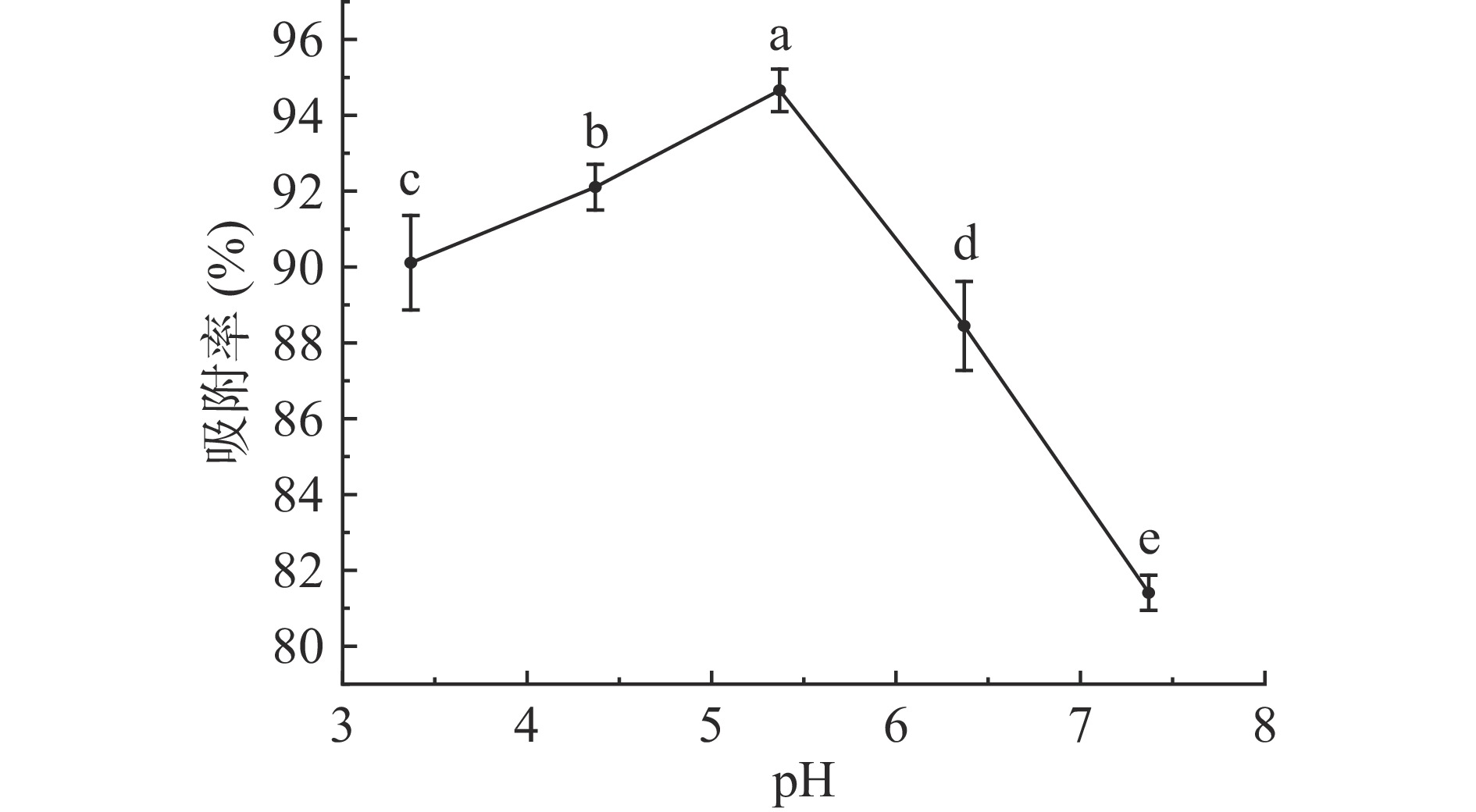
样品溶液的pH会通过改变茶多酚的电离程度来影响茶多酚与树脂之间的亲和力,从而影响树脂对茶多酚的吸附情况[21],因此考察茶汤pH对LX-8树脂吸附率的影响。从图3可以看出,当茶汤pH从3.37增加到5.37时,LX-8树脂的吸附率呈上升趋势,在pH为5.37,即茶汤原本pH时,LX-8树脂的吸附率达到最高值(94.66%),而后pH的升高导致LX-8树脂的吸附率逐渐下降。这是因为茶多酚是一种弱酸类物质,含有大量的酚羟基,容易电离出H+,以离子形式存在[25]。在酸性条件下,会抑制H+电离,从而使茶多酚能以分子的形式被树脂所吸附,而随着pH的升高,溶液中的OH−增多,与H+反应,从而使茶多酚浓度降低,吸附率下降[26],因此,以茶汤pH4.37、5.37、6.37为后续响应面试验因素考察水平。
2.4.2 茶汤浓度对树脂吸附率的影响
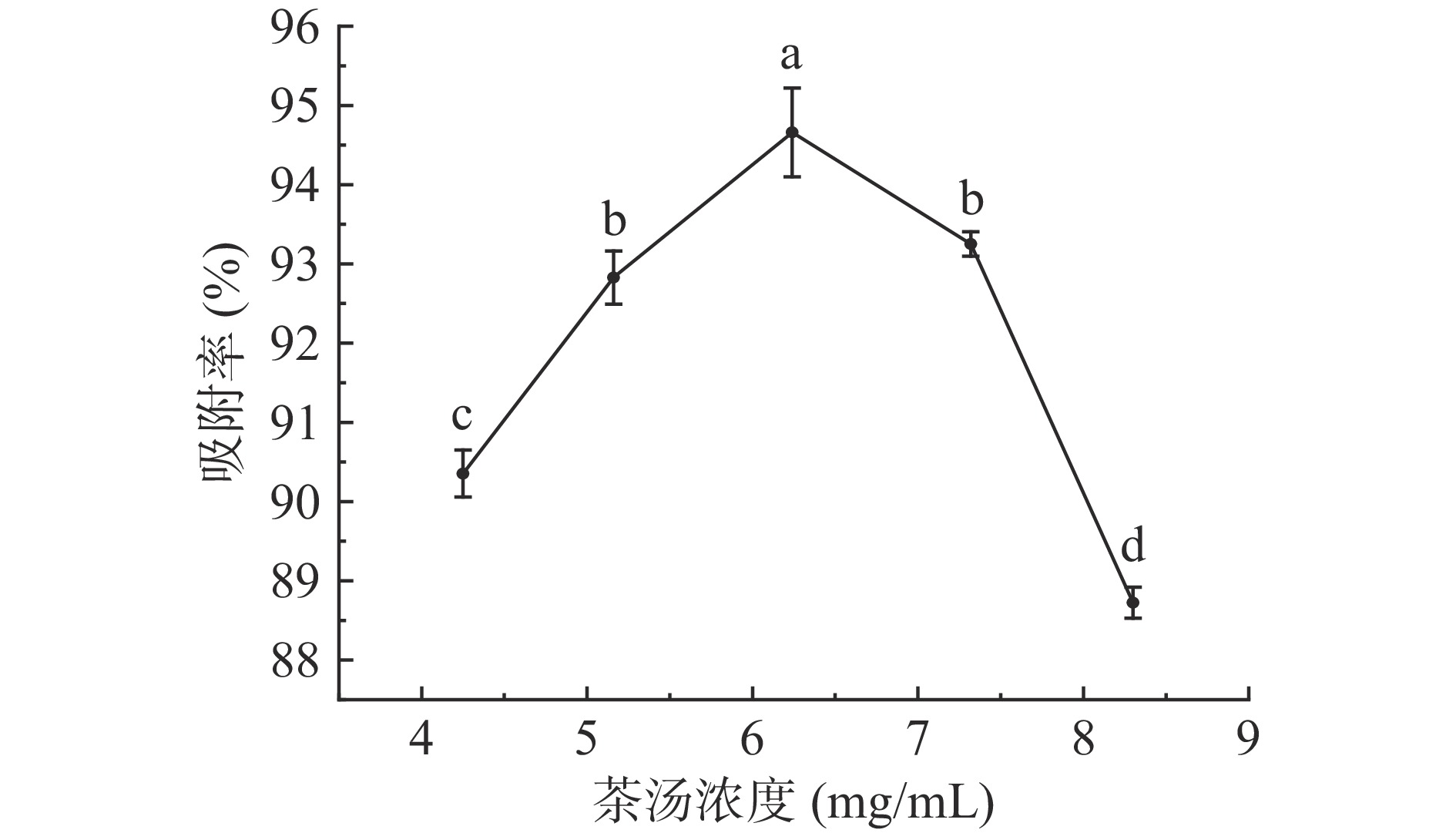
在上样流速一定的情况下,上样液的浓度会影响树脂的动态吸附,适中的浓度不仅能够使树脂的利用率最大化[27],同时还能缩短吸附时间,提高吸附效率,因此考察不同茶汤浓度对LX-8树脂吸附率的影响。由图4可得,一开始,LX-8树脂的吸附率随茶汤浓度的增加而升高,且差异显著(P<0.05),当茶汤达到一定浓度(6.24 mg/mL)后,LX-8树脂的吸附率开始随茶汤浓度的增加而下降。这是因为茶汤浓度过低会导致其本身的多酚含量偏低,降低树脂的吸附动力[28],从而使LX-8树脂的吸附率下降,而茶汤浓度过高会使样液在树脂中产生积絮和沉淀,影响多酚在溶液和树脂中的扩散,造成树脂堵塞,从而降低LX-8树脂的吸附率[29]。因此,以茶汤浓度5.16、6.24、7.32 mg/mL为后续响应面试验因素考察水平。
2.4.3 不同吸附流速的泄露曲线
当流出液中茶多酚浓度达到初始浓度的 1/10 时,则认定目标物在此刻开始流出,称为“泄漏点”[28]。而吸附流速主要是影响溶质向树脂表面的扩散,流速不同树脂的泄漏点也不同,因此考察在不同流速下树脂的泄露曲线。由图5可知,随着茶汤体积的增加,树脂的吸附能力减弱,流出液中茶多酚浓度逐渐增加。当上样流速分别为1、2、3 mL/min时,茶汤体积分别在100、80、60 mL时开始出现泄漏点,流速越快,泄漏时间越早,树脂的吸附量也就越少。陈荣义[21]通过研究树脂吸附实验,发现上样流速过快会导致树脂与茶多酚还未充分接触,溶质分子来不及进入树脂内表面被吸附,就直接被溶液冲出柱子而流出,从而使树脂的吸附率降低。因此,确定最佳吸附流速1 mL/min、茶汤体积100 mL。
2.4.4 乙醇浓度对树脂解吸率的影响
在同等条件下,茶多酚在乙醇中的溶解性要高于在水中的溶解性[30],且乙醇可以回收再利用,故解吸试验中选择乙醇作为解吸剂,而乙醇浓度的不同会影响茶多酚与树脂之间的范德华力,从而导致解吸性能的不同,因此考察不同乙醇浓度对LX-8树脂解吸率的影响。从图6可以看出,当乙醇浓度增加时,LX-8树脂的解吸率也不断升高,并在乙醇浓度达到70%时,LX-8树脂的解吸率达到最高值,之后进一步的增加乙醇浓度,LX-8树脂的解吸率反而开始出现下降趋势。李洋[31]通过树脂纯化茶多酚的研究也发现,当乙醇浓度过高时,洗脱剂的流动性相对较差,不利于目标物质的溶出,因此,以乙醇浓度60%、70%、80%为后续响应面试验因素考察水平。
2.4.5 不同解吸流速的解吸曲线
当茶多酚被树脂吸附饱和后,合适的解吸流速有利于解吸剂在树脂中的扩散,增强树脂的解吸效果,因此考察在不同流速下树脂的解吸曲线。从图7可以看出,当流速为1 mL/min、乙醇用量为180 mL时,茶多酚全部被解吸下来,解吸曲线单一、对称、无明显拖尾现象。而随着流速的加快,乙醇用量逐渐增加,峰型越来越宽,解吸曲线出现明显拖尾现象,这是因为乙醇溶液与树脂接触的时间过短,还未来得及与被树脂吸附的茶多酚充分溶解,就因流速过快被冲出柱外[32]。因此,确定最佳解吸流速1 mL/min、解吸剂用量180 mL。
2.5 响应面试验
2.5.1 响应面试验设计及结果
根据上述单因素实验结果,以pH (A)、茶汤浓度(B)、乙醇浓度(C)为自变量,茶多酚回收率(Y)为响应值,进行3因素3水平的响应面试验分析。响应面Box-Behnken试验设计及结果与分析见表6。
表 6 响应面试验设计及结果Table 6. Design and results of response surface experiment试验号 A pH B 茶汤浓度 C 乙醇浓度 Y 回收率(%) 1 1 0 1 82.6±0.26 2 0 0 0 86.4±0.17 3 −1 0 −1 80.4±0.10 4 0 0 0 87.5±0.29 5 1 −1 0 72.8±0.26 6 1 0 −1 74.7±0.30 7 −1 0 1 81.2±0.44 8 −1 −1 0 77.9±0.40 9 0 1 1 83.8±0.46 10 0 0 0 87.2±0.17 11 0 −1 1 81.6±0.30 12 0 −1 −1 79.2±0.10 13 0 1 −1 82.7±0.20 14 1 1 0 77.4±0.36 15 −1 1 0 78.3±0.17 16 0 0 0 87.6±0.30 17 0 0 0 87.9±0.10 2.5.2 模型建立与方差分析
依据表6开始试验,响应值是茶多酚回收率(Y),利用Design-Expert软件对表3进行多元线性回归方程的拟合,得到以下方程:
Y=87.32−1.29A+1.34B+1.52C+1.05AB+1.77AC−0.32BC−6.41A2−4.31B2−1.18C2
对模型进行显著性检验,结果如表7所示。模型P<0.0001,极显著,表明该试验设计可行。失拟项P=0.1118>0.05,不显著,说明模型选择正确,试验数据具有参考价值。模型中的回归系数R2=0.9852和校正系数R2adj=0.9663均大于0.9,表明试验误差较小,该试验模型拟合良好,可以对茶多酚的回收率有准确的分析和预测。
表 7 回归模型方差分析Table 7. Variance analysis of regression model方差来源 平方和 自由度 均方 F值 P值 显著性 模型 341.23 9 37.91 51.93 < 0.0001 ** A 13.26 1 13.26 18.16 0.0037 ** B 14.31 1 14.31 19.60 0.0031 ** C 18.60 1 18.60 25.48 0.0015 ** AB 4.41 1 4.41 6.04 0.0436 * AC 12.60 1 12.60 17.26 0.0043 ** BC 0.42 1 0.42 0.58 0.4717 A2 173.00 1 173.00 236.97 < 0.0001 ** B2 78.22 1 78.22 107.13 < 0.0001 ** C2 5.91 1 5.91 8.10 0.0248 * 残差 5.11 7 0.73 失拟项 3.80 3 1.27 3.88 0.1118 不显著 纯误差 1.31 4 0.33 总和 346.34 16 R2=0.9852 R²adj=0.9663 注:“*”表示对结果影响差异显著(P<0.05);“**”表示对结果影响差异极显著(P<0.01)。 从模型中各个因素的P值可以看出,一次项(A、B、C)、二次项(A2、B2)和交互项AC对茶多酚回收率的影响均极显著(P<0.01);二次项C2和交互项AB对茶多酚回收率的影响显著(P<0.05);而交互项BC对茶多酚回收率的影响不显著(P>0.05)。通过F值大小可知,三个因素对茶多酚回收率的影响效果的大小顺序为C>B>A,即乙醇浓度>茶汤浓度>pH。
2.5.3 响应面分析
根据回归方程绘制响应面分析图,pH、茶汤浓度、乙醇浓度三个因素之间的交互作用对茶多酚回收率影响的响应面及等高线如图8所示。响应曲面图趋于弧形,曲面坡度陡峭,且投射下来的等高线数量越多,表明两个因素的交互作用越显著,反之,响应曲面图趋于平面,曲面坡度平缓,且投射下来的等高线数量越少,表明两个因素的交互作用不显著。
由图8a可知,随着pH和茶汤浓度的增加,茶多酚回收率先升高后降低,茶多酚回收率存在最高值,在pH5.37和茶汤浓度6.24 mg/mL附近,曲面图呈弧形,曲面坡度较陡,这说明pH和茶汤浓度的交互作用对茶多酚回收率有显著影响,与模型方差结果一致。
由图8b可知,随着茶汤浓度和乙醇浓度的升高,茶多酚回收率先增加后降低,曲面图呈弧形,但曲面投射下来的等高线数量较少,这说明茶汤浓度和乙醇浓度的交互作用对茶多酚回收率的影响不显著,与模型方差结果一致。
由图8c可知,随着pH和乙醇浓度的增加,茶多酚回收率呈现升高后下降的趋势,茶多酚回收率存在最高值,在pH5.37和乙醇浓度70%附近,曲面坡度十分陡峭,且曲面投射下来的等高线数量多,呈椭圆,这说明pH和乙醇浓度的交互作用对茶多酚回收率的影响极显著,与模型方差结果一致。
2.5.4 验证试验结果
通过回归方程模型拟合分析,预测得到的最优工艺参数为pH5.37、茶汤浓度6.38 mg/mL、乙醇浓度76.24%,在此工艺条件下得到的预测茶多酚回收率为87.9%;考虑到实际操作条件,将工艺条件修正为pH5.4、茶汤浓度6.4 mg/mL、乙醇浓度76%,在此工艺条件下得到的实际茶多酚回收率为86.9%±0.45%,这与理论预测值基本一致,说明该响应面模型拟合的工艺条件准确可靠,具有可行性。
2.6 LX-8树脂重复使用和再生实验
2.6.1 重复使用次数考察
该树脂初次使用时,对茶多酚的吸附率可达到92.6%,随着重复次数的增加,树脂的吸附能力也逐渐减弱,由图9可知,当树脂重复次数达到第6次时,树脂的吸附率为58.9%,比初始下降了33.7%。LX-8树脂是极性树脂,其与茶多酚的吸附主要是通过氢键作用[33],树脂在吸附过程中,茶多酚会优先占据最佳的吸附位置,重复次数增多,树脂表面和内部会残留许多杂质,导致树脂的吸附位置减少,当再次进行吸附时,吸附能力减弱,吸附率降低,一般认为树脂的吸附率比初次使用下降30%时,便需要进行再生,因此LX-8树脂可以重复使用5次。
2.6.2 再生实验考察
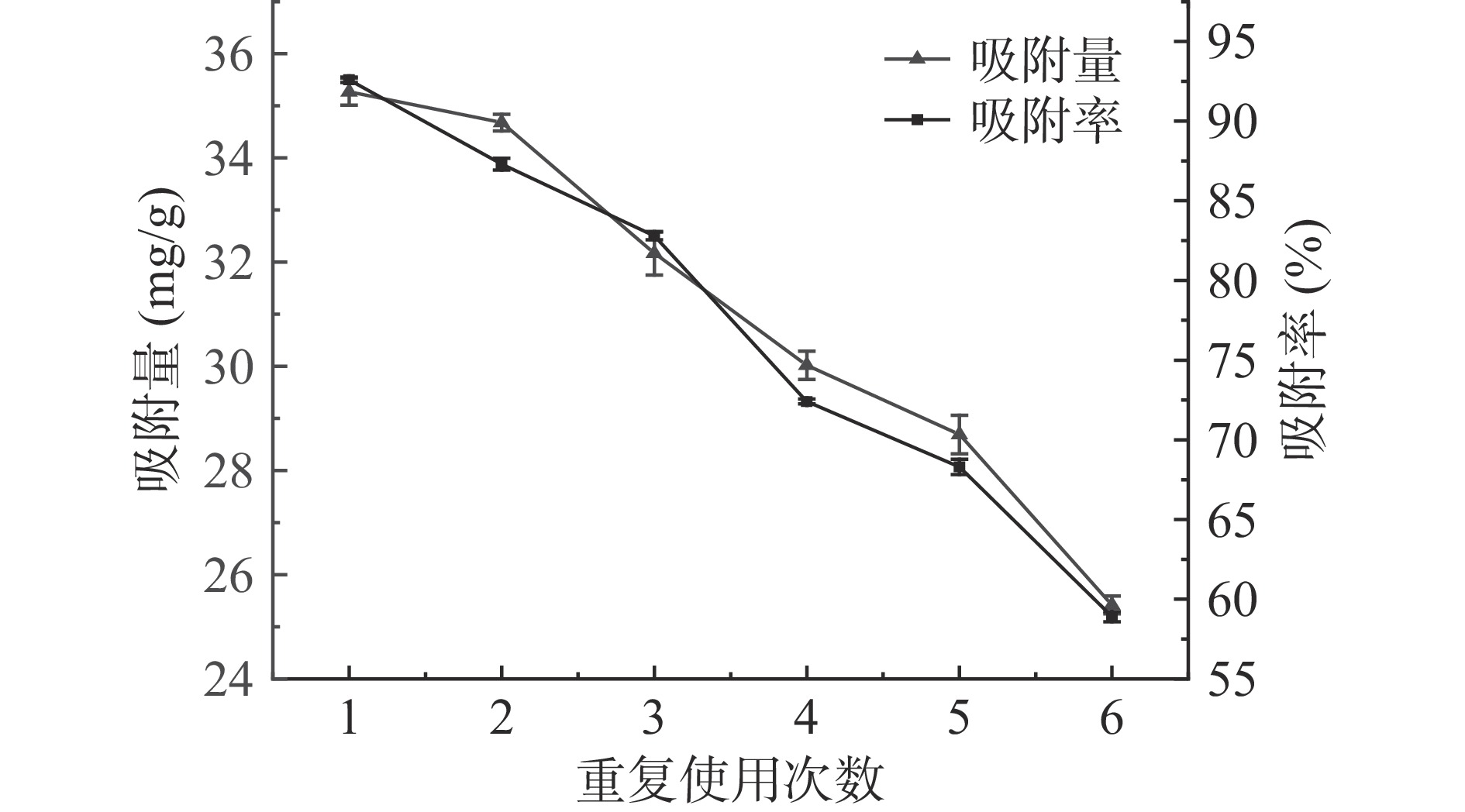
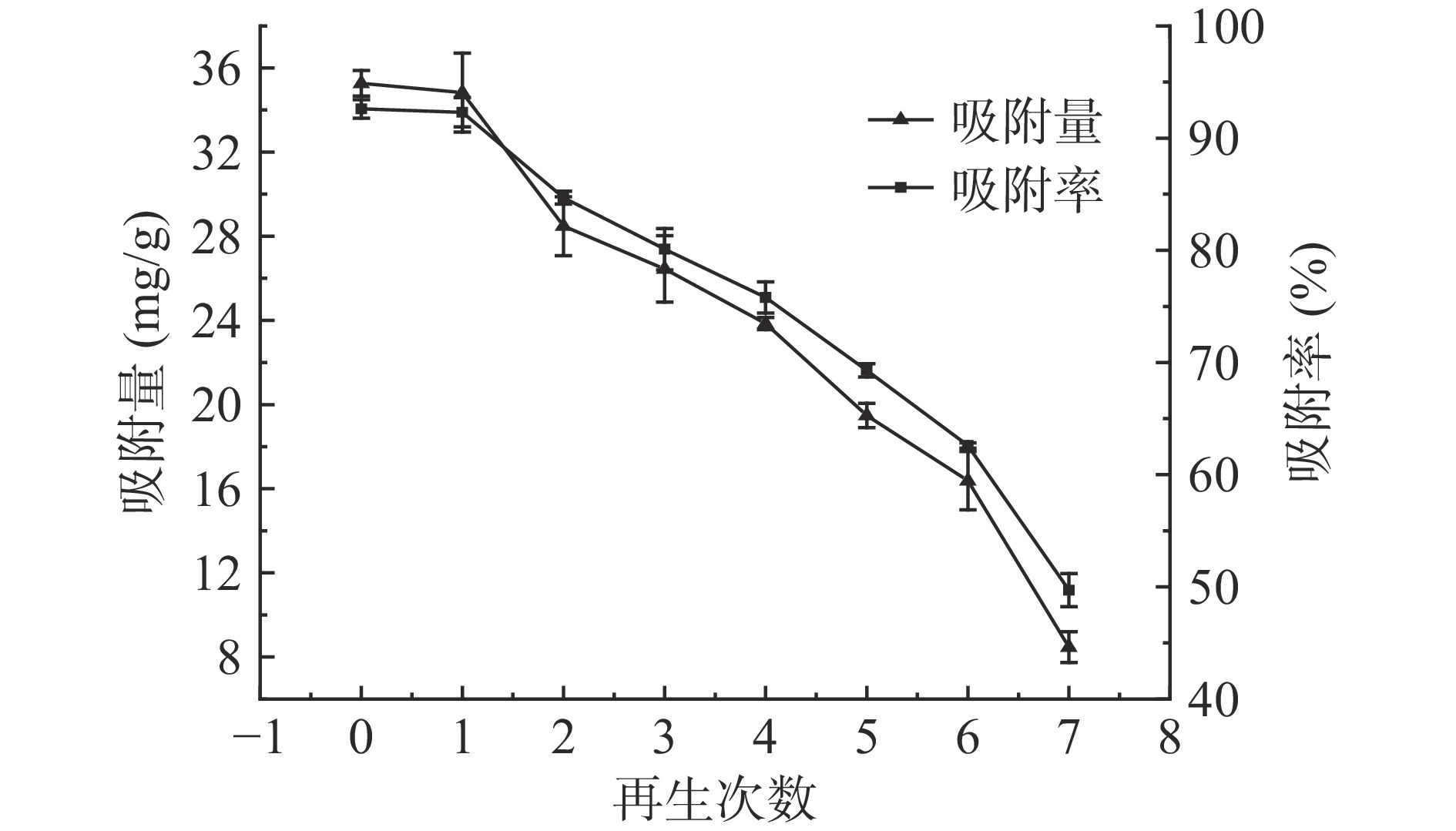
通常多次使用的树脂会因为吸附物质中杂质的污染使柱效降低,从而导致树脂的吸附量和吸附率下降,所以需要通过酸碱再生,使其恢复吸附能力[16]。由图10可知,通过再生处理的树脂,再次上样后,吸附量和吸附率分别为(34.83±1.88)mg/g和92.3%±1.31%,其吸附率仅比第一次使用树脂时低了0.3%,这说明LX-8树脂可以通过再生工艺继续投入使用。但再生次数也是有限的,从图中可以看出,随着再生次数的增加,树脂的吸附量和吸附率不断下降,当再生次数达到第7次时,其树脂吸附率下降到49.7%±1.48%,比初次使用下降了42.9%,表明此时树脂已经不能再使用,需要更换新的树脂。
2.7 纯化前后茶多酚的抗氧化活性效果
2.7.1 总抗氧化能力(T-AOC)效果
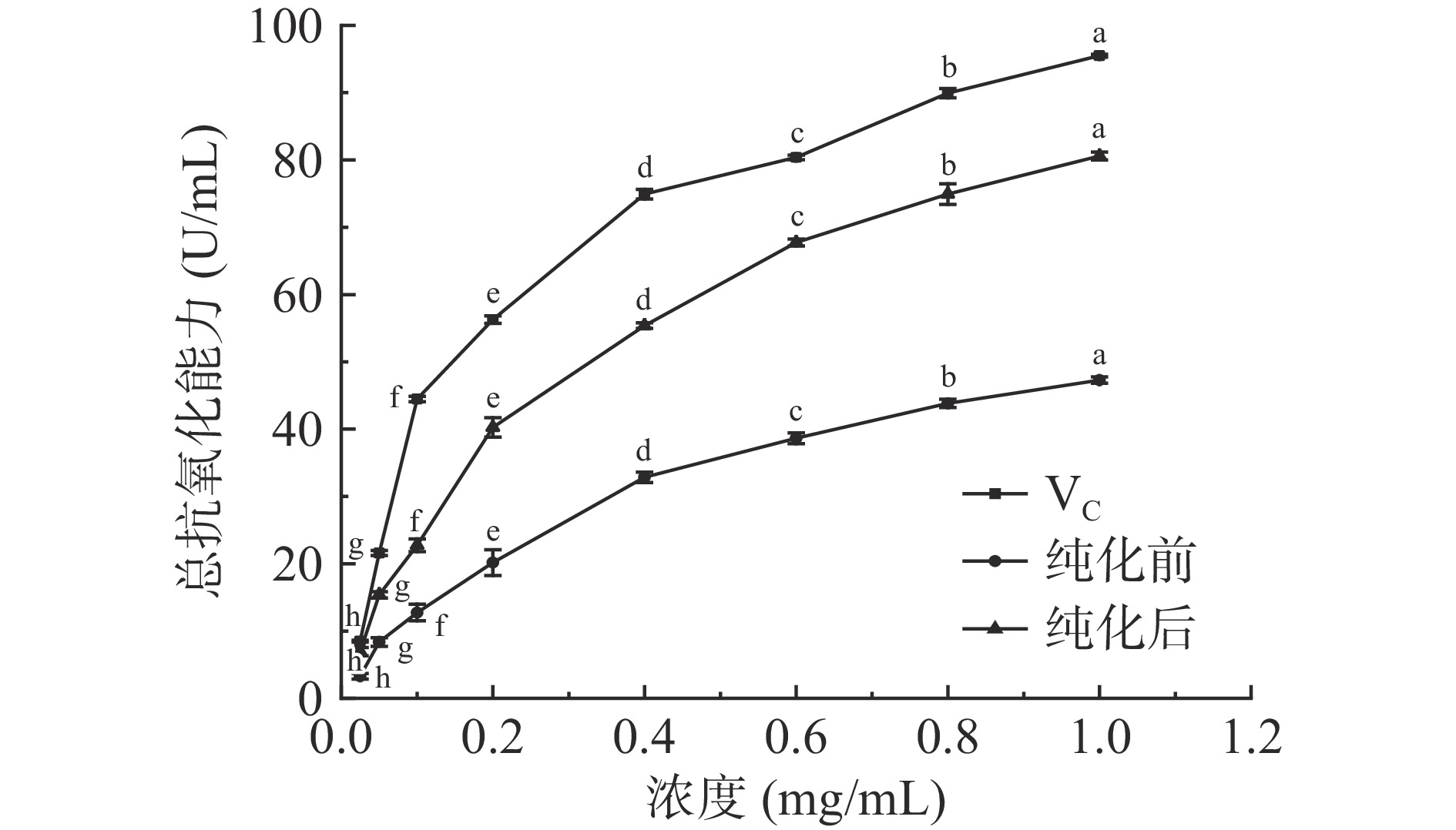
选择VC作为对照组,考察纯化前后,不同浓度茶多酚的总抗氧化能力。由图11可知,样品浓度越高,其总抗氧化能力也就越强,且在不同浓度间呈显著差异(P<0.05)。郭雷等[34]通过超声辅助法获得的茶多酚,其总抗氧化能力也随着提取物浓度的增加而升高。纯化前,样品的总抗氧化能力偏低,纯化后,样品的总抗氧化能力逐渐增强,并不断接近VC的总抗氧化能力,当浓度为1.0 mg/mL时,其总抗氧化能力可达(80.59±0.60)U/mL。三种样品的总抗氧化能力大小为VC>纯化后>纯化前,这表明树脂的纯化能够显著提高茶多酚的总抗氧化能力。
2.7.2 DPPH·的清除效果
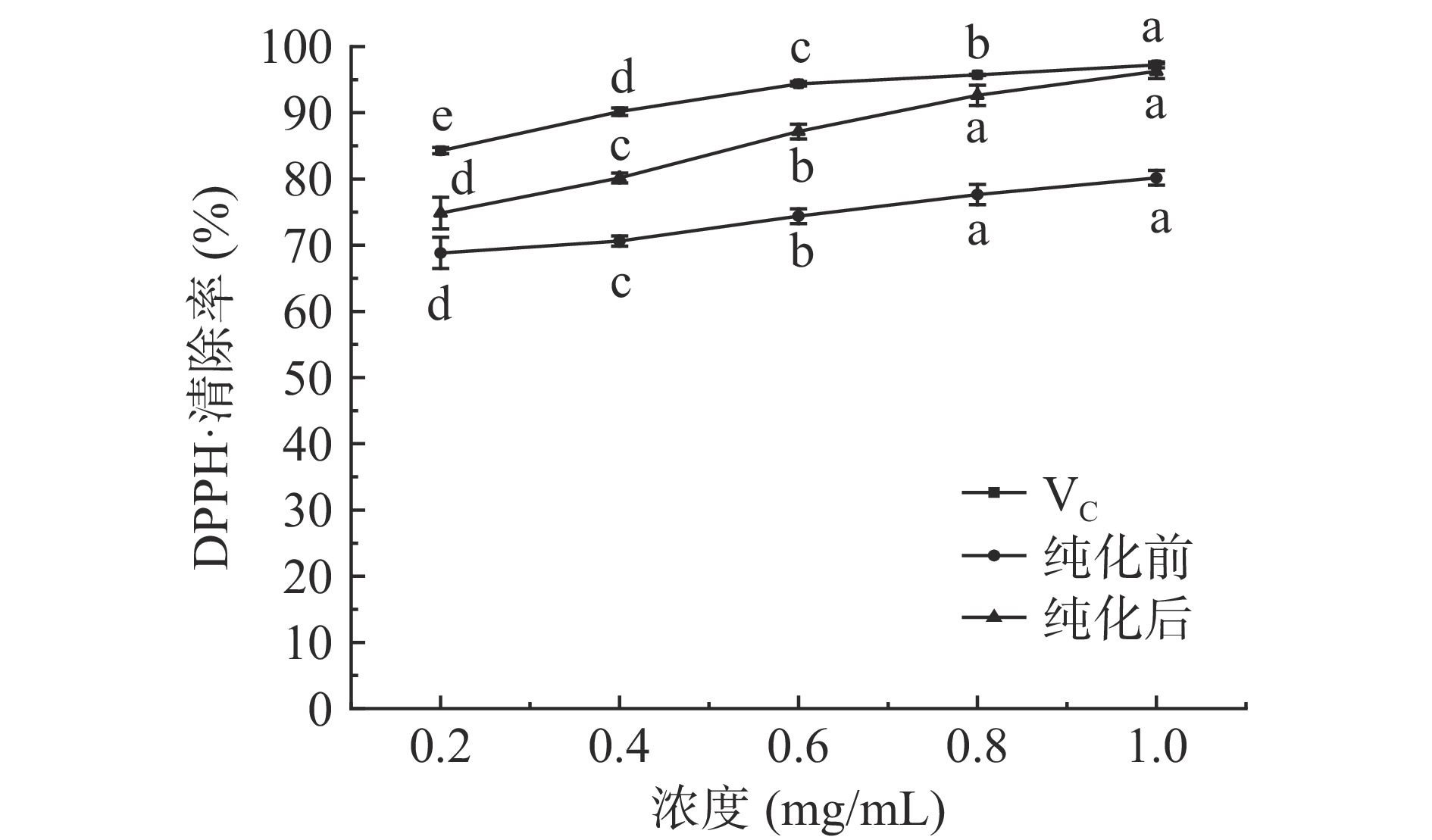
茶多酚纯化前后对DPPH·清除效果如图12所示,在0.2~1.0 mg/mL浓度范围内,随着浓度的增加,茶多酚对DPPH·的清除率也逐渐增大,且纯化后茶多酚的清除能力更强,表明通过树脂进行纯化可以提高茶多酚对DPPH·的清除能力。当纯化后的茶多酚浓度为1.0 mg/mL时,DPPH·清除率达到了96.27%±1.98%,与该浓度下对照组VC的清除率97.24%±0.45%相接近。IC50越小,表示清除效果越好,抗氧化能力越强[35],VC、纯化前、纯化后的IC50值分别为0.0029、0.0407、0.0326 mg/mL,优于吴婕等[9]通过研究HPD-826树脂纯化茶多酚(IC50=0.553 mg/mL)的DPPH·的清除能力。
2.7.3 ·OH的清除效果
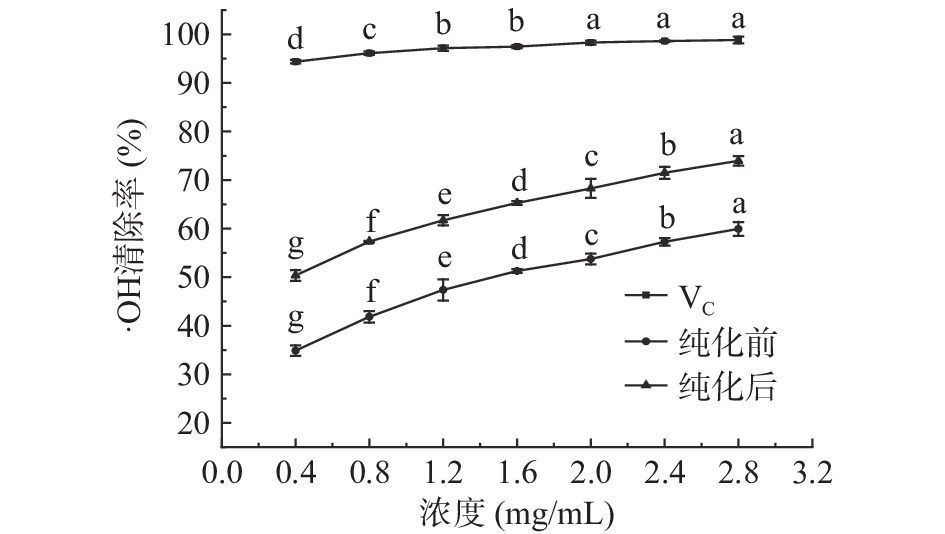
不同浓度样品对·OH的清除效果如图13所示,随着浓度的增加,三者的清除率均不断升高。虽然纯化前后,其茶多酚的清除率都要低于VC的清除率,但通过树脂纯化,浓度为1.0 mg/mL对应的清除率由59.93%±1.43%提高到73.96%±0.99%。同样通过方程计算得出VC、纯化前和纯化后的IC50值分别为0.0016、1.4059和0.4167 mg/mL,三者的·OH清除能力大小由强到弱的顺序表现为VC>纯化后>纯化前。在喻铭佳等[36]的研究中发现,经 HP-20 大孔树脂富集后的茶多酚对·OH的清除率可达66.94%,同等浓度下·OH清除能力低于本研究制备的茶多酚。
3. 结论
本研究通过比较14种树脂的静态吸附-解吸性能,选用LX-8树脂进行茶多酚的动态吸附,采用单因素和响应面试验对其工艺进行优化,并对LX-8树脂连续吸附和再生情况进行考察。结果表明,最佳纯化工艺参数:100 mL浓度为6.4 mg/mL、pH5.4的茶汤以1 mL/min流速上样至LX-8树脂后,经180 mL 76%乙醇溶液,以1 mL/min流速解吸,在该条件下茶多酚的回收率为86.9%,纯度为74.6%。LX-8树脂可以连续使用5次,再生6次,说明该树脂用于纯化茶多酚可以有效减少成本,应用于工业化生产。此外,随着温度的升高,树脂的吸附量下降,表明LX-8树脂吸附茶多酚是放热过程,其吸附过程符合Langmuir模型和二级动力学模型。
以VC为对照,通过总抗氧化、DPPH·和·OH 3种抗氧化活性评价方法对提纯前后茶多酚的抗氧化能力进行综合评价,结果表明,VC和纯化前后茶多酚(1 mg/mL)的总抗氧化能力分别为95.49、47.29、80.59 U/mL;对DPPH·清除能力的IC50值分别为0.0029、0.0407、0.0326 mg/mL;对·OH清除能力的IC50值分别为0.0016、1.4059和0.4167 mg/mL。纯化后茶多酚的总抗氧化能力、DPPH·清除能力和·OH清除能力虽然低于VC的抗氧化活性,但均高于纯化前的茶多酚,说明通过该工艺,能够显著提高茶多酚的抗氧化活性,且当纯化后茶多酚浓度为1 mg/mL时,其DPPH·清除率已经接近VC的DPPH·清除率,这为茶多酚的应用提供了数据支持和理论依据。后续还可以针对其抗病毒、抗衰老[37]等具体功效展开体内活性实验的研究,进一步挖掘茶多酚的开发利用价值,此外,茶多酚对某些环境和胃肠道条件敏感,其口服利用度低[38],因此未来应用茶多酚时如何提高其稳定性和生物利用度也是需要解决的问题。
-
表 1 Box-Behnken试验设计因素与水平
Table 1 Factors and levels of Box-Behnken experiments design
水平 A pH B茶汤浓度(mg/mL) C 乙醇浓度(%) −1 4.37 5.16 60 0 5.37 6.24 70 1 6.37 7.32 80 表 2 14种大孔树脂的静态吸附和解吸效果
Table 2 Static adsorption and desorption effects of 14 macroporous resins
树脂型号 极性 吸附量(mg/g) 吸附率(%) 解吸量(mg/g) 解吸率(%) LX-B14 极性 39.20±0.55b 90.85±1.27a 28.52±0.65b 72.77±0.86ef XDA-8G 极性 21.86±0.23f 68.80±0.72b 17.26±0.29d 78.95±1.98d LX-8 极性 33.09±0.27c 90.65±0.74a 29.87±0.69a 90.26±1.92ab SP207 极性 25.83±0.26e 58.20±0.59d 16.89±0.93d 65.39±3.59g D301 极性 41.76±0.30a 90.69±0.66a 11.46±0.87e 27.44±1.88h HZW635 极性 26.59±0.69de 68.07±1.78b 20.87±0.50c 78.56±3.84d HZW636 极性 27.01±0.80d 62.64±1.86c 20.35±0.97c 75.46±5.88de ADS-17 中极性 1.90±0.53h 3.42±0.96e 1.54±0.44f 81.12±1.97cd HPD450 中极性 2.90±0.82gh 4.69±1.32e 1.96±0.52f 67.84±1.72fg AB-8 弱极性 2.35±0.48gh 4.87±0.98e 2.11±0.38f 90.26±4.24ab X-5 非极性 2.66±0.37gh 4.39±0.62e 2.04±0.32f 76.72±2.23de D101 非极性 2.24±0.41h 4.83±0.89e 1.92±0.44f 85.09±4.57bc H103 非极性 3.33±0.86g 5.17±1.32e 2.10±0.46f 63.65±2.83g HPD100 非极性 2.89±0.56gh 5.32±1.02e 2.64±0.55f 91.02±1.83a 注:同列不同字母表示差异显著(P<0.05)。 表 3 不同温度下的Langmuir模型拟合参数
Table 3 Fitting parameters of Langmuir models at different temperatures
表 4 不同温度下的Freundlich模型拟合参数
Table 4 Fitting parameters of Freundlich models at different temperatures
温度(℃) Freundlich方程 KF 1/n R2 25 lnqe=0.4806InCe−3.4963 0.03 0.4806 0.9831 35 lnqe=0.5678InCe−3.2386 0.04 0.5678 0.9805 45 lnqe=0.6557InCe−2.814 0.06 0.6557 0.9235 表 5 吸附动力学模型拟合参数
Table 5 Fitting parameters of adsorption kinetics models
拟合模型 拟合方程 qe k R2 一级动力学 ln(qe-qt)=−0.3252t+1.2 3.32 0.325 0.846 二级动力学 t/qt=0.1285t+2.2022 7.78 0.008 0.9996 表 6 响应面试验设计及结果
Table 6 Design and results of response surface experiment
试验号 A pH B 茶汤浓度 C 乙醇浓度 Y 回收率(%) 1 1 0 1 82.6±0.26 2 0 0 0 86.4±0.17 3 −1 0 −1 80.4±0.10 4 0 0 0 87.5±0.29 5 1 −1 0 72.8±0.26 6 1 0 −1 74.7±0.30 7 −1 0 1 81.2±0.44 8 −1 −1 0 77.9±0.40 9 0 1 1 83.8±0.46 10 0 0 0 87.2±0.17 11 0 −1 1 81.6±0.30 12 0 −1 −1 79.2±0.10 13 0 1 −1 82.7±0.20 14 1 1 0 77.4±0.36 15 −1 1 0 78.3±0.17 16 0 0 0 87.6±0.30 17 0 0 0 87.9±0.10 表 7 回归模型方差分析
Table 7 Variance analysis of regression model
方差来源 平方和 自由度 均方 F值 P值 显著性 模型 341.23 9 37.91 51.93 < 0.0001 ** A 13.26 1 13.26 18.16 0.0037 ** B 14.31 1 14.31 19.60 0.0031 ** C 18.60 1 18.60 25.48 0.0015 ** AB 4.41 1 4.41 6.04 0.0436 * AC 12.60 1 12.60 17.26 0.0043 ** BC 0.42 1 0.42 0.58 0.4717 A2 173.00 1 173.00 236.97 < 0.0001 ** B2 78.22 1 78.22 107.13 < 0.0001 ** C2 5.91 1 5.91 8.10 0.0248 * 残差 5.11 7 0.73 失拟项 3.80 3 1.27 3.88 0.1118 不显著 纯误差 1.31 4 0.33 总和 346.34 16 R2=0.9852 R²adj=0.9663 注:“*”表示对结果影响差异显著(P<0.05);“**”表示对结果影响差异极显著(P<0.01)。 -
[1] 杨新, 陈莉, 卢红梅, 等. 茶多酚提取与纯化方法及其功能活性研究进展[J]. 食品工业科技,2019,40(5):322−328, 332. [YANG Xin, CHEN Li, LU Hongmei, et al. Research progress on extraction and purification methods of tea polyphenols and its functional activities[J]. Science and Technology of Food Industry,2019,40(5):322−328, 332. YANG Xin, CHEN Li, LU Hongmei, et al. Research progress on extraction and purification methods of tea polyphenols and its functional activities[J]. Science and Technology of Food Industry, 2019, 40(5): 322-328, 332.
[2] 丁东晴, 申懿玲, 杜晶, 等. 黑茶多酚提取工艺及对鲜切苹果品质影响[J]. 粮食与油脂,2022,35(4):129−134. [DING Dongqing, SHEN Yiling, DU Jing, et al. Effects of extraction technology of dark tea polyphenols on quality of fresh-cut apple[J]. Cereals and Oils,2022,35(4):129−134. doi: 10.3969/j.issn.1008-9578.2022.04.032 DING Dongqing, SHEN Yiling, DU Jing, et al. Effects of extraction technology of dark tea polyphenols on quality of fresh-cut apple[J]. Cereals and Oils, 2022, 35(4): 129-134. doi: 10.3969/j.issn.1008-9578.2022.04.032
[3] 洪思慧, 张涛麟. 茶多酚提取专利技术综述[J]. 江西化工,2021,37(3):69−72. [HONG Sihui, ZHANG Taolin. Review of patented technology of tea polyphenol extraction[J]. Jiangxi Chemical Industry,2021,37(3):69−72. doi: 10.3969/j.issn.1008-3103.2021.03.020 HONG Sihui, ZHANG Taolin. Review of patented technology of tea polyphenol extraction[J]. Jiangxi Chemical Industry, 2021, 37(3): 69-72. doi: 10.3969/j.issn.1008-3103.2021.03.020
[4] ZHANG Yuting, CHENG Lu, LIU Yanan, et al. Omics analyses of intestinal microbiota and hypothalamus clock genes in circadian disturbance model mice fed with green tea polyphenols[J]. Journal of Agricultural and Food Chemistry,2022,70(6):1890−1901. doi: 10.1021/acs.jafc.1c07594
[5] LUO Yue, ZHANG Jianan, TANG Hochi, et al. Management of Maillard reaction-derived reactive carbonyl species and advanced glycation end products by tea and tea polyphenols[J]. Food Science and Human Wellness,2022,11(3):557−567. doi: 10.1016/j.fshw.2021.12.012
[6] HONG Mengyu, CHENG Lu, LIU Yanan, et al. A natural plant source-tea polyphenols, a potential drug for improving immunity and combating virus[J]. Nutrients,2022,14(3):550−565. doi: 10.3390/nu14030550
[7] TRUONG V, JEONG W. Antioxidant and anti-inflammatory roles of tea polyphenols in inflammatory bowel diseases[J]. Food Science and Human Wellness,2022,11(3):502−511. doi: 10.1016/j.fshw.2021.12.008
[8] 高海荣, 王亚鑫, 谢晨, 等. XDA-5大孔树脂分离茶叶中茶多酚工艺优化[J]. 中国食品添加剂,2019,30(11):67−72. [GAO Hairong, WANG Yaxin, XIE Chen, et al. Optimization of separation for tea polyphenols by XDA-5 macroporous resin[J]. China Food Additives,2019,30(11):67−72. GAO Hairong, WANG Yaxin, XIE Chen, et al. Optimization of separation for tea polyphenols by XDA-5 macroporous resin[J]. China Food Additives, 2019, 30(11): 67-72.
[9] 吴婕, 宫江宁. 大孔树脂纯化甜茶多酚及其对α-葡萄糖苷酶抑制活性和DPPH·抗氧化性的研究[J]. 中国农业科技导报,2021,23(6):113−119. [WU Jie, GONG Jiangning. Purification of polyphenols from sweet tea by the microporous resins and its inhibitory activity on α-glucosidase and DPPH·[J]. Journal of Agricultural Science and Technology,2021,23(6):113−119. WU Jie, GONG Jiangning. Purification of polyphenols from sweet tea by the microporous resins and its inhibitory activity on α-glucosidase and DPPH·[J]. Journal of Agricultural Science and Technology, 2021, 23(6): 113-119.
[10] 曹雪文. 大孔树脂对茶多酚提取纯化及茶多酚抗氧化性能研究[D]. 赣州: 江西理工大学, 2020 CAO Xuewen. Study on the extraction and purification of tea polyphenols by macroporous resin and the antioxidant properties of tea polyphenols[D]. Ganzhou: Jiangxi University of Science and Technology, 2020.
[11] 欧淑琼, 唐倩, 李媛, 等. 茶树花中多酚浸提工艺的优化研究[J]. 茶叶通讯,2020,47(3):467−471. [OU Shuqiong, TANG Qian, LI Yuan, et al. Optimization of the extraction process of polyphenols from tea flower[J]. Journal of Tea Communication,2020,47(3):467−471. OU Shuqiong, TANG Qian, LI Yuan, et al. Optimization of the extraction process of polyphenols from tea flower[J]. Journal of Tea Communication, 2020, 47(3): 467-471.
[12] 蓝梧涛. 油茶叶多酚提取纯化及稳定性、抗氧化活性的研究[D]. 广州: 华南农业大学, 2019 LAN Wutao. Study on extraction, purification, stability and antioxidant activity of polyphenols from Camellia oleifera[D]. Guangzhou: South China Agricultural University, 2019.
[13] 张沛, 吴楠, 宋志军, 等. 响应面法优化大孔树脂纯化黄芪毛蕊异黄酮工艺[J]. 食品工业科技,2021,42(10):209−214. [ZHANG Pei, WU Nan, SONG Zhijun, et al. Purification of calycosin from Astragalus membranceus with macroporous resins by response surface analysis[J]. Science and Technology of Food Industry,2021,42(10):209−214. ZHANG Pei, WU Nan, SONG Zhijun, et al. Purification of calycosin from Astragalus membranceus with macroporous resins by response surface analysis[J]. Science and Technology of Food Industry, 2021, 42(10): 209-214.
[14] BAI Y D, MA J, ZHU W F, et al. Highly selective separation and purification of chicoric acid from echinacea purpurea by quality control methods in macroporous adsorption resin column chromatography[J]. J Sep Sci,2019,42(5):1027−1036.
[15] ZHANG L, ZHENG D, ZHANG Q F. Purification of total flavonoids from Rhizoma Smilacis Glabrae through cyclodextrin-assisted extraction and resin adsorption[J]. Food Sci Nutr,2019,7(2):449−456. doi: 10.1002/fsn3.809
[16] 沈志伟, 方芳, 龚云麒, 等. 以曲札茋苷为评价指标的大孔树脂再生工艺优化[J]. 中国民族民间医药,2019,28(8):45−48. [SHEN Zhiwei, FANG Fan, GONG Yunqi, et al. Optimization of regeneration process of macroporous resin with Quzhazhigan as evaluation index[J]. Chinese Journal of Ethnomedicine and Ethnopharmacy,2019,28(8):45−48. doi: 10.3969/j.issn.1007-8517.2019.8.zgmzmjyyzz201908013 SHENG Zhiwei, FANG Fan, GONG Yunqi, et al. Optimization of regeneration process of macroporous resin with Quzhazhigan as evaluation index[J]. Chinese Journal of Ethnomedicine and Ethnopharmacy, 2019, 28(8): 45-48. doi: 10.3969/j.issn.1007-8517.2019.8.zgmzmjyyzz201908013
[17] 田富林, 黄文晶, 张驰, 等. HPD600型大孔树脂纯化麦麸多酚及其抗氧化活性和定性分析[J]. 食品与机械,2022,38(5):173−178,242. [TIAN Fulin, HUANG Wenjing, ZHANG Chi, et al. Antioxidant activity and qualitative analysis of wheat bran polyphenols purified using HPD600 macroporous resin[J]. Food and Machinery,2022,38(5):173−178,242. TIAN Fulin, HUANG Wenjing, ZHANG Chi, et al. Antioxidant activity and qualitative analysis of wheat bran polyphenols purified using HPD600 macroporous resin[J]. Food and Machinery, 2022, 38(5): 173-178, 242.
[18] FATIHA E B, CLOTILDE N, LI L, et al. A new colorimetric DPPH radical scavenging activity method: Comparison with spectrophotometric assay in some medicinal plants used in moroccan pharmacopoeia[J]. Pharmaceutical Fronts,2022,4(2):89−102.
[19] 谢雨寻, 叶有明, 李龙越, 等. 茶酒糟中茶多酚提取工艺优化及其抗氧化活性的研究[J]. 中国酿造,2022,41(2):204−209. [XIE Yuxun, YE Youming, LI Longyue, et al. Optimization of extraction process and antioxidant activity of tea polyphenols from tea distiller's grains[J]. China Brewing,2022,41(2):204−209. XIE Yuxun, YE Youming, LI Longyue, et al. Optimization of extraction process and antioxidant activity of tea polyphenols from tea distiller's grains[J]. China Brewing, 2022, 41(2): 204-209.
[20] 沈嘉森, 苏永昌, 陈晓婷, 等. 龙须菜ACE抑制肽的体外稳定性和抗氧化活性研究[J]. 食品工业科技,2022,43(7):384−392. [SHEN Jiasen, SU Yongchang, CHEN Xiaoting, et al. Study on in vitro stability and antioxidant activity of ACE inhibitory peptide from Gracilaria lemaneiformis[J]. Science and Technology of Food Industry,2022,43(7):384−392. SHEN Jiasen, SU Yongchang, CHEN Xiaoting, et al. Study on in vitro stability and antioxidant activity of ACE inhibitory peptide from Gracilaria lemaneiformis[J]. Science and Technology of Food Industry, 2022, 43(7): 384-392.
[21] 陈荣义. 茶多酚的提取纯化及其改性的研究[D]. 成都: 四川大学, 2005 CHEN Rongyi. Study on extraction, purification and modification of tea polyphenols[D]. Chengdu: Sichuan University, 2005.
[22] 马荣锴. 大孔树脂纯化菥蓂水提物黄酮的研究[D]. 南宁: 广西大学, 2012 MA Rongkai. Study on the purification of flavonoids from water extract of molaria by microporous resin[D]. Nanning: Guangxi University, 2012.
[23] KALAM S, ABUKHAMSIN S A, KAMAL M S, et al. Surfactant adsorption isotherms: A review[J]. ACS Omega,2021,6(48):32342−32348. doi: 10.1021/acsomega.1c04661
[24] HU W Z, HOU M Y, FENG K. Adsorption kinetics and isotherms of flavonoids from Pteris esquiroliion macroporous resin[J]. Indian Journal of Pharmaceutical Sciences,2019,81(1):S9−S10.
[25] 邢俊红. 花生壳多酚的提取工艺及活性研究[D]. 大连: 大连工业大学, 2015 XING Junhong. Study on the extraction technology and activity of polyphenols from peanut shells[D]. Dalian: Dalian Polytechnic University, 2015.
[26] 任晓婷. 猕猴桃皮渣多酚提取、纯化及其成分分析[D]. 太原: 山西大学, 2017 REN Xiaoting. Kiwi peel residue polyphenol extraction, purification, and component analysis[D]. Taiyuan: Shanxi University, 2017.
[27] 王力. 适合工业化制备茶叶儿茶素EGCG的方法及提高EGCG生物利用度的研究[D]. 无锡: 江南大学, 2021 WANG Li. A method suitable for industrial preparation of tea catechin EGCG and study on improving the bioavailability of EGCG[D]. Wuxi: Jiangnan University, 2021.
[28] 高凝轩. 黑果腺肋花楸多酚提取纯化工艺及其抗氧化活性与稳定性研究[D]. 沈阳: 沈阳农业大学, 2017 GAO Ningxuan. Study on the extraction and purification process of polyphenols from rowan nigra and study on their antioxidant activity and stability[D]. Shenyang: Shenyang Agricultural University, 2017.
[29] 高婷. 葡多酚的提取、纯化工艺及抗氧化性研究[D]. 长沙: 中南大学, 2013 GAO Ting. Extraction and purification process and antioxidant study of gluc polyphenols[D]. Changsha: Central South University, 2013.
[30] 陈琳. EGCG制备及其对小麦淀粉糊化和回生性质的影响研究[D]. 杭州: 浙江大学, 2018 CHEN Lin. Preparation of EGCG and its effect on gelatinization and retrogradation of wheat starch[D]. Hangzhou: Zhejiang University, 2018.
[31] 李洋. 微波—超声耦合双水相提取、树脂纯化茶多酚工艺研究[D]. 赣州: 江西理工大学, 2018 LI Yang. Study on microwave-ultrasonic coupled aqueous phase extraction and resin purification of tea polyphenols[D]. Ganzhou: Jiangxi University of Science and Technology, 2018.
[32] 巫永华, 刘恩岐, 张建萍, 等. 山楂叶多酚的纯化及其抗氧化特性与组分分析[J]. 食品与发酵工业,2020,46(2):165−172. [WU Yonghua, LIU Enqi, ZHANG Jianping, et al. Purification, antioxidant capacity and component analysis of hawthoen leaf polyphenols[J]. Food and Fermentation Industries,2020,46(2):165−172. WU Yonghua, LIU Enqi, ZHANG Jianping, et al. Purification, antioxidant capacity and component analysis of hawthoen leaf polyphenols[J]. Food and Fermentation Industries, 2020, 46(2): 165-172.
[33] 张琪. 绿茶中茶多酚的提取分离及其对慢性胃炎大鼠胃粘膜的保护作用[D]. 西安: 陕西师范大学, 2015 ZHANG Qi. Extraction and isolation of tea polyphenols in green tea and their protective effect on gastric mucosa in rats with chronic gastritis[D]. Xian: Shaanxi Normal University, 2015.
[34] 郭雷, 郭家才, 郑洪伟. 花果山云雾茶中多酚和多糖的超声同步提取工艺[J]. 食品研究与开发,2017,38(16):33−39. [GUO Lei, GUO Jiacai, ZHENG Hongwei. Ultrasonic-assisted synchronous extraction process of tea polyphenols and polysaccharides from Huaguoshan Yunwu tea[J]. Food Research and Development,2017,38(16):33−39. doi: 10.3969/j.issn.1005-6521.2017.16.008 GUO Lei, GUO Jiacai, ZHENG Hongwei. Ultrasonic-assisted synchronous extraction process of tea polyphenols and polysaccharides from Huaguoshan Yunwu tea[J]. Food Research and Development, 2017, 38(16): 33-39. doi: 10.3969/j.issn.1005-6521.2017.16.008
[35] BOUCHEFFA S, SOBHI W, ATTOUI A, et al. Effect of the main constituents of Pistacia lentiscus leaves against the DPPH radical and xanthine oxidase: Experimental and theoretical study[J]. Journal of Biomolecular Structure and Dynamics,2021,39:11−15.
[36] 喻铭佳, 索化夷. 巫山茶多酚提取物体外抗氧化活性研究[J]. 食品安全质量检测学报,2021,12(14):5822−5827. [YU Mingjia, SUO Huayi. Study on the in vitro antioxidant activity of the Wushan tea polyphenol extract[J]. Journal of Food Safety and Quality,2021,12(14):5822−5827. YU Mingjia, SUO Huayi. Study on the in vitro antioxidant activity of the Wushan tea polyphenol extract[J]. Journal of Food Safety and Quality, 2021, 12(14): 5822-5827.
[37] JAGDEO J, KURTTI A, HERNANDEZ S, et al. Novel vitamin C and E and green tea polyphenols combination serum improves photoaged facial skin[J]. Journal of Drugs in Dermatology,2021,20(9):996−1003. doi: 10.36849/JDD.5818
[38] YIN Zhiya, ZHENG Ting, HO Chitang, et al. Improving the stability and bioavailability of tea polyphenols by encapsulations: A review[J]. Food Science and Human Wellness,2022,11(3):537−556. doi: 10.1016/j.fshw.2021.12.011
-
期刊类型引用(2)
1. 顾丹丹,董雪,张金秀,王晓茹,赵宗硕,王立安. 小麦羊肚菌菌粮制备工艺优化及营养成分、理化性质和抗氧化活性分析. 食品工业科技. 2025(04): 237-245 .  本站查看
本站查看
2. 马莉,季爱兵,曾胤,严亮. 蘑菇多糖生物活性及提取研究进展. 热带农业科学. 2024(06): 123-130 .  百度学术
百度学术
其他类型引用(1)










 下载:
下载:



 下载:
下载:
