Optimization of Extraction Process of Polysaccharides from Hovenia dulcis Fruit Pedicels and Its Antioxidant Activity
-
摘要: 为获得枳椇果梗多糖,并进一步评价其自由基清除及抑制生物大分子(蛋白质、脂质、DNA)氧化的能力。以枳椇果梗为试验材料,在单因素实验的基础上,结合正交试验及方差分析优化枳椇果梗多糖热水提取工艺条件;对所提多糖清除DPPH、ABTS+自由基能力进行测定;并利用Cu2+/H2O2、FeSO4、APPH分别诱导牛血清蛋白、亚油酸、鲱鱼精子DNA氧化,构建体外蛋白质、脂质、DNA氧化模型,对所提多糖体外抑制生物大分子氧化能力进行评价。结果表明:醇沉体积分数对枳椇果梗多糖的得率有显著性(P<0.05)的影响,最佳的热水提取工艺条件为:料液比1:25 g/mL,提取温度85 ℃,提取时间1 h,醇沉体积分数80%,此时多糖得率为3.06%±0.181%;且随着浓度的增大,所提多糖对自由基的清除和生物大分子的氧化抑制效果也逐渐提高,对DPPH自由基、ABTS+自由基清除IC50分别为1.687、1.824 mg/mL,对牛血清蛋白羰基化、亚油酸过氧化和鲱鱼精子DNA氧化抑制IC50分别为:13.84、10.88、74.70 mg/mL。研究结果可为枳椇果梗多糖的提取及在功能性食品中的应用提供参考。Abstract: The aim of this study was to obtain polysaccharides from Hovenia dulcis fruit pedicels, and further evaluate its ability to scavenge free radicals and inhibit the oxidation of biological macromolecules (proteins, lipids, DNA). On the basis of a single-factor experiment, the hot water extraction process of polysaccharides from Hovenia dulcis fruit pedicels was optimized using orthogonal test combined with an analysis of variance. The ability of the extracted polysaccharides to scavenge DPPH and ABTS+ free radicals was determined. In addition, Cu2+/H2O2, FeSO4 and APPH were used to induce the oxidation of bovine serum albumin, linoleic acid and herring sperm DNA, respectively, to construct in vitro protein, lipid and DNA oxidation models and the ability of the extracted polysaccharides to inhibit biological macromolecule oxidation in vitro was evaluated. The results showed that the volume fraction of ethanol precipitation had a significant effect on the yield of polysaccharides from Hovenia dulcis fruit pedicels (P<0.05). The optimal hot water extraction conditions were as follows: solid-liquid ratio, 1:25 g/mL, extraction temperature 85 ℃, extraction time 1 h, ethanol precipitation volume fraction 80%, with the polysaccharide yield of 3.06%±0.181%. With the increase in the concentration, the effects of the extracted polysaccharides in scavenging free radicals and inhibiting the oxidation of biological macromolecules were gradually improved. The IC50 for scavenging DPPH and ABTS+ free radicals were 1.687 and 1.824 mg/mL, and the IC50 for inhibiting bovine serum albumin carbonylation, linoleic acid peroxidation and herring sperm DNA oxidation were 13.84, 10.88 and 74.70 mg/mL, respectively. The results can provide a reference for the extraction of polysaccharides from Hovenia dulcis fruit pedicels and its application in functional food.
-
机体代谢过程会产生大量的自由基,正常情况下体内自由基的产生和清除处于动态平衡的过程中。但异常情况下自由基的产生会超过机体代偿能力,引起大量自由基积累,体内氧化还原平衡被打破,过量的自由基会进一步破坏蛋白质、脂质、核酸等生物大分子最终导致机体损伤和疾病[1-3]。多糖是一种由酮糖或醛糖通过糖苷键连接形成天然大分子聚合物,具有多种生物活性,例如:抗氧化、抗炎、保肝护肝、免疫调节、抗肿瘤等[4-7]。与化学合成的抗氧化剂相比,天然多糖一般具有良好的生物相容性、生物降解性和无毒性等优点[8]。因此,从可食用的自然资源中开发利用具有抗氧化能力的多糖具有重要意义。
枳椇(Hovenia dulcis)又称拐枣、万寿果、甜半夜,属于鼠李科枳椇属,传统医学认为枳椇性甘、酸,味平,归心、脾经,具解酒毒,止渴除烦,止呕,利二便的功效[9-10]。占枳椇果实90%总重的果梗(可食用肉质部分)肉质肥厚、外形扭曲、口味独特,总糖含量可达19.4%~28.3%,并富含多种其他营养成分,利用前景可观[11-12]。我国枳椇资源丰富,尤其在西南地区有着广泛的分布。枳椇果梗目前主要被鲜食或简单粗加工制作果汁、果酒、果醋等产品,综合开发利用率低。因此,作为枳椇果梗最主要的营养成分,枳椇果梗多糖的提取和抗氧化性研究对于枳椇果梗的利用尤为重要。
目前植物多糖的提取还是以水提法、超声辅助法、微波辅助法为主,虽然也不断地有新兴提取工艺出现并取得了一定的效果,但每一种方法也都存在一定的局限性,例如:设备昂贵、操作复杂,条件不易控制等[13-14]。植物多糖水溶性大,通过水提法进行多糖的提取,提取过程简单,不需要特殊设备且条件易于控制,该方法更适合大量多糖样品生产制备[15],而对于枳椇多糖的提取还主要集中于枳椇子,果梗多糖的提取研究还相对较少。同时,对于植物多糖的抗氧化性评价主要还是集中于自由基清除能力[16-17],而涉及“氧化应激”下游生物大分子损伤的抑制作用还鲜有报道。
因此,本文以枳椇果梗为研究对象,对枳椇果梗多糖的水提取工艺条件进行优化;并对其清除DPPH、ABTS+自由基能力及体外抑制生物大分子(蛋白质、脂质、DNA)氧化能力进行评价,旨在为枳椇果梗多糖的开发利用提供理论依据,为进一步扩展枳椇果梗资源在功能性食品领域的应用提供参考。
1. 材料与方法
1.1 材料与仪器
新鲜枳椇 购于遵义市官仓镇;无水乙醇、石油醚、苯酚、浓硫酸、葡萄糖、三氯甲烷、正丁醇、CuSO4、30% H2O2、FeSO4、亚油酸、维生素C(VC) 均为分析纯,国药集团化学试剂有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-trinitrophenylhydrazine,DPPH)、2,2-联氮-二(3-乙基-苯并噻唑-6-磺酸)二铵盐(2,2-azo-di (3-ethyl-benzothiazol-6-sulfonic acid) diammonium salt,ABTS)、牛血清蛋白(bovine serum protein,BSA)、鲱鱼精DNA(herring sperm DNA,hsDNA)、2,2-偶氮二异丁基脒二盐酸盐(2,2-azo diisobutyl amidine dihydrochloride,AAPH)、2,4-二硝基苯肼(2,4-Dinitrophenylhydrazine,DNPH) 美国Sigma-Aldrich公司;丙二醛(malonaldehyde,MDA)含量检测试剂盒 南京建成生物工程研究所;8-羟基脱氧鸟苷(8-hydroxydeoxyguanosine,8-OHdG)检测试剂盒 美国eBioscience公司。
TDZ5-WS离心机 长沙湘仪离心仪器有限公司;RE-52AA旋转蒸发仪 北京科伟永兴仪器有限公司;BGG-9140A电热鼓风干燥箱 上海一恒科学仪器有限公司;1530酶标仪 赛默飞世尔科技(中国)有限公司。
1.2 实验方法
1.2.1 枳椇预处理
将新鲜枳椇去除枝条、枳椇子,流水去除表面杂质,沥干水分,置于60 ℃热风干燥箱中干燥72 h,随后使用粉碎机制备粉末,60目过筛收集枳椇果梗粉末,阴凉处保存备用。称取一定量的枳椇果梗粉末于索氏提取中,按料液比1:8(g/mL)加入石油醚回流脱脂(70 ℃,4 h),回流结束后抽滤,残渣在50 ℃下烘干至恒重,置于干燥器中保存备用[18]。
1.2.2 枳椇果梗多糖提取物的制备
取预处理后的枳椇果梗干粉置于圆底烧瓶中,按照一定的料液比、提取时间、提取温度,进行热水回流提取;提取后4000 r/min离心20 min收集上清液,离心管底部粉末按上述流程再重复提取一次,混合两次提取的上清液;用旋转蒸发仪浓缩至初始体积的1/4,向浓缩液中按一定的醇沉体积分数加入无水乙醇,搅拌均匀后4 ℃醇沉过夜。过夜后5000 r/min离心15 min收集沉淀,沉淀加入适量蒸馏水复溶,冷冻干燥后得到枳椇果梗多糖提取物,称重记录重量。
1.2.3 单因素实验
以蒸馏水为提取溶剂:a.按料液比1:25 g/mL分别于75、80、85、90、95 ℃下浸提2 h,在醇沉体积分数80%的条件下进行沉淀;b.按料液比1:25 g/mL于95 ℃下分别浸提0.5、1、1.5、2、2.5 h,在醇沉体积分数80%的条件下进行沉淀;c.分别按料液比1:20、1:25、1:30、1:35、1:40 g/mL于95 ℃下浸提2 h,在醇沉体积分数80%的条件下进行沉淀;d.按料液比1:25 g/mL于95 ℃下浸提2 h,分别在醇沉体积分数50%、60%、70%、80%、90%的条件下进行沉淀;以枳椇果梗多糖得率为评价指标,考察提取温度、提取时间、料液比、醇沉体积分数对枳椇果梗多糖得率的影响。
1.2.4 正交试验
按照L9(34)正交表设计,以枳椇果梗多糖得率为评价指标,以提取温度、提取时间、料液比、醇沉体积分数为因素,每个因素设置3个水平进行正交试验,因素水平见表1。
表 1 正交试验因素水平表Table 1. Orthogonal test factor level table水平 A 提取温度(℃) B 提取时间(h) C 料液比(g/mL) D 醇沉体积分数(%) 1 85 1 1:25 60 2 90 1.5 1:30 70 3 95 2 1:35 80 1.2.5 葡萄糖标准曲线的制作及多糖得率的测定
参考文献方法[18],采用苯酚-硫酸法制作葡萄糖标准曲线并测定枳椇果梗多糖提取物中多糖的含量,所得标准曲线线性回归方程:y=7.9479x−0.0002,决定系数R2=0.9953。将所得枳椇果梗多糖提取物用蒸馏水配制成1 mg/mL的待测液,依据葡萄糖标准曲线计算待测液中多糖浓度,计算多糖得率。
(1) 式中:W:枳椇果梗多糖得率,%;C:依据葡萄糖标准曲线计算待测液中多糖浓度,μg/mL;V:枳椇果梗多糖提取物待测液体积,mL;m:提取所用枳椇果梗干粉质量,g。
1.2.6 枳椇果梗多糖样品的制备
取枳椇果梗干粉,按照正交优化试验所得的最佳提取工艺条件进行多糖提取,获得枳椇果梗多糖提取物,将提取物复溶于水中,采用Sevage法去除蛋白质[19],脱蛋白后的溶液置于透析袋(8000~14000 Da)自来水透析48 h,蒸馏水透析24 h,每隔12 h换液,真空冷冻干燥得到枳椇果梗精制多糖供后续抗氧化活性检测使用。
1.2.7 枳椇果梗多糖清除自由基能力测定
DPPH自由基清除能力参考文献方法进行测定[20],1 mL 0.5、1、1.5、2、2.5、3、3.5、4 mg/mL枳椇果梗多糖(阳性对照为不同浓度的VC)与1.25 mL DPPH溶液(100 μmol/L)室温避光反应0.5 h,517 nm测定吸光度。
(2) 式中:A0:加水后DPPH溶液的吸光值,A1:枳椇果梗多糖加DPPH溶液的吸光值,A2:枳椇果梗多糖加水的吸光值。
ABTS+自由基清除能力参考文献方法进行测定[20],0.1 mL 0.5、1、1.5、2、2.5、3、3.5、4 mg/mL枳椇果梗多糖(阳性对照为不同浓度的VC)与2 mL ABTS(7 mol/L)避光反应6 min,734 nm测定吸光度。
(3) 式中:A0:加水后ABTS溶液的吸光值,A1:枳椇果梗多糖加ABTS溶液的吸光值,A2:枳椇果梗多糖加水的吸光值。
1.2.8 枳椇果梗多糖对蛋白质羰基化的影响
取200 mg BSA,分别加入10 mL 2.5、5、10、20、40 mg/mL枳椇果梗多糖溶液,混合均匀后依次加入6.4 mg CuSO4、1.133 g 30% H2O2溶液,混合均匀后加入蒸馏水,使最终反应体系总体积为100 mL,置于37 ℃水浴反应,反应时间为90 min,采用DNPH法检测BSA羰基含量[21]。
(4) 式中:A0:空白对照组羰基含量(BSA),A1:诱导组羰基含量(BSA+CuSO4+H2O2),A2:氧化抑制组羰基含量(BSA+CuSO4+H2O2+不同浓度多糖)。
1.2.9 枳椇果梗多糖对亚油酸氧化的影响
取28 mg亚油酸,分别加入10 mL 2.5、5、10、20、40 mg/mL枳椇果梗多糖溶液,混合均匀后加入1.52 mg FeSO4,混合均匀后加入蒸馏水,使最终反应体系总体积为100 mL,置于37 ℃水浴避光反应24 h,以MDA含量表示亚油酸脂质氧化水平,采用MDA试剂盒测定样品中MDA含量[21-22]。
(5) 式中:B0:空白对照组MDA含量(亚油酸),B1:诱导组MDA含量(亚油酸+FeSO4),B2:氧化抑制组MDA含量(亚油酸+FeSO4+不同浓度多糖)。
1.2.10 枳椇果梗多糖对DNA氧化的影响
取200 mg hsDNA,分别加入10 mL 2.5、5、10、20、40 mg/mL枳椇果梗多糖溶液,混合均匀后加入1.084 g AAPH,混合均匀后加入蒸馏水,使最终反应体系总体积为 100 mL,置于 37 ℃ 水浴反应 12 h,采用 8-OH-dG检测试剂盒测定样品中8-OH-dG含量[23]。
(6) 式中:C0:空白对照组8-OH-dG含量(hsDNA),C1:诱导组8-OH-dG含量(hsDNA+AAPH),C2:氧化抑制组8-OH-dG含量(hsDNA+AAPH+不同浓度多糖)。
1.3 数据处理
采用SPSS 13.0(SPSS,美国)进行正交试验设计,采用单因素方差分析(ANOVA)结合Duncan检验分析差异性,差异显著水平为P<0.05,数据统计图使用GraphPad Prism 8.0(San Diego,美国)生成。
2. 结果与分析
2.1 单因素实验结果
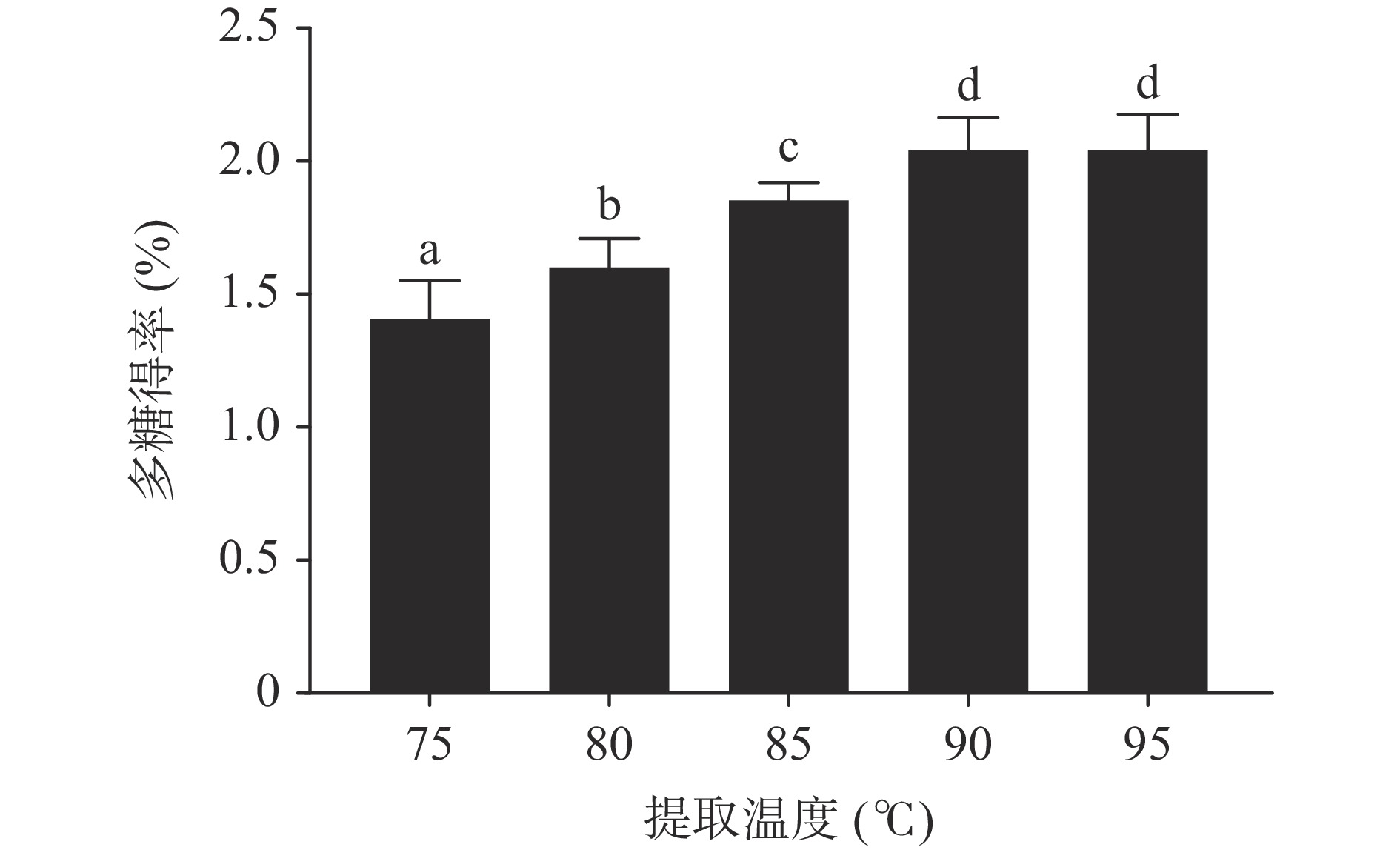
2.1.1 提取温度对枳椇果梗多糖得率的影响
由图1可知,枳椇果梗多糖得率在一定温度范围内随着提取温度的提高而逐渐增大,当温度达到90 ℃时多糖得率最高,继续提高提取温度到95 ℃,多糖得率与90 ℃相比没有显著性变化(P>0.05)。随着提取温度的升高,多糖的溶解度会逐渐增大,但是当温度过高可能会引起多糖链断裂,导致多糖难回收[24],因此虽然提取温度升高至95 ℃,多糖溶解度增大,但是得率并未显著增加,但与85 ℃相比得率有显著性提高(P<0.05),因此选择85、90、95 ℃作为正交试验提取温度的3个水平。
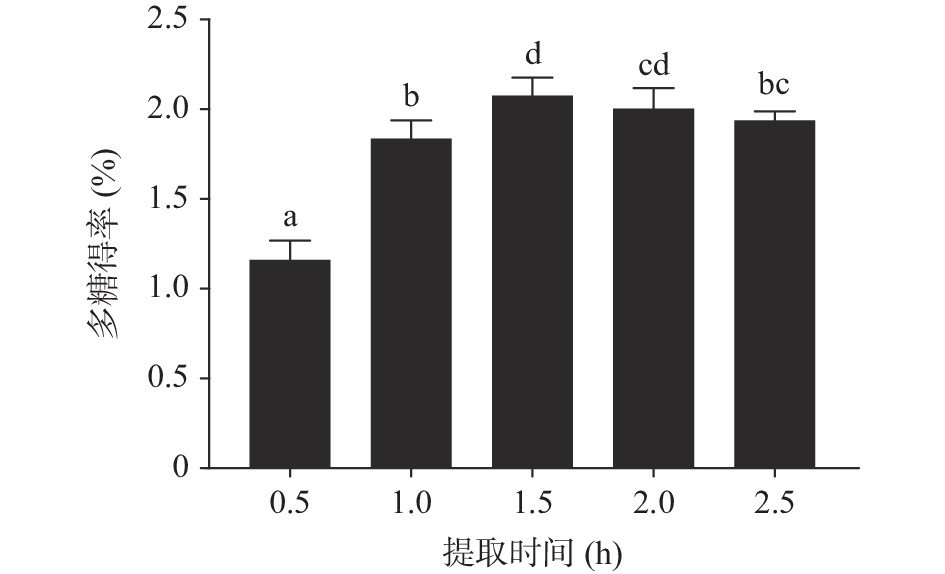
2.1.2 提取时间对枳椇果梗多糖得率的影响
由图2可知,枳椇果梗多糖得率随着提取时间的增加而先增加后减少,当时间达到1.5 h时多糖得率最高,继续延长提取时间至2 h,多糖得率与1.5 h相比并没有显著性变化(P>0.05),当提取时间延长至2.5 h后多糖得率与1.5 h相比出现了显著性的下降(P<0.05)。在一定的时间范围内随着提取时间的延长虽然可以使得更多的多糖溶解释放,但是如果在高温提取环境中长时间提取,可能会发生多糖的降解,导致得率下降,另外还可能导致多糖中杂质过多[25]。因此选择1、1.5、2 h作为正交试验提取时间的3个水平。
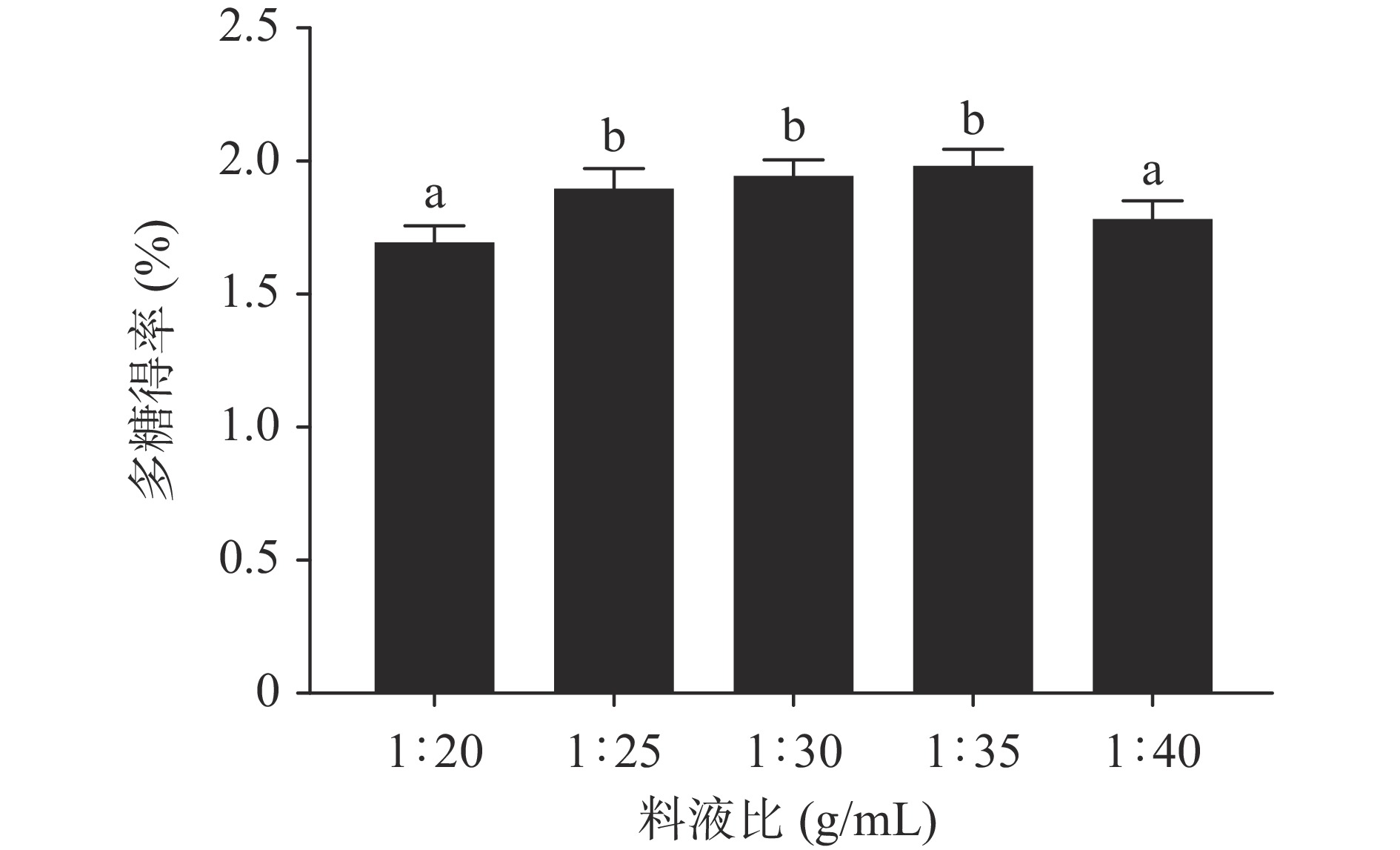
2.1.3 料液比对枳椇果梗多糖得率的影响
由图3可知,枳椇果梗多糖得率随着料液比的增大呈现出先增加后降低的趋势,当料液比为1:35 g/mL时多糖得率最高,且与料液比为1:25、1:30 g/mL相比并未出现显著性差异(P>0.05),说明在料液比1:25~1:35 g/mL的范围,多糖得率高。但当料液比增大到1:40 g/mL,得率与1:35 g/mL相比出现了显著性的下降(P<0.05)。料液比的增大虽然可以增大溶剂与枳椇果梗粉末的接触进而促进多糖的溶出,但是当料液比过大后,溶质接触面已经达到饱和,多糖的溶出提升可能并不明显,由于溶液过多产生的稀释效应同时又可能导致提取效率下降[26]。由于最高多糖得率出现的范围为料液比1:25~1:35 g/mL,因此选择1:25、1:30、1:35 g/mL作为正交试验料液比的3个水平。
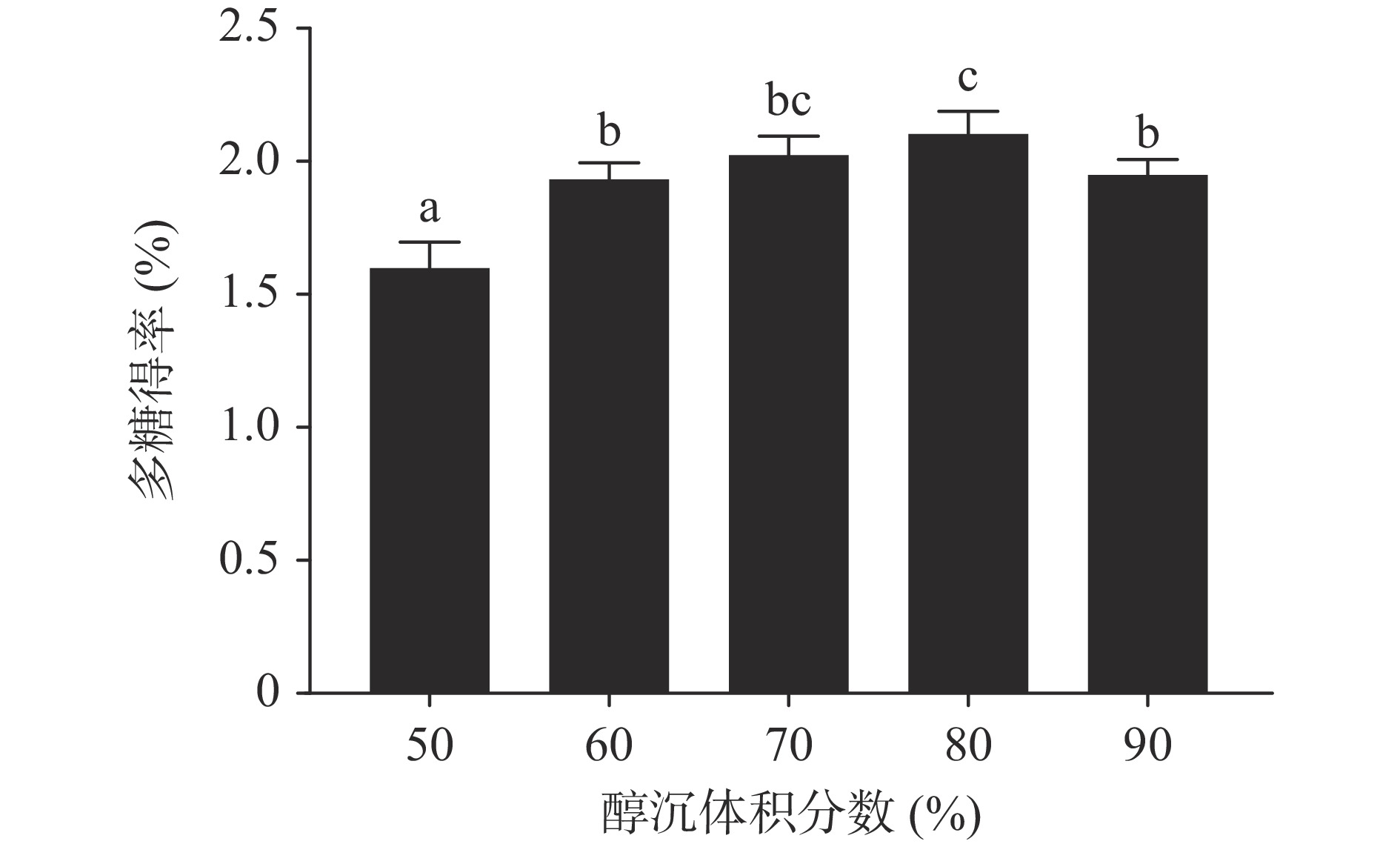
2.1.4 醇沉体积分数对枳椇果梗多糖得率的影响
由图4可知,枳椇果梗多糖得率随着醇沉体积分数的增大呈现出先增加后降低的趋势,当体积分数为80%时多糖得率最高,且与体积分数为70%相比并未出现显著性差异(P>0.05)。但当体积分数增大到90%,得率与80%相比出现了显著性的下降(P<0.05),与60%相比并无显著性差异(P>0.05)。乙醇可以通过降低水溶液的介电常数使多糖脱水从而产生沉淀来分离多糖,但当乙醇浓度过大时析出的主要是小分子糖类[27],而在本文中体积分数60%和90%时的多糖得率无显著性差异(P>0.05),因此综合考虑多糖得率和乙醇消耗,选择60%、70%、80%作为正交试验醇沉体积分数的3个水平。
2.2 正交试验结果
根据以上单因素实验结果,选择提取温度、提取时间、料液比、醇沉体积分数4个影响枳椇果梗多糖提取工艺的因素,以多糖得率作研究指标,设计L9(34)正交试验。通过直观分析(表2)极差R可判断所选择的4个因素对枳椇果梗多糖得率影响的大小顺序为:D(醇沉体积分数)>A(提取温度)>C(料液比)>B(提取时间),方差分析结果表明(表3),因素D(醇沉体积分数)具有显著性差异(P<0.05),说明醇沉体积分数的不同水平对多糖得率有显著性影响。
表 2 正交试验设计与结果Table 2. Design and results of orthogonal test试验号 因素 多糖得率(%) A B C D 1 1 1 1 1 1.36 2 1 2 2 2 1.31 3 1 3 3 3 2.56 4 2 1 2 3 2.70 5 2 2 3 1 1.07 6 2 3 1 2 1.54 7 3 1 3 2 1.57 8 3 2 1 3 2.91 9 3 3 2 1 1.57 K1 1.743 1.877 1.937 1.333 K2 1.770 1.763 1.860 1.473 K3 2.017 1.890 1.733 2.723 极差R 0.274 0.127 0.204 1.390 表 3 正交试验方差分析Table 3. Variance analysis of orthogonal test因素 偏差平方和 自由度 F比 F临界值 P值 显著性 A 0.136 2 4.690 19.000 0.183 B 0.029 2 1.000 19.000 0.039 C 0.063 2 2.172 19.000 0.085 D 3.514 2 121.172 19.000 0.008 * 误差 0.03 2 注:*表示P<0.05。 通过正交试验直观分析可知,以多糖得率为指标时的最佳工艺条件为:A3B3C1D3,即料液比1:25 g/mL,提取温度95 ℃,提取时间2 h,醇沉体积分数80%,由于D(醇沉体积分数)对多糖得率影响显著,且3个水平中ΔK3-2明显大于ΔK2-1,说明随着醇沉体积分数增大对多糖得率的影响在增大,因此选择80%为最佳工艺条件的醇沉体积分数,由于A(提取温度)和C(料液比)对多糖得率影响不显著(P>0.05),所以从降低能耗和生产成本的角度考可虑选择A1B1C1D3为最佳工艺。在正交试验直观分析中,因素B(提取时间)的极差较小,说明枳椇果梗多糖的水溶性比较大可以很快地溶解于水中,延长提取时间对多糖得率的影响不明显。
为了对以上两个工艺条件A3B3C1D3与A1B1C1D3进行对比,在两个工艺条件下对枳椇果梗多糖进行提取,得率分别为:2.94%±0.174%、3.06%±0.181%,二者并无显著性差异(P>0.05),因此从降低能耗和生产成本的角度综合考虑,确定A1B1C1D3(料液比1:25 g/mL,提取温度85 ℃,提取时间1 h,醇沉体积分数80%)为最佳工艺条件。
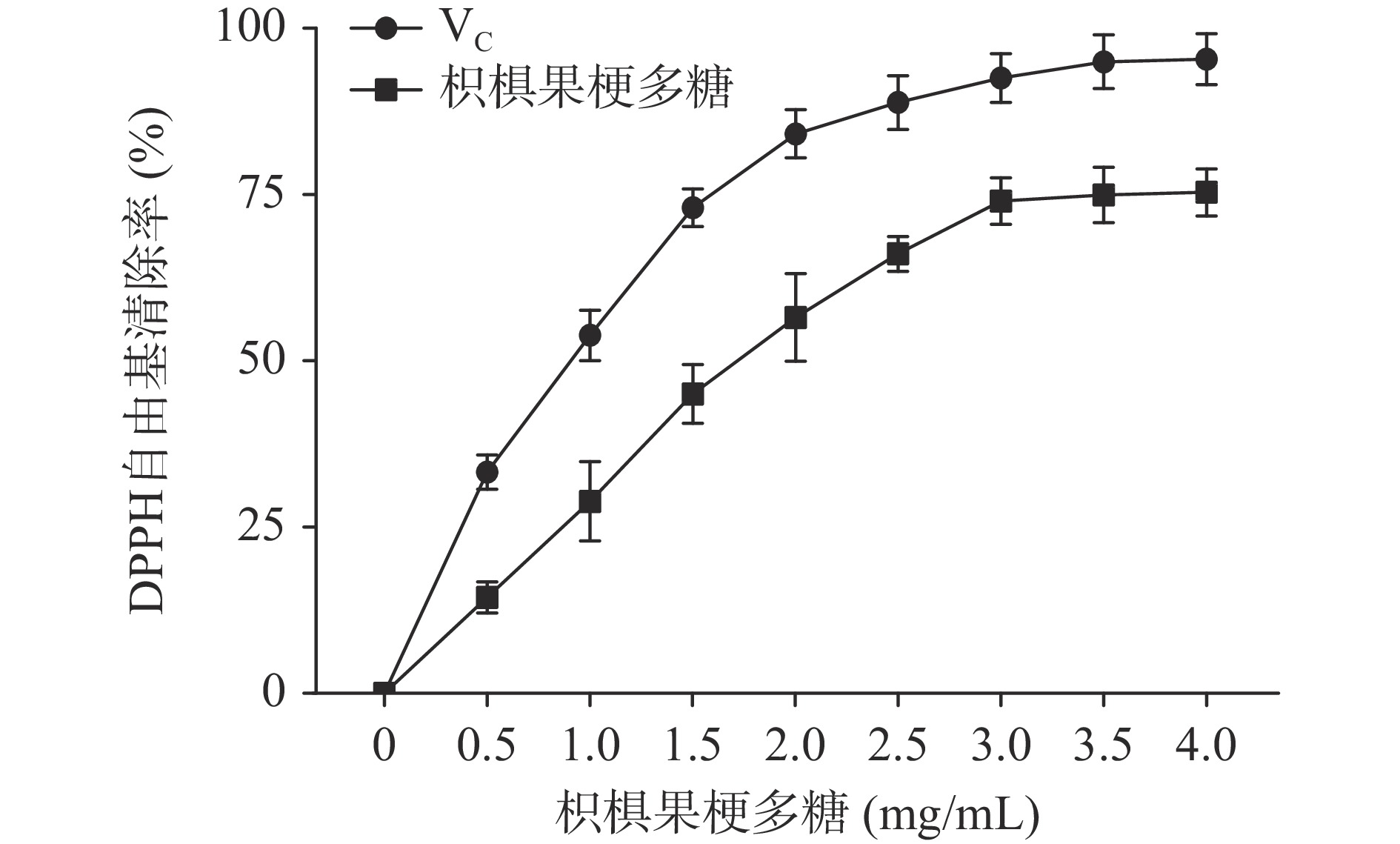
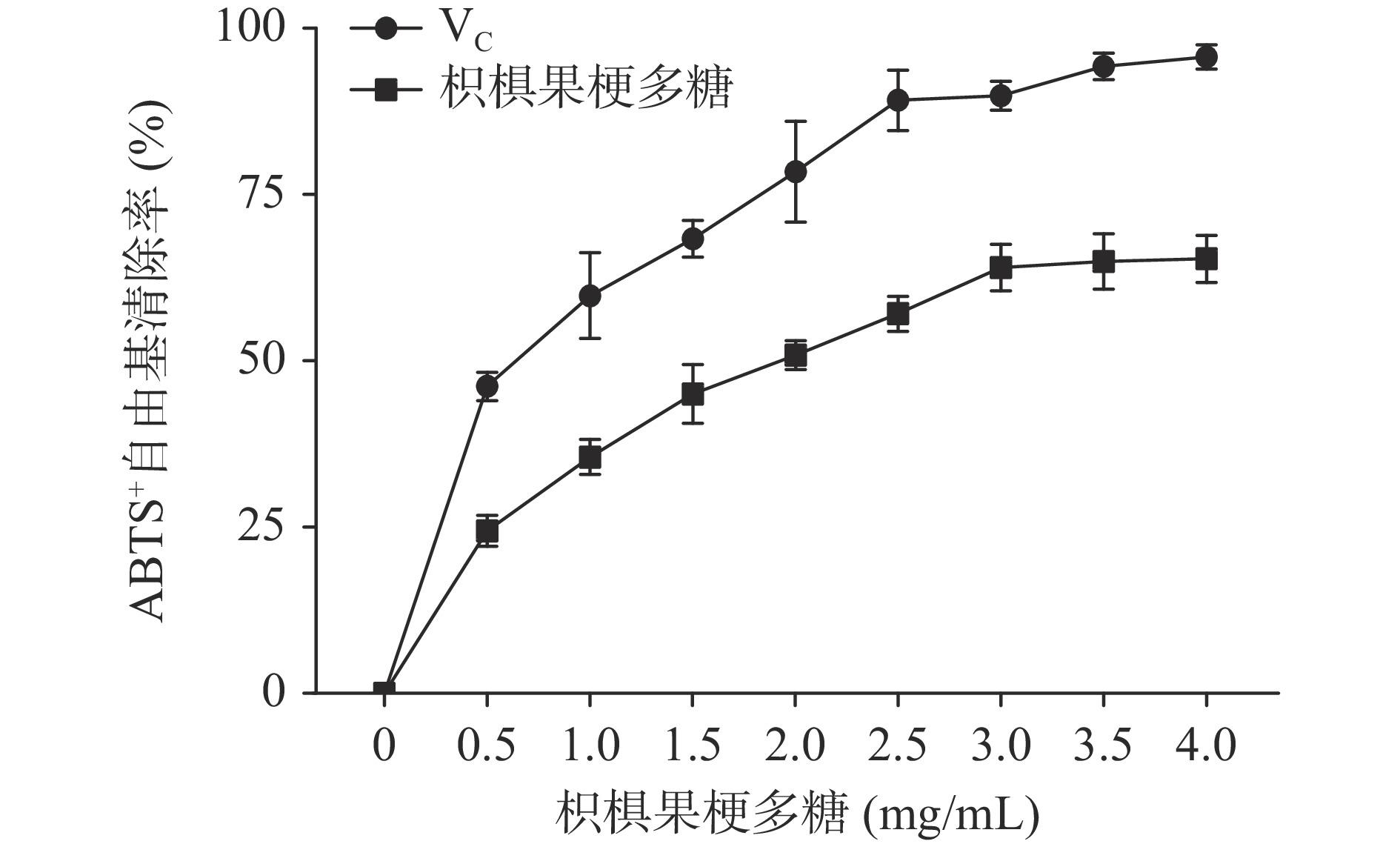
2.3 枳椇果梗多糖清除自由基能力
如图5、图6所示,枳椇果梗多糖对DPPH自由基和ABTS+自由基的清除率均随着浓度的增加呈上升趋势,对于DPPH自由基、ABTS+自由基清除IC50分别为1.687、1.824 mg/mL,同等条件下VC对于DPPH自由基、ABTS+自由基清除IC50分别为0.8159、0.7100 mg/mL。与其他植物多糖相比,本研究中枳椇果梗多糖清除DPPH、ABTS+自由基的IC50低于山茱萸籽、玉竹、慈竹等植物多糖,且与前期枳椇多糖相关研究结果类似[28-31],说明本研究所提取的枳椇果梗多糖具有较强的清除自由基能力。
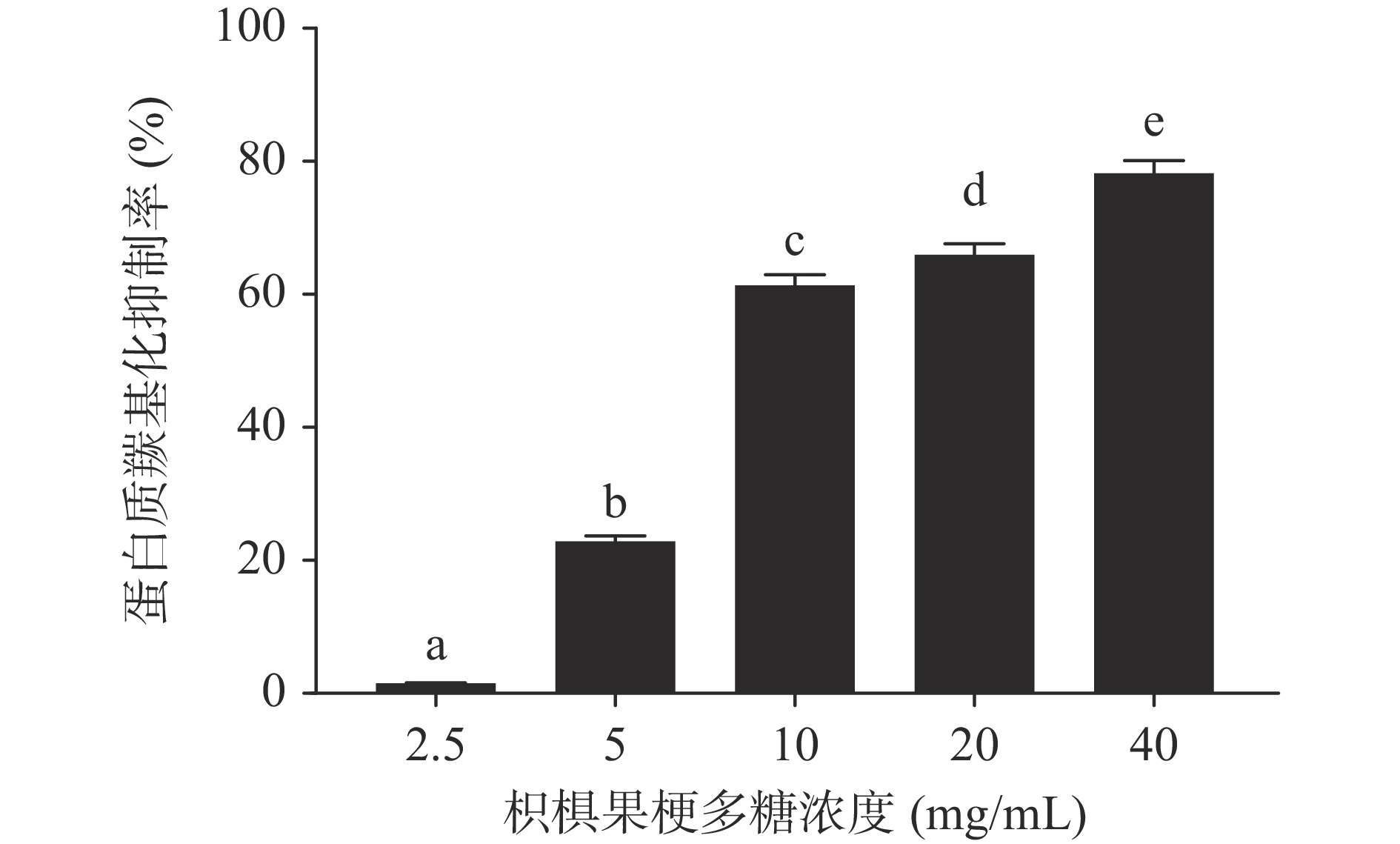
2.4 枳椇果梗多糖对蛋白质羰基化的影响
蛋白质氨基酸侧链受自由基攻击后会发生羰基化,羰基化是蛋白质经自由基修饰造成氧化损伤的重要标记物,羰基化的蛋白质很难被机体自身抗氧化系统修复,慢慢积累会引起蛋白质的功能和结构的改变,进而引起一系列的相关疾病[32]。Cu2+/H2O2体系可诱导BSA羰基化,本研究通过加入不同浓度枳椇果梗多糖后氧化体系中羰基的含量来测定多糖对BSA羰基化的抑制情况。如图7所示,随着枳椇果梗多糖浓度的升高,多糖对BSA羰基化抑制率逐渐增加,不同浓度组之间均存在显著性的差异(P<0.05),IC50为13.84 mg/mL,当多糖浓度达到40 mg/mL时BSA羰基化的抑制率可达78.20%±1.946%。Cu2+/H2O2体系主要通过产生·OH诱导BSA氨基酸侧链羰基化,说明枳椇果梗多糖对于·OH有一定的清除作用,进而可以抑制蛋白质的羰基化。
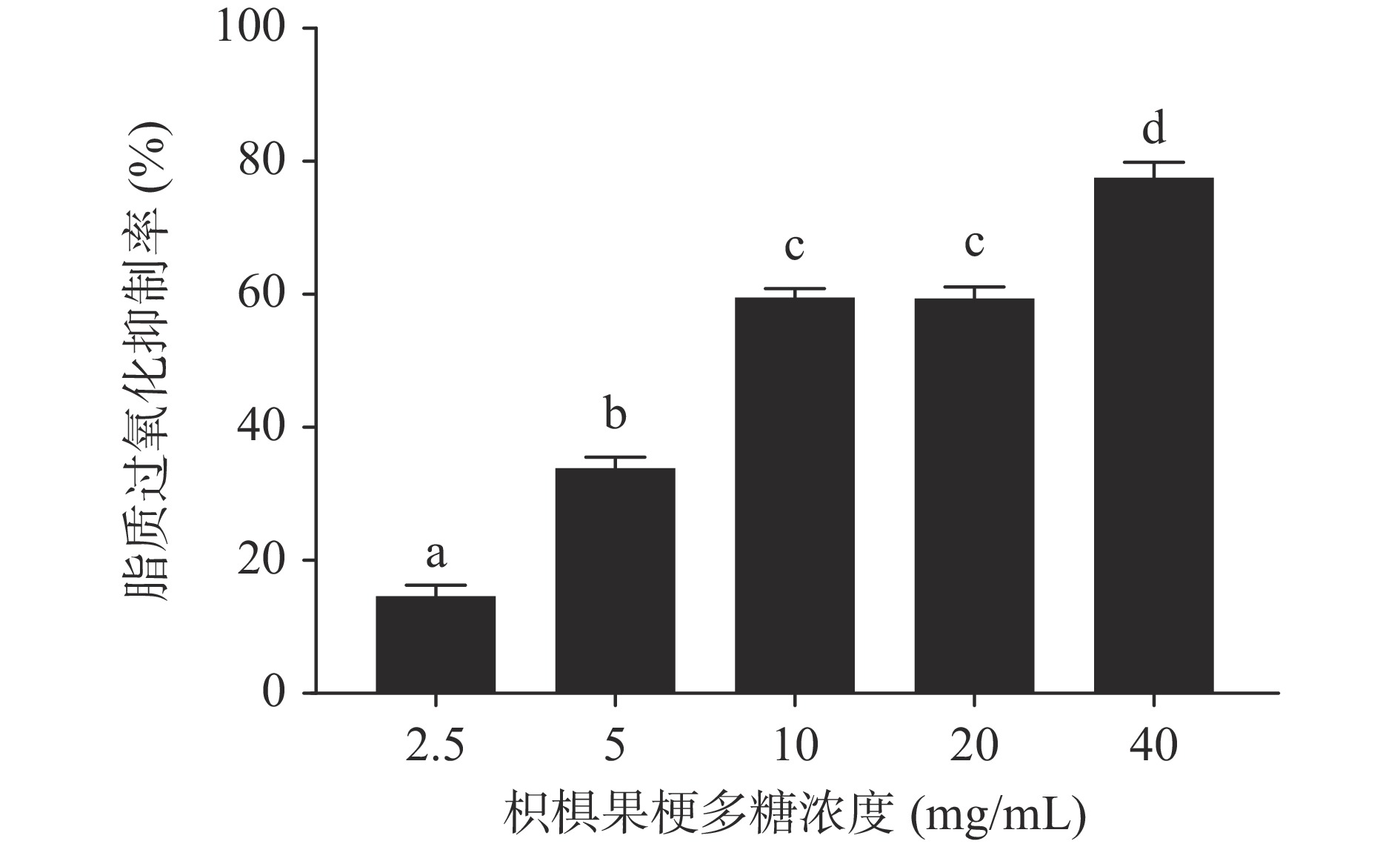
2.5 枳椇果梗多糖对脂质过氧化的影响
脂质过氧化作用是一系列自由基的连锁反应,高度活泼的自由基与脂类不饱和脂肪酸反应,形成中间体自由基,再与分子氧化反应形成脂质过氧化自由基。作为细胞膜的主要成分,脂质的过氧化最终会导致细胞膜结构和功能的改变。MDA作为一种典型的脂质过氧化产物是常用的衡量脂质过氧化的指标[33]。本研究通过加入不同浓度枳椇果梗多糖后氧化体系中MDA的含量来测定多糖对亚油酸过氧化的抑制情况。如图8所示,随着枳椇果梗多糖浓度的升高,多糖对FeSO4诱导的亚油酸过氧化抑制率逐渐增加,IC50为10.88 mg/mL,当多糖浓度达到40 mg/mL时抑制率可达77.52%±2.330%。枳椇果梗多糖具有较强的清除自由基能力,说明枳椇果梗多糖可以通过对脂质过氧化途径中的自由基清除达到对FeSO4诱导的亚油酸过氧化的抑制作用。
2.6 枳椇果梗多糖对DNA氧化的影响
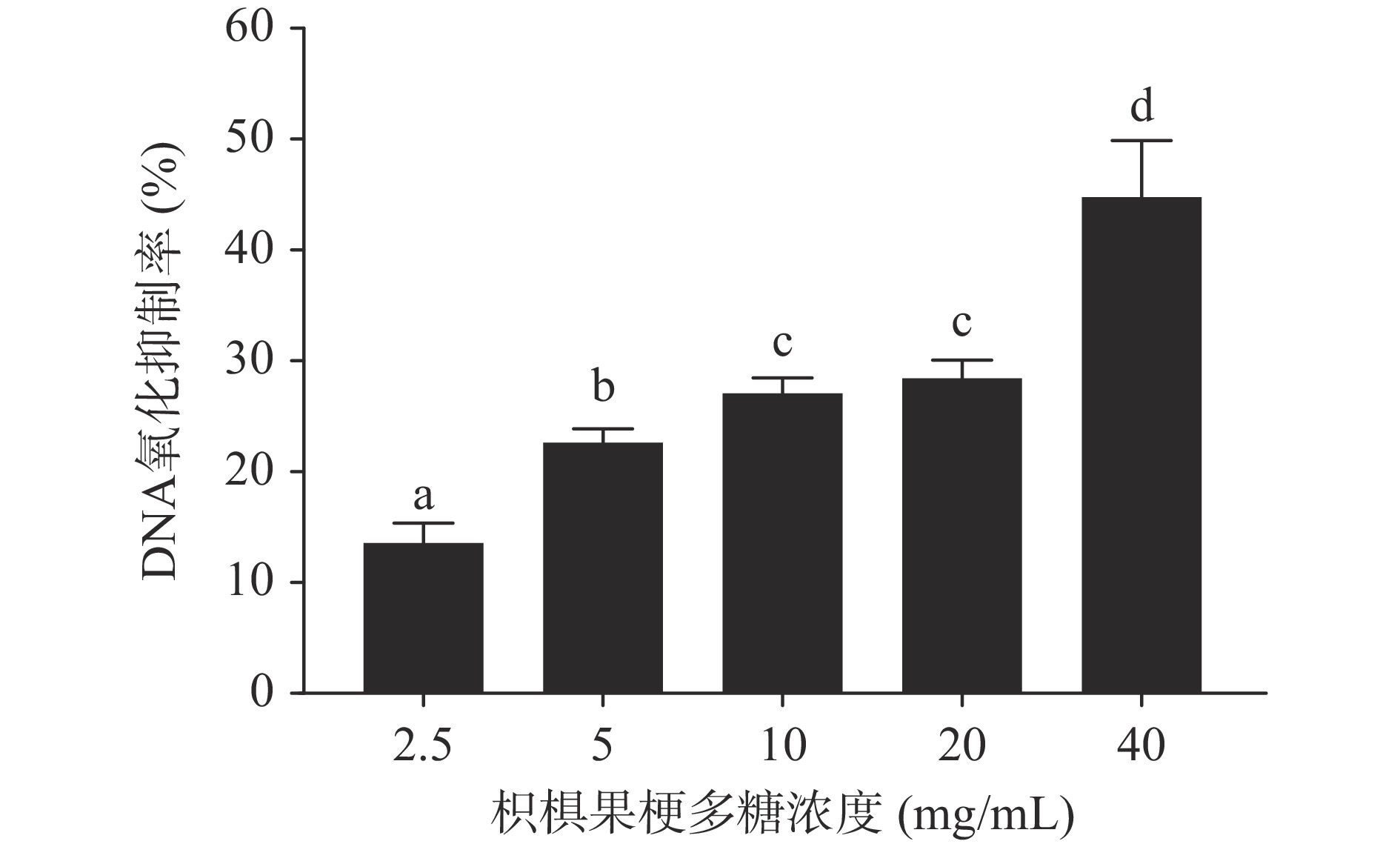
DNA作为遗传信息的重要载体,氧化修饰不但会造成DNA结构和功能的改变,甚至会造成基因突变。在DNA的碱基中,鸟嘌呤的分子轨道具有较高的能级,其8位碳原子容易被氧化损伤而生成修饰碱基8-OH-dG,其化学性质稳定可作为衡量DNA氧化损伤的主要指标[23]。本研究通过加入不同浓度枳椇果梗多糖后氧化体系8-OH-dG的含量来测定多糖对hsDNA氧化损伤的抑制情况。如图9所示,随着枳椇果梗多糖浓度的升高,多糖对hsDNA氧化损伤的抑制率逐渐增加,IC50为74.70 mg/mL。当多糖浓度为40 mg/mL时抑制率为44.76%±5.099%。AAPH通过产生的烷氧自由基对hsDNA攻击导致hsDNA损伤,说明枳椇果梗多糖可通过清除烷氧自由基对hsDNA进行保护。
3. 结论
通过水提法进行多糖的提取,提取过程简单,不需要特殊设备且条件易于控制,更适合大量多糖样品生产制备,所优化的该工艺最佳条件为:料液比1:25 g/mL,提取温度85 ℃,提取时间1 h,醇沉体积分数80%,在此条件下枳椇果梗多糖得率为3.06%±0.181%;所得枳椇果梗多糖对DPPH、ABTS+自由基有较强的清除能力;且对自由基引发的蛋白质羰基化、脂质过氧化、DNA氧化损伤均有明显的抑制作用。在最佳工艺条件下所获得的枳椇果梗多糖具有显著的清除自由基和抑制生物大分子氧化的能力,作为一种来源广泛的天然资源,枳椇果梗多糖的应用前景广阔。
-
表 1 正交试验因素水平表
Table 1 Orthogonal test factor level table
水平 A 提取温度(℃) B 提取时间(h) C 料液比(g/mL) D 醇沉体积分数(%) 1 85 1 1:25 60 2 90 1.5 1:30 70 3 95 2 1:35 80 表 2 正交试验设计与结果
Table 2 Design and results of orthogonal test
试验号 因素 多糖得率(%) A B C D 1 1 1 1 1 1.36 2 1 2 2 2 1.31 3 1 3 3 3 2.56 4 2 1 2 3 2.70 5 2 2 3 1 1.07 6 2 3 1 2 1.54 7 3 1 3 2 1.57 8 3 2 1 3 2.91 9 3 3 2 1 1.57 K1 1.743 1.877 1.937 1.333 K2 1.770 1.763 1.860 1.473 K3 2.017 1.890 1.733 2.723 极差R 0.274 0.127 0.204 1.390 表 3 正交试验方差分析
Table 3 Variance analysis of orthogonal test
因素 偏差平方和 自由度 F比 F临界值 P值 显著性 A 0.136 2 4.690 19.000 0.183 B 0.029 2 1.000 19.000 0.039 C 0.063 2 2.172 19.000 0.085 D 3.514 2 121.172 19.000 0.008 * 误差 0.03 2 注:*表示P<0.05。 -
[1] TAN B L, NORHAIZAN M E, LIEW W P. Nutrients and oxidative stress: friend or foe?[J]. Oxidative Medicine and Cellular Longevity,2018,31:9719584.
[2] DAS M, BABU K, REDDY N P, et al. Oxidative damage of plasma proteins and lipids in epidemic dropsy patients: Alterations in antioxidant status[J]. Biochimica et Biophysica ACTA-Subjects,2005,1722(2):209−217. doi: 10.1016/j.bbagen.2004.12.014
[3] POPRAC P, JOMOVA K, SIMUNKOVA M, et al. Targeting free radicals in oxidative stress-related human diseases[J]. Trends in Pharmacological Science,2017,38(7):592−607. doi: 10.1016/j.tips.2017.04.005
[4] 杨斯惠, 向月, 曹亚楠, 等. 植物多糖的益生作用及其影响因素研究进展[J]. 食品科学,2022,43(11):301−310. [YANG S H, XIANG Y, CAO Y N, et al. Progress in research on the prebiotic effects of plant polysaccharides and the factors influencing them[J]. Food Science,2022,43(11):301−310. doi: 10.7506/spkx1002-6630-20210610-132 [5] HUANG G, MEI X, HU J. The antioxidant activities of natural polysaccharides[J]. Current Drug Targets,2017,18(11):1296−1300.
[6] ZENG P, LI J, CHEN Y, et al. The structures and biological functions of polysaccharides from traditional Chinese herbs[J]. Progress in Molecular Biology and Translational Science,2019,163:423−444.
[7] XIE L, SHEN M, HONG Y, et al. Chemical modifications of polysaccharides and their anti-tumor activities[J]. Carbohydrate Polymers,2020,229:115436. doi: 10.1016/j.carbpol.2019.115436
[8] LIU Y, SUN Y Y, HUANG G L. Preparation and antioxidant activities of important traditional plant polysaccharides[J]. International Journal of Biological Macromolecules,2018,111:780−786. doi: 10.1016/j.ijbiomac.2018.01.086
[9] 于俊俊, 徐德平. 枳椇子降尿酸功效成分[J]. 食品科技,2019,44(11):227−231, 237. [YU J J, XU D P. Uric acid-lowering ingredients of Semen Hoveniae[J]. Food Science and Technology,2019,44(11):227−231, 237. doi: 10.13684/j.cnki.spkj.2019.11.041 [10] 陆石英, 覃志高. 药食两用枳椇的研究进展[J]. 食品安全质量检测学报,2020,11(6):1865−1870. [LU S Y, QIN Z G. Research progress on Hovenia dulcis Lindl. for medicine and food[J]. Journal of Food Safety and Quality,2020,11(6):1865−1870. doi: 10.19812/j.cnki.jfsq11-5956/ts.2020.06.031 [11] 向进乐, 杜琳, 朱文学, 等. 枳椇果梗营养功能与加工利用[J]. 中国林副特产,2015,1:98−101. [XIANG J L, DU L, ZHU W X, et al. Research progress in nutrition and utilization of Hovenia peduncles[J]. Forest By-Product and Speciality in China,2015,1:98−101. doi: 10.13268/j.cnki.fbsic.2015.01.045 [12] 李维新, 何志刚, 林晓姿, 等. 拐枣的营养保健功能及其果汁饮料的研制[J]. 食品科学,2005,8:249−251. [LI W X, HE Z G, LIN X Z, et al. Nutritional health function of Hovenia dulcis Thunb and research of juice beverage[J]. Food Science,2005,8:249−251. doi: 10.3321/j.issn:1002-6630.2005.03.063 [13] 肖芳, 陈涛, 伍振煌, 等. 植物多糖的提取工艺、生物学功能及其在动物生产中的研究进展[J]. 饲料研究,2022,14:125−128. [XIAO F, CHEN T, WU Z H, et al. Research progress on extraction technology, biological function and animal production of plant polysaccharides[J]. Feed Reaearch,2022,14:125−128. doi: 10.13557/j.cnki.issn1002-2813.2022.14.027 [14] 王文丽, 张金玲, 魏亚宁, 等. 天然多糖提取、纯化及生物活性研究进展[J]. 食品工业科技,2022,43(22):470−480. [WANG W L, ZHANG J L, WEI Y N, et al. Extraction, purification, and bioactivity of natural polysaccharides: A review[J]. Science and Technology of Food Industry,2022,43(22):470−480. doi: 10.13386/j.issn1002-0306.2021120256 [15] WANG W Q, LIU Z C, LIU Y J et al. Plant polypeptides: A review on extraction, isolation, bioactivities and prospects[J]. International Journal of Biological Macromolecules,2022,207:169−178. doi: 10.1016/j.ijbiomac.2022.03.009
[16] 杨海涛, 曹小燕. 超声辅助浸提拐枣中多糖及抗氧化性研究[J]. 应用化工,2017,46(11):2174−2177. [YANG H T, CAO X Y. Study on ultrasonic wave assisted extraction of polysaccharide from Hovenia dulcis and its antioxidant activity[J]. Applied Chemical Industry,2017,46(11):2174−2177. doi: 10.3969/j.issn.1671-3206.2017.11.026 [17] 张保, 李立天, 张萌, 等. 拐枣枝多糖提取工艺优化与其抗氧化性研究[J]. 中国酿造,2016,35(7):155−160. [ZHANG B, LI L T, ZHANG M, et al. Optimization of extraction technology of Hovenia acerba sticks polysaccharides and its antioxidant activity[J]. China Brewing,2016,35(7):155−160. doi: 10.11882/j.issn.0254-5071.2016.07.034 [18] 魏丕伟, 王凌云, 熊俐, 等. 枳椇多糖提取工艺研究[J]. 江苏农业科学,2012,40(8):272−274. [WEI P W, WANG L Y, XIONG L, et al. Study on the extraction process of Hovenia acerba polysaccharide[J]. Jiangsu Agricultural Science,2012,40(8):272−274. doi: 10.3969/j.issn.1002-1302.2012.08.108 [19] 刘佳维, 周君, 高亚杰, 等. 红参多糖脱蛋白的研究[J]. 食品科技,2018,43(7):188−192. [LIU W J, ZHOU J, GAO Y J, et al. Deproteinization of polysaccharide from red ginseng[J]. Food Science and Technology,2018,43(7):188−192. doi: 10.13684/j.cnki.spkj.2018.07.033 [20] YANG B, WU Q J, LUO Y X, et al. High-pressure ultrasonic-assisted extraction of polysaccharides from Hovenia dulcis: Extraction, structure, antioxidant activity and hypoglycemic[J]. International Journal of Biological Macromolecules,2019,137:676−687. doi: 10.1016/j.ijbiomac.2019.07.034
[21] 刘胜男, 余敏敏, 郭晓莉, 等. 迷迭香提取物对自由基诱导蛋白质、油脂及DNA氧化的抑制作用[J]. 食品研究与开发,2020,41(14):22−27. [LIU S N, YU M M, GUO X L, et al. Inhibition effect of rosemary extract against oxidation of protein, lipid and DNA induced by free radicals[J]. Food Research and Development,2020,41(14):22−27. doi: 10.12161/j.issn.1005-6521.2020.14.004 [22] 张月, 刘茜, 肖春霞. 辣椒碱对生物大分子氧化损伤的保护作用[J]. 现代食品科技,2017,33(2):41−47. [ZHANG Y, LIU Q, XIAO CX. Protective effect of capsaicin against oxidative damage to biomolecules[J]. Modern Food Science and Technology,2017,33(2):41−47. doi: 10.13982/j.mfst.1673-9078.2017.2.007 [23] 杨忠敏, 王祖文, 黄先智, 等. 桑叶生物碱对D-半乳糖诱导小鼠生物大分子氧化损伤的改善作用及机理[J]. 食品科学,2020,41(5):135−142. [YANG Z M, WANG Z W, HUANG X Z, et al. Effect and underlying mechanism of mulberry leaf alkaloid on improving D-galactose-induced oxidative damage in mice[J]. Food Science,2020,41(5):135−142. [24] 张双奇, 刘琳, 何念武, 等. 超声辅助提取陕产天麻多糖的工艺优化及抗氧化活性研究[J]. 中国农学通报,2021,37(9):131−136. [ZHANG S Q, LIU L, HE N W, et al. Gastrodia elata polysaccharide from Shanxi by ultrasound-assisted hot water extraction: Process optimization and antioxidant activity[J]. Chinese Agricultural Science Bulletin,2021,37(9):131−136. doi: 10.11924/j.issn.1000-6850.casb2020-0235 [25] CHEN C, YOU L J, ABBASI A M, et al. Optimization for ultrasound extraction of polysaccharides from mulberry fruits with antioxidant and hyperglycemic activityin vitro[J]. Carbohydrate Polymers,2015,130:122−132. doi: 10.1016/j.carbpol.2015.05.003
[26] 龚频, 王思远, 陈雪峰, 等. 响应面法优化杏鲍菇粗多糖提取条件及其体外活性[J]. 陕西科技大学学报,2019,37(6):60−65. [GONG P, WANG S Y, CHEN X F, et al. Optimization of crude polysaccharide extraction conditions from Pleurotus eryngii by response surface methodology and its vitro activities[J]. Journal of Shanxi University of Science & Technology,2019,37(6):60−65. doi: 10.3969/j.issn.1000-5811.2019.06.010 [27] 朱梅, 毕宏涛, 杨威, 等. 乙醇浓度对人参多糖分离的影响[J]. 东北师范大学报(自然科学版),2019,37(6):60−65. [ZHU M, BI H T, YANG W, et al. The effects of ethanol concentrations on isolation of ginseng polysaccharides[J]. Journal of Northeast Normal University (Natural Science Edition),2019,37(6):60−65. [28] 何坤明, 王国锭, 白新鹏, 等. 山茱萸籽多糖分离纯化、结构表征及抗氧化活性[J]. 食品科学,2021,42(19):81−88. [HE K M, WANG G D, BAI X P, et al. Solation, purification, structure characterization and antioxidant activity of Cornus officinalis seed polysaccharides[J]. Food Science,2021,42(19):81−88. doi: 10.7506/spkx1002-6630-20201111-109 [29] 霍达, 张霞, 陈君诚, 等. 玉竹多糖的提取工艺优化、结构表征及抗氧化活性的研究[J]. 食品科技,2020,45(7):200−208. [HUO D, ZHANG X, CHEN J C, et al. Optimization of extraction, structure characterization and antioxidant activity of polysaccharide from Polygonatum ordoratum (Mill.) druce[J]. Food Science and Technology,2020,45(7):200−208. doi: 10.13684/j.cnki.spkj.2020.07.035 [30] 郭磊, 管雨晴, 李梅云. 慈竹竹叶多糖体外抗氧化作用研究[J]. 食品研究与开发,2013,34(16):9−11. [GUO L, GUAN Y Q, LI M Y. Study on antioxidative effects of polysaccharide from Neosinocalamus affinis leaves[J]. Food Research and Development,2013,34(16):9−11. doi: 10.3969/j.issn.1005-6521.2013.16.003 [31] 叶文斌, 樊亮. 响应面与酶法优化拐枣多糖的提取工艺及其抗氧化活性研究[J]. 安徽农业大学学报,2016,43(2):182−189. [YE W B, FAN L. Extraction of polysaccharides from Hovenia acerba Lindi. by optimization enzymolysis and response surface methodology and its antioxidant capacity[J]. Journal of Anhui Agricultural University,2016,43(2):182−189. doi: 10.13610/j.cnki.1672-352x.20160311.030 [32] 左高隆, 黄霞, 林勇, 等. 蛋白质羰基化及茶多酚的预防作用研究进展[J]. 茶叶通讯,2019,46(3):257−262. [ZUO G L, HUANG X, LIN Y, et al. Research progress on protein carbonylation and prevention of tea polyphenols[J]. Journal of Tea Communication,2019,46(3):257−262. doi: 10.3969/j.issn.1009-525X.2019.03.002 [33] 童鑫怡, 韦铮, 陈梅, 等. 茶多糖-茶多酚对D-半乳糖诱导的小鼠脑组织氧化损伤的改善作用[J]. 食品工业科技,2022,43(16):377−383. [TONG X Y, WEI Z, CHEN M, et al. Effect of tea polysaccharide-tea polyphenol on improving D-galactose-induced oxidative damage of brain in mice[J]. Science and Technology of Food Industry,2022,43(16):377−383. doi: 10.13386/j.issn1002-0306.2021110008 -
期刊类型引用(5)
1. 何遂庆,吴芳丽,李爱珍. 高效液相色谱法快捷测定黄原胶中D-甘露糖含量的探究. 安徽医药. 2024(06): 1109-1111 .  百度学术
百度学术
2. 陈士国,张唯希,朱凯,侯志强,叶兴乾. 食源性碳水化合物结构解析新技术前沿与展望. 中国食品学报. 2024(09): 1-17 .  百度学术
百度学术
3. 高文庆,王晴,霍志鹏,何毅. UFLC-MS/MS检测微晶纤维素中葡萄糖和纤维二糖的方法建立及其在热降解分析中的应用. 天津药学. 2024(06): 26-30 .  百度学术
百度学术
4. 王洋,刘永灵. 超高效液相色谱-串联质谱法测定4种运动饮料中多糖的单糖组成及含量. 中国食品添加剂. 2023(07): 240-247 .  百度学术
百度学术
5. 蔡肖,刘军玲,邢丽花,张晓倩,马梦真,吕家慧,冯唯一,俞年军. 霍山石斛超微粉物理特性及石斛多糖中单糖分析. 中国食品添加剂. 2023(10): 143-152 .  百度学术
百度学术
其他类型引用(0)





 下载:
下载:






 下载:
下载:



